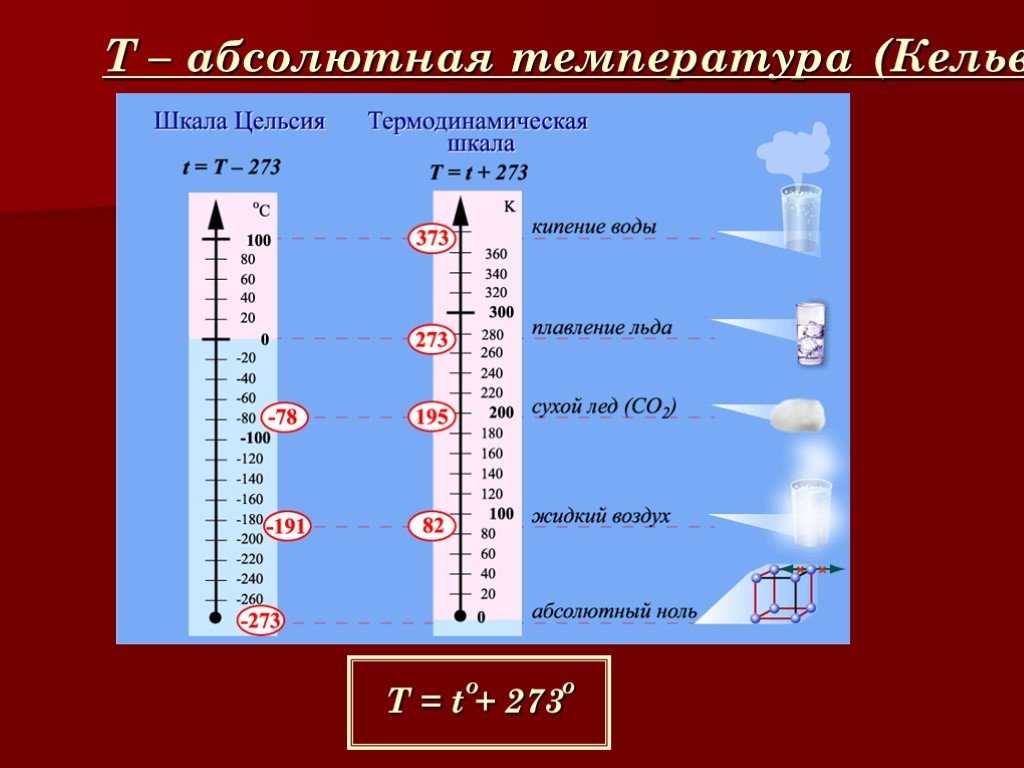
Температура и ее измерение. Абсолютный нуль температуры. Термодинамическая шкала температур.
Температу́ра (от лат. temperatura — надлежащее смешение, нормальное состояние) — скалярная физическая величина, характеризующая приходящуюся на одну степень свободы среднюю кинетическую энергию частиц макроскопической системы, находящейся в состояниитермодинамического равновесия.
В Международной
системе единиц (СИ) термодинамическая
температура входит в состав семи основных
единиц и выражается в кельвинах.
В состав производных величин СИ, имеющих
специальное название, входит
температура Цельсия,
измеряемая в градусах
Цельсия[1].
На практике часто применяют градусы
Цельсия из-за исторической привязки к
важным характеристикам воды —
температуре таяния льда (0 °C) и
температуре кипения (100 °C). Это удобно,
так как большинство климатических
процессов, процессов в живой природе и
т. д. связаны с этим диапазоном
д. связаны с этим диапазоном
В рамках применимости термодинамики абсолютный нуль на практике недостижим. Его существование и положение на температурной шкале следует из экстраполяции наблюдаемых физических явлений, при этом такая экстраполяция показывает, что при абсолютном нуле энергия теплового движения молекул и атомов вещества должна быть равна нулю, то есть хаотическое движение частиц прекращается, и они образуют упорядоченную структуру, занимая чёткое положение в узлах кристаллической решётки (жидкий гелийсоставляет исключение)
ТЕРМОДИНАМИЧЕСКАЯ
ТЕМПЕРАТУРНАЯ шкала(Кельвина
шкала)
— абсолютная шкала температур,
не зависящая от свойств термометрического
вещества (началоотсчета
— абсолютный нуль температуры). Построение термодинамической температурной
шкалы основано на втором начале
термодинамики и, в частности, на
независимости кпд Карно цикла от природы
рабочего тела.Единица термодинамической
температуры — кельвин (К)
— определяется как 1/273,16 часть термодинамической
температуры тройной точки воды.
Построение термодинамической температурной
шкалы основано на втором начале
термодинамики и, в частности, на
независимости кпд Карно цикла от природы
рабочего тела.Единица термодинамической
температуры — кельвин (К)
— определяется как 1/273,16 часть термодинамической
температуры тройной точки воды.
По значению
удельного электрического
сопротивления полупроводникизанимают
промежуточное место между хорошими
проводниками и диэлектриками. К числу
полупроводников относятся многие
химические элементы (германий, кремний,
селен, теллур, мышьяк и др.), огромное
количество сплавов и химических
соединений. Почти все неорганические
вещества окружающего нас мира –
полупроводники. Самым распространенным
в природе полупроводником является
кремний, составляющий около 30 % земной
коры. Качественное отличие полупроводников
от металлов проявляется прежде всего
в зависимости удельного сопротивления
от температуры. С понижением температуры
сопротивление металлов падает
(см.
Билет №15
Газовые законы. Уравнение состояния идеального газа. Молярная газовая постоянная.
Уравнение состояния
идеального газа (иногда уравнениеКлапейрона или уравнение Менделеева — Клапейрона) — формула, устанавливающая зависимость между давлением,молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:где — давление, — молярный объём, — универсальная газовая постоянная — абсолютная температура,К.
2. Молярная газовая постоянная. Для одного моля любого газа при нормальных условиях имеем: p = 1 атм = 1,013·105 Па, V = 22,4 л = 0,0224 м3, t = 0°C или T = 273 К.
 Вычислим
произведение давления на объем, деленное
на температуру:
Полученное
значение, отнесенное к одному молю,
называется
Вычислим
произведение давления на объем, деленное
на температуру:
Полученное
значение, отнесенное к одному молю,
называется
Электрическая проводимость полупроводников. Полупроводниковые приборы.
Полупроводники
— это вещества,
удельное сопротивление которых убывает
с повышением температуры, наличием
примесей, изменением освещенности. По
этим свойствам они разительно отличаются
от металлов. Обычно к полупроводникам
относятся кристаллы, в которых
для освобождения электрона требуется
энергия не более 1,5—2 эВ. Типичными
полупроводниками являются кристаллы
германия и кремния, в которых
атомы объединены ковалентной связью.
При температуре, близкой к абсолютному нулю, полупроводник ведет себя как абсолютный непроводник, потому что в нем нет свободных электронов. Если повышения температуры нет, связь валентных электронов с атомными ядрами ослабевает и некоторые из них вследствие теплового движения могут покидать свои атомы. Вырвавшийся из межатомной связи электрон становится свободным (на рис. 1, б — черная точка), а там, где он был до этого, образуется пустое место. Это пустое место в межатомной связи полупроводника условно называют дыркой (на рис. 1 ,б — разорвавшаяся линия электрона). Чем выше температура полупроводника, тем больше в нем появляется свободных электронов и дырок. Таким образом, образование в массе полупроводника дырки связано с уходом из оболочки атома валентного электрона, а возникновение дырки соответствует появлению положительного электрического заряда, равного отрицательному заряду электрона.
Билет №16
Температура – мера средней кинетической энергии хаотического движения молекул.
Магнитное поле, особый вид материи.
Магни́тное по́ле — силовое поле, действующее на движущиеся электрические заряды и на тела, обладающиемагнитным моментом, независимо от состояния их движения[1], магнитная составляющая электромагнитного поля[2]
Магнитное поле может создаваться током заряженных частиц и/или магнитными моментами электронов в атомах (и магнитными моментами других частиц, хотя в заметно меньшей степени) (постоянные магниты).
Магнитное поле можно назвать особым видом материи[7], посредством которого осуществляется взаимодействие между движущимися заряженными частицами или телами, обладающими магнитным моментом.
Магнитные поля являются необходимым (в контексте специальной теории относительности) следствием существования электрических полей.
Вместе,
магнитное и электрическое поля
образуют электромагнитное
поле,
проявлениями которого являются, в
частности, свет и
все другие электромагнитные
волны.
Билет №17
Термодинамическая шкала температур
Еще в 1848 г. В. Томсон отметил, что теоремой Карно можно воспользоваться, чтобы построить рациональную температурную шкалу, которая не зависит от особенностей термометрического вещества и устройства термометра.
Поэтому прежде чем перейти непосредственно к рассмотрению термодинамической шкалы температур, сформулируем теорему, которая называется теоремой Карно:
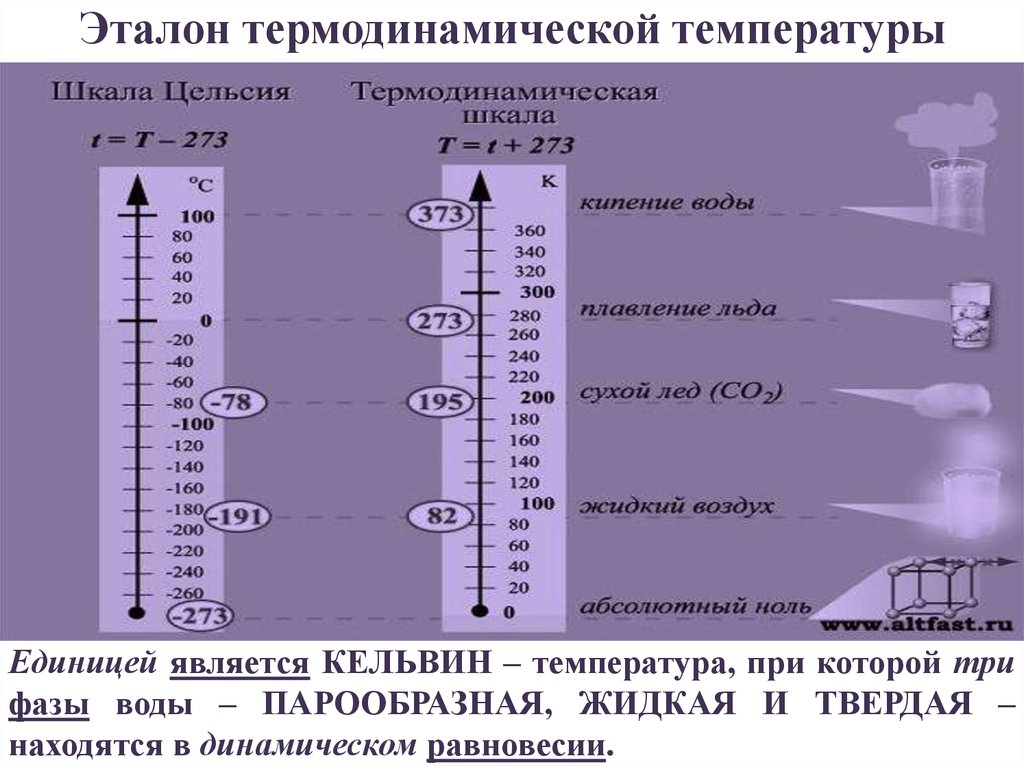
КПД ($\eta $) тепловой машины можно рассчитать по формуле:
\[\eta =1-\frac{Q_{ch}}{Q_n}\ \left(1\right),\]
где $Q_n$ — количество теплоты, полученное рабочим телом от нагревателя, $Q_{ch}$- количество теплоты, отданное рабочим телом холодильнику. Так как $\eta $ имеет одинаковые значения для всех тепловых машин, работающих по обратимому циклу Карно с температурой нагревателя и температурой холодильника. Обозначим временно величины этих температур ${\theta }_1\ и\ {\theta }_2,$ то для отношение $\frac{Q_{ch}}{Q_n}$ можно записать:
\[\frac{Q_{ch}}{Q_n}=f\left({\theta }_1\ ,\ {\theta }_2\right)\left(2\right),\]
где $f\left({\theta }_1\ ,\ {\theta }_2\right)$ — функция температур холодильника и нагревателя, универсальная для всех циклов Карно. Покажем, что $f\left({\theta }_1\ ,\ {\theta }_2\right)$ можно представить в виде:
\[f\left({\theta }_1\ ,\ {\theta }_2\right)=\frac{\varphi \left({\theta }_1\right)}{\varphi \left({\theta }_2\right)}\ \left(3\right),\]
где $\varphi \left(\theta \right)$ — универсальная функция от температуры.
Рассмотрим две обратимые машины (рис.1). Холодильник одной машины — нагреватель для другой. Допустим, что вторая машина отбирает от нагревателя с температурой ${\theta }_2$- столько тепла, сколько отдает ему первая машина (${Qch}_2={Qn}_2$). Исходя из (2), для каждой машины запишем:
\[\frac{Q_{ch3}}{Q_{n1}}=f\left({\theta }_1\ ,\ {\theta }_2\right)\left(4\right),\] \[\frac{Q_{ch4}}{Q_{ch3}}=f\left({\theta }_2\ ,\ {\theta }_3\right)\left(5\right).\]
Если рассмотреть машину на рис.1 как единую с тепловым резервуаром температуры (${\theta }_1$) и холодильником с температурой (${\theta }_3$), то получим:
\[\frac{Q_{ch4}}{Q_{n1}}=f\left({\theta }_1\ ,\ {\theta }_3\right)\left(6\right).\]
Рис. 1
Разделим (6) на (4), имеем:
\[\frac{Q_{ch4}}{Q_{ch3}}=\frac{f\left({\theta }_1\ ,\ {\theta }_3\right)}{f\left({\theta }_1\ ,\ {\theta }_2\right)}=\frac{Q_{n2}}{Q_{ch3}}\left(7\right). \]
\]
Сравниваем (7) и (5), получаем:
\[f\left({\theta }_2\ ,\ {\theta }_3\right)=\frac{f\left({\theta }_1\ ,\ {\theta }_3\right)}{f\left({\theta }_1\ ,\ {\theta }_2\right)}\ \left(8\right).\]
Уравнение (8) связывает температуры, связывает все температуры${\ \theta }_1\ ,\ {\theta }_2,\ {\theta }_3.$ Решим, что ${\ \theta }_1$ постоянна, получим, что функция $f\left({\theta }_1\ ,\ \theta \right)$ — функция одной переменной $\theta $. Обозначим эту функцию $\varphi (\theta )$, тогда уравнение (8) примет вид:
\[f\left({\theta }_2\ ,\ {\theta }_3\right)=\frac{\varphi \left({\theta }_3\ \right)}{\varphi \left({\theta }_2\ \right)}\ \left(9\right),\]
или
\[f\left({\theta }_1\ ,\ {\theta }_2\right)=\frac{\varphi \left({\theta }_2\ \right)}{\varphi \left({\theta }_1\ \right)}\ \left(10\right),\]
Что совпадает с тем, что мы хотели доказать, то есть с выражением (3).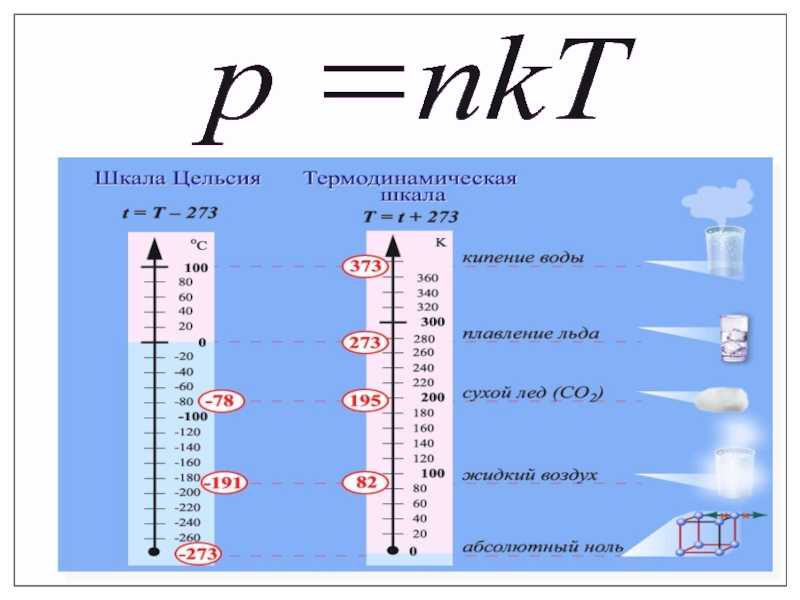
Функция $\varphi \left(\theta \ \right)$ зависит только от температуры. Поэтому ее значение можно использовать для характеристики температуры соответствующего тела, то есть полагать температуру равной $\varphi $, где $\varphi =\varphi \left(\theta \ \right).$ В таком случае уравнение (4) примет вид:
\[\frac{Q_{ch3}}{Q_{n1}}=\frac{{\varphi }_2}{{\varphi }_1}\ \left(11\right).\]
Соотношение (11) ложится в основу термодинамической шкалы температур. Ее преимущество — независимость от выбора рабочего тела в цикле Карно, которое используют для измерения температуры.
Величину $\varphi $ принимают за меру температуры тела и называют абсолютной термодинамической температурой. В примерах мы покажем, что она совпадает с используемой нами ранее с абсолютной температурой T по шкале идеального газового термометра. В выражении (11) мы видим отношение двух термодинамических температур. Чтобы определить температуру одного тела можно:
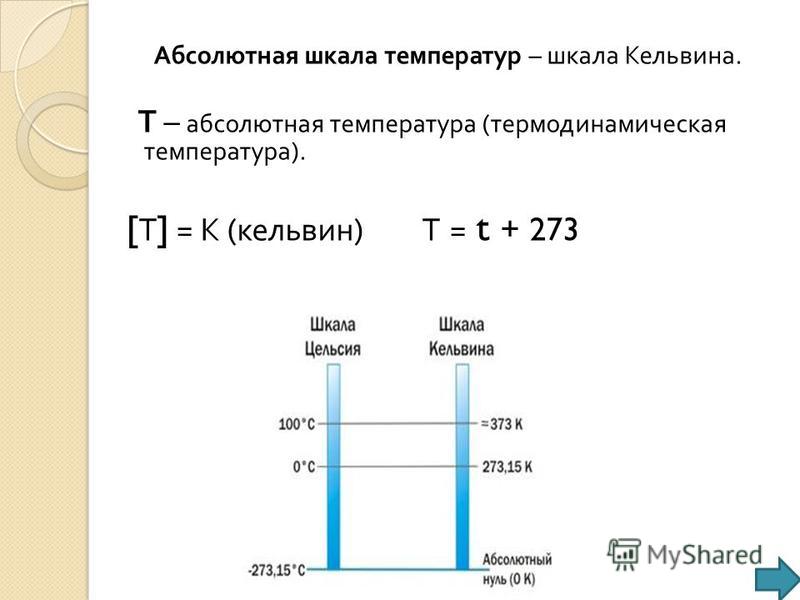
Абсолютная термодинамическая температура не может быть отрицательной.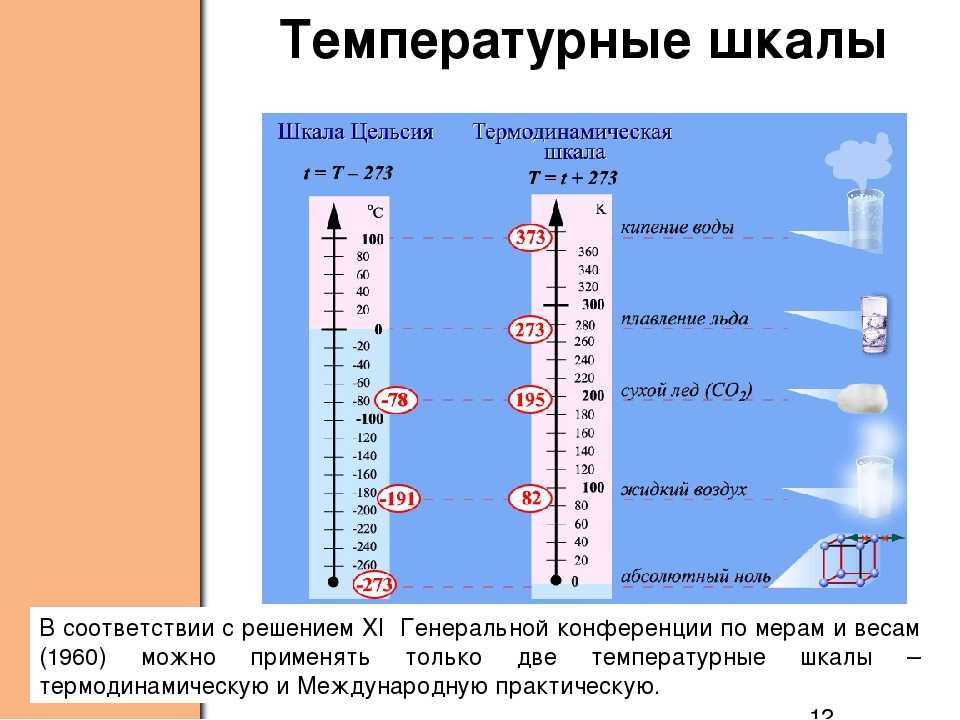 Самая низкая температура, которую допускает второе начало термодинамики: T=0K. Абсолютная термодинамическая шкала температур тождественна с абсолютной шкалой.
Самая низкая температура, которую допускает второе начало термодинамики: T=0K. Абсолютная термодинамическая шкала температур тождественна с абсолютной шкалой.
температура — Разница между абсолютной термодинамической шкалой и ИТС-90
спросил
Изменено 8 лет, 2 месяца назад
Просмотрено 2к раз
$\begingroup$
Чем отличается абсолютная термодинамическая шкала температур от практической температурной шкалы: ИТС-90?
- температура
$\endgroup$
$\begingroup$
Абсолютная термодинамическая шкала температур — это шкала, фиксируемая абсолютным нулем и (по крайней мере, для кельвинов, я не уверен насчет шкалы Ренкина) тройной точкой воды, где абсолютный ноль определяется как 0 К, а тройная точка воды определяется как 273,16 К.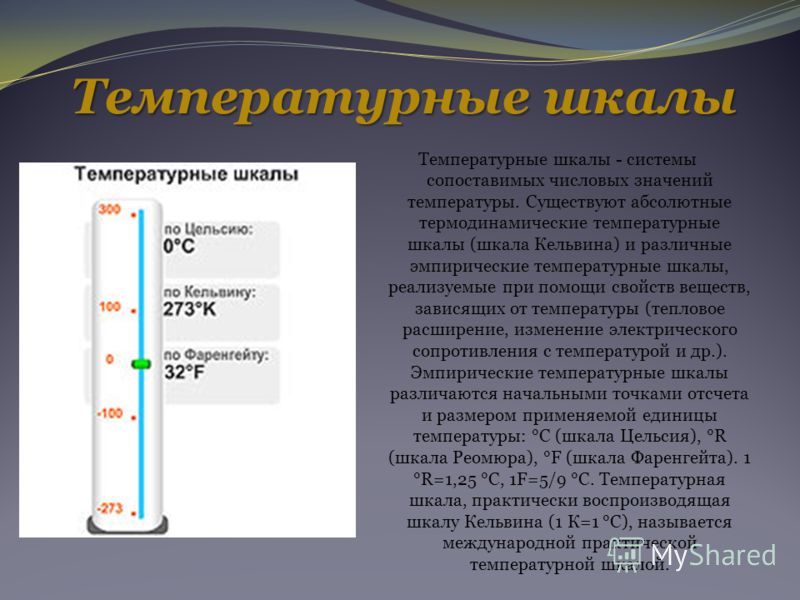 Остальная часть шкалы представляет собой прямую линию от нуля до 273,16 К до бесконечности. Однако эта шкала опирается только на две определенные точки (только одна из которых может быть фактически измерена, а абсолютный нуль устанавливается из термодинамических соотношений).
Остальная часть шкалы представляет собой прямую линию от нуля до 273,16 К до бесконечности. Однако эта шкала опирается только на две определенные точки (только одна из которых может быть фактически измерена, а абсолютный нуль устанавливается из термодинамических соотношений).
При практическом использовании, для целей калибровки термометров и т.п., это не очень большой масштаб, поскольку две точки калибровки могут находиться далеко от области температур, которую нужно измерить. Обычный способ справиться с этим — использовать другие контрольные точки вне фактического определения. Чтобы разные люди делали это максимально последовательно, ИТС-90 создавался как практическая реализация абсолютной шкалы, задающая дополнительные опорные точки (все фазовые переходы) на определенные значения, интерполируя между ними для получения других значений. Технически это не шкала сама по себе, а просто стандарт для калибровки температур, максимально приближенных к абсолютной шкале. Убедившись, что все используют одни и те же опорные точки, измерения могут быть более последовательными, чем если бы опорные точки выбирались произвольно и, возможно, им присваивались разные значения.
Например, если кто-то хочет сделать термометр для общего лабораторного использования, можно выбрать тройную точку ртути, тройную точку воды и точку плавления галлия из стандарта ITS-90 в качестве эталонных точек, зная, что другие термометры в этом диапазоне, соответствующие стандарту, также будут откалиброваны таким образом, вместо того, чтобы выбирать, скажем, точки плавления и кипения воды, что увеличивает вероятность согласованных измерений с другими термометрами.
$\endgroup$
Зарегистрируйтесь или войдите в систему
Зарегистрируйтесь с помощью Google
Зарегистрироваться через Facebook
Зарегистрируйтесь, используя электронную почту и пароль
Опубликовать как гость
Электронная почта
Требуется, но никогда не отображается
Опубликовать как гость
Электронная почта
Требуется, но не отображается
Нажимая «Опубликовать свой ответ», вы соглашаетесь с нашими условиями обслуживания, политикой конфиденциальности и политикой использования файлов cookie
.
Определение термодинамической температуры в физике.
(существительное)
Температура определяется в терминах законов термодинамики, а не свойств реального материала: выражается в кельвинах.
Обзор нулевого закона
- Нулевой закон оправдывает использование термодинамической температуры , определяемой как общая температура трех указанных систем, находящихся в равновесии.
- Этот вывод может показаться очевидным, потому что все три имеют одинаковую температуру , но нулевой закон лежит в основе термодинамики .
- Нулевой закон оправдывает использование термодинамической температуры : общая «метка», которую разделяют три системы в приведенном выше определении, определяется как температура систем.
- Термометры на самом деле измеряют свою температуру , а не температуру объекта, который они измеряют.

- Обсудите, как работает нулевой закон термодинамики оправдывает использование термодинамического температурного
Абсолютная температура
- Абсолютная температура является наиболее часто используемой термодинамической температурной единицей и является стандартной единицей температуры .
- Термодинамический температура является абсолютной мерой температуры .
- Это один из основных параметров термодинамики и кинетическая теория газов.
- Термодинамическая температура является «абсолютной» шкалой, поскольку она является мерой фундаментального свойства, лежащего в основе температуры : ее нуль или нулевая точка («абсолютный ноль») — это температура , при которой частицы составляют материю иметь минимальное движение и не может стать холоднее.
- Используя шкалу абсолютной температуры (система Кельвина), которая является наиболее часто используемой термодинамическая температура , мы показали, что средняя поступательная кинетическая энергия (КЭ) частицы в газе имеет простую зависимость от температуры :
Шкала Кельвина
- Кельвин — единица измерения температуры ; нулевой точкой шкалы Кельвина является абсолютный ноль, самая низкая возможная температура .

- Шкала Кельвина является абсолютной, термодинамической температура шкала с использованием абсолютного нуля в качестве нулевой точки.
- В классическом описании термодинамики абсолютным нулем является температура , при которой прекращается всякое тепловое движение.
- Кельвин определяется как доля 1/273,16 от термодинамической температуры тройной точки воды (ровно 0,01°C или 32,018°F).
- Краткое введение в температура и температура 9Весы 0067 для студентов, изучающих теплофизику или термодинамику .
- Кельвин — единица измерения температуры ; нулевой точкой шкалы Кельвина является абсолютный ноль, самая низкая возможная температура .
Абсолютный ноль
- Абсолютный ноль — самая холодная возможная температура ; формально это температура , при которой энтропия достигает минимального значения.
- Абсолютный ноль — это самая холодная возможная температура .
- Однако в интерпретации классической термодинамики кинетическая энергия может быть равна нулю, а тепловая энергия вещества обращается в нуль.

- Нулевая точка термодинамической температурной шкалы, такой как шкала Кельвина, устанавливается на абсолютный ноль.
- Краткое введение в температурные и температурные весы для студентов, изучающих теплофизику или термодинамику .
Нулевой закон термодинамики
- Нулевой закон термодинамики утверждает, что системы, находящиеся в тепловом равновесии, находятся в одном и том же температура .
- Есть несколько способов сформулировать Нулевой Закон Термодинамики , но самый простой из них следующий: системы, находящиеся в тепловом равновесии, существуют при одной и той же температуре .
- Нулевой закон термодинамики означает, что температуру стоит измерять, потому что она показывает, будет ли тепло перемещаться между объектами.
- Температура не упоминается явно, но подразумевается, что температура существует.
- Системы A, B и C имеют одинаковую температуру .
Шкала Цельсия
- Цельсий или градус Цельсия — это шкала и единица измерения температуры .
- Это один из наиболее часто используемых температурных блоков .
- Это определение также точно связывает шкалу Цельсия со шкалой Кельвина, которая определяет базовую единицу СИ термодинамического температура и который использует символ K.
- Помимо выражения конкретных температур по шкале (например, «Галлий плавится при 29,7646 ° C» и « температура снаружи составляет 23 градуса Цельсия»), градус Цельсия также подходит для выражения температурных интервалов — различий между температурами или их неопределенностями (например,
- Краткое введение в температура и температура 9Весы 0067 для студентов, изучающих теплофизику или термодинамику .

Изотермические процессы
- Изотермический процесс представляет собой изменение термодинамической системы, при котором температура остается постоянной.
- Изотермический процесс – это изменение системы, при котором температура остается постоянной: ΔT = 0,
- В термодинамике работа, необходимая для перехода газа из состояния A в состояние B, равна просто
- Также стоит отметить, что для многих систем, если температура поддерживается постоянной, внутренняя энергия системы также постоянна, и поэтому $\Delta U = 0$.
- Из первого начала термодинамики следует, что $Q =-W$ для этого самого изотермического процесса.
Второй закон
- Второй закон термодинамики гласит, что теплопередача происходит самопроизвольно только от высших к низшим температура тел.
- Второй закон термодинамики касается направления самопроизвольных процессов.

- Например, теплота включает передачу энергии от более высокой к более низкой температуре .
- Закон, запрещающий эти процессы, называется вторым законом термодинамики .
- Второй закон термодинамики (первое выражение): Теплопередача происходит самопроизвольно от более высоких к более низким температуры тела но никогда самопроизвольно в обратном направлении.
Термодинамика
- Черное тело, конечно, характеризуется одной температурой , $T$.
- Обычно используются три характеристики температуры : яркость температура , эффективная температура и цвет температура .
- Яркость температура определяется путем приравнивания яркости или интенсивности астрофизического источника к интенсивности черного тела и решения для температура соответствующего черного тела.
- В каком режиме начинает нарушаться линейная зависимость между яркостью температурой и интенсивностью?
- Наконец, эффективная температура — это температура абсолютно черного тела, которое излучает на своей поверхности тот же поток, что и источник, т.

