Урок 06. Лекция 05. Абсолютная температура как мера средней кинетической энергии частиц.
Понятие температуры – одно из важнейших в молекулярной физике.
Температура — это физическая величина, которая характеризует степень нагретости тел.
Беспорядочное хаотическое движение молекул называется тепловым движением.
Кинетическая энергия теплового движения растет с возрастанием температуры. При низких температурах средняя кинетическая энергия молекулы может оказаться небольшой. В этом случае молекулы конденсируются в жидкое или твердое вещество; при этом среднее расстояние между молекулами будет приблизительно равно диаметру молекулы. При повышении температуры средняя кинетическая энергия молекулы становится больше, молекулы разлетаются, и образуется газообразное вещество.
Понятие температуры тесно связано с понятием теплового равновесия. Тела, находящиеся в контакте друг с другом, могут обмениваться энергией.
Рассмотрим пример. Если положить нагретый металл на лед, то лед начнет плавится, а металл – охлаждаться до тех пор, пока температуры тел не станут одинаковыми. При контакте между двумя телами разной температуры происходит теплообмен, в результате которого энергия металла уменьшается, а энергия льда увеличивается.
Энергия при теплообмене всегда передается от тела с более высокой температурой к телу с более низкой температурой. В конце концов, наступает состояние системы тел, при котором теплообмен между телами системы будет отсутствовать. Такое состояние называют тепловым равновесием.
Тепловое равновесие – это такое состояние системы тел, находящихся в тепловом контакте, при котором не происходит теплопередачи от одного тела к другому, и все макроскопические параметры тел остаются неизменными.
Температура
– это физический параметр, одинаковый для всех тел, находящихся в тепловом равновесии.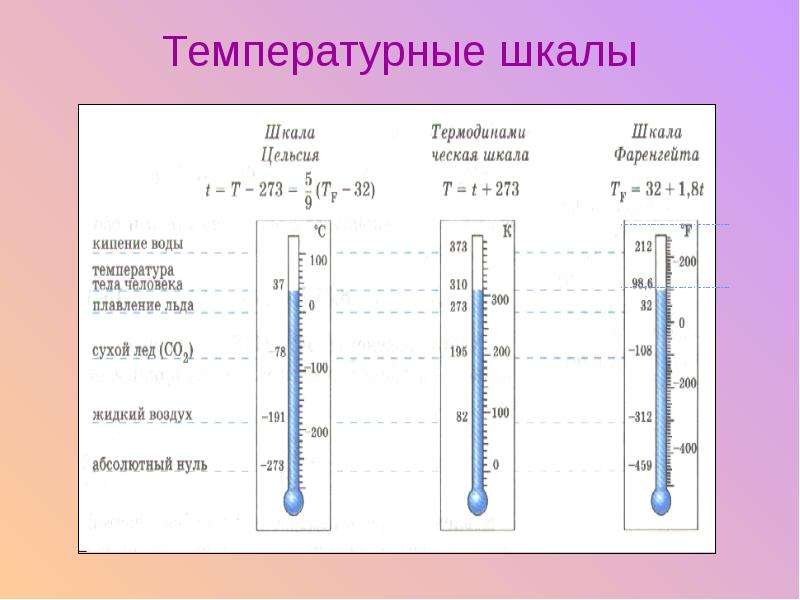 Возможность введения понятия температуры следует из опыта и носит название нулевого закона термодинамики.
Возможность введения понятия температуры следует из опыта и носит название нулевого закона термодинамики.Тела, находящиеся в тепловом равновесии, имеют одинаковые температуры.
Для измерения температур чаще всего используют свойство жидкости изменять объем при нагревании (и охлаждении).
Прибор, с помощью которого измеряется температура, называется термометр.
Для создания термометра необходимо выбрать термометрическое вещество (например, ртуть, спирт) и термометрическую величину, характеризующую свойство вещества (например, длина ртутного или спиртового столбика). В различных конструкциях термометров используются разнообразные физические свойства вещества (например, изменение линейных размеров твердых тел или изменение электрического сопротивления проводников при нагревании). Термометры должны быть откалиброваны. Для этого их приводят в тепловой контакт с телами, температуры которых считаются заданными. Чаще всего используют простые природные системы, в которых температура остается неизменной, несмотря на теплообмен с окружающей средой – это смесь льда и воды и смесь воды и пара при кипении при нормальном атмосферном давлении.
Обыкновенный жидкостный термометр состоит из небольшого стеклянного резервуара, к которому присоединена стеклянная трубка с узким внутренним каналом. Резервуар и часть трубки наполнены ртутью. Температуру среды, в которую погружен термометр определяют по положению верхнего уровня ртути в трубке. Деления на шкале условились наносить следующим образом. Цифру 0 ставят в том месте шкалы, где устанавливается уровень столбика жидкости, когда термометр опущен в тающий снег (лед), цифру 100 – в том месте, где устанавливается уровень столбика жидкости, когда термометр погружен в пары воды, кипящей при нормальном давлении (10 5 Па). Расстояние между этими отметками делят на 100 равных частей, называемых градусами. Такой способ деления шкалы введен Цельсием. Градус по шкале Цельсия обозначают ºС.
По температурной шкале Цельсия точке плавления льда приписывается температура 0 °С, а точке кипения воды – 100 °С. Изменение длины столба жидкости в капиллярах термометра на одну сотую длины между отметками 0 °С и 100 °С принимается равным 1 °С.
В ряде стран (США) широко используется шкала Фаренгейта (TF), в которой температура замерзающей воды принимается равной 32 °F, а температура кипения воды равной 212 °F. Следовательно,
Ртутные термометры
Электрический термометр – термосопротивление – в нем используется зависимость сопротивления металла от температуры.
Особое место в физике занимают газовые термометр, в которых термометрическим веществом является разреженный газ (гелий, воздух) в сосуде неизменного объема (V = const), а термометрической величиной – давление газа p. Опыт показывает, что давление газа (при V = const) растет с ростом температуры, измеренной по шкале Цельсия.
Чтобы проградуировать газовый термометр постоянного объема, можно измерить давление при двух значениях температуры (например, 0 °C и 100 °C), нанести точки p0 и p100 на график, а затем провести между ними прямую линию.
Газовые термометры громоздки и неудобны для практического применения: они используются в качестве прецизионного стандарта для калибровки других термометров.
Показания термометров, заполненных различными термометрическими телами, обычно несколько различаются. Чтобы точное определение температуры не зависело от вещества, заполняющего термометр, вводится термодинамическая шкала температур.
Чтобы её ввести, рассмотрим, как зависит давление газа от температуры, когда его масса и объём остаются постоянными.
Термодинамическая шкала температур. Абсолютный нуль.
Возьмем закрытый сосуд с газом, и будем нагревать его, первоначально поместив в тающий лед. Температуру газа t определим с помощью термометра, а давление p манометром. С увеличением температуры газа его давление будет возрастать.
Если продолжить график в область низких давлений, можно определить некоторую «гипотетическую» температуру, при которой давление газа стало бы равным нулю. Опыт показывает, что эта температура равна –273,15 °С и не зависит от свойств газа. Невозможно на опыте получить путем охлаждения газ в состоянии с нулевым давлением, так как при очень низких температурах все газы переходят в жидкие или твердые состояния. Давление идеального газа определяется ударами хаотически движущихся молекул о стенки сосуда. Значит, уменьшение давления при охлаждении газа объясняется уменьшением средней энергии поступательного движения молекул газа Е; давление газа будет равно нулю, когда станет равна нулю энергия поступательного движения молекул.
Английский физик У. Кельвин (Томсон) выдвинул идею о том, что полученное значение абсолютного нуля соответствует прекращению поступательного движения молекул всех веществ. Температуры ниже абсолютного нуля в природе быть не может. Это предельная температура при которой давление идеального газа равно нулю.
Температуры ниже абсолютного нуля в природе быть не может. Это предельная температура при которой давление идеального газа равно нулю.
Температуру, при которой должно прекратиться поступательное движение молекул, называют абсолютным нулем (или нулем Кельвина).
Кельвин в 1848 г. предложил использовать точку нулевого давления газа для построения новой температурной шкалы –термодинамической шкалы температур (шкала Кельвина). За начало отсчета по этой шкале принята температура абсолютного нуля.
В системе СИ принято единицу измерения температуры по шкале Кельвина называть
Размер градуса кельвина определяют так, чтобы он совпадал с градусом Цельсия, т.е 1К соответствует 1ºС.
Температура, отсчитанная по термодинамической шкале температур, обозначается Т. Её называют абсолютной температурой илитермодинамической температурой.
Температурная шкала Кельвина называется абсолютной шкалой температур. Она оказывается наиболее удобной при построении физических теорий.
Она оказывается наиболее удобной при построении физических теорий.
Кроме точки нулевого давления газа, которая называется абсолютным нулем температуры, достаточно принять еще одну фиксированную опорную точку. В шкале Кельвина в качестве такой точки используется температура тройной точки воды (0,01 °С), в которой в тепловом равновесии находятся все три фазы – лед, вода и пар. По шкале Кельвина температура тройной точки принимается равной 273,16 К.
Связь между абсолютной температурой и температурой по шкале Цельсия выражается формулой Т = 273,16 + t , где t – температура в градусах Цельсия.
Чаще пользуются приближенной формулой Т = 273 + t и t = Т – 273
Абсолютная температура не может быть отрицательной.
Температура газа – мера средней кинетической энергии движения молекул.
В опытах Шарлем была найдена зависимость p от t. Эта же зависимость будет и между р и Т: т.е. между р и Т прямопропорциональная зависимость.
между р и Т прямопропорциональная зависимость.
С одной стороны, давление газа прямопропорционально его температуре, с другой стороны, мы уже знаем, что давление газа прямопропорционально средней кинетической энергии поступательного движения молекул Е (p = 2/3*E*n ). Значит, Е прямопропорциональна Т.
Е = (3/2)kТ
Из этой формулы следует, что среднее значение кинетической энергии поступательного движения молекул не зависит от природы газа, а определяется только его температурой.
Так как Е = m*v2/2, то m*v2/2 = (3/2)kТ
откуда средняя квадратичная скорость молекул газа
Постоянная величина k называется постоянная Больцмана.
В СИ она имеет значение k = 1,38*10-23 Дж/К
Если подставить значение Е в формулу p = 2/3*E*n , то получим p = 2/3*(3/2)kТ* n, сократив, получим p = n* k*Т
Давление газа не зависит от его природы, а определяется только концентрацией молекул n и температурой газа Т.
Соотношение p = 2/3*E*n устанавливает связь между микроскопическими (значения определяются с помощью расчетов) и макроскопическими (значения можно определить по показаниям приборов) параметрами газа, поэтому его принято называть основным уравнением молекулярно – кинетической теории газов.
АБСОЛЮТНАЯ ТЕМПЕРАТУРА — МИФ ИЛИ РЕАЛЬНОСТЬ?
E-mail: [email protected] Физика Главная
ОГЛАВЛЕНИЕ
1. Исследования по термическому расширению газов.
2. Абсолютная шкала температур.
3. О строении и свойствах физических объектов.
3.1. Строение вещества.
3.2. Обмен энергией между физическими объектами.
3.3. Коэффициент термического расширения тел.
3.4. Изменение агрегатных состояний –
свойство материи.
4. Состояние знаний об охлаждении газов во время введения шкалы Томсона.
5. Сжиженные газы и их свойства.
6. Температура ниже абсолютного нуля.
7. Постулат Томпсона – заблуждение физической науки.
8. Философские аспекты абсолютной температуры.
9. Выводы.
a1. Исследования по термическому расширению газов.
Исследования по термическому расширению
газов проложили путь для создания шкалы абсолютной температуры. В работе [1]
приводится исторический обзор изучения теплового расширения газообразных
веществ. Многие физики 18 века проводили исследования теплового расширения
воздуха, но их данные находились в удручающем
несоответствии друг с другом. Одни приходили к выводу, что воздух расширяется
равномерно, другие – что неравномерно, и на все это накладывалась путаница
представлений. Как следует из основополагающей работы Вольты (1793 г.),
значения величины расширения при нагреве газов на один градус стоградусной
шкалы, даваемые различными экспериментаторами, имели
большие расхождения. Но Вольта пришёл к важному выводу и показал, что
расхождение между экспериментальными данными обусловлено тем, что
предшествующие экспериментаторы работали не с сухим воздухом, а с влажным.
Наличие паров воды в воздухе искажало ход явления. Вольта пользовался воздушным
термометром, и после многочисленных тщательных экспериментов, сопровождавшихся
параллельными контрольными опытами с влажным воздухом, пришел к следующему
утверждению: при нагреве на каждый градус воздух испытывает одинаковое
увеличение объема как в самом начале, вблизи температуры таяния льда, так и при
приближении к точке кипения воды. Найденное Вольта значение коэффициента
расширения равно, таким образом, 1/270 = 0,0037037 на градус Цельсия.
Как следует из основополагающей работы Вольты (1793 г.),
значения величины расширения при нагреве газов на один градус стоградусной
шкалы, даваемые различными экспериментаторами, имели
большие расхождения. Но Вольта пришёл к важному выводу и показал, что
расхождение между экспериментальными данными обусловлено тем, что
предшествующие экспериментаторы работали не с сухим воздухом, а с влажным.
Наличие паров воды в воздухе искажало ход явления. Вольта пользовался воздушным
термометром, и после многочисленных тщательных экспериментов, сопровождавшихся
параллельными контрольными опытами с влажным воздухом, пришел к следующему
утверждению: при нагреве на каждый градус воздух испытывает одинаковое
увеличение объема как в самом начале, вблизи температуры таяния льда, так и при
приближении к точке кипения воды. Найденное Вольта значение коэффициента
расширения равно, таким образом, 1/270 = 0,0037037 на градус Цельсия.
В этом же историческом обзоре [1]
сообщается, что независимо от Вольты в 1802 году Гей-Люссак предпринял исследование теплового расширения газов. Гей-Люссак в своей работе привёл неопубликованные данные Шарля. Шарль нашел, что кислород, азот,
углекислый газ и воздух расширяются одинаково в интервале температур от 0 и до
100 °С. Гей-Люссак дополнил и обобщил работу Шарля и пришел к следующему
фундаментальному утверждению: если полное увеличение объёма разделить на
число градусов, вызвавших это увеличение, то получим, принимая объём при
нулевой температуре равным единице, что увеличение объёма составляет 1/266,66
на каждый градус стоградусной шкалы. Данное Гей-Люссаком значение
коэффициента расширения 1/266,66 = 0,00375 рассматривалось как одна из наиболее
точно известных физических констант. В 1841 году появилась классическая работа Реньо, которая дала для коэффициента расширения значение
0,0036706, оставшееся почти неизменным до наших дней. В 1842 году Реньо установил, что коэффициенты расширения газов не в
точности постоянны. Газы, которые легко сжижаются, имеют больший коэффициент
расширения, и он даже увеличивается с ростом плотности.
Гей-Люссак в своей работе привёл неопубликованные данные Шарля. Шарль нашел, что кислород, азот,
углекислый газ и воздух расширяются одинаково в интервале температур от 0 и до
100 °С. Гей-Люссак дополнил и обобщил работу Шарля и пришел к следующему
фундаментальному утверждению: если полное увеличение объёма разделить на
число градусов, вызвавших это увеличение, то получим, принимая объём при
нулевой температуре равным единице, что увеличение объёма составляет 1/266,66
на каждый градус стоградусной шкалы. Данное Гей-Люссаком значение
коэффициента расширения 1/266,66 = 0,00375 рассматривалось как одна из наиболее
точно известных физических констант. В 1841 году появилась классическая работа Реньо, которая дала для коэффициента расширения значение
0,0036706, оставшееся почти неизменным до наших дней. В 1842 году Реньо установил, что коэффициенты расширения газов не в
точности постоянны. Газы, которые легко сжижаются, имеют больший коэффициент
расширения, и он даже увеличивается с ростом плотности.
В работе [2] приводятся данные измерений температурного коэффициента объёмного расширения различных газов в интервале температур от 0 до 100 ºС, полученные Гей-Люссаком: воздух – 0,003671, водород – 0,003661, окись азота – 0,003720, циан – 0,003877, двуокись углерода – 0,003710, окись углерода – 0,003669, двуокись серы – 0,003903. Опыт показывает, что при малых плотностях газов коэффициент объёмного расширения одинаков для всех газов и равен 1/273 на 1/ºС.
Таким образом, Вольта более чем за полвека до предложения Томсоном абсолютной температуры установил, что коэффициент расширения воздуха равен 0,0037037 на градус Цельсия, а Реньо в 1841 году уточнил этот результат, который стал 0,0036706. То есть цифры 270 – 273 были известны задолго до введения Томсоном термометрической шкалы.
a2. Абсолютная шкала температур.
С развитием атомистической теории и
понимания молекулярной природы газов стало понятно, что объём газа определяется скоростью его молекул [3]. Чем выше
температура и чем быстрее двигаются молекулы, тем дальше они разбегаются и тем
больше им требуется пространства. С понижением температуры газы занимают
меньший объём. У.Томсон высказал идею, что средняя энергия молекул с каждым
градусом понижается на величину 1/273 и что при охлаждении к нулю стремится не
объём газа, а его энергия. Из этого предположения вытекало, что такой
энергетической точкой является температура – 273 ºС, которая принята за абсолютный нуль, или
нуль Кельвина. У физиков возник огромный интерес попытаться достичь абсолютного
нуля. Ещё до открытия Томсона исследователи, занимавшиеся проблемой низких
температур, ставили цель получить сжиженные газы. В 20-х годах 19 века
М.Фарадей установил, что даже при обычных температурах многие газы переходят в
жидкое состояние за счёт давления, и получил жидкий хлор, двуокись серы и
аммиак.
Чем выше
температура и чем быстрее двигаются молекулы, тем дальше они разбегаются и тем
больше им требуется пространства. С понижением температуры газы занимают
меньший объём. У.Томсон высказал идею, что средняя энергия молекул с каждым
градусом понижается на величину 1/273 и что при охлаждении к нулю стремится не
объём газа, а его энергия. Из этого предположения вытекало, что такой
энергетической точкой является температура – 273 ºС, которая принята за абсолютный нуль, или
нуль Кельвина. У физиков возник огромный интерес попытаться достичь абсолютного
нуля. Ещё до открытия Томсона исследователи, занимавшиеся проблемой низких
температур, ставили цель получить сжиженные газы. В 20-х годах 19 века
М.Фарадей установил, что даже при обычных температурах многие газы переходят в
жидкое состояние за счёт давления, и получил жидкий хлор, двуокись серы и
аммиак.
В 1848 г. Томсон ввел «абсолютную
термометрическую шкалу» [4]. Он объяснил ее название следующим образом:
«Для этой шкалы характерна полная независимость от физических свойств
какого-либо конкретного вещества». Томсон отмечает, что «бесконечный
холод должен соответствовать конечному числу градусов воздушного термометра ниже
нуля», а именно: точке, «соответствующей объему воздуха, уменьшенному до
нуля, что будет отмечено на шкале как – 273 °С».
Он объяснил ее название следующим образом:
«Для этой шкалы характерна полная независимость от физических свойств
какого-либо конкретного вещества». Томсон отмечает, что «бесконечный
холод должен соответствовать конечному числу градусов воздушного термометра ниже
нуля», а именно: точке, «соответствующей объему воздуха, уменьшенному до
нуля, что будет отмечено на шкале как – 273 °С».
Самой низкой температурой, или еще так называемым «абсолютным нулем», считается нуль градусов по шкале Кельвина [5]. В рамках применимости термодинамики абсолютный нуль на практике недостижим. Его существование и положение на температурной шкале следует из экстраполяции наблюдаемых физических явлений, при этом такая экстраполяция показывает, что при абсолютном нуле энергия теплового движения молекул и атомов вещества должна быть равна нулю, то есть хаотическое движение частиц прекращается вообще.
Абсолютный нуль температуры – минимальный предел температуры, которую может иметь физическое
тело во Вселенной [6].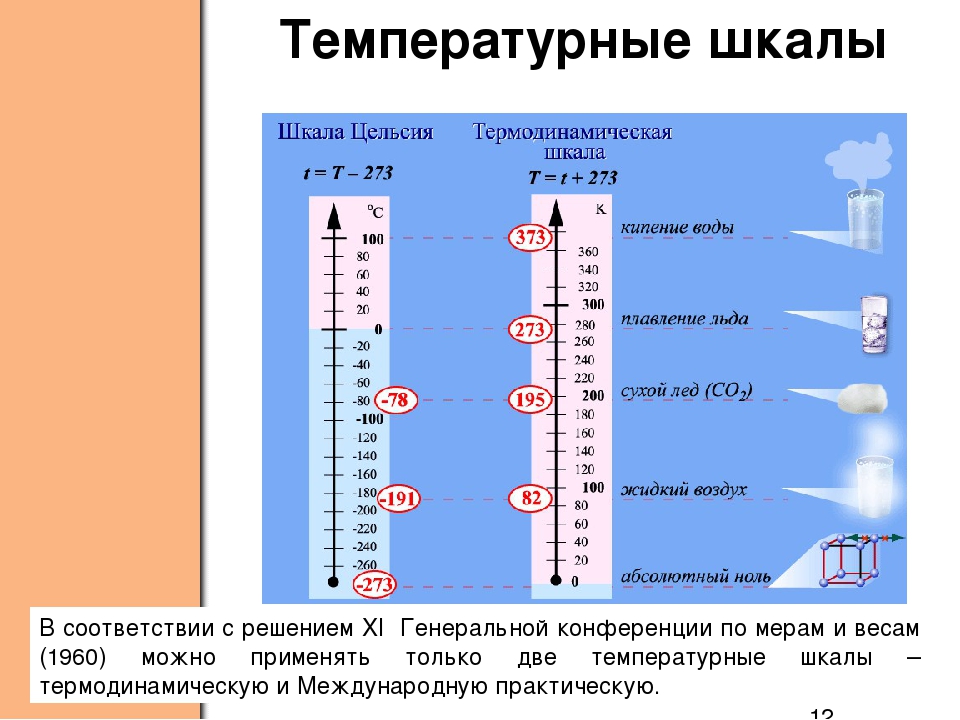 Абсолютный нуль служит началом отсчёта абсолютной
температурной шкалы, например, шкалы Кельвина. В 1954 году X Генеральная
конференция по мерам и весам установила термодинамическую температурную шкалу с
одной реперной точкой – тройной точкой воды,
температура которой принята 273,16 К. На практике абсолютный нуль недостижим. Его существование и положение на температурной шкале
следует из экстраполяции наблюдаемых
физических явлений. Экстраполяция показывает, что при абсолютном нуле энергия теплового
движения молекул и атомов вещества должна быть равна нулю, то есть хаотическое движение частиц прекращается, и они
образуют упорядоченную структуру, занимая чёткое положение в узлах кристаллической решётки. Однако, с точки зрения квантовой
физики и при абсолютном нуле температуры существуют нулевые колебания, которые обусловлены квантовыми свойствами частиц и физического
вакуума, их окружающего.
Абсолютный нуль служит началом отсчёта абсолютной
температурной шкалы, например, шкалы Кельвина. В 1954 году X Генеральная
конференция по мерам и весам установила термодинамическую температурную шкалу с
одной реперной точкой – тройной точкой воды,
температура которой принята 273,16 К. На практике абсолютный нуль недостижим. Его существование и положение на температурной шкале
следует из экстраполяции наблюдаемых
физических явлений. Экстраполяция показывает, что при абсолютном нуле энергия теплового
движения молекул и атомов вещества должна быть равна нулю, то есть хаотическое движение частиц прекращается, и они
образуют упорядоченную структуру, занимая чёткое положение в узлах кристаллической решётки. Однако, с точки зрения квантовой
физики и при абсолютном нуле температуры существуют нулевые колебания, которые обусловлены квантовыми свойствами частиц и физического
вакуума, их окружающего.
В работе [7] отмечается, что физическое
понятие «абсолютный нуль температуры» имеет для современной науки чрезвычайно
большое значение: с ним тесно связано такое понятие, как сверхпроводимость. Путь к абсолютному нулю температур проложили А. Цельсий и Ж. Гей-Люссак. В 1742
году шведский астроном А. Цельсий предложил свою температурную шкалу, где
основными точками стали температура таяния льда и кипения воды. В
1802 году французский ученый Ж. Гей-Люссак обнаружил, что объем массы газа при
постоянном давлении находится в прямой зависимости от температуры. Но самое
любопытное состояло в том, что при изменении температуры на 10 по шкале
Цельсия, объем газа увеличивался или уменьшался на одну и ту же величину.
Произведя необходимые вычисления, Гей-Люссак установил, что эта величина
равнялась 1/273 от объема газа при температуре, равной 0 ºС.
Из этого закона следовал напрашивающийся вывод: температура, равная – 273 ºС, является
наименьшей температурой, даже подойдя к которой вплотную, достичь ее
невозможно. Именно эта температура получила название «абсолютный нуль
температуры». Более того, абсолютный нуль стал отправной точкой для создания
шкалы абсолютной температуры, активное участие в котором принял английский
физик У.
Путь к абсолютному нулю температур проложили А. Цельсий и Ж. Гей-Люссак. В 1742
году шведский астроном А. Цельсий предложил свою температурную шкалу, где
основными точками стали температура таяния льда и кипения воды. В
1802 году французский ученый Ж. Гей-Люссак обнаружил, что объем массы газа при
постоянном давлении находится в прямой зависимости от температуры. Но самое
любопытное состояло в том, что при изменении температуры на 10 по шкале
Цельсия, объем газа увеличивался или уменьшался на одну и ту же величину.
Произведя необходимые вычисления, Гей-Люссак установил, что эта величина
равнялась 1/273 от объема газа при температуре, равной 0 ºС.
Из этого закона следовал напрашивающийся вывод: температура, равная – 273 ºС, является
наименьшей температурой, даже подойдя к которой вплотную, достичь ее
невозможно. Именно эта температура получила название «абсолютный нуль
температуры». Более того, абсолютный нуль стал отправной точкой для создания
шкалы абсолютной температуры, активное участие в котором принял английский
физик У. Томсон. Его основное исследование касалось доказательства того, что ни
одно тело в природе не может быть охлаждено ниже, чем абсолютный нуль. При этом
он активно использовал второй закон термодинамики, поэтому, введенная им в 1848 году
абсолютная шкала температур стала называться термодинамической или «шкалой
Кельвина». Основной физический смысл абсолютного нуля состоит в том, что,
согласно физическим законам, при такой температуре энергия движения
элементарных частиц, таких как атомы и молекулы, равна нулю, и в этом случае
должно прекратиться любое хаотическое движение частиц. При температуре, равной
абсолютному нулю, атомы и молекулы должны занять чёткое положение в основных
пунктах кристаллической решетки, образуя упорядоченную систему.
Томсон. Его основное исследование касалось доказательства того, что ни
одно тело в природе не может быть охлаждено ниже, чем абсолютный нуль. При этом
он активно использовал второй закон термодинамики, поэтому, введенная им в 1848 году
абсолютная шкала температур стала называться термодинамической или «шкалой
Кельвина». Основной физический смысл абсолютного нуля состоит в том, что,
согласно физическим законам, при такой температуре энергия движения
элементарных частиц, таких как атомы и молекулы, равна нулю, и в этом случае
должно прекратиться любое хаотическое движение частиц. При температуре, равной
абсолютному нулю, атомы и молекулы должны занять чёткое положение в основных
пунктах кристаллической решетки, образуя упорядоченную систему.
В работе [8] задаётся вопрос: если
предельную температуру, при которой объем идеального газа
становится равным нулю, принимают за абсолютный нуль температуры, но объем
реальных газов при абсолютном нуле температуры обращаться в нуль не может,
имеет ли смысл предельное значение температуры? И отвечают на вопрос:
предельная температура, существование которой вытекает из закона Гей-Люссака,
имеет смысл, так как практически можно приблизить свойства реального газа к
свойствам идеального. Для этого надо брать все более разреженный газ, так чтобы
его плотность стремилась к нулю. У такого газа, действительно, объем с
понижением температуры будет стремиться к нулю. Английский ученый У. Кельвин
ввел абсолютную шкалу температур. Нулевая температура по шкале Кельвина
соответствует абсолютному нулю, и единица температуры по этой шкале равна градусу
по шкале Цельсия. С точки зрения
молекулярно-кинетической теории абсолютная температура связана со средней
кинетической энергией хаотического движения атомов или молекул, при температуре
0 ºК тепловое движение
молекул прекращается.
Для этого надо брать все более разреженный газ, так чтобы
его плотность стремилась к нулю. У такого газа, действительно, объем с
понижением температуры будет стремиться к нулю. Английский ученый У. Кельвин
ввел абсолютную шкалу температур. Нулевая температура по шкале Кельвина
соответствует абсолютному нулю, и единица температуры по этой шкале равна градусу
по шкале Цельсия. С точки зрения
молекулярно-кинетической теории абсолютная температура связана со средней
кинетической энергией хаотического движения атомов или молекул, при температуре
0 ºК тепловое движение
молекул прекращается.
Что же пишет сам У.Томсон (Кельвин) об
абсолютной шкале температур. Он в работе [9] отмечает, что в настоящее время мы
обладаем настолько полным практическим решением определения температуры,
насколько это может быть желательно даже для наиболее точных изысканий. Однако теория
термометрии ещё весьма далека от удовлетворительного состояния. Совершенный
термометр должен показывать равные приращения теплоты, как соответствующие
равным приростам температуры, оцениваемым по числу делений этой шкалы. Но,
установлен как экспериментально доказанный факт, что термометрия на этих
условиях невозможна, и мы остались без
какого-либо принципа, на котором можно было бы основать абсолютную
термометрическую шкалу. И хотя мы имеем точный принцип создания определенной
системы для оценки температуры, нельзя считать, что получили абсолютную шкалу,
можно рассматривать эту реально принятую шкалу лишь как условное множество
оцифрованных точек отсчета, достаточно близкое к требованиям термометрии.
Поэтому при современном состоянии физической науки возникает исключительно
интересный вопрос: существует ли какой-либо принцип, на котором может быть
основана абсолютная термометрическая шкала? Представляется, что теория Карно о
движущей силе тепла позволяет нам дать на него утвердительный ответ.
Совершенный
термометр должен показывать равные приращения теплоты, как соответствующие
равным приростам температуры, оцениваемым по числу делений этой шкалы. Но,
установлен как экспериментально доказанный факт, что термометрия на этих
условиях невозможна, и мы остались без
какого-либо принципа, на котором можно было бы основать абсолютную
термометрическую шкалу. И хотя мы имеем точный принцип создания определенной
системы для оценки температуры, нельзя считать, что получили абсолютную шкалу,
можно рассматривать эту реально принятую шкалу лишь как условное множество
оцифрованных точек отсчета, достаточно близкое к требованиям термометрии.
Поэтому при современном состоянии физической науки возникает исключительно
интересный вопрос: существует ли какой-либо принцип, на котором может быть
основана абсолютная термометрическая шкала? Представляется, что теория Карно о
движущей силе тепла позволяет нам дать на него утвердительный ответ. Поскольку
мы независимо располагаем определенной системой для измерения количеств
теплоты, нам представляется и мера для интервалов, в соответствии с которой
могут оцениваться абсолютные разности температур. В соответствии с формулами
Карно для различных частей шкалы рассчитаны величины механического действия,
вызванного опусканием единицы теплоты на один градус воздушного термометра.
Полученные результаты весьма определенно показывают, что величина, которую мы с
большим основанием можем назвать градусом воздушного термометра, зависит от
того, в какой части шкалы она берется. Характерное свойство той шкалы, которую я теперь предлагаю, состоит в том, что все
градусы имеют одну и ту же величину, т. е. единица теплоты, опускающаяся от
тела А с температурой Т по этой шкале к телу В с
температурой (Т – 1), должна создавать одно и то же механическое действие,
каким бы ни было число Т. Такая шкала справедливо
может быть названа абсолютной, поскольку ее характеристика совершенно не
зависит от физических свойств какого-либо конкретного вещества.
Поскольку
мы независимо располагаем определенной системой для измерения количеств
теплоты, нам представляется и мера для интервалов, в соответствии с которой
могут оцениваться абсолютные разности температур. В соответствии с формулами
Карно для различных частей шкалы рассчитаны величины механического действия,
вызванного опусканием единицы теплоты на один градус воздушного термометра.
Полученные результаты весьма определенно показывают, что величина, которую мы с
большим основанием можем назвать градусом воздушного термометра, зависит от
того, в какой части шкалы она берется. Характерное свойство той шкалы, которую я теперь предлагаю, состоит в том, что все
градусы имеют одну и ту же величину, т. е. единица теплоты, опускающаяся от
тела А с температурой Т по этой шкале к телу В с
температурой (Т – 1), должна создавать одно и то же механическое действие,
каким бы ни было число Т. Такая шкала справедливо
может быть названа абсолютной, поскольку ее характеристика совершенно не
зависит от физических свойств какого-либо конкретного вещества. Это то, что мы
могли предвидеть, поскольку считаем, что бесконечный холод должен
соответствовать конечному числу градусов воздушного термометра ниже нуля. Если
мы доведем строгий принцип градуировки достаточно далеко, то достигнем точки, соответствующей
объему воздуха, уменьшенному до нуля, что будет отмечено на шкале как – 273° (полученные как – 100/0,366, если 0,366 есть коэффициент
расширения). Поэтому – 273° воздушного
термометра – это точка, которой не может достигнуть никакая конечная
температура, сколь бы низкой она ни была.
Это то, что мы
могли предвидеть, поскольку считаем, что бесконечный холод должен
соответствовать конечному числу градусов воздушного термометра ниже нуля. Если
мы доведем строгий принцип градуировки достаточно далеко, то достигнем точки, соответствующей
объему воздуха, уменьшенному до нуля, что будет отмечено на шкале как – 273° (полученные как – 100/0,366, если 0,366 есть коэффициент
расширения). Поэтому – 273° воздушного
термометра – это точка, которой не может достигнуть никакая конечная
температура, сколь бы низкой она ни была.
a3. О строении и свойствах физических объектов.
Процесс охлаждения физического объекта –
сложное явление, и для того чтобы понять его сущность, необходимо иметь
представления, прежде всего, о строении вещества. Охлаждение предопределяет
обмен энергией между объектом и окружающей средой, поэтому надо знать физику
процесса теплопередачи. При изменении температуры тела изменяются его
геометрические размеры и, соответственно, объём, поэтому правильное понимание
физики процесса позволит безошибочно определить коэффициенты расширения в
каждом температурном диапазоне. Необходимо также знание о фазовых переходах при
охлаждении физических объектов от газообразного состояния до твёрдого тела и,
наоборот, при нагревании от твёрдого тела до газа.
При изменении температуры тела изменяются его
геометрические размеры и, соответственно, объём, поэтому правильное понимание
физики процесса позволит безошибочно определить коэффициенты расширения в
каждом температурном диапазоне. Необходимо также знание о фазовых переходах при
охлаждении физических объектов от газообразного состояния до твёрдого тела и,
наоборот, при нагревании от твёрдого тела до газа.
3.1. Строение вещества.
Абсолютно все физические объекты устроены
так, как стекло в расплавах (жидкости) и в твёрдых телах [10]. Аналогичное
устройство имеют и газы. Основой строения всех физических тел, элементарных химических
веществ и их смесей, является коллективная химическая связь. Атомы в любой
структуре создают физическое поле и располагаются в соответствии своих
электрических зарядов, фактически не создавая молекул. Стехиометрический состав
физического объекта можно считать формулой вещества в привычном для химии виде.
Устройство всех физических объектов универсально. В жизни мы привыкли видеть физические объекты природы при нормальных условиях температуры и давления в обычных пределах в виде газов, жидкостей и твёрдых тел. В ряде случаев можно, даже в быту, наблюдать переход материи из одного состояния в другое. Наиболее характерным веществом, способным находиться в бытовых условиях в трёх состояниях материи, является вода в виде жидкости, пара и льда. Так же, как и вода, и другие физические объекты могут иметь различные агрегатные состояния в зависимости от внешних условий: температуры и давления. Каждый физический объект можно перевести в любое агрегатное состояние.
В силовом электрическом поле физического
объекта принцип построения структуры – создание конструкции с минимальной
потенциальной энергией. Так устроены элементарные вещества и их смеси. Смеси могут быть разнообразными: твёрдое тело – твёрдое тело,
твёрдое тело – жидкость (структурная), жидкость – жидкость, жидкость – твёрдое
тело, жидкость – газ, газ – газ, газ – жидкость и так далее. Примерами
таких объектов являются горные породы, сплавы металлов, растворы, морская вода
(растворённые газы и соли), воздух (смесь газов), влажный воздух (газ и вода).
Примерами
таких объектов являются горные породы, сплавы металлов, растворы, морская вода
(растворённые газы и соли), воздух (смесь газов), влажный воздух (газ и вода).
Все тела в любом агрегатном состоянии имеют строго определённую структуру с минимумом потенциальной энергии. Физическое поле определяет структуру любого объекта и чутко реагирует на изменение внешних условий: изменяется потенциальная энергия объекта, а вместе с ней расположение атомов структуры вплоть до перехода в иное агрегатное состояние.
3.2. Обмен энергией между физическими объектами.
Если температура всех тел в замкнутом
пространстве равна, не происходит процессов излучения и поглощения энергии
между ними [11]. Это означает, что электроны на орбитах атомов не излучают. Но
только стоит появиться нагретому телу, например, включить электрическую
лампочку или утюг, немедленно возникает разность потенциалов состояния и
появляется тепловой поток. Неукоснительное свойство физических объектов –
выравнивание потенциалов состояния. Горячее тело излучает энергию, окружающая
среда поглощает её. Передача энергии от одного физического объекта другому
осуществляется единственным универсальным способом – через электромагнитные
волны.
Неукоснительное свойство физических объектов –
выравнивание потенциалов состояния. Горячее тело излучает энергию, окружающая
среда поглощает её. Передача энергии от одного физического объекта другому
осуществляется единственным универсальным способом – через электромагнитные
волны.
Что же происходит с телами, окружающими источник энергии и самим источником? За счёт подведённой энергии электроны источника излучения работают как генераторы излучения, а электроны тел окружающей среды – как приёмники излучения. Процесс теплопередачи идёт до тех пор, пока есть разность потенциалов состояния, то есть до выравнивания температур.
Физические объекты излучают и поглощают
энергию только поверхностью. Излучение и поглощение энергии возможно на границе
раздела между телами или внутри тела между соседними атомами при наличии
градиента температур. Чем больше поверхность излучающего или поглощающего тела,
тем интенсивнее идёт процесс.
Какова физика процессов передачи энергии в
массивных телах? Процесс излучения энергии складывается из процессов излучения
и поглощения энергии между соседними слоями атомов и теле. Электроны служат
только трансляторами энергии. При излучении энергии электроны наружного слоя
тела при вращении вокруг собственной оси на первой полуволне излучают
электромагнитные волны, а на второй полуволне поглощают энергию от электронов
рядом лежащего атома, чтобы на следующей полуволне снова излучить её. Излучение
и поглощение энергии происходит на границе двух атомных слоёв физического тела,
имеющих различные потенциалы состояния, т.е. при наличии разности потенциалов
или, что равносильно, разности температур. Так, за слоем слой, продолжается
процесс излучения горячего тела через акты излучения – поглощения до выравнивания
потенциалов состояния. По мере остывания тела уменьшается мощность излучаемой
энергии и изменяется спектр волн электромагнитных колебаний.
Таким же образом происходит поглощение энергии, только в этом случае часть энергии идёт на выравнивание потенциалов состояния. Каждый электрон тела периодически поглощает и излучает энергию. Иначе не прогреется весь объём нагреваемого тела. Когда от источника тепла нагревается первый слой атомов, он начинает излучать энергию второму слою и т.д. Таким образом, за слоем слой тело прогревается, пока имеется источник нагревания. Волновой состав поглощённой и излученной энергии идентичен. Внутренняя энергия атома изменяется аналогово.
3.3. Коэффициент термического расширения тел.
Температура твёрдого тела складывается из
температуры его атомов [12, 10]. Рассмотрим отдельно взятый атом с одним
электроном – атом водорода. Если к этому атому подводить тепло, нет сил, в
результате действия которых атом начнёт совершать тепловые колебания, то есть
изменять своё местонахождение. Но атом отреагирует на подвод к нему внешней
энергии: электрон в атоме возбудится и перейдёт из основного уровня при
комнатной температуре с наименьшей энергией на более высокий энергетический
уровень. При дальнейшем подводе тепла повторится такой переход, и электрон
перейдёт на ещё более высокий уровень. При охлаждении атома идёт обратный
процесс.
Но атом отреагирует на подвод к нему внешней
энергии: электрон в атоме возбудится и перейдёт из основного уровня при
комнатной температуре с наименьшей энергией на более высокий энергетический
уровень. При дальнейшем подводе тепла повторится такой переход, и электрон
перейдёт на ещё более высокий уровень. При охлаждении атома идёт обратный
процесс.
Таким образом, нагревание тела – процесс, при котором электроны составляющих его атомов или ионов из всех атомных оболочек устойчивого состояния, соответствующего минимально возможному значению его энергии, переходят на более высокие атомные орбитали.
Температура тела определяется состоянием атомных орбиталей атомов или ионов, входящих в его структуру. Чем более высокие атомные орбитали занимают электроны в атомах (ионах) тела, тем выше его температура.
При переходе электронов на более высокие орбитали увеличиваются геометрические размеры атомов, что
приводит к уменьшению силы химических связей между всеми структурными
элементами тела и отдалению их друг от друга. При нагревании любых тел
расстояния между центрами атомов увеличивается, а ослабление химических связей
приводит к снижению механической прочности нагретых твёрдых тел (например:
ковка металлов). Хотя расстояние между центрами атомов при нагревании
увеличивается, но при этом расстояния между атомами уменьшается. Такое
предположение хорошо согласуется с повышением электросопротивления
металлов с увеличением их температуры.
При нагревании любых тел
расстояния между центрами атомов увеличивается, а ослабление химических связей
приводит к снижению механической прочности нагретых твёрдых тел (например:
ковка металлов). Хотя расстояние между центрами атомов при нагревании
увеличивается, но при этом расстояния между атомами уменьшается. Такое
предположение хорошо согласуется с повышением электросопротивления
металлов с увеличением их температуры.
Таким образом, при нагревании твёрдых тел
увеличиваются геометрические размеры атомов, и в связи с ослаблением химических
связей растёт расстояние между центрами
соседних атомов (ионов), что приводит к их тепловому расширению. Природа
термического расширения любых тел заключается в повышении энергетических уровней
атомных орбиталей атомов (ионов) за счёт подведения
внешнего тепла. При нагревании тела электроны переходят на более высокие орбитали, при этом увеличиваются размеры атомов (ионов) и
уменьшается сила химических связей между соседними атомами, что приводит к
удлинению связей и росту объёма любых тел при нагревании. Температура тела
определяется состоянием атомных орбиталей его атомов
или ионов, или, что то же, уровень атомных орбиталей атомов (ионов), составляющих тело, определяет его
температуру.
Температура тела
определяется состоянием атомных орбиталей его атомов
или ионов, или, что то же, уровень атомных орбиталей атомов (ионов), составляющих тело, определяет его
температуру.
3.4. Изменение агрегатных состояний – свойство материи.
Любому состоянию вещества должны соответствовать определённые условия (или наоборот) [10]. Такими условиями являются температура, давление и гравитационное поле. Агрегатное состояние вещества определяется, прежде всего, внутренним строением. Газообразное, жидкое и твёрдое агрегатные состояния вещества характеризуется уровнем потенциальной энергии атомов. Каждое вещество или смеси веществ способны существовать в любом агрегатном состоянии.
a4. Состояние знаний об охлаждении газов во время введения шкалы Томсона.
Проблема сжижения газов имеет вековую
историю, берущую свое начало во второй половине XVIII столетия [13]. Началось
все со сжижения аммиака простым охлаждением, которое произвел ван Марум, серного ангидрида –
Монж и Клуэ, хлора – Нортмор
(1805 г.) и сжижения аммиака компрессионным методом, предложенным Баччелли (1812 г.). Определяющий
вклад в решение этой проблемы одновременно и независимо внесли Шарль Каньяр де Латур (1777 – 1859) и
Майкл Фарадей (1791 – 1867). В серии работ, опубликованных в 1822 и 1823
гг., Каньяр де Латур описал
опыты, проведенные им для определения существования для жидкости некоторого
предельного расширения, дальше которого независимо от приложенного давления вся
она переходит в парообразное состояние. Более конкретный
результат содержали опыты Фарадея, проведенные в 1823 году с загнутыми
стеклянными трубками, более длинное плечо которых было
запаяно. Нагревая в трубке бикарбонат натрия, Фарадей получил жидкую углекислоту,
таким же способом он получал жидкий сероводород, хлористый водород, серный
ангидрид и др.
Началось
все со сжижения аммиака простым охлаждением, которое произвел ван Марум, серного ангидрида –
Монж и Клуэ, хлора – Нортмор
(1805 г.) и сжижения аммиака компрессионным методом, предложенным Баччелли (1812 г.). Определяющий
вклад в решение этой проблемы одновременно и независимо внесли Шарль Каньяр де Латур (1777 – 1859) и
Майкл Фарадей (1791 – 1867). В серии работ, опубликованных в 1822 и 1823
гг., Каньяр де Латур описал
опыты, проведенные им для определения существования для жидкости некоторого
предельного расширения, дальше которого независимо от приложенного давления вся
она переходит в парообразное состояние. Более конкретный
результат содержали опыты Фарадея, проведенные в 1823 году с загнутыми
стеклянными трубками, более длинное плечо которых было
запаяно. Нагревая в трубке бикарбонат натрия, Фарадей получил жидкую углекислоту,
таким же способом он получал жидкий сероводород, хлористый водород, серный
ангидрид и др. Фарадей был уверен, что рано или поздно удастся получить твердый
водород, полагал, что одного давления недостаточно для сжижения некоторых
газов, прозванных тогда «перманентными» или «неукротимыми». В 1845 г. Фарадей высказал это соображение Реньо.
Фарадей был уверен, что рано или поздно удастся получить твердый
водород, полагал, что одного давления недостаточно для сжижения некоторых
газов, прозванных тогда «перманентными» или «неукротимыми». В 1845 г. Фарадей высказал это соображение Реньо.
Любой газ можно превратить в жидкость
простым сжатием, если только его температура ниже критической [14]. Первый газ
(аммиак) был обращен в жидкость уже в 1799 г. Дальнейшие успехи в сжижении
газов связаны с именем английского физика М. Фарадея, который сжижал газы путем
их одновременного охлаждения и сжатия. Ко второй половине XIX века из всех
известных в то время газов остались не обращенными в жидкость только шесть:
водород, кислород, азот, оксид азота, оксид углерода и метан, – их назвали
постоянными газами. Задержка в сжижении этих газов еще на четверть столетия
произошла потому, что техника понижения температуры была развита слабо, и они
не могли быть охлаждены до температуры ниже критической. Когда физики научились
получать температуры порядка 1 ºК,
удалось все газы, в том числе и гелий, обратить не только в жидкое, но и в
твердое состояние. Превращение всех газов в жидкое состояние лишний раз
подтвердило единство в строении веществ. Оно показало, что состояние вещества
зависит от его температуры и давления, а не определено раз и навсегда для
данного тела.
Когда физики научились
получать температуры порядка 1 ºК,
удалось все газы, в том числе и гелий, обратить не только в жидкое, но и в
твердое состояние. Превращение всех газов в жидкое состояние лишний раз
подтвердило единство в строении веществ. Оно показало, что состояние вещества
зависит от его температуры и давления, а не определено раз и навсегда для
данного тела.
После окончания университета в 1845 году Томсон
стажировался в лаборатории известного
экспериментатора В. Реньо в области физики тепловых
явлений [15, 16], и на время
предложения абсолютной шкалы температур должен был знать о достижениях физики
по охлаждению газов. В 1852 году сам Томсон совместно с Джоулем
производит известное исследование по охлаждению газов при расширении без
совершения работы, которое послужило переходной ступенью от теории газов
идеальных к теории действительных газов [17]. К 1848 году уже были сжижены многие газы, тем не менее,
Томсону пришла сумасбродная мысль решить идею абсолютной температуры через
коэффициенты объёмного термического расширения некоторых газов в газообразном
состоянии.
a5. Сжиженные газы и их свойства.
Жидкий водород удалось получить Д. Дьюару только в 1900 году по новой схеме охлаждения, предложенной Кельвином-Томсоном и Дж. Джоулем [3]. Было показано, что даже в естественном состоянии газ можно охладить, если дать ему резко расшириться и одновременно изолировать от внешнего нагрева. С помощью этого метода, повторяя этот цикл ещё и ещё раз, сжатый водород при температуре – 240 ºС был переведен в жидкое состояние. Продолжая ступенчатое охлаждение и дальше, Дьюар сумел получить водород и в твёрдом состоянии.
Азот в жидком состоянии находится при температуре ниже – 195,8 ºС. При охлаждении до 209,86 ºС жидкий азот переходит в твёрдое состояние в виде снегоподобной массы или больших белоснежных кристаллов [18].
Жидкий кислород имеет умеренно криогенные
свойства с точкой замерзания – 222,65 ºС и точкой кипения – 182,96 ºС. Коэффициент расширения кислорода при смене жидкого агрегатного состояния на
газообразное составляет 1:860 при 20 ºС [19].
Коэффициент расширения кислорода при смене жидкого агрегатного состояния на
газообразное составляет 1:860 при 20 ºС [19].
При стандартном атмосферном давлении азот имеет температуру кипения – 196 ºС [20]. Жидкий азот получают из сжиженного воздуха. Температура замерзания жидкого азота – 210 ºС. Коэффициент объёмного расширения жидкого азота равен 694: из одного объёма жидкого газа при испарении получается 694 объёма газа.
Температурные коэффициенты объёмного расширения жидкостей приведены в работе [21]: воздух жидкий (в интервале от –259 до –253 ºС) – 0,00015, кислород жидкий (в интервале от –205 до –184 ºС) – 0,00385.
Тепловое расширение вещества
характеризуется коэффициентом объёмного расширения, его числовые значения
сильно зависят от температуры и давления [22]. Для жидкостей значения
коэффициента при одинаковых температурах могут меняться весьма значительно. Так
для жидкой углекислоты при повышении температуры от 0 до 20 ºС коэффициент теплового расширения 0,0105
возрастает вдвое. Увеличение давления несколько снижает его значение.
Увеличение давления несколько снижает его значение.
Объемные коэффициенты теплового расширения твердой углекислоты в диапазоне температур от –56 до –80 град. имеют значения от 0,001855 до 0,001170 [23].
a6. Температура ниже абсолютного нуля.
Британский физик лорд Кельвин создал шкалу абсолютной температуры и
определил, что ничто не может быть
холоднее, чем абсолютный ноль [24]. Если частицы находятся при
температуре абсолютного нуля, они прекращают движение, и у них отсутствует
энергия. Температура объекта – мера того, насколько интенсивно атомы движутся.
Чем холоднее объект, тем медленнее движение атомов. При температуре абсолютного
нуля атомы перестают двигаться. Однако учёные из Университета
Людвига-Максимилиана в Мюнхене и Институте квантовой оптики Макса Планка в Гархинге создали газ, который стал холоднее абсолютного
нуля на несколько нанокельвинов. Они охладили около 100 000 атомов до положительной температуры нескольких нанокельвинов и использовали сеть лазерных лучей и
магнитных полей, чтобы контролировать поведение атомов, и подтолкнуть их к
новому пределу температуры.
Они охладили около 100 000 атомов до положительной температуры нескольких нанокельвинов и использовали сеть лазерных лучей и
магнитных полей, чтобы контролировать поведение атомов, и подтолкнуть их к
новому пределу температуры.
Об этих же достижениях немецких физиков сообщается в работе [25]. Учёные создали квантовое облако атомов калия, распределение энергии в котором таково, что его температура имеет отрицательное абсолютное значение.
Об абсурдности абсолютного нуля температур говорится в работе [26]. Вывод по логике физики: элементарная частица, которую привели в состояние абсолютного покоя, приводится на порог своего существования, ей перекрыта энергетическая подпитка, и она должна исчезнуть, то есть аннигилировать, выделив энергию e = mc2! Таким образом, тело, охлаждённое до нуля по Кельвину, превращается в бомбу.
Интересна работа [27], в которой автор сообщает, что по американскому научно-популярному телеканалу прошла удивительная информация – там, где летают американские космические аппараты, температура на 13 градусов ниже абсолютного нуля. На первый взгляд – это очевидный бред, поскольку из физики известно, что температуры ниже абсолютного нуля быть не может. Сам абсолютный ноль отражает прекращение колебательного движения электронов в атомах замороженного вещества. При остановке колебательного движения любого тела невозможно задать этому телу более высокую степень остановки, чтобы таким образом получить более высокую степень отрицательности температуры. С другой стороны, из физики известно, что электрон состоит из составных частей, колебания которых не останавливаются вместе с прекращением таковых электроном. Следовательно, есть следующий горизонт, при достижении которого можно вновь говорить об охлаждении этой части вещества – составных частей электрона.
a7. Постулат Томпсона – заблуждение физической науки.
Томсон предложил абсолютную шкалу температур, в которой все градусы имеют одну и ту же величину. Характеристика такой шкалы совершенно не зависит от физических свойств какого-либо конкретного вещества. Бесконечный холод должен соответствовать конечному числу градусов воздушного термометра ниже нуля. Если мы доведем строгий принцип градуировки достаточно далеко, то достигнем точки, соответствующей объему воздуха, уменьшенному до нуля, что будет отмечено на шкале как минус 273° (полученные как – 100/0,366, если 0,366 есть коэффициент расширения). Поэтому – 273 °С воздушного термометра – это точка, которой не может достигнуть никакая конечная температура, сколь бы низкой она ни была [9].
Одержимый идеей об абсолютной температуре в природе Томсон не смог отказаться от неё, хотя к реализации идеи не было никаких предпосылок. В предложенной Томсоном абсолютной температуре некорректно поставлена задача и ещё более некорректно реализовано её решение. Томпсон без всякого обоснования установил отрицательную абсолютную температуру минус 273 градуса совершенно анекдотическим образом.
Постулат Томсона прост – он предположил, что когда объём некоторых газов, имеющих коэффициент термического расширения 0,00366, при охлаждении уменьшится до нуля, это будет абсолютная отрицательная температура. Ниже абсолютной температуры – 273 ºС материальные объекты охладить нельзя.
Мечта Томсона оказалась сильнее здравого смысла. Желание найти абсолютную точку холода победило истину, Томсон проявил дилетантский подход, не совместимый с физическим мышлением. Термическое сужение некоторых газов при охлаждении до нулевого объёма не является ошибкой Томсона, а осознанным введением науки в преднамеренную ложь.
Интерполяция коэффициента расширения газов в диапазоне 0 – 100 ºС в область низких температур неправомерна. По крайней мере, наивно полагать, что коэффициент термического расширения газов в диапазоне температур 0 – 100 ºС будет распространяться вплоть до температуры – 273 ºС. Если при 0 – 100 ºС газ находится в газообразном состоянии, то по мере снижения температуры газ переходит в жидкое, и далее в твёрдое состояния с совершенно иными коэффициентами термического расширения.
В предложении абсолютной шкалы температуры есть целый ряд ошибок. Ведь существуют иные газы с отличительными от принятого Томсоном коэффициентами термического расширения, например двуокись углерода – 0,003726 [28]. Кроме того, Томсон хорошо знал (раздел 4), что при понижении температуры газы переходят в жидкое, а затем в твёрдое агрегатное состояние. К примеру, объемные коэффициенты теплового расширения твёрдой углекислоты в диапазоне температур от –56 до –80 град. имеют значения от 0,001855 до 0,001170 [23]. Следуя логике Томсона, абсолютная температура, рассчитанная по коэффициентам термического расширения твёрдой углекислоты должна быть 1/0,001855 = 539 или 1/0,001170 = 854,7 градусов Цельсия.
Но в природе существуют жидкости и твёрдые тела. Если же по этой методике определить абсолютную температуру для воды и алюминия, значения будут резко отличаться от температуры Томсона. Для воды 1/0,00021 = 4761,9, а для алюминия 1/0,000024 = 41666,6 градусов Цельсия [29].
Английский физик У. Томсон принял участие в создании шкалы абсолютной температуры, отмечается в работе [7]. И ввёл физическую науку в заблуждение. Жанр сказки недопустим в физике. Абсолютная температура – 273 ºС – невообразимая глупость, не совместимая со здравым смыслом. Но эта сказка овладела массами физиков, вошла в школьные учебники и не вызывает сомнений. Абсолютная температура – ничем не обоснованная выдумка, которая ввергла в обман и увела физику на ложный путь, начиная с 1848 года, и по сей день.
Фактически шкала температур Кельвина есть шкалой температур Цельсия с произвольно назначенным нулём, который назван абсолютной температурой. В шкале Цельсия нуль можно перенести в любую иную точку. Важно, что градус есть 1/100 от показаний термометра между таянием льда и кипением воды. Шкала Томсона – это шкала Цельсия.
Достичь нельзя только бесконечности. Но, если нельзя достичь абсолютной температуры, выраженной конкретной цифрой, то это – фикция. Вклад Томсона в шкалу абсолютных температур – необоснованный вымысел об абсолютном нуле.
Удивляет физическое сообщество, которое приняло ложь за благодать и уже более 150 лет не желает искать истины. Как можно всерьёз принять такую нелепицу как абсолютная температура? Хотя многие публикации, скрашивая большое заблуждение Томсона, и пишут, что он обосновал абсолютную температуру, но такие заявления безосновательны. Почему-то физики упорно хранят ошибки учёных предыдущих поколений. Такой подход к наследию прошлого уводит физику далеко от истины.
Мечта Томсона осуществилась, когда была изобретена термопара, и можно было измерять температуру не по объёмному расширению рабочего тела в термометре, а по состоянию внутренней энергии вещества. Но в термометрии не произошло революции: не термометры были отградуированы по термопаре, а термопары всех типов были отградуированы по термометру.
При абсолютном нуле энергия теплового движения молекул и атомов вещества должна быть равна нулю, то есть хаотическое движение частиц прекращается, и они образуют упорядоченную структуру, занимая чёткое положение в узлах кристаллической решётки [6].
Если во времена Томсона, когда ещё не было известно строение атома, прекращение теплового движения в физическом объекте было допустимо объяснять с позиций молекулярно-кинетической теории, то в настоящее время это – нонсенс. В работах [11,10,30] показано, что молекулярно-кинетическая теория – профанация науки, и всё, что с ней связано – ложь. Все выводы, сделанные на основе МКТ, не соответствуют истине.
МКТ совершенно бессильна объяснить физику процесса изменения какого-либо физико-механического свойства вещества. Все математические выводы, относящиеся к МКТ и абсолютной температуре Кельвина, ошибочны и бесполезны для науки. Рудиментом МКТ является абсолютная отрицательная температура.
Температура – характеристика состояния вещества, свойство материи, которое выражается внутренней энергией физического объекта. Внутренняя энергия определяется высотой орбит электронов над ядром. Снижение температуры физического объекта – уменьшение его потенциальной энергии, что выражается в переходе электронов на позиции с меньшими радиусами и, соответственно, сопровождается уменьшением объёма.
Но понижение температуры тела ни коим образом не влияет на электрические и магнитные характеристики атома. Как магнитное поле протона вело электроны вокруг ядра, с такой же скоростью электроны будут вращаться при сколь угодно низких температурах. Так как электрон является средством передачи – приёма энергии, прекращение движения при абсолютном нуле Томсона свидетельствует о том, что эта материя уже никогда не способна нагреться при любой сверхвысокой температуре.
Нематериальная субстанция (абстракция по работе [30]) не подвержена воздействию температуры и давления. Заряду, магнитному и электромагнитному полям безразлично, какая температура и давление. Они стабильны и могут изменяться лишь под действием абстракции.
О несоответствии истине абсолютного нуля и термометрической шкалы Томсона свидетельствует факт, что температура ниже минус 273 градуса Цельсия уже получена (раздел 6). Долгое время абсолютная температура сдерживала развитие криогенной техники. Исправление этой большой ошибки в физике откроет пути для созданий совершенного оборудования и новых технологий получения низких температур.
a8. Философские аспекты абсолютной температуры.
По постулату Томсона при температуре – 273 ºС объём охлаждаемого воздуха уменьшается до нуля. При абсолютной температуре прекращается хаотическое движение частиц. Конкретное значение абсолютной температуры свидетельствует о конечности свойств: более низкой температуры быть не может.
Рассмотрим философские аспекты абсолютной температуры. Ведь материя не исчезает и не возникает!
Бесконечность или вечность существования материи во времени обусловлена ее несотворимостью и неуничтожимостью, сохранением при самых различных превращениях [31]. При этом вечность не сводится к одной только неограниченной длительности существования материи во времени. Она включает в себя бесконечную смену качественных состояний материи, возникновение новых форм движения и типов материальных систем. Любые микрообъекты обладают неисчерпаемым многообразием свойств, внутренних и внешних связей, способностью к постоянным изменениям.
Материя есть движение!
Движение есть неотъемлемое, необходимое и существенное свойство, способ существования материи [32]. «Материя без движения, – писал Ф. Энгельс, – так же немыслима, как и движение без материи». Движение представляет собой необходимое, неотъемлемое свойство материи, без которого она не может существовать. Нигде, никогда, ни при каких условиях не было ни одного материального объекта, ни одного явления, которые были бы лишены движения. Имеющиеся факты в физике подтверждают положение о связи движения с материей. При условиях близких к абсолютному нулю материальные объекты не перестают изменяться.
Любой материальный объект существует благодаря тому, что в нем воспроизводятся определенные типы движения [33]. При условии их уничтожения объект прекращает существование, переходит в другие объекты, которые, в свою очередь, характеризуются определенным набором типов и форм движения. Иначе говоря, движение внутренне присуще материи.
Материя бесконечна вширь и вглубь!
То, что материя бесконечна вширь, предполагали еще древние мыслители. Нижний предел делимости вплоть до конца XIX в. естествоиспытатели и философы видели в атоме [34]. Революция в естествознании окунула человеческое познание в неведомые глубины мироздания. Она, сделав подвижной нижнюю границу представления о строении мира, поставила вопрос о неисчерпаемости материи. Неисчерпаемость – всеобщее неотъемлемое свойство материи и её атрибутов, которое проявляется в бесконечности материи вширь и вглубь в количественном и качественном отношении; находит свое конкретное выражение в неисчерпаемости свойств, связей, взаимодействий и структур любых материальных систем.
Если отрицательная температура конечна, то и материя вглубь должна быть конечной. Но такое представление противоречит тезису о бесконечности материи вглубь. Температурная шкала Томсона, из которой вытекает, что отрицательная абсолютная температура составляет 273 градуса Цельсия, несостоятельна.
Абсолютная температура минус 273 градуса Цельсия – просто выдумка. Но материя бесконечна вглубь! Это свидетельствует, что абсолютной температуры не существует вообще, температура бесконечна как максимальная, так и минимальная. Если признать абсолютную температуру как непреложный факт, надо делать выбор: либо абсолютная температура, либо материя – конечна вглубь.
Абсолютная температура противоречит свойству материи о бесконечности вглубь, она соответствует исчерпаемости свойств физических объектов.
Исходя из положения, что материя бесконечна вширь и вглубь, а посему и бесконечны её свойства, следует неопровержимый вывод, что абсолютной температуры, положительной и отрицательной согласно шкале Цельсия, не существует. Температура бесконечна, как вширь, так и вглубь.
a9. Выводы.
1. К 1848 году уже были сжижены многие газы, тем не менее, Томсон реализовал идею абсолютной температуры через коэффициенты объёмного термического расширения некоторых газов в газообразном состоянии.
2. Томсон предположил: когда объём некоторых газов, имеющих коэффициент термического расширения 0,00366, при охлаждении уменьшится до нуля, это будет абсолютная отрицательная температура и что ниже абсолютной температуры – 273 ºС материальные объекты охладить нельзя.
3. Томсон знал, что существуют газы с иным коэффициентом термического расширения и что при понижении температуры газы переходят в жидкое, а затем в твёрдое агрегатное состояние.
4. В природе существуют жидкости и твёрдые тела. Если по методике Томсона для них определить абсолютную температуру, значения будут резко отличаться от абсолютной температуры – 273 градуса.
5. Фактически шкала температур Кельвина есть шкалой температур Цельсия с произвольно назначенным нулём, который назван абсолютной температурой.
6. Достичь нельзя только бесконечности. Но, если нельзя достичь абсолютной температуры, выраженной конкретной цифрой, то такая температура – фикция.
7. Вклад Томсона в шкалу абсолютных температур – необоснованный вымысел об абсолютном нуле.
8. Молекулярно-кинетическая теория совершенно бессильна объяснить физику процесса изменения какого-либо физико-механического свойства вещества. Все математические выводы, относящиеся к МКТ и абсолютной температуре Кельвина, ошибочны и бесполезны для науки.
9. Понижение температуры тела ни коим образом не влияет на электрические и магнитные характеристики атома. Как магнитное поле протона вело электроны вокруг ядра, с такой же скоростью электроны будут вращаться при сколь угодно низких температурах.
10. Так как электрон является средством передачи – приёма энергии, прекращение движения при абсолютном нуле Томсона свидетельствует о том, что эта материя уже никогда не способна нагреться при любой сверхвысокой температуре.
11. О несоответствии истине абсолютного нуля и термометрической шкалы Томсона свидетельствует факт, что температура ниже минус 273 градуса Цельсия уже получена.
12. Абсолютная температура минус 273 градуса Цельсия – просто выдумка. Материя бесконечна вглубь, это свидетельствует, что абсолютной температуры не существует вообще, температура бесконечна как максимальная, так и минимальная.
13. Если признать абсолютную температуру как непреложный факт, надо делать выбор: либо абсолютная температура, либо материя – конечна вглубь.
14. Абсолютная температура противоречит основным философским категориям: об не исчезновении и не возникновении материи, о движении материи и о бесконечности материи вширь и вглубь.
ССЫЛКИ НА ИСТОЧНИКИ
[1] http://pandia.ru/401674/
[2] http://festival.1september.ru/articles/585152/
[3] http://ufo-legacy.ru/absolytnii-nul-temperaturi/kriticheskaya-temperatura-zamerzaniya-gazov-ili-kak-bil-polu.php
[4] http://chippfest.blogspot.ru/2014/06/Lord-Kelvin-absolute-zero.html
[5] http://samiesamie.ru/samaya-nizkaya-temperatura-vo-vselennoy/
[6] https://ru.wikipedia.org/wiki/Абсолютный_нуль_температуры
[7] http://fb.ru/article/51890/absolyutnyiy-nol-istoriya-otkryitiya-i-osnovnoe-primenenie
[8] http://www.studfiles.ru/preview/2383541/page:28/
[9] У.Томсон (Кельвин). Об абсолютной термометрической шкале, основанной на теории Карно о движущей силе тепла и рассчитанной из наблюдений Реньо. Сборник: Классики физической науки, стр. 407– 415, М., 1989.
[10] А.И.Болутенко. http://ngipoteza.narod.ru/phys3.htm
[11] А.И.Болутенко. http://ngipoteza.narod.ru/phys2.htm
[12] А.И.Болутенко. Научные гипотезы. Физика стекла, гип. 11, 2012.
[13] http://www.portal-slovo.ru/impressionism/40427.php
[14] http://scicenter.online/osnovyi-fiziki/sjijenie-gazov-24487.html
[15] http://fizikaklass.ru/interesnoe-o-fizike/uchenie-fiziki/1168.html
[16] http://ether-wind.narod.ru/Golin_1989/
[17] http://www.great-people.ru/biog_10_kelvin.html
[18] http://www.gas-weld.ru/component/content/article/85-azot.html
[19] https://ru.wikipedia.org/wiki/Жидкий_кислород
[20] http://www.ndva.ru/gazi/zhidkiy_azot.html
[21] http://www.cryocatalog.ru/info/teplkoefliq.php
[22] http://www.physicexperts.ru/pexps-1073-1.html
[23] https://lozinskij.ru/a58134-svojstva-uglekisloty.html
[24] https://www.infoniac.ru/news/Uchenye-sozdali-gaz-s-temperaturoi-nizhe-absolyutnogo-nolya.html
[25] https://lenta.ru/news/2013/01/04/subzero/
[26] http://panteizm.chat.ru/Articles/Lozh.htm
[27] А.А. Тюняев. http://www.organizmica.org/archive/412/tnn.shtml
[28] https://www.fxyz.ru/справочные_данные/термодинамические_свойства_веществ/коэффициент_объемного_расширения_газов/
[29] http://minkor.ru/upload/spravochnik/220709-5.pdf
[30] А.И.Болутенко. http://ngipoteza.narod.ru/phys4.htm
[31] https://progs-shool.ru/kratkij-slovar-po-filosofii/184-konechnoe-i-beskonechnoe.html
[32] http://www.studfiles.ru/preview/433482/
[33] http://studbooks.net/17568/filosofiya/materiya_dvizhenie_prostranstvo_vremya_svoystva
[34] http://bookish.link/filosofiya-osnovi/neischerpaemost-materii-16995.html
14.09.2017
Температура и её измерение. Абсолютная температура.
⇐ ПредыдущаяСтр 4 из 6Следующая ⇒При тепловом равновесии 2-х тел:
— отсутствует теплообмен и фазовые переходы
— у 2-х тел одинаковы температуры и кинетические энергии молекул
— не меняются давление и объем.
Температура – физическая величина, описывающая состояние термодинамического равновесия, характеризующая интенсивность хаотического движения молекул.
Измерение температуры происходит с помощью термометров.
Термометр – прибор, в котором объем газа или жидкости, зависит от температуры.
Термометры бывают газовые и жидкостные (ртутные и спиртовые).
Термометры всегда приводят в контакт с измеряем телом до наступления теплового равновесия.
Температура – характеристика всего тела, а не отдельной молекулы.
Температурные шкалы.
Билет №8. Уравнение Менделеева-Клапейрона. Уравнение Клапейрона. Изопроцессы в газах.
Уравнение Менделеева-Клапейрона.
Это уравнение описывает состояние термодинамической системы.
Уравнение связывает между собой макропараметры определенного газа (давление , объем и температуру) с его массой.
| P – давление (Па) V – объем ( ) T – абсолютная температура (К) m – масса (кг) 𝝁 – молярная масса (кг/моль) | 𝝂 – количество вещества (моль) R – универсальная газовая постоянная R = 8,31 Дж/моль К |
• = R
• = R
Уравнение Клапейрона.
Это уравнение описывает состояние термодинамической системы при неизменной массе газа.
Уравнение связывает между собой макропараметры определенного газа (давление , объем и температуру) неизменной массы.
=
Изопроцессы в газах.
Изопроцесс — процесс, при котором один из макроскопических параметров состояния данной массы газа остается постоянным.
V , p , T
Изо – постоянный
Билет № 9. Испарение и конденсация. Насыщенные и ненасыщенные пары. Относительная влажность воздуха и её измерение.
В отличии от идеального газа, реальный газ не полностью подчиняется закону Бойля-Мариотта: при сжатии сначала его давление увеличивается, а потом происходит сжижение при постоянном давлении, затем объем не уменьшается.
Испарение – переход части молекул жидкости в газообразное состояние. Происходит с поглощением энергии.
Конденсация – переход части молекул газа в объем жидкости. Происходит с выделением энергии.
Динамическое равновесие – состояние при котором число испарившихся молекул равно числу проконденсировавших.
Насыщенный пар – находится в динамическом равновесии со своей жидкостью. Давление насыщенного пара зависит только от температуры. Пример- жидкость в закрытом сосуде.
Ненасыщенный пар – находится под давление ниже давления насыщенного пара. Пример – жидкость в открытом сосуде.
Кипение – испарение из объема жидкости. Кипение начинается только тогда, когда давление в пузырьке газа, становится равно атмосферному.
Температура кипения зависит от давления окружающего воздуха. С ростом давления температура кипения увеличивается и наоборот.
Влажность воздуха – абсолютная и относительная.
Абсолютная влажность – число водяных паров в 1 м3 воздуха. (т.е. парциальное давление).
Относительная влажность – отношение парциального давления к давлению насыщенного пара, выраженное в процентах.
| Р — парциальное давление (Па) Рн – давление насыщенного пара (Па) – относительная влажность (%) |
Парциальное давление – это давление части газа, находящегося в газовой смеси.
Относительная влажность измеряется психрометрами и гигрометрами.
Психрометр – волос, соединённый со стрелкой, который меняет свою длину, в зависимости от влажности воздуха.
Гигрометр – два термометра, один измеряет температуру сухого воздуха, а другой увлажненного. По разности показаний сухого и влажного термометров и психрометрической таблице определяют относительную влажность воздуха.
Читайте также:
Температура в термодинамике
Определение 1
Термодинамическая температура — единственная функция состояния термодинамической системы, характеризующая направление самопроизвольного теплообмена между материальными телами.
Рисунок 1. Понятие термодинамики. Автор24 — интернет-биржа студенческих работ
Термодинамическая температура в физике всегда обозначается буквой T, измеряется в кельвинах (обозначается K) и отсчитывается исключительно по абсолютной термодинамической шкале под названием шкал Кельвина. Абсолютная температура в термодинамике является основной шкалой в физике и в термодинамических уравнениях.
Молекулярно-кинетическая гипотеза, со своей стороны, непосредственно соединяет абсолютную температуру со средним коэффициентом кинетической энергией прямолинейного движения молекул идеального газа в условиях постоянного равновесия.
История измерения температуры
Измерение температуры в термодинамики прошло достаточно долгий и трудный путь в своём развитии. Так как температура невозможно измерить непосредственно, то для её измерения ученые применяли свойства термометрических веществ, находившиеся в функциональной зависимости от коэффициента температуры. На этой основе в итоге были созданы различные температурные шкалы, получившие название эмпирических, а измеренная посредством их температура носит название эмпирической.
Замечание 1
Весомыми недостатками эмпирических шкал считается наличие несовпадения и непостоянства значений температур для различных термометрических тел: как между реперными материальными точками, так и за их границами.
Такое явление связано с отсутствием в природе универсального вещества, способного сохранять свои свойства в диапазоне всевозможных температур. В 1848 году Томсон решил с помощью экспериментов выбрать наиболее подходящий градус температурной среды таким образом, чтобы в её пределах эффективность тепловой машины была при любых условиях одинаковой.
В дальнейшем, в марте 1854 года, исследователи использовали обратную функцию Карно для создания новой шкалы в термодинамике, не зависящей от свойств, активно действующих в системе термометрических тел. Однако, практическое внедрение этой идеи оказалась невозможной. В начале XIX столетия в поисках «абсолютного» устройства для измерения температуры наука вновь вернулась к теории идеального газового термометра, базирующейся на законах веществ Гей-Люссака и Шарля.
Газовый термометр в течение длительного периода времени был единственным методом воспроизведения и закрепления абсолютной температуры. Новые направления в разработке идеальной температурной шкалы основаны на реализации уравнений Стефана ─ Больцмана в бесконтактной термометрии и формулы Гарри (Харри) Найквиста ─ в контактной.
Температура как интенсивное свойство
Рисунок 2. Термодинамическая температура. Автор24 — интернет-биржа студенческих работ
Чтобы определить температуру, как интенсивное свойство любой системы, необходимо наполнить бочку холодной водой из других ведер. Сумма объемов жидкости в ведрах равна объему бочки. Однако сколько бы холодной воды ни поместить в бочку, горячей воды при этом невозможно получить. Такое рассуждение не смешно и не наивно, как может показаться с первого раза, ведь опыт не очевиден сам собой. Это один из важнейших законов природы, к которому люди просто привыкли.
Определение 2
Физика — великое торжество человеческого разума, но она практически всегда развивалась в связи с исследованием кажущихся тривиальностей.
Например, из нескольких коротких палок возможно быстро составить одну длинную, если соединить их встык между собой. Объем и длина – основные свойства системы. Но теперь желательно добавить к ним площадь и массу, которые выступают в качестве примеров экстенсивных свойств. Такие величины постепенно складываются, а на основе закона сложения базируется и метод их дальнейшего измерения.
Замечание 2
Определение экстенсивной величины — это сравнение ее с однородной в отношении концепции величиной.
Измерять температуру необходимо так, как измеряют площадь, длину, объем, массу, нельзя: температуры никогда не складываются. Единица температуры, которой можно сразу измерять любую температурную шкалу, просто невозможна. Температура – яркий пример интенсивных свойств концепции, поэтому к ней закон сложения неприменим.
Пример 1
Например, если разделить железный стержень на несколько частей, температура каждой из них останется прежней, а вот длина, соответственно, изменится.
Непосредственно установить конкретное числовое соотношение между различными температурами бессмысленно и нереально. Поэтому цель ученых измерить температуру без использования метода, пригодным для экстенсивных величин оказалась невыполнимой.
Основы построения термодинамической шкалы температур
Рисунок 3. Абсолютная температура в термодинамике. Автор24 — интернет-биржа студенческих работ
Шкала температур в термодинамике может быть построена принципиально на основании гипотезы Карно, которая предполагает:
- независимость показателя полезного действия теплового идеального двигателя от самой природы материального тела;
- самостоятельность от конструкции мотора;
- зависимость от температур холодильника и нагревателя.
Такое соотношение возможно использовать для построения абсолютной термодинамической температуры. Если изометрическое явление цикла Карно осуществлять при температуре тройной точки воды, то коэффициент объема движущихся веществ изменится. Установленная таким образом шкала называется в физике термодинамической шкалой Кельвина. К сожалению, точность и надежность измерения количества теплоты низкая, что не позволяет реализовать вышеуказанный метод на практике.
Абсолютная температурная шкала может быть представлена в качестве некого термометрического элемента идеального газа. Если измерять давление этого вещества, близкого по свойствам к идеальному, расположенного в герметичном сосуде постоянного объёма, т
Абсолютный ноль температуры – точка прекращения движения молекул
27.10.2020 Кот учёный Природа
Термин «температура» появился во времена, когда ученые-физики думали, что теплые тела состоят из большего количества специфической субстанции – теплорода, – чем такие же тела, но холодные. А температура трактовалась как величина, соответствующая количеству теплорода в теле. С тех пор температуру любых тел измеряют в градусах. Но на самом деле это мера кинетической энергии движущихся молекул, и, исходя из этого, ее следует измерять в Джоулях, в соответствии с Системой единиц Си.
Понятие «абсолютный ноль температуры» исходит из второго начала термодинамики. По нему процесс перехода тепла от холодного тела к горячему невозможен. Это понятие введено английским физиком У. Томсоном. Ему за достижения в физике королевой Англии было даровано дворянское звание «лорд» и титул «барон Кельвин». В 1848 г. У. Томсон (Кельвин) предложил использовать температурную шкалу, в которой за начальную точку принял абсолютный ноль температуры, соответствующий предельному холоду, а ценой деления взял градус Цельсия. Единицей Кельвина является 1/27316 доля температуры тройной точки воды (около 0 град. С), т. е. температуры, при которой чистая вода сразу находится в трех видах: лед, жидкая вода и пар. Абсолютный ноль температуры – это минимально возможная низкая температура, при которой движение молекул останавливается, и из вещества уже невозможно извлечь тепловую энергию. С тех пор шкала абсолютных температур стала называться его именем.
Температура измеряется по разным шкалам
Наиболее употребляемая шкала температуры носит название «шкала Цельсия». Она построена на двух точках: на температуре фазового перехода воды из жидкости в пар и воды в лед. А. Цельсий в 1742 г. предложил расстояние между опорными точками разделить на 100 промежутков, а точку кипения воды принять за ноль, при этом точку замерзания за 100 градусов. Но швед К. Линней предложил сделать наоборот. С тех пор вода замерзает при ноле градусов А. Цельсия. Хотя точно по Цельсию она должна кипеть. Абсолютный ноль по Цельсию соответствует минус 273,16 градусов Цельсия.
Есть еще несколько температурных шкал: Фаренгейта, Реомюра, Ранкина, Ньютона, Рёмера. Они имеют разные опорные точки и цену деления. Например шкала Реомюра тоже построена на реперах кипения и замерзания воды, но она имеет 80 делений. Шкала Фаренгейта, появившаяся в 1724 г., используется в быту только в некоторых странах мира, в т. ч. США; реперные точки: одна — температура смеси водяной лед – нашатырь и другая — человеческого тела. Шкала делится на сто делений. Ноль Цельсия соответствует 32 градусам Фаренгейта. Перевод градусов в фаренгейты можно сделать по формуле: F = 1,8 C + 32. Обратный перевод: С = (F — 32) /1,8, где: F – градусы Фаренгейта, С – градусы Цельсия. Если вам лень считать, сходите в онлайн-сервис по переводу Цельсия в Фаренгейты. В рамочке наберите число градусов Цельсия, нажмите «Рассчитать», выберите «Фаренгейт» и нажмите «Пуск». Результат появится сразу.
Шкала Ранкина названа в честь английского (точнее шотландского) физика Уильяма Дж. Ранкина, бывшего современником Кельвина и одним из создателей технической термодинамики. В его шкале важных точек три: начало – абсолютный ноль, точки замерзания воды 491,67 градус Ранкина и закипания воды 671,67 град. Число делений между замерзанием воды и ее закипанием и у Ранкина, и у Фаренгейта равно 180.
Большинством этих шкал пользуются исключительно физики. А 40% опрошенных в наши дни американских школьников выпускных классов сказали, что они не знают, что такое абсолютный ноль температуры.
Источник: fb.ru
Об измерение температуры и что такое температура.
В быту и на производстве мы часто обращаемся к «температуре» и «измерение температуры» «термометрами»:
— меряем температуру тела;
— смотрим на уличный термометр за окном, чтобы решить как одеться;
— контроль технологических или химических процессов…
Обычно под температурой мы понимаем просто степень нагретости тела: горячо — жарко, холодно — тепло.
Для точного измерения температуры в рамках какого-либо технологического процесса необходимо создать измерительную систему с учетом всех влияющих факторов. Тот же процесс инкубации яиц, чтобы вывести яйца в инкубаторе необходимо регулировать температуру.
Из четырёх величин Международной системы единиц (СИ), неразрывно связанных с человеческой деятельностью: массой, длиной, временем и температурой, последняя оставалась полной загадкой для человечества вплоть до 18 века.
Но и сегодня не все, кто пользуется различными средствами измерения температуры, понимают, что же они измеряют.
То же давление легко воспринимается, так как оно связано с силой и может быть без труда определено количественно. С температурой невозможно связать количественную величину.
Теория (кратко).
В быту мы оцениваем температуру по ощущениям: горячо, тепло, холодно. Казалось бы, если одно тело горячее другого, то и его температура должна быть больше. Но это не так. Попробуйте взять в разогретой сауне в руку деревянный ковшик и металлический ковшик. Совершенно разные ощущения, хотя температура одна. Но если мы хотим сравнить температуру одинаковых по своей природе объектов, то можем сделать это с высокой точностью.
Рукой можно определить, повышена ли температура другого человека, фактически измерить её с точностью ±0,5⁰С. Также находясь в помещении можно с точностью до 1…2⁰С определить температуру воздуха. Человек хорошо чувствует этот физический параметр и в то же время мало кто сможет чётко сказать, что же это такое — температура.
Совершенно обратная ситуация с влажностью воздуха: очень трудно определить влажность воздуха по своим ощущениям. Однако эта характеристика прекрасно понимается в количественном выражении – это количество молекул воды в единице объёма.
Существуют несколько определений температуры. Одно из них наиболее близкое людям, занимающимся практическими измерениями и исходит из нулевого закона термодинамики:
если два тела находятся в состоянии теплового равновесия, то они имеют одинаковую температуру.
Таким образом, если мы обеспечим хороший тепловой контакт термометра с измеряемой средой, то по прошествии некоторого времени, необходимого для установления теплового равновесия, температуры термометра и среды будут одинаковы. Естественно, что данный вывод будет верен, только если наша система изолирована от других тел и не совершается никакой работы.
Ну а само понимание физической природы температуры приходит только после изучения статистической механики, где температура представлена как мера кинетической энергии тела.
Для корректного изложения вопросов измерения температуры необходимо дать ее точное физическое определение.
Температура — физическая величина, количественно характеризующая меру средней кинетической энергии теплового движения молекул какого-либо тела или вещества.
Из определения температуры следует, что она не может быть колличественно измерена непосредственно и судить о ней можно по изменению других физических свойств тел (объема, давления, электрического сопротивления, термоЭДС, интенсивности излучения и т.д.).
В зависимости от диапазона измеряемых температур различают две основные группы методов измерения:
- контактные (собственно термометрия) — жидкостные, манометрические, термоэлектрические термометры, термометры сопротивления и др.
- безконтактные (пирометрия или термометрия излучения), применяемые в основном для измерения очень высоких температур — для измерения криогенных температур используются также газовые, акустические и магнитные термометры.
Кроме того, в системах, не требующих высокой точности измерений, в определенном диапазоне температур широко используются полупроводниковые датчики температуры на диодах, транзисторах и специальных интегральных микросхемах.
Историческая справка.
Первое достоверно известное устройство для измерения температуры было создано Г. Галилеем около 1595 г. Этот прибор (термоскоп) использовал явление изменения объема газа при нагревании и охлаждении. Однако этот прибор (и последующие аналоги) имел большой недостаток: его шкала была относительной и показания не могли быть выражены в численной форме.
Крупным шагом в развитии термометрии было введение изобретателем ртутного термометра Г.Фаренгейтом (G. Fahrenheit) в начале 18 века первой температурной шкалы, названной его именем, опирающейся на две опорные точки. В качестве нижней опорной точки (0°F) он использовал температуру замерзания солевого раствора, самую низкую воспроизводимую в то время, а в качестве верхней точки температуру тела человека (96°F — в старину было удобнее считать дюжинами). Сам изобретатель определял вторую эталонную точку как температуру под мышкой здорового англичанина.
Привычная нам десятичная температурная шкала была предложена А. Цельсием (A. Celsius) в 1742 году. В качестве опорных точек для нее используются температура плавления льда (0°C) и температура кипения воды (100°C).
Наконец, в начале 19 века английским ученым лордом Кельвином (Kelvin) была предложена универсальная абсолютная термодинамическая температурная шкала, ставшая стандартной в современной термометрии. Одновременно Кельвин обосновал понятие абсолютного нуля температуры.
Перевести температуру из одной шкалы в другую можно с помощью следующих простых соотношений:
T(°C)= (T(°F) — 32)*5/9
T(K)=T(°C) + 273,15
Таким образом,
0°C соответствует 32°F и 273,15 К,
а 100°C — 212°F и 373,15 К.
Выбор между этими опорными точками 100 делений у шкалы Цельсия и 180 делений у шкалы Фаренгейта является чисто условным (как, впрочем, и выбор самих опорных точек).
Для обеспечения единства измерений температуры в качестве международного стандарта в 1968 году принята Международная Практическая Температурная Шкала МПТШ68 (в настоящее время в качестве стандарта принята уточненная в 1990 году версия шкалы ITS90), использующая в качестве опорных точек температуры изменения агрегатного состояния определенных веществ, которые могут быть воспроизведены. Кроме того, стандарт определяет типы образцовых средств измерения во всем диапазоне температур.
Перечень основных фиксированных точек МПТШ68
| Наименование | Температура, К | Образцовое средство измерения |
| Точка затвердевания золота | 1337,58 | свыше 1337,58 К — спектральный пирометр |
| Точка затвердевания серебра | 1235,08 | от 903,89 К до 1337,58 К — термопара платина/платина%родий (10% Rh) |
| Точка затвердевания цинка | 692,73 | от 13,81 К до 903,89 К — платиновый термометр сопротивления |
| Точка кипения воды | 373,15 | |
| Тройная точка воды | 273,16 | |
| Точка кипения кислорода | 90,188 | |
| Тройная точка кислорода | 54,361 | |
| Точка кипения неона | 27,102 | |
| Точка кипения равновесного водорода | 20,28 |
Принято считать, что первый термометр, работающий на расширении воздуха, был изобретён Галилеем примерно в 1592 г. А в 1641 году появился первый, реально работающий спиртовой стеклянный термометр, созданный герцогом Тосканским. С этого момента началось быстрое развитие термометрии. В начале 18-ого века Фаренгейт первым изготовил ртутный стеклянный термометр и предложил температурную шкалу, в которой одной из фиксированных точек служила температура человеческого тела, которую он принял за 96 градусов, а другой – температура таяния льда -32 градуса. Ну а кульминационной точкой в развитии практической термометрии явилось принятие в 1927 году Международной температурной шкалы МТШ-27. В дальнейшем температурная шкала совершенствовалась и расширялась практически до 0 К.
Температура — параметр, который можно измерить только косвенно, по изменению других физических параметров. Термометрию различают на первичную и вторичную. В первичной термометрии температура явно описывается через другие физические параметры, например для газовых термометров это давление и объём. Примерами вторичных термометров являются термометры сопротивления и термопары. В промышленности термометры сопротивления и термопары являются основными средствами контроля температуры, закрывая диапазон измерения от минус 200 до + 2500⁰С и более.
В последнее время платиновые термосопротивления активно начали вытеснять медные и термопары. Связано это с появлением на рынке недорогих платиновых плёночных термочувствительных элементов, которые в отличие от медных являются более стабильными и работают в более широком диапазоне температур. А по сравнению с термопарами — обеспечивают более высокую точность измерения и не требуют использования дорогого термокомпенсационного кабеля.
Однако в России медные термометры до сих пор находят широкое применение. Одно из основных преимуществ меди — это очень хорошая линейная зависимость её сопротивления от температуры в диапазоне от минус 50 до + 200⁰С и более высокая чем у платины чувствительность. Свыше 200⁰С медь начинает очень быстро окисляться на воздухе, поэтому обычно верхний предел измерения для медных термосопротивлений устанавливается до 180⁰С. При производстве используется проволока диаметром от 30 до 80 мкм. При дальнейшем уменьшении диаметра стоимость проволоки резко возрастает, а изготовление термосопротивления с заданными параметрами становится проблематичным.
Также следует обращать внимание на максимальный измерительный ток. Например, для термометров сопротивления, изготовленных из проволоки диаметром 30 мкм уже при токе 0,2мА становится заметным явление саморазогрева от протекающего тока, а значит, использование таких термометров с большинством измерительных приборов становится невозможным. Обычно диаметр используемой проволоки определяется исходя из диаметра зонда, в который будет устанавливаться проволочный чувствительный элемент. Например, для зонда диаметром 2 мм используют проволоку диаметром 30 мкм, 4 мм – 40 мкм, 5…6 мм – 50 мкм, 8…10 мм- 80 мкм.
Большое значение имеет схема соединения проводников термосопротивления. Различают три основных схемы: 2-х, 3-х и 4-х проводную.
При двухпроводной схеме к сопротивлению ЧЭ добавляется сопротивление внешних проводов, что приводит к появлению дополнительной погрешности измерения. Ясно, что такой способ можно использовать только для ЧЭ с большим сопротивлением. Из наиболее употребляемых — это Pt1000. Легко подсчитать, что для обеспечения точности измерения 0,1⁰С общее сопротивление внешних проводников не должно быть больше 3,8 Ом.
В трёхпроводной схеме подключения автоматически из полного сопротивления вычитается сопротивление внешних проводов. Но это только в случае, если сопротивление проводников 1 и 2 трёхпроводной схемы равны между собой. Тем не менее, 3-х проводная схема подключения термосопротивлений на сегодняшний момент является самой популярной. Практически все вторичные приборы (измерители, регуляторы) имеют входные цепи, рассчитанные под эту схему. Трёхпроводная схема позволяет увеличить расстояние от датчика до прибора до 50…100 метров. При этом не обязательно, чтобы сам термометр сопротивления был изготовлен по 3-х проводной схеме. Можно использовать и датчики с двумя клеммами, подключив к одной клемме один провод, а ко второй – два.
Четырёхпроводная схема используется в основном только для точных измерений и в эталонных приборах. Данная схема позволяет автоматически компенсировать влияние на результат измерения не только сопротивления проводников, но и ЭДС в местах контактов.
Советы при выборе и монтаже термометров сопротивления
Есть банальные истины, которыми нужно руководствоваться при выборе подходящего датчика температуры. Конечно же, нужно в первую очередь обратить внимание на диапазон измерения и точность. Во-вторых, нужно решить вопрос с основным конструктивным исполнением: в клеммной головке, или с кабельным выводом. Датчики с кабельным выводом более миниатюрны и менее инерционны. Они уже полностью готовы к подключению к вторичному прибору. Но вышеперечисленные преимущества одновременно являются и их недостатками. Миниатюрный корпус – следовательно, небольшой размер чувствительного элемента и малый измерительный ток. Жёстко присоединённый кабель несёт за собой худшую, чем для датчиков в клеммной головке степень защиты от воды. Эти датчики заведомо дороже из-за высокой стоимости применяемого высокотемпературного кабеля. Они менее надёжны при механических воздействиях опять-таки из-за наличия кабеля. С термосопротивлением в клеммной головке не обязательно использовать высокотемпературный кабель. Минус этих датчиков в одном – габаритных размерах, что бывает важно в ряде случаем.
При монтаже датчика температуры нужно максимально увеличить его тепловой контакт с контролируемой средой и одновременно уменьшить отток тепла от места подключения. Необходимо помнить, что чувствительный элемент имеет конечную длину, поэтому глубина погружения датчика должна быть как минимум на несколько диаметров зонда больше, чем длина ЧЭ. При монтаже датчиков контроля поверхности очень важно место соединения предварительно смазать каким-либо вязким веществом. Также важно обеспечить тепловой контакт кабеля с контролируемым объектом, чтобы минимизировать отвод тепла от ЧЭ датчика по кабелю. Ещё лучше, если и датчик и подводящий кабель будут закрыты хорошим теплоизолятором, например пенополиуретаном, или пенополиэтиленом.
Датчики температуры воздуха лучше устанавливать в тех местах помещения, которые наиболее важны для контроля. При плохой конвекции воздуха в помещении градиент температуры может составить до 5-ти и более градусов.
При экспресс контроле температуры поверхности теплоёмкость датчика должна быть минимальной. Дело в том, что самое большое зло при контактном способе измерения температуры поверхности состоит в том, что датчик уменьшает температуру поверхности в месте установки. Процесс восстановления начальной температуры может идти очень долго, что зачастую приводит к неправильным результатам и выводам. Примером может служить ситуация с «занижением» показаний медицинских электронных термометров.
Термопары
По сравнению с термометрами сопротивления термопары обладают рядом очень больших преимуществ и таких же больших недостатков. По большому счёту эти два класса приборов очень органично дополняют друг друга. И задача киповца — определить, какой датчик температуры ему нужен для той или иной задачи.
Термопары имеют очень большой диапазон рабочих температур. При этом, чем больше максимальная рабочая температура термопары, тем меньше её чувствительность. С этим фактом связан большой ассортимент применяемых термопар. При помощи термопар можно измерять температуру очень маленьких объектов. Для этого достаточно сварить между собой две термоэлектродные проволоки маленького диаметра. Естественно, что такая термопара имеет и очень незначительную инерционность. Термопара из недрагоценных металлов малой длины дешевле термосопротивления. Однако при увеличении длины стоимость её значительно возрастает. В то же время термопары значительно уступают термосопротивлениям в точности измерения. Связано это с рядом причин. Сигнал с термопары значительно более нелинеен. Для получения абсолютной измеренной температуры необходимо знать температуру холодного спая термопары. А это означает, что общая погрешность измерения сложится из двух: погрешности измерения разности температур рабочего и холодного спая термопары и погрешности измерения температуры холодного спая. На практике же всё ещё сложнее. Очень непросто измерить с хорошей точностью температуру выводов термопары на входе вторичного прибора. На практике эта погрешность составляет около 1⁰С. При измерении высоких температур значение данной погрешности несколько нивелируется.
Советы по выбору и применению термопар
Для использования в диапазоне до +200⁰С лучше применять платиновые или медные термосопротивления. В случае контроля температуры очень небольшого объекта малой теплоёмкости можно использовать термопару медь-константан, которая замечательна тем, что очень легко сваривается над поверхностью раствора медного купороса, имеет самую высокую чувствительность и очень низкую стоимость.
Для диапазона до +800⁰С в России используется термопара ХК(L) хромель-копель. Данные термопары имеют очень высокую чувствительность в широком диапазоне начиная от -200⁰С. В других странах данный тип термопары не применяется. Самыми популярными в промышленности являются термопары типа ХА(К) хромель-алюмелевые. Теоретический диапазон их использования составляет от -200 до +1300⁰С. Термопары типа К замечательны хорошей линейностью характеристики от 0 до 1000⁰С. В реальности наиболее высокотемпературные термопары работают до 1100⁰С. Так как при высокой температуре от +800⁰С термоэлектродные проволоки начинают активно окисляться, то единственным путём увеличить срок службы термопары и температуру эксплуатации является увеличение диаметра термоэлектродных проволок до 2…3 мм. При температуре выше 800⁰С нержавеющую сталь кожуха меняют на специальную высокотемпературную сталь или керамику.
Для измерения температуры вплоть до +1700⁰С применяют термопары, изготовленные из драгоценных металлов платиновой группы. Они отличаются высокой стабильностью параметров, но имеют крайне низкую чувствительность при низких температурах и очень высокую стоимость. Наиболее высокотемпературные термопары – вольфрам-рениевые. Но они не могут работать в окислительной атмосфере при температуре уже выше 500⁰С. Оболочку этих датчиков необходимо наполнять инертным газом. Так как герметичный корпус для высоких температур изготовить проблематично, то для продолжительной работы по внутренней полости этих термопар постоянно пропускают инертный газ.
Для контроля температуры поверхности или воздуха лучше применять гибкую термопару без защитного чехла. Для контроля поверхности нужно обеспечить хороший тепловой контакт с поверхностью не только рабочего конца термопары, но и термоэлектродов на расстоянии не менее 50 мм, чтобы уменьшить теплоотвод от места контроля. При использовании термопары при высокой температуре в окислительной или агрессивной атмосфере может наблюдаться деградация параметров, связанная с окислением и изменением химического состава термоэлектродов. Необходимо периодически контролировать качество термопары хотя бы по её полному сопротивлению постоянному току. Для использования в экстремальных условиях в течение непродолжительного времени существуют ТП разового применения и ТП кратковременного применения.
Преобразование температуры из Цельсия в Фаренгейт
Быстрый градус Цельсия ( ° C, ) / Фаренгейт ( ° F, ) Преобразование:Инструмент преобразования Просто введите значение в любое поле: Или воспользуйтесь интерактивным термометром, Или этот метод:
(объяснение ниже…) |
Типичные температуры
| ° С | ° F | Описание | |
|---|---|---|---|
| 180 | 356 | Духовка среднего размера | |
| 100 | 212 | Вода закипает | |
| 40 | 104 | Горячая ванна | |
| 37 | 98.6 | Температура тела | |
| 30 | 86 | Погода на пляже | |
| 21 | 70 | Комнатная температура | |
| 10 | 50 | Прохладный день | |
| 0 | 32 | Температура замерзания воды | |
| −18 | 0 | Очень холодный день | |
| −40 | −40 | Extremely Cold Day (и столько же!) | |
| ( полужирный точно) | |||
16 — около 61
28 — около 82
Пояснение
Существуют две основные температурные шкалы:
- ° C , шкала Цельсия (часть метрической Система, используемая в большинстве стран)
- ° F , шкала Фаренгейта (используется в США) и
Они оба измеряют одно и то же (температуру!), Но используют разные номера:
- Кипящая вода (при нормальном давлении) измеряет 100 ° по Цельсию, но 212 ° по Фаренгейту
- И замерзание воды измеряет 0 ° по Цельсию, но 32 ° по Фаренгейту
Как это:
Изменение климата: глобальная температура | NOAA Климат.gov
Учитывая размер и огромную теплоемкость мирового океана, требуется огромное количество тепловой энергии, чтобы повысить среднегодовую температуру поверхности Земли даже на небольшую величину. Повышение средней глобальной температуры поверхности на 2 градуса, которое произошло с доиндустриальной эры (1880-1900), может показаться небольшим, но это означает значительное увеличение накопленного тепла. Это дополнительное тепло приводит к региональным и сезонным экстремальным температурам, сокращению снежного покрова и морского льда, усилению проливных дождей и изменению ареалов обитания растений и животных, расширяя одни и сокращая другие.
История глобальной температуры поверхности с 1880 года
Изучите этот интерактивный график: Щелкните и перетащите, чтобы отобразить различные части графика. Чтобы сжать или растянуть график в любом направлении, удерживайте нажатой клавишу Shift, затем щелкните и перетащите. На графике показаны среднегодовые глобальные температуры с 1880 года (исходные данные) в сравнении с долгосрочным средним значением (1901-2000 годы). Нулевая линия представляет собой долгосрочную среднюю температуру для всей планеты; синие и красные полосы показывают разницу выше или ниже среднего за каждый год.
Условия в 2019 году
Согласно отчету о глобальном климате за 2019 год, подготовленному Национальными центрами экологической информации NOAA, 2019 год начался с явления Эль-Ниньо от слабого до умеренного, происходящего в тропической зоне Тихого океана. На большей части суши и океана в течение большей части года температуры были выше средних.
Рекордно высокие годовые температуры над землей были измерены в некоторых частях Центральной Европы, Азии, Австралии, южной части Африки, Мадагаскара, Новой Зеландии, Северной Америки и восточной части Южной Америки.Рекордно высокие температуры поверхности моря наблюдались во всех частях всех океанов, включая северную и южную части Атлантического океана, западную часть Индийского океана и районы северной, центральной и юго-западной частей Тихого океана. Ни одна из областей суши или океана не была рекордно холодной за год, и единственный значительный карман с температурами на суше ниже средних был в центральной части Северной Америки. Подробную информацию о регионах и дополнительную статистику климата за 2019 год см. В Ежегодном климатическом отчете за 2019 год от национальных центров NOAA по экологической информации.
Изменение с течением времени
Хотя потепление не было равномерным по всей планете, тенденция к повышению глобальной средней температуры показывает, что больше областей нагреваются, чем охлаждаются. Согласно Глобальному климатическому обзору NOAA 2019, с 1880 года общая температура суши и океана повышалась в среднем на 0,07 ° C (0,13 ° F) за десятилетие; однако средняя скорость роста с 1981 г. (0,18 ° C / 0,32 ° F) более чем в два раза выше.
Все 10 самых теплых лет за всю историю наблюдений приходятся на период с 1998 г., а 9 из 10 — с 2005 г.1998 год — единственный год двадцатого века среди десяти самых теплых лет за всю историю наблюдений. Оглядываясь назад на 1988 год, вырисовывается закономерность: за исключением 2011 года, когда каждый новый год добавляется к историческим данным, он становится одним из 10 самых теплых за всю историю наблюдений в то время, но в конечном итоге заменяется окном «первой десятки» сдвигается вперед во времени.
К 2020 году модели прогнозируют, что глобальная температура поверхности будет более чем на 0,5 ° C (0,9 ° F) выше, чем в среднем за 1986–2005 годы, независимо от того, по какому пути выбросов углекислого газа будет следовать мир.Это сходство температур независимо от общего объема выбросов — краткосрочное явление: оно отражает огромную инерцию обширных океанов Земли. Высокая теплоемкость воды означает, что температура океана не мгновенно реагирует на повышенное тепло, удерживаемое парниковыми газами. Однако к 2030 году дисбаланс нагрева, вызванный парниковыми газами, начинает преодолевать тепловую инерцию океанов, и прогнозируемые температурные траектории начинают расходиться, причем неконтролируемые выбросы углекислого газа, вероятно, приведут к нескольким дополнительным степеням потепления к концу века.
О температуре поверхности
Представление о средней температуре для всего земного шара может показаться странным. В конце концов, в этот самый момент самые высокие и самые низкие температуры на Земле, вероятно, различаются более чем на 100 ° F (55 ° C). Температуры варьируются от ночи к дню и от сезонных экстремумов в Северном и Южном полушариях. Это означает, что некоторые части Земли довольно холодные, а другие — совершенно горячие. Поэтому говорить о «средней» температуре может показаться чепухой.Однако концепция глобальной средней температуры удобна для обнаружения и отслеживания изменений в энергетическом балансе Земли — сколько солнечного света Земля поглощает за вычетом того, сколько он излучает в космос в виде тепла — с течением времени.
Чтобы вычислить среднюю глобальную температуру, ученые начинают с измерений температуры в разных точках земного шара. Поскольку их цель — отслеживать изменений температуры, измерения преобразуются из абсолютных показаний температуры в температурные аномалии — разницу между наблюдаемой температурой и долгосрочной средней температурой для каждого местоположения и даты.Несколько независимых исследовательских групп по всему миру проводят собственный анализ данных о температуре поверхности, и все они демонстрируют аналогичную тенденцию к росту.
В недоступных областях, где мало измерений, ученые используют температуру окружающей среды и другую информацию для оценки недостающих значений. Каждое значение затем используется для расчета средней глобальной температуры. Этот процесс обеспечивает последовательный и надежный метод мониторинга изменений температуры поверхности Земли с течением времени.Узнайте больше о том, как создается глобальный рекорд температуры поверхности, в нашем пособии по климатическим данным.
Список литературы
Санчес-Луго, А., Беррисфорд, П., Морис, К., и Аргуэс, А. (2018). Температура [в Состояние климата в 2018 году ]. Бюллетень Американского метеорологического общества, 99 (8), S11 – S12.
Национальные центры экологической информации NOAA, Состояние климата: глобальный климатический отчет за 2019 год, опубликовано в Интернете в январе 2020 года, получено 16 января 2020 года по адресу https: // www.ncdc.noaa.gov/sotc/global/201913.
МГЭИК, 2013: Резюме для политиков. В: Изменение климата 2013: основы физических наук. Вклад Рабочей группы 1 в 5-й доклад об оценке Межправительственной группы экспертов по изменению климата [Stocker, T.F., D. Qin, G.-K. Платтнер, М. Тиньор, С.К. Аллен, Дж. Бошунг, А. Науэльс, Ю. Ся, В. Бекс и П.М. Мидгли (ред.)]. Издательство Кембриджского университета, Кембридж, Великобритания и Нью-Йорк, штат Нью-Йорк, США.
Интерактивный график данных
Годовые аномалии глобальной температуры для суши и океана вместе взятые, выраженные как отклонения от среднего значения за 1901–2000 годы.Национальный центр климатических данных.
SAT Physics Subject Test: Полнометражный практический тест 2_cracksat.net
1.
Блок массой м , совершающий простое гармоническое движение. Силы трения незначительны, и ими можно пренебречь.
Какое количество НЕ остается постоянным после начала движения?
A. Амплитуда
B. Частота
C. Период
D. Положение блока
E. Полная механическая энергия блока
2.
Блок массой м , совершающий простое гармоническое движение. Силы трения незначительны, и ими можно пренебречь.
Какая величина обратно пропорциональна квадратному корню из массы блока?
A. Амплитуда
B. Частота
C. Период
D. Положение блока
E. Полная механическая энергия блока
3.
Блок массой м совершает простое гармоническое движение. Силы трения незначительны, и ими можно пренебречь.
Какая величина всегда была бы больше, если бы блок колебался с меньшей силовой постоянной?
A. Амплитуда
B. Частота
C. Период
D. Положение блока
E. Полная механическая энергия блока
4.
Блок массой м совершает простое гармоническое движение. Силы трения незначительны, и ими можно пренебречь.
Какому количеству пропорциональна максимальная скорость блока?
А. Амплитуда
Б.Частота
C. Период
D. Положение блока
E. Полная механическая энергия блока
5.
Блок массой м совершает простое гармоническое движение. Силы трения незначительны, и ими можно пренебречь.
График какой величины (от времени) будет выглядеть как синусоида?
A. Амплитуда
B. Частота
C. Период
D. Положение блока
E. Полная механическая энергия блока
6. Какой тип распада приведет к уменьшению числа нейтронов в ядре на 1?
A. Альфа-распад
B. β — распад
C. β + распад
D. Захват электронов
E. Гамма-распад
7. В каком типе распада идентичность ядра не изменилась ?
A. Альфа-распад
B. β — распад
C. β + распад
D. Захват электронов
E. Гамма-распад
8. Какой тип распада выбрасывает самую тяжелую частицу?
А.Альфа-распад
B.
