принцип работы, из чего состоит, назначение и схема акб
Автор Aluarius На чтение 10 мин. Просмотров 13.4k. Опубликовано
Содержание
- 1 Что такое аккумулятор
- 2 Устройство и принцип работы аккумулятора
- 2.1 Схема строения
- 3 Виды аккумуляторов
- 3.1 Классификация акб по составу активного вещества
- 3.2 Классификация батарей по типу электролита
- 4 Основные технические характеристики аккумуляторов
- 4.1 Номинальная емкость аккумулятора
- 4.2 Пусковой ток
- 4.3 Полярность
- 4.4 Исполнение корпуса
- 4.5 Тип и размер клемм
- 4.6 Тип крепления
- 5 Назначение аккумуляторных батарей
- 5.1 В каких сферах используется
Принципиально устройство аккумулятора больше чем за 150 лет с момента его изобретения не изменилось, хотя современность внесла серьёзные новшества в технологические процессы их изготовления и используемые материалы, из чего состоит аккумулятор.
Что такое аккумулятор
Аккумулятор – автономный источник электричества, который накапливает, сохраняет и отдает энергию. Аккумуляторная батарея – важный элемент электрооборудования транспортного средства. Назначение акб определяется в запуске двигателя и обеспечении подачи электричества в бортовую сеть. Все электроприборы, когда выключен мотор, и не работает генератор, работают от батареи. Накопитель помогает в пробке, когда энергии генератора не хватает.
Устройство и принцип работы аккумулятора
Для того, чтобы разобраться, как работает аккумулятор, необходимо знать устройство акб, что внутри аккумулятора обеспечивает работу прибора. Основной принцип работы аккумулятора заключается в разности потенциалов при погружении двух пластин в электролит. В 12-ти вольтовой батарее объединены шесть аккумуляторов, каждый из которых вырабатывает 2 вольта. Все они объединены совместным корпусом, который образует единое целое конструкции.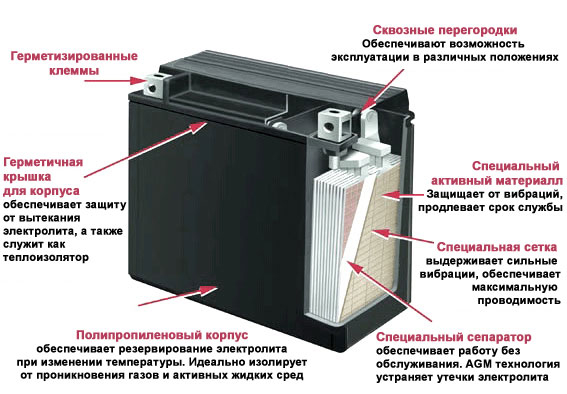
При работе этой конструкции, пластинки из-за действия серной кислоты выделяют сульфат свинца, в результате чего образуется электрический ток. Также выделяется вода, и поэтому концентрация электролита становится менее плотной. Во время зарядки АКБ процесс осуществляется в обратном порядке, свинец снова обретает металлическую форму, электролит становится более концентрированным. Принцип работы аккумулятора основан на методе двойной сульфатации, который позволяет полностью восстанавливать первоначальные свойства батареи. Срок службы аккумулятора зависит от качества используемых материалов, из чего состоит акб.
Схема строения
Схема строения
Виды аккумуляторов
Классификация акб по составу активного вещества
Свинцовые пластины, используемые в старых аккумуляторах перестали устраивать потребителей. Возникала необходимость по улучшению качества работы акб. Сначала добавили сурьму к свинцу, что позволило заметно продлить срок эксплуатации батареи. На следующем этапе – уменьшили процентное содержания сурьмы до оптимальной концентрации. Такой подход привел к созданию малообслуживаемых аккумуляторов, потому что в них уже намного реже требовался долив воды.
На следующем этапе – уменьшили процентное содержания сурьмы до оптимальной концентрации. Такой подход привел к созданию малообслуживаемых аккумуляторов, потому что в них уже намного реже требовался долив воды.
При использовании металлического кальция для покрытия пластин появились кальциевые энергосберегающие источники. В предыдущих моделях потери воды из-за электролиза на 12 вольт требовали постоянного долива, а кальций позволил повысить этот порог до 16 вольт. Так появилась возможность в производстве необслуживаемых аккумуляторов использовать герметичный, неразборной корпус.
- Сурьмянистые батареи относятся к классике из-за повышенного состава сурьмы, которая ускоряет процесс электролиза.
- В малосурьмянистых акб материалом для пластин служит свинец с небольшой примесью сурьмы. В них степень саморазряда значительно меньше, чем в сурьмянистых АКБ.
- При производстве кальциевых источников свинцовые пластины легированы до 0,1% кальцием. Они могут иметь различные заряды, как отрицательный, так и положительный.

- Гибридные источники энергии вытесняют кальциевые. Конструктивные отличия состоят в том, что при их производстве объединили две технологии: одна, когда пластины формируются из сплава свинца и сурьмы, положительные электроды, а другая – когда пластины формируются из сплава свинца и кальция, отрицательные электроды.
- EFB является улучшенной жидкозаполненной батареей. Свинцовые пластины в ЕФБ аккумуляторах в два раза толще, чем у обычных, вследствие чего увеличивается их ёмкость. Каждая из пластин закрыта в пакет из специальной ткани, который наполнен жидким сернокислотным электролитом.
- В гелевых аккумуляторах применяется гелеобразный электролит. Такая технология позволила снизить текучесть электролита, в котором содержится агрессивная серная кислота.
- В литиевых акб используется жидкий электролит, представляющий собой раствор фторсодержащих солей лития в смеси эфиров угольной кислоты.
- Отличительной особенностью AGM является то, что в электролит с помощью специальной технологии между пластинами вставляются стекловолоконные микропористые прокладки.

- Во всех щелочных батареях применяется растворенная в воде щёлочь.
Классификация батарей по типу электролита
Электролиты бывают кислотными, щелочными. Щелочные растворы используются в заправке аккумуляторных батарей. Щелочные аккумуляторные жидкости представляют собой сильные основания, которые проявляют большую активность по отношению к металлам и кислотам. При реакциях с кислотами образуются соль и вода. Растворы щелочей подвергаются гидролизу. Химические свойства позволяют использовать этот тип электропроводящей жидкости для накопления электрической энергии в аккумуляторе.
Кислотные смеси с дистиллированной водой применяются в основном в автомобильных аккумуляторах. Такие составы можно приобрести в специализированных магазинах или же приготовить самостоятельно в домашних условиях. На заводе процесс изготовления таких смесей осуществляется в масштабном производстве по ГОСТу. В домашней обстановке также возможно довольно точно при соблюдении обязательных пропорций и правил техники безопасности смешать кислоту с дистиллированной водой.
Важно! вода при минусовых температурах превращается в лед. Всегда при морозе нужно применять меры, необходимые для предотвращения замерзания аккумулятора.
Основные технические характеристики аккумуляторов
Номинальная емкость аккумулятора
Номинальная емкость элемента – способность накапливать и отдавать электроэнергию постоянного тока, определяет время автономной работы ИБП. Емкость электрического аккумулятора показывает время питания подключенной к нему нагрузки.
Важно! Емкость не характеризует полностью энергию аккумулятора, т.е. энергию, которая может быть накоплена в полностью заряженном аккумуляторе. Чем больше напряжение аккумулятора, тем больше накопленная в нем энергия.
Емкость всегда указывается на корпусе АКБ, а также на упаковке, ведь именно по этому критерию большинство пользователей выбирают нужную модель.
Пусковой ток
Величину, характеризующую параметр тока, протекающего в стартере автомобиля в момент пуска силового узла, принято считать пусковым током.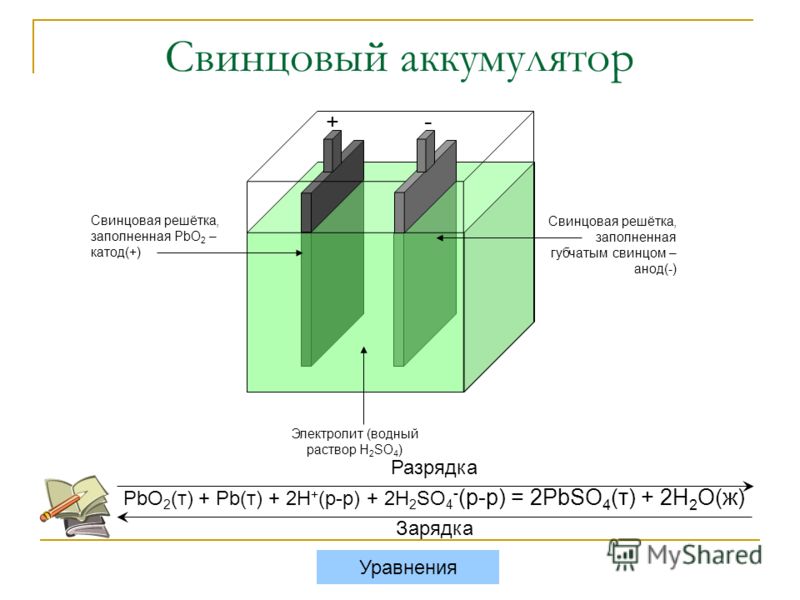 Пусковой ток или стартерный возникает в момент, когда в замке зажигания поворачивается ключ и начинает проворачиваться стартер. Единица измерения величины – Ампер. Он же ток холодной прокрутки является показателем, как аккумулятор поведет себя в морозную погоду и сможет запустить двигатель при минусовых показателях. Определяется мощностью тока, которую батарея может выдать в течение первых 30 секунд при температуре -18°С. При высоких показателях пускового тока увеличиваются шансы завести машину при минусовой температуре.
Пусковой ток или стартерный возникает в момент, когда в замке зажигания поворачивается ключ и начинает проворачиваться стартер. Единица измерения величины – Ампер. Он же ток холодной прокрутки является показателем, как аккумулятор поведет себя в морозную погоду и сможет запустить двигатель при минусовых показателях. Определяется мощностью тока, которую батарея может выдать в течение первых 30 секунд при температуре -18°С. При высоких показателях пускового тока увеличиваются шансы завести машину при минусовой температуре.
Полярность
Порядок расположения на крышке аккумулятора присоединительных клемм, которые являются токовыводящими соединительными элементами, называется полярностью. Полюса всего два – положительный и отрицательный, вариантов расположения – прямое и обратное.
Прямая полярность – отечественная разработка. Чтобы ее определить, нужно повернуть аккумулятор таким образом, чтобы этикетка была перед глазами. При расположении плюсовой клеммы слева, а минусовой справа, можно утверждать, что акб с прямой полярностью. На иномарках устанавливаются аккумуляторные батареи обратной полярности.
На иномарках устанавливаются аккумуляторные батареи обратной полярности.
Исполнение корпуса
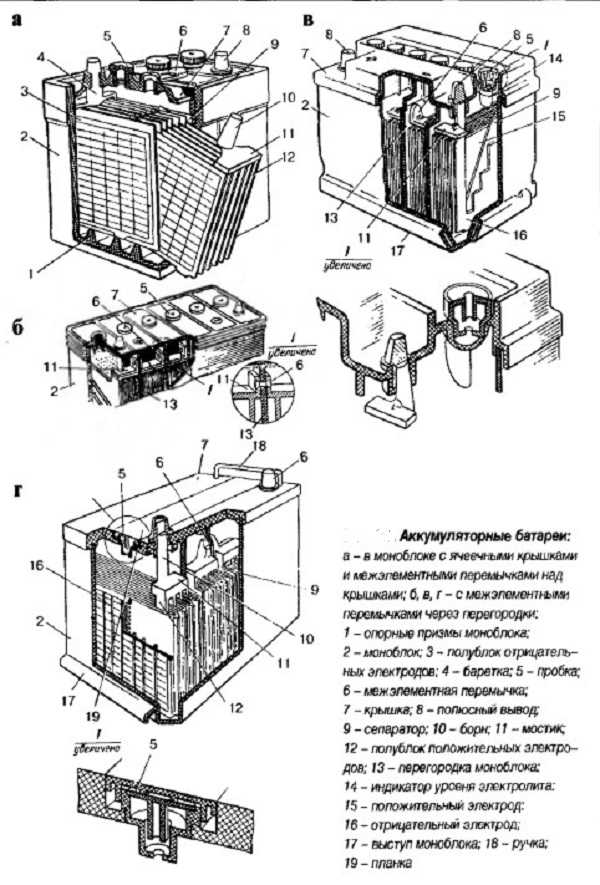
Корпус большинства аккумуляторов состоит из ударопрочного полипропилена, который характеризуется как материал легкий, не вступающий в химическую реакцию с агрессивным электролитом АКБ. Полипропилен довольно стоек к перепадам температур, возникающих под капотом автомобиля, нагрев может достигать до +60 ̊С, а при морозах до -30°С. Корпус большинства АКБ состоит из ручки для переноса, пробок, индикатора заряда, клемм для подключения к электросети. Вес АКБ емкостью 55Ач около 16,5 кг. Традиционно появились американский, европейский, азиатский и российский типы корпусов.Европейские корпусы и американские имеют идентичные габариты. Например, у батарей емкостью 60 Ач общая высота от 17,5 до 19 сантиметров. У азиатских этот показатель немного выше, до 22 сантиметров за счет верхнего расположения электродов. Именно поэтому важно корректно анализировать возможности посадочного места под капотом, чтобы надежно закрепить АКБ прижимной планкой и избежать замыкания при случайном касании токоотводами металлических частей кузова.
У АКБ с европейским типом корпуса клеммы находятся в углублении, их верхний край не выступает над плоскостью крышки. Иногда клеммы дополнительно защищены от внешнего воздействия специальными крышечками. Азиатский тип корпуса – это коробка, на которой клеммы расположились на верхней крышке, верхний край клемм является самой высокой точкой аккумулятора. Какую клемму снимать с аккумулятора первой читайте здесь.
Важно! При приобретении акб нужно знать, что европейские производители указывают габаритные размеры аккумулятора по корпусу. На азиатских корпусах могут указывать высоту батареи с учетом клемм или без них.
Российский стандарт акб
| Обозначение | Описание букв |
| А | АКБ имеет общую крышку для всего корпуса |
| З | Корпус батареи залит и она является полностью заряженной изначально |
| Э | Корпус-моноблок АКБ выполнен из эбонита |
| Т | Корпус-моноблок АБК выполнен из термопластика |
| М | В корпусе использованы сепараторы типа минпласта из ПВХ |
| П | В конструкции использованы полиэтиленовые сепараторы-конверты |
Европейские корпусы и американские имеют идентичные габариты
Тип и размер клемм
Распространены аккумуляторы с клеммами трех разных стандартов: тип Euro – Type 1, и Asia –Type 3, «под болт» – американский стандарт. В типе Euro плюсовая клемма имеет диаметр 19,5 мм, минусовая клемма – 17,9 мм. В типе Asia клемма плюс имеет диаметр 12,7 мм, клемма минусовая – 11,1 мм. Клеммы «под болт» находятся на боковой стенке аккумулятора и сверху. Болт, соединённый с проводом, продевается в отверстие клеммы и фиксируется гайкой.
В типе Euro плюсовая клемма имеет диаметр 19,5 мм, минусовая клемма – 17,9 мм. В типе Asia клемма плюс имеет диаметр 12,7 мм, клемма минусовая – 11,1 мм. Клеммы «под болт» находятся на боковой стенке аккумулятора и сверху. Болт, соединённый с проводом, продевается в отверстие клеммы и фиксируется гайкой.
Тип крепления
При выборе акб особое внимание следует обращать на тип крепления АКБ, при котором батарея может крепиться снизу или сверху. Вверху крепится элемент с помощью специальной монтажной рамки, которая охватывает аккумулятор. Крепление аккумулятора происходит с помощью планки и двух шпилек. Чаще такой вид установки и фиксации аккумуляторной батареи встречается на автомобилях китайского или корейского производства.
Тип крепления встречается на «азиатах»
Нижнее крепление применимо на европейских автомобилях. На нижней части корпуса акб находится выступ, за который аккумулятор прижимается к платформе с помощью пластины и винта.
Нижнее креплениеНазначение аккумуляторных батарей
Автомобильная аккумуляторная батарея выступает как источником электрического тока, необходимого для пуска двигателя, так и резервным источником питания, в случае, если энергии, вырабатываемой генератором, оказывается мало для электроснабжения авто. Аккумуляторная батарея действует как стабилизатор напряжения, так как она выполняет роль накопителя электроэнергии, отдающего во время пуска двигателя за короткое время большой ток, и пополняемого постепенно генератором автомобиля в процессе подзарядки.
Аккумуляторная батарея действует как стабилизатор напряжения, так как она выполняет роль накопителя электроэнергии, отдающего во время пуска двигателя за короткое время большой ток, и пополняемого постепенно генератором автомобиля в процессе подзарядки.
Важно! Перед проверкой системы электроснабжения и электрического пуска, необходимо убедиться в том, что аккумуляторная батарея находится в заряженном состоянии и готова к эксплуатации.
В каких сферах используется
Аккумуляторные батареи используются как дополнительный или основной источник питания. Надежность, простота в использовании позволяет применять батареи в различных областях:
- автомобильная промышленность;
- освещение в аварийном состоянии;
- переносное электрооборудование;
- медицинское оборудование;
- игрушки;
- сигнализация в разных сферах применения;
- телекоммуникационное оборудование.
Применение батареи в игрушках
 Применение источника энергии практически во всех отраслях доказывает значимость и необходимость знаний о внутреннем содержимом батарей. С использованием в автомобилях широкого разнообразия электроприборов, кондиционеров, мультимедийных центров, генераторы не всегда справляются с обеспечением их энергией. В этом случае подпитка энергией поступает от АКБ, который кроме этого выполняет основную функцию, обеспечивает электроэнергией стартер двигателя. Водителю необходимо знать, как устроен аккумулятор, чтобы выявить сбои в работе источника энергии, назначение аккумулятора, чтобы правильно использовать ресурс, подобрать батарею к условиям эксплуатации и автомобилю. О способах и рекомендациях как проверить аккумулятор читай тут.
Применение источника энергии практически во всех отраслях доказывает значимость и необходимость знаний о внутреннем содержимом батарей. С использованием в автомобилях широкого разнообразия электроприборов, кондиционеров, мультимедийных центров, генераторы не всегда справляются с обеспечением их энергией. В этом случае подпитка энергией поступает от АКБ, который кроме этого выполняет основную функцию, обеспечивает электроэнергией стартер двигателя. Водителю необходимо знать, как устроен аккумулятор, чтобы выявить сбои в работе источника энергии, назначение аккумулятора, чтобы правильно использовать ресурс, подобрать батарею к условиям эксплуатации и автомобилю. О способах и рекомендациях как проверить аккумулятор читай тут.Принцип работы и устройство аккумулятора автомобиля
Исправно работающая аккумуляторная батарея — такой же неотъемлемый атрибут, как рулевое управление или колёса с нормальным давлением в шинах. Они выпускаются сегодня в разных интерпретациях, требуют определённого ухода и отличаются конструктивными особенностями.
Назначение аккумулятора в автомобиле
Главные функции, которые призван выполнять автомобильный аккумулятор, заключаются в том, чтобы запускать двигатель машины и ещё обеспечивать током некоторые приборы-потребители. Это источник тока, который относится к возобновляемым, то есть, ёмкость батареи может и должна восстанавливаться, если она исправна. Каждая АКБ превращает электроэнергию в химическую, а впоследствии этот процесс происходит в обратном порядке.
Более всего это устройство востребовано на этапе запуска двигателя внутреннего сгорания. Однако аккумулятор также отвечает за работоспособность и питание всего электрооборудования на борту транспортного средства. Как только запущен мотор, то питание приборов осуществляется уже за счёт генератора, который одновременно заряжает и аккумулятор, ведь каждый запуск приводит к уменьшению его ёмкости.
За последние годы автомобили всех марок активно насыщаются электроприборами, системами климатического контроля, звука и видео, а все они питаются за счёт бортового электрического тока. Если генератор не справляется с его поставкой, то дополнительно идёт подпитка от батареи. Однако ключевая задача её заключается всё-таки в подаче тока для запуска стартера. Наибольший разряд АКБ случается в холодное время года, когда и возникает большинство проблем у автолюбителей.
Если генератор не справляется с его поставкой, то дополнительно идёт подпитка от батареи. Однако ключевая задача её заключается всё-таки в подаче тока для запуска стартера. Наибольший разряд АКБ случается в холодное время года, когда и возникает большинство проблем у автолюбителей.
Параметры АКБ
Необходимость знать основные параметры аккумулятора важна не только на этапе его покупки, но и в процессе обслуживания. Одной из ключевых характеристик считается ёмкость этого оборудования, которая даст информацию о длительности его бесперебойной работы. Для измерения используется такая единица, как ампер-часы, показывающая срок, в течение которого изделие может работать без дозаряда, расходуя свою ёмкость. На само значение ёмкости оказывают влияние внешние факторы: температура окружающего воздуха, сила тока и особенности конструкции.
Другой важный критерий называют пусковой силой тока АКБ. Для того чтобы его узнать, измеряют значение, которое обеспечивает батарея при температуре 18 по Цельсию. Именно показатель пусковой силы тока берут во внимание, когда хотят определить исправность оборудования. Нормальное напряжение обычно находится около отметки в 12,6 В, но может колебаться в пределах 13–14 В, в зависимости от модели.
Именно показатель пусковой силы тока берут во внимание, когда хотят определить исправность оборудования. Нормальное напряжение обычно находится около отметки в 12,6 В, но может колебаться в пределах 13–14 В, в зависимости от модели.
Каждая банка должна давать напряжение порядка 2В, а измерить его можно при помощи специальной нагрузочной вилки. Она устанавливает сопротивление, которое приходится на каждую из банок, учитывая также их ёмкость.
Важно помнить: перезарядка тоже нежелательна для аккумулятора, как и слабый заряд. Если не отключить вовремя зарядное устройство, это может спровоцировать закипание электролита.
Мощность заряда батареи можно получить, перемножив между собой напряжение и силу пускового тока. Однако, чтобы говорить о мощности, следует ещё учитывать температуру воздуха за окном машины. Слишком холодая погода отрицательно влияет на мощность. Потребуется больше тока для запуска, а потому зимой нужна большая мощность, нежели в тёплое время года.
Чтобы узнать детальные характеристики, лучше обратиться к маркировке — как правило, она наносится на корпусе изделия. На ней можно найти производителя и год выпуска, товарный знак и тип аккумулятора, вес, количество банок и другие необходимые стандарты. Основным материалом может выступать эбонит, термопласт или пластмасса, прошедшая специальную обработку. Вес батареи не относится к базовым характеристикам и может даже отличаться от того значения, что заявил производитель. Это может произойти из-за того, что свинцовые пластины взаимодействуют с электролитом и постепенно разрушаются.
Устройство аккумулятора
Разберёмся далее, как устроен автомобильный аккумулятор. Он состоит из нескольких гальванических элементов, которые ещё принято называть банками. Они находятся в отдельных ячейках изолированно друг от друга. Каждая из таких ячеек содержит в себе блок с электродами, часть из которых аноды, а другая часть — катоды. Полублок состоит из большого количества тонких пластин, которые обладают сетчатой структурой. Чтобы разделить между собой анод и катод, применяется специальный материал-сепаратор.
Чтобы разделить между собой анод и катод, применяется специальный материал-сепаратор.
В полость заливают раствор разбавленной серной кислоты, которая хорошо проводит электрический ток. В традиционных аккумуляторах требовалось доливать дистиллированную воду. Из-за вступания в реакцию молекул кислорода и водорода плотность электролита постепенно повышалась. Современные батареи не требуют вмешательства человека, потому их принято называть необслуживаемыми. Излишек газов, который образуется под крышкой, автоматически выходит наружу при помощи специальных клапанов.
Разбирая устройство автомобильного аккумулятора, нужно заглянуть под его крышку. Там мы увидим 6 банок, которые подключены последовательно в одну цепь. Сам корпус устойчив к воздействию серной кислоты, а производится он обычно из специального пластика или другого изолята. В каждую из банок помещаются как положительные, так и отрицательные электроды, а на каждый из них, в свою очередь, наносится активная обмазочная масса.
Электрическое замыкание аккумуляторной батареи машины не происходит из-за разделяющих элементов, сепараторов. Для производства проводящих ток электродов чаще всего используется свинец с определёнными добавками. Если соединить его с кальцием, это позволит понизить уровень саморазряда и необходимость частого долива дистиллята.
Решётки электродов также могут быть изготовлены по разнообразным технологиям. Главная их задача заключается в отводе тока для снижения внутреннего сопротивления изделия. В конструкцию решётки для придания ей большей прочности вставляют направляющие и опорную раму. Иногда их могут располагать вертикально или в шахматном порядке — это тоже делает конструкцию более прочной. Чтобы улучшить взаимодействие с веществом-электролитом, на решётки наносят активную обмазку. В случае с положительными пластинами – это диоксид свинца, в случае с отрицательными — свинец губчатый.
Подавляющее большинство современных автомобилей работает на батареях свинцово-кислотного типа, основу которых составляет жидкий электролит, помещённый под крышку корпуса.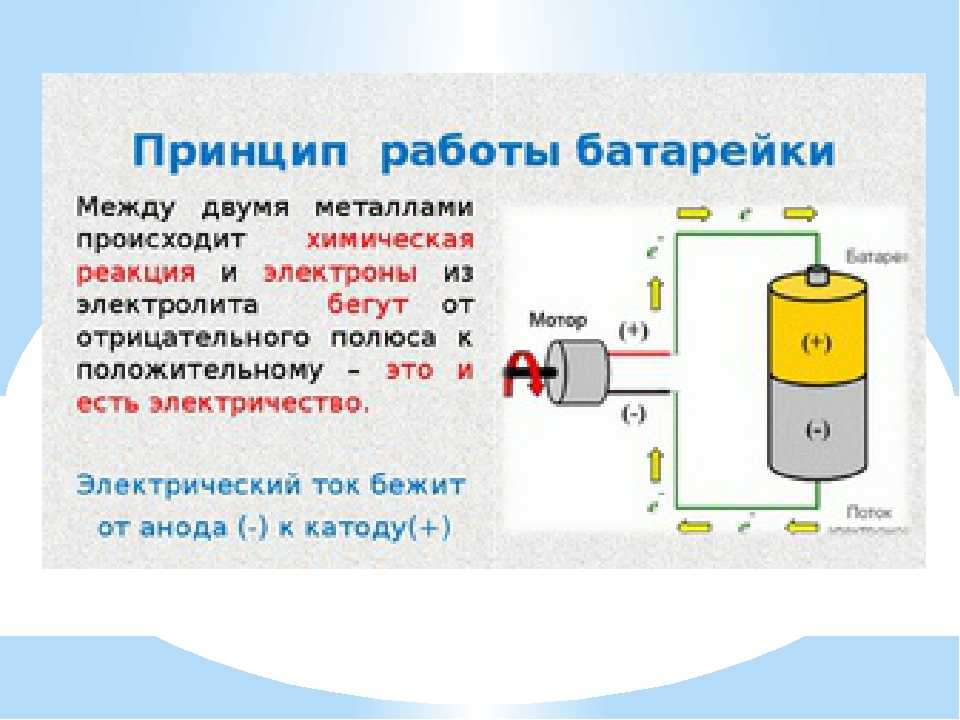 Однако за последние пару десятилетий широкое признание получили принципиально новые конструкции, избавленные от многих недостатков.
Однако за последние пару десятилетий широкое признание получили принципиально новые конструкции, избавленные от многих недостатков.
Кроме изделий с классическим жидким электролитом, на рынке можно встретить АКБ типа AGM или GEL. В них производитель также помещает электролит, но уже в связанном состоянии. Материал наподобие стекловолокна пропитывается электролитом и за счёт своей пористой структуры держит его как губка. В таком виде он и прилегает к пластинам. В другие типы аккумуляторов помещают гелеобразный электролит благодаря оксиду кремния, который добавляют в серную кислоту.
Принцип работы
Даже опытные автолюбители не всегда в полном объёме представляют себе принцип работы автомобильного аккумулятора. Основу составляет электрохимическая окислительная реакция свинца, которая происходит в растворе разбавленной водой серной кислоты. Когда происходит заряд, снижается количество диоксида свинца на пластине со знаком «минус». В это же самое время на положительной пластине количество свинца возрастает. При разряде аккумулятора осуществляются обратные процессы. Одновременно, когда АКБ автомобиля разряжается, возрастает объём воды в банках, а объём серной кислоты улетучивается. В большей степени это касалось батарей обслуживаемого типа.
При разряде аккумулятора осуществляются обратные процессы. Одновременно, когда АКБ автомобиля разряжается, возрастает объём воды в банках, а объём серной кислоты улетучивается. В большей степени это касалось батарей обслуживаемого типа.
Итак, принцип работы аккумулятора в машине можно свести к сложным химическим реакциям. Как только включается любой электропотребитель (стартер на запуске или другой прибор), батарея начинает утрачивать свою ёмкость. Диоксид свинца, помещённый на пластины со знаком «плюс», а также свинец обычный на отрицательных, вступают во взаимодействие с раствором серной кислоты. Как результат — появляются вода и сульфат свинца. Одновременно электролит становится менее плотным.
Когда мы подключаем аккумуляторную батарею своего автомобиля к зарядному устройству, начинается противоположная реакция. Накопленный сульфат свинца и дистиллированная вода обратно преобразовываются в серную кислоту и свинцовый диоксид. Чем дольше идёт заряд АКБ, тем большей становится плотность электролита. Одновременно происходит процесс сульфатации пластин.
Одновременно происходит процесс сульфатации пластин.
Во время поездок на автомобиле происходит непрерывный, хотя и не быстрый, заряд аккумулятора, если, конечно, мы имеем дело с исправным генератором. То есть, восстанавливается его максимальная ёмкость, которую можно возобновить и принудительно, но для этого придётся снимать батарею и подключать её к зарядному устройству.
Немалое значение отводится температуре окружающего воздуха. Если она повышена, то мощность возрастает, но вместе с ней увеличиваются расход воды и разряд. Во время пониженной температуры все эти химические реакции замедляются, но вместе с ними уменьшаются ёмкость и значения пускового тока. В обычных условиях эксплуатации длительность службы АКБ не превышает 3–5 лет. Многое зависит от типа батареи и входящих в состав пластин добавок, а также от ухода за ней и климатических условий эксплуатации.
Чтобы алгоритм работы любой АКБ не нарушался, водитель должен уметь её обслуживать и соблюдать некоторые рекомендации для продления эксплуатационного срока службы. Они сводятся к следующим правилам:
- если оборудование относится к категории обслуживаемых, периодически проверяем уровень электролита в нём;
- клеммы и их наконечники должны быть сухими и чистыми, гарантировать хороший контакт;
- при окислении проводов или их наконечников их следует осторожно отсоединить, зачистить и проверить надёжность контакта;
- корпус батареи нужно держать в чистоте и сухости, убирать лишнюю пыль или следы масла.
Это основные советы для поддержания АКБ в своем автомобиле в исправном состоянии, что одновременно поможет продлить его эксплуатационный ресурс.
Как устроена батарея.
 Инженерное мышление
Инженерное мышлениеБатареи, мы используем их каждый день по всему миру, но как они работают? Об этом мы расскажем в этой статье, спонсируемой Squarespace. Перейдите на сайт sqarespace.com, чтобы начать бесплатную пробную версию, или используйте инженерное мышление, чтобы сэкономить 10 % на веб-сайтах и доменах.
АккумуляторыПрокрутите вниз, чтобы посмотреть видео на YouTube.
Что такое батарея?
Аккумулятор — это устройство, используемое для хранения энергии, когда она нам нужна. Мы используем их для питания небольших электрических устройств, таких как фонарики. Энергия хранится в виде химической энергии, и ее можно превратить в электрическую энергию, когда она нам понадобится. Мы увидим, как это работает чуть позже в статье.
Цепь батареи и лампы Если мы посмотрим на простую цепь батареи и лампы. Чтобы зажечь лампу, нам нужно, чтобы через нее протекали электроны. Батарея будет обеспечивать толкающую силу, позволяющую электронам течь через лампу. Нам просто нужно подключить лампу к положительной и отрицательной клеммам батареи, чтобы замкнуть цепь. Батарея может выталкивать электроны только в течение определенного времени, это время зависит от того, сколько энергии хранится внутри батареи и сколько требуется нагрузке.
Нам просто нужно подключить лампу к положительной и отрицательной клеммам батареи, чтобы замкнуть цепь. Батарея может выталкивать электроны только в течение определенного времени, это время зависит от того, сколько энергии хранится внутри батареи и сколько требуется нагрузке.
Когда мы говорим о нагрузке в электрической цепи, мы имеем в виду любые компоненты, для работы которых требуется электричество, например резисторы, светодиоды, двигатели постоянного тока или даже целые печатные платы. Некоторые батареи можно перезаряжать, и это будет четко указано сбоку, но типичная бытовая щелочная батарея не может, поэтому ее просто утилизируют, когда в ней заканчивается энергия. Они могут быть переработаны, поэтому убедитесь, что вы утилизируете их ответственно.
Между прочим, если вы хотите узнать, как работает двигатель постоянного тока, мы уже подробно рассказывали об этом ранее — посмотрите ЗДЕСЬ.
Что внутри батареи?
Типичная щелочная батарея на 1,5 В выглядит примерно так, но цвета зависят от производителя.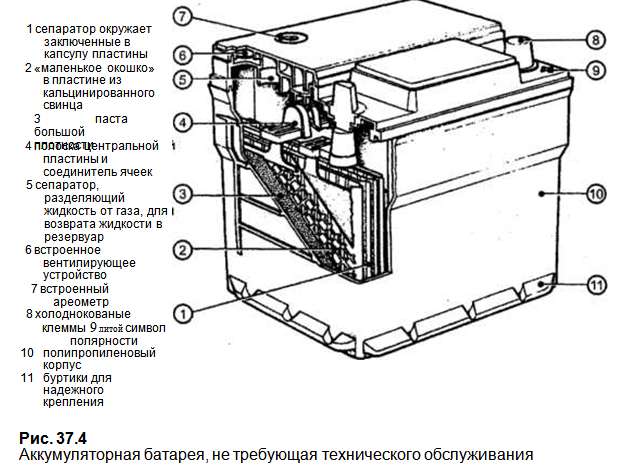 Когда мы смотрим на батарею, у нас обычно есть пластиковая обертка, плотно прикрепленная к внешней стороне, она изолирует батарею, но также сообщает нам важную информацию, такую как емкость и напряжение, а также то, какой конец является положительным, а какой отрицательным.
Когда мы смотрим на батарею, у нас обычно есть пластиковая обертка, плотно прикрепленная к внешней стороне, она изолирует батарею, но также сообщает нам важную информацию, такую как емкость и напряжение, а также то, какой конец является положительным, а какой отрицательным.
Положительный конец известен как катод и имеет расширенную поверхность, выступающую наружу.
Положительный конецОтрицательный конец будет плоским, отрицательный конец известен как анод. Эти две клеммы электрически изолированы друг от друга.
Negative EndПод оберткой находится основной кожух, который обычно изготавливается из стали с никелированием. Это удерживает все внутренние компоненты на месте и предотвращает их взаимодействие с элементами атмосферы, такими как воздух и вода.
Under Wrapper Внутри корпуса у нас есть несколько слоев различных материалов, эти материалы специально отобраны, потому что их химические реакции создают определенные уровни напряжения и тока. Первый слой — это катод, представляющий собой смесь оксида марганца (MnO2) и графита. Этот материал находится в контакте с металлом положительной клеммы. Графит добавляется для улучшения проводимости смеси и увеличения плотности энергии.
Первый слой — это катод, представляющий собой смесь оксида марганца (MnO2) и графита. Этот материал находится в контакте с металлом положительной клеммы. Графит добавляется для улучшения проводимости смеси и увеличения плотности энергии.
Затем мы находим слой пористого материала, обычно волокнистой бумаги, который образует барьер. Барьер предотвращает прямой контакт материалов анода и катода друг с другом, что помогает батарее дольше работать, когда она не используется. Если бы барьера не было, то произошло бы короткое замыкание батареи. Микроскопические отверстия внутри материала позволяют атомам ионов проходить сквозь него. Мы рассмотрим это более подробно позже в этой статье.
БарьерЖидкий электролит из гидроксида калия затем распыляется на сепаратор во время производственного процесса, который пропитывает его и впитывается в материал анода. Используемый электролит является щелочным, поэтому мы называем этот тип батареи щелочной батареей.
Electrolyte Liquid Spray На другой стороне барьера у нас есть анод, который представляет собой пасту, изготовленную из порошка цинка (Zn), а также гелеобразователя. Желирующий агент просто удерживает цинк во взвешенном состоянии, поэтому он не скапливается в одном месте. Цинк находится в форме порошка для увеличения площади поверхности материала, что снижает внутреннее сопротивление и, таким образом, улучшает перенос электронов.
Желирующий агент просто удерживает цинк во взвешенном состоянии, поэтому он не скапливается в одном месте. Цинк находится в форме порошка для увеличения площади поверхности материала, что снижает внутреннее сопротивление и, таким образом, улучшает перенос электронов.
Стальная капсула закрыта нейлоновой пластиковой крышкой. Затем в цинк вставляется латунный штифт, на который надевается стальной колпачок. Это дает нам отрицательную клемму. Обратите внимание, что положительные и отрицательные клеммы разделены пластиковой крышкой. Это гарантирует, что они электрически изолированы друг от друга, в противном случае электроны могут пройти через корпус и достичь положительной клеммы, что приведет к короткому замыканию батареи.
Разделение положительного и отрицательногоОсновы электричества
Нам нужно понять некоторые основы того, как работает электричество, прежде чем мы сможем понять аккумулятор.
Во-первых, электричество — это поток электронов в цепи. Батареи могут обеспечить толкающую силу, которая перемещает электроны по цепи. Электроны хотят вернуться к своему источнику, и они немедленно пойдут по любому пути, чтобы достичь этого. Помещая такие вещи, как лампы, на пути электронов, мы можем заставить их выполнять работу за нас, например, освещать лампу.
Батареи могут обеспечить толкающую силу, которая перемещает электроны по цепи. Электроны хотят вернуться к своему источнику, и они немедленно пойдут по любому пути, чтобы достичь этого. Помещая такие вещи, как лампы, на пути электронов, мы можем заставить их выполнять работу за нас, например, освещать лампу.
Батареи производят электричество постоянного или постоянного тока. Это означает, что электроны текут только в одном направлении от отрицательного к положительному. Осциллограф покажет постоянный ток в виде плоской линии в положительной области. Вы можете думать об электричестве постоянного тока как о реке, которая течет только в одном направлении.
Постоянный ток В этих анимациях мы показываем поток электронов, который идет от отрицательного к положительному, но вы, возможно, привыкли видеть обычный ток, который идет от положительного к отрицательному. Электронный поток — это то, что происходит на самом деле, но обычный ток был исходной теорией, которая до сих пор широко используется и преподается по сей день. Просто знайте о двух и о том, какой из них мы используем.
Просто знайте о двух и о том, какой из них мы используем.
Электричество, которое вы получаете от электрических розеток в своих домах, представляет собой электричество переменного или переменного тока, это отличается от электричества, обеспечиваемого аккумулятором. При переменном токе электроны непрерывно текут вперед и назад, подобно морскому приливу, который течет между приливом и отливом. Осциллограф покажет переменный ток как волну, проходящую как через положительную, так и через отрицательную области, потому что она течет вперед, это положительно, и назад, это отрицательно.
Переменный токЕсли мы посмотрим на отрезок медного провода, внутри него мы обнаружим атомы меди. В центре атома у нас есть протоны и нейтроны, протоны заряжены положительно, а нейтроны считаются нейтральными, поэтому они не имеют заряда. Вокруг них вращаются электроны, электроны заряжены отрицательно.
Медная проволока Некоторые из этих электронов могут свободно перемещаться к другим атомам. Они будут естественным образом перемещаться между другими атомами, но в случайных направлениях, что для нас бесполезно. Нам нужно, чтобы много электронов текло в одном направлении, и мы можем сделать это, обеспечив разность напряжений от источника питания, такого как батарея.
Они будут естественным образом перемещаться между другими атомами, но в случайных направлениях, что для нас бесполезно. Нам нужно, чтобы много электронов текло в одном направлении, и мы можем сделать это, обеспечив разность напряжений от источника питания, такого как батарея.
Когда мы говорим об атомах, вы часто будете слышать термин «ион». Ион — это просто атом, который имеет неравное количество электронов или протонов. Атом имеет нейтральный заряд, когда в нем одинаковое количество протонов и электронов, потому что протоны заряжены положительно, а электроны отрицательно заряжены, поэтому они уравновешиваются. Если в атоме больше электронов, чем протонов, то это отрицательный ион. Если в атоме больше протонов, чем электронов, то это положительный ион.
Ион Напряжение похоже на давление в резервуаре с водой. Чтобы узнать, какое у нас давление, мы должны сравнить давление внутри трубы с давлением снаружи, и для этого мы используем манометр. Когда дело доходит до напряжения, мы используем вольтметр для измерения разницы напряжения между двумя разными точками. Если мы измерим разницу между батареями, мы получим 1,5 В, но если мы измерим тот же конец, мы получим 0 В, потому что это тот же конец, поэтому разницы нет.
Если мы измерим разницу между батареями, мы получим 1,5 В, но если мы измерим тот же конец, мы получим 0 В, потому что это тот же конец, поэтому разницы нет.
Некоторые материалы позволяют электронам легко проходить через них, они известны как проводники. Примерами этого являются медь и большинство металлов. Другие материалы не пропускают электроны, они известны как изоляторы. Примерами этого являются резина и большинство пластмасс. Поэтому мы используем медные провода с резиновой изоляцией. Медь переносит электричество туда, где оно нам нужно, а резина защищает нас.
Смешивая определенные материалы, мы можем вызывать химические реакции. Это когда атомы одного материала взаимодействуют с атомами другого материала и во время этого взаимодействия атомы будут связываться друг с другом или распадаться, электроны также могут быть захвачены или освобождены атомами в ходе химической реакции.
Хорошо, теперь, когда мы рассмотрели основы, давайте заглянем внутрь батареи и посмотрим, как она работает.
Как работает щелочная батарея?
Помните, мы кратко говорили об атомах. Ну, все эти материалы внутри батареи состоят из множества различных атомов, плотно упакованных вместе. Они представлены цветными шариками, каждый цвет которых соответствует разному материалу и, следовательно, разному атому для нашего очень упрощенного примера. Когда мы объединим все эти материалы вместе внутри капсулы, мы получим небольшую химическую реакцию, в которой атомы начнут взаимодействовать друг с другом.
Внутри батареиПрежде всего, атом иона гидроксида в электролите соединяется с атомом цинка в анодной части. Эта химическая реакция известна как окисление и создаст гидроксид цинка, поскольку соединение цинка и гидроксида высвобождает электроны. Эти электроны теперь могут свободно двигаться и будут собираться на латунном штифте.
В то же время атом оксида марганца соединяется с молекулой воды из электролита, а также со свободным электроном в химической реакции, известной как восстановление. Во время химической реакции оксид марганца превращается в немного другую версию оксида марганца, этой версии больше не нужен атом иона гидроксида, поэтому он выбрасывает его в электролит. Атом воды замещается атомом, выброшенным из реакции окисления. Ион гидроксида теперь свободен и может пройти через сепаратор. Но пока не будет, потому что в анодной секции для него нет места.
Во время химической реакции оксид марганца превращается в немного другую версию оксида марганца, этой версии больше не нужен атом иона гидроксида, поэтому он выбрасывает его в электролит. Атом воды замещается атомом, выброшенным из реакции окисления. Ион гидроксида теперь свободен и может пройти через сепаратор. Но пока не будет, потому что в анодной секции для него нет места.
Итак, как вы можете видеть, у нас есть накопление электронов на отрицательном выводе. Поскольку электроны заряжены отрицательно, и теперь у нас больше электронов на отрицательной клемме, чем на положительной, это означает, что у нас есть разница в напряжении между двумя концами, и мы можем измерить эту разницу с помощью мультиметра.
Помните, что мы можем измерить только разницу в напряжении между двумя разными точками. Если мы измерим одну и ту же точку, мы получим ноль вольт, потому что разницы нет.
Электроны отталкиваются друг от друга и хотят переместиться в область с меньшим количеством электронов.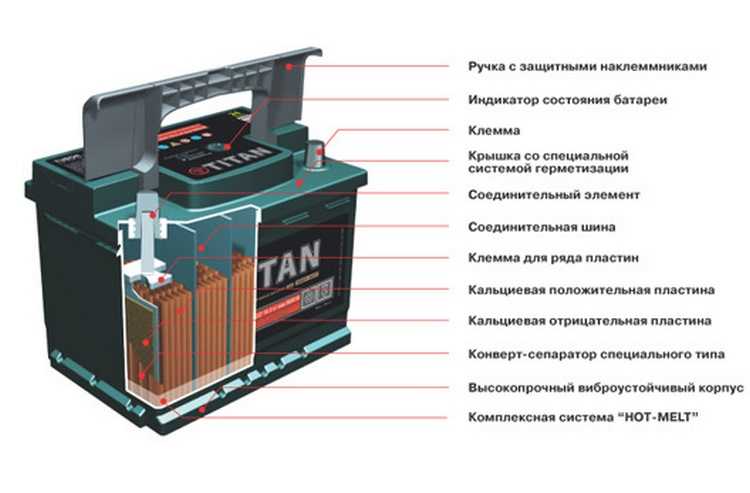 В положительной области меньше электронов, поэтому они попытаются добраться до этой клеммы. Сепаратор не позволяет им течь внутрь аккумулятора и достигать положительной клеммы.
В положительной области меньше электронов, поэтому они попытаются добраться до этой клеммы. Сепаратор не позволяет им течь внутрь аккумулятора и достигать положительной клеммы.
Следовательно, электронам нужен другой путь. Если мы предоставим электронам внешний путь, такой как провод, электроны будут течь по нему, чтобы добраться до положительной клеммы. Помещая такие вещи, как лампа, на пути электронов, электроны должны будут проходить через нее, и поэтому мы заставляем их выполнять работу за нас, например, освещать лампу.
Зажигание лампыПока у нас есть замкнутая цепь между клеммами, химическая реакция будет продолжаться, и электроны текут от отрицательной клеммы. Если мы удалим провод или разомкнем цепь, то химическая реакция прекратится.
Итак, давайте вспомним происходящую химическую реакцию. Свободные электроны попадают в батарею через положительный полюс. Это объединяется с оксидом марганца и молекулой воды на катоде, который высвобождает ион гидроксида в электролит.
Ион гидроксида проходит через сепаратор и соединяется с атомом цинка, образуя гидроксид цинка, при этом высвобождаются электроны и молекула воды. Электроны хотят добраться до области с меньшим количеством электронов, положительный полюс имеет меньше электронов, поэтому они будут течь по проводу, чтобы достичь этого, и поэтому химическая реакция повторяется снова и снова непрерывно.
Однако внутри батареи содержится лишь определенное количество материала, поэтому со временем химическая реакция будет продолжаться все труднее и труднее, и в конечном итоге электроны перестанут течь. Аккумулятор больше не будет использоваться, и его необходимо утилизировать.
Соединение батарей вместе
Мы можем использовать батарею для питания некоторых компонентов, но обычно одной батареи недостаточно для питания наших устройств, для этого нам нужно объединить батареи.
Аккумуляторы можно подключать двумя способами. Серийно или параллельно. Ранее мы подробно рассмотрели эти типы схем, посмотрите серию ЗДЕСЬ, и параллельную ЗДЕСЬ.
Когда мы соединяем батареи последовательно, напряжение каждой батареи суммируется. Таким образом, две батареи по 1,5 В дают нам 3 В, а 3 батареи дают нам 4,5 В и т. д. Фактическое напряжение может немного отличаться в реальном мире. Напряжение увеличивается, потому что каждая батарея ускоряет входящие в нее электроны, поэтому мы получаем более высокое напряжение.
ПараллельноЕсли мы подключим батареи параллельно, то мы получим только 1,5 В, независимо от того, сколько мы подключим. Это потому, что путь сливается на подаче, но разделяется на обратном пути, поэтому электроны не будут ускоряться. Однако этот тип конфигурации сможет обеспечить больший ток, а также будет иметь большую емкость, поэтому мы сможем питать что-то дольше. Например, если батарея имела емкость 1200 мАч и мы поставили две параллельно, у нас будет емкость 2400 мАч, но напряжение 1,5 В. Если мы подключим их последовательно, у нас будет емкость 1200 мАч, но напряжение 3 В.
Серия и параллельЕмкость
Мы используем батареи для питания наших цепей. Но как долго батарея может питать нашу схему? Когда мы смотрим на упаковку или лист данных для батареи, мы видим значение с буквами m.A.h рядом с ним. Это рейтинг в миллиампер-часах.
Но как долго батарея может питать нашу схему? Когда мы смотрим на упаковку или лист данных для батареи, мы видим значение с буквами m.A.h рядом с ним. Это рейтинг в миллиампер-часах.
Например, этот имеет номинал 2500 мАч. Это означает, что теоретически он может обеспечить ток 2500 миллиампер в час, или 1250 мА в течение 2 часов, или 20 мА в течение 125 часов. Однако в реальной жизни это, вероятно, не продлится так долго, потому что химическая реакция замедляется, поэтому внутреннее сопротивление батареи меняется по мере ее разрядки. Есть много других вещей, которые влияют на это, например, возраст и температура.
Нет реального способа точно рассчитать продолжительность жизни, лучше всего просто проверить ее. Однако мы можем оценить срок службы по следующей формуле:
Срок службы батареи = Емкость (мАч) / ток цепи (мА).
На нашем веб-сайте мы создали простой бесплатный калькулятор, с помощью которого вы можете рассчитать время работы аккумулятора, а также необходимую емкость. Проверьте это ЗДЕСЬ .
Проверьте это ЗДЕСЬ .
Так, например, в этой схеме мы вычисляем спрос 19мА, а батарея имеет емкость 3000 мАч. Итак, 3000/19 дает нам 157,9 часа. Это действительно лучший сценарий, и на самом деле он почти наверняка не достигнет этого.
Срок службы батареиКак измерить с помощью мультиметра
Чтобы измерить напряжение, мы просто выбираем функцию постоянного тока на нашем мультиметре, а затем подключаем красный провод к положительной клемме, а черный провод к отрицательной. Это даст нам показания напряжения.
Номинальное значение батареиВы можете видеть, что эта батарея рассчитана на 1,5 В, но когда мы протестировали ее, мы получили 1,593 В
Батарея разряженаКогда батарея разряжена, мы получаем более низкое напряжение, это показывает 1,07 В, поэтому она полностью разряжена.
Однако иногда мы могли получить напряжение около 1,5 В, даже если батарея разряжена.
Чтобы полностью протестировать батарею, нам нужно протестировать ее под нагрузкой, чтобы проверить, может ли она еще быть полезной.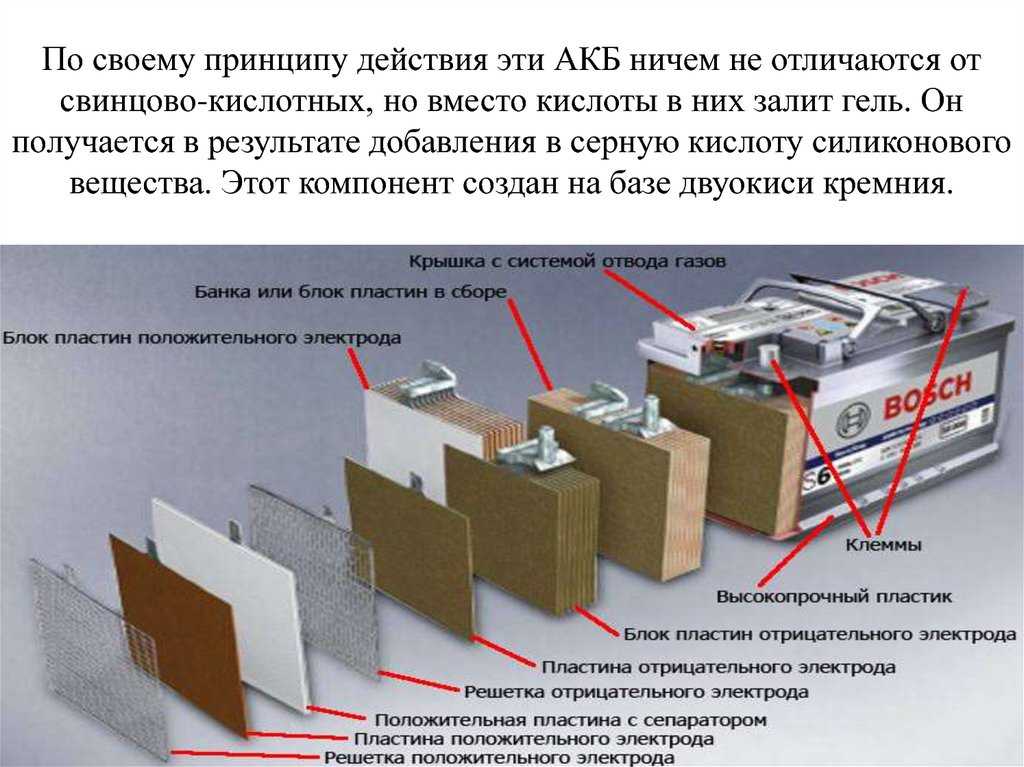 Для этого нам понадобится резистор.
Для этого нам понадобится резистор.
Итак, мы берем резистор около 100 Ом, хотя он не обязательно должен быть именно таким, но мы подключаем резистор между нашими двумя щупами. В этом случае мы просто использовали несколько зажимов типа «крокодил», чтобы соединить резистор между щупами, вот так.
Таким образом, ток будет протекать через резистор, и мы сможем снять показания напряжения, когда это произойдет. Если батарея еще в порядке, то уровень напряжения снизится лишь незначительно.
Пример батареиНапример, эта батарея имеет номинальное напряжение 1,5 В, без нагрузки 1,593 В, с подключенным резистором 1,547 В, так что это все еще хорошо.
Пример батареиЭта батарея также рассчитана на 1,5 В, когда мы измеряем ее без нагрузки, она показывает точно 1,5 В, но когда мы подключаем резистор, она падает до 0,863 В, поэтому мы знаем, что она разрядилась.
Батарея разряжена Но теперь, когда вы полностью заряжены, зайдите на сайт Squarespace.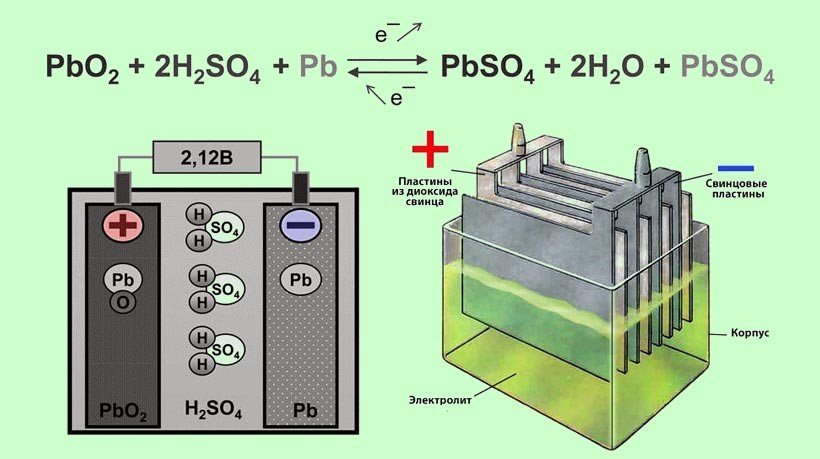 com и создайте свое собственное веб-присутствие в Интернете, которое содержит множество функций, позволяющих людям запускать, делиться и продвигать свои собственные проекты.
com и создайте свое собственное веб-присутствие в Интернете, которое содержит множество функций, позволяющих людям запускать, делиться и продвигать свои собственные проекты.
Мощные инструменты для ведения блога, чтобы демонстрировать фотографии, видео и обновления ваших проектов.
Вы можете легко планировать встречи для занятий и сессий с членами команды и клиентами с помощью встроенного инструмента. И вы даже можете собирать платежи или пожертвования, чтобы помочь поддержать ваше дело.
Посетите сайт Squarespace.com, чтобы получить бесплатную пробную версию, а когда будете готовы к запуску, перейдите по адресу Squarespace.com/engineeringmindset , чтобы сэкономить 10% на первой покупке веб-сайта или домена.
Свинцово-кислотный аккумулятор — устройство и принцип работы, разновидности
Конструкция и принцип действия классического свинцово-кислотного аккумулятора основаны на обратимых электрохимических реакциях свинца и диоксида свинца с водным раствором серной кислоты: при разряде аккумулятора до нагрузки оксид свинца на катоде и свинец на аноде, взаимодействуя с анионами серы, переходят в сульфат свинца (на катоде восстанавливается диоксид свинца, на аноде свинец окисляется).
При зарядке аккумулятора сульфат свинца на пластинах распадается на ионы, на катоде образуется оксид свинца, а на аноде снова металлический свинец. При этом концентрация раствора серной кислоты увеличивается, так как ионы серной кислоты, воссоединяясь с водородом, снова образуют серную кислоту. Таким образом, можно использовать одну и ту же батарею снова и снова, просто время от времени ее подзаряжая.
В процессе разрядки аккумулятора снижается концентрация серной кислоты — уменьшается плотность электролита. И когда в конце заряда количество сульфата свинца на электродах практически исчерпывается, начинается процесс электролиза воды. Это явление можно наблюдать в виде обилия пузырьков кислорода и водорода, что является признаком перезаряда свинцово-кислотного аккумулятора, и многие автолюбители знают об этом не понаслышке.
Такого явления лучше не допускать, так как в этом случае, во-первых, безвозвратно расходуется вода, во-вторых, возникает опасность взрыва. Поэтому все обычные зарядные устройства уменьшают ток заряда при достижении определенного напряжения на клеммах аккумуляторной батареи. Что касается потерь воды, то их традиционно восполняют добавлением в аккумулятор дистиллированной воды.
Что касается потерь воды, то их традиционно восполняют добавлением в аккумулятор дистиллированной воды.
На самом деле внутри корпуса 12-вольтового свинцово-кислотного аккумулятора находится батарея из шести последовательно соединенных друг с другом ячеек — ячеек. Одна ячейка (максимальное напряжение одной такой ячейки 2,17 вольта) состоит из двух электродов и разделительных пластин — сепараторов, которые химически не взаимодействуют с электролитом, но мешают контакту между электродами.
Электроды представляют собой решетки из чистого свинца с порошком диоксида свинца, запрессованным в решетку анода, и порошком свинца, запрессованным в катодную решетку. Порошки здесь используются для того, чтобы максимально увеличить площадь взаимодействия электродов с электролитом, и тем самым получить максимально возможную электрическую емкость аккумулятора, так как электроды погружены в электролит. Аккумуляторы на 3, 6 или 12 ячеек дают соответственно 6, 12 и 24 вольта на клеммах аккумулятора.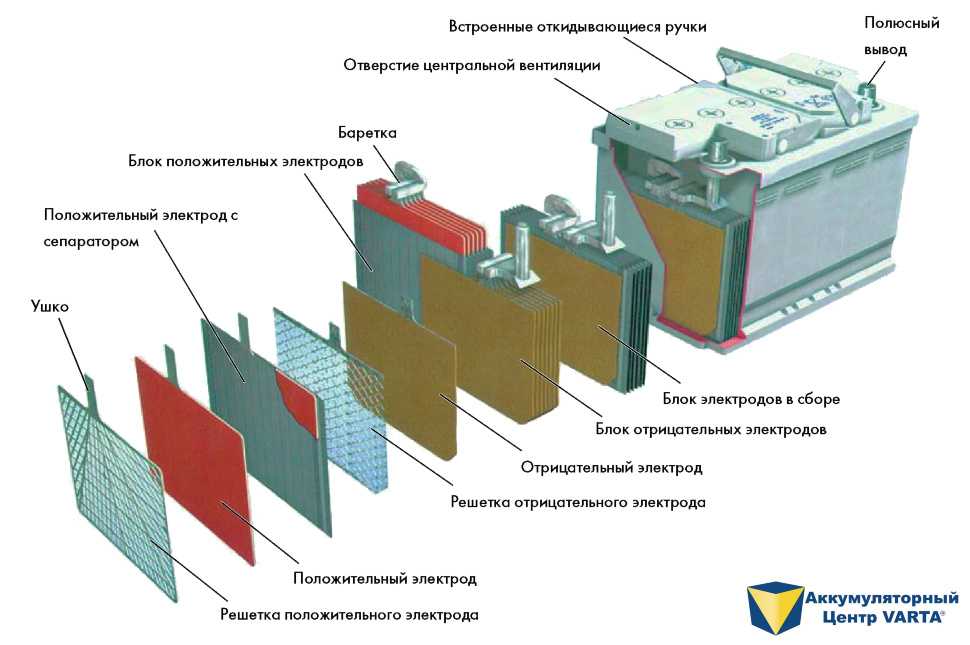
Автомобильный стартерный аккумулятор (с жидким электролитом)
Классические автомобильные аккумуляторы — кислотные аккумуляторы, с жидким электролитом, на номинальное напряжение 12 вольт. Крышка такой батареи имеет 6 отверстий с заглушками для удобства обслуживания — плотность электролита можно проверить с помощью ареометра, при необходимости долить дистиллированной воды. Диапазон мощностей от 35 до 230 А*ч; они обеспечивают пусковые токи от 330 до 1500 А.
Задача такой батареи — проворачивать стартер в момент запуска автомобиля, а также питать бортовую сеть (фары, приборы, бортовые потребители через прикуриватель и др.) Аккумуляторы этого формата на жидком электролите постепенно уходят в прошлое, уступая место более современным аккумуляторам с загущенным электролитом.
Гелевые аккумуляторы (GEL) для ИБП, систем безопасности и др.
В бытовых источниках бесперебойного питания (ИБП, ИБП) (см. — Как устроены и работают ИБП?), в цепях питания систем охранной сигнализации и других аналогичных применений, представляют собой герметичные свинцово-кислотные аккумуляторы с загущенным электролитом — гелевые аккумуляторы.
Жидкий кислотный электролит здесь загущен до пастообразной консистенции водным щелочным раствором силикатов натрия (Na2Si2O4). Аккумуляторы этого типа не требуют обслуживания и доливки дистиллированной воды. Гелевые аккумуляторы выпускаются емкостью от 1 до 100 А*ч.
AGM Technology
Улучшенный вариант гелевого аккумулятора — необслуживаемый свинцово-кислотный аккумулятор с пористыми сепараторами из стекловолокна (Absorbent Glass Mat), допускающий более жесткие условия зарядки и эксплуатации. Отличительной особенностью технологии AGM является использование пропитанного стекловолокном пористого заполнителя, наполненного пористым заполнителем.
Микропоры такого материала не полностью заполнены электролитом, и свободный от электролита объем здесь используется для рекомбинации газа. Аккумулятор, изготовленный по технологии AGM, имеет ряд преимуществ: виброустойчивость, нормальную работу в любом положении (главное не перевернуть, так как сверху есть аварийные клапаны).
