Добавка к бензину и автомобильное топливо, ее содержащее
Изобретение относится к области нефтепереработки и нефтехимии, в частности к высокооктановым добавкам к автомобильным бензинам и автомобильному топливу, модифицированному этой добавкой. Добавка к бензинам содержит ароматический амин (его производные) общей формулы где R1-R3 — радикалы, выбранные из групп Н, СН3, С2Н5, в комбинации с оксигенатом общей формулы: R4-O-R5, где R4-Н или алкил С1-С3, конкретно Н, метил, этил, изопропил, R5 — один из алкильных радикалов от С1 до С6, конкретно метил, этил, (н-, изо-)пропил, (н-, изо-, трет-)бутил, изопентил, изогексил, или их смесь с добавкой гидразина или его водного раствора при массовом соотношении компонентов — ароматический амин (его производные) : оксигенат : гидразин = 0,5-70 : 93,5-29,995 : 0,005-2. Добавка может содержать антиоксидант в количестве, не превышающем 5 мас. % в расчете на массу композиции добавки. Автомобильное топливо содержит 0,3-25 мас.% добавки. Дополнительно топливо может содержать моющую и/или антикоррозионную присадку. Содержание антиоксиданта, моющей и антикоррозионной присадки в топливе не более 0,5 мас.% от состава топлива. 2 c. и 7 з.п. ф-лы, 7 табл.
% в расчете на массу композиции добавки. Автомобильное топливо содержит 0,3-25 мас.% добавки. Дополнительно топливо может содержать моющую и/или антикоррозионную присадку. Содержание антиоксиданта, моющей и антикоррозионной присадки в топливе не более 0,5 мас.% от состава топлива. 2 c. и 7 з.п. ф-лы, 7 табл.
Настоящее изобретение относится к нефтепереработке и нефтехимии, в частности к высокооктановым добавкам к автомобильным топливам, а также к автомобильному топливу, содержащему эту добавку.
Известно, что азотароматические высокооктановые добавки позволяют увеличивать октановое число бензина с исходным RON /исследовательский метод/ 90,5 (Papachistos M. et al.// J. of the Institute of Energy. — 1991. — V.44, 459. — P. 113-123). В табл. 1 представлены азотсодержащие амины и показано влияние их на качество бензина. Однако указанные в таблице азотсодержащие органические соединения обладают недостаточно выраженными антидетонационными свойствами.
Известно также, что введение в бензин N-метилбензиламина и бензиламина в количестве 2,7 и 1,6 мас.% повышает октановое число RON неэтилированного бензина на 1,0 и 8,0 единиц соответственно (Патент US 4321063, 1982), а введение в бензин пиперидина и его производных в количестве 0,1 моля повышает октановое число на 0,7-1,1 единиц (патент US 4321061, 1982).
В качестве беззольной азотсодержащей антидетонаторной присадки в бензинах могут быть использованы алифатические С2, С3 или C4 диамины. При введении 1,0 мас.% этилендиамина, пропандиамина или бутандиамина-1,4 октановое число RON бензина увеличивается соответственно на 0,8, 1,4 или 1,0 единиц (патент US 4445900, 1984).
Недостатком указанных N-органических присадок, как и вышеописанных, является невысокая антидетонаторная способность при их введении в автомобильное топливо.
Известна топливная бензиновая композиция, которая может содержать обводненные спирты C1-C5 и спирты C4-C8 в количестве 5-40 об. % (патент US 3822119, 1974). Недостатком такой композиции являются невысокие антидетонационные свойства (октановое число смешения RON спиртов не превышает 130), плохие низкотемпературные свойства и высокая коррозионная активность топливной композиции.
% (патент US 3822119, 1974). Недостатком такой композиции являются невысокие антидетонационные свойства (октановое число смешения RON спиртов не превышает 130), плохие низкотемпературные свойства и высокая коррозионная активность топливной композиции.
Известна оксигенатная топливная композиция, содержащая базовое автомобильное топливо и 2-65 об.% смеси кислородсодержащих добавок, таких как метил-трет-бутиловый эфир, изопропил-трет-бутиловый эфир и изобутил-трет-бутиловый эфир. Кроме того, базовое топливо может содержать до 85 об.% добавки, включающей один или несколько спиртов, а именно: изобутиловый спирт, трет-бутиловый спирт, изопропиловый спирт и метиловый спирт (патент ЕР 0064253, 1982). Недостатком такой топливной композиции является использование значительного количества метил-трет-бутилового эфира, что является неэкономичным как с позиции приготовления, так и хранения топлива, поскольку метил-трет-бутиловый эфир является бионеразлагаемым веществом, что может нанести необратимый вред окружающей среде при его утечке.
Известны композиции моторных топлив, содержащие бензин, этиловый спирт, метил-трет-бутиловый эфир, этил-трет-бутиловый эфир, трет-бутиловый спирт (патенты US 4207076, 4207077, 1980). Недостатком таких композиций при высоком содержании оксигенатов (более 20%) является высокая гигроскопичность и, как следствие, фазовая нестабильность и значительная коррозионность такого топлива.
Известна многофункциональная добавка к автомобильным бензинам на основе N-метиланилина, содержащая дополнительно органические соединения марганца, моющую добавку «АВТОМАГ» и 2,6-ди-трет-бутил-4-метилфенол (патент RU 2114901, 1998).
Также известна топливная композиция для двигателей внутреннего сгорания, содержащая N-метиланилин и органические соединения марганца (патент RU 2114900, 1998).
Недостатком марганецсодержащих добавок на основе N-метиланилина и автомобильных топлив, их содержащих, является повышенное нагарообразование на свечах автомобилей; их химическая неустойчивость — разложение на свету с потерей антидетонационных свойств; нарушение нормальной работы каталитических нейтрализаторов выхлопных газов автомобилей (Применение присадок в топливах для автомобилей. Данилов А.М. / Справочн.изд. — М.: Химия, 2000 — стр.36).
Данилов А.М. / Справочн.изд. — М.: Химия, 2000 — стр.36).
Известна многофункциональная добавка к автомобильным бензинам (Патент RU 2132359, 1999), содержащая в своем составе, мас.%: Ферроцен — 0,05-3,0 Антиоксидант — 0,1-0,2 Анилин — 0,1-10,0 Присадка «АВТОМАГ» — Не более 6,0 Спирты С3-С5 и/или их простые эфиры — Не более 95,0 N-метиланилин — 4,0-98,0 Добавка указанного состава вводится в автомобильные бензины в концентрации 0,2-20,0 мас.%.
Известна также добавка к бензину (патент RU 2129141, 1999), содержащая, мас.%:
N-метиланилин — 5,0-10,0
Ферроцен и/или -гидроксиизопропил-ферроцен — 0,05-0,15
Стабилизированный этиловый спирт — Остальное до 100
Указанная добавка вводится в топливную композицию в количестве 1,5-5 мас.%.
Также известна топливная композиция для двигателей внутреннего сгорания (патент RU 2110561, 1998), содержащая, мас.%:
Метилтретбутиловый эфир — 0,5-3,5
Органические соединения железа — 0,001-0,008
N-метиланилин и/или ксилидин — Не более 0,25-0,3
Бензин — Остальное до 100
Недостатком железосодержащих добавок и топлив (топливных композиций), их содержащих, так же, как и марганецсодержащих добавок и композиций, включающих их, является повышенное нагарообразование на свечах автомобиля и дополнительные отложения в двигателе внутреннего сгорания. Кроме того, добавки и топлива, содержащие марганец и железо, запрещены к применению Мировой топливной хартией 1998 г. (Применение присадок в топливах для автомобилей. Данилов А.М. / Справочн. изд. — М.: Химия, 2000 — стр.8).
Кроме того, добавки и топлива, содержащие марганец и железо, запрещены к применению Мировой топливной хартией 1998 г. (Применение присадок в топливах для автомобилей. Данилов А.М. / Справочн. изд. — М.: Химия, 2000 — стр.8).
Наиболее близкой по составу и техническому результату является многофункциональная добавка к бензинам и топливо для двигателей внутреннего сгорания, содержащее ее (Евразийский Патент 000882, 2000).
Добавка имеет следующий состав, мас.%:
N-метиланилин — 6,0-12,0
Стабилизатор — спирты С3-C5 — 0,2-20,0
Моющая присадка на основе амида — 0,5-1,5
Антиоксидант — 2,6-ди-трет-бутил-4-метилфенол или раствор смеси экранированных фенолов в толуоле — 0,01-0,1
Этиловый спирт — Остальное до 100
Добавка указанного состава вводится в автомобильное топливо в количестве от 2 до 15 мас.%.
Основными недостатками данной добавки и топлива, ее содержащего (Евразийский патент 000882, 2000), являются:
— необходимость использования стабилизатора — алифатических спиртов С3-С5,
— недостаточно высокая антидетонаторная способность,
— недостаточно высокая химическая стабильность композиции и автомобильного топлива, содержащего добавку указанного состава, особенно при хранении.
Задачей настоящего изобретения является разработка новой добавки к автомобильному топливу, позволяющей повысить антидетонационные свойства бензинов и увеличить срок хранения при сохранении качества топлива.
Поставленная задача достигается настоящей добавкой следующего состава:
ароматический амин общей формулы:
где R1…R3 — радикалы, выбранные из Н, СН3, C2H5
или их смесь,
оксигенат общей формулы формулы:
R4-O-R5,
где R4 — один из радикалов: Н, СН3, С2Н5, изо-С3Н7;
R5 — один из радикалов: СН3, С2Н5, С3Н7 (н-, изо-), С4Н9 (н-, изо-, трет-), изо-С5Н11, изо-С6Н13
или их смесь и гидразин или его водный раствор при массовом соотношении компонентов — ароматический амин: оксигенат: гидразин = 0,5-70: 93,5-29,995: 0,005-2.
Для дополнительной химической стабилизации при транспортировке и длительном хранении добавка может модифицироваться введением антиоксидантов — ионола (агидол-1), трет-бутилпирокатехина или раствора экранированных алкилфенолов в толуоле (агидола-12) в количествах не более 5 мас.% (в расчете на массу добавки).
Антидетонационные свойства выбранных ароматических аминов представлены ниже в сравнении с известными аминами и оксигенатами в табл. 2.
Учитывая склонность ароматических аминов (их производных) к окислению и осмолению, необходимым являлось решение задачи эффективного разбавления и ингибирования N-ароматических соединений с вышеуказанной формулой. Разбавителями ароматических аминов могут являться оксигенаты. При этом в ароматический амин и/или оксигенат необходимо вводить кислородпоглощающий компонент — гидразин или его концентрированный водный раствор — гидразингидрат. Кроме того, гидразин в предлагаемой композиции проявляет хорошо выраженный антидетонационный эффект.
Предлагаемая добавка, содержащая ароматический амин (его производные) — R3-C6H4-NR1R2, оксигенат R4-O-R5 и гидразин N2H4 или его водный раствор используются для приготовления конечного автомобильного топлива и может храниться (использоваться) как компонент автомобильного топлива.
Таким образом, задачей настоящего изобретения также является разработка автомобильного топлива с высоким октановым числом, высокими показателями стабильности при хранении и эксплуатации.
Поставленная задача решается автомобильным топливом, содержащим добавку, включающую ароматические амины или их смесь, соответствующие формуле R3-C6H4-NR1R2, оксигенат (их смесь) химического состава R4-O-R5, гидразин или его водный раствор, в количестве 0,3-25 мас. % (в расчете на массу топлива).
% (в расчете на массу топлива).
Автомобильное топливо имеет следующий состав, мас.%:
Ароматический амин (его производные) R3-C6H4-NR1R2 — 0,2-5
Оксигенат R4-O-R5 — Не более 20
Гидразин N2H4 — Не более 0,5
Антиоксиданты, моющие и антикоррозионные присадки — Не более 0,5 суммарно
Углеводородный компонент — Остальное до 100
Получаемое автомобильное топливо может модифироваться известными присадками, такими как антиоксиданты, антикоррозионные и моющие присадки.
В качестве моющей присадки используют продукт конденсации полиамина общей формулы NH2-(СН2)-(NH-(CH2)2)n-NH2, где n=0-4, с карбоновыми кислотами с числом атомов углерода C10-С20.
В качестве антикоррозионной присадки используют присадку, выбранную из группы, включающей смесь предельных алифатических алкиламинов общей формулы RNH2, где R представляет собой C12-C20 алкил,четвертичные аммониевые соли высших карбоновых или алкоксиароматических кислот с числом атомов углерода C12-C20, полиэтилен-(или полипропилен-) полиаминов с числом аминогрупп от 2 до 8; или сукцинимиды на основе алкенилянтарного ангидрида с числом атомов углерода от 12 до 36 и предельных аминов RNH2, где R представляет собой C12-С20 алкил или их смесь.
Эффективность предлагаемой добавки и автомобильного топлива, ее содержащего, испытывалась известными методами, обычно используемыми для определения октанового числа топлива, а также стабильность при хранении.
Результаты испытаний сведены в табл. 1-7.
Настоящее изобретение иллюстрируется следующими примерами.
Пример 1
Для сравнительных испытаний были выбраны известные амины, в том числе и характеризующиеся формулой R3-C6H4-NR1R2. Характеристика исходных аминов представлена в табл. 3. Используемый для сравнительных испытаний бензин получали смешением алкилата, изопентана, риформата, бензина каталитического крекинга и прямогонного бензина в двух видах:
а) с октановым числом RON 90,6 — состав, мас.%:
изоалканы 32,5, н-алканы 10,4,
циклоалканы 7,3, олефины 21,3, ароматические 28,7;
б) с октановым числом RON 98,0 — состав, мас. %:
%:
изоалканы 28,7, н-алканы 8,1,
циклоалканы 6,0, олефины 24,4, ароматические 32,8.
Оценка антидетонационной эффективности исходных ароматических аминов проводилась на бензинах вышеуказанного состава при введении в каждый вид бензина — а) и б) по 1 об.% каждого амина.
Результаты сравнительных испытаний приведены в табл. 4.
Из данных табл. 3, 4 видно, что используемые ароматические амины, соответствующие формуле R3-C6H4-NR1R2, значительно превосходят по антидетонационным свойствам другие N-органические соединения (амины), не соответствующие выбранной химической формуле.
Пример 2
Предлагаемая добавка к бензину, содержащая ароматический амин, соответствующий формуле R3-C6H4-NR1R2, оксигенаты, соответствующие формуле R4-O-R5, и гидразин N2H4 или его водный раствор, их композиции были испытаны на бензине а) с RON 90,6 из примера 1. При этом в исходную добавку и/или в конечный бензин вводился антиоксидант — смесь экранированных алкилфенолов — в основном 2,6-ди-трет-бутил-4-метилфенол — ионол (агидол-1) или его раствор в толуоле (агидол-12) или трет-бутил-пирокатехин. В конечный бензин, кроме антиоксиданта, вводились присадки:
При этом в исходную добавку и/или в конечный бензин вводился антиоксидант — смесь экранированных алкилфенолов — в основном 2,6-ди-трет-бутил-4-метилфенол — ионол (агидол-1) или его раствор в толуоле (агидол-12) или трет-бутил-пирокатехин. В конечный бензин, кроме антиоксиданта, вводились присадки:
моющая присадка — продукт конденсации полиамина общей формулы NH2-(CH2)-(NH-(CH2)2)n-NH2, где n= 0-4, с карбоновыми кислотами с числом атомов углерода С10-С20,
антикоррозионная присадка, выбранная из группы, включающей смесь предельных алифатических алкиламинов общей формулы RNH2, где R представляет собой C12-C20 алкил, четвертичные аммониевые соли высших карбоновых или алкоксиароматических кислот с числом атомов углерода С12-С20, полиэтилен-(или полипропилен-) полиаминов с числом аминогрупп от 2 до 8; или сукцинимиды на основе алкенилянтарного ангидрида с числом атомов углерода от 12 до 36 и предельных аминов RNH2, где R представляет собой C12-C20 алкил или их смесь.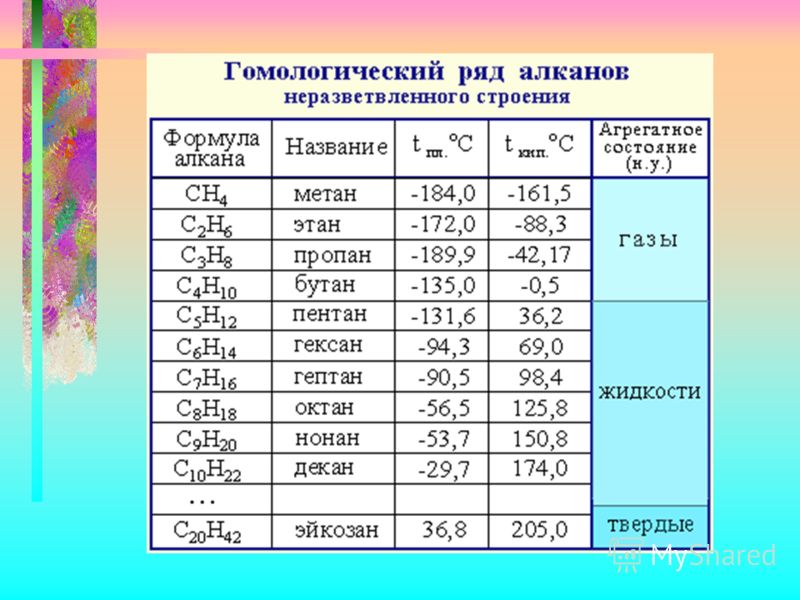
Оксигенаты для испытаний выбирают чистотой не менее 96 мас.% по основному веществу и по содержанию влаги не более 1 мас.% Причем введение оксигенатов не требовало введения стабилизаторов — спиртов С3-C5 по сравнению с прототипом.
Результаты испытаний сведены в табл. 5 и 6.
Из табл. 5 следует, что оптимальным соотношением компонентов добавки является ароматический амин: оксигенат: гидразин = 0,5-70: 93,5-29,995: 0,005-2.
Результаты табл. 6 показывают, что качественное автомобильное топливо можно получить при введении добавки в количестве 0,3-25 мас.%.
Пример 3
Для сравнения эффективности и устойчивости добавки согласно изобретению, а также автомобильного топлива, ее содержащего, и известной добавки, раскрытой в Евразийском патенте 000882, были проведены испытания, результаты которых сведены в табл. 7.
7.
В качестве образцов сравнения были приготовлены:
— добавка А (известная добавка, раскрытая в ЕА 000882) (табл.1, пример 1) содержащая, мас. %:
— N-метиланилин 6; смесь алифатических спиртов С3-С5 (изопропанол 99,5%): изобутанол (99,0%):изопентанол (99,1%) 1:1:1-0,5; моющая присадка на основе амида 0,5; антикоррозионная присадка 0,4; этиловый спирт (99,6%) 92,6,
— добавка В согласно изобретению, содержащая, мас. %:
— N-метиланилин 6; смесь алифатических спиртов С3-C5 0,5; этиловый спирт 92,6.
Как видно из данных табл. 7, известная добавка (образец сравнения «А») не обладает достаточно стабильными физико-химическими характеристиками, что отражается отрицательно как на свойствах самой добавки, так и на модифицируемом этой добавкой автомобильном бензине. Особенно важным является тот факт, что предлагаемая добавка хранится практически без видимого изменения оптической плотности, т. е. практически не осмоляется, а автомобильный бензин, модифицированный этой добавкой, не накапливает фактических смол более допустимого по действующим стандартам на автомобильные топлива уровня — 4-5 мг/100 мл (разрешенный максимум).
е. практически не осмоляется, а автомобильный бензин, модифицированный этой добавкой, не накапливает фактических смол более допустимого по действующим стандартам на автомобильные топлива уровня — 4-5 мг/100 мл (разрешенный максимум).
Формула изобретения
1. Добавка к бензину, содержащая ароматический амин и оксигенат, отличающаяся тем, что в качестве ароматического амина она содержит производное общей формулы
где R1 является одним из радикалов, выбранным из Н, СН3, С2Н5,
R2 является одним из радикалов, выбранным из Н, СН3, С2Н5,
R3 является Н или радикалом СН3, С2Н5 в мета-, пара- или ортоположении,
или их смесь и оксигенат общей формулы
R4-О-R5,
где R4 является одним из радикалов, выбранным из Н, СН3, C2H5, изо-С3Н7,
R5 является одним из радикалов, выбранным из: СН3, С2Н5, (н-, изо-)С3Н7, (н-, изо-, трет-)С4Н9, изо-С5Н11, изо-С6Н13,
или их смесь и добавку гидразина или его водного раствора при массовом соотношении компонентов ароматический амин (R3-C6H4-NR1R2): оксигенат (R4-O-R5): гидразин (в пересчете на N2H4) = 0,5-70: 93,5-29,995: 0,005-2.
2. Добавка по п. 1, отличающаяся тем, что она дополнительно содержит антиоксидант.
3. Добавка по п. 2, отличающаяся тем, что антиоксидантом является ионол(агидол-1), или трет-бутилпирокатехин, или раствор экранированных алкилфенолов в толуоле (агидол-12).
4. Добавка по п. 3, отличающаяся тем, что антиоксидант содержится в количестве не более 5 мас. % (в расчете на массу композиции добавки).
5. Автомобильное топливо, содержащее добавку, отличающееся тем, что оно содержит в качестве добавки добавку по пп. 1-4 в количестве 0,3-25 мас. % (в расчете на массу топлива).
6. Автомобильное топливо по п. 5, отличающееся тем, что оно дополнительно содержит моющую и/или антикоррозионную присадки.
7. Автомобильное топливо по п. 6, отличающееся тем, что моющая композиция представляет собой продукт конденсации полиамина общей формулы NH2-(CH2)2-[NH-(CH2)2] n-NH2, где n= 0-4, с карбоновыми кислотами с числом атомов углерода С10-С20.
8. Автомобильное топливо по п. 5, отличающееся тем, что антикоррозионную присадку выбирают из группы, включающей смесь предельных алифатических алкиламинов общей формулы RNH2, где R представляет собой C12-C20 алкил, четвертичные аммониевые соли высших карбоновых или алкоксиароматических кислот с числом атомов углерода C12-C20, полиэтилен-(или полипропилен-)полиаминов с числом аминогрупп 2 — 8; или сукцинимиды на основе алкенилянтарного ангидрида с числом атомов углерода 12 — 36 и предельных аминов RNH2, где R представляют собой C12-C20 алкил или их смеси.
9. Автомобильное топливо по пп. 5-9, отличающееся тем, что оно содержит компоненты в следующем составе, мас. %:
Ароматический амин (его производные) R3-C6H4-NR1R2 — 0,2-5
Оксигенат R4-O-R5 — Не более 20
Гидразин N2H4 — Не более 0,5
Антиоксидант, моющие и антикоррозионные присадки — Не более 0,5 суммарно
Углеводородный компонент — Остальное до 100
РИСУНКИ
Рисунок 1, Рисунок 2, Рисунок 3, Рисунок 4, Рисунок 5, Рисунок 6, Рисунок 7, Рисунок 8, Рисунок 9, Рисунок 10, Рисунок 11, Рисунок 12, Рисунок 13
NF4A Восстановление действия патента СССР или патента Российской Федерации на изобретение
Дата, с которой действие патента восстановлено: 27. 04.2007
04.2007
Извещение опубликовано: 27.04.2007 БИ: 12/2007
Гексан, структурная формула, химические, физические свойства
1
H
ВодородВодород
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
ГелийГелий
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
ЛитийЛитий
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
БериллийБериллий
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
БорБор
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
УглеродУглерод
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
7
N
АзотАзот
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
КислородКислород
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
ФторФтор
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
НеонНеон
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
НатрийНатрий
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
МагнийМагний
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
АлюминийАлюминий
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
КремнийКремний
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
ФосфорФосфор
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
СераСера
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
ХлорХлор
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
АргонАргон
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
КалийКалий
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
КальцийКальций
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
СкандийСкандий
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
ТитанТитан
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
ВанадийВанадий
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
ХромХром
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
МарганецМарганец
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
ЖелезоЖелезо
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
КобальтКобальт
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
НикельНикель
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
МедьМедь
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
ЦинкЦинк
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
ГаллийГаллий
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
ГерманийГерманий
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
МышьякМышьяк
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
СеленСелен
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
БромБром
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
КриптонКриптон
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
РубидийРубидий
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
СтронцийСтронций
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
ИттрийИттрий
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
ЦирконийЦирконий
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
НиобийНиобий
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
МолибденМолибден
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
ТехнецийТехнеций
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
РутенийРутений
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
РодийРодий
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
ПалладийПалладий
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
СереброСеребро
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
КадмийКадмий
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
ИндийИндий
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
ОловоОлово
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
СурьмаСурьма
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
ТеллурТеллур
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
ИодИод
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
КсенонКсенон
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
ЦезийЦезий
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
БарийБарий
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
ЛантанЛантан
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
ЦерийЦерий
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
ПразеодимПразеодим
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
НеодимНеодим
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
ПрометийПрометий
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
СамарийСамарий
150,36
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
ЕвропийЕвропий
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
ГадолинийГадолиний
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
ТербийТербий
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
ДиспрозийДиспрозий
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
ГольмийГольмий
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
ЭрбийЭрбий
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
ТулийТулий
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
ИттербийИттербий
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
ЛютецийЛютеций
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
ГафнийГафний
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
ТанталТантал
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
ВольфрамВольфрам
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
РенийРений
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
ОсмийОсмий
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
ИридийИридий
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
ПлатинаПлатина
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
ЗолотоЗолото
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
РтутьРтуть
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
ТаллийТаллий
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
СвинецСвинец
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
ВисмутВисмут
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
ПолонийПолоний
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
АстатАстат
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
РадонРадон
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
ФранцийФранций
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
РадийРадий
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
АктинийАктиний
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
ТорийТорий
232,04
f-элемент
Серый мягкий металл
91
Pa
ПротактинийПротактиний
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
УранУран
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
НептунийНептуний
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
ПлутонийПлутоний
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
АмерицийАмериций
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
КюрийКюрий
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
БерклийБерклий
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
КалифорнийКалифорний
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
ЭйнштейнийЭйнштейний
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
ФермийФермий
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
МенделевийМенделевий
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
НобелийНобелий
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
ЛоуренсийЛоуренсий
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
РезерфордийРезерфордий
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
ДубнийДубний
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
СиборгийСиборгий
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
БорийБорий
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
ХассийХассий
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
МейтнерийМейтнерий
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
ДармштадтийДармштадтий
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Алканы
1
H
ВодородВодород
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
ГелийГелий
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
ЛитийЛитий
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
БериллийБериллий
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
БорБор
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
УглеродУглерод
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
АзотАзот
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
КислородКислород
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
ФторФтор
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
НеонНеон
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
НатрийНатрий
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
МагнийМагний
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
АлюминийАлюминий
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
КремнийКремний
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
ФосфорФосфор
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
СераСера
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
ХлорХлор
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
АргонАргон
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
КалийКалий
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
КальцийКальций
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
СкандийСкандий
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
ТитанТитан
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
ВанадийВанадий
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
ХромХром
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
МарганецМарганец
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
ЖелезоЖелезо
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
КобальтКобальт
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
НикельНикель
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
МедьМедь
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
ЦинкЦинк
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
ГаллийГаллий
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
ГерманийГерманий
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
МышьякМышьяк
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
СеленСелен
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
БромБром
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
КриптонКриптон
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
РубидийРубидий
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
СтронцийСтронций
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
ИттрийИттрий
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
ЦирконийЦирконий
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
НиобийНиобий
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
МолибденМолибден
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
ТехнецийТехнеций
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
РутенийРутений
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
РодийРодий
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
ПалладийПалладий
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
СереброСеребро
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
КадмийКадмий
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
ИндийИндий
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
ОловоОлово
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
СурьмаСурьма
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
ТеллурТеллур
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
ИодИод
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
КсенонКсенон
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
ЦезийЦезий
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
БарийБарий
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
ЛантанЛантан
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
ЦерийЦерий
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
ПразеодимПразеодим
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
НеодимНеодим
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
ПрометийПрометий
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
СамарийСамарий
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
ЕвропийЕвропий
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
ГадолинийГадолиний
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
ТербийТербий
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
ДиспрозийДиспрозий
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
ГольмийГольмий
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
ЭрбийЭрбий
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
ТулийТулий
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
ИттербийИттербий
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
ЛютецийЛютеций
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
ГафнийГафний
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
ТанталТантал
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
ВольфрамВольфрам
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
РенийРений
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
ОсмийОсмий
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
ИридийИридий
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
ПлатинаПлатина
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
ЗолотоЗолото
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
РтутьРтуть
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
ТаллийТаллий
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
СвинецСвинец
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
ВисмутВисмут
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
ПолонийПолоний
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
АстатАстат
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
РадонРадон
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
ФранцийФранций
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
РадийРадий
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
АктинийАктиний
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
ТорийТорий
232,04
f-элемент
Серый мягкий металл
91
Pa
ПротактинийПротактиний
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
УранУран
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
НептунийНептуний
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
ПлутонийПлутоний
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
АмерицийАмериций
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
КюрийКюрий
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
БерклийБерклий
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
КалифорнийКалифорний
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
ЭйнштейнийЭйнштейний
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
ФермийФермий
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
МенделевийМенделевий
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
НобелийНобелий
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
ЛоуренсийЛоуренсий
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
РезерфордийРезерфордий
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
ДубнийДубний
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
СиборгийСиборгий
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
БорийБорий
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
ХассийХассий
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
МейтнерийМейтнерий
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
ДармштадтийДармштадтий
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Что такое природный газ? Определение, факты и цифры
Мы используем природный газ в качестве источника энергии больше, чем любое другое топливо. Будучи самым быстрорастущим и экологически чистым ископаемым топливом, природный газ обеспечивает почти одну треть нашего общего спроса на энергию и почти четверть нашего производства электроэнергии.
Если вы не являетесь отраслевым экспертом, велика вероятность того, что вы не знакомы с основными деталями природного газа. Читайте дальше, чтобы получить подробное представление об ископаемом топливе, от которого мы так сильно зависим.
Что такое природный газ? Если вы посмотрите на Dictionary.com, определение природного газа — это «горючая смесь газообразных углеводородов, которая накапливается в пористых осадочных породах, особенно тех, которые дают нефть, состоящая обычно из более чем 80% метана вместе с небольшими количествами этана, пропан, бутан, азот и иногда гелий».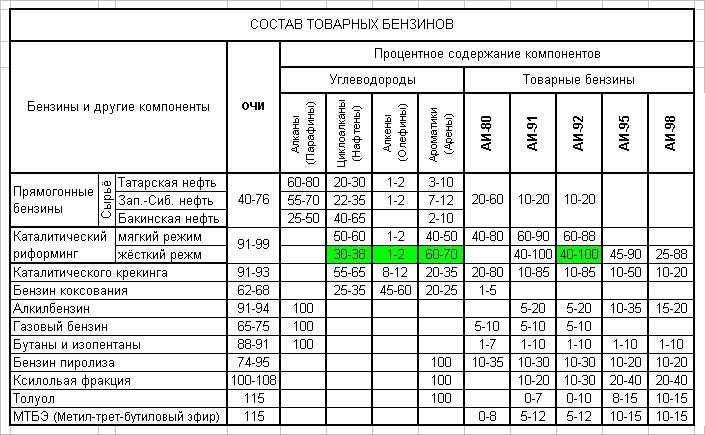
Ого, что? Это много, чтобы переварить. Давайте разобьем всю эту информацию на что-то более простое для понимания. Мы рассмотрим это определение по частям, начиная с четырех природных газов.
Почтовый индекс
Какие основные типы газа составляют природный газ?Вообще говоря, существует четыре природных газа. При смешивании в правильных пропорциях они образуют природный газ. Они известны как четыре природных газа и включают в себя первые четыре алкана — метан, этан, бутан и пропан.
Алкан представляет собой углеводород, в котором одинарные связи соединяют каждый атом. Углеводороды представляют собой химические соединения, состоящие исключительно из атомов углерода и водорода. Метан, этан, бутан и пропан — группы алканов, из которых состоит природный газ — имеют много общего. Все они бесцветные, без запаха и горючие газы. Однако все они имеют разную молекулярную структуру и индивидуальное применение.
Что такое 4 природных газа?источник
1. Метан
Метан Метан, нетоксичный газ, является основным компонентом природного газа, составляющим более 80% смеси. Его химическая формула – CH₄, что делает его простейшей формой молекул углеводорода. Поскольку метан не имеет запаха, к нему добавляют вонючие соединения серы, когда он используется в качестве газа, чтобы мы могли обнаруживать утечки. При сгорании выбросы метана попадают в атмосферу, где они становятся парниковым газом.
2. ЭтанХимическая формула этана C₂H₆ — это единственный двухуглеродный алкан. Этан обычно составляет от 1% до более 6% смеси природного газа, что делает его вторым по величине компонентом ископаемого топлива. Этан в основном используется в качестве нефтехимического сырья для производства этилена.
Нефтехимическое сырье — это материал (сырье), получаемый из нефти (нефтехимии) для производства бесчисленных предметов повседневного обихода. Возможно, прямо сейчас вы даже используете некоторые нефтехимические продукты, в том числе аккумуляторы, одежду, цифровые устройства, запчасти для электромобилей, медицинское оборудование, солнечные батареи, лопасти ветряных турбин, и этот список можно продолжить.
Этан также является парниковым газом, но в гораздо меньших масштабах, чем метан. Забавный факт: Уран, Нептун, Юпитер, Сатурн и спутник Сатурна Титан имеют следы этана в своей атмосфере.
3. Пропан
Химическая формула пропана C₃H₈, что делает его трехуглеродным алканом. Небольшие количества пропана входят в состав смеси природного газа. Однако в основном мы используем его в качестве топлива для грилей, переносных печей, автобусов, такси, вилочных погрузчиков и транспортных средств для отдыха. В сельских районах Соединенных Штатов мы также используем пропан для бытовых приборов, таких как печи, сушилки для белья и водонагреватели. Сгорание пропана не такое чистое, как природный газ, но намного чище бензина.
4. Бутан Хотя мы считаем, что бутан не имеет запаха, он имеет слабый неприятный запах, похожий на запах природного газа или нефти. Бутан легко воспламеняется и легко сжижается. Его химическая формула C₄H₁₀. Бутан составляет небольшую часть смеси природного газа, но он более известен тем, что используется в зажигалках, паяльных лампах и переносных печах, а также в качестве пропеллента для аэрозолей, хладагента и топлива для обогрева.
Бутан составляет небольшую часть смеси природного газа, но он более известен тем, что используется в зажигалках, паяльных лампах и переносных печах, а также в качестве пропеллента для аэрозолей, хладагента и топлива для обогрева.
Что общего между газом и природным газом? Большинство американцев будут использовать их оба каждый день. Оба они также состоят из углеводородов, а поскольку они сделаны из ископаемого топлива, они являются невозобновляемыми ресурсами. Но газ и природный газ — это не одно и то же. У них может быть одно и то же имя, но они очень разные, как ночная летучая мышь и бита, которую мы используем в бейсболе.
Чем отличаются газ и природный газ?Мы рассмотрели многие аспекты сходства газа и природного газа. Теперь давайте взглянем на некоторые характеристики, которые отличают их друг от друга. Вот четыре главных отличия:
- Мы используем природный газ в качестве источника тепла, для приготовления пищи и для производства электроэнергии.
 Газ или бензин (также известный как бензин, потому что это продукт нефти и сырой нефти) используется в основном в качестве моторного топлива для транспортных средств.
Газ или бензин (также известный как бензин, потому что это продукт нефти и сырой нефти) используется в основном в качестве моторного топлива для транспортных средств.
- Природный газ производит почти на 25 % меньше углекислого газа, чем бензин, что делает его более чистым ресурсом.
- В естественном состоянии бензин представляет собой жидкость, тогда как природный газ на самом деле представляет собой газ.
- Хотя оба они созданы из углеводородов, природный газ содержит меньше атомов, чем бензин.
Встречающиеся в природе газы образуются из слоев разлагающихся животных и растительных веществ, обнаруженных под отложениями, землей и морем. Когда погребенное органическое вещество лишается кислорода, оно подвергается термическому распаду под действием сильного тепла и давления под поверхностью Земли. Этот процесс, который происходит в течение миллионов лет, превращает органическое вещество в углеводороды и оставляет его в газообразном состоянии природного газа.
Когда погребенное органическое вещество лишается кислорода, оно подвергается термическому распаду под действием сильного тепла и давления под поверхностью Земли. Этот процесс, который происходит в течение миллионов лет, превращает органическое вещество в углеводороды и оставляет его в газообразном состоянии природного газа.
Существует две категории природного газа, которые мы определяем по происхождению и местоположению газа. Категории делятся на обычные и нетрадиционные.
В чем разница между традиционным и нетрадиционным природным газом?Традиционные месторождения природного газа в основном встречаются вместе с нефтяными пластами и относительно легко доступны. Мы добываем обычный природный газ с помощью оригинального метода бурения (называемого бурением вертикальных скважин) и традиционных методов закачки. Мы вернемся к этому чуть позже.
Доступ к нетрадиционным месторождениям природного газа затруднен. Плохая доступность может быть связана с тем, насколько глубоко под поверхностью Земли они расположены. Вообще говоря, мы находим нетрадиционные залежи природного газа в горных породах, которые мы классифицируем как непроницаемые. Нетрадиционный природный газ обычно добывается из метана угольных пластов, гидратов метана, сланцевого газа и газоносных песчаников.
Вообще говоря, мы находим нетрадиционные залежи природного газа в горных породах, которые мы классифицируем как непроницаемые. Нетрадиционный природный газ обычно добывается из метана угольных пластов, гидратов метана, сланцевого газа и газоносных песчаников.
Почтовый индекс
Как получить природный газ?источник
После полного формирования залежи природного газа оказываются запертыми под землей в горных породах. Мы можем добывать оттуда природный газ. Этот процесс протекает легче всего, если окружающие отложения и горные породы обладают высокой проницаемостью и пористостью.
Что такое проницаемость? То, что может пройти через жидкость или газ, является проницаемым. Чем легче его пройти, тем выше у него проходимость. Проницаемость породы измеряется тем, как поровые пространства взаимосвязаны. Предположим, что природный газ имеет меньшую плотность, чем окружающие его горные породы. В этом случае он будет течь вверх через эти поры, пока не достигнет плотных скальных образований, и там он осядет. Именно здесь сегодня мы находим много месторождений природного газа.
Именно здесь сегодня мы находим много месторождений природного газа.
Когда что-то полно отверстий или крошечных отверстий, мы считаем это пористым. Камни с высокой пористостью имеют много маленьких отверстий или пустого пространства внутри зерен породы. Эти пустоты позволяют жидкости и газу легко поглощаться. Песчаник является примером породы с высокой пористостью, потому что в его зернах есть большое количество свободного пространства или места для хранения.
Как найти месторождения природного газа? Во-первых, мы не можем добывать природный газ из старых горных пород. Сначала нам нужно определить, где разместить месторождения природного газа. Мы можем идентифицировать их с помощью сейсмических испытаний. Сейсмические волны генерируются в районах, где предположительно находятся подземные горные породы, содержащие залежи природного газа, такие как угольные пласты и сланцевые породы.
Геофизики интерпретируют результаты с помощью акустических приемников, называемых геофонами. После того, как месторождение природного газа обнаружено и выбрано для разработки, предпринимается ряд шагов.
Сначала буровая компания встретится с землевладельцем, чтобы обсудить и согласовать их права доступа на поверхность. Затем бригада определит, какой метод бурения потребуется для добычи газа. И они пробурят разведочную скважину, чтобы выяснить, есть ли достаточно большое месторождение природного газа, чтобы оправдать добычу.
Как добывается природный газ?источник
Существует три различных метода добычи природного газа. Метод выбирается в зависимости от геологии района и доступности месторождений природного газа. Три режима добычи включают вертикальное бурение, горизонтальное бурение и гидравлический разрыв пласта, также известный как фрекинг.
Что такое вертикальное бурение? Возвращаясь к обычному природному газу, вертикальное бурение обычно используется только тогда, когда месторождения природного газа находятся непосредственно под поверхностью земли. Скважины бурят прямо в пористых горных породах, которые содержат эти традиционные залежи природного газа. В соответствии со своим названием сверление происходит прямо вниз, в вертикальном направлении.
Скважины бурят прямо в пористых горных породах, которые содержат эти традиционные залежи природного газа. В соответствии со своим названием сверление происходит прямо вниз, в вертикальном направлении.
Вертикальное бурение — первый метод добычи природного газа с поверхности Земли. Фактически до 19В 80-х годах вертикальное бурение было единственным методом, который у нас был. Мы до сих пор используем этот метод, когда можем, поскольку это самый простой и экономичный метод извлечения.
Что такое горизонтальное бурение? Не все месторождения природного газа находятся в легкодоступных местах. Вспомните 1980-е годы, когда появилось горизонтальное бурение. Это изобретение позволило геологам повернуть бурение в другом направлении — буквально. Ранее недоступные месторождения природного газа теперь извлекаются благодаря технологии горизонтального бурения. Здесь гибкая бурильная труба и управляемое буровое долото работают вместе, чтобы перемещаться по плотным горным породам, изгибая вертикальную скважину, а затем буря под горизонтальным углом через залежь природного газа.
источник
Гидравлический разрыв пласта или гидроразрыв пласта — это метод, используемый в Северной Америке для извлечения природного газа, который ранее был недоступен из-за непроницаемых горных пород. Процесс фрекинга включает закачку смеси химикатов, песка и воды в скважину под высоким давлением. Эти высокие давления разрушают горные породы, которые залегают глубоко под поверхностью Земли, отсюда и название гидроразрыва пласта.
В результате разрушения горных пород происходит выброс захваченного природного газа. Когда газ высвобождается, он движется вверх к поверхности Земли, где попадает в скважину. Продолжая подниматься, природный газ затем выходит из устья скважины в трубопровод, где он перекачивается в близлежащие резервуары для хранения.
Какие опасения вызывает гидроразрыв? Хотя это может позволить нам получить доступ к месторождениям природного газа, которые мы иначе не могли бы достичь, многие люди обеспокоены влиянием фрекинга на окружающую среду. Ниже перечислены некоторые из основных причин, почему.
Ниже перечислены некоторые из основных причин, почему.
- Мы должны использовать большое количество воды для гидроразрыва пласта, что не так экологично. Это также усложняет и удорожает процесс, поскольку тяжелую воду часто необходимо транспортировать в отдаленные места.
- Промышленность, занимающаяся ископаемым топливом, не прозрачна в отношении того, какие химические вещества они используют в смеси. Эта непрозрачность вызывает обеспокоенность по поводу возможного загрязнения подземных вод.
- Фрекинг может быть причиной некоторых землетрясений.
После завершения бурения и подачи природного газа в скважину буровое оборудование демонтируется и заменяется устьем. Сборные трубопроводы затем перемещают подачу газа на объекты перерабатывающего завода.
Сборные трубопроводы затем перемещают подачу газа на объекты перерабатывающего завода.
На газовых заводах природный газ перерабатывается с помощью системы фильтрации. Фильтрация удаляет нежелательные газы и другие примеси, такие как кислота, сероводород, ртуть, азот, диоксид серы и водяной пар. Некоторые газовые установки удаляют даже побочные продукты, такие как бутан, этан, пентан и пропан.
Мы можем перерабатывать природный газ в две различные формы: сжатый природный газ (СПГ) и сжиженный природный газ (СПГ). По завершении переработки природный газ считается чистым и готовым к реализации потребителю.
Что такое сжатый природный газ (СПГ)?источник
Сжатый природный газ в основном состоит из метана. Высокое давление, используемое для создания СПГ, уменьшает объем газа до менее 1% от его первоначального объема. В сочетании с воздухом и воспламенением СПГ работает как топливо.
СПГ имеет много преимуществ по сравнению с традиционным бензином. Это проще для двигателей, цены на природный газ значительно ниже, чем цены на бензин, и он легко доступен в Соединенных Штатах. Это также лучше для окружающей среды, чем бензин, поскольку при сгорании КПГ образуется меньше углеводородов, угарного газа и оксидов азота.
Поскольку природный газ не имеет запаха и цвета, компании, работающие с природным газом, добавляют в СПГ одоранты в качестве меры предосторожности. Запах похож на запах тухлых яиц. Газовые компании добавляют к СПГ неприятный запах, чтобы предупредить людей о потенциальных утечках. Если утечка происходит на открытом воздухе, СПГ настолько легкий, что должен просто рассеяться. Но утечка в закрытом помещении может оказаться опасной, так как может вызвать пожар или взрыв, а также привести к серьезным проблемам со здоровьем, включая удушье.
Со сжатым природным газом легче обращаться, чем со сжиженным природным газом. В дополнение к своим преимуществам, СПГ дешевле в производстве и имеет неограниченное время удержания, что означает, что срок его хранения никогда не истечет во время хранения.
источник
Сжиженный природный газ по-прежнему в основном состоит из метана, но он был переработан в жидкое состояние. Для этого необходимо удалить все, что может замерзнуть, например углекислый газ, некоторые углеводороды и водяной пар, а газ охладить до минус 260 градусов по Фаренгейту. Эта экстремальная температура может сделать его трудным и опасным в обращении.
После преобразования объем СПГ примерно в 600 раз меньше исходного газа. Это преобразование делает СПГ идеальной формой природного газа для хранения, особенно потому, что при необходимости его можно легко преобразовать обратно в газообразное состояние. Сжиженный природный газ обладает многими из тех же преимуществ, что и СПГ, кроме того, он негорюч и невзрывоопасен, что делает его значительно более безопасным как для внутренних, так и для международных перевозок.
Однако, в отличие от КПГ, СПГ не содержит одоранта, что затрудняет обнаружение утечек. В автомобилях, работающих на СПГ, установлены электронные датчики метана для обнаружения любых утечек. Утечки СПГ так же опасны, как и утечки СПГ. Они могут вызвать пожар или привести к удушью. Установка детекторов газа может снизить риск и предупредить потребителей о любых потенциальных утечках.
В автомобилях, работающих на СПГ, установлены электронные датчики метана для обнаружения любых утечек. Утечки СПГ так же опасны, как и утечки СПГ. Они могут вызвать пожар или привести к удушью. Установка детекторов газа может снизить риск и предупредить потребителей о любых потенциальных утечках.
Обширная сеть газопроводов используется для безопасной транспортировки природного газа от мест добычи к перерабатывающим заводам и далее к конечному пункту назначения. Отсюда газораспределительные или газовые компании доставляют природный газ предприятиям и домам или безопасно хранят его для последующего использования.
Природный газ растет или падает? Имеет смысл предположить, что газы тяжелее воздуха будут падать на землю, а газы легче воздуха подниматься вверх. И, в принципиальном смысле, это, на самом деле, правильно. Если в вашем доме произойдет значительная утечка природного газа, метан, который имеет меньшую плотность, чем воздух, поднимется к потолку. Итак, чтобы ответить на вопрос выше, природный газ поднимается.
Итак, чтобы ответить на вопрос выше, природный газ поднимается.
Однако плотность газа недостаточно отличается от плотности воздуха, чтобы он не смешивался и не рассеивался относительно быстро. Из-за этого, если утечка слишком маленькая или слишком медленная, она может вообще не подняться. Через некоторое время даже газы, которые поднимаются и скапливаются на потолке, смешиваются с воздухом и равномерно распределяются по всему их пространству.
Безопасность природного газаОчень важно знать, как защитить себя от потенциальных утечек природного газа и что делать, если вы подозреваете их. Если вы используете природный газ в качестве ресурса, подумайте о покупке и установке детектора утечки газа.
Хотя утечки газа случаются редко, они могут произойти в любое время. Следующие признаки могут указывать на утечку внутри или вокруг вашего имущества:
- Шипящий звук или рев
- Мертвые или обесцвеченные растения
- Замерзшие участки на земле в теплых районах
- Запах тухлых яиц или серы
Если вы подозреваете, что у вас может быть утечка природного газа, воздержитесь от любых действий, которые могут вызвать искру или воспламенение. Немедленно покиньте свое имущество и отправляйтесь в более безопасное место. Затем позвоните на горячую линию вашей коммунальной службы по утечке газа, чтобы сообщить о проблеме.
Немедленно покиньте свое имущество и отправляйтесь в более безопасное место. Затем позвоните на горячую линию вашей коммунальной службы по утечке газа, чтобы сообщить о проблеме.
источник
В 2009 году Соединенные Штаты израсходовали около 22,8 трлн кубических футов природного газа. Сегодня мы по-прежнему сильно зависим от этого невозобновляемого ископаемого топлива в удивительно большом количестве способов. Почему? Что ж, хотя мы знаем, что ископаемые виды топлива, такие как природный газ, оказывают негативное воздействие на окружающую среду, мы также пришли к выводу, что их не так-то просто заменить.
Интеграция альтернативных и возобновляемых источников энергии прошла долгий путь. Но такие ресурсы, как ветряные турбины и солнечные панели, в настоящее время не могут производить достаточно энергии для удовлетворения потребительского спроса. Чтобы иметь возможность полностью заменить ископаемое топливо, нам необходимо разработать систему, которая будет соответствовать ценовой доступности, доступности и эффективности систем, основанных на ископаемом топливе, которые мы создали за последние 200 лет. До тех пор мы будем продолжать рассматривать природный газ как основной ресурс, используемый для обогрева домов, обеспечения электричеством и многого другого.
До тех пор мы будем продолжать рассматривать природный газ как основной ресурс, используемый для обогрева домов, обеспечения электричеством и многого другого.
На данный момент мы разделяем способы использования природного газа на пять основных категорий:
- Производство электроэнергии
- Промышленное использование
- Жилое использование
- Коммерческое использование
- Автомобильное топливо
Существует три основных вида использования природного газа. Вот быстрый взгляд на то, что они собой представляют.
1. Электростанции Более одной трети всего природного газа, используемого в Соединенных Штатах, используется для производства электроэнергии. По оценкам Управления энергетической информации США, в 2019 году коммунальные электростанции произвели примерно 4,13 триллиона киловатт-часов (кВтч) электроэнергии в США. . Из них природный газ был наиболее используемым ресурсом на сегодняшний день, обеспечивая более 38% производства электроэнергии.
. Из них природный газ был наиболее используемым ресурсом на сегодняшний день, обеспечивая более 38% производства электроэнергии.
Сразу после электростанций промышленное использование претендует на второе место. Промышленность также составляет примерно одну треть потребления природного газа в Соединенных Штатах. Природный газ используется в качестве источника тепла для обогрева заводов и сжигания отходов. Но он также используется в невероятном количестве производственных целей.
Мы используем природный газ в качестве источника тепла для производства основных продуктов, таких как:
- Кирпичи
- Цемент
- Керамика
- Продукты питания
- Стекло
- Бумага
- Сталь
- Плитка
В производстве природный газ также используется в качестве ингредиента для производства таких продуктов, как:
- Антифриз
- Ткани
- Удобрение
- Фармацевтика
- Пластмассы
Кроме того, мы используем природный газ для производства химикатов, в том числе:
- Уксусная кислота
- Аммиак
- Бутан
- Этан
- Метанол
- Пропан
 Использование в жилых помещениях
Использование в жилых помещениях Более половины домов в США используют природный газ в качестве ресурса. Большинство этих бытовых потребителей используют его в качестве источника тепла для обогревателей помещений и водонагревателей. Природный газ также широко используется для приготовления пищи, стирки, зажигания каминов и питания некоторых осветительных приборов.
Где найти природный газ?источник
Всего в 10 странах находится почти 80% крупнейших мировых запасов природного газа. Саудовская Аравия, Объединенные Арабские Эмираты, Венесуэла, Нигерия и Алжир завершают список с шестого по десятое место соответственно. Вот первая пятерка:
1. Россияисточник
На долю России приходится чуть более 19% мировых запасов ископаемого топлива, а Россия может похвастаться примерно четвертью мировых запасов газа. Более половины запасов природного газа страны находится в Сибири. Ямбург, Уренгой и Медвежье — три крупных заповедника региона. Тем не менее, большая часть запасов газа в России находится в Надым-Пур-Тазовском (НПТ) регионе в верхней части Западной Сибири.
Ямбург, Уренгой и Медвежье — три крупных заповедника региона. Тем не менее, большая часть запасов газа в России находится в Надым-Пур-Тазовском (НПТ) регионе в верхней части Западной Сибири.
Хотя Ирану принадлежат вторые по величине запасы природного газа в мире, большинство из них не разрабатываются. Более 60% запасов природного газа страны находятся на шельфе. Крупнейшее газовое месторождение Ирана — Южный Парс. Другими значительными запасами природного газа в стране являются Северный Парс, Киш и Канган.
3. КатарКатар занимает третье место как крупнейший в мире поставщик СПГ. Запасы природного газа страны покрывают площадь, равную площади самого Катара. Северное месторождение, ведущий источник природного газа в стране, является крупнейшим месторождением попутного газа в мире.
4. Туркменистан Хотя Туркменистан сталкивается с некоторыми трудностями при разработке своих запасов газа, эта центральноазиатская страна является домом для четвертых по величине запасов природного газа в мире. Одним из старейших и крупнейших его газовых месторождений является Даулетабадское месторождение в бассейне Амударьи. Район Южный Иолотен, расположенный в восточном регионе, также содержит значительные запасы природного газа.
Одним из старейших и крупнейших его газовых месторождений является Даулетабадское месторождение в бассейне Амударьи. Район Южный Иолотен, расположенный в восточном регионе, также содержит значительные запасы природного газа.
Большая часть природного газа в США добывается в Техасе и вокруг Мексиканского залива. Ключевые регионы, содержащие природный газ, расположены в сланцевых породах Марцеллус на востоке США и в сланцевых породах Барнетт в Техасе. Сланцевые образования были обнаружены более чем в 30 штатах. В настоящее время США являются крупнейшим потребителем и крупнейшим производителем природного газа в мире.
Как измеряется природный газ? Как правило, мы измеряем природный газ в кубических футах (cf). Однако при расчете количества энергии, вырабатываемой природным газом, единицей измерения являются британские тепловые единицы (БТЕ). Повышение температуры одного фунта воды на один градус по Фаренгейту эквивалентно одной БТЕ. Читая свой счет за газ, вы, вероятно, увидите, что потребление природного газа указано в британских тепловых единицах. Один кубический фут равен 1027 британским тепловым единицам.
Читая свой счет за газ, вы, вероятно, увидите, что потребление природного газа указано в британских тепловых единицах. Один кубический фут равен 1027 британским тепловым единицам.
Мировой спрос на энергию неуклонно растет, а ископаемое топливо, включая природный газ, остается ведущим энергоресурсом. К сожалению, эти ресурсы быстро истощаются из-за резкого увеличения населения и спроса.
Мы так опасно близки к тому, чтобы исчерпать запасы природного газа, поэтому изменение регулирующих мер и усилия по повышению энергоэффективности имеют решающее значение. Если мы не внесем изменений, мы исчерпаем наши запасы природного газа до того, как сегодняшние дети состарятся.
По оценкам Управления энергетической информации США, по состоянию на 1 января 2019 года запасы природного газа составляли всего около 7 177 триллионов кубических футов (триллионов кубических футов).
Предположим, что текущий уровень добычи природного газа остается прежним. В этом случае, по нашим оценкам, запасов природного газа хватит всего на 40–52 года. Поскольку нефти осталось даже меньше, чем газа, мы могли бы быть вынуждены увеличить потребление природного газа, что приблизило бы нас к концу этого временного промежутка.
В этом случае, по нашим оценкам, запасов природного газа хватит всего на 40–52 года. Поскольку нефти осталось даже меньше, чем газа, мы могли бы быть вынуждены увеличить потребление природного газа, что приблизило бы нас к концу этого временного промежутка.
источник
Хотя природный газ считается самым чистым ископаемым топливом, а некоторые считают его формой чистой энергии, многие теперь заявляют, что, хотя он может быть «чище», природный газ на самом деле не является чистой энергией. ресурс. При сгорании природный газ выделяет в атмосферу Земли выбросы углерода, что ученые связывают с экологическими осложнениями. Он известен как причина загрязнения воздуха, хронических проблем со здоровьем, изменения климата, глобального потепления, разрушения среды обитания и стихийных бедствий.
Как я могу помочь с сохранением природного газа? В качестве альтернативного ресурса используется возобновляемый природный газ (RNG), также известный как биометан, который представляет собой топливо, получаемое из отходов полигонов, домашнего скота и других органических материалов путем анаэробного сбраживания.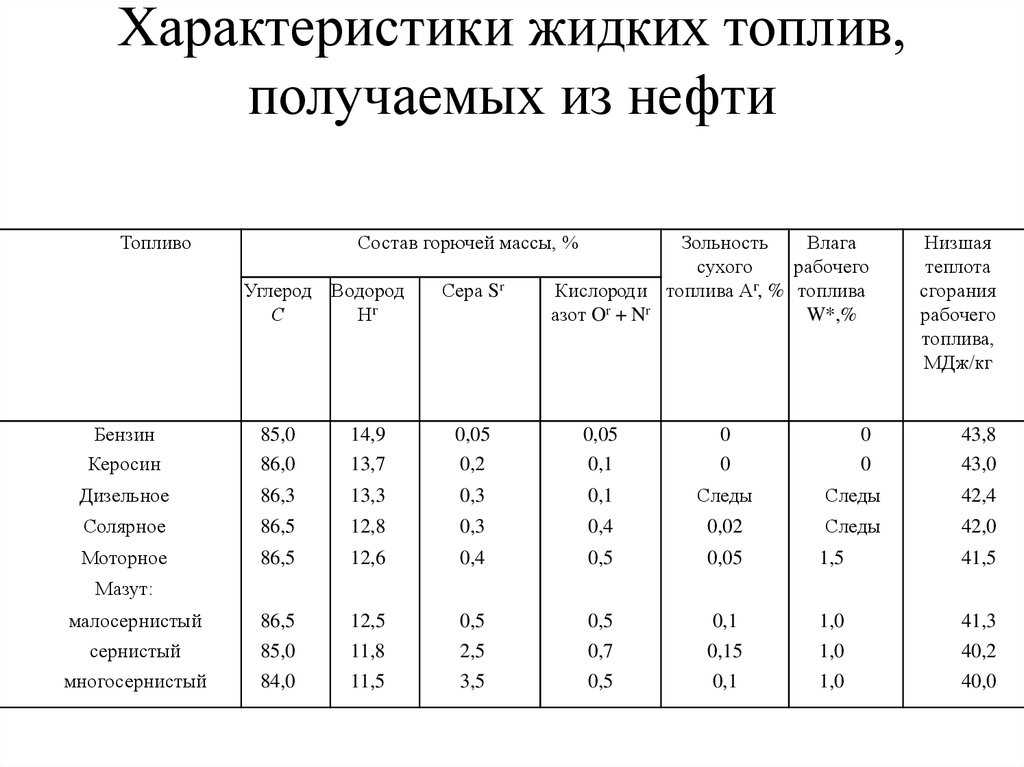 Это не ископаемое топливо, но ГСЧ по химическому составу идентичен обычному природному газу. Это сходство позволяет использовать ту же систему распределения, что и природный газ.
Это не ископаемое топливо, но ГСЧ по химическому составу идентичен обычному природному газу. Это сходство позволяет использовать ту же систему распределения, что и природный газ.
ГСЧ — это лишь один из многих вариантов альтернативной энергии, доступных сегодня. Больше нельзя терять время. Обратитесь к своему поставщику энергии, чтобы узнать о продуктах экологически чистой энергии, которые они могут предложить. Начните свой путь к энергосбережению сегодня.
Предоставлено вам justenergy.com
Все изображения предоставлены по лицензии Adobe Stock.
Избранное изображение:
БЕНЗИН | Камео Химикаты | NOAA
Добавить в MyChemicals Страница для печати
Химический паспорт
Химические идентификаторы | Опасности | Рекомендации по ответу | Физические свойства | Нормативная информация | Альтернативные химические названия
Химические идентификаторы
Что это за информация?
Поля химического идентификатора
включают общие идентификационные номера,
алмаз NFPA
Знаки опасности Министерства транспорта США и общий
описание хим. Информация в CAMEO Chemicals поступает
из множества
источники данных.
Информация в CAMEO Chemicals поступает
из множества
источники данных.
| Номер CAS | Номер ООН/НА | Знак опасности DOT | Береговая охрана США КРИС Код |
|---|---|---|---|
|
|
|
|
| Карманный справочник NIOSH | Международная карта химической безопасности | ||
| Бензин |
| ||
NFPA 704
| Алмаз | Опасность | Значение | Описание |
|---|---|---|---|
| Здоровье | 1 | Может вызывать сильное раздражение. | |
| Воспламеняемость | 3 | Может воспламеняться практически при любых температурах окружающей среды. | |
| нестабильность | 0 | Обычно стабилен даже в условиях пожара. | |
| Специальный |
(NFPA, 2010)
Общее описание
Прозрачная летучая жидкость от бесцветного до янтарного цвета с нефтяным запахом. Температура вспышки ниже 0°F. Менее плотный, чем вода, нерастворим в воде. Поэтому плавает на воде. Пары тяжелее воздуха. Утечки паров могут попасть к источнику воспламенения, а затем вспыхнуть обратно к источнику.
Опасности
Что это за информация?
Опасные поля
включают
специальные предупреждения об опасности
воздух и вода
реакции, пожароопасность, опасность для здоровья, профиль реактивности и
подробности о
задания реактивных групп
а также
потенциально несовместимые абсорбенты. Информация в CAMEO Chemicals поступает из различных источников.
источники данных.
Информация в CAMEO Chemicals поступает из различных источников.
источники данных.
Предупреждения о реактивности
- Легковоспламеняющиеся
Реакции с воздухом и водой
Легко воспламеняется.
Пожароопасность
Особые опасности продуктов горения: Нет
Поведение в огне: Пары тяжелее воздуха и могут распространяться на значительное расстояние до источника воспламенения и возвращаться вспышкой. (Геологическая служба США, 1999 г.)
Опасность для здоровья
Раздражение слизистых оболочек и возбуждение с последующим угнетением центральной нервной системы. Вдыхание паров может также вызвать головокружение, головную боль и нарушение координации или, в более тяжелых случаях, анестезию, кому и остановку дыхания. Если жидкость попадет в легкие, это вызовет сильное раздражение, кашель, позывы на рвоту, отек легких, а позднее — признаки бронхопневмонии и пневмонита. Глотание может вызвать нерегулярное сердцебиение. (USCG, 1999)
(USCG, 1999)
Профиль реактивности
БЕНЗИН может быть несовместим с сильными окислителями, такими как азотная кислота, пероксиды и перхлораты. Может произойти обугливание с последующим воспламенением непрореагировавшего углеводорода и других близлежащих горючих веществ. В остальных настройках в основном не реагирует. Не подвержен влиянию водных растворов кислот, щелочей, большинства окислителей и большинства восстановителей. При достаточном нагревании или при воспламенении в присутствии воздуха, кислорода или сильных окислителей сгорает экзотермически с образованием углекислого газа и воды.
Принадлежит к следующей реакционной группе(ам):
- Углеводороды, алифатические насыщенные
Потенциально несовместимые абсорбенты
Информация отсутствует.
Рекомендации по ответу
Что это за информация?
Поля рекомендации ответа
включают в себя расстояния изоляции и эвакуации, а также рекомендации по
пожаротушение, пожарное реагирование, защитная одежда и первая помощь. информация в CAMEO Chemicals поступает из различных
источники данных.
информация в CAMEO Chemicals поступает из различных
источники данных.
Изоляция и эвакуация
Выдержка из Руководства ERG 128 [Горючие жидкости (не смешивающиеся с водой)]:
НЕМЕДЛЕННЫЕ МЕРЫ ПРЕДОСТОРОЖНОСТИ: Изолируйте место разлива или утечки на расстоянии не менее 50 метров (150 футов) во всех направлениях.
КРУПНЫЙ РАЗЛИВ: Рассмотрите первоначальную эвакуацию по ветру на расстояние не менее 300 метров (1000 футов).
ПОЖАР: Если цистерна, железнодорожная цистерна или автоцистерна вовлечены в пожар, ИЗОЛИРОВАТЬ на расстоянии 800 метров (1/2 мили) во всех направлениях; также рассмотрите первоначальную эвакуацию на 800 метров (1/2 мили) во всех направлениях. (ЭРГ, 2020)
Пожаротушение
Выдержка из Руководства ERG 128 [Горючие жидкости (не смешивающиеся с водой)]:
ВНИМАНИЕ: Большинство этих продуктов имеют очень низкую температуру воспламенения. Использование распыления воды при тушении пожара может быть неэффективным.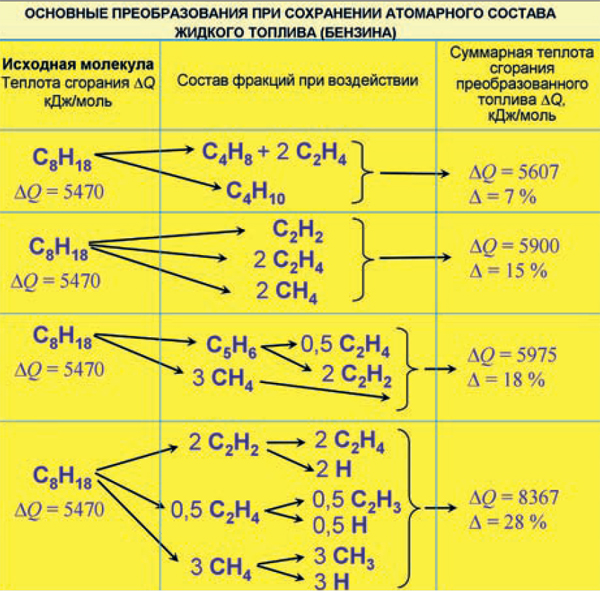 ВНИМАНИЕ: Для смесей, содержащих спирт или полярный растворитель, спиртостойкая пена может оказаться более эффективной.
ВНИМАНИЕ: Для смесей, содержащих спирт или полярный растворитель, спиртостойкая пена может оказаться более эффективной.
НЕБОЛЬШОЙ ПОЖАР: Сухие химикаты, CO2, распыление воды или обычная пена.
БОЛЬШОЙ ПОЖАР: Распыление воды, туман или обычная пена. Избегайте направления прямых или сплошных струй непосредственно на продукт. Если это можно сделать безопасно, уберите неповрежденные контейнеры из зоны вокруг огня.
ПОЖАР, ВКЛЮЧАЮЩИЙ РЕЗЕРВУАРЫ ИЛИ АВТОМОБИЛЬНЫЕ/ТРЕЙЛЕРНЫЕ НАГРУЗКИ: Тушить огонь с максимального расстояния или использовать беспилотные устройства основного потока или контрольные насадки. Охладите контейнеры заливающим количеством воды до тех пор, пока огонь не погаснет. Для нефтяной сырой нефти не распыляйте воду непосредственно в поврежденную цистерну. Это может привести к опасному закипанию. Немедленно отозвать в случае усиления звука от вентиляционных предохранительных устройств или обесцвечивания бака. ВСЕГДА держитесь подальше от танков, охваченных огнем. При массовом возгорании используйте беспилотные устройства управления потоком или стволы-мониторы; если это невозможно, отойдите от зоны и дайте огню гореть. (ЭРГ, 2020)
При массовом возгорании используйте беспилотные устройства управления потоком или стволы-мониторы; если это невозможно, отойдите от зоны и дайте огню гореть. (ЭРГ, 2020)
Непожарное реагирование
Выдержка из Руководства ERG 128 [Горючие жидкости (не смешивающиеся с водой)]:
УСТРАНИТЕ все источники воспламенения (не курить, факелы, искры или пламя) в непосредственной близости. Все оборудование, используемое при работе с продуктом, должно быть заземлено. Не прикасайтесь к рассыпанному материалу и не ходите по нему. Остановите утечку, если вы можете сделать это без риска. Не допускать попадания в водные пути, канализацию, подвалы или замкнутые пространства. Для уменьшения паров можно использовать пароподавляющую пену. Впитать или засыпать сухой землей, песком или другим негорючим материалом и переложить в контейнеры. Используйте чистые, искробезопасные инструменты для сбора абсорбированного материала.
БОЛЬШОЙ РАЗЛИВ: Оборудуйте дамбу далеко перед разливом жидкости для последующего удаления. Распыление воды может уменьшить испарение, но не может предотвратить возгорание в закрытых помещениях. (ЭРГ, 2020)
Распыление воды может уменьшить испарение, но не может предотвратить возгорание в закрытых помещениях. (ЭРГ, 2020)
Защитная одежда
Выдержка из Карманного справочника NIOSH по бензину:
Кожа: ПРЕДОТВРАТИТЬ КОНТАКТ С КОЖЕЙ — Носите соответствующую защитную одежду для предотвращения контакта с кожей.
Глаза: ПРЕДОТВРАЩАЙТЕ ПОПАДАНИЕ В ГЛАЗА — Носите соответствующую защиту для глаз, чтобы предотвратить попадание в глаза.
Мытье кожи: ПРИ ЗАГРЯЗНЕНИИ — Рабочий должен немедленно вымыть кожу, когда она становится загрязненной.
Снять: ПРИ ВЛАЖНОСТИ (ЛЕГКОВОСПЛАМЕНЯЮЩЕЙСЯ) — Рабочую одежду, которая намокла, следует немедленно снять из-за ее опасности воспламенения (например, для жидкостей с температурой вспышки <100°F).
Смена: Нет рекомендаций, указывающих на необходимость смены работником одежды после рабочей смены.
Предоставьте:
• ПРОМЫВКИ ДЛЯ ГЛАЗ. В зонах, где существует вероятность того, что рабочие могут подвергнуться воздействию этих веществ, должны быть предусмотрены фонтанчики для промывки глаз; это не зависит от рекомендации по ношению защиты глаз.
• БЫСТРОЕ ОБМАЧИВАНИЕ. В непосредственной близости от рабочей зоны должны быть предусмотрены средства для быстрого обливания тела в экстренных случаях, когда существует вероятность воздействия. [Примечание: предполагается, что эти сооружения обеспечивают достаточное количество или поток воды для быстрого удаления вещества с любых участков тела, которые могут подвергаться воздействию. Фактическое определение того, что представляет собой адекватное оборудование для быстрого смачивания, зависит от конкретных обстоятельств. В некоторых случаях должен быть легко доступен проточный душ, тогда как в других случаях адекватным может считаться наличие воды из раковины или шланга.] (NIOSH, 2022)
Ткани DuPont Tychem® Suit Fabrics
Обозначение ткани, сведения об испытаниях и предостережение от DuPont
Tychem® Fabric Legend
| QS = Tychem 2000 SFR |
| Контроль качества = Tychem 2000 |
| SL = Tychem 4000 |
| C3 = Тайхем 5000 |
| TF = Tychem 6000 |
| TP = Tychem 6000 FR |
| RC = Tychem RESPONDER® CSM |
| ТК = Тайхем 10000 |
| RF = Tychem 10000 FR |
Детали тестирования
Данные о проницаемости ткани были получены для DuPont третьей стороной
лаборатория. Данные о проникновении промышленных химикатов получены в
ASTM F739. Нормализованное время прорыва (время, в которое
скорость проникновения превышает 0,1 мкг/см2/мин) сообщается в минутах. Все
химические вещества были испытаны при температуре приблизительно от 20°C до 27°C, если
в противном случае указано. Все химические вещества были протестированы в концентрации
больше 95%, если не указано иное.
Боевые отравляющие вещества (люизит, зарин, зоман, сернистый иприт, табун
и VX Nerve Agent) были протестированы при температуре 22°C и относительной влажности 50%.
в соответствии с военным стандартом MIL-STD-282. «Время прорыва» для химической
боевых отравляющих веществ определяется как время, когда кумулятивная масса,
проникновение через ткань превышает предел MIL-STD-282 [либо
1,25 или 4,0 мкг/см2].
Данные о проникновении промышленных химикатов получены в
ASTM F739. Нормализованное время прорыва (время, в которое
скорость проникновения превышает 0,1 мкг/см2/мин) сообщается в минутах. Все
химические вещества были испытаны при температуре приблизительно от 20°C до 27°C, если
в противном случае указано. Все химические вещества были протестированы в концентрации
больше 95%, если не указано иное.
Боевые отравляющие вещества (люизит, зарин, зоман, сернистый иприт, табун
и VX Nerve Agent) были протестированы при температуре 22°C и относительной влажности 50%.
в соответствии с военным стандартом MIL-STD-282. «Время прорыва» для химической
боевых отравляющих веществ определяется как время, когда кумулятивная масса,
проникновение через ткань превышает предел MIL-STD-282 [либо
1,25 или 4,0 мкг/см2].
Предупреждение DuPont
Эта информация основана на технических данных, которые, по мнению DuPont,
быть достоверным на дату выпуска.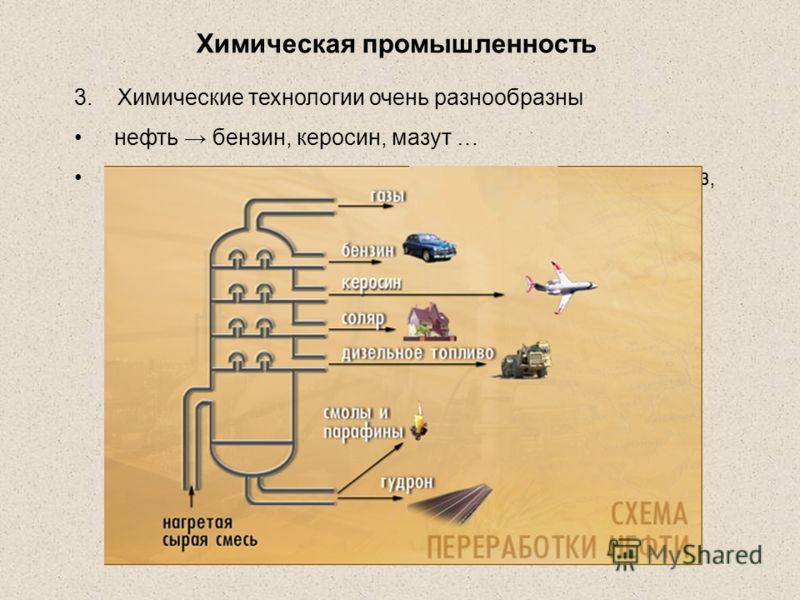 подлежит доработке как доп.
приобретаются знания и опыт. Информация отражает
лабораторное исследование тканей, некомплектных швейных изделий, под
контролируемые условия. Предназначен для информационного использования лицами
наличие технических навыков для оценки в соответствии с их конкретным конечным использованием
условиях, на свое усмотрение и риск. это пользователь
ответственность за определение уровня токсичности и надлежащее
необходимы средства индивидуальной защиты. Любой, кто собирается использовать это
Информация должна сначала подтвердить, что выбранная одежда подходит
для предполагаемого использования. Во многих случаях швы и застежки имеют более короткую длину.
время прорыва и более высокие скорости проникновения, чем у ткани. Если
ткань разорвана, потерта или проколота, или если швы или застежки выходят из строя,
или если прикрепленные перчатки, козырьки и т. д. повреждены, конечный пользователь должен
прекратите использование одежды, чтобы избежать потенциального воздействия химических веществ.
подлежит доработке как доп.
приобретаются знания и опыт. Информация отражает
лабораторное исследование тканей, некомплектных швейных изделий, под
контролируемые условия. Предназначен для информационного использования лицами
наличие технических навыков для оценки в соответствии с их конкретным конечным использованием
условиях, на свое усмотрение и риск. это пользователь
ответственность за определение уровня токсичности и надлежащее
необходимы средства индивидуальной защиты. Любой, кто собирается использовать это
Информация должна сначала подтвердить, что выбранная одежда подходит
для предполагаемого использования. Во многих случаях швы и застежки имеют более короткую длину.
время прорыва и более высокие скорости проникновения, чем у ткани. Если
ткань разорвана, потерта или проколота, или если швы или застежки выходят из строя,
или если прикрепленные перчатки, козырьки и т. д. повреждены, конечный пользователь должен
прекратите использование одежды, чтобы избежать потенциального воздействия химических веществ. Поскольку условия использования находятся вне нашего контроля, DuPont не делает никаких
гарантии, явные или подразумеваемые, включая, помимо прочего,
гарантии товарной пригодности или пригодности для конкретного использования и
не несет никакой ответственности в связи с любым использованием этой информации.
Эта информация не предназначена для использования в качестве лицензии на работу или
рекомендацию о нарушении любого патента, товарного знака или технического
информацию DuPont или других лиц, касающуюся любого материала или его использования.
Поскольку условия использования находятся вне нашего контроля, DuPont не делает никаких
гарантии, явные или подразумеваемые, включая, помимо прочего,
гарантии товарной пригодности или пригодности для конкретного использования и
не несет никакой ответственности в связи с любым использованием этой информации.
Эта информация не предназначена для использования в качестве лицензии на работу или
рекомендацию о нарушении любого патента, товарного знака или технического
информацию DuPont или других лиц, касающуюся любого материала или его использования.
| Химическая промышленность | Номер CAS | Состояние | КС | КК | СЛ | С3 | ТФ | ТП | РЦ | ТК | РФ |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Бензин неэтилированный | 86290-81-5 | Жидкость | имм | >480 | >480 | >480 | >480 | >480 | >480 |
> указывает больше чем.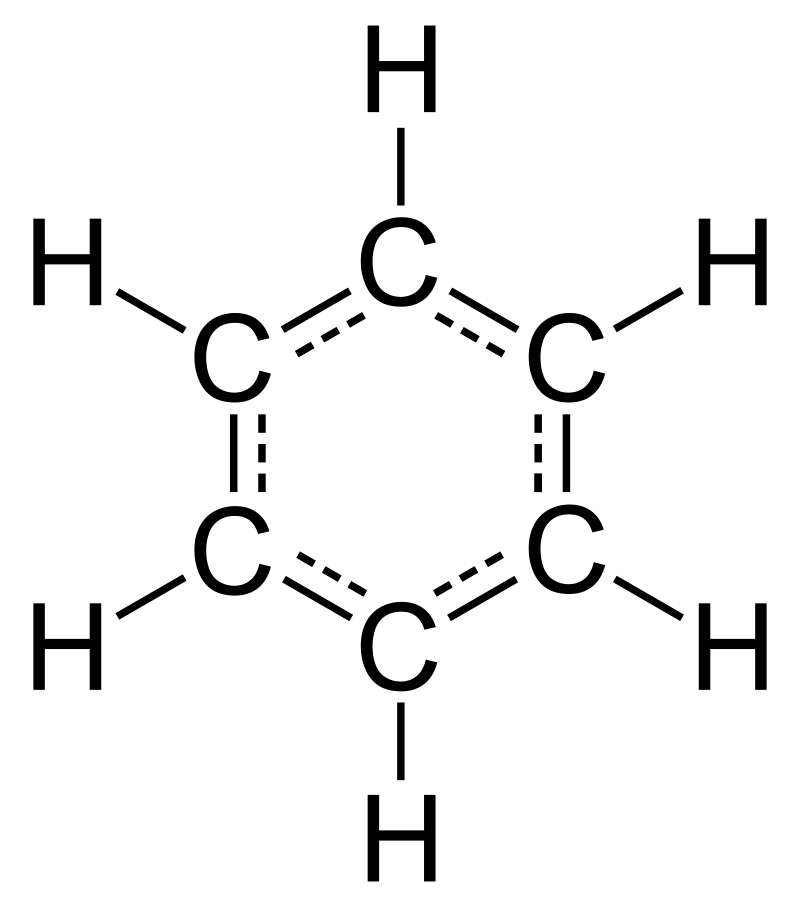
«imm» указывает на немедленное; с нормализованным временем прорыва 10 минут или менее.
Специальное предупреждение от DuPont: ткани Tychem® и Tyvek® не должны используется вблизи тепла, пламени, искр или в потенциально легковоспламеняющихся или взрывоопасные среды. Только…
Подробнее…
…Tychem® ThermoPro, Tychem® Reflector® и Tychem® TK моделей 600T/601T
(с алюминированным верхним костюмом) одежда разработана и испытана, чтобы помочь
уменьшить ожоги при спасении от внезапного пожара. Пользователи Tychem®
Модели ThermoPro, Tychem® Reflector® и Tychem® TK 600T/601T (с
алюминизированный верхний костюм) предметы одежды не должны заведомо попадать во взрывчатое вещество
Окружающая среда. Одежда Tychem® с прикрепленными носками должна носиться внутри.
защитную верхнюю обувь и не подходят в качестве верхней обуви. Эти
прикрепленные носки не обладают достаточной прочностью или сопротивлением скольжению, чтобы быть
носится как наружное покрытие стопы.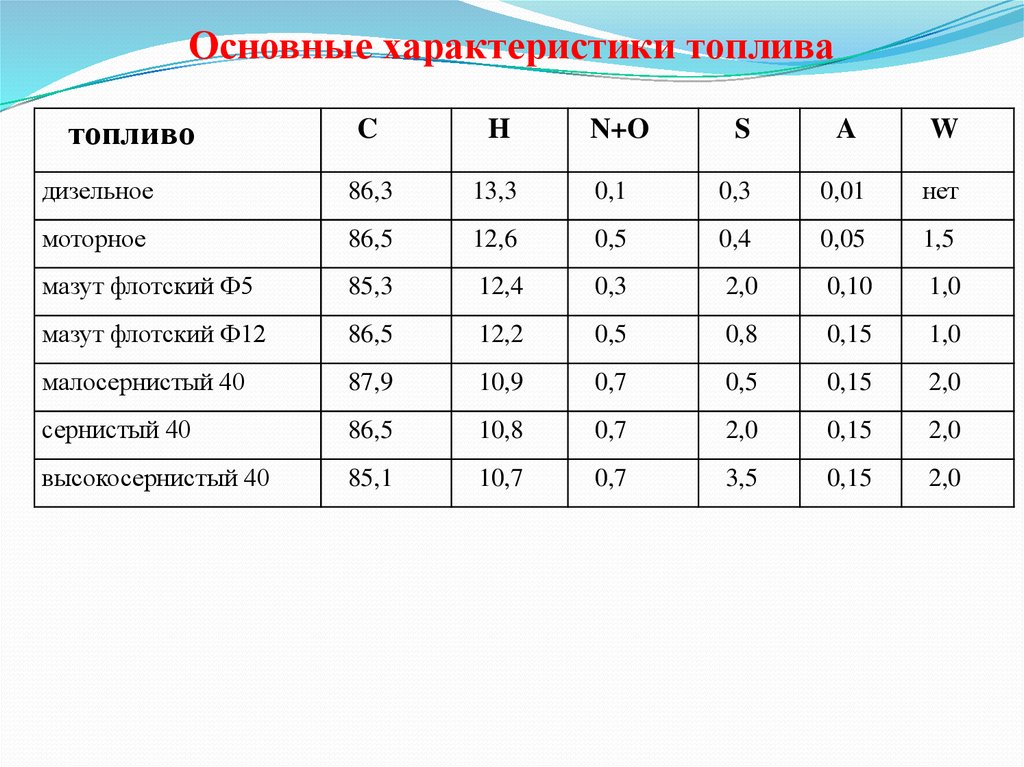
(Дюпон, 2022)
Первая помощь
Выдержка из Карманного справочника NIOSH по бензину:
Глаза: НЕМЕДЛЕННО ПРОРОШЬТЕ — Если это химическое вещество попало в глаза, немедленно промойте (промойте) глаза большим количеством воды, время от времени поднимая нижнее и верхнее веко. Немедленно обратитесь за медицинской помощью.
Кожа: НЕМЕДЛЕННО ПРОМЫТЬ МЫЛОМ — Если это химическое вещество попало на кожу, немедленно промойте загрязненную кожу водой с мылом. Если это химическое вещество проникло через одежду, немедленно снимите одежду и промойте кожу водой. Если после мытья раздражение сохраняется, обратитесь за медицинской помощью.
Дыхание: ПОДДЕРЖКА ДЫХАНИЯ — Если человек вдыхает большое количество этого химического вещества, немедленно выведите пострадавшего на свежий воздух. Если дыхание остановилось, сделайте искусственное дыхание. Держите пострадавшего в тепле и в покое. Как можно скорее обратитесь за медицинской помощью.
Проглатывание: НЕМЕДЛЕННО ОБРАТИТЕ ВНИМАНИЕ — Если это химическое вещество было проглочено, немедленно обратитесь за медицинской помощью. (НИОСХ, 2022 г.)
Физические свойства
Что это за информация?
Поля физических свойств включают в себя такие свойства, как давление пара и температура кипения, а также пределы взрываемости и пороги токсического воздействия Информация в CAMEO Chemicals поступает из различных источников. источники данных.
Химическая формула: данные недоступны
Температура вспышки: -36°F (USCG, 1999)
Нижний предел взрываемости (НПВ): 1,4 % (USCG, 1999)
Верхний предел взрываемости (ВПВ): 7,4 % (USCG, 1999)
Температура самовоспламенения: 853°F (USCG, 1999)
Температура плавления: данные отсутствуют
Давление паров: 382,58 мм рт.ст. (USCG, 1999)
Плотность паров (относительно воздуха): данные недоступны
Удельный вес: 0,7321 при 68°F (USCG, 1999)
Точка кипения:
от 140 до 390°F
при 760 мм рт. ст.
(USCG, 1999)
ст.
(USCG, 1999)
Молекулярный вес: 110 (приблизительно) (NIOSH, 2022)
Растворимость в воде: Нерастворимый (NIOSH, 2022)
Энергия/потенциал ионизации: данные отсутствуют
IDLH: Потенциальный профессиональный канцероген. (НИОСХ, 2022 г.)
AEGL (рекомендательные уровни острого воздействия)
Информация об AEGL отсутствует.ERPG (Руководство по планированию аварийного реагирования)
| Химическое вещество | ЭРПГ-1 | ЭРПГ-2 | ЭРПГ-3 | |
|---|---|---|---|---|
| Бензин (86290-81-5) | 200 частей на миллион | 1000 частей на миллион | 4000 частей на миллион | НПВ = 14000 частей на миллион |
указывает, что запах должен ощущаться вблизи ERPG-1.
указывает, что значение составляет 10-49% НПВ.
(AIHA, 2020)
PAC (критерии защитных действий)
| Химические вещества | ПАК-1 | ПАК-2 | ПАК-3 | |
|---|---|---|---|---|
| Бензин (86290-81-5) | 200 частей на миллион | 1000 частей на миллион | 4000 частей на миллион | НПВ = 13000 частей на миллион |
указывает, что значение составляет 10-49% НПВ.
(DOE, 2018)
Нормативная информация
Что это за информация?
Поля нормативной информации
включить информацию из
Сводный список III Агентства по охране окружающей среды США
списки,
Химический завод Агентства кибербезопасности и безопасности инфраструктуры США
антитеррористические стандарты,
и Управление по охране труда и здоровья США
Перечень стандартов по управлению безопасностью технологического процесса при работе с особо опасными химическими веществами
(подробнее об этих
источники данных).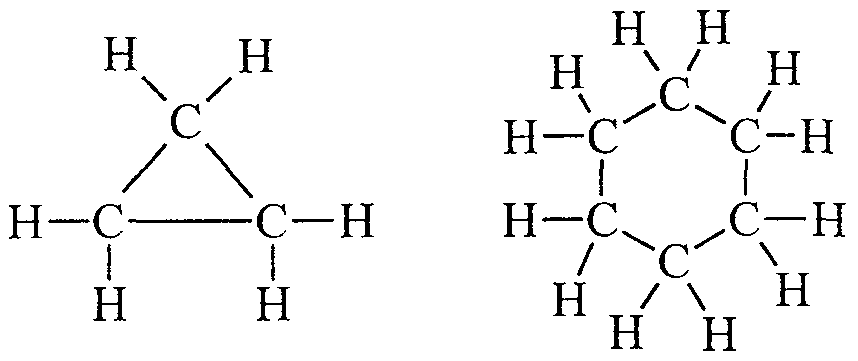
Сводный перечень списков EPA
Отсутствует нормативная информация.
Антитеррористические стандарты CISA Chemical Facility (CFATS)
Отсутствует нормативная информация.
Перечень стандартов OSHA по управлению безопасностью процессов (PSM)
Отсутствует нормативная информация.
Альтернативные химические названия
Что это за информация?
В этом разделе приводится список альтернативных названий этого химического вещества, включая торговые названия и синонимы.
- А 76
- А 76 (ТОПЛИВО)
- АИ 3
- АИ 93 (ТОПЛИВО)
- АКВАЗИН
- БЕНЗИН (МОТОРНОЕ ТОПЛИВО)
- ТОПЛИВО, БЕНЗИН
- БЕНЗИН
- БЕНЗИН, СИНТЕТИЧЕСКИЙ
- БЕНЗИНЫ: АВТОМОБИЛЬНЫЕ (<4,23 Г СВИНЦА/ГАЛЛ)
- ГЕРБИЦИД ES
- ИНДОЛЕН
- МОТОРНОЕ ТОПЛИВО
- МОТОРНЫЙ ДУХ
- МОТОРНЫЕ ДУХИ
- КОНДЕНСАТЫ ПРИРОДНОГО ГАЗА, БЕНЗИН
- ПРИРОДНЫЙ БЕНЗИН
- НЕФРАС С 150/200
- НЕФРАС С 50/170
- БЕНЗИН
- БЕНЗИН, ПРИРОДНЫЙ
- БЕНЗИН, СИНТЕТИКА
- СИНТФОПЛИВ
- СИНТЕТИЧЕСКИЙ БЕНЗИН
1 галлон бензина · BlueSkyModel
Бензин
Подобно топливу для реактивных двигателей, бензин представляет собой смесь углеводородов, точный состав которой зависит от сырой нефти, из которой он был получен. Кроме того, большинство бензинов содержат такие присадки, как антиоксиданты, ингибиторы статического электричества, ингибиторы коррозии и т.д.
Кроме того, большинство бензинов содержат такие присадки, как антиоксиданты, ингибиторы статического электричества, ингибиторы коррозии и т.д.
То, что мы покупаем на заправке, представляет собой смесь сотен соединений. Однако, учитывая температуру кипения, используемую для перегонки бензина (120-400 градусов по Фаренгейту), мы знаем, что его углеводороды имеют от 6 до 12 атомов углерода. Большинство людей считают октановое число — C 8 H 18 — приемлемым средним значением 1 . Октан имеет плотность 0,703 г / мл или 2661,14 г / галлонов .
- Крис Кайзер, Mad Science Network, «RE: Химическая формула обычного бензина». http://www.madsci.org/posts/archives/2001-04/987004809.Ch.r.html (посещено в марте 2013 г.).
Горение
В бензиновом двигателе смесь бензина и воздуха сгорает для привода поршней. Поршни вращают приводной вал, а приводной вал вращает колеса. В реакции горения бензин (он же октан, C 8 H 18 ) соединяется с кислородом воздуха ( O 2 ) с образованием диоксида углерода ( CO 2 ) и воды ( H 5 099 ):
Поршни вращают приводной вал, а приводной вал вращает колеса. В реакции горения бензин (он же октан, C 8 H 18 ) соединяется с кислородом воздуха ( O 2 ) с образованием диоксида углерода ( CO 2 ) и воды ( H 5 099 ):
C 8 H 18 + O 2 -> CO 2 + H 8 59 (1 09095)Это та же самая реакция горения, которая происходит в нашем организме для получения энергии из пищи. Конечно, другие элементы в воздухе, такие как азот и углекислый газ, сжигаются в двигателе так же, как и кислород. Эти другие элементы будут создавать другие молекулы, такие как нитраты и озон, но мы будем игнорировать их в наших расчетах.
Конечно, нам нужно сбалансировать уравнение, чтобы одинаковое количество элементов входило и выходило из нашей реакции:
2 C 8 H 18 + 25 O 2 -> 16 CO 2 + 18 H 2 0 (2)Мы видим, что на каждые две молекулы октана, вступающие в нашу реакцию горения, образуется 16 молекул углекислого газа (или, уменьшая дробь, одна молекула октана дает восемь молекул углекислого газа).
Однако молекулы октана и молекулы углекислого газа не имеют одинаковой массы, и масса должна сохраняться.
Чтобы определить, сколько граммов углекислого газа произведено, нам нужно рассчитать молекулярную массу углекислого газа, молекулярную массу октана и соотношение между ними:
(1 м * 12,011 а.е.м. ) + (2 м * 15,999 а.е.м. ) = 44,009 а.е. (3)(8 м * 12,011 а.е.м. ) + (18 м * 1,008 а.е.м. ) = 114,232 а.е.м. (4)44,009 а.е.м. / 114,232 а.е.м. = 0,385 (5)Мы знаем, что на каждую молекулу октана, которая вступает в нашу реакцию, образуется восемь молекул двуокиси углерода (уравнение 2), и мы знаем, что одна молекула двуокиси углерода составляет 38,5% массы молекулы октана (уравнение 5).
В результате мы можем посчитать, сколько граммов углекислого газа получается из одного грамма октана (он же бензин):
8 * 0,385 = 3,080 г CO 2 / г C 8 H 18 (6)Зная плотность октана (0,703 г / мл или 2661,144 г / галлонов ), мы можем рассчитать количество фунтов углекислого газа, вырабатываемого одним галлоном октана (он же бензин):
2661.144 г C 8 H 18 / галлонов * 3,080 г CO 2 / g C 8 H 18 * 1 lb /453.592 g = 18.07 lbs CO 2 / gal (7)
Вывод
Вот оно! Насколько нам известно, в среднем один галлон бензина производит 18,07 фунта углекислого газа. Если ваш автомобиль расходует 20 миль на галлон, а вы проезжаете 10 000 миль в год, вы будете производить 4,5 коротких тонны углекислого газа.
Внимание! В 2012 году Управление энергетической информации США оценило, что один галлон газа производит 19,6 фунтов углекислого газа. Несоответствие, вероятно, связано с тем, что они тестировали настоящий бензин со всеми его присадками и другими соединениями, а не только октановое число. Кроме того, они, вероятно, учитывали влияние других газов в воздухе, таких как азот, углекислый газ и т. д.
Не забудьте! В реакции участвуют другие молекулы. Мы не говорим, что вы получаете 18,1 фунта углерода из 5,7 фунта углерода (около веса галлона газа).

