Как повысить плотность электролита в аккумуляторе своими руками
Аккумуляторная батарея в автомобиле – вещь, которая полежит замене в любом случае через некоторое время. Иногда причина в посыпавшихся пластинах, но чаще всего падает плотность электролита. С необслуживаемыми аккумуляторами ситуация ясна, их можно только выбросить. А вот там, где есть доступ к банкам, за продление жизни батареи еще можно побороться. Разберемся, как именно это сделать.
Почему падает плотность электролита
Основная рабочая жидкость в большинстве аккумуляторов для автомобилей – серная кислота. Точнее, ее раствор примерно в 35%. Без этой жидкости вся батарея – просто набор пластика и свинца, кислота же служит катализатором электрохимического процесса. Полости для нее называются банками, а именно для того, чтобы отслеживать уровень раствора, в обслуживаемых аккумуляторах сделаны закручивающиеся пробки. Это не только преимущество, но и слабая точка одновременно: через оставшиеся щели выкипает электролит. В необслуживаемых аналогах вероятность такого намного меньше.
В необслуживаемых аналогах вероятность такого намного меньше.
Плотность электролита как раз является показателем заряженности АКБ. Чем она выше, тем выше уровень заряда в батарее. Но часто бывает так, что при выкипании электролита водители просто доливают в батарею дистиллированную воду и продолжают ездить дальше. Сколько в полученном растворе осталось кислоты – никто не определит. И после нескольких операций подобного толка номинальная плотность электролита падает до уровня, когда зарядить его уже не получится.
Как проверить плотность электролита
Для того, чтобы узнать уровень заряда в аккумуляторе, достаточно воспользоваться мультиметром. У полностью заряженного аккумулятора напряжение примерно 14,5 Вольт, может, немного выше. Исходя из этого, после зарядки можно перемерить уровень тока на клеммах. Если после стандартного времени заряда (скажем, в 8 часов) напряжение не больше 13,5 Вольт, то есть меньше половины, то можно смело говорить о том, что и плотность электролита примерно в 2 раза ниже требуемой.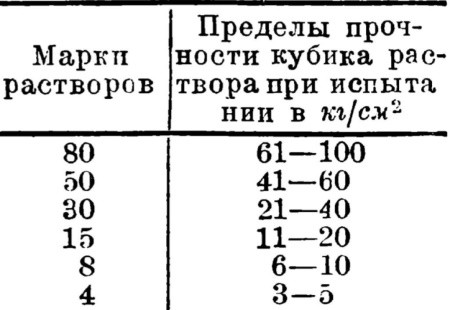
Но этот метод очень неточный и ориентироваться в первую очередь на него не стоит. Куда эффективнее себя покажет ареометр, который измеряет заряд как раз по плотности. Он состоит из спринцовки, колбы и шкалы с пробкой. Набирается электролит, по тому, насколько сильно погружается шкала, определяется плотность.
- Важно! Не забываем о том, что основа электролита – серная кислота, и даже в таком растворе она все еще обладает очень сильными разъедающими свойствами. Потому не забываем об аккуратности, защите для рук, лица и не проводим проверку над тонкими проводами и металлом. Если упадет капля – останется след на всем.
В норме минимально приемлемое значение плотности электролита – около 1,25…1,3 г/см3. Промерять нужно каждую банку, разброс значения должен быть не больше 0,1. Меньшая плотность в любой банке будет означать потерю емкости всей АКБ.
Заливка свежего электролита
Он продается во многих автомобильных магазинах и стоит не очень дорого. Если плотность упала не сильно ниже минимального значения, то электролит можно просто долить, добавив свежего к тому, что имеется в банке, до нужного уровня.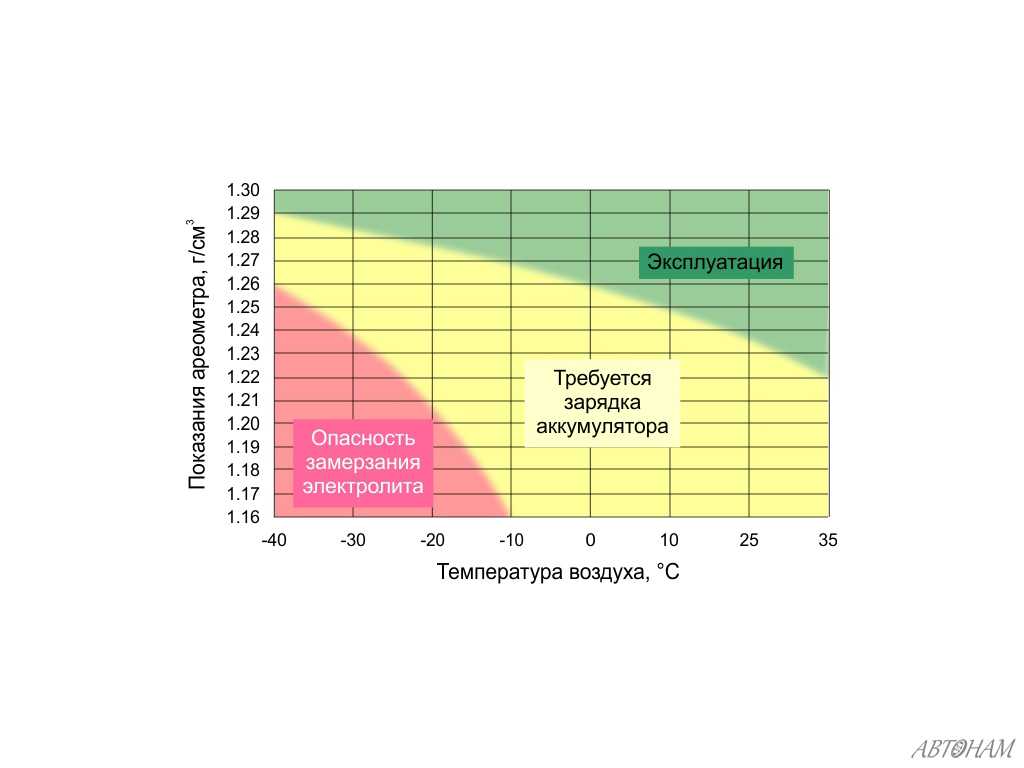 Помните, что не нужно заливать банку под самые края, примерно 10% стоит оставить свободными. Из каждой банки сливается электролит отдельно, затем к нему добавляется свежий раствор в количестве, достаточном для заполнения банки. И так каждый раз.
Помните, что не нужно заливать банку под самые края, примерно 10% стоит оставить свободными. Из каждой банки сливается электролит отдельно, затем к нему добавляется свежий раствор в количестве, достаточном для заполнения банки. И так каждый раз.
Если значение плотности упало до 1,18 г/см3, такой способ не подойдет – нужный уровень не достигнуть. Для того, чтобы реанимировать такой аккумулятор, нужна кислота с плотностью выше, чем у электролита. Где ее взять? Увы, в свободной продаже в автомагазинах ее обычно нет, но на заводах ее найти можно. Процедура такая же, как и в первом случае, и после заливки каждую банку нужно проверять на плотность отдельно, пока не будет достигнуто оптимальное значение.
Если же плотность электролита упала значительно ниже этого значения, его можно только полностью заменить. Возможно, придется купить две банки раствора, одной можно и не обойтись. Электролит спринцовкой выбирается полностью, на его место заливается свежий в полном объеме. Мелкие остатки старого электролита нежелательны, но все же с ними можно смириться.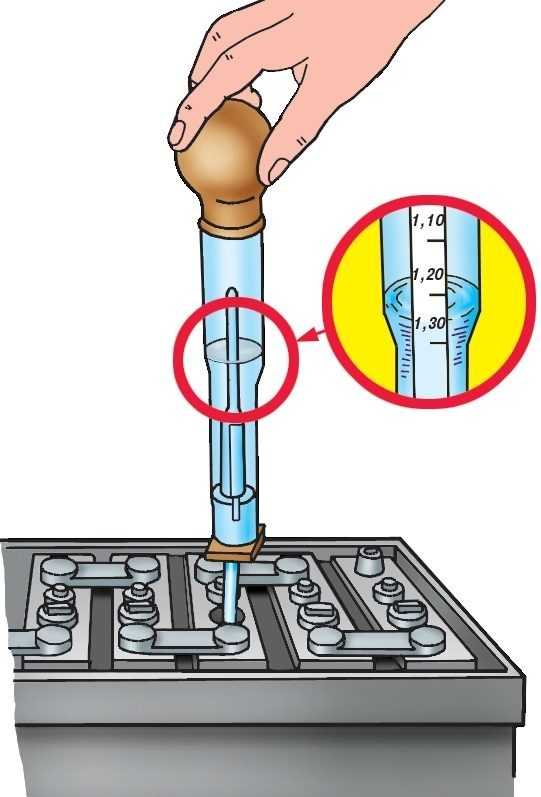 После заливки нового электролита в любом количестве аккумулятор считается полностью разряженным и его нужно перезарядить в полной мере.
После заливки нового электролита в любом количестве аккумулятор считается полностью разряженным и его нужно перезарядить в полной мере.
Повыше плотности при помощи зарядки
Еще один способ повысить плотность раствора серной кислоты – испарение воды. Аккумулятор ставится на зарядку слабым током, но на длительное время, не меньше суток. За это время электролит закипит, из него выделятся пузырьки воды и будут испаряться. Вместо испарившейся жидкости восстанавливаем ее уровень свежим электролитом. Повторяем несколько раз до получения нужно уровня плотности. Затраты небольшие по финансам, но занятие это муторное и нудное.
Вообще падение уровня электролита и его плотности – уже сигнал к тому, что жить в машине этому аккумулятору осталось совсем недолго. Стоит запастись хотя бы дистиллированной водой, чтобы она была всегда с собой, если срочно нужно будет восполнить уровень жидкости. Повышение плотности электролита – тоже временная мера, но она позволяет заметно продлить жизнь аккумулятору. Следите за батареей, и вы сможете избежать многих проблем в пути!
Следите за батареей, и вы сможете избежать многих проблем в пути!
Как поднять плотность электролита АКБ? — АвтоСаратов
MAF
Новичок
- #1
Как поднять до нормы плотность электролита в аккуме?Замер ареометром показал 1200 кг/м3.
evn
LPD: Земля
- #2
зарядить?
Alex74
Активный участник
- #3
evn сказал(а):
зарядить?
Нажмите, чтобы раскрыть…
+1
В теплом помещении еще лучче.
Mig
Новичок
- #4
Можно старый, плохой вылить и залить нормальный)))))))))). Так даже быстрее получится.
Oleg 31rus
Хабист
- #5
Mig сказал(а):
Можно старый, плохой вылить и залить нормальный)))))))))). Так даже быстрее получится.
Нажмите, чтобы раскрыть…
Думаю не стоит, я в своем слил,и залил новый так у меня акб вообще сдох. ((((
MAF
Новичок
- Thread Starter
- #6
evn сказал(а):
зарядить?
Нажмите, чтобы раскрыть.
..
Извиняюсь,забыл уточнить-аккум заряжал почти сутки,сначала малым током(2А),затем как положено 6А(ТАВ 60 А/ч).Малым заряжал по той причине,что не выставлялась норма в 6А.
boris
Активный участник
- #7
MAF, скока лет батарейке? Кто изготовитель?
MAF
Новичок
- Thread Starter
- #8
Заряжал дома,до этого еще почти сутки в тепле был.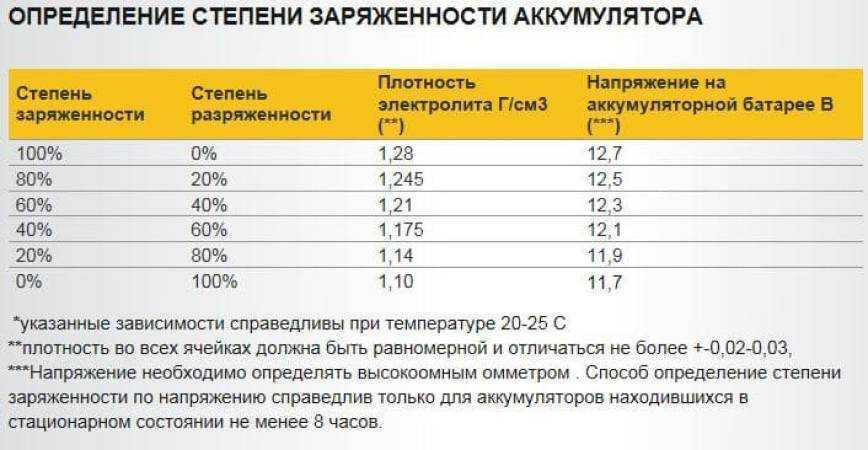 Аккум «молодой»,8 месяцев,правда ЗУ он видел впервые….
Аккум «молодой»,8 месяцев,правда ЗУ он видел впервые….
maik
Участник
- #9
Eсли ты заряжал аккум сутки и его плотность не повысилась , значит аккум сдох .
evn
LPD: Земля
- #10
Oleg 31rus сказал(а):
Думаю не стоит, я в своем слил,и залил новый так у меня акб вообще сдох.
((((
Нажмите, чтобы раскрыть…
ты наверно, что бы слить, аккумулятор переворачивал? %)
evn
LPD: Земля
- #11
MAF сказал(а):
Заряжал дома,до этого еще почти сутки в тепле был.Аккум «молодой»,8 месяцев,правда ЗУ он видел впервые….
Нажмите, чтобы раскрыть…
вобщем мне почему то так кажеца…твое ЗУ не совсем зарядное)))
если в центре живешь…могу дать свое. саветцкое)))
MAF
Новичок
- Thread Starter
- #12
Уровень электролита в норме,напряжение 13,1В.Да,кстати мерять надо по-ходу во всех банках,спешил-успел только в одной..
Mig
Новичок
- #13
:b3b4e46f21f040a62b4
ALEX_099
Новичок
- #14
Mig сказал(а):
Можно старый, плохой вылить и залить нормальный)))))))))). Так даже быстрее получится.
Нажмите, чтобы раскрыть…
учите химию
Mig
Новичок
- #15
MAF сказал(а):
Уровень электролита в норме,напряжение 13,1В.Да,кстати мерять надо по-ходу во всех банках,спешил-успел только в одной.
.
Нажмите, чтобы раскрыть…
А что это такой сложный процесс замер плотности электролита?
Mig
Новичок
- #16
ALEX_099 сказал(а):
учите химию
Нажмите, чтобы раскрыть…
Ок. Пошел за учебником.
Дачник
Новичок
- #17
Если он у тебя побыл разряженным на улице в сильные морозы, то очень высока вероятность, что он уже труп. Вздутия легкого не заметно?
Электролит в любом случае менять бессмысленно.
MAF
Новичок
- Thread Starter
- #18
evn сказал(а):
вобщем мне почему то так кажеца…твое ЗУ не совсем зарядное)))
если в центре живешь…могу дать свое. саветцкое)))Нажмите, чтобы раскрыть…
Советское,канешна,есть гуд!Живу как раз в центре,есть еще самодельное ЗУ,да все некогда до ума довести.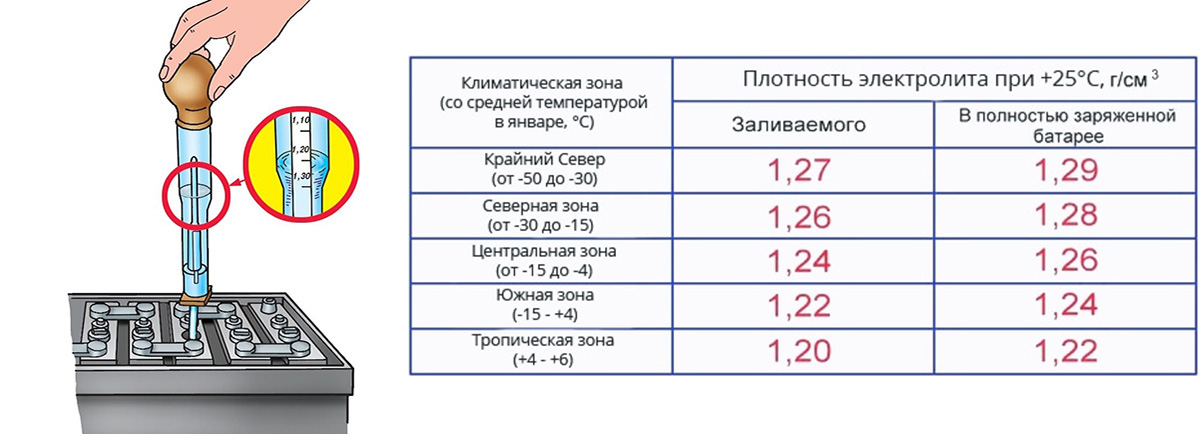 …
…
Anthrax
лорд Канцлер
- #19
Mig сказал(а):
Можно старый, плохой вылить и залить нормальный)))))))))). Так даже быстрее получится.
Нажмите, чтобы раскрыть…
http://ru.wikipedia.org/wiki/Вредные_советы
ALEX_099
Новичок
- #20
Mig сказал(а):
Ок. Пошел за учебником.
Нажмите, чтобы раскрыть…
Глинка — Общая химия — советую настоятельно, очень хороший букварь
Последнее редактирование:
Международный журнал химических и физических наук
Вода известна как наиболее полезная, структурно наиболее сложная и аномальная жидкость, известная людям. Он играет важную роль в жизненных процессах и является неотъемлемой частью животных клеток и тканей растений. Две неподеленные пары электронов на атоме кислорода заставляют два связанных атома водорода придавать характерную V-образную форму с валентным углом 104,5 °. Эта полярность дает обширные водородные связи между молекулами воды, которые ответственны за многие аномальные свойства воды.
Эта полярность дает обширные водородные связи между молекулами воды, которые ответственны за многие аномальные свойства воды.
Некоторыми важными и хорошо известными аномалиями воды являются чрезвычайно высокие температуры плавления (0 °C) и кипения (100 °C). Особенно важным аномальным свойством воды является температура максимальной плотности (TMD) на уровне 3,98 °C. Томас Чарльз Хоуп1 — первый ученый, зафиксировавший TMD воды в 1805 году, измерив характер конвекции воды в сборке из цилиндра, снабженного двумя термометрами и металлическим резервуаром, который известен как прибор
Сопоставимые вещества, такие как Nh4, Ch5, HF и h3S, ведут себя иначе, чем вода. Вода проявляет характерные свойства ассоциированной жидкости более заметные, чем гидриды элементов группы VIA.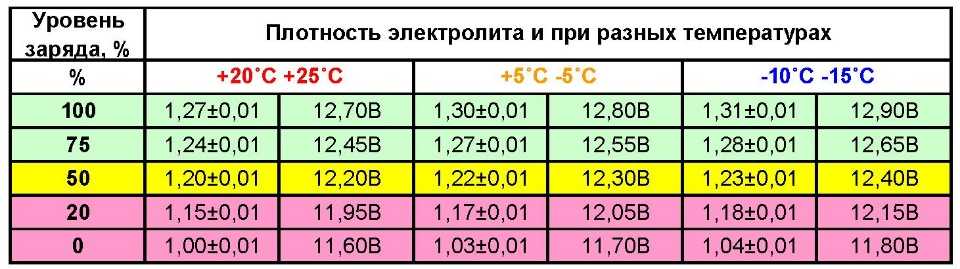 Температуры плавления и кипения этих гидридов упорядоченно уменьшаются с уменьшением молекулярной массы от h3Te, h3Se до h3S, однако вода имеет удивительно высокие значения, указывающие на наличие сильного взаимодействия, известного как водородная связь. Из-за этого вода существует в виде мономеров, димеров, полимеров, клеточных кластеров и многих сложных структур, но полости в структуре приводят к более низкой плотности.
Температуры плавления и кипения этих гидридов упорядоченно уменьшаются с уменьшением молекулярной массы от h3Te, h3Se до h3S, однако вода имеет удивительно высокие значения, указывающие на наличие сильного взаимодействия, известного как водородная связь. Из-за этого вода существует в виде мономеров, димеров, полимеров, клеточных кластеров и многих сложных структур, но полости в структуре приводят к более низкой плотности.
Conway2 определил понятие структуры в жидкой воде следующим простым образом: Способность растворенных веществ создавать/разрушать структуру воды можно определить с точки зрения влияния на время молекулярной переориентации (10-11 с), в результате чего либо от вращательной или поступательной диффузии. Если растворенное вещество заметно удлиняет этот период, его называют структурообразователем/промотором. И наоборот, если растворенное вещество сокращает этот период, это называется разрушением структуры.
При 3,98°C вода достигает максимальной плотности из-за разрыва сети водородных связей, что позволяет разрыхленным молекулам воды заполнять пустоты в открытой структуре, что приводит к сокращению объема и увеличению плотности. Таким образом, TMD регулируется критическим равновесием между мономерами или димерами и молекулами воды, связанными водородными связями. При растворении растворенного вещества в воде вышеуказанное равновесие нарушается. Если растворенное вещество усиливает водородные связи (например, t-BuOH), то TMD увеличивается, а если растворенное вещество имеет тенденцию разрушать водородные связи (например, большинство электролитов), то TMD уменьшается.
Таким образом, TMD регулируется критическим равновесием между мономерами или димерами и молекулами воды, связанными водородными связями. При растворении растворенного вещества в воде вышеуказанное равновесие нарушается. Если растворенное вещество усиливает водородные связи (например, t-BuOH), то TMD увеличивается, а если растворенное вещество имеет тенденцию разрушать водородные связи (например, большинство электролитов), то TMD уменьшается.
Видимый прямолинейный график сдвига TMD (Dqobs) в зависимости от «m» называется правилом Деспреца3, уравнение (1).
Dqobs = m. км или Dqobs = x. KD … (1)
Константы Km (oC/моль/кг)4-6 или KD (oC)7, известные как константа Деспреца, являются характерными для электролитов. «m» и «x» — моляльность и молярная доля растворенного вещества соответственно.
Rosetti8,9 проанализировал ранние работы по сдвигу TMD воды путем добавления растворенного вещества для нескольких простых солей.
Далее, Розетти8,9 пытался связать сдвиг ТМД воды с понижением температуры ее замерзания за счет добавления того же растворенного вещества, но ему не удалось сформулировать какой-либо общей закономерности между этими двумя явлениями, так как понижение температуры температура замерзания связана с осмотическим давлением раствора и, таким образом, зависит только от концентрации. Однако сдвиг TMD характерен для растворенного вещества, т.е. его взаимодействия с Н-связью и концентрацией растворенного вещества.
Райт10 изучал снижение TMD воды для некоторых солей. Его выводы удовлетворительно согласуются с законом Депреца. Далее он обнаружил, что высокоионизированные соли органических кислот ведут себя нормально, как сильные электролиты и минеральные кислоты. Coppet4 и Wright10 измерили сдвиг TMD только при 2–3 концентрациях, которых было недостаточно для надежной оценки константы Деспреца.
Bernal & Fowler13 продемонстрировали применимость принципа аддитивности к парциальным молярным объемам (V ) электролитов при бесконечном разбавлении. Вирт24 разделил V электролитов на их ионные компоненты, предполагая, что V = V, учитывая, что радиусы кристаллов K+ и F- почти одинаковы. Эта аддитивность парциального молярного объема электролитов при бесконечном разведении в воде также была адекватно продемонстрирована рядом исследователей (Bernal & Fowler13, Horne15, Millero16, Scoot17, Desnoyers et al18, Couture & Laidler19).). Было обнаружено, что это правило аддитивности распространяется до умеренных концентраций, при которых ионное спаривание невелико.
Многие другие электролитические свойства, такие как коэффициент вязкости B, ионные радиусы, проводимость и т. д., также подчиняются правилу аддитивности. Каминский20 показал аддитивность коэффициентов вязкости В для водных растворов электролитов при различных температурах. Он предположил, что BK+ = BCl-, основываясь на почти одинаковых числах переноса катионов и анионов для KCl при всех температурах, и рассчитал ионные B-значения для нескольких ионов, которые хорошо согласовывались с данными, полученными другими исследователями.
Применимость правила аддитивности к поведению TMD сильных электролитов наблюдалась Райтом10 с использованием данных TMD Coppet4, Wada & Miura7, Rosetti8,9. Coppet4, Wada & Miura7, Rosetti8,9 также продемонстрировали справедливость правила аддитивности для поведения TMD некоторых галогенидов щелочных металлов, используя данные TMD, приведенные в литературе. (ИКТ11).
Lilley & Murphy5, вывели уравнение (2) выражая ∂V /∂T через постоянную Деспреца Km, как указано ниже:
– ∂V /∂T = Km / 64,1 (2)
Где V обозначает парциальный молярный объем электролита при бесконечном разбавлении.
Видно хорошее соответствие между значениями Km, полученными из измерений плотности с использованием уравнения. (2) со значениями Km, полученными при измерении TMD (Wright10 и ICT11). Однако данные, используемые для измерений TMD и плотности, имеют высокую концентрацию, что не может дать надежных значений. Следовательно, значения Km, сообщаемые ими, необходимо изменить с использованием измерений TMD и плотности при достаточно низких концентрациях, где теория Дебая – Хюккеля для взаимодействия ионов с водой будет справедливой.
[1]. TC Hope, Trans. Королевский соц. Эдинбург, 9 , 5 , 1805, 379-405.
[2]. BE Conway, Ионная гидратация в химии и биофизике, Elsevier Sc. Издательская компания 12 , 1981
[3].М. К. Депрец, Ann. Чим. физ. , 70, 1839, 49; 73, 1840, 296.
[4]. Коппет Энн. Чим. Phys ., 1894, 246; 1899, 1559; 1900, 178; 1901, 1218.
[5]. Т. Х. Лилли и С. Мерфи J Хим. Термодинамика 5 , 1973, 467.
[6]. Т. Вакабаяси и К. Такайзуми, Bull. хим. соц. Япония. 55 , 1982, 3072.
[7]. Г. Вада и М. Миура, Bull. хим. соц. Япония. 42 , 1969, 2498.
[8]. MF Rosetti, Annales de Chimie et de Physique , 10 , 1867, 461-473.
[9]. М.Ф. Розетти, Annales de Chimie et de Physique , 17 , 1869, 370-384.
[10]. R. Wright, J Chem. соц. 115 ,1919,119
[11]. Международные критические таблицы числовых данных, физики, химии и технологии, Национальный исследовательский совет
, III , 1928, 107-111.
[12]. В. К. Покале, доктор философии Диссертация, Нагпурский университет, Индия, 1991.
[13]. J.D.Bernal & R.H.Fowler, J Chem Phys, 1 , 1933, 515
[14]. HE Wirth, J Marine Res. , 3 , 1940, 230
HE Wirth, J Marine Res. , 3 , 1940, 230[15]. Р. А. Хорн, Вода и водные растворы, Wiley Inter Sc. Нью-Йорк 1971
[16]. FJ Millero, Chem. , 71 , 1971, 147
[17]. AF Scoot, J Phys. хим. 35 , 1931, 2315, 3379
[18]. Дж. Э. Деснойерс, М. Arel, G. Perron & C. Jolicoeur, J Phys. хим. 73 , 1969, 3346
[19]. A.M.Couture & K.J.Laidler, , Can J Chem. 34 , 1956, 1209
[20]. М. Каминский, Дис. Фарадей Сок. 24 , 1957, 171
[21]. K. Nakanishi, N. Kato, Maruyama, J. Phys Chem , 71 , 1967, 814
[22]. G. Wada, S. Umeda, Bull Chem Soc Jpn , 35 , 1962, 646
[23]. G. Wada, S. Umeda, Bull Chem Soc Jpn , 35 , 1962, 1797
[24]. Ф. Франкс, Б. Уотсон,
[25]. AJ Darnel, J Greyson, J Phys Chem , 72 , 1968, 3021, 3032
AJ Darnel, J Greyson, J Phys Chem , 72 , 1968, 3021, 3032
[26]. D.D.Macdonald, M.D.Smith, J.B.Hyne, Can J Chem , 49 , 1971, 2817
[27]. M.V.Kaulgud, WK Pokale, J. Chem Soc Faraday Trans , 91(6), 1995, 999
[28]. Г. А. Боттомли, Л. Г. Глоссоп, В. П. Стонтон, , Австралия. J. Chem, 32, 1979, 699
[29]. M.V.Kaulgud, V.S.Bhagde, S.S.Dhondge, Ind. J Chem. 24А, 1985, 373-378
[30]. JL Kavanan, Water & Solute Water Interactions, Holdenday Inc., Сан-Франциско, Калифорния, 1964,
,[31]. Дж. Грейсон, J Phys. хим. 71 , 1967, 2210
[32]. Дж. Р. Купперс, J Phy. хим. 78 , 1974, 1041; 79 , 1975, 2105
[33]. Р. А. Робинсон и Р. Х. Стоукс, Электролитные растворы, Баттерворт, Лондон, 2ndedn, 19.59
[34]. R. Zana and E. Yeager, J Phys. хим. , 71, 1967, 52
Yeager, J Phys. хим. , 71, 1967, 52
[35]. Э. Дж. Кинг, J Phys. Хим , 74, 1970, 4590
[36]. Г. Вада, Э. Нагао, Н. Кавамура и К. Кинумото, Bull. хим. соц. яп. 51 , 1978, 1937
[37]. FJ Millero, J. Phys. Chem., 72 , 1968, 4589
[38]. J. V. Leyendekkers, J. Chem. Soc., Faraday Trans. 1, 76 , 1980, 1206
[39]. J.V.Leyendekkers, J. Chem. Soc., Faraday Trans. 1 , 77 , 1981, 1529
[40]. J.V.Leyendekkers, J. Chem. Soc., Faraday Trans. 1 , 78 , 1982, 357
[41]. J.V.Leyendekkers, J. Chem. Soc., Faraday Trans. 1 , 78 , 1982, 3383
[42]. J.V.Leyendekkers, J. Chem. Soc., Faraday Trans. 1 , 79 , 1983, 1109
[43]. J.V.Leyendekkers, J. Chem. Soc., Faraday Trans. 1 , 79 , 1983, 1123
J.V.Leyendekkers, J. Chem. Soc., Faraday Trans. 1 , 79 , 1983, 1123
[44]. BE Conway & RE Verral, J Phys. Chem, 70 , 1966, 3952
[45]. J. Padova & I. Abrahamer, J Phys. Chem, 70 , 1966, 3961
[46]. F. Franks & HT Smith, Trans Faraday Soc. 63 , 1967, 2586
[47]. Дж. Э. Деснойерс и М. Арел, Кан. Дж. Хим. 45 , 1967, 359
[48]. Ф. Дж. Миллеро и В. Дрост-Хансен, J Phy. Химия . 72 , 1968, 1758
[49]. И. Ли и Дж. Б. Хайн, , Кан. J Chem . 46 , 1968, 2333
[50]. R.L.Kay, T.Vituccio, C.Zawoyski&D.F.Evans, J Phy. Chem, 70 , 1966, 2366.
[51]. Д. Ф. Эванс, Г. П. Каннингем и Р. Л. Кей, J Phy Chem , 70 , 1966, 2974.
[52]. R. A. Horne & R. P. Young, J Phy Chem , 72 , 1968, 1763.
[53]. R. H. Wood, H. L. Anderson, J. D. Beck, J. R. France, W. R. De Vry & L. J. Soltzberg, J Phy Chem ,
71 , 1967, 2149
[54]. F. Franks & D.L. Clarke, J Phy Chem, 71 , 1967, 1155
[55]. H. E. Worth & A. L. Surdo, J Phy Chem, 72 , 1968, 751
[56]. K.W.Bunzl, J Phy Chem, 71 , 1967, 1358
[57]. H. E. Worth J Phy Chem, 71 , 1967, 2922
[58]. P.R.Daneai, F.Orlandini&G.Scibona, J InorgNucl Chem , 30 , 1968, 2513
[59]. Т. С. Шарма, Р. К. Моханти и Дж. К. Ахлувалия, Trans. Фарадей Сок. 65 , 1969, 2333
[60]. JD Worley & I.M. Klotz, J Chem Phys., 45, 1966, 2868
[61]. И. М. Клотц, Федеральная прокуратура. , 24 , 1965, с 24
[62]. M. M. MarciaqRousselot, A. Trobriand & M. Lucas, J Phy Chem , 76 , 1972, 1455
Lucas, J Phy Chem , 76 , 1972, 1455
[63]. G.P.Kreishman & L.Leifer, J Sol Chem , 7 , 1978, 239
[64]. G. Perron, N.Desrosier & J.E.Desnoyers, Can J Chem, 54 , 1976, 2163
[65]. К. Такайзуми, Т. Вакабаяши, Bull Chem Soc Jpn , 55 ,1982, 2239
[66]. S. Subramanian & J. C. Ahluwalia, J Phy Chem , 72 , 1968, 2525.
[67]. TS Sharma & JC Ahluwalia, J Phy Chem , 74 , 1970, 3547
[68]. А. М. Дешпанде, к.т.н. Диссертация, Нагпурский университет, 1997
[69]. А. М. Дешпанде, В. К. Покале, А. В. Покале , J Res & Dev Multidis Int Ref, 2020, 389-395
[70]. Справочник по химии и физике, Химическая резина Co . Кливленд, Огайо, 1968, , 48-е издание .
[71]. M.V.Kaulgud, K.S.M.Rao, Indian J Chem , 27A , 1988, 12-17
[72]. В. С. Бхагаде – кандидат философских наук. Диссертация, Нагпурский университет, 1984
В. С. Бхагаде – кандидат философских наук. Диссертация, Нагпурский университет, 1984
[73]. MV Kaulgud, GH Pandya, Indian J Chem , 14A , 1976, 91-93
[74]. SeigfriedLindenbaum, J Chem Thermodyn, 3 , 1971, 625-629
[75]. К. А. (младший) Хартман, 9 лет0045 J Phys Chem , 70 , 1960, 270
[76]. Diamond, J Phys Chem , 67 , 1963, 2513
[77]. JC Ahluwalia, B. Chawala, J Soln Chem , 6 , 1975, 383
[78]. G. Wada, S. Umeda, Bull ChemSocJpn , 42 , 1969, 2498
[79]. G. M. Watson & Felsing, J Am Chem Soc , 63 , 1941, 410
[80]. М. В. Каулгуд, А. Шривастава и М. Р. Аводе, Indian J Chem , 29 A , 1990, 439-444
[81]. M. Tariq, JMSS Esperança, MRC Soromenho, LPN Rebelo & JN Canongia Lopes,
Royal Society of Chemistry, J. Phys. хим. хим. физ. , 15 , 2013, 10960-10970
Phys. хим. хим. физ. , 15 , 2013, 10960-10970
[82] S. Thirumran & P Inbam, Ind J Pure & App Phy, 49 , 2011, 451-459,
[83] J. T. Deige, G, G, G, G, G, 451-459,
[83] J. T. Deago, G, G, 451-459,
[83] J. , Salgado & L. Romani?, J of Chemical &Engg Data , 2019[84]. К. Р. Фостер и Э. Д. Финч Дж. физ. Chem., 78 (22) ,1974 , 2305–2306
[85]. М.Ф. Коули, Д. МакГлинн, П.А. Mooney, International Journal of Heat and Mass Transfer, 49 , 2006, 1763–1772
[86]. Джерард Коттер, доктор философии. Диссертация, Национальный университет Ирландии, округ Мейнут, Килдэр, 23 сентября 2010 г.
[87]. А. Брэдшоу, К.Е. Шлейхер, Deep-Sea Res. , 17 , 1970, 691-706.
[88]. C. T. Chen, F.J Millero, Deep-Sea Res ., 23 , 1976, 595-612.
[89]. КТ Чен, Р.А. Fine, FJ Millero, J. Chem. физ. , 66 , 1977, 2142-2144.
КТ Чен, Р.А. Fine, FJ Millero, J. Chem. физ. , 66 , 1977, 2142-2144.
[90]. КТ Чен, Ф. Дж. Миллеро, J. Marine Res ., 36 , 1978, 657-691.
[91]. Ф.Дж. Миллеро, К.Т. Чен, А. Брэдшоу, К. Шлейхер, Deep-Sea Res. , 27А , 1980, 255-264.
[92]. С.Дж. Хендерсон, Р.Дж. Спиди, J. Phys. хим. , 91 , 1978, 3062-3068.
[93]. П. Фофонофф, Р.К. Миллард, ЮНЕСКО, 1983. Технологии ЮНЕСКО. Пап. In Mar. Sci., 44 , 1983, 53.
