Устройство «умного аккумулятора» | Логический Элемент ⚡ Зарядные устройства для аккумуляторов
Обычная батарея аккумуляторов говорить не умеет, она — немая, т.к. по ней очень сложно определить степени ее заряда, или ее состояние. Пользователю остается только рассчитывать, что аккумулятор отключенный от зарядного устройства исправно выполнит свои функции.
В последнее время все более широкое распространение получают так называемые разумные аккумуляторы (батареи). Внутри батареи установлен микрочип, способный обмениваться информацией с заряжающим устройством и выдавать пользователю статистические данные об аккумуляторе. Обычно такие аккумуляторные батареи применяются для питания ноутбуков, сотовых телефонов и видеокамер, а также некоторых типов оборудования медицинского и военного предназначения.
Существуют разные типы разумных аккумуляторных батарей, отличающихся количеством функций, производительностью и стоимостью. Наиболее простыми считаются аккумуляторные батареи со встроенным чипом, предназначенным для идентификации типа аккумулятора в многофункциональных зарядных устройствах, для того чтобы автоматически установить правильный алгоритм заряда. Аккумуляторные батареи со встроенной защитой от перезаряда, недозаряда и короткого замыкания, разумными называть не следует.
Аккумуляторные батареи со встроенной защитой от перезаряда, недозаряда и короткого замыкания, разумными называть не следует.
Наиболее совершенные разумные батареи обеспечивают определение состояния заряда. Первые чипы для разумных батарей появились в начале 90-ых годов. Сейчас их производством занимается большое число компаний. В конце 90-ых годов была разработана архитектура разумных аккумуляторных батарей с возможностью считывания степени их заряда. Это были 1- и 2-проводные системы. Большинство 2-проводных систем действует по протоколу SMBus(System Management Bus).
Аккумуляторные батареи с 1-проводным интерфейсом 1-Wire
Системы с 1-проводным интерфейсом 1-Wire принадлежат к наиболее простым, и обмен данными в них реализовывается по одному проводу. Аккумуляторная батарея со встроенной системой с 1-проводным интерфейсом 1-Wire имеет только три вывода: положительный, отрицательный и вывод информации. Некоторые производители в целях безопасности вывод датчика температуры делают отдельно (рисунок 1).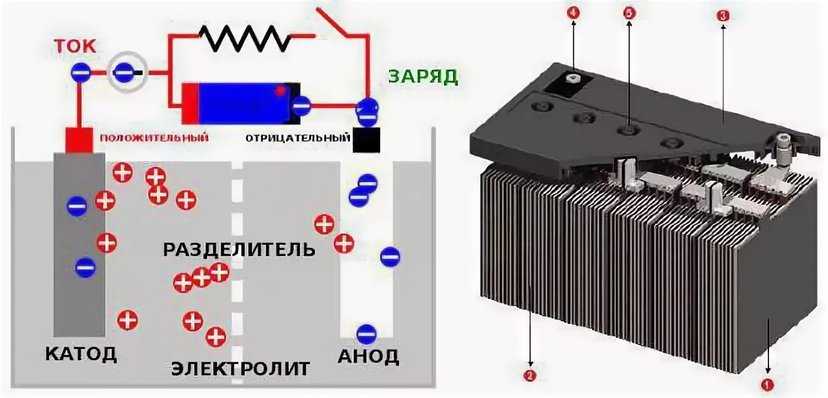
Рис.1. Схема аккумуляторной батареи с 1-проводным интерфейсом
Современные батареи с 1-проводным интерфейсом 1-Wire хранят специфические данные об аккумуляторе и отслеживают его температуру, напряжение, ток, степень заряда. Из-за простоты и относительно низкой цены они нашли широкое применение для аккумуляторов мобильных телефонов, портативных радиостанций.
Большинство аккумуляторных батарей с 1-проводным интерфейсом 1-Wire не имеют общего форм-фактора, не стандартизованы в них и способы измерения состояния аккумулятора. Все это в целом порождает проблему концепции универсального зарядного устройства. Кроме того, батареи с 1-проводным интерфейсом 1-Wire позволяют определять состояние аккумулятора только в том случае, если батарея установлена в специально разработанное под эту систему зарядное устройство.
Аккумуляторные батареи с шиной SMBus
SMBus — наиболее совершенная из всех систем, так как является стандартом для портативных электронных устройств и использует единый стандартный протокол обмена данными. SMBus представляет из себя 2-проводной интерфейс, посредством которого простые микросхемы системы электропитания могут обмениваться данными с системой. По одному проводу передаются данные, по другому — сигналы синхронизации (рисунок 2). Основу этой шины составляет архитектура шины I 2C. Разработанная фирмой Philips, шина I2C представляет собой синхронную многоточечную систему двунаправленного обмена данными, действующую при частоте синхронизации 100 кГц.
SMBus представляет из себя 2-проводной интерфейс, посредством которого простые микросхемы системы электропитания могут обмениваться данными с системой. По одному проводу передаются данные, по другому — сигналы синхронизации (рисунок 2). Основу этой шины составляет архитектура шины I 2C. Разработанная фирмой Philips, шина I2C представляет собой синхронную многоточечную систему двунаправленного обмена данными, действующую при частоте синхронизации 100 кГц.
Рис.2. Схема аккумуляторной батареи с шиной SMBus
Системная архитектура разумных аккумуляторных батарей, используемая в настоящее время, была стандартизована компаниями Duracell/Intel еще в 1993 г. До этого производители портативных компьютеров разрабатывали собственные умные батареи. На основе новой спецификации был построен универсальный интерфейс, что к тому же позволило обойти отдельные препятствия, связанные с патентованной интеллектуальной собственностью.
Первые образцы аккумуляторных батарей с SMBus имели проблемы: электронные схемы не обеспечивали обработки данных с достаточной точностью, не обеспечивалось отображение как значения тока, так и значений напряжения и температуры в режиме реального времени. Было и множество других значительных проблем. В результате практически все технические решения, касающиеся реализации разумной батареи на базе SMBus, были модифицированы.
Смысл новых решений заключался в том, чтобы перенести функции управления процессом заряда с зарядного устройства на аккумуляторную батарею. Теперь уже не зарядное устройство, а сама батарея с системой на основе SMBus задавала алгоритм собственного заряда. Таким образом, обеспечивались совместимость зарядных устройств с батареями разных типов, правильная установка значений тока и алгоритма заряда, точное отсоединение батареи в момент окончания заряда. И, что важно, пользователю стало ненужным знать, аккумулятор какого типа он использует, — все эти заботы батарея брала на себя, а его функции сводились только к тому, чтобы вовремя ее заряжать.
Рассмотрим, что же такое разумная аккумуляторная батарея изнутри. Батарея с системой SMBus имеет микросхему, в которой запрограммированы постоянные и временные данные. Постоянные данные программируют на заводе-производителе, и они включают идентификационный номер батареи, сведения о ее типе, заводской номер, наименование производителя и дату выпуска. Временные данные — это те данные, которые периодически обновляются. К ним принадлежат количество циклов заряда, пользовательские данные и эксплуатационные требования.
SMBus разделяется на три уровня. Уровень 1 в настоящее время не применяется, т.к. не обеспечивает заряд различных по типу аккумуляторных батарей. Уровень 2 предназначен для внутрисхемного заряда. Пример этого — аккумуляторная батарея ноутбука, которая заряжается, будучи установленной. Уровень 3 зарезервирован для применения в многофункциональных внешних зарядных устройствах. К сожалению, из-за сложности такие зарядные устройства получаются дорогостоящими.
Аккумуляторные батареи с SMBus имеют и недостатки. Даже самые простые из них приблизительно на 25% дороже обычных аккумуляторных батарей. Несмотря на то, что разумные батареи были предназначены для того, чтобы упростить конструкцию зарядных устройств, зарядные устройства уровня 3 обходятся намного дороже зарядных устройств для обычных аккумуляторов.
Даже самые простые из них приблизительно на 25% дороже обычных аккумуляторных батарей. Несмотря на то, что разумные батареи были предназначены для того, чтобы упростить конструкцию зарядных устройств, зарядные устройства уровня 3 обходятся намного дороже зарядных устройств для обычных аккумуляторов.
Существует и еще одна проблема — необходимость калибровки. Дело в том, что в процессе использования батарея может работать при различных токах нагрузки, и ее разряд может быть неполным. При этом часто случается так, что она запоминает текущее состояние емкости, которое не соответствует истинному значению. Поэтому периодически следует переучивать батарею, для того чтобы она при установлении алгоритма заряда учитывала свою реальную емкость. Выполняется это путем выполнения цикла полного разряда с последующим полным зарядом. Периодичность такой операции — ориентировочно один раз в три месяца или через каждые 40 циклов заряд/разряд. Такой же цикл следует провести и после длительного хранения батареи, перед ее вводом в эксплуатацию.
Недостатком является и проблема несовместимости: более поздние и более совершенные версии SMBus несовместимы с более ранними вариантами.
Материал сайта: www.powerinfo.ru
Аккумуляторная батарея на автомобиле. Устройство, эксплуатация, маркировка
Содержание страницы
- 1. Принцип действия аккумулятора
- 2. Устройство аккумулятора
- 3. Конструкция аккумуляторных батарей
- 4. Маркировка аккумуляторных батарей
- 5. Параметры автомобильных батарей
- 6. Заряд автомобильных батарей
- 7. Эксплуатация аккумуляторных батарей
- 8. Техническое обслуживание аккумуляторных батарей
- 9. Неисправности автомобильных АКБ
- 10. Техника безопасности при работе с АКБ
Химическим источником тока называется устройство, в котором энергия протекания окислительно-восстановительных реакций преобразуется в электрическую.
По характеру работы эти источники делятся на две группы:
- первичные источники тока, или гальванические элементы;
- вторичные источники тока, или аккумуляторы.

Первичные источники допускают только однократное использование и являются необратимыми источниками энергии.
Вторичные источники являются обратимыми источниками энергии: после разряда их работоспособность можно восстановить путем пропускания тока в обратном направлении.
Аккумуляторная батарея на автомобиле выполняет четыре основные функции:
- Надежный запуск двигателя.
- Энергоснабжение при выключенном двигателе (неработающем генераторе).
- Компенсация дефицита энергии при работе совместно с генератором.
- Сглаживание пульсаций напряжения бортовой сети.
Стартерные аккумуляторные батареи должны удовлетворять следующим основным требованиям (ГОСТ Р 53165-2008):
- Обеспечивать необходимый для работы стартера разрядный ток.
- Обладать запасом энергии для питания потребителей при неработающем двигателе или в аварийной ситуации.
- Сохранять работоспособность при повышенной (до плюс 60 °С) и пониженной (до минус 50 °С) температуре окружающей среды.

- Обладать герметичностью. Электролит не должен выливаться при наклоне на 45°.
- Принимать заряд для восстановления израсходованной емкости.
- Удовлетворять требованиям стандарта по расходу воды и саморазряду.
- Иметь высокую механическую и вибрационную прочность.
- Срок службы батареи должен составлять не менее 24 (48) месяцев или 90 (100) тыс. км пробега.
На подавляющем большинстве автомобилей получили применение свинцово-кислотные аккумуляторы.
1. Принцип действия аккумулятора
В свинцово-кислотном аккумуляторе в токообразующих процессах участвуют:
- диоксид свинца PbO2 (окислитель) положительного электрода;
- губчатый свинец Pb (восстановитель) отрицательного электрода;
- электролит — водный раствор серной кислоты (H2SO4).
Рисунок 1 – Принцип работы свинцово-кислотного аккумулятора
При подключении потребителя происходит разложение серной кислоты и образование воды. На положительном и отрицательном электродах образуется сульфат свинца (PbSO 4).
На положительном и отрицательном электродах образуется сульфат свинца (PbSO 4).
Рисунок 2 – Процесс разряда аккумулятора
При подключении источника происходит восстановление губчатого свинца на отрицательном электроде, диоксида свинца – на положительном электроде и серной кислоты в электролите.
Рисунок 3 – Процесс заряда аккумулятора
Химическая реакция, протекающая в аккумуляторе описывается следующим уравнением:
2. Устройство аккумулятораАккумулятор содержит два полублока отрицательных и положительных пластин, разделенных между собой сепараторами. Каждая пластина состоит из активной массы и решетки, которая служит токоотводом и основой удерживающей активную массу.
Рисунок 4 – Устройство аккумулятора
В верхней части решетки имеется ушко, с помощью которого пластины привариваются к соединительному мостику (баретке), имеющему общий вывод для соединения аккумуляторов в батарею.
Рисунок 5 – Положительная (слева) и отрицательная решетки аккумулятора
Основой материала решеток является свинец с добавками других веществ. Добавление к свинцу сурьмы увеличивает прочность, но приводит к повышенному расходу воды.
Замена сурьмы кальцием уменьшает расход воды практически до нуля, однако снижает устойчивость батареи к глубоким разрядам. Гибридные батареи имеют в составе положительных пластин – сурьму, а в отрицательных – кальций.
Легирование серебром предохраняет свинцовую основу от коррозии и снижает деформацию решеток.
Сепаратор, изготовленный из микропористого кислотостойкого материала, служит для предотвращения замыкания разноименных пластин и обеспечения запаса электролита.
Рисунок 6 – Сепаратор-конверт из полиэтилена
3. Конструкция аккумуляторных батарейАккумуляторная батарея представляет собой ряд (3,6,12) последовательно соединенных аккумуляторов, помещенных в единый корпус (моноблок), изготовленный из термопластмассы.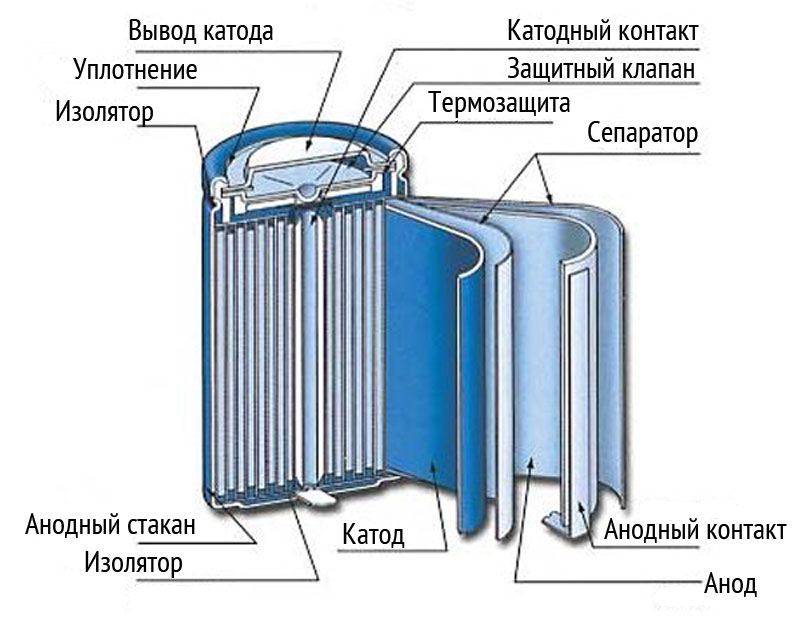
Для соединения аккумуляторов служат межэлементные соединения. Сверху моноблок закрывается общей крышкой, образуя неразборную конструкцию. На крышке имеется два полюсных вывода (терминала) для присоединения батареи во внешнюю цепь.
Положительный вывод (терминал) больше отрицательного, для исключения возможности неправильного подключения аккумуляторной батареи.
Полюсные выводы (терминалы) помимо конструктивных отличий могут различаться расположением: прямая и обратная полярность.
Рисунок 7 – Размеры полюсных выводов
Рисунок 8 – Конструкция аккумуляторной батареи: 1 – крышка корпуса, 2 – корпус (моноблок), 3 – аккумулятор, 4 – полюсный вывод (терминал), 5 – заливная пробка, 6 – перемычка, 7 – ручка для переноски, 8 — индикатор
Рисунок 9 – Типы полюсных выводов (терминалов)
Индикатор позволяет оценить степень заряженности батареи и уровень электролита в батарее.
Рисунок 10 – Полярность аккумуляторных батарей
Зеленый цвет индикатора свидетельствует о достаточной степени заряженности батареи (>65 %) и ее исправности.
Черный цвет свидетельствует о недостаточной степени заряженности батареи (<65 %) и необходимости ее подзаряда.
Бесцветный глазок свидетельствует о слишком низком уровне электролита и необходимости замены батареи.
Рисунок 11 – Индикатор степени заряженности батареи Батареи с жидким электролитом.
Батареи с жидким электролитом оснащаются заливными пробками, имеющими вентиляционные отверстия. К достоинствам можно отнести невысокую стоимость, большое количество моделей на рынке, пригодность для установки в моторном отсеке, возможность долива электролита.
К недостаткам таких батарей относят возможность выливания электролита и повышенный расход воды.
Батареи типа VRLA (Valve Regulated Lead Acid Battery).
Пробки ячеек не выворачиваются. Образующиеся при перезаряде водород и кислород обычно ячейки батареи не покидают и реагируют между собой с образованием воды. Подобные батареи не требуют обслуживания и пригодны для установки в моторном отсеке. К недостаткам таких батарей относят повышенную стоимость, отсутствие возможности долива электролита, высокие требования к зарядному напряжению (не более 14,4 В).
К недостаткам таких батарей относят повышенную стоимость, отсутствие возможности долива электролита, высокие требования к зарядному напряжению (не более 14,4 В).
Батареи с гелеобразным электролитом.
В электролит этих батарей добавлена кремниевая кислота, превращающая его в гель. Добавление фосфорной кислоты существенно повышает их циклическую стойкость и способность к восстановлению после глубокого разряда.
К достоинствам можно отнести отсутствие необходимости обслуживания, высокую циклическая стойкость, невозможность выливания электролита. Недостатками таких батарей считают высокую стоимость, непереносимость высоких температур, ухудшенные пусковые свойства при низких температурах, ограниченное количество моделей на рынке.
Рисунок 12 – Центральная система вентиляции
Батареи типа AGM.
Так называют батареи, у которых электролит впитывается и удерживается стекломатами. Стекломаты представляют собой микропористый нетканый материал из переплетающихся между собой ультратонких стекловолокон. Стекломаты выполняют функции сепараторов. В батарею заливается только то количество электролита, которое могут впитать стекломаты. Достоинства — не требуют обслуживания, высокая циклическая стойкость, нет возможности выливания электролита, хорошие пусковые свойства. Недостатки — высокая стоимость и ограниченное количество моделей на рынке.
Стекломаты выполняют функции сепараторов. В батарею заливается только то количество электролита, которое могут впитать стекломаты. Достоинства — не требуют обслуживания, высокая циклическая стойкость, нет возможности выливания электролита, хорошие пусковые свойства. Недостатки — высокая стоимость и ограниченное количество моделей на рынке.
Рисунок 13 – Устройство батареи типа AGM
Батареи OPTIMA
Основное отличие заключается в применении технологии Optima Spiralcell® Technology: вместо пластин, используемых в обычных аккумуляторах, в батареях OPTIMA применяются «рулонные элементы» — две свитые в рулон тонкие свинцовые ленты с сепаратором из стекловолокна, содержащим кислоту.
Такая технология позволяет значительно снизить толщину свинцовых лент и на 50-100 % увеличить их активную площадь в сравнении с обычными пластинами.
Рисунок 14 – Устройство батареи OPTIMA
Достоинства — не требуют обслуживания, высокая циклическая стойкость, нет возможности выливания электролита, очень хорошие пусковые свойства, сохраняют пусковые качества даже после года хранения без подзарядки.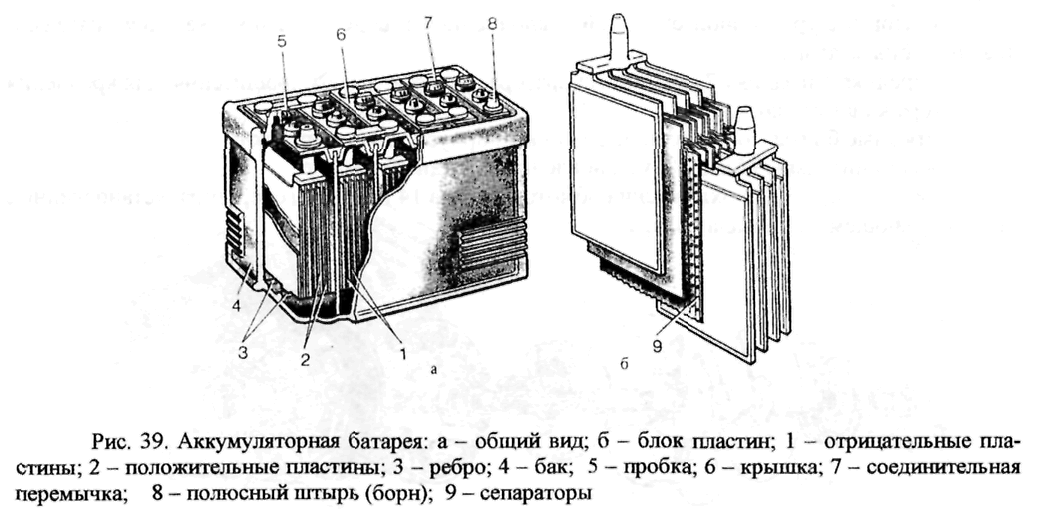 Недостатки — высокая стоимость и большая масса.
Недостатки — высокая стоимость и большая масса.
Рисунок 15 – Маркировка аккумуляторных батарей: 1 – обозначение типа батареи, 2 – товарный знак завода-изготовителя, 3 – номинальная емкость, А·ч, 4 – ток холодной прокрутки, А, 5 – номинальное напряжение, В, 6 – дата изготовления, 7 – масса батареи, кг, 8 – обозначение полярности, 9 – знаки безопасности, 10 – уровень электролита
Согласно ГОСТ Р 53165-2008 обозначение типа батареи включает:
- – цифра, указывающая число последовательно соединённых аккумуляторов в батарее (
- – буквы, характеризующие назначение батареи по функциональному признаку (СТ – стартерная)
- – число, указывающее номинальную ёмкость батареи в ампер-часах (55)
- – буквы, обозначающие конструкторско-технологическое исполнение (N – с нормальным расходом воды, L – с малым расходом воды, VL – с очень малым расходом воды, VRLA – с регулирующим клапаном)
На батареи наносят символы безопасности (таблица 1).
Таблица 1 — Символы безопасности
| Символ | Расшифровка |
| Соблюдайте инструкцию | |
| Опасно. Едкие и коррозионные вещества | |
| Запрещается пользоваться открытым огнем и курить | |
| Пользуйтесь защитными очками | |
| Хранить вдали от детей | |
| Взрывоопасно | |
| Запрещается выбрасывать с бытовыми отходами | |
| Символ переработки |
К основным параметрам автомобильных АКБ относят ЭДС, напряжение под нагрузкой, внутреннее сопротивление, номинальную и разрядную ёмкость, ток холодной прокрутки и другие.
Электродвижущая сила (ЭДС) батареи – представляет собой разность потенциалов при разомкнутой внешней цепи:
Е = 6·(0,84 + ρ) (1)
где ρ — плотность электролита, приведенная к 25 °С, г/см3.
Напряжение АКБ – отличается от ЭДС на величину падения напряжения в электрической цепи при прохождении разрядного или зарядного тока:
Uр = E — Iр·(r + Rн) напряжение при разряде (2)
Uз = E + Iз·(r + Rн) напряжение при заряде (3)
где r – внутреннее сопротивление батареи, Ом; Rн – сопротивление внешней цепи, Ом.
Ёмкостью, С, аккумулятора называется максимальное количество электричества, выраженное в ампер-часах, которое аккумулятор может отдать во внешнюю цепь при полном разряде до установленного конечного напряжения:
С = Iр·τр (4)
где Iр – разрядный ток, А; τр – время разряда, ч.
Номинальная разрядная ёмкость С20 (указываемая на батарее) определяется при 20-часовом режиме разряда током I = 0,05·С20 при t = 25 °C.
Разряд должен прекратиться при U = 10,5 В.
Рисунок 16 — Временные характеристики АКБ при разряде и заряде
Рисунок 17 – Типичные значения номинальной ёмкости
Резервная ёмкость RC (reserve capasity) – способность АКБ обеспечить необходимый минимум электрической нагрузки при выходе из строя генератора.
Минимум электрической нагрузки складывается из токов, потребляемых системами зажигания и освещения, стеклоочистителем и контрольно-измерительными приборами в режиме «Зима-ночь» и составляет 25 А.
Резервная ёмкость определяется временем разряда в минутах полностью заряженной батареи током 25 А до напряжения на выводах 10,5 В.
Рисунок 18 – Типичное значение резервной ёмкости
Ток холодной прокрутки ССА (cold cranking amps) – это максимальный разрядный ток, который батарея может обеспечить при t = — 18 °С (0 °F) в течение 30 с, сохраняя напряжение на выводах не менее 7,2 В.
Внутреннее сопротивление, r, батареи составляет несколько тысячных долей Ома и увеличивается по мере ее разряда и снижения температуры электролита.
Рисунок 19 – Типичное значение тока холодной прокрутки
6. Заряд автомобильных батарейАккумуляторные батареи заряжают от источника постоянного тока, напряжение на выводах которого выше напряжения заряжаемой батареи.
Используют следующие методы заряда:
- постоянной силой тока,
- постоянным напряжением,
- комбинированный,
- форсированный,
- контрольнотренировочный цикл.
Заряд при постоянной силе тока.
В этом случае заряжаемые батареи соединяются между собой последовательно и подключаются к зарядному устройству.
Сила зарядного тока в этом режиме не должна превышать:
Iз ≤ 0,1·С20 (5)
Заряд при постоянной силе тока отличается сравнительной простотой и обеспечивает полный заряд батарей.
Недостатками этого способа являются повышение температуры в конце заряда и отрицательное влияние перезаряда вследствие кипения электролита.
Заряд при постоянном напряжении.
При этом способе заряда батареи подключают непосредственно к источнику питания, напряжение которого поддерживается постоянным.
Сила зарядного тока устанавливается автоматически.
Батарею можно зарядить до 90-95 % от номинальной емкости. В этом режиме заряжаются батареи на автомобиле.
В этом режиме заряжаются батареи на автомобиле.
Форсированный заряд.
Для быстрого восстановления работоспособности сильно разряженной батареи проводят форсированный заряд силой тока 0,7·С20 в течение 30 минут. Применять форсированный заряд можно в исключительных случаях, так как многократное повторение такого способа заметно сокращает срок службы батареи.
Смешанный режим.
Объединяет достоинства заряда постоянным током и постоянным напряжением: первоначально батарея заряжается первым способом, а затем – вторым. Это позволяет снизить время заряда батареи (по сравнению с чисто вторым способом) и исключить неблагоприятное воздействие перезаряда (свойственное первому способу).
Контрольно-тренировочный цикл.
Данный цикл включает в себя заряд батареи током 0,1·С20, разряд батареи током 0,05·С20 и окончательный заряд силой тока 0,05·С20.
Контрольно-тренировочный цикл проводят для устранения частичной сульфатации и других неисправностей АКБ.
Эксплуатация батарей при низких температурах осложняется следующим рядом факторов:
- При недостаточной плотности возможно замерзание электролита (см. таблицу 2).
- Ухудшается процесс заряда (батарею можно зарядить только до 60-70 % от номинальной ёмкости).
- В результате повышения вязкости моторного масла и электролита ухудшаются условия запуска двигателя.
Эксплуатация батарей при высоких температурах осложняется по следующим причинам:
- Ускоряется разрушение и сульфатация пластин.
- Происходит интенсивное испарение воды (требуется проверка уровня электролита).
Хранение автомобильных батарей.
Хранить автомобильные батареи необходимо в неотапливаемом помещении при температуре от 0 до минус 20°С, что способствует снижению саморазряда.
Таблица 2 – Температура замерзания электролита
| Напряжение, В | Степень заряженности, % | Плотность электролита, г/см3 | Температура замерзания, °С |
| 12,7 | 100 | 1,28 | <-50 |
| 12,5 | 80 | 1,24 | — 40 |
| 12,3 | 60 | 1,21 | — 30 |
| 12,1 | 40 | 1,18 | — 20 |
| 11,9 | 20 | 1,14 | — 14 |
| 11,7 | 0 | 1,10 | — 5 |
Саморазряд – самопроизвольная потеря заряда отключенной батареи. Бывает нормальным и ускоренным. Интенсивность саморазряда зависит от устройства батареи и температуры окружающей среды.
Бывает нормальным и ускоренным. Интенсивность саморазряда зависит от устройства батареи и температуры окружающей среды.
При нормальном саморазряде батарея теряет 50 % заряженности за 6 месяцев – для обслуживаемых, 18 месяцев – для необслуживаемых.
Рисунок 20 – Интенсивность саморазряда АКБ
8. Техническое обслуживание аккумуляторных батарейВизуальный осмотр.
При проведении визуального осмотра особое внимание уделяют следующим факторам:
- Состояние моноблока. Поверхность моноблока притирают ветошью, смоченной в растворе кальцинированной соды или нашатырного спирта.
- Состояние полюсных выводов и клемм. Проверяют затяжку клемм, полюсные выводы смазывают техническим вазелином. При необходимости очищают полюсные выводы и наконечники проводов от окислов.
- Крепление батареи. Прижимная планка должна плотно прилегать к крепёжному выступу моноблока и заходить в фиксирующие выемки на нем.
При необходимости между ней и выступом следует установить переходную планку. Крепёжные болты следует затягивать моментом предписанной величины.
Крепёжные болты следует затягивать моментом предписанной величины.
Рисунок 21 – Щетка для очистки полюсных выводов
Измерение уровня электролита.
В батареях с прозрачным корпусом имеются отметки min/max, позволяющие оценить уровень электролита. В батареях с непрозрачным корпусом уровень электролита измеряют стеклянной трубкой диаметром Ø3-5 мм. Уровень электролита должен быть на 15-20 мм выше верхнего края пластин. Если уровень электролита ниже нормы, то в батарею добавляют дистиллированную воду, а если выше – отбирают излишки с помощью груши.
Измерение плотности электролита.
Для измерения плотности электролита используют следующие приборы: ареометр, денсиметр и плотномер. Плотность электролита позволяет оценить степень заряженности батареи. Уменьшение плотности на 0,01 г/см3 соответствует уменьшению заряженности на 6 %.
Если степень заряженности батареи составляет менее 75 % — то батарею можно эксплуатировать только в летнее время года, менее 50 % — эксплуатация запрещена.
Измерение напряжения батареи.
Для измерения напряжения батареи под нагрузкой используют нагрузочные вилки. Если напряжение в конце 5-ой секунды разряда превышает U=8,9 В, то батарея исправна (не имеет внутренних дефектов).
9. Неисправности автомобильных АКБК числу основных неисправностей АКБ относят:
- сульфатацию пластин,
- повреждение полюсных выводов,
- отстающие аккумуляторы,
- трещины в моноблоке,
- короткое замыкание,
- ускоренный саморазряд.
Под сульфатацией понимают такое состояние батареи, при котором она не заряжается при пропускании нормального зарядного тока в течение установленного промежутка времени.
Внешне проявляется наличием на поверхности крупных, трудно растворимых при заряде кристаллов или сплошного слоя сульфата свинца.
Рисунок 22 — Нормальная сульфатация
Рисунок 23 – Необратимая сульфатация
Сульфатация возникает в результате несоблюдения правил обслуживания и эксплуатации АКБ.
Сульфатация характеризуется следующими признаками:
- при заряде быстро повышается температура электролита;
- плотность электролита при заряде практически не повышается;
- газовыделение начинается значительно раньше;
- при контрольном разряде ёмкость значительно меньше номинальной.
Причины сульфатации:
- применение загрязнённого электролита;
- длительное нахождение батарей в разряженном состоянии;
- систематический недозаряд батарей;
- снижение уровня электролита ниже допустимого;
- эксплуатация батарей при недопустимо высокой температуре и плотности электролита.
Частичную сульфатацию можно устранить путем проведения контрольно-тренировочного цикла.
К числу внешних (определяемых визуально) неисправностей относят повреждения полюсных выводов и моноблока.
Трещины в моноблоке устраняют тепловой сваркой, а повреждение выводов путем наплавки.
Отстающие аккумуляторы.
Если в батарее хотя бы один аккумулятор будет разряжаться раньше остальных, то работоспособность батареи определяется именно этим, отстающим аккумулятором.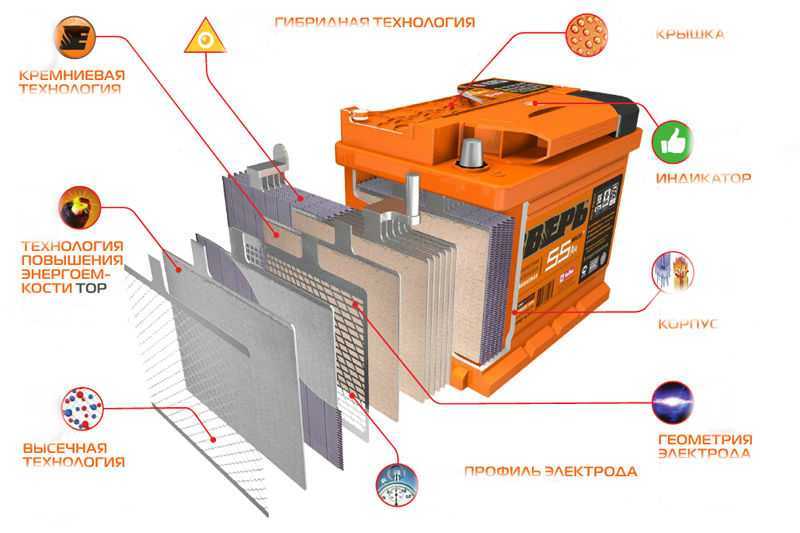
Для устранения подобной неисправности производят заряд батареи малым током в течение длительного времени (не менее 24 часов).
Короткое замыкание.
Внутренние короткие замыкание в аккумуляторах происходят между разноименными пластинами за счет заполнения наиболее крупных пор сепараторов активной массой («прорастание»).
Характерными признаками короткозамкнутого аккумулятора являются:
- отсутствие или очень малая величина ЭДС;
- непрерывное уменьшение плотности даже во время заряда;
- быстрая потеря ёмкости после заряда.
Ускоренный саморазряд.
Ускоренный саморазряд вызывается следующими основными причинами:
- наличие на поверхности батареи загрязнений, проводящих электрический ток;
- применение воды или электролита, содержащих вредные примеси;
- хранение батарей при повышенной температуре воздуха;
- чрезмерная эксплуатация батареи (в режиме такси).
 Техника безопасности при работе с АКБ
Техника безопасности при работе с АКБАккумуляторные батареи являются источниками повышенной опасности. Чтобы исключить возникновение опасных ситуаций, при работе с батареями необходимо следовать указаниям, которые приведены на их корпусах и в руководстве по эксплуатации автомобиля.
Необученный персонал, например, ученики или практиканты, могут привлекаться к работам с автомобильными батареями только под присмотром специалиста: механика, мастера или электрика.
Электролит обладает разъедающим действием. При неосторожном обращении с батареями возникает опасность поражения персонала кислотой. Поэтому необходимо иметь под рукой средства, противодействующие вредным воздействиям кислоты. К таким средствам, относится, например, раствор мыла.
Вылившийся из батареи электролит может привести к поражению кожи человека и к коррозионному повреждению деталей автомобиля. Среди этих деталей могут оказаться такие, которые существенно влияют на безопасность пассажиров.
При заряде батареи и некоторое время после него из электролита выделяется взрывоопасный гремучий газ. При особых обстоятельствах ненадлежащее обращение с батареей может привести к ее взрыву.
При особых обстоятельствах ненадлежащее обращение с батареей может привести к ее взрыву.
Вблизи батарей запрещается производить работы, сопровождающиеся парообразованием. К таким работам относятся шлифование, сварка, резка и т.п. Запрещено также курение. Помимо этого, следует исключить разряды статического электричества. Например, такой разряд можно предотвратить, если снять статическое электричество касанием кузова перед соприкосновением с батареей.
Все работы с батареями следует проводить в хорошо проветриваемых помещениях, приспособленных для этой цели. При работе с кислотой необходимо использовать индивидуальные средства защиты.
К этим средствам относятся:
- защитные очки;
- кислотоустойчивый фартук;
- кислотоустойчивые резиновые перчатки.
Чтобы исключить поражение глаз, защитные очки рекомендуется использовать при различных работах с батареями, например, при их транспортировке.
Если, несмотря на принятые меры предосторожности, электролит попал на кожу или в глаза, незамедлительно нужно оказать первую помощь пострадавшему.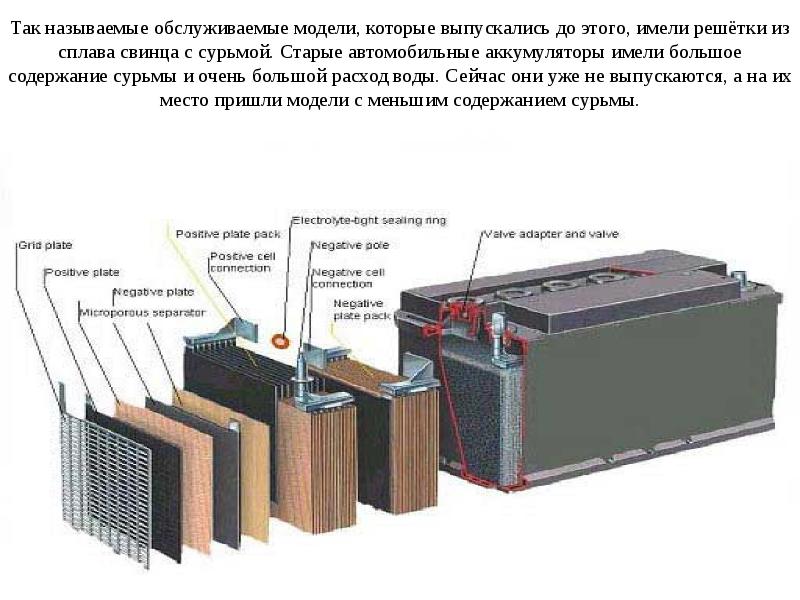
При этом нужно срочно нейтрализовать участки одежды и кожи мыльным раствором и затем тщательно промыть их в течение нескольких минут чистой водой. Попавшие в глаза брызги необходимо вымывать чистой водой в течение не менее 10 минут.
Для этой цели можно использовать приспособление для промывки глаз, которое подключается к водопроводу с питьевой водой. Желательно иметь место для подключения к водопроводу в мастерской вблизи помещения, где производится заряд батарей. В ином случае необходимо держать емкость для промывки глаз непосредственно на рабочем месте.
Эта емкость должна быть всегда заполнена водой, которую следует регулярно контролировать и заменять по гигиеническим соображениям. После оказания первой помощи в виде интенсивного промывания глаз или кожи следует в любом случае обратиться к врачу.
Рисунок 24 – Средства индивидуальной защиты
Просмотров: 154
принцип работы аккумуляторной батареи, устройство АКБ автомобиля, типы устройств
Независимые элементы питания сейчас стали одними из наиболее востребованных устройств, изобретённых людьми. Конструкция большинства гаджетов и их назначение часто предполагает отсутствие непрерывного доступа к электросети, поэтому и стали необходимыми такие устройства, как аккумуляторы. Они дают возможность пользоваться нужными приборами в любых требуемых условиях.
Конструкция большинства гаджетов и их назначение часто предполагает отсутствие непрерывного доступа к электросети, поэтому и стали необходимыми такие устройства, как аккумуляторы. Они дают возможность пользоваться нужными приборами в любых требуемых условиях.
Содержание
- Что называют аккумулятором
- Разряд элемента питания
- Цикл заряда батареи
- Типы соединения аккумуляторов
- Параллельное соединение
- Последовательный способ
- Типы источников тока
- Основные характеристики
- Устройство электродов
- Проводящее вещество
- Области применения АКБ
Что называют аккумулятором
Аккумулятором в самом общем значении этого понятия называется техническое приспособление, которое используется для накопления какого-либо вида энергии с целью её последующей равномерной отдачи в течение достаточно длительного периода времени (в отличие от конденсатора, который отдаёт накопленный заряд моментально). Конденсатор сохраняет непосредственно электрический заряд, в отличие от аккумулятора, который при зарядке преобразует электрическую энергию в энергию химической реакции, а когда будет работать под нагрузкой, превратит накопленную химическую энергию в электрическую.
Принцип работы аккумуляторной батареи заключается в том, что постоянно происходит химическая реакция между жидкостью-электролитом и металлическими пластинами-электродами. Единичные аккумуляторы очень слабы и не могут давать ток, достаточный для работы большинства устройств. Поэтому чаще всего они объединяются в аккумуляторные батареи, в которых используется последовательное или параллельное соединение отдельных элементов питания.
Разряд элемента питания
Конструкция подобных источников питания предполагает наличие двух клемм: плюса и минуса. Их работа происходит таким образом: при отсутствии нагрузки электрическая цепь разомкнута, а при подключении к полюсам какого-либо устройства цепь замыкается и начинается разрядка АКБ. Ток разряда, протекающий по батарее в таких условиях, возникает за счёт перемещения между электродами ионов: анионов и катионов.
Более подробно процесс разрядки батареи удобнее всего будет рассмотреть на конкретном примере.
Катод (положительный электрод в источнике тока) состоит из гидрата закиси никеля, в который для улучшения проводимости добавляется графитовый порошок.
Для изготовления анода (отрицательного электрода) в батареях такого типа применяются железные сетки с губчатым кадмием. Электролитом в таком устройстве будет смесь гидроксидов калия и лития. Оксид-гидроксид никеля в таком щелочном источнике питания вступает в химическое взаимодействие с атомами кадмия и молекулами воды. В результате такой реакции образуются гидроксиды кадмия и лития, а также выделяется электроэнергия.
Цикл заряда батареи
Для начала зарядки от клемм аккумулятора необходимо отключить нагрузку. На свободные клеммы батареи подаётся постоянный ток со значением напряжения большим, чем выходное напряжение заряжаемого устройства.
При осуществлении зарядки следует строго соблюдать полярность, то есть должны совпадать положительные и отрицательные контакты батареи и зарядного устройства. Важно учитывать, что устройство для зарядки необходимо выбирать с большей мощностью, чем сам аккумулятор, для того, чтобы преодолевать сопротивление оставшейся в нём энергии и производить электрический ток с направлением, противоположным току разряда. В результате обратимые химические реакции, протекающие в АКБ, поменяют своё направление.
Важно учитывать, что устройство для зарядки необходимо выбирать с большей мощностью, чем сам аккумулятор, для того, чтобы преодолевать сопротивление оставшейся в нём энергии и производить электрический ток с направлением, противоположным току разряда. В результате обратимые химические реакции, протекающие в АКБ, поменяют своё направление.
Для рассмотрения примера можно взять также никель-кадмиевую батарею. В реакцию вступают гидроксиды кадмия и никеля, образовавшиеся при цикле разряда. Продуктами этой реакции будут оксид-гидроксид никеля, вода и восстановленный кадмий.
Из всего вышесказанного следует, что во время рабочего цикла меняется только химический состав электродов. Электролит лишь создаёт требуемую для протекания реакций среду. С течением времени он может испаряться, что не самым лучшим образом скажется на продолжительности работы батареи. Рассмотренный принцип работы верен для любого типа аккумуляторов, будет изменяться только химический состав электродов и электролита.
Типы соединения аккумуляторов
Отдельные аккумулирующие элементы позволяют получать малые напряжение и силу тока. Например, чаще всего значение напряжения будет находиться в пределах 1−2 вольта. Для работы большинства устройств таких значений явно недостаточно. Чтобы повысить получаемое напряжение или силу тока, нужно устроить соединение аккумуляторов в батарею. Нужно подробнее остановиться на описании этих способов.
Параллельное соединение
Для соединения аккумулирующих элементов в батарею или нескольких АКБ требуется соединять их положительные клеммы с положительными, а отрицательные с отрицательными. К нагрузке присоединяются соединённые выводы всех элементов. При таком способе соединения напряжение в цепи будет таким же, как у каждой батареи по отдельности (если использовать батареи с одинаковым напряжением). А ёмкость станет равна сумме ёмкостей всех входящих в батарею элементов. Соответственно, вырастет и сила тока, которую такое устройство будет способно давать за определённый период до полной разрядки.
Последовательный способ
При использовании последовательного способа соединения АКБ следует связывать разнополярные контакты. Положительную клемму одного устройства соединяют с отрицательной клеммой другого, а электрическая схема подключается к свободным контактам первой и последней батарей. Итоговое выходное напряжение при применении такого вида соединения будет равняться сумме выходных напряжений всех задействованных источников электрического тока.
Например, чтобы получить АКБ с выходным напряжением двенадцать вольт, следует соединить последовательно четыре источника с напряжением три вольта или десяток аккумуляторов с выходным напряжением 1,2 вольта. Общая ёмкость собранных при помощи последовательного соединения АКБ будет равна ёмкости каждого аккумулятора по отдельности, то есть не изменится.
Типы источников тока
АКБ различаются по своему предназначению, характеристикам, тому как устроен аккумулятор и материалам, используемым при их изготовлении. На сегодняшний день в мире производится более трёх десятков типов различных аккумуляторов, основное различие между которыми заключается в химическом составе электродов, а также используемым видом электролита. Так, к примеру, в группу литий-ионных аккумуляторов входит двенадцать различных моделей. Наиболее популярными из всех производимых являются следующие типы:
Так, к примеру, в группу литий-ионных аккумуляторов входит двенадцать различных моделей. Наиболее популярными из всех производимых являются следующие типы:
- свинцово-кислотные;
- литиевые;
- никель-кадмиевые.
На них приходится значительная часть рынка элементов питания. Для лучшего представления о том, из каких материалов могут изготавливаться современные аккумуляторы стоит привести их полный список:
- железо;
- свинец;
- титан;
- литий;
- кадмий;
- кобальт;
- никель;
- цинк;
- ванадий;
- серебро;
- алюминий;
- целый ряд прочих металлов, которые, правда, используются крайне редко.
Применение при производстве различных материалов оказывает значительное влияние на итоговые эксплуатационные показатели и, как следствие, на область возможного использования. Например, литий-ионные АКБ часто устанавливаются в мобильные компьютеры и другие гаджеты.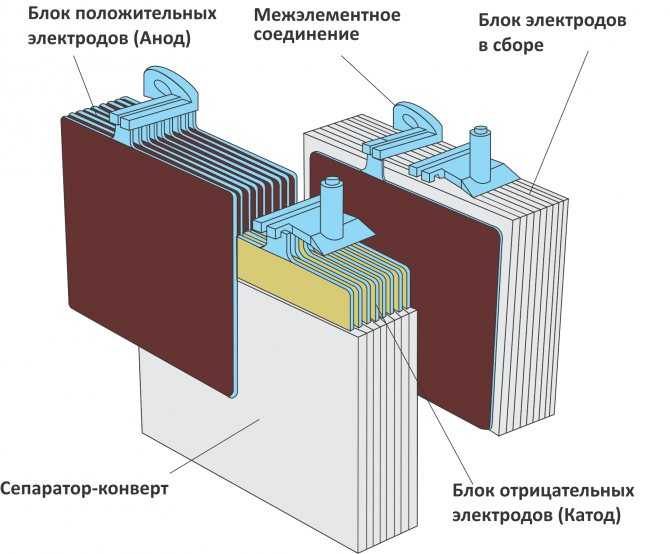
В то время как никель-кадмиевые аккумуляторы в основном используются как альтернатива простым одноразовым батарейкам. В теории аккумуляторные батареи любого типа могут сочетаться с любым устройством. Дело лишь в целесообразности и себестоимости производства.
Основные характеристики
Выше были рассмотрены материалы, применяющиеся при изготовлении перезаряжаемых элементов питания, основные принципы их работы и способы соединения. Теперь можно перейти к их эксплуатационным качествам. Важнейшими эксплуатационными характеристиками являются:
- Плотность энергии АКБ. Этот показатель равен отношению полного количества электроэнергии, которую аккумулятор способен отдать, к его массе или объёму.
- Ёмкостью называют максимальный отдаваемый аккумулятором заряд во течение цикла разрядки, до достижения минимального значения напряжения на клеммах. В метрической системе такая величина выражается в кулонах (Кл), но в повседневной жизни гораздо чаще применяется внесистемная единица ампер-час (Ah) или, для слабых элементов питания миллиампер-час.
 Также в некоторых случаях может использоваться показатель, называемый энергетической ёмкостью. Он выражается в джоулях (система СИ) или в ватт-часах. Ёмкость показывает прибор какой мощности и в течение какого времени может питаться от конкретной АКБ.
Также в некоторых случаях может использоваться показатель, называемый энергетической ёмкостью. Он выражается в джоулях (система СИ) или в ватт-часах. Ёмкость показывает прибор какой мощности и в течение какого времени может питаться от конкретной АКБ. - Температурный режим — диапазон значений температуры окружающей среды, в котором производитель рекомендует использование этого аккумулятора. При значительном отклонении от рекомендуемого изготовителем диапазона эксплуатационных температур, сильно возрастает вероятность того, что источник питания придёт в негодность. Это можно объяснить влиянием пониженных и повышенных температур на скорость течения химических реакций, а также на изменение давления внутри батареи.
- Саморазрядом АКБ называют потерю заряда, происходящую в заряженной батарее, при условии отсутствия нагрузки, подключённой к контактам. Величина этого показателя определяется, в основном, конструкцией батареи. Она может со временем возрастать из-за нарушения изоляции межу электродами по целому ряду причин.

Все эти параметры аккумуляторных батарей предоставляют наибольший интерес для конечного пользователя.
Устройство электродов
В качестве примера можно использовать свинцово-кислотную батарею. Каждая ячейка такого аккумулятора содержит пару электродов и разделительные пластины, которые изготовляются из пористого материала, не вступающего в химическое взаимодействие с кислотой. Такие пластины призваны препятствовать короткому замыканию погруженных в электролит электродов, и называются сепараторами.
Электроды в таких аккумуляторах выполняются в виде плоских свинцовых решёток. В ячейки таких решёток запрессовывается порошкообразная двуокись свинца (в пластинах-анодах) и металлический свинец в порошковой форме (в пластинах-катодах). Применение порошков обусловлено стремлением увеличить площадь поверхности раздела на границе электролит — электрод, что значительно повышает ёмкость такого источника тока.
Имеются экспериментальные образцы аккумуляторов, в которых свинцовые решётки замешены электродами, состоящими из сплетённых нитей углеволокна, которые покрываются тончайшим свинцовым напылением. Такая технология позволяет использовать значительно меньше свинца за счёт распределения его по большой площади, что делает аккумуляторную батарею не только миниатюрнее и легче, но и повышает её эффективность. КПД выше, чем у традиционных, а время зарядки сильно снижено.
Проводящее вещество
Пластины электродов и сепараторов опущены в электролит, в качестве которого в свинцово-кислотных аккумуляторах используется серная кислота, разведённая дистиллированной водой. Такая вода применяется для приготовления раствора потому, что она не оказывает влияния на кислотность среды. Проводимость получаемого таким образом раствора зависит лишь от концентрации серной кислоты и комнатных условиях будет максимальной при значении плотности жидкости-электролита в 1,23 грамма на кубический сантиметр.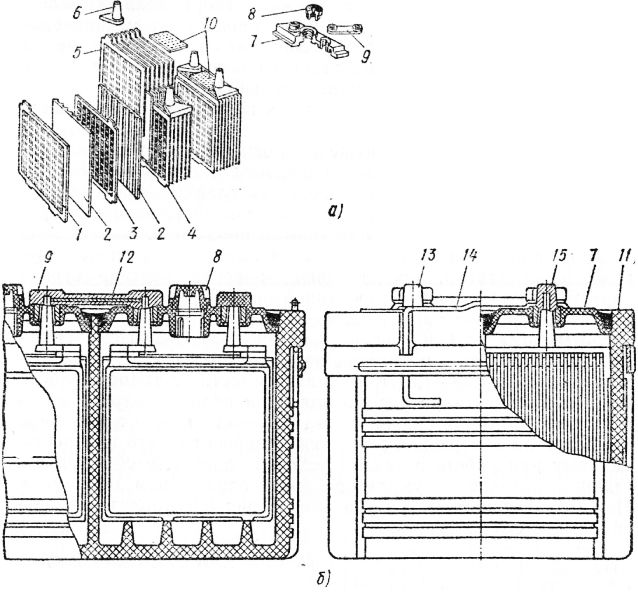
Проводимость электролита обратно пропорциональна внутреннему сопротивлению источника питания, и, соответственно, повышение проводимости снижает потери энергии и увеличивает КПД. Стоит отметить, что в областях холодного климата часто используют повышенные до 1,29−1,31 грамма на кубический сантиметр концентрации серной кислоты. Это делается для предотвращения замерзания электролита. Ведь образующийся лёд может повредить корпус аккумулятора.
В батареях, которые устанавливаются в бытовые источники бесперебойного питания, системы сигнализации и другие бытовые приборы, жидкий электролит иногда сгущается до состояния пасты раствором силиката натрия. Но принцип работы АКБ остаётся тем же.
Области применения АКБ
Аккумуляторные батареи получили широчайшее распространение во всех видах технических устройств. Без них не обходится ни одно портативное электронное устройство: от наручных часов до ноутбуков.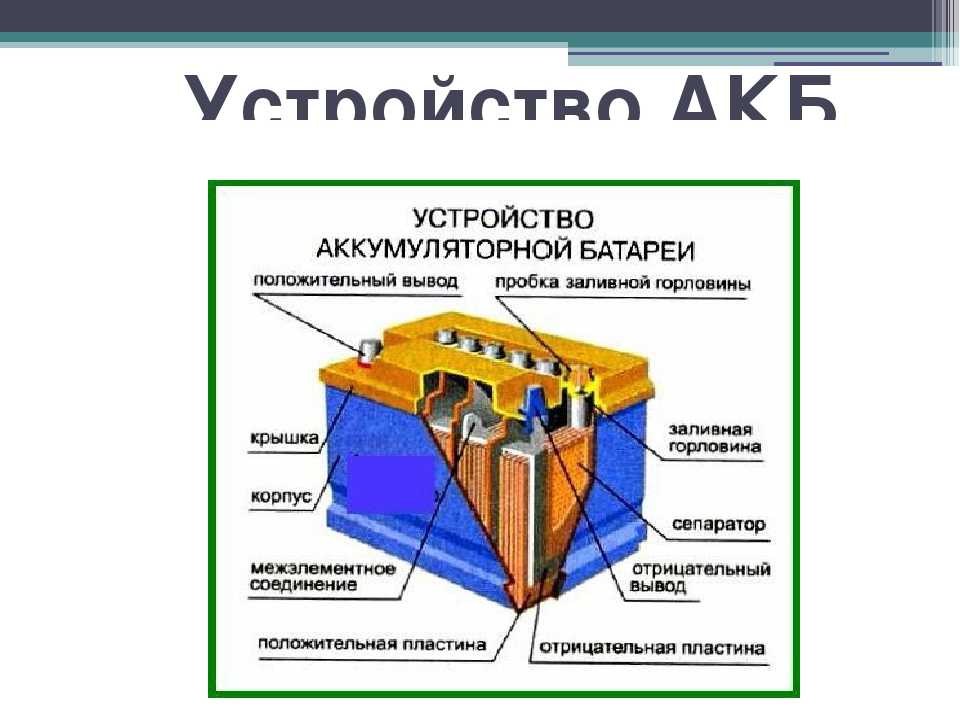 Даже в простых электрических фонарях производители предпочитают использовать встроенные АКБ вместо сменных элементов питания.
Даже в простых электрических фонарях производители предпочитают использовать встроенные АКБ вместо сменных элементов питания.
Не стали исключением и автомобили. В машинах привычных конструкций автомобильный аккумулятор используется для запуска двигателя и бесперебойного питания бортовой электрики и электроники. В набирающих всё большую популярность гибридных и электромобилях аккумуляторы играют ещё более важную роль. Причём в этом случае требования, предъявляемые к устройству АКБ автомобиля, ещё выше.
Крайне важны такие параметры: ток запуска, глубина разряда и максимальное количество циклов перезарядки, которое способен выдержать аккумулятор. Можно смело утверждать, что современный образ жизни был бы невозможен без аккумуляторных батарей.
Химия аккумуляторов — Дизайн аккумуляторов
Основы химии аккумуляторов или, точнее, электрохимия. Это катод, анод и электролит. Что это такое, кто их производит, что будет дальше в плане развития, каковы последние исследования и каковы плюсы и минусы каждого из них.
Основные химические вещества:
Алюминий Воздух
Высокая плотность энергии и низкая стоимость. Алюминиевый анод и воздушный катод вместе с водным электролитом вырабатывают энергию за счет окисления алюминия кислородом воздуха. Однако серьезной проблемой является коррозия алюминиевого анода, что снижает емкость и сокращает календарный срок службы.
Ион алюминия
Металлический алюминиевый анод может обмениваться тремя электронами во время электрохимического процесса, следовательно, может обеспечивать высокую теоретически высокую объемную и гравиметрическую емкость. Однако требуется разработка анода, катода и электролита, прежде чем этот тип элемента сможет использовать высокую плотность энергии со стабильностью в течение срока службы циклов.
Dual-Ion
Аккумуляторная технология, предлагающая недорогое решение для сетевого хранения. Катионы и анионы участвуют в процессах интеркаляции и деинтеркаляции с использованием графита в качестве материала катода и анода.
Fluoride-Ion
Рассматривается как замена литиевой и, возможно, постлитиевой технологии с «до 7-кратным увеличением Втч/кг» текущей литиевой технологии.
Свинцово-кислотный
Свинцово-кислотный аккумулятор представляет собой аккумулятор с электродами из оксида свинца и металлического свинца, которые разделены электролитом из серной кислоты. Энергоемкость 40-60 Втч/кг.
Lithium Air
Обещанная ионно-литиевая технология с непревзойденной плотностью энергии. Однако, несмотря на то, что было предпринято огромное количество научных усилий для понимания химии и реакций, на данном этапе она еще недостаточно развита, чтобы превратиться в работоспособную батарею. Во всяком случае, акцент сместился на твердотельные литий-ионные аккумуляторы.
Литий-ионный
В перезаряжаемой ионно-литиевой батарее ионы лития перемещаются от отрицательного электрода к положительному во время разрядки и обратно при зарядке. Текущие производственные ячейки имеют плотность энергии ~ 280 Втч / кг.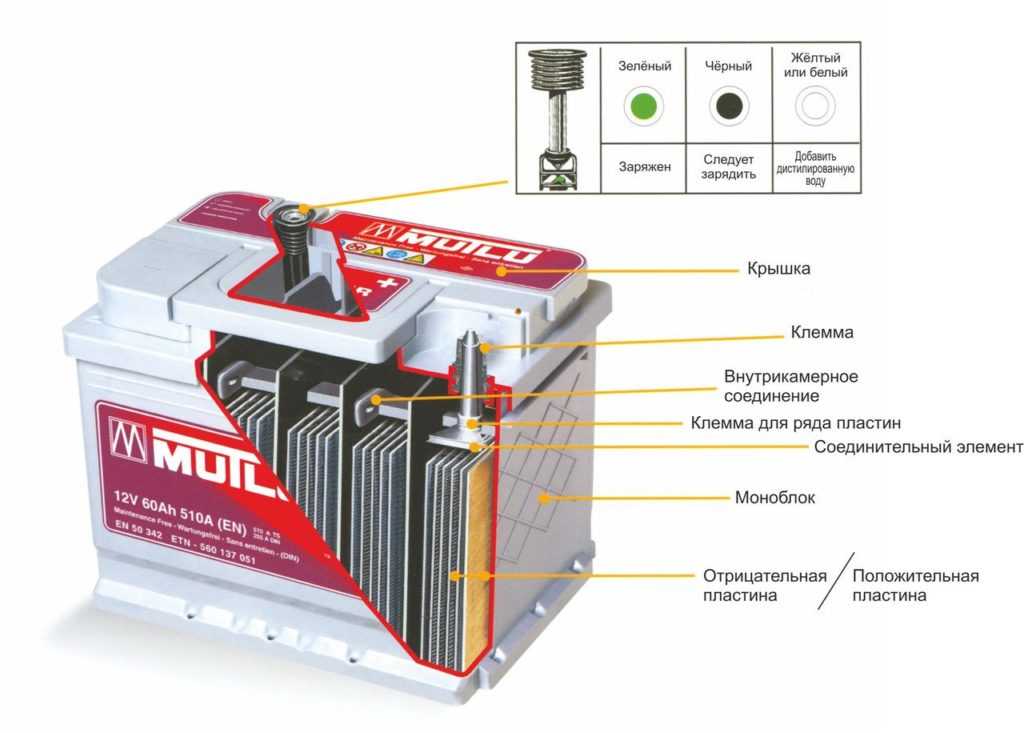
Катод представляет собой оксид лития из переходного металла, например, марганец или кобальт, или комбинацию переходных металлов: LCO, LMO, NCA, NMC, LFP, LMFP. Анод обычно представляет собой материал на основе графита, который может интеркалировать или выделять литий, он может содержать процент кремния для увеличения емкости. В качестве альтернативы анодом может быть титанат лития (LTO).
Lithium Sulfur
Возможно, наиболее зрелый химический состав литий-ионных аккумуляторов с потенциальной плотностью энергии >600 Втч/кг. Также с возможностью существенного снижения затрат и повышения безопасности. Тем не менее, ряд проблем означает, что срок службы цикла был плохим. Поэтому потенциал привлекает внимание и столь необходимые исследования на этапе фундаментальной химии.
Magnesium-Ion
Функция очень похожа на литий-ионные батареи, сравнимая плотность энергии с литий-ионными батареями, а также потенциал для улучшения, поскольку на каждый отдельный ион магния приходится вдвое больше электронов. Магния больше, чем лития. Однако возможных побочных реакций с ионом магния намного больше.
Магния больше, чем лития. Однако возможных побочных реакций с ионом магния намного больше.
Никель-кадмий
Перезаряжаемая батарея, в которой в качестве электродов используется гидроксид оксида никеля и металлический кадмий.
Никель-металлогидридный аккумулятор
Никель-металлогидридный аккумулятор имеет катод из гидроксида никеля, анод из гидрида металла (используются различные металлические сплавы) и электролит на основе водного раствора гидроксида калия. Это химия перезаряжаемой батареи, которая была заменена ионно-литиевой, но нашла широкое применение в гибридах Toyota. Плотность энергии 40-110 Втч/кг на уровне ячейки.
Ион калия
Потенциал может быть недорогой химией, основанной на хранении, но большое большое изменение ~60% графита с введением ионов К создает высокую нагрузку на решетку и, таким образом, ограничивает циклирование. Развитие технологий отстает от аккумуляторов на основе лития и натрий-иона.
Натрий-ион
Аналогичен литий-ионному аккумулятору, но с использованием ионов натрия (Na+) в качестве носителей заряда. Работа химического состава на основе натрия и конструкция элемента почти идентичны работе коммерчески распространенных типов литий-ионных аккумуляторов, но вместо соединений лития используются соединения натрия.
Работа химического состава на основе натрия и конструкция элемента почти идентичны работе коммерчески распространенных типов литий-ионных аккумуляторов, но вместо соединений лития используются соединения натрия.
Твердотельный
Любая аккумуляторная технология, в которой используются твердые электроды и твердый электролит. Это предлагает потенциальные улучшения плотности энергии и безопасности, но имеет очень серьезные проблемы с цикличностью, производством и долговечностью твердого сэндвича.
Цинк-Воздух
Пожалуй, самая многообещающая технология металл-воздушных батарей. Обычно он имеет цинковый анод, проницаемый для кислорода катод, сепаратор и едкий щелочной электролит. Перспективная низкая стоимость, высокая стабильность и высокая плотность энергии.
Ссылки
- Jianmin Ma et al, «Дорожная карта аккумуляторных технологий на 2021 год» , 2021 J. Phys. Д: заявл. физ. 54 183001
Разработка лучших аккумуляторов для электромобилей | Новости Массачусетского технологического института
Настоятельная необходимость сократить выбросы углерода побуждает к быстрому переходу к электрифицированной мобильности и расширенному использованию солнечной и ветровой энергии в электрической сети. Если эти тенденции будут усиливаться, как ожидается, потребность в более совершенных методах хранения электроэнергии возрастет.
Если эти тенденции будут усиливаться, как ожидается, потребность в более совершенных методах хранения электроэнергии возрастет.
«Нам нужны все стратегии, которые мы можем получить, чтобы противостоять угрозе изменения климата», — говорит Эльза Оливетти, доктор философии 2007 года, адъюнкт-профессор Эстер и Гарольда Э. Эдгертон в области материаловедения и инженерии. «Очевидно, что разработка технологий для хранения на основе сетки в больших масштабах имеет решающее значение. Но для мобильных приложений — в частности, для транспорта — многие исследования сосредоточены на адаптации сегодняшней литий-ионной батареи, чтобы сделать ее более безопасной, компактной и способной хранить больше энергии для своего размера и веса».
Традиционные литий-ионные аккумуляторы продолжают совершенствоваться, но у них есть ограничения, которые сохраняются, отчасти из-за их структуры. Литий-ионный аккумулятор состоит из двух электродов — положительного и отрицательного — зажатых вокруг органической (углеродсодержащей) жидкости. Когда батарея заряжается и разряжается, электрически заряженные частицы (или ионы) лития проходят от одного электрода к другому через жидкий электролит.
Когда батарея заряжается и разряжается, электрически заряженные частицы (или ионы) лития проходят от одного электрода к другому через жидкий электролит.
Одна из проблем этой конструкции заключается в том, что при определенных напряжениях и температурах жидкий электролит может стать летучим и загореться. «Батарейки, как правило, безопасны при нормальном использовании, но риск все же существует», — говорит Кевин Хуанг, доктор философии 15 года, научный сотрудник группы Оливетти.
Другая проблема заключается в том, что литий-ионные аккумуляторы не подходят для использования в транспортных средствах. Большие и тяжелые аккумуляторные батареи занимают место и увеличивают общий вес автомобиля, снижая эффективность использования топлива. Но сделать современные литий-ионные батареи меньше и легче, сохраняя при этом их плотность энергии, то есть количество энергии, которое они хранят на грамм веса, оказывается непросто.
Чтобы решить эти проблемы, исследователи меняют ключевые характеристики литий-ионной батареи, чтобы сделать ее полностью твердотельной или «твердотельной» версией. Они заменяют жидкий электролит в середине тонким твердым электролитом, который стабилен в широком диапазоне напряжений и температур. С этим твердым электролитом они используют положительный электрод большой емкости и отрицательный электрод большой емкости из металлического лития, который намного тоньше, чем обычный слой пористого углерода. Эти изменения позволяют значительно уменьшить общую емкость батареи, сохранив при этом ее емкость для накопления энергии, тем самым достигнув более высокой плотности энергии.
Они заменяют жидкий электролит в середине тонким твердым электролитом, который стабилен в широком диапазоне напряжений и температур. С этим твердым электролитом они используют положительный электрод большой емкости и отрицательный электрод большой емкости из металлического лития, который намного тоньше, чем обычный слой пористого углерода. Эти изменения позволяют значительно уменьшить общую емкость батареи, сохранив при этом ее емкость для накопления энергии, тем самым достигнув более высокой плотности энергии.
«Эти функции — повышенная безопасность и большая плотность энергии — вероятно, являются двумя наиболее часто рекламируемыми преимуществами потенциальной твердотельной батареи», — говорит Хуанг. Затем он быстро поясняет, что «все эти вещи являются перспективными, ожидаемыми и не обязательно реализованными». Тем не менее, многие исследователи изо всех сил пытаются найти материалы и конструкции, которые могут выполнить это обещание.
Думая за пределами лаборатории
Исследователи придумали много интригующих вариантов, которые выглядят многообещающе — в лаборатории. Но Оливетти и Хуанг считают, что дополнительные практические соображения могут быть важны, учитывая безотлагательность проблемы изменения климата. «Всегда есть показатели, которые мы, исследователи, используем в лаборатории для оценки возможных материалов и процессов», — говорит Оливетти. Примеры могут включать емкость накопителя энергии и скорость зарядки/разрядки. При проведении фундаментальных исследований, которые она считает необходимыми и важными, эти показатели уместны. «Но если целью является внедрение, мы предлагаем добавить несколько показателей, специально учитывающих возможности быстрого масштабирования», — говорит она.
Но Оливетти и Хуанг считают, что дополнительные практические соображения могут быть важны, учитывая безотлагательность проблемы изменения климата. «Всегда есть показатели, которые мы, исследователи, используем в лаборатории для оценки возможных материалов и процессов», — говорит Оливетти. Примеры могут включать емкость накопителя энергии и скорость зарядки/разрядки. При проведении фундаментальных исследований, которые она считает необходимыми и важными, эти показатели уместны. «Но если целью является внедрение, мы предлагаем добавить несколько показателей, специально учитывающих возможности быстрого масштабирования», — говорит она.
Основываясь на отраслевом опыте работы с современными литий-ионными батареями, исследователи из Массачусетского технологического института и их коллега Гербранд Седер, заслуженный профессор инженерии Дэниела М. Теллепа Калифорнийского университета в Беркли, предлагают три общих вопроса, которые могут помочь определить потенциальные ограничения на будущее масштабирование в результате выбора материалов. Во-первых, с такой конструкцией батареи могут ли доступность материалов, цепочки поставок или волатильность цен стать проблемой при расширении производства? (Обратите внимание, что экологические и другие проблемы, связанные с расширением добычи, выходят за рамки этого исследования.) Во-вторых, будет ли изготовление батарей из этих материалов включать в себя сложные производственные этапы, во время которых детали могут выйти из строя? И, в-третьих, производственные меры, необходимые для обеспечения высокопроизводительного продукта на основе этих материалов, в конечном итоге снижают или повышают стоимость производимых аккумуляторов?
Во-первых, с такой конструкцией батареи могут ли доступность материалов, цепочки поставок или волатильность цен стать проблемой при расширении производства? (Обратите внимание, что экологические и другие проблемы, связанные с расширением добычи, выходят за рамки этого исследования.) Во-вторых, будет ли изготовление батарей из этих материалов включать в себя сложные производственные этапы, во время которых детали могут выйти из строя? И, в-третьих, производственные меры, необходимые для обеспечения высокопроизводительного продукта на основе этих материалов, в конечном итоге снижают или повышают стоимость производимых аккумуляторов?
Чтобы продемонстрировать свой подход, Olivetti, Ceder и Huang изучили некоторые химические составы электролитов и структуры батарей, которые в настоящее время изучаются исследователями. Чтобы выбрать свои примеры, они обратились к предыдущей работе, в которой они и их сотрудники использовали методы анализа текста и данных для сбора информации о материалах и деталях обработки, описанных в литературе. Из этой базы данных они выбрали несколько часто упоминаемых вариантов, которые представляют собой ряд возможностей.
Из этой базы данных они выбрали несколько часто упоминаемых вариантов, которые представляют собой ряд возможностей.
Материалы и наличие
В мире твердых неорганических электролитов существует два основных класса материалов — оксиды, содержащие кислород, и сульфиды, содержащие серу. Olivetti, Ceder и Huang сосредоточились на одном многообещающем варианте электролита в каждом классе и рассмотрели ключевые элементы, вызывающие озабоченность для каждого из них.
Сульфидом, который они рассматривали, был LGPS, который объединяет литий, германий, фосфор и серу. Исходя из соображений доступности, они сосредоточились на германии, элементе, который вызывает опасения отчасти потому, что он обычно не добывается сам по себе. Вместо этого это побочный продукт, получаемый при добыче угля и цинка.
Чтобы выяснить его доступность, исследователи изучили, сколько германия ежегодно производилось за последние шесть десятилетий при добыче угля и цинка, а затем сколько можно было произвести. Результат показал, что даже в последние годы можно было произвести в 100 раз больше германия. Учитывая этот потенциал предложения, доступность германия вряд ли будет ограничивать масштабирование твердотельной батареи на основе электролита LGPS.
Результат показал, что даже в последние годы можно было произвести в 100 раз больше германия. Учитывая этот потенциал предложения, доступность германия вряд ли будет ограничивать масштабирование твердотельной батареи на основе электролита LGPS.
Ситуация выглядела менее многообещающе с выбранным исследователями оксидом LLZO, который состоит из лития, лантана, циркония и кислорода. Добыча и переработка лантана в основном сосредоточены в Китае, и доступные данные ограничены, поэтому исследователи не пытались анализировать его доступность. Остальные три элемента доступны в изобилии. Однако на практике необходимо добавить небольшое количество другого элемента, называемого легирующей добавкой, чтобы облегчить обработку LLZO. Поэтому команда сосредоточилась на тантале, наиболее часто используемой легирующей примеси, как на главном элементе, вызывающем озабоченность в LLZO.
Тантал производится как побочный продукт добычи олова и ниобия. Исторические данные показывают, что количество тантала, полученного при добыче олова и ниобия, было гораздо ближе к потенциальному максимуму, чем в случае с германием. Таким образом, доступность тантала больше беспокоит возможное масштабирование батареи на основе LLZO.
Таким образом, доступность тантала больше беспокоит возможное масштабирование батареи на основе LLZO.
Но знание о наличии элемента в земле не относится к шагам, необходимым для доставки его производителю. Поэтому исследователи исследовали дополнительный вопрос, касающийся цепочек поставок критически важных элементов — добычи, переработки, переработки, доставки и так далее. Предполагая, что имеются обильные запасы, могут ли цепочки поставок, которые доставляют эти материалы, расширяться достаточно быстро, чтобы удовлетворить растущий спрос на батареи?
В ходе выборочного анализа они рассмотрели, насколько цепочки поставок германия и тантала должны будут расти из года в год, чтобы обеспечивать батареями планируемый парк электромобилей в 2030 году. Например, парк электромобилей часто называют целью к 2030 году потребуется произвести достаточное количество батарей, чтобы вырабатывать в общей сложности 100 гигаватт-часов энергии. Чтобы достичь этой цели, используя только батареи LGPS, цепочка поставок германия должна будет расти на 50 процентов из года в год — натяжка, поскольку максимальный темп роста в прошлом составлял около 7 процентов. Используя только батареи LLZO, цепочка поставок тантала должна вырасти примерно на 30 процентов — темпы роста намного превышают исторический максимум примерно в 10 процентов.
Используя только батареи LLZO, цепочка поставок тантала должна вырасти примерно на 30 процентов — темпы роста намного превышают исторический максимум примерно в 10 процентов.
Эти примеры демонстрируют важность учета доступности материалов и цепочек поставок при оценке различных твердых электролитов с точки зрения их потенциала масштабирования. «Даже когда количество доступного материала не вызывает беспокойства, как в случае с германием, масштабирование всех этапов цепочки поставок в соответствии с будущим производством электромобилей может потребовать буквально беспрецедентных темпов роста», — говорит Хуанг. .
Материалы и обработка
При оценке потенциала масштабирования конструкции батареи следует учитывать еще один фактор — сложность производственного процесса и то, как он может повлиять на стоимость. Изготовление твердотельной батареи неизбежно включает в себя множество этапов, и сбой на любом этапе увеличивает стоимость каждой успешно произведенной батареи.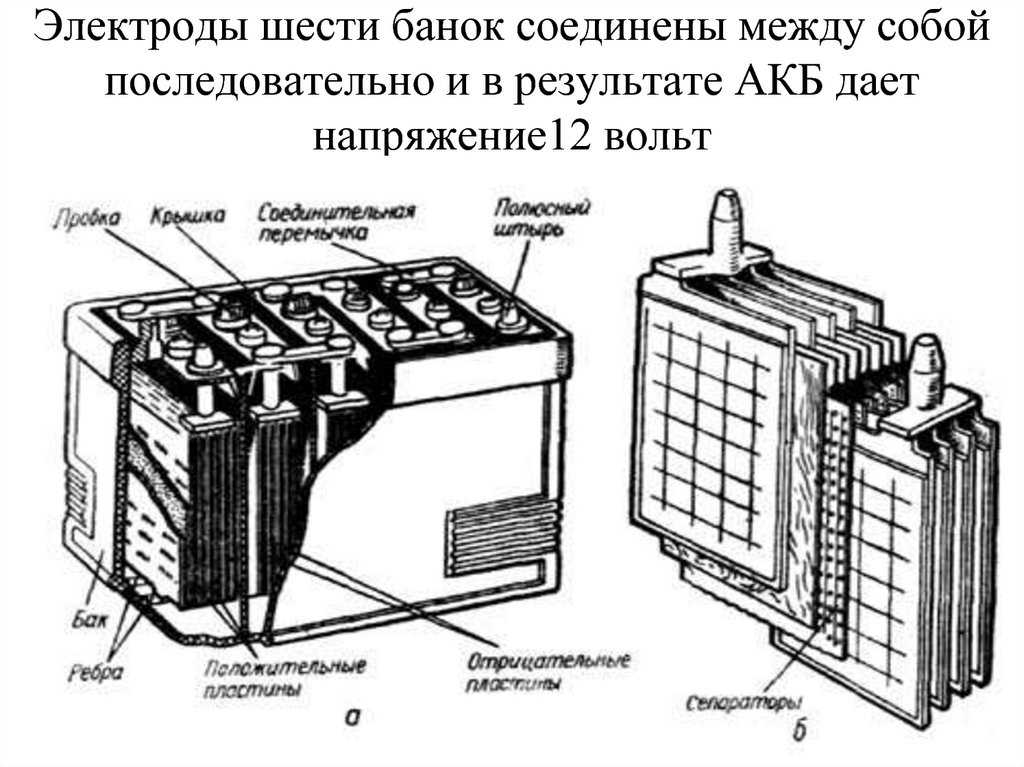 Как объясняет Хуанг: «Вы не отправляете неисправные аккумуляторы; ты их выбрасываешь. Но вы все равно потратили деньги на материалы, время и обработку».
Как объясняет Хуанг: «Вы не отправляете неисправные аккумуляторы; ты их выбрасываешь. Но вы все равно потратили деньги на материалы, время и обработку».
В качестве показателя сложности производства Olivetti, Ceder и Huang изучили влияние частоты отказов на общую стоимость выбранных конструкций твердотельных батарей в своей базе данных. В одном примере они сосредоточились на оксиде LLZO. LLZO чрезвычайно хрупок, и при высоких температурах, связанных с производством, большой лист, достаточно тонкий для использования в высокопроизводительной твердотельной батарее, может треснуть или деформироваться.
Чтобы определить влияние таких отказов на стоимость, они смоделировали четыре ключевых этапа сборки аккумуляторов на основе LLZO. На каждом этапе они рассчитывали стоимость на основе предполагаемого выхода — то есть доли от общего числа единиц, которые были успешно обработаны без сбоев. У LLZO выход был намного ниже, чем у других исследованных ими конструкций; и по мере того, как доходность снижалась, стоимость каждого киловатт-часа (кВтч) энергии батареи значительно росла. Например, когда на последнем этапе нагрева катода вышли из строя еще 5 % блоков, стоимость увеличилась примерно на 30 долларов за кВтч — нетривиальное изменение, учитывая, что общепринятая целевая стоимость таких батарей составляет 100 долларов за кВтч. Ясно, что производственные трудности могут оказать сильное влияние на жизнеспособность конструкции для широкомасштабного внедрения.
Например, когда на последнем этапе нагрева катода вышли из строя еще 5 % блоков, стоимость увеличилась примерно на 30 долларов за кВтч — нетривиальное изменение, учитывая, что общепринятая целевая стоимость таких батарей составляет 100 долларов за кВтч. Ясно, что производственные трудности могут оказать сильное влияние на жизнеспособность конструкции для широкомасштабного внедрения.
Материалы и характеристики
Одна из основных проблем при проектировании полностью твердотельной батареи связана с «интерфейсами», то есть где один компонент встречается с другим. Во время производства или эксплуатации материалы на этих границах раздела могут стать нестабильными. «Атомы начинают перемещаться туда, куда не должны, и производительность батареи снижается», — говорит Хуанг.
В результате большое количество исследований посвящено поиску методов стабилизации интерфейсов в батареях различных конструкций. Многие из предложенных методов действительно повышают производительность; и в результате стоимость батареи в долларах за кВтч снижается. Но реализация таких решений, как правило, требует дополнительных материалов и времени, что увеличивает стоимость кВтч при крупномасштабном производстве.
Но реализация таких решений, как правило, требует дополнительных материалов и времени, что увеличивает стоимость кВтч при крупномасштабном производстве.
Чтобы проиллюстрировать этот компромисс, исследователи сначала исследовали свой оксид LLZO. Здесь цель состоит в том, чтобы стабилизировать поверхность раздела между электролитом LLZO и отрицательным электродом, вставив между ними тонкий слой олова. Они проанализировали влияние — как положительное, так и отрицательное — на стоимость внедрения этого решения. Они обнаружили, что добавление сепаратора олова увеличивает емкость накопления энергии и улучшает производительность, что снижает удельную стоимость в долларах/кВтч. Но стоимость включения слоя олова превышает экономию, так что окончательная стоимость выше первоначальной стоимости.
В другом анализе они рассмотрели сульфидный электролит под названием LPSCl, который состоит из лития, фосфора и серы с небольшим добавлением хлора. В этом случае положительный электрод включает в себя частицы материала электролита — метод обеспечения того, чтобы ионы лития могли найти путь через электролит к другому электроду. Однако добавленные частицы электролита несовместимы с другими частицами в положительном электроде — еще одна проблема интерфейса. В этом случае стандартным решением является добавление «связующего», другого материала, который заставляет частицы склеиваться.
Однако добавленные частицы электролита несовместимы с другими частицами в положительном электроде — еще одна проблема интерфейса. В этом случае стандартным решением является добавление «связующего», другого материала, который заставляет частицы склеиваться.
Их анализ подтвердил, что без связующего вещества производительность низкая, а стоимость батареи на основе LPSCl превышает 500 долларов США за кВтч. Добавление связующего значительно повышает производительность, а стоимость снижается почти на 300 долларов за кВтч. В этом случае стоимость добавления связующего во время изготовления настолько низка, что по существу реализуется все снижение стоимости от добавления связующего. Здесь метод, реализованный для решения проблемы интерфейса, окупается меньшими затратами.
Исследователи провели аналогичные исследования других многообещающих твердотельных батарей, о которых сообщалось в литературе, и их результаты были последовательными: выбор материалов батареи и процессов может повлиять не только на краткосрочные результаты в лаборатории, но также на осуществимость и стоимость производство предлагаемой твердотельной батареи в масштабе, необходимом для удовлетворения будущего спроса. Результаты также показали, что рассмотрение всех трех факторов вместе — доступности, потребностей в обработке и производительности батареи — важно, поскольку могут иметь место коллективные эффекты и компромиссы.
Результаты также показали, что рассмотрение всех трех факторов вместе — доступности, потребностей в обработке и производительности батареи — важно, поскольку могут иметь место коллективные эффекты и компромиссы.
Оливетти гордится широким кругом проблем, которые может исследовать подход команды. Но она подчеркивает, что это не предназначено для замены традиционных показателей, используемых для выбора материалов и обработки в лаборатории. «Вместо этого он призван дополнить эти показатели, также широко рассматривая вещи, которые могут помешать масштабированию» — важное соображение, учитывая то, что Хуан называет «срочным тиканьем часов» чистой энергии и изменения климата.
Это исследование было поддержано Программой посевного фонда Энергетической инициативы Массачусетского технологического института (MITEI) Центр низкоуглеродной энергетики для хранения энергии; компанией Shell, одним из основателей MITEI; и Управлением по энергоэффективности и возобновляемым источникам энергии Министерства энергетики США, Управлением транспортных технологий в рамках Программы перспективных исследований аккумуляторных материалов. Работа по анализу текста поддерживалась Национальным научным фондом, Управлением военно-морских исследований и MITEI.
Работа по анализу текста поддерживалась Национальным научным фондом, Управлением военно-морских исследований и MITEI.
Эта статья опубликована в весеннем выпуске 2021 года Energy Futures , журнала MIT Energy Initiative.
Понимание, проектирование и оптимизация аккумуляторных систем
Литий-ионные аккумуляторы
В модуле проектирования аккумуляторов представлены самые современные модели литий-ионных аккумуляторов. Вы найдете различные механизмы старения и высокоточные модели, такие как модель Ньюмана, доступные в 1D, 2D и полном 3D. Помимо самостоятельного моделирования электрохимических реакций, вы можете комбинировать их с теплообменом и учитывать структурные напряжения и деформации, вызванные расширением и сжатием в результате интеркаляции лития. Модуль также предоставляет функциональные возможности для настройки гетерогенных моделей, описывающих фактические формы пористого электролита и электродных частиц.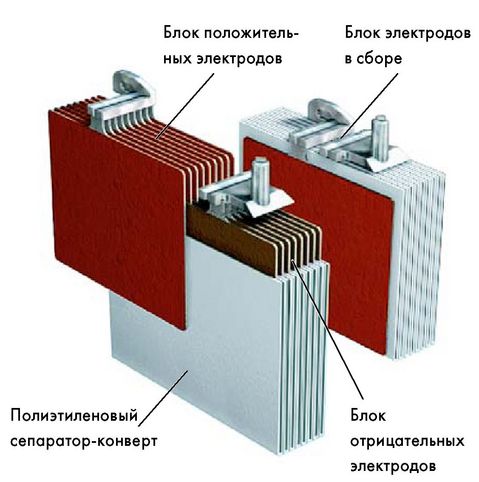 Изучение микроструктуры батареи помогает глубже понять ее характеристики.
Изучение микроструктуры батареи помогает глубже понять ее характеристики.
Свинцово-кислотные батареи
Для моделирования свинцово-кислотных батарей программа включает зависимые переменные для ионного потенциала и состава электролита, а также электрического потенциала и пористости твердых электродов. Модель учитывает растворение и отложение твердых веществ. Встроенные функции позволяют также изучить, как различные конструктивные параметры влияют на производительность батареи, такие как толщина и геометрия электродов и сепараторов, геометрия токосъемников и фидеров и многое другое.
Generic Batteries
«Рабочая лошадка» модуля проектирования батарей — это подробная модель отдельных элементов батареи с положительным электродом, отрицательным электродом и сепаратором. С помощью общего описания пористых электродов вы можете определить любое количество конкурирующих реакций в электроде, а также связать их с электролитом произвольного состава. Модуль позволяет описать пористый электролит и электролит в сепараторе любого состава с помощью теории концентрированных, разбавленных (уравнения Нернста-Планка) и фоновых электролитов в сочетании с теорией пористого электрода.
Модуль позволяет описать пористый электролит и электролит в сепараторе любого состава с помощью теории концентрированных, разбавленных (уравнения Нернста-Планка) и фоновых электролитов в сочетании с теорией пористого электрода.
Что можно моделировать с помощью модуля проектирования батарей
Выполнение различных электрохимических анализов батарей с помощью программного обеспечения COMSOL ® .
Гетерогенные и гомогенные модели
Моделирование подробной структуры пористых электродов и пористого электролита для типового элементарного элемента батареи.
Рост границы твердого электролита (SEI)
Моделирование старения отрицательного графитового электрода литий-ионной батареи.
Напряжение, вызванное диффузией
Вычислить интеркаляционные напряжения и деформации, вызванные расширением и сжатием. 1
Короткое замыкание
Исследование внутреннего короткого замыкания батареи.
Pseudo-Dimension
Моделирование интеркаляции лития в частицы электрода.
Двухслойная емкость
Модели электрохимических конденсаторов и наноэлектродов.
Аккумуляторы NiMH и NiCd
Аккумуляторы модели с бинарными щелочными (1:1) электролитами.
Flow Batteries
Моделирование проточных свинцово-кислотных и ванадиевых аккумуляторов во время приложенного цикла зарядки-разрядки.
Металлическое покрытие
Укажите емкость узла электрода, чтобы избежать металлического литиевого покрытия во время высокоскоростной зарядки.
Эффекты пористости
Моделирование химических реакций под влиянием переноса частиц в пористой среде.
Спектроскопия импеданса
Изучение гармонического отклика батареи с использованием моделей высокой точности, основанных на физике.
Сосредоточенные модели с оценкой параметров
Определите упрощенную модель батареи на основе небольшого набора сосредоточенных параметров, которые соответствуют результатам высокоточных моделей экспериментальным результатам.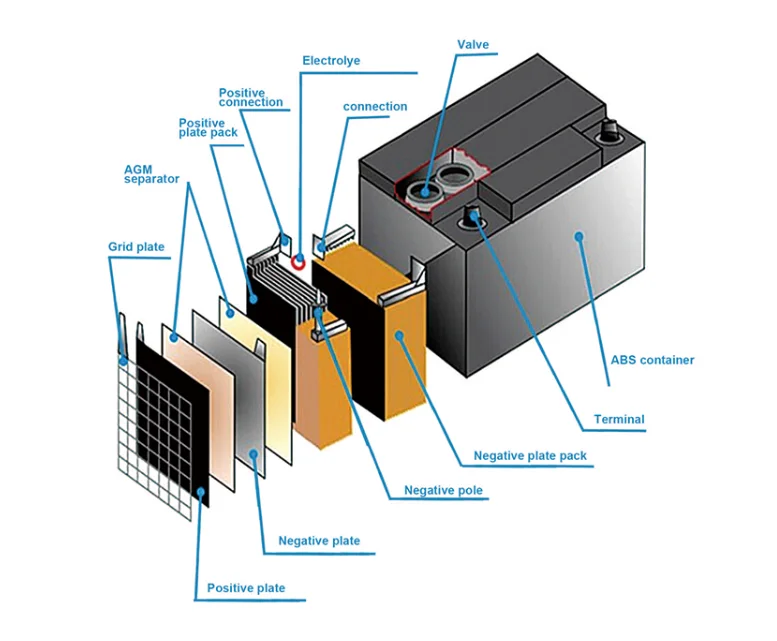 2
2
Особенности и функциональные возможности модуля проектирования аккумуляторов
Модуль проектирования аккумуляторов предлагает набор специализированных инструментов для имитации работы аккумуляторов в различных условиях эксплуатации.
Упрощенное моделирование аккумуляторов
Для более быстрого теплового анализа трехмерных аккумуляторных блоков можно использовать проверенные сосредоточенные (упрощенные) модели для каждого аккумулятора в аккумуляторном блоке. После проверки сосредоточенные модели могут давать превосходную точность в определенном диапазоне операций. Модуль проектирования батарей содержит сосредоточенные модели, основанные на физике и решающие электрохимические уравнения в нескольких пространственных измерениях.
Интерфейс Single Particle Battery моделирует распределение заряда в аккумуляторе с использованием отдельной одночастичной модели для положительного и отрицательного электродов аккумулятора. Интерфейс Lumped Battery использует небольшой набор параметров с сосредоточенными параметрами для добавления вкладов в сумму всех потерь напряжения в батарее, происходящих от омических сопротивлений и, опционально, процессов переноса заряда и диффузии. Кроме того, вы можете определить модель батареи на основе произвольного количества элементов электрической цепи с помощью Интерфейс эквивалентной цепи батареи .
Интерфейс Lumped Battery использует небольшой набор параметров с сосредоточенными параметрами для добавления вкладов в сумму всех потерь напряжения в батарее, происходящих от омических сопротивлений и, опционально, процессов переноса заряда и диффузии. Кроме того, вы можете определить модель батареи на основе произвольного количества элементов электрической цепи с помощью Интерфейс эквивалентной цепи батареи .
Пористые электроды с произвольным количеством электрохимических реакций
Аккумуляторные системы и химические вещества часто подвержены нежелательным побочным реакциям на электродах, и вы можете исследовать их влияние на циклы заряда и разряда, а также на саморазряд.
Типичные побочные реакции, которые вы можете смоделировать, включают выделение водорода, выделение кислорода, рост границы раздела твердого электролита, нанесение металлического покрытия, коррозию металла и окисление графита.
Исследования полностью нестационарной и импедансной спектроскопии
Аккумуляторные системы часто представляют собой закрытые системы, которые трудно изучать во время работы.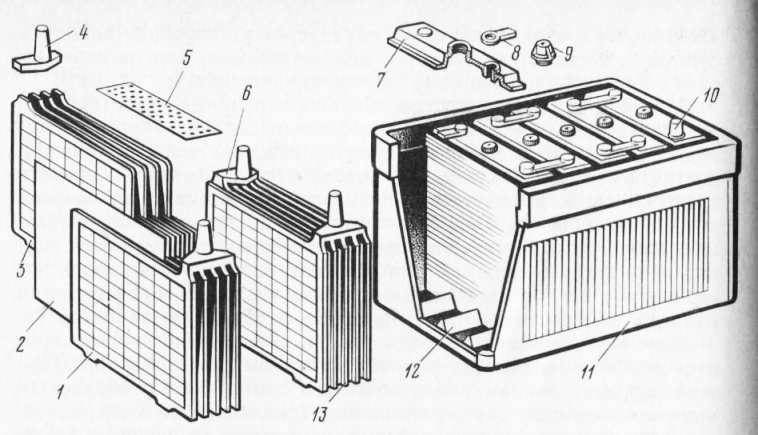 Переходные методы, такие как скачок потенциала, прерывание тока и спектроскопия импеданса, могут использоваться для характеристики батареи во время работы.
Переходные методы, такие как скачок потенциала, прерывание тока и спектроскопия импеданса, могут использоваться для характеристики батареи во время работы.
Выполняя исследования переходных процессов, вы можете выполнять оценку параметров в различных временных масштабах и на разных частотах, чтобы отделить омические, кинетические, транспортные и другие потери, которые могут быть причиной старения батареи. Используя переходные методы, моделирование и оценку параметров, вы можете очень точно оценить состояние аккумуляторной системы.
Высокоточное моделирование аккумуляторов
Интерфейс Lithium-Ion Battery используется для расчета распределения потенциала и тока в литий-ионном аккумуляторе. Можно использовать несколько промежуточных электродных материалов, а также учитывать потери напряжения из-за слоев SEI.
Интерфейс Battery with Binary Electrolyte используется для расчета распределения потенциала и тока в обычной батарее. Можно использовать несколько интеркалирующих электродных материалов, а также можно учитывать потери напряжения из-за образования пленки на пористых электродах.
Можно использовать несколько интеркалирующих электродных материалов, а также можно учитывать потери напряжения из-за образования пленки на пористых электродах.
Интеркалирующие частицы и транспорт в пористых структурах
Частицы в пористых аккумуляторных электродах могут быть твердыми (литий-ионный электрод) или пористыми (свинцово-кислотный, NiCd). В случае твердых частиц пористость в электроде находится между упакованными частицами. Однако перенос и реакции могут происходить в твердых частицах для небольших атомов, таких как атомы водорода и лития. Эти интеркалирующие частицы моделируются с помощью отдельного уравнения диффузии-реакции, определяемого по радиусу твердых частиц. Поток интеркалирующих частиц соединяется на поверхности частиц с частицами, которые транспортируются в пористом электролите между частицами. Виды интеркаляции и реакции предопределены для литий-ионных аккумуляторов, но вы можете использовать те же функции для моделирования интеркаляции водорода, например, в NiMH батареях.
