какая должна быть зимой и летом, как проверить, как поднять
Плотность электролита в аккумуляторе — важный параметр автомобильных сернокислотных АКБ. От него зависит уровень заряда. В нашей статье подробно рассмотрим какая плотность должна быть зимой и летом, как проверить плотность аккумулятора, а также как поднять плотность электролита.
Содержание:
- Какая плотность должна быть в аккумуляторе
- Плотность электролита в аккумуляторе зимой
- Плотность электролита в аккумуляторе летом
- Как проверить плотность аккумулятора
- Как поднять плотность в аккумуляторе
Уровень плотности позволяет оценить степень разрядки аккумулятора и его техническое состояние. Если АКБ быстро разряжается, то нужно проверить состояние электролита, протестировав его в каждой из банок.
Какая плотность должна быть в аккумуляторе
Для проверки используется специальный прибор, который называется ареометром. Эталонные показатели получают при температуре воздуха +25°С.
Эталонные показатели получают при температуре воздуха +25°С.
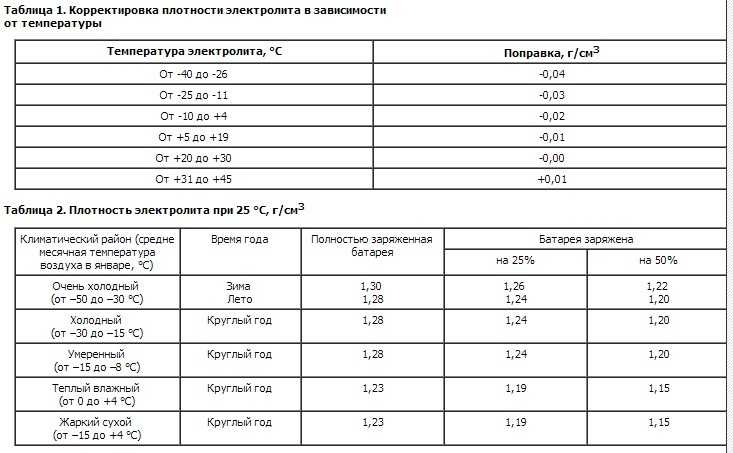
Так как идеальные условия бывают редко, то используется специальная таблица, в которой характеристики плотности скорректированы с учетом погодных условий.
Проверка должна производится регулярно, хотя бы раз в 2 месяца. Естественно, что делается это только на обслуживаемых АКБ.
На таких устройствах имеются специальные выкручивающиеся пробки, сняв, которые можно получить доступ к содержимому каждой банки.
Выкрученная пробка из аккумулятора.
Плотность электролита должна иметь оптимальную плотность, но нужно учитывать также климатическую зону, так как температура окружающего воздуха вносит свои коррективы в показатели.
Так в условиях умеренного климата электролит должен иметь плотность от 1,25 до 1,27 г/куб. см.
Допустимо отклонение от указанного значения не более чем на 0,01 г/куб. см.
В арктической зоне, где зимой обычны морозы порядка -30°C, плотность нужно держать на 0,01 г/куб. см выше, а вот в субтропиках наоборот – на 0,01 г/куб. см ниже.
см выше, а вот в субтропиках наоборот – на 0,01 г/куб. см ниже.
Оптимальная плотность зимой и летом немного отличаются, что показано на иллюстрации ниже:
Интересной особенностью является то, что при меньшей плотности в аккумуляторе он служит больше, но при этом снижается его емкость.
Также нужно учитывать, что указанные выше значения относятся к заряженной на 100% батарее.
В жизни АКБ имеет зарядку около 80-90%, соответственно, и плотность у электролита будет немного меньшей.
На практике зимой плотность электролита делают чуточку большим, чем нужно для полного заряда. Это делается для того, чтобы при понижениях температуры, которые у нас происходят постоянно, аккумулятор все равно мог стабильно заводить двигатель.
Летом лучше так не делать, так как чем больше плотность, тем больше риск закипания жидкости в батарее.
Внимание! Повышенная плотность электролита ведет к снижению срока эксплуатации АКБ. Однако низкая понижает напряжение и емкость, ухудшает запуск мотора.
Лучше всего придерживаться оптимальных рекомендованных значений. Во время морозов плотность можно чуть-чуть повысить, но очень незначительно.
Таблица плотности электролита в аккумуляторе
При составлении таблицы плотности электролита по климатическим зонам руководствуются усредненными среднемесячными температурами в январе.
Для зон с температурами выше -15°C плотность зимой и летом не меняют, используя одну концентрацию кислоты круглый год.
Достаточно следить, чтобы значение не отклонялось от требуемого. А вот в арктических районах плотность требует сезонного изменения, иначе зимой АКБ просто не сможет завести двигатель.
Рекомендуемая плотность электролита в аккумуляторной батарее |
|||||
| Климатические районы | Время года | Плотность электролита, приведенная к 25°C, г/см3 | |||
| Заливаемого в аккумулятор | Заряженной батареи | При зарядке батареи на | |||
| 25% | 50% | ||||
| С резко континентальным климатом и температурой зимой ниже -40°C | Зима | 1.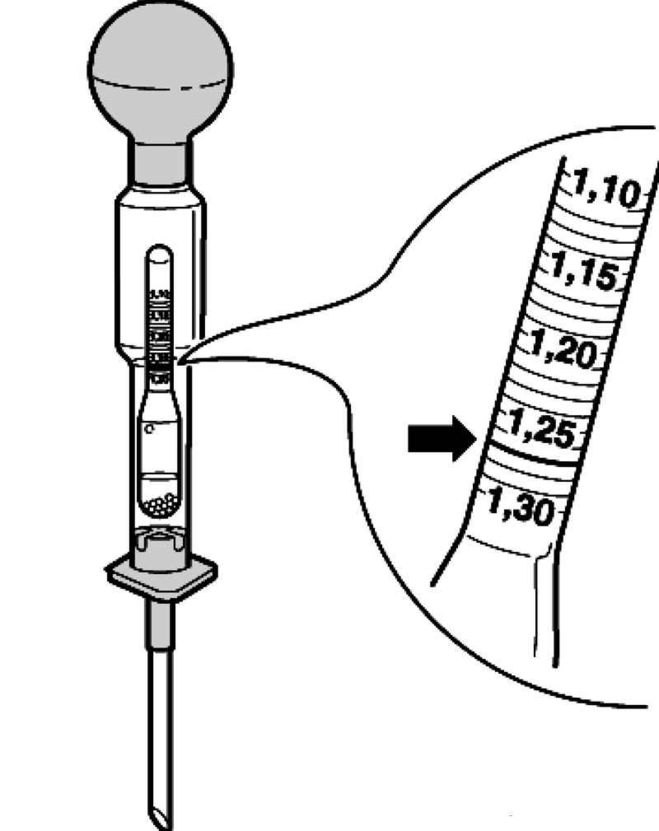 28 28 |
1.30 | 1.26 | 1.22 |
| Северные с температурой зимой -40°C | Круглый год | 1.26 | 1.28 | 1.24 | 1.20 |
| Центральные с температурой до зимой -30°C | 1.25 | 1.27 | 1.23 | 1.19 | |
| Южные | 1.23 | 1.25 | 1.21 | 1.17 | |
Плотность электролита летом и зимой в разных климатических регионах.
Плотность электролита в аккумуляторе зимой
Зимой плотность должна составлять 1,27 г/куб. см. Если в местности январская температура опускается до – 35 градусов, то плотность повышается до 1,28 г/куб. см.
Иначе зимой емкость снизится и запускать автомобиль станет трудно.
Внимание! При падении значения плотности до отметки 1,09 г/куб. см оборачивается тем, что жидкость в банках АКБ замерзает при опускании столбика термометра до – 7°С.
Это приводит к разрывам и деформациям корпуса, разрушению пакетов пластин из-за расширения льда.
Когда зимой происходит понижение плотности, это не значит что нужно поднимать концентрацию раствора в банках. Необходимо подзарядить батарею зарядным устройством.
Большинство личных автомобилей используются в основном для поездок на работу, в торговые центры.
Обычно расстояния при этом преодолеваются небольшие, при запуске мотора аккумулятор разряжается, а небольшая дальность поездки не позволяет ему нормально зарядиться, тем более что из-за длительных простоев на улице электролит находится в холодном виде.
Нормальная зарядка происходит только, если электролит теплый. Таким образом, если не подзаряжать регулярно АКБ, то ее уровень заряда будет постепенно уменьшаться вместе с падением плотности.
Поэтому подзарядку при помощи зарядного устройства также нужно делать в отапливаемом помещении.
Оно должно быть нежилым, иметь хорошую вентиляцию. Это важно, так как в процессе зарядки электролит выделяет газ, вредный для здоровья человека.
Это важно, так как в процессе зарядки электролит выделяет газ, вредный для здоровья человека.
Внимание! Самому корректировать плотность электролита настоятельно не советуем! Для этого нужен опыт. Кроме того, работать с соляной кислотой опасно, это требует соблюдение техники безопасности. Поэтому самостоятельно можно только долить дистиллированную воду в банки, если ее уровень понизится слишком низко.
Он находится на отметке 1,5 см над верхним краем пластин у легковых автомобилей и 3 см – у грузовиков.
У только что купленной, новой батареи плотность электролита должна быть на уровне 0,15-0,16 г/куб. см.
Внимание! Нельзя пользоваться в мороз сильно разряженным аккумуляторов, это может привести к замерзанию внутри него электролита, что как минимум разрушит пластины. Но могут деформироваться также перегородки между банками или внешний корпус.
В таблице ниже указано при каких плотностях и температурах происходит замерзание электролита.
| Плотность электролита, г/куб. см | Температура замерзания, °С |
| 1.10 | -8 |
| 1.11 | -9 |
| 1.12 | -10 |
| 1.13 | -12 |
| 1.14 | -14 |
| 1.15 | -16 |
| 1.16 | -18 |
| 1.17 | -20 |
| 1.18 | -22 |
| 1.19 | -25 |
| 1.20 | -28 |
| 1.21 | -34 |
| 1.22 | -40 |
| 1.23 | -45 |
| 1.24 | -50 |
| 1.25 | -54 |
| 1.28 | -74 |
Исходя из таблицы легко понять, что АКБ, даже заряженная на все 100%, все равно замерзнет, если температура опустится до -70°С.
Если она разряжена до 40% от номинала, то точка замерзания поднимется до -25°С. Разряд же до 10% емкости приведет к тому, что лед внутри банок появится при -10°С, что довольно немного для нашей страны.
Если ареометра нет, то уровень разреженности батареи проверяют при помощи нагрузочной вилки. При этом показатель напряжения в разных банках не должен отличаться более чем на 0,2 В.
| Индикатор нагрузочной вилки показывает, В | Уровень разрядки АКБ, % |
| 1,8–1,7 | 0 |
| 1,7–1,6 | 25 |
| 1,6–1,5 | 50 |
| 1,5–1,4 | 75 |
| 1,4–1,3 | 100 |
Внимание! Ставить батарею на подзарядку пора, если зимой она разряжена наполовину, а летом – на 75%.
Плотность электролита в аккумуляторе летом
Если зимой главная проблема АКБ – снижение емкости, то летом – испарение электролита.
Точнее испаряется вода, повышая постепенно концентрацию раствора кислоты. Если не следить за уровнем, то жидкость оголит верх свинцовых пластин.
Доводить до такого состояния нельзя, так как на воздухе они начинают активно разрушаться.
Чтобы в жару концентрация кислоты не повышалась слишком сильно (что вредно для пластин), плотность нередко делают меньше на 0,02 г/куб. см, чем это считается оптимальным. Обычно в теплую погоду это не ухудшает запуск двигателя, зато продлевает срок службы аккумулятора.
Выкипанию воды из электролита способствует то, что в подкапотном пространстве, где расположен двигатель, летом очень жарко.
Крышку капота раскаляет солнце, работающий мотор также сильно нагревается.
При высокой температуре токоотдача повышается и АКБ становится способной легко проворачивать стартер даже в том случае, если плотность электролита находится на уровне всего 1,22 г/куб. см (этот уровень считается минимально допустимым для влажного теплого климата).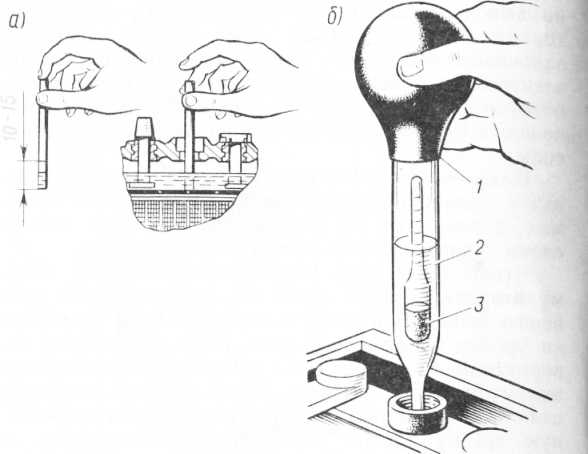
При испарении воды происходит снижение уровня жидкости в банках, плотность растет. Как результат ускоряются разрушительные процессы платин.
Поэтому летом нужно проверять уровень электролита хотя бы 1 раз в месяц, а лучше 2 раза и периодически доливать в банки дистиллированную воду.
В противном случае произойдет перезаряд из-за высокой плотности электролита, а пластины подвергнутся ускоренной сульфатации.
Внимание! Увеличенная плотность электролита летом приводит к значительному уменьшению срока эксплуатации аккумуляторной батареи.
Летом зарядка с помощью зарядного устройства требуется редко, но тоже применяется. Однако, если вы достали ЗУ, то заодно проверьте состояние АКБ – измерьте уровень электролита в каждой банке, долейте при необходимости дистиллят.
Хотя выкипает в основном вода, но кислота тоже испаряется. Поэтому постоянное добавление дистиллированной воды в раствор в конце концов приведет к падению концентрации.
Это приводит к невозможности батареей держать заряд, и, соответственно, эксплуатировать ее. Чтобы вернуть работоспособность, плотность электролита нужно будет поднять. Для этого требуется проверить ее уровень.
Как проверить плотность аккумулятора
Рекомендуется проверять значение плотности после пробега 15-20 тысяч километров.
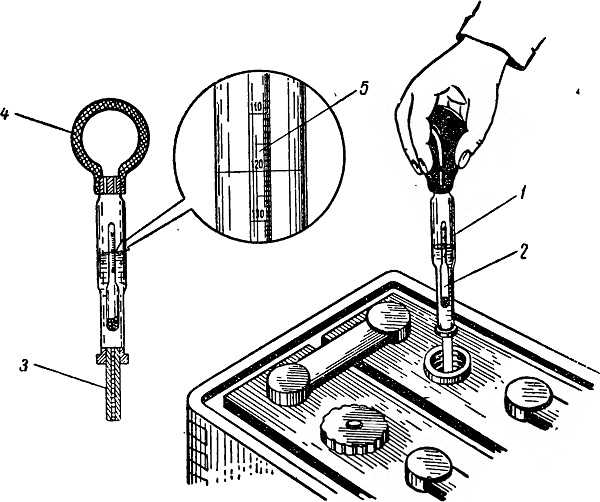
Для этого нужно купить денсиметр – этот прибор легко приобрести в автомагазинах. Он состоит из стеклянной колбы в виде сужающейся к одному концу трубки, на другом конце которой находится резиновая груша. В расширенной части денсиметра помещен поплавок-ареометр.
Для проведения измерения нужно снять пробки с аккумулятора. Узкий конец денсиметра вставляют в банку, погружают в электролит и при помощи сжатия груши набирают внутрь раствор.
Его количество должно быть таким, чтобы ареометр свободно всплыл внутри денсиметра. По совмещения шкал на ареометре и колбе денсиметра определяют точное значение плотности, которое свидетельствует о величине заряда АКБ.
Проверить плотность можно далеко не на всех аккумуляторах. Сейчас на легковом транспорте многие водители предпочитают покупать необслуживаемые модели, у которых нет доступа внутрь банок. Также имеются так называемые малообслуживаемые модели, у которых единственное, что допускается делать – доливать дистиллят.
У таких аккумуляторов плотность определяют с помощью специального индикатора, находящегося на верхней крышке. Он представляет собой цветное окошечко. Если оно зеленого цвета, это значит, что уровень зарядки 65-100%, половинная зарядка или ниже показывается черным цветом, белый или красных колер сигнализирует о необходимости доливки воды.
Индикатор степени зарядки на АКБ.
Уточнить значение цвета на индикаторе всегда можно на маркировке батареи, она размещается всегда.
Внимание! Чтобы узнать, нужно ли проводить корректировку плотности электролита, проверять ее нужно только на полностью заряженной АКБ.
Первым делом нужно проверить уровень и долить при необходимости дистиллированной воды. Затем производит полную зарядку зарядным устройством.
Затем производит полную зарядку зарядным устройством.
После выключения ЗУ аккумулятору нужно дать постоять часа 2-3, чтобы данные измерения были максимально достоверны.
Чтобы не сделать ошибки, измерьте термометром температуру воздуха в помещении, где производилась зарядка и посмотрите, какая плотность должна быть при такой температуре в таблице.
Теперь можно приступать к процессу проверки. Денсиметром наберите электролит так, чтобы ареометр свободно всплыл.
Он должен спокойно плавать, не соприкасаясь со стенками колбы. Поднимите устройство на уровень глаз и снимите показания, сразу же записав их.
Замеры нужно производить для каждой банки.
Проверка плотности электролита денсиметром.
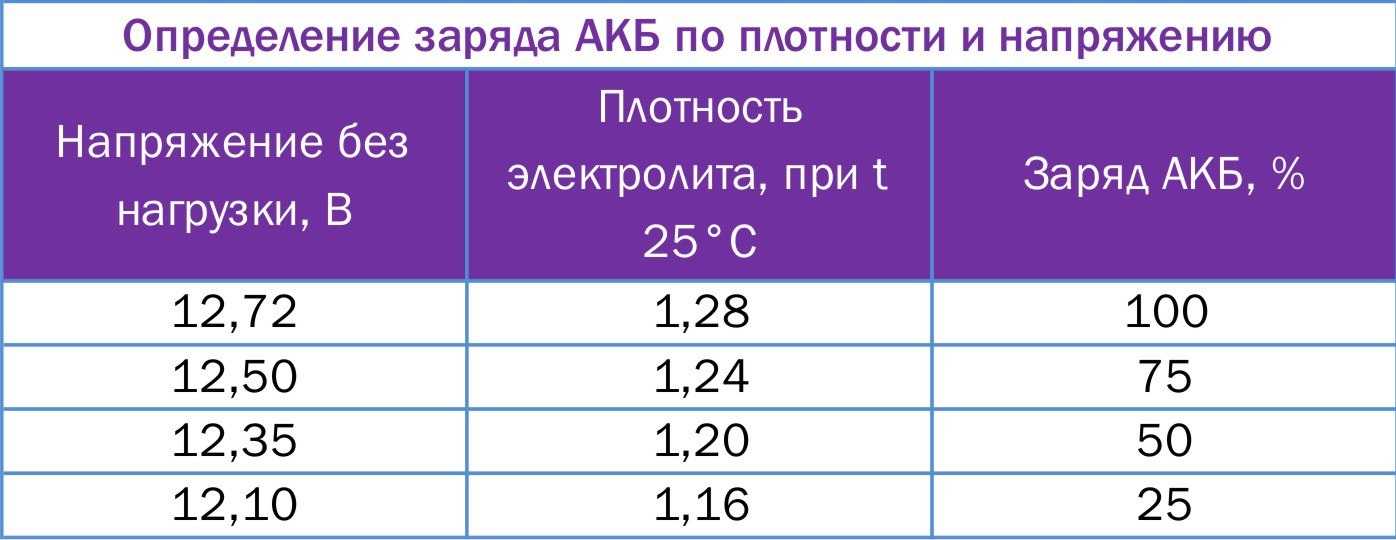
Руководствуйтесь следующей таблицей определения степени заряженности аккумулятора в зависимости от его плотности:
| Температура в помещении, °С | Степень зарядки, % | ||
| 100 | 70 | Разряженный | |
| Более 25 | 1,21–1,23 | 1,17–1,19 | 1,05–1,07 |
| Менее 25 | 1,27–1,29 | 1,23–1,25 | 1,11–1,13 |
Внимание! Плотность в разных банках на АКБ не должна различаться.
Если в каких-то банках плотность понижена по сравнению с другими ячейками, это значит, что она дефектная и между пластинами имеется короткое замыкание.
Если же показатель низкий во всех элементах, то это говорит, что батарея полностью разряжена, либо произошла сульфатация пластин. Также возможно, аккумулятор просто старый и выработал свои сроки.
Установить точную причину можно тщательной проверкой, при которой помимо плотности также замеряется напряжение на выходах АКБ под нагрузкой и без нее.
Кривая зависимости плотности от напряжения в соответствии с заряженностью.
Слишком высокая плотность в банках – тоже не повод для радости. Это может значить, что электролит кипел при зарядке. При его вскипании плотность повышается.
Измерить степень плотности электролита, чтобы выяснить уровень зарядки батареи, можно без денсиметра и не вытаскивая аккумулятор из посадочного места на автомобиле.
Для проверки потребуется только мультиметр и таблица ниже, в которой указаны соотношения между показателями напряжения и плотностью.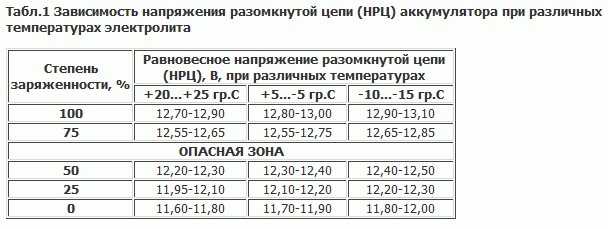
| Уровень заряженности аккумулятора, % | Значение плотности электролита, г/куб. см | Напряжение на выводах, батареи В |
| 100 | 1.28 | 12.7 |
| 80 | 1.245 | 12.5 |
| 60 | 1.21 | 12.3 |
| 40 | 1.175 | 12.1 |
| 20 | 1.14 | 11.9 |
| 0 | 1.10 | 11.7 |
Внимание! Во всех ячейках батареи плотность должна быть одинаковой. Максимальное отклонение не должно превышать 0,02–0,03 г/куб. см.
Указанное в таблице напряжение действительно для АКБ, выдержанных в покое не меньше 8 часов.
Чтобы восстановить работоспособность аккумулятора, снизившуюся из-за падения концентрации электролита, требуется произвести корректировку уровня плотности.
Для этого отбирается часть электролита из батареи, а вместо него добавляется корректирующий раствор, имеющий плотность 1,4 г/куб. cм.
Если плотность слишком высока, то после отобранный электролит замещается дистиллированной водой.
Затем аккумулятор в течение получаса заряжается при номинальном токе, после чего выдерживается в состоянии покоя на протяжении нескольких часов, чтобы плотность электролита стала одинаковой во всех банках.
Внимание! При проведении всех работ с электролитом нужно соблюдать повышенную осторожность. Рядом должна находится сода и источник проточной воды. Это позволит быстро нейтрализовать кислоту в случае попадания ее на кожу. Вдыхать пары также весьма вредно, поэтому работы проводятся только в хорошо вентилируемом нежилом помещении.
Как поднять плотность в аккумуляторе
Правильно поднять плотность электролита в батарее не так просто, поэтому остановимся на этом вопросе подробно.
Поднимают плотность, если после многократного разбавления дистиллятом, концентрации уже не хватает для нормальной работы аккумулятора зимой.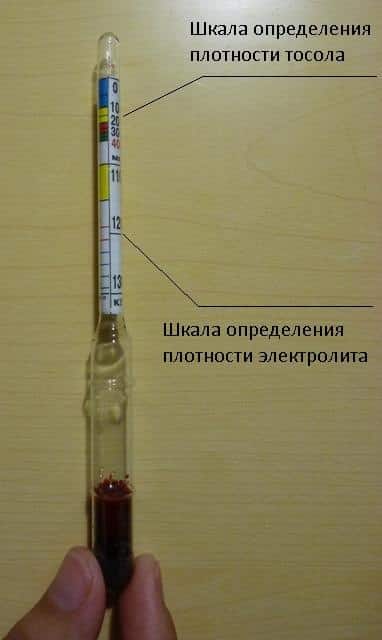
Также процедуру нужно проводить, если батарея подвергалась несколько раз длительному перезаряду. Снижение скорости цикла заряд-разряд свидетельствует о том, что пора корректировать состав электролита.
Для поднятия плотности используется:
- корректировочный электролит с плотностью 1,40 г/куб. см;
- концентрированная серная кислота.
Внимание! Непрофессионалам лучше не использовать кислоту, так как малейшая неосторожность может привести к травмам и даже инвалидности.
Для работы понадобятся:
- денсиметр;
- серный стаканчик со шкалой;
- резиновая груша или клизма;
- корректирующий электролит;
- тара для разведения электролита;
- дистиллированная вода.
Алгоритм повышения концентрации раствора выглядит так:
- Из банки грушей забираем небольшой объем электролита.

- Взамен возвращаем такое же количество корректирующего раствора.
- Батарею нужно 30 минут подзарядить зарядным устройством, чтобы произошло смешивание жидкости.
- После цикла зарядки АКБ отсоединяют от ЗУ и оставляют в покое, чтобы электролит остыл, плотность стала равномерной во всех банках и вышли пузырьки. Это делается для точности последующего измерения.
- Производят контрольный замер, чтобы узнать, нужно ли повторять цикл корректировки.
Внимание! Если значение плотности в отдельных элементах АКБ превышает 0,01 г/куб. см, то аккумулятор нужно еще раз поставить на зарядку при значении тока в 2-3 раза ниже, чем номинальный.
Для вычисления того, сколько воды или концентрированного электролита нужно добавить в батарею, требуется точно знать ее объем.
Состав электролита примерно 40% серной кислоты и 60% воды.
Чтобы было проще изменять концентрацию раствора, воспользуйтесь следующей таблицей:
Таблица корректировки концентрации электролита.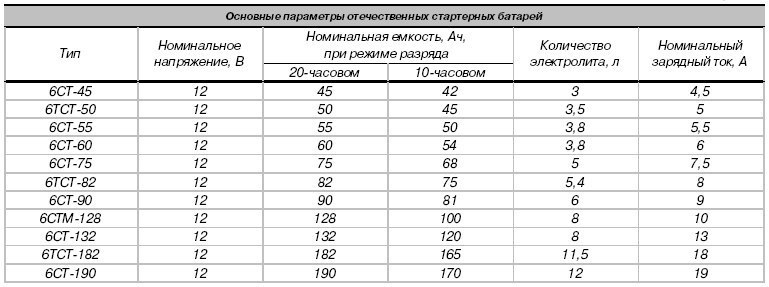
Если вам нужно сделать большую плотность – доливаете корректировочный электролит, если меньшую – дистиллированную воду.
Таблица рассчитана только на применение концентрированного электролита с плотностью 1,40 г/куб. см, а не кислоты.
Оптимальная плотность электролита в аккумуляторе зимой и летом
Споры по вопросу правильной эксплуатации автомобильных аккумуляторов ведутся давно, и конца им не видно. Это объясняется, в том числе, и тем, что число автолюбителей неуклонно растет, и каждый из тех, кто смог проехать самостоятельно даже пару сотню метров, уже априори считает себя авторитетом в данной области и высказывает «авторские», порой безапелляционные, суждения.
Если «пройтись» по Интернету, то порой встречается и такое, что вполне можно засомневаться в собственной компетенции, пожалеть о напрасно потраченных годах и даже пересмотреть свое мировоззрение.
Но это еще полбеды. Дело в том, что даже у профессионалов мнения по некоторым вопросам не всегда совпадают. Поэтому попробуем суммировать всю доступную информацию и вывести «среднее арифметическое», не кидаясь в крайности. Не будем утруждать читателя пояснениями относительно всех нюансов химических процессов, протекающих в АКБ, специфическими терминами, а рассмотрим проблему поддержания плотности электролита в аккумуляторе зимой и летом на приемлемом уровне с чисто практической точки зрения.
Поэтому попробуем суммировать всю доступную информацию и вывести «среднее арифметическое», не кидаясь в крайности. Не будем утруждать читателя пояснениями относительно всех нюансов химических процессов, протекающих в АКБ, специфическими терминами, а рассмотрим проблему поддержания плотности электролита в аккумуляторе зимой и летом на приемлемом уровне с чисто практической точки зрения.
Главный советчик по уходу и сбережению аккумулятора, в том числе, и по плотности электролита – Производитель!
К каждой батарее прилагается сопроводительный документ (памятка, инструкция или что-то еще – не суть важно). Но именно в нем написано то, что необходимо знать автовладельцу и учитывать при эксплуатации конкретной батареи. Только тот, кто ее изготовил, разбирается во всех тонкостях ухода.
Например, к какой категории относится АКБ – обслуживаемые, малообслуживаемые (не требующие регулярной доливки воды на протяжении многих месяцев) или необслуживаемые. А то, что они бывают разными и по материалам, и по технологии изготовления (и так далее), объяснять, думается, никому не стоит.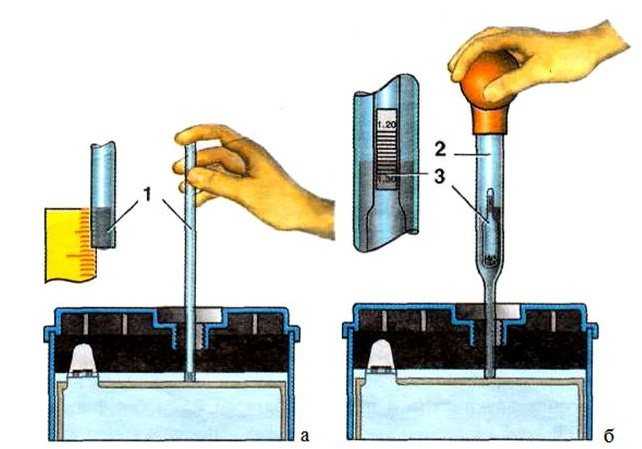
Максимальный, причем систематический, разряд батареи резко снижает срок ее пригодности к эксплуатации. Это никем не оспаривается. Дело в том, что он вызывает повышенную сульфатацию пластин (отложение солей), и часто такой процесс становится необратимым. Слишком «запущенный» аккумулятор восстановлению не подлежит, и его дальнейший путь – в утиль, даже если он не так уж и давно приобретен.
Для батареи одинакова вредна как пониженная, так и повышенная плотность электролита. Если он (в силу разряженности аккумулятора) мало чем отличается от воды, то банки при низких температурах могут просто замерзнуть. Кроме того, такие понятия, как «плотность» и «емкость» батареи, взаимосвязаны (прямая зависимость). Следовательно, возникнут не только проблемы с запуском движка, но и с необходимостью более частой постановки на зарядку.
Излишняя же плотность провоцирует активацию химических процессов, которые в батарее протекают постоянно, независимо от того, «работает» она или «отдыхает».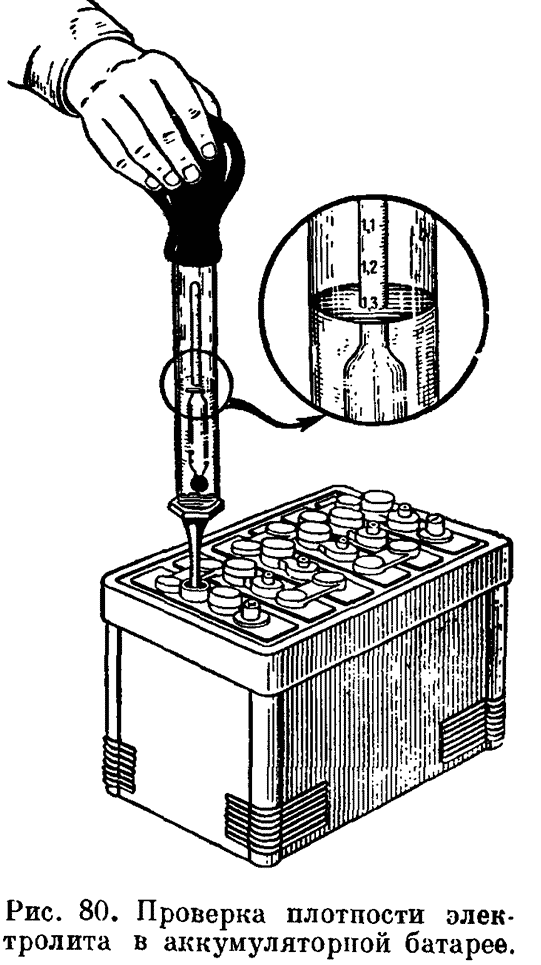 А это влечет более интенсивное разрушение пластин и снижает срок службы изделия.
А это влечет более интенсивное разрушение пластин и снижает срок службы изделия.
Для каждого региона есть свое значение оптимальной плотности электролита, поэтому единой рекомендации изначально быть не может. Например, для условий Крайнего Севера – не менее 1,29. Поэтому необходимо ориентироваться не только на сезон, но и на критические значения температуры, которыми характеризуется данная местность. Следовательно, встречающиеся в интернете советы о поддержании плотности на уровне 1,26 – 1,27 можно расценивать только как общую рекомендацию. Кстати, такой показатель приемлем для большей части территории РФ, наверное, поэтому его часто и упоминают.
Учитывая сказанное, есть смысл выяснить минимально допустимое (критическое) значение плотности, ниже которого оно не должно опускаться. И вот тут нужно вспомнить об инструкции Производителя! Хотя есть и распространенное правило – не менее 1,23.
Практические советы
- В зимний период запуск двигателя, как правило, затруднен.
 Поэтому, если машина стояла в холодном боксе и АКБ с нее не снималась, то ее желательно предварительно прогреть (повысить температуру электролита). Самый простой способ – включить осветительные приборы (например, дальний свет).
Поэтому, если машина стояла в холодном боксе и АКБ с нее не снималась, то ее желательно предварительно прогреть (повысить температуру электролита). Самый простой способ – включить осветительные приборы (например, дальний свет). - Необходимо чаще контролировать состояние клемм, особенно при сезонном понижении температуры. Уменьшение плотности электролита влечет увеличение значения внутреннего сопротивления батареи, а, следовательно, и всей эл/цепи «запуска». Вспомнив закон Ома, несложно понять, что пусковой ток становится несколько меньше, что и затрудняет работу стартера (не создается должный крутящий момент).
- Если в батарею требуется долить воду (дистиллированную), то специалисты рекомендуют делать это, не снимая АКБ с машины и при запущенном двигателе. Объясняется это следующими причинами.
Во-первых, значения плотностей электролита и воды отличаются, и такой способ доведения уровня в банках до нормы обеспечивает качественное перемешивание жидкостей.
Во-вторых, если долить воды и после этого не эксплуатировать машину, а уйти хотя бы на время, то она может элементарно замерзнуть, так как легче электролита и, следовательно, будет являться «поверхностным слоем» жидкости в каждой банке.
- Ни в коем случае нельзя добиваться повышения значения плотности путем банального добавления в электролит кислоты!!! Объяснение простое – чем агрессивнее среда, тем меньше срок пригодности АКБ к использованию. Именно по этой причине некоторые автомобилисты не могут понять, почему уже через год после приобретения вроде бы новая батарея уже ни на что не годится. Вывод – только постановка на зарядку.
- Многие автомобилисты в зимний период ставят машину «на прикол». Им не рекомендуется оставлять АКБ по месту установки. Целесообразнее ее снять, полностью зарядить и перенести в прохладное помещение (например, спустить в погреб), предварительно «укутав» во влагонепроницаемый материал. В каждом регионе «своя» зима (по продолжительности). Поэтому не реже раза в пару месяцев ее стоит проверять «на плотность» и при необходимости подзаряжать. Такая аккуратность в уходе вполне окупится более продолжительным сроком эксплуатации батареи.
И напоследок — не нужно стесняться спрашивать советов у людей опытных. В любом гаражном комплексе есть автолюбители, которые характеризуются продолжительной безаварийной эксплуатацией, аккуратностью в уходе за «железным конем». А если такой человек имеет и большой стаж вождения (а значит, и обслуживания), то его рекомендации (и по плотности тоже), лишними никак не будут.
В любом гаражном комплексе есть автолюбители, которые характеризуются продолжительной безаварийной эксплуатацией, аккуратностью в уходе за «железным конем». А если такой человек имеет и большой стаж вождения (а значит, и обслуживания), то его рекомендации (и по плотности тоже), лишними никак не будут.
Плотность аккумулятора: как измерить и повысить.
Аккумулятор состоит из отдельных гальванических элементов, преобразующих химическую реакцию в электрическую энергию. Каждый элемент имеет напряжение 2 V. Плотность аккумулятора (электролита) формируется шестью элементами, последовательно соединенными в одном пластмассовом корпусе. Работают они на повышение напряжения. А силу тока можно увеличить, соединив их параллельно.
Устройство
Аккумуляторная батарея (АКБ) является химическим источником тока, резервирующим электрическую энергию для питания стартера. Она же снабжает током приборы автомобиля. Считается хорошим подспорьем, когда наблюдается низкая мощность генератора.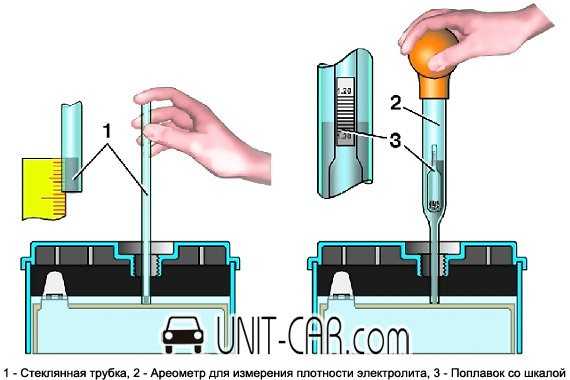
К основным параметрам АКБ следует отнести:
- номинальную емкость;
- напряжение;
- ток холодного запуска двигателя.
Данные маркируются на корпусе аккумулятора.
Практически все автомобильные аккумуляторы работают на свинцово — кислотных батареях. Материал корпуса из пропилена, изоляционный, стойкий к кислоте. Каждый аккумулятор содержит попеременно расположенные положительно и отрицательно заряженные электроды. Между пластинами (электродами) размещаются пластиковые сепараторы, отделяющие пластины друг от друга.
Сами электроды представляют собой свинцово–кальциевый сплав, рассчитанный на ограничение степени саморазряда. То есть, за полтора года он может разрядиться на 50%. Эти аккумуляторы относятся к категории не обслуживаемых, поскольку потеря воды в них составляет всего 1 гр/Ач. Кстати, добавление серебра или олова в электроды заметно повышает их коррозионную стойкость.
Структура решетки положительных и отрицательных элементов имеют разную технологию изготовления. Например, на отрицательных электродах делаются просечки свинцовой пластины, затем проводят растяжку. Положительные электроды состоят из опорной рамы с жилками конкретной направленности. Такая конструкция обеспечивает качественную жесткость и ограничивает их линейное расширение. Более того, положительные пластины покрываются диоксидом свинца, а отрицательные, губчатым свинцом. Отрицательные и положительные элементы помещаются в сернокислотный раствор, величина плотности которой зависит от уровня зарядки батареи.
Например, на отрицательных электродах делаются просечки свинцовой пластины, затем проводят растяжку. Положительные электроды состоят из опорной рамы с жилками конкретной направленности. Такая конструкция обеспечивает качественную жесткость и ограничивает их линейное расширение. Более того, положительные пластины покрываются диоксидом свинца, а отрицательные, губчатым свинцом. Отрицательные и положительные элементы помещаются в сернокислотный раствор, величина плотности которой зависит от уровня зарядки батареи.
Принцип работы
Действие аккумулятора является результатом способности его преобразовывать химическую реакцию в электрическую энергию при разряде, наоборот, при заряде. Исходя из этого принципа, все АКБ работают в циклическом режиме.
То есть, подключение потребителей вызывает разряд активной положительной и отрицательной масс, взаимодействующих с электролитом. В этом случае плотность падает, «садится». Но АКБ заряжается от генератора. Зарядку батарей можно получить и от зарядного устройства.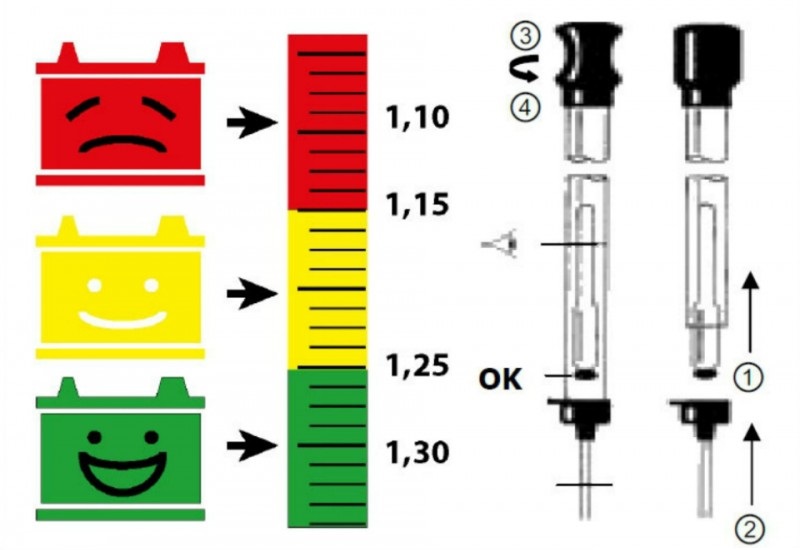 Происходит процесс преобразования раствора в двуокись свинца и соединение серной кислоты, что приводит к повышению плотности раствора.
Происходит процесс преобразования раствора в двуокись свинца и соединение серной кислоты, что приводит к повышению плотности раствора.
Нужно отметить, что работоспособность батареи во многом зависит от температуры среды. При повышенной температуре отдаваемая мощность повышается, что приводит к саморазряду, величина которого находится в прямой зависимости от температуры среды и конструкции электродов.
Продолжительность работы АКБ составляет 4÷5 лет и это средняя величина.
Плотность
Определяется визуально, так называемым, стеклянным глазом или цветным датчиком. Зеленый оттенок на нем свидетельствует о заряженности, черный цвет – среднем уровне зарядки и желтый означает низкую величину зарядки. Значит, принцип работы этого визуального прибора построен на плотности электролита.
Автомобильные батареи рассчитаны на жесткое крепление, посредством рамки, во избежание его опрокидывания или разлива.
Способ проверки
Плотность электролита в аккумуляторе проверяется простым автомобильным ареометром. Это стеклянная колбочка с резиновой грушей на верхнем конце и длинной резиновой трубкой снизу. Внутри колбы помещается обычный ареометр. Нажимая на грушу, выпускается из нее воздух. Резиновая трубка прибора опускается в банку как можно ниже. Расслабляя руку, выбирается из нее содержимое. При этом ареометр внутри колбы начинает всплывать и, не касаясь чего-либо, становится на отметке. Нижняя градуировка (мениск) и покажет плотность. Нажатием груши содержимое колбы сливается обратно. Процедура повторяется с каждой банкой.
Это стеклянная колбочка с резиновой грушей на верхнем конце и длинной резиновой трубкой снизу. Внутри колбы помещается обычный ареометр. Нажимая на грушу, выпускается из нее воздух. Резиновая трубка прибора опускается в банку как можно ниже. Расслабляя руку, выбирается из нее содержимое. При этом ареометр внутри колбы начинает всплывать и, не касаясь чего-либо, становится на отметке. Нижняя градуировка (мениск) и покажет плотность. Нажатием груши содержимое колбы сливается обратно. Процедура повторяется с каждой банкой.
Оптимальный уровень зарядки
Уровень зарядки автомобильного аккумулятора зимой достигает 25%. Это сигнал о необходимости произвести зарядку. Следует помнить, что зимой, при температуре среды–20° C и плотности 1г/см³, аккумулятор склонен замерзнуть. Поводом для подзарядки может стать и разная плотность отдельных банок в пределах 0,02 г/см³. При этом оптимальный ток не должен превышать 0,05 самой батареи. Например, для зарядки батареи, емкость которой составляет 60 Ач, сила тока будет 3,0 Ач.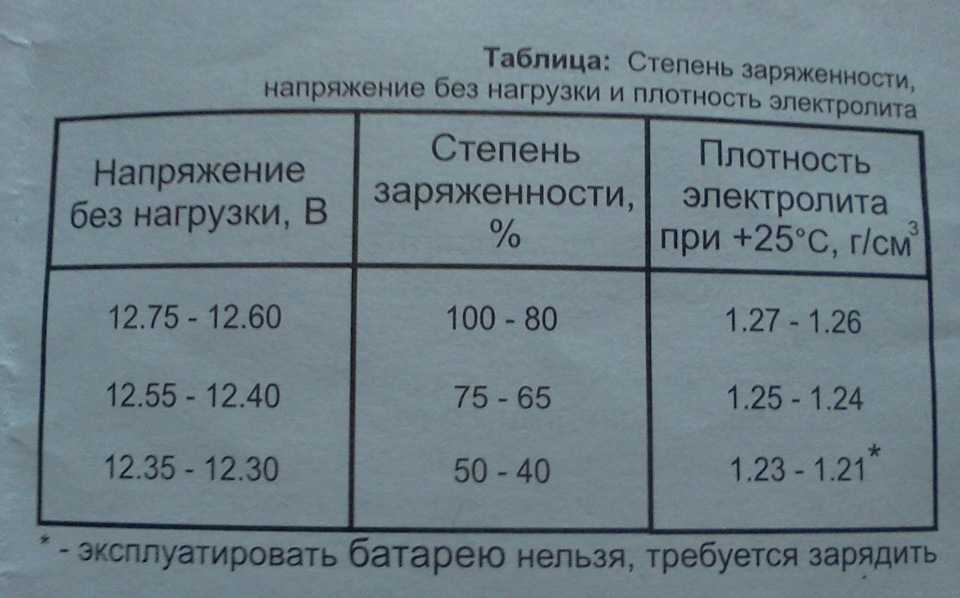 Лучше не доводить электролит до кипения сильным током. Кстати, слабый ток подзарядит батарею лучше. Если в течение двух часов раствор не закипает, а плотность остается без изменения, то считается аккумулятор полностью заряженным.
Лучше не доводить электролит до кипения сильным током. Кстати, слабый ток подзарядит батарею лучше. Если в течение двух часов раствор не закипает, а плотность остается без изменения, то считается аккумулятор полностью заряженным.
При исправной работе генератора и реле, аккумулятор получает наибольшую зарядку во время езды.
Нужно знать, что с запуском двигателя зимой аккумулятор начинает заряжаться только после достижения электролитом положительной температуры. Информация к тому, что зимние переезды, даже на короткие расстояния могут стать поводом полной разрядки источника тока.
Кстати, летом для плотности раствора достаточно 1.18
Проверка
Как проверить плотность аккумулятора денсиметром, если электролит уже разбавлялся дистиллированной водой. Здесь плотность замеряют через 40 минут после запуска двигателя. По наименьшему показателю плотности одной банки определяется, общая разрядка батареи. К примеру, если плотность электролита в аккумуляторе не удается измерить, степень разрядки проверяют нагрузкой стартера. Для этого используется специальная нагрузочная вилка. Посредством лапок, клемма каждой банки поочередно замыкается на 5 секунд, для фиксации показаний вольтметра. Разность по каждой банке не должна составлять более 0,2 V. При высокой разности, банка заменяется.
Для этого используется специальная нагрузочная вилка. Посредством лапок, клемма каждой банки поочередно замыкается на 5 секунд, для фиксации показаний вольтметра. Разность по каждой банке не должна составлять более 0,2 V. При высокой разности, банка заменяется.
Повышение плотности
Вопрос как поднять плотность аккумулятора стоит всегда, когда стартер отказывает крутить маховик. Это, прежде всего, падение плотности батареи, которая может произойти по разным причинам. Что же делать? Нужно замерить показания электролита каждой банки, зная, что плотность его не должна превышать 1.29. Для северных реалий шкала может быть и выше. Но если цифра показывает, например, 1.18–1.20, добавка электролита с показателем 1.27 только повысит плотность. Процедура откачки старого остатка из одной банки выполняется при помощи клизмы–груши. Поочередно доливается новый раствор из расчета половины объема удаленного. После небольшой встряски, на предмет качественного смешения раствора, делается замер плотности.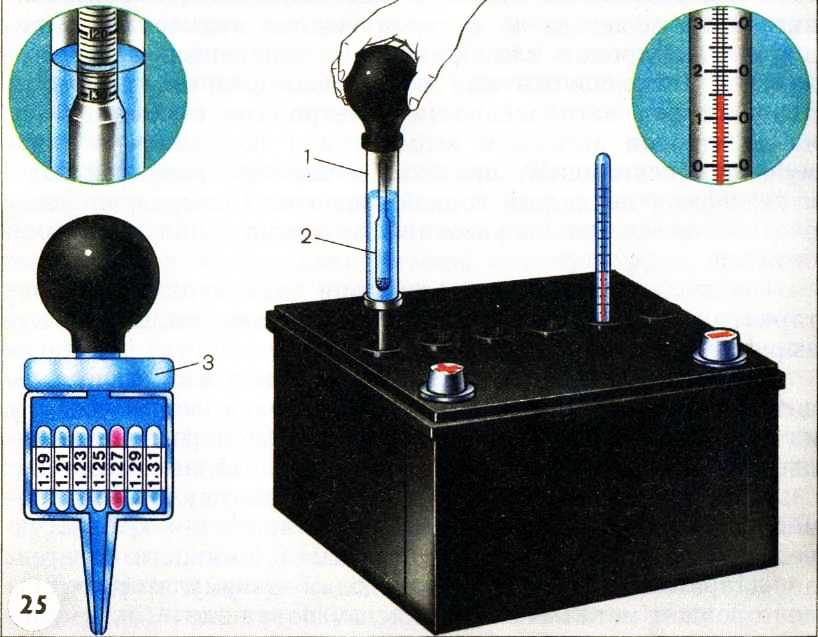 Если значение ее меньше нужного, доливается остальной объем. Процесс ведется до достижения необходимой плотности.
Если значение ее меньше нужного, доливается остальной объем. Процесс ведется до достижения необходимой плотности.
При всем желании, полная замена электролита не выдаст тех результатов, которые показывают новые батареи.
Влияние сульфатации
Это процесс окисления и затем кристаллизации, так или иначе, происходящих химических реакций. В результате элементы пластины становятся очагом высокого сопротивления внутри батареи. В этой ситуации имеет место резкое повышение сопротивления и закипание электролита. Незнание о появлении коричневых или бело–грязных пятен на пластинах вовсе не гарантирует нормальную работу аккумулятора.
Высокий уровень сульфатации приводит к скачкам температуры в момент запуска двигателя, повышению газовыделения. Фактор сказывается на емкости батареи, цвете и плотности раствора. Если оказия обнаружена своевременно, то можно воспользоваться процедурой разрядки–зарядки батареи.
Для этого нужно полностью зарядить ее и довести плотность до 1. 285 г/см³, заправляя постепенно электролитом. Если переборщили, можно разбавить дистиллированной водой. Полностью зарядив батарею, начинают процесс разрядки, методом подключения лампы накаливания в пять ампер. Когда напряжение будет доведено до 10,2 V, нужно остановиться, поскольку эта величина равна напряжению 1,7 V каждой банки. При желании процесс можно повторить.
285 г/см³, заправляя постепенно электролитом. Если переборщили, можно разбавить дистиллированной водой. Полностью зарядив батарею, начинают процесс разрядки, методом подключения лампы накаливания в пять ампер. Когда напряжение будет доведено до 10,2 V, нужно остановиться, поскольку эта величина равна напряжению 1,7 V каждой банки. При желании процесс можно повторить.
Есть утверждения о целесообразности этой методики спасения батареи.
Что ускоряет износ
- Использование некачественного раствора, непроверенной дистиллированной воды;
- длительное время хранения в разряженном состоянии;
- случаи замерзания раствора также весьма пагубно сказываются на работоспособности аккумулятора.
Плотность электролита в аккумуляторе — какая должна быть
Автомобильный аккумулятор предназначен для обеспечения бортовой сети транспортного средства и накопления энергии, которую вырабатывает генератор.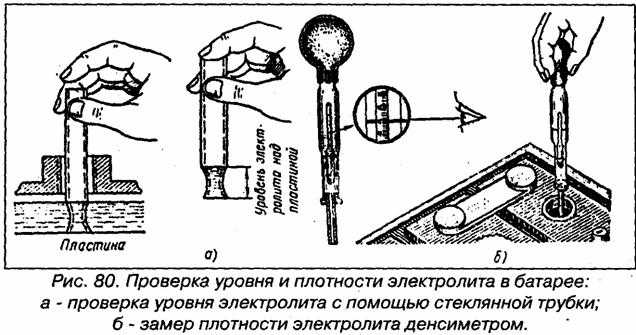 Больше века кислотно-свинцовые батареи применяются в автомобильной промышленности и по-прежнему удерживают лидирующие позиции. Причина долголетия проста – высокая эффективность при дешевой себестоимости. Подобные батареи состоят из гальванических элементов, которые взаимодействуя с водным раствором серной кислоты, вырабатывают электрическую энергию. Такие источники питания имеют стабильную плотность электролита в аккумуляторе, отличаются высокой морозоустойчивостью и длительным сроком работы.
Больше века кислотно-свинцовые батареи применяются в автомобильной промышленности и по-прежнему удерживают лидирующие позиции. Причина долголетия проста – высокая эффективность при дешевой себестоимости. Подобные батареи состоят из гальванических элементов, которые взаимодействуя с водным раствором серной кислоты, вырабатывают электрическую энергию. Такие источники питания имеют стабильную плотность электролита в аккумуляторе, отличаются высокой морозоустойчивостью и длительным сроком работы.
Плотность электролита
Электролит — это основной компонент аккумулятора, а именно, вещество, проводящее электрический ток вследствие распада на ионы в растворе. Основным свойством, которое необходимо знать при использовании АКБ в автомобиле, является плотность электролита — в науке данный термин означает соотношение массы жидкости к занимаемому объему. В АКБ роль раствора выполняет электролит, состоящий из кислоты и дистиллированный воды.
Непосредственно плотность зависит от температуры электролита (чем ниже температура, тем выше плотность).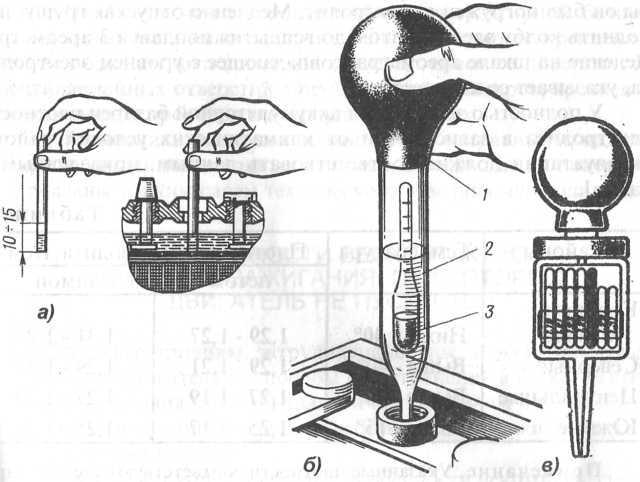 Работа аккумулятора – это чередование циклов разрядки и зарядки, во время которых происходит широкий спектр химических реакций. При разрядке батареи химическая энергия трансформируется в электрический ток, при зарядке электричество превращается в химическую энергию. Данные процессы оказывают серьезное влияние на плотность электролитического раствора. Процесс зарядки повышает плотность электролита, разряд элемента питания – понижает это значение.
Работа аккумулятора – это чередование циклов разрядки и зарядки, во время которых происходит широкий спектр химических реакций. При разрядке батареи химическая энергия трансформируется в электрический ток, при зарядке электричество превращается в химическую энергию. Данные процессы оказывают серьезное влияние на плотность электролитического раствора. Процесс зарядки повышает плотность электролита, разряд элемента питания – понижает это значение.
Температура замерзания электролита в зависимости от плотности — Таблица 1
С помощью прибора ареометра можно замерить плотность электролита в аккумуляторе, а также точно определить степень зарядки АКБ. При полном разряде батареи, показатель плотности падает настолько, что между пластинами остается практически дистиллированная вода. Сульфат свинца, который избыточно вырабатывается во время разряда, полноценно не расходуется при зарядке батареи и покрывает свинцовые пластины белым налетом. Сульфатация негативно влияет на емкость аккумулятора, сокращая рабочий ресурс источника питания.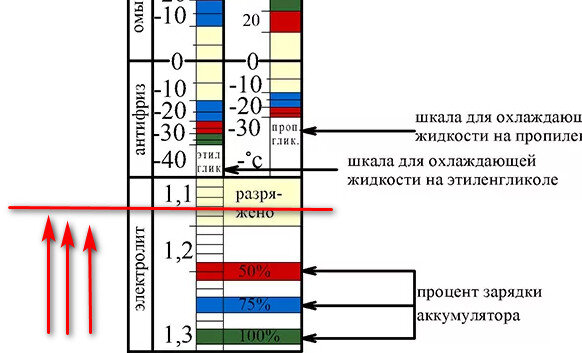 Свинцовые пластины со временем начинают осыпаться, что приводит к короткому замыканию внутри батареи.
Свинцовые пластины со временем начинают осыпаться, что приводит к короткому замыканию внутри батареи.
Поскольку электролит является смесью воды и кислоты, то плотность электролита в аккумуляторе может возрастать. При зарядке АКБ происходит электролиз – выкипание дистиллированной воды из корпуса, благодаря чему концентрация кислоты в растворе возрастает, увеличивая его плотность. Печальная перспектива электролиза очевидна. Потеря воды неизбежно приведет к уменьшению уровня жидкости. Свинцовые пластины оголятся и вступят в химическую реакцию с кислородом, что приведет к осыпанию свинца и выходу батареи из строя. Именно поэтому важно остановить зарядку батареи при первых признаках кипения жидкости и своевременно доливать дистиллят при низком уровне электролита в обслуживаемых батареях.
Устройство и принцип работы АКБ
Для того чтобы качественно провести обслуживание аккумулятора и обеспечить правильную его работу, необходимо хотя бы приблизительно представлять, что у него внутри и как все это работает. Поэтому, прежде чем перейти к вопросам об электролите, необходимо понять, как устроен автомобильный аккумулятор и по какому принципу он работает.
Поэтому, прежде чем перейти к вопросам об электролите, необходимо понять, как устроен автомобильный аккумулятор и по какому принципу он работает.
Конструкция батареи
Практически все свинцово–кислотные батареи имеют одинаковую конструкцию. Состоят они из отдельных секций (банок), каждая из которых имеет набор положительных и отрицательных пластин. Первые называются катодными и выполнены из металлического свинца. Вторые, анодные, сделаны из диоксида свинца. Пластины собраны в пакет и помещены в кислотостойкую емкость, в которую впоследствии заливается рабочая жидкость – водный раствор серной кислоты или так называемый электролит.
Устройство секции свинцово-кислотного аккумулятора:
- 1 – крышка банки;
- 2 – корпус банки;
- 3 – ребристый отстойник;
- 4 – пластины, собранные в пакет;
- 5 – отрицательный (анодный) вывод;
- 6 – отрицательный (анодные) пластины;
- 7 – диэлектрическая прокладка – сепаратор;
- 8 – положительный (катодный) вывод;
- 9 – положительные (катодные) пластины.
Готовые секции, соединенные последовательно, и являются аккумуляторной батареей. В шестивольтовых АКБ таких секций три, в 12-ти вольтовых – шесть.
Как это работает
Итак, конструкция АКБ достаточно проста, но каким образом на ее выводах появляется напряжение? Действительно, если взять батарею прямо из магазина и подключить к ней вольтметр, то прибор покажет «0». Отсутствие тока обусловлено тем, что электролит не заливается в батарею сразу после изготовления, и в стоящем на магазинной полке аккумуляторе пластины сухие. Рабочая жидкость заливается в АКБ уже после покупки.
Самое время выяснить, для чего нужен электролит. Поскольку положительные и отрицательные пластины имеют различный химический состав, между ними, погруженными в кислотный раствор, возникает разность потенциалов (примерно 2 В на секцию, чем и обусловлено количество секций в батарее). При подключении к клеммам АКБ нагрузки между пластинами, благодаря высокой электропроводности электролита, начинает течь ток.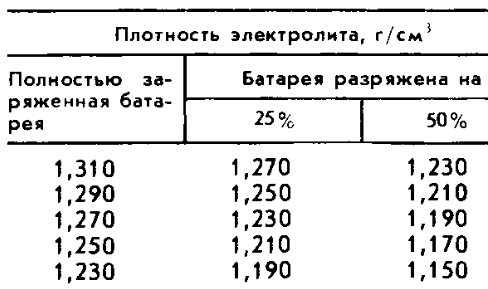 Одновременно начинается химический процесс преобразования диоксида свинца в сульфат свинца с участием серной кислоты. Как только количество диоксида и серной кислоты упадет до определенного уровня, процесс прекратится, и батарея перестанет вырабатывать ток – разрядится.
Одновременно начинается химический процесс преобразования диоксида свинца в сульфат свинца с участием серной кислоты. Как только количество диоксида и серной кислоты упадет до определенного уровня, процесс прекратится, и батарея перестанет вырабатывать ток – разрядится.
В процессе разрядки серная кислота и диоксид свинца расходуются на образование сульфата свинца
Рекомендуем: Характеристики автомобильного аккумулятора Bosch s5
Но аккумуляторы, в отличие от гальванических элементов (батареек), могут восстанавливать свои химические свойства. Если подключить АКБ к источнику постоянного тока, то под его действием сульфат начнет разлагаться на диоксид свинца и серную кислоту. Батарея начнет заряжаться, преобразуя электрическую энергию в химическую. Как только количество диоксида и кислоты достигнет исходных величин, батарею можно считать заряженной.
Химические процессы, возникающие в батарее при ее разрядке и зарядке
Серная кислота, входящая в состав электролита, играет одну из основных ролей в работе АКБ.
Именно от ее свойств будет зависеть качественная и долговременная работа батареи в целом.
Какая должна быть плотность электролита в аккумуляторе
Отечественные автовладельцы ведут отчаянный спор о правилах эксплуатации аккумуляторных батарей. Количество автомобилей стремительно растет, и каждый водитель пытается сформулировать свою позицию по данному вопросу. Даже среди профильных специалистов мнения существенно разнятся. Поэтому будем отталкиваться от рекомендаций производителей, ведь только разработчики элементов питания способны сформулировать нюансы эксплуатации собственных изделий. Любая новая АКБ имеет сопроводительную инструкцию, в которой конкретно прописаны мероприятия по техническому обслуживанию.
Аккумуляторная батарея негативно воспринимает и повышенную, и пониженную плотность электролита. Высокий показатель плотности активизирует химические процессы, делая электролит «агрессивным», что приводит к значительному снижению рабочего ресурса изделия. Низкая плотность уменьшит емкость АКБ, что способствует проблемам запуска силового агрегата, особенно в зимнее время. Именно по этой причине необходимо придерживаться значений, рекомендованных производителем. Плотность полностью заряженного нового аккумулятора должна составлять 1.27 г/см3 при температуре +25 °С. При жарком климате допускается понижение плотности на 0,01 г/см3 , а при морозах — на 0,01 — 0,02 г/см3 больше.
Низкая плотность уменьшит емкость АКБ, что способствует проблемам запуска силового агрегата, особенно в зимнее время. Именно по этой причине необходимо придерживаться значений, рекомендованных производителем. Плотность полностью заряженного нового аккумулятора должна составлять 1.27 г/см3 при температуре +25 °С. При жарком климате допускается понижение плотности на 0,01 г/см3 , а при морозах — на 0,01 — 0,02 г/см3 больше.
Плотность электролита в аккумуляторе зимой и летом
Современный аккумулятор – устройство, сбалансированное и беспричинно корректировать электролит бессмысленно. Плотность электролита в аккумуляторе 1.27 г/см3 не позволит кристаллизоваться жидкости до –50°С. Подобные экстремальные температуры встречаются только на крайнем севере. В таких регионах плотность увеличивают, чтобы предотвратить замерзание электролита. Лучше своевременно заряжать батарею и не допускать разряда, чтобы показатель плотности держался в номинальном значении. Поскольку температура окружающей среды изменчива, то для замера плотности электролита предлагаем использовать специальную таблицу с поправками.
Плотность электролита в аккумуляторе зимой и летом — Таблица 2
Как проверить плотность электролита в аккумуляторе
Данную процедуру необходимо выполнять с периодичностью в три месяца или каждые 15-20 тыс. км, дабы контролировать работоспособность элемента питания. Также замеры производят при покупке новой батареи или при возникновении проблем во время запуска двигателя. Проверку можно выполнить на станции технического обслуживания или самостоятельно в условиях гаража. Перед проверкой показателя электролита следует полностью зарядить аккумулятор и сделать временную паузу длительностью шесть часов. Ведь во время зарядки плотность электролита повышается и информация будет некорректной. Для процедуры измерения потребуется ареометр, который можно приобрести в любом автомагазине. Данное устройство вполне доступно, так как имеет низкую цену.
Для работы потребуется:
- Ареометр
- Защитные очки
- Сухая хлопчатобумажная ткань
- Резиновые перчатки.

Перед измерением источник питания необходимо установить на ровную поверхность и выкрутить заглушки. Далее следует рукой сжать резиновую грушу прибора и опустить наконечник ареометра в крайнюю банку АКБ. Погрузив устройство в электролит, грушу можно отпустить. Разряженный воздух в колбе, начнёт засасывать жидкость из банки. Теперь нужно визуально оценить уровень раствора в ареометре. Количество жидкости должно позволить измерительному поплавку свободно плавать внутри прибора.
После того, как поплавок прекратит колебательные движения, можно зафиксировать показатель плотности электролита, который должен составлять 1,24 – 1,29 г/см3. Если цифры существенно отличаются, то следует выполнить коррекцию плотности раствора. Аналогичные процедуры необходимо произвести со всеми банками аккумулятора. Следует помнить, что любые операции с электролитом необходимо выполнять в защитных перчатках и очках. После завершения работ пластиковый корпус АКБ рекомендуется насухо протереть чистой тряпкой, дыбы исключить саморазряд батареи.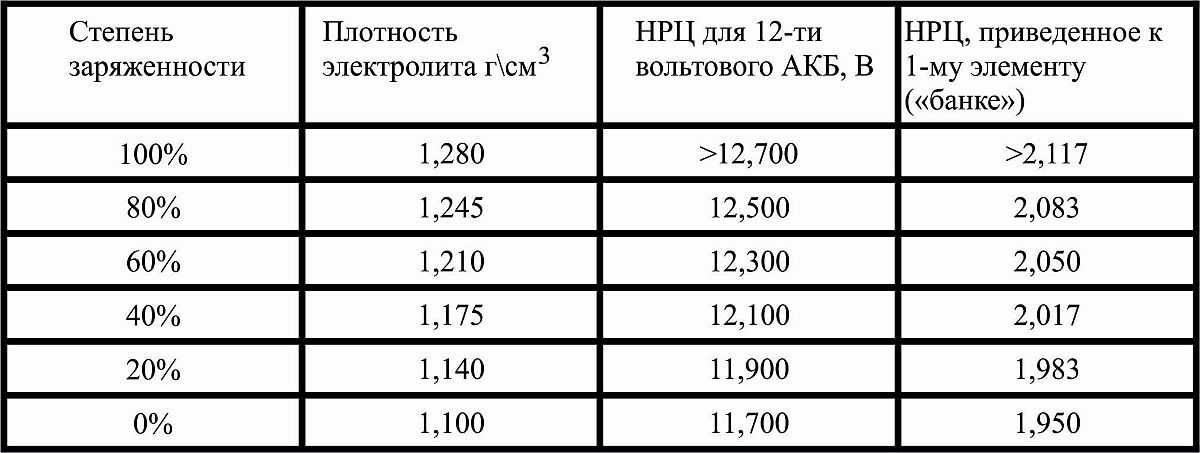
Когда и чем доливают аккумулятор
Необходимость доливки рабочей жидкости в батарею возникает нечасто, но она бывает необходимв. Что, сколько и в каких случаях нужно доливать? Всего таких случаев два: низкий уровень электролита и ненормальная кислотность рабочей жидкости.
Низкий уровень в секциях
Эта ситуация возникает часто, поскольку в процессе работы батареи вода испаряется или, как принято говорить, выкипает. При этом уровень раствора в секциях уменьшается, и края пластин оказываются сухими. Определить это можно визуально, просто свинтив пробки с секций и заглянув в заливные горловины. Нормальный уровень жидкости в секции должен быть примерно на 1 см выше уровня среза пластин. В некоторых АКБ даже имеется специальная метка, отштампованная на корпусе. Если уровень низкий, то ситуация хоть и серьезна, но устранить ее легко. Для этой операции понадобятся:
- медицинский шприц без иглы или автомобильный ареометр;
- дистиллированная вода;
- средства защиты (очки и резиновые перчатки).
Дистиллированная вода набирается в шприц и заливается в соответствующие секции, до нужного уровня. После доливки жидкости в аккумулятор его ставят на зарядку. В этом плане автоареометр намного предпочтительней, поскольку, долив воду, тут же можно проконтролировать плотность раствора.
Следует соблюдать осторожность: нельзя работать с кислотой, если глаза не защищены.
Ненормальная кислотность
Если изначально батарея была заправлена как положено, то чрезмерно большая плотность электролита в аккумуляторе может появиться только в случае, если выкипела вода или измерения проводились при сильном морозе (с понижением температуры плотность повышается, и это нормально). В первом случае достаточно просто долить воду, во втором – произвести перерасчет или, что проще и правильнее, заняться измерениями в отапливаемом помещении.
А вот падение концентрации кислоты – ситуация реальная. Обычно это происходит из-за неправильной эксплуатации АКБ или ввиду ее «преклонного возраста». Причина – появление нерастворимого сульфата, который при своем образовании использовал кислоту, но уже не разлагается при зарядке, а значит, вернуть ее обратно в раствор не может. Ситуация не особо радостная, но восстановить плотность необходимо хотя бы для того, чтобы дотянуть до покупки новой батареи.
Причина – появление нерастворимого сульфата, который при своем образовании использовал кислоту, но уже не разлагается при зарядке, а значит, вернуть ее обратно в раствор не может. Ситуация не особо радостная, но восстановить плотность необходимо хотя бы для того, чтобы дотянуть до покупки новой батареи.
Коррекция плотности электролита
Эксплуатация автомобиля подразумевает циклическую нагрузку на АКБ, во время которой катализатор электрохимического процесса изменяет свою структуру. Поскольку электролит состоит из кислоты(35%) и дистиллированной воды(65%), то это соотношение способно изменяться в зависимости от степени заряженности источника энергии. Во время движения транспортного средства генератор постоянно подает на батарею электрический ток.
Когда емкость восстанавливается, начинается процесс электролиза, во время которого электролит закипает и испаряется. Аналогичный процесс происходит при длительной зарядке специальным устройством. Количество воды в растворе уменьшается, из-за чего увеличивается плотность и убавляется объем жидкости. Чтобы восстановить номинальное значение необходимо долить дистиллированную воду в каждую банку батареи.
Чтобы восстановить номинальное значение необходимо долить дистиллированную воду в каждую банку батареи.
Причины снижения плотности электролита
Чтобы поддержать работоспособность элемента питания автовладельцы добавляют в батарею дистиллированную воду, забывая проверить показатели плотности. Большая концентрация воды приводит к сильному электролизу, во время которого вместе с водой начинает испаряться серная кислота, что снижает плотность электролита. Со временем содержание кислоты в растворе становится критическим и раствор перестает выполнять функцию катализатора химических процессов, что негативно отражается на функциональности аккумулятора.
Инструкция проверки
Проверить уровень плотности – задача не трудная. Для ее выполнения нужно лишь обзавестись специальным прибором. Некоторые автоэксперты советуют денсиметр, другие – ареометр.
В данном материале будет подана инструкция того, как проверить плотность при помощи ареометра.
Рекомендуем: ДМРВ: что это такое
Прежде чем приступить непосредственно к проверке плотности, нужно запомнить, что делать это желательно при температуре +25°С. А также, помимо ареометра, понадобятся мерный стакан и клизма-груша, собственно сам электролит, но обязательно свежий, также дистиллированная вода и, при отдельной необходимости, о чем будет рассказано немного позже, аккумуляторная кислота, паяльник и дрель.
Итак, пошаговая инструкция правильной проверки параметра плотности в АкБ:
- Отдельно для каждой банки измерить параметры электролита.
- При помощи клизмы-груши откачать из каждой банки поочередно максимальное количество старого раствор. При этом также нужно замерить его объем.
- Долить свежий электролит в количестве половины объема от ранее выкачанного.
- Активно потрясти/покачать аккумулятор, чтобы обеспечить смешивание жидкостей.
- Проверить анализируемый параметр путем погружения ареометра в электролит благодаря заливному отверстию в корпусе АкБ.
 При этом электролит перетечет в стеклянную трубку, а поплавок прибора всплывет в корпусе, не прикасаясь к стенкам трубки. После того, как колебания ареометра прекратятся, уровень плотности будет показан не шкале. В случае, если значение не достигло оптимального, ранее перечисленные операции следует производить повторно до тех пор, пока показатели будет нормальные.
При этом электролит перетечет в стеклянную трубку, а поплавок прибора всплывет в корпусе, не прикасаясь к стенкам трубки. После того, как колебания ареометра прекратятся, уровень плотности будет показан не шкале. В случае, если значение не достигло оптимального, ранее перечисленные операции следует производить повторно до тех пор, пока показатели будет нормальные. - Остаток долить дистиллированной водой.
Как повысить плотность электролита в аккумуляторе в домашних условиях
Любая батарея состоит из нескольких банок, поэтому, чтобы поднять плотность электролита в аккумуляторе, придется корректировать электролитический раствор в каждой отдельной емкости. С помощью спринцовки жидкость выкачивается и отправляется в мерную емкость. После чего в банку заливается аналогичное количество нового электролита, который в готовом виде можно приобрести в магазине. Данная операция выполняется с каждой банкой, после чего аккумулятор необходимо зарядить в течение 30 минут, чтобы раствор перемешался. Затем после двухчасовой паузы повторно измеряем показатели плотности. При необходимости нужно повторить коррекцию электролита. Важно помнить, что разность плотности в банках не должна превышать 0.01 г/см3.
Затем после двухчасовой паузы повторно измеряем показатели плотности. При необходимости нужно повторить коррекцию электролита. Важно помнить, что разность плотности в банках не должна превышать 0.01 г/см3.
Бывают ситуации, когда показатель плотности падает ниже значения 1.18 г/см3. В таких случаях вышеописанная технология не поможет восстановить работоспособность батареи – необходима полная замена электролитического раствора.
Как поднять плотность электролита зарядным устройством
Существует еще один способ, которым следует поделиться. Он требует меньших трудозатрат и больше времени. Суть процесса проста – необходимо поставить батарею на зарядку, выставив минимальный ток (не более 1A). Достигнув полного заряда, аккумуляторная батарея начнет «кипеть». При этом дистиллированная вода будет активно испаряться. Уровень жидкости в корпусе постепенно снизится. Вместо испарившейся воды, доливаем электролит номинальной плотности. Процесс очень длительный, однако, за несколько суток можно добиться необходимого результата.
Как выбрать АКБ для зимы?
Выбирая запчасти, иногда очень сложно определить, какой аккумулятор лучше для зимы. Чего делать не следует, так это обращать внимание на надписи типа «Арктический», «Arctic» и им подобные. Дело в том, что производители имеют полное право написать на корпусе или в названиях своих аккумуляторов любое слово, но технической характеристикой оно при этом являться не будет. Так что, если на нем написано «зимний», а в руководстве по эксплуатации этого не отражено, то надпись можно смело игнорировать.
Какие батареи хорошо работают даже самыми холодными зимами? Объективно лучшими для холодного времени года являются гелевые необслуживаемые устройства. От других аккумуляторов они отличаются тем, что там используется электролит консистенции геля. Такое устройство не требуется многократно подзаряжать, да и замерзнуть гелю сложнее, чем жидкости. Но устанавливать его на старый автомобиль можно только в том случае, если генератор современный, способен обеспечить подачу тока с минимальными колебаниями напряжения.
На что нужно обратить внимание, чтобы приобрести хороший аккумулятор для отрицательных температур:
- Емкость. Тут все просто. Чем выше этот показатель, тем легче будут заводиться даже очень замерзшие автомобили.
- Соответствие технических требований АКБ и машины.
- Соблюдение производителем стандартов качества и безопасности.
Чтобы быть всегда довольным батареями на своей машине, автовладельцу нужно не только выбирать хорошие, качественные устройства, но и поддерживать их в работоспособном состоянии. Своевременная зарядка, контроль уровня и густоты электролита — все это не сложно. А наградой станет хороший, корректно работающий аккумулятор.
Как заменить электролит в аккумуляторе
С помощью замены электролита в аккумуляторе владелец автомобиля может значительно продлить рабочий ресурс АКБ. Замена потребует наличие следующих компонентов:
- Стеклянная линейка с узкой горловиной
- Емкость с дистиллятом
- Электролит необходимой плотности
- Зарядное устройство
- Ареометр
- Пищевая сода
- Средства защиты: (перчатки, фартук, очки)
- Резиновая груша
- Чистая ветошь.

Снятый с машины аккумулятор, тщательно протираем чистой ветошью, удаляя с поверхности грязь и пыль. Рекомендуется производить замену при комнатной температуре. После демонтажа крышек с банок производится откачка раствора. Переворачивать АКБ категорически запрещено, ведь химический осадок, скопившийся на дне, способен вызвать короткое замыкание в пластинах, после чего батарея придёт в негодность. Для удаления остатков электролита необходимо на дне каждой банки просверлить небольшое отверстие, через которое вытекут остатки жидкости.
Теперь в пустые банки заливается дистиллят, чтобы тщательно промыть внутренности батареи. Далее необходимо запаять отверстия специальным пластиком стойким к воздействию кислот. С помощью стеклянной воронки заливаем до необходимого уровня новый электролит, после чего аккумулятор ставится на зарядку. Для восстановления оптимальной емкости источник питания следует разрядить и снова зарядить. Заряженная полностью батарея должна выдавать напряжение 12. 7 В. Процесс замены окончен, аккумулятор можно устанавливать на автомобиль.
7 В. Процесс замены окончен, аккумулятор можно устанавливать на автомобиль.
Использованный электролит необходимо правильно утилизировать. Для этой цели потребуется сода, которая является щелочью и способна нейтрализовать разрушительное действие серной кислоты. В емкость с раствором высыпаем половину пачки соды и наблюдаем бурную химическую реакцию. После окончания бурления получившуюся субстанцию можно вылить в канализацию.
И напоследок совет: своевременно проверяйте плотность электролита своего аккумулятора и регулярно заряжайте батарею. Тогда источник питания «отблагодарит» своего хозяина длительной и бесперебойной работой.
что это такое и ее значения
Большинство автомобилей комплектуются свинцово-кислотными аккумуляторными батареями. Принцип действия свинцовых аккумуляторов заключается в обратимой химической реакции свинца и его окиси, расположенный в пластинах и раствора электролита. В качестве электролита используется водный раствор серной кислоты Плотность электролита показывает концентрацию (степень разбавленности) кислоты.
Содержание
- Что такое плотность электролита
- Какую плотность имеет электролит в аккумуляторах
- Зависимость плотности от степени заряженности
- Рекомендуемые значения плотности
- Коррекция плотности при смене сезона
- Выравнивание плотности
Что такое плотность электролита
Серная кислота и вода могут смешиваться в любых пропорциях. Понятие плотность электролита введено для того, чтобы показать, какое количество чистой кислоты содержится в единице объем электролита.
Смешивая кислоту с водой, получают промежуточные значения. Чем больше воды содержит раствор, тем меньшее значение плотности он имеет, поскольку концентрированная кислота гораздо тяжелее:
- дистиллированная вода – 1.00 г/см3;
- концентрированная серная кислота – 1.84 г/см3.
Какую плотность имеет электролит в аккумуляторах
Плотность электролита в аккумуляторе имеет определенные значения, которые существенны для нормального протекания химических реакций в процессе работы. В зимний период и летом концентрация кислоты должна иметь разные значения. Особенно это касается регионов с большими колебаниями температуры. Несоответствие плотности оптимальным значениям может привести к отрицательным последствиям:
В зимний период и летом концентрация кислоты должна иметь разные значения. Особенно это касается регионов с большими колебаниями температуры. Несоответствие плотности оптимальным значениям может привести к отрицательным последствиям:
- Низкая плотность:
- снижение КПД батареи из-за повышения внутреннего сопротивления;
- снижение емкости, так как свинец пластин не полностью вступает в реакцию из-за недостатка кислоты;
- вероятность замерзания при низких отрицательных температурах;
- Высокая плотность:
- Сульфатация пластин из-за образования крупных труднорастворимых кристаллов сульфида свинца;
- Осыпание пластин.
Важно! Плотность электролита в АКБ не является постоянной величиной. Это связано с тем, что во время разряда кислота из раствора реагирует с материалом пластин и ее концентрация падает. Во время зарядки происходит обратная реакция. Разность плотностей заряженного и разряженного аккумулятора составляет примерно 0.
15 – 0.16 г/см3.
Таким образом, зная параметры электролита в полностью заряженном аккумуляторе, можно определить степень разрядки, не пользуясь измерительными приборами, а определив состояние электролита при помощи ареометра.
Измерения производят с учетом температуры, так как наблюдается сильная зависимость. Рекомендуемые значения относятся к измерениям при температуре от +20 до +30°С В других случаях поправки к измерениям должны иметь такие значения:
- от +31 до +45°С + 0.01 гр/см3;
- от +20 до +30°С + 0.00 гр/см3;
- от +5 до +19°С — 0.01 гр/см3;
- от +4 до -10°С — 0.02 гр/см3;
- от -11 до -25° -03 гр/см3;
- от -26 до -40° -04 гр/см3.
Зависимость плотности от степени заряженности
Для электролита автомобильного аккумулятора с нормальной плотностью 1.27 гр/см3 можно привести следующую зависимости от степени разряда батареи:
| Плотность гр/см3 | Уровень заряда | Температура замерзания |
1. 27 27 | 100%, | – 60°С; |
| 1.26 | 95%, | – 55°С; |
| 1.25 | 87%, | – 50°С; |
| 1.24 | 80%, | – 46°С; |
| 1.23 | 75%, | – 42°С; |
| 1.22 | 70%, | – 37°С; |
| 1.21 | 63%, | – 32°С; |
| 1.20 | 56%, | – 27°С; |
| 1.19 | 50%, | – 24°С; |
| 1.18 | 44%, | – 18°С; |
| 1.17 | 37%, | – 16°С; |
| 1.16 | 31%, | – 14°С; |
| 1.15 | 25%, | – 13°С; |
| 1.14 | 19%, | – 11°С; |
| 1.13 | 13%, | – 9°С; |
| 1.12 | 6%, | – 8°С; |
В таблице плотности электролита приведена зависимость плотности и температуры замерзания. Приведенные данные показывают, что глубокий разряд батареи чреват ее замерзанием уже при температуре 8 — 16°С
Рекомендуемые значения плотности
Часто задаваемый вопрос – какая должна быть плотность электролита для лета и для зимы? Большинство производителей аккумуляторов рекомендуют придерживаться следующих значений плотности, в зависимости от минимальной зимней температуры. Важность контроля плотности электролита зимой связана не только с недопущением перемерзания электролита, но и повышением КПД батареи для успешного запуска непрогретого двигателя:
Важность контроля плотности электролита зимой связана не только с недопущением перемерзания электролита, но и повышением КПД батареи для успешного запуска непрогретого двигателя:
- от +6 до +4° 22 гр/см3;
- от +4 до -15° 24 гр/см3;
- от -4 до -15° 26 гр/см3;
- от -15 до -30° 28 гр/см3;
- от -30 до -50° 29 гр/см3;
Перечисленные значения справедливы для полностью заряженных батарей. Заливка электролита в новую батарею производится раствором меньшей концентрации – на 0.02 гр/см3. В процессе зарядки значение поднимется до необходимой величины.
Нормой плотности электролита в средней полосе принято считать 1.26 – 1.27 гр/см3.
Коррекция плотности при смене сезона
При большой разнице среднесуточных температур в летний и зимний период рекомендуется корректировать значение плотности. Процесс не представляет сложности, но опасен из-за агрессивности электролита.
Если машина храниться в гараже и эксплуатируется регулярно, то необходимость в коррекции не возникает, поскольку в результате длительных поездок батарея успевает зарядиться до нормального состояния и содержание кислоты не палает до критических значений.
Кратковременные поездки не способствуют нормальному заряду. Старые аккумуляторы имеют повышенные значения саморазряда, поэтому после длительного простоя плотность может упасть до недопустимых значений.
Электролит корректируется на полностью заряженном аккумуляторе. Важно знать, что в большинстве автомобилей с правильно отрегулированной системой регулировки напряжения, уровень заряда аккумулятора не превышает 80 – 90%. В зимнее время при наличии большого числа мощных потребителей (вентилятор печки, обогрев стекол и сидений, свет фар), это значение еще меньше. Для правильной подготовки батареи к зимнему сезону необходима полная зарядка специализированным зарядным устройством.
Заряд производят при слабом кипении электролита до тех пор, пока в течении текущих двух часов плотность расти уже не будет. Рост плотности говорит о том, что заряд еще не окончен.
Плотность электролита в заряженном аккумуляторе измеряют через два часа после зарядки, чтобы пластины полностью освободились от пузырьков газа и снизилась температура. Не забывайте про учет температуры электролита!
Не забывайте про учет температуры электролита!
Содержание кислоты повышают при помощи корректирующего электролита, который добавляют в банки взамен части основного электролита.
Важно! Отбор раствора из каждой банки батареи должен быть одинаковым! Количество добавляемого корректора также одинаково. Сколько убрано жидкости, столько корректирующего раствора нужно добавлять
Плотность электролита в аккумуляторе и зимой и летом проверяется после получаса дополнительного заряда с последующей двухчасовой выдержкой. Это делается с целью равномерного перемешивания электролита. Обязателен учет температуры.
Переход на летнюю эксплуатацию делается аналогично, только вместо более крепкой кислоты добавляется дистиллированная вода. Дополнительный заряд должен продолжаться более длительное время, поскольку добавляемая вода из-за низкого удельного веса будет находится в верхнем слое.
Важно! Нельзя ускорять перемешивание покачиванием и переворачиванием батареи, поскольку осадок с дна емкости попадет между пластинами и батарея выйдет из строя.
Выравнивание плотности
В процессе эксплуатации аккумулятора можно увидеть, что разные банки имеют расхождения при измерении плотности. Если эта величина не превосходит 0.01 – 0.02 гр/см3, то ничего страшного нет. Большая разница свидетельствует, что банка с меньшим значением начинает выходить из строя.
Встречаются рекомендации исправлять состояние неисправной банки путем долива корректирующего раствора. Этого делать нельзя ни в коем случае. Простое увеличение концентрации кислоты даст только отрицательный эффект и ускорит выход банки из строя.
В данной ситуации необходимо произвести тренировочный цикл заряда. Полностью заряженный аккумулятор разряжают до 50% номинальной емкости, а затем заряжают малым током до полного заряда. Повторяя процесс несколько раз, можно полностью восстановить неисправные банки батареи.
Такие же требования предъявляются к выравниванию уровня электролита. В процессе зарядки током бортовой сети происходит частичное испарение воды из банок. Особенно активно этот процесс происходит летом. Кислота при этом не испаряется, вопреки некоторым источникам из интернета. Поэтому уровень электролита выравнивается исключительно дистиллированной водой.
Особенно активно этот процесс происходит летом. Кислота при этом не испаряется, вопреки некоторым источникам из интернета. Поэтому уровень электролита выравнивается исключительно дистиллированной водой.
https://www.youtube.com/watch?v=dZDnSmBlPmwVideo can’t be loaded because JavaScript is disabled: Плотность электролита в аккумуляторе (https://www.youtube.com/watch?v=dZDnSmBlPmw)
какая она должна быть в норме (зимой и летом)
Главная-Цифровая техника-Аккумуляторы-Проверка плотности аккумулятора, норма плотности
- На что влияет плотность электролита
- Нормативные показатели электролитической плотности
- Назначение свинцово-кислотных аккумуляторов
- Зависимость от температуры работы
- Как проверить плотность электролита в кислотном аккумуляторе
- Условия, при которых следует проводить измерения
- Степень заряженности АКБ
- Температура при проведении измерений
Все, кто имел дело с аккумуляторными батареями, знают, что их основными характеристиками являются номинальное напряжение и емкость заряда.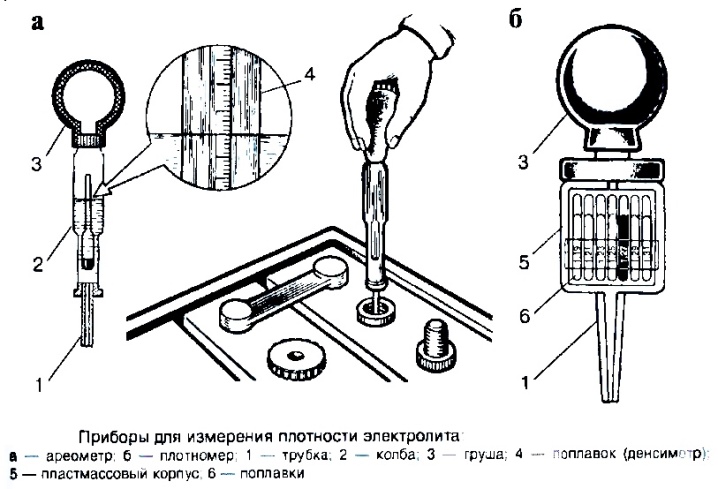 Но для поддержания работоспособности АКБ не менее важным является такой параметр как плотность аккумулятора. Конечно, на самом деле речь идет о плотности электролита, находящегося в аккумуляторной батарее. Но зачастую используется именно это жаргонное выражение. Контролировать концентрированность электролита так же необходимо, как и регулярно заряжать источник тока.
Но для поддержания работоспособности АКБ не менее важным является такой параметр как плотность аккумулятора. Конечно, на самом деле речь идет о плотности электролита, находящегося в аккумуляторной батарее. Но зачастую используется именно это жаргонное выражение. Контролировать концентрированность электролита так же необходимо, как и регулярно заряжать источник тока.
На что влияет плотность электролита
В большинстве аккумуляторных батарей применяются свинцовые пластины, а рабочая среда – серная кислота, разбавленная водой. Насыщенность раствора, измеряемая в грамм/см3, и является той характеристикой, которая влияет на способность аккумулятора накапливать заряд для последующей работы.
Схема устройства свинцово-кислотной АКБ
Концентрация кислоты в растворе электролита и работоспособность аккумуляторной батареи напрямую связаны между собой.
- При малой плотности падает и способность источника тока накапливать ту емкость заряда, которая обеспечивает его рабочие характеристики.
 При малой плотности батарея быстрее разряжается и не выдает положенный максимальный ток.
При малой плотности батарея быстрее разряжается и не выдает положенный максимальный ток. - Если величина этого параметра опустится ниже определенного значения, то в мороз вода в электролите может замерзнуть, и аккумулятор полностью выйдет из строя.
- Но при высокой плотности резко ускоряется процесс сульфатации свинцовых пластин. Это означает, что при слабом заряде АКБ на них образуется свинцовый сульфат, который уже не преобразуется при заряде обратно в свинец. Это также приводит к уменьшению способности накапливать необходимый заряд, а с течением времени – к полному выходу батареи из строя.
Поэтому важно поддерживать значение этого параметра в соответствии с установленными и проверенными нормами. Значительное уменьшение или превышение нормативных значений не способствует продуктивной работе аккумуляторной батареи.
Холод, при котором возможно замерзание содержимого батареи, показаны на рисунке.
Точка замерзания водно-кислотного раствора в зависимости от его плотности
Нормативные показатели электролитической плотности
Наверняка многие автолюбители, знакомые с проблемами поддержания работоспособности аккумуляторов, знают цифру 1,27 г/см3. Именно такой считается оптимальная плотность, при которой кислотные аккумуляторы способны максимально реализовывать свои возможности.
Именно такой считается оптимальная плотность, при которой кислотные аккумуляторы способны максимально реализовывать свои возможности.
Но это значение справедливо не для всех типов аккумуляторов и их рабочих назначений. К тому же оптимальная плотность меняется для разных температур, при которых приходится работать батарее. Поэтому оптимальные значения зимой и летом будут несколько отличаться.
Назначение свинцово-кислотных аккумуляторов
- Стартерные АКБ предназначены для выдачи максимально возможного тока при запуске различных двигателей. Это, в первую очередь, автомобильные АКБ. Нормативное значение плотности для них 1,26 – 1,28 г/см3.
- Тяговые АКБ должны обеспечивать работу электродвигателей постоянным током в течение длительного времени. Одно из их применений – электрокары и другие движущие средства на электрической тяге. Наилучшее значение плотности электролита для этих АКБ тоже находится в пределах 1,26 – 1,28 г/см3.
- Стационарные АКБ применяют для питания любых электрических схем и приборов.
 Обычно находятся на одном месте в помещении. Для них рекомендована пониженное значение 1,22 – 1,24 г/см3.
Обычно находятся на одном месте в помещении. Для них рекомендована пониженное значение 1,22 – 1,24 г/см3.
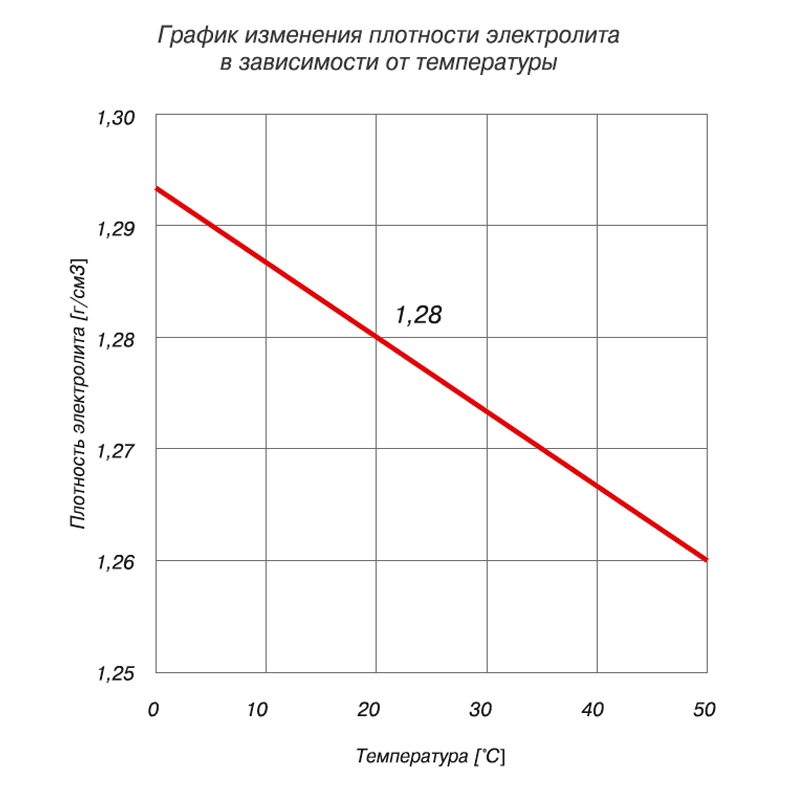
Зависимость от температуры работы
Изменяется окружающая температура – изменяются и значения плотности водно-кислотного раствора. При возрастании температуры способность аккумуляторной батареи накапливать заряд увеличивается примерно на 1% с каждым градусом. С понижением температуры, естественно, эта способность уменьшается. Поэтому рекомендуется в холодную погоду держать АКБ при повышенных плотностных значениях, а для жаркой погоды – снижать эти показатели.
Работоспособность АКБ при различных температурах в зависимости от плотности
Конечно, никто не будет заниматься изменением при каждом скачке погоды. Просто перед наступлением холодов полезно немного увеличить аккумуляторную плотность, а перед летним сезоном – понизить ее. Кроме того, существуют нормы оптимальной плотности для районов с различным климатом. Этих нормативных значений полагается придерживаться круглый год, за редкими исключениями. Для разных регионов считается нормальной:
Для разных регионов считается нормальной:
- В холодном климате 1,27 – 1,30 г/см3
- В средней полосе 1,25 – 1,28 г/см3
- В теплых районах 1,22 – 1,25 г/см3
Более подробно эти нормативы указаны в таблице.
Нормативные значения плотности электролита АКБ для различных температурных условий
Как проверить плотность электролита в кислотном аккумуляторе
Для проверки этой характеристики выпускаются простые измерители, называемые автомобильными ареометрами или денсиметрами. Их работа основана применении закона Архимеда, то есть способности груза погружаться на разную глубину в зависимости от плотности жидкости. Конструктивно ареометр содержит:
- Стеклянную или пластиковую колбу.
- Стеклянный поплавок с грузом и нанесенными на нем делениями, соответствующими измеряемым значениям.
- С одной стороны колбы одевается резиновая груша, предназначенная для засасывания электролита внутрь колбы.
- С противоположной стороны – резиновый носик, через который происходит забор жидкости из заливного отверстия АКБ.

Измеряемое значение определяется по той черте на поплавке, до которой доходит жидкость, набранная в ареометр.
Автомобильный ареометр с одним поплавком
Существуют более простые ареометры, в которых в колбе находятся несколько грузиков-палочек с разным весом у каждой. На каждом грузике (или на самой колбе напротив него) нанесено соответствующее значение плотности. Результат измерения определяется по максимальному значению всплывших грузиков. Такой ареометр более дешевый, но не обладает достаточной точностью.
Автомобильный ареометр с несколькими поплавками
Само измерение ареометром проводится так:
- Носик ареометра опускается в аккумулятор через заливное отверстие. Есть приборы не с резиновым, а с пластиковым носиком. В этом случае нужно погружать его в электролит осторожно, чтобы не повредить свинцовые пластины.
- С помощью груши в колбу набирается электролит. Для ареометров с одним поплавком нужно контролировать количество набираемой жидкости.
 Ее должно быть столько, чтобы поплавок свободно плавал внутри колбы. Но нельзя набирать и много жидкости. Тогда поплавок может упереться в верхний край колбы. Показания ареометра в этом случае будут недостоверны.
Ее должно быть столько, чтобы поплавок свободно плавал внутри колбы. Но нельзя набирать и много жидкости. Тогда поплавок может упереться в верхний край колбы. Показания ареометра в этом случае будут недостоверны. - После забора жидкости смотрим – напротив какой риски на поплавке находится ее уровень. Цифры рядом с риской покажут значение плотности.
Для ареометров с несколькими поплавками значение плотности определяется по всплывшим поплавочкам. Плавающий грузик с максимальным числом на нем как раз и показывает результат измерения.
Получение показаний с помощью ареометра
Для аккумуляторных батарей из нескольких элементов проверка проводится отдельно в каждой банке.
Обычная цена деления в аккумуляторных ареометрах составляет 0,01 г/см3. Но выпускаются ареометры и с более точной шкалой.
После окончания измерений необходимо тщательно промыть ареометр дистиллированной водой.
Условия, при которых следует проводить измерения
Прежде чем начать замеры концентрированности электролита, необходимо придерживаться несложных правил. А в некоторых случаях придется корректировать показания ареометра в зависимости от условий, при которых они были получены.
А в некоторых случаях придется корректировать показания ареометра в зависимости от условий, при которых они были получены.
Самым необходимым условием является поддержание требуемого уровня жидкости в самой АКБ. Плотность будет замерена правильно, но для безопасной работы батареи необходимо будет довести уровень до нормы. А это приведет к изменению плотности.
Степень заряженности АКБ
Плотность электролита меняется при заряде/разряде аккумулятора. При разряде она уменьшается, при заряде – увеличивается. В зависимости от степени разряда аккумуляторной батареи значения меняются следующим образом.
Зависимость показаний ареометра от степени заряда батареи
Вряд ли можно точно определить уровень разряда. Поэтому сначала необходимо полностью зарядить аккумулятор, подождать несколько часов, и только потом проводить измерения.
Если с водно-кислотным раствором проводились какие-либо действия – долив дистиллированной воды или самой кислоты, то не стоит замерять плотность сразу после них. Необходимо подождать, пока долитая жидкость полностью перемешается в аккумуляторе.
Необходимо подождать, пока долитая жидкость полностью перемешается в аккумуляторе.
Температура при проведении измерений
Калибровка стандартных ареометров ориентируется на температуру +25 °С. Для получения наиболее точных показаний замеры плотности электролита нужно проводить при такой же температуре. Зимой тестируемую АКБ надо занести в теплое место и дать ей прогреться до нужной температуры. Но не стоит проводить измерения буквально в домашних условиях. Раствор кислоты может случайно испортить мебель или одежду. Лучше воспользоваться отапливаемым помещением, приспособленным для таких работ.
Если же нет возможности проводить измерения при рекомендованной температуре в 20 – 25 °С, то можно сделать замеры при любой температуре, а затем воспользоваться корректировочной таблицей:
Корректировочные значения для измерений при разных температурах
Регулярные проверки плотности электролита в аккумуляторе позволят не только поддерживать его в оптимальных условиях для работы, но и своевременно выявить возможные проблемы и неисправности.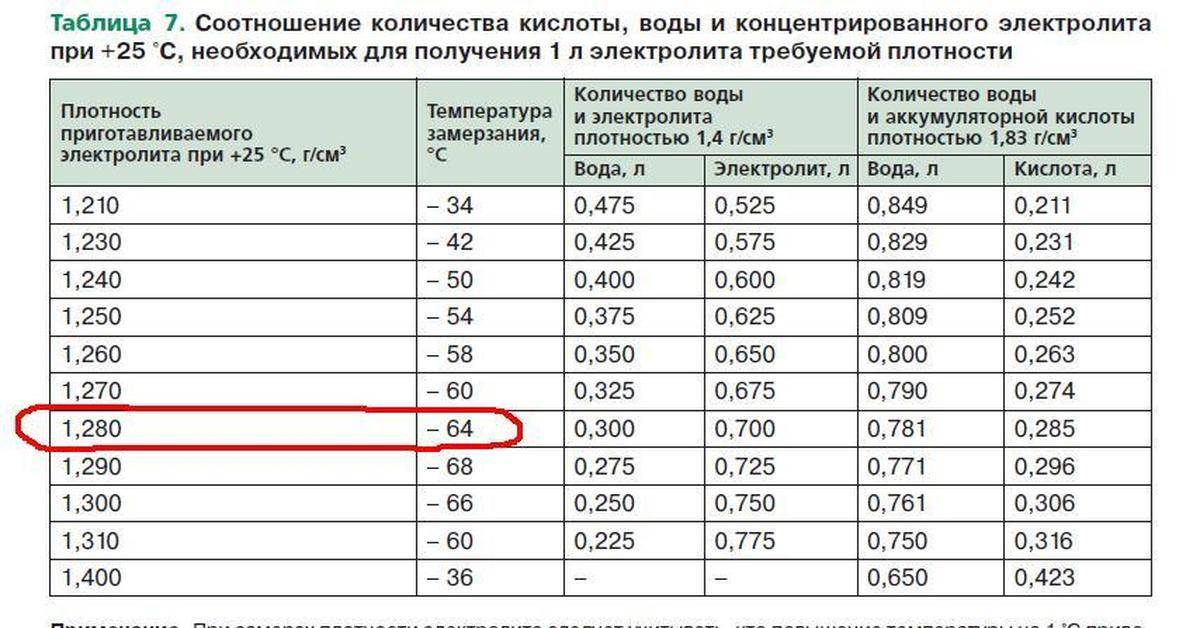
Нам важна ваша оценка!
Холодная погода и ваши батареи.
Холодная погода меняет все.
Сейчас декабрь, и на большей части территории США нас ждут серьезные холода. Холод оказывает большое негативное влияние на автономное питание и радиолюбительское оборудование. Если вы не учли холодную погоду должным образом, ваше снаряжение подведет вас, когда оно вам больше всего понадобится. В некоторых случаях отсутствие планирования в холодную погоду может привести к дорогостоящему ущербу. Сегодня мы обсудим влияние низких температур на ваше оборудование и аккумуляторы. Если вы живете в районе, где всегда тепло, я надеюсь, что вы все равно останетесь с нами и получите полезную справочную информацию.
Радиоприемники на морозе.
Большинство современных радиоаппаратур достаточно хорошо переносят низкие температуры. Вы можете заметить, что в холодную погоду циферблаты поворачиваются с трудом, а переключатели кажутся немного тяжелыми. ЖК-дисплеи также могут иметь медленный/запаздывающий отклик, а батареи работают не так долго, как обычно. Технические характеристики, касающиеся рабочей температуры окружающей среды, имеют тенденцию быть щедрыми на верхнем уровне и не такими щедрыми на низком уровне. Например, Yaesu FT-818 имеет указанный рабочий диапазон 14-140F (от -10C до +60C). Маловероятно, что вы когда-нибудь увидите 140F, но 14F довольно распространены для многих из нас.
Технические характеристики, касающиеся рабочей температуры окружающей среды, имеют тенденцию быть щедрыми на верхнем уровне и не такими щедрыми на низком уровне. Например, Yaesu FT-818 имеет указанный рабочий диапазон 14-140F (от -10C до +60C). Маловероятно, что вы когда-нибудь увидите 140F, но 14F довольно распространены для многих из нас.
Принося радиоприемники внутрь с холода, некоторые радиолюбители настаивают на том, чтобы их оборудование прогрелось до комнатной температуры, прежде чем включать его. Это не так важно, как в те времена, когда в радиоприемниках были лампы. О чем должны заботиться современные радиолюбители, так это о конденсате. Если на радиоприемнике образовался конденсат, когда его принесли с холода, дайте ему полностью высохнуть, прежде чем включать его. Имейте в виду, что внутренности радиоприемника будут дольше нагреваться и рассеивать воду, чем внешние поверхности. Холод не убивает радио… но вода убивает!
Залитые батареи и холодная погода.
Это помогает понять, как температура влияет на химический состав и емкость батареи. Типичная полностью заряженная залитая батарея будет иметь плотность электролита около 1,265, измеренную ареометром. Важно знать, что 1.265 предполагает стандартную базовую температуру батареи 80F (27C). Чтобы компенсировать температуру, вычтите 0,004 на каждые десять градусов ниже 80F (27C).
Типичная полностью заряженная залитая батарея будет иметь плотность электролита около 1,265, измеренную ареометром. Важно знать, что 1.265 предполагает стандартную базовую температуру батареи 80F (27C). Чтобы компенсировать температуру, вычтите 0,004 на каждые десять градусов ниже 80F (27C).
Например, у вас есть полностью заряженный аккумулятор с температурой электролита 50F (10C). Занимаюсь математикой:
1,265 (измеренная плотность электролита батареи)
-0,012 (0,004 x 3, учитывая разницу между стандартизированной базовой температурой и фактической температурой)
=1,253 (измерение плотности с поправкой на температуру).
Плотность 1,253 соответствует около 92%-95% для нашей «полностью заряженной» залитой батареи при 50F (10C). Ссылаясь на график ниже, от 50F падение становится более выраженным. Некоторые солнечные контроллеры имеют отдельный датчик температуры. Этот датчик присоединяется к клемме аккумулятора и позволяет контроллеру изменять ток или напряжение для компенсации температуры.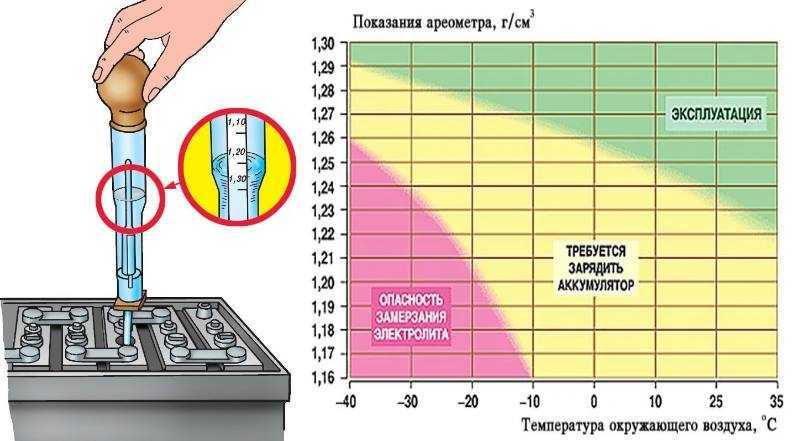 Эти устройства работают до определенного момента, но реалии химии нельзя полностью отрицать. В холодную погоду ваша залитая батарея просто уменьшит емкость.
Эти устройства работают до определенного момента, но реалии химии нельзя полностью отрицать. В холодную погоду ваша залитая батарея просто уменьшит емкость.
Кривая температуры залитой батареи. ГРАФИКА ПРЕДОСТАВЛЕНА ROLLS BATTERY USA.
Залитые аккумуляторы и фактор замерзания.
Поскольку плотность электролита изменяется в зависимости от цикла зарядки-разрядки, изменяется и температура его замерзания. Это оказывает значительное влияние на вашу залитую батарею.
Электролит в полностью заряженной батарее замерзает при температуре -80F (-62C). Скорее всего, вы никогда этого не увидите, но разряженная батарея замерзнет примерно при 20F (-7C). Имейте в виду, что эти цифры относятся к температуре замерзания электролита, а не к допустимым рабочим температурам. Как только батарея физически замерзнет, она, скорее всего, исчезнет навсегда.
В холодную погоду залитые аккумуляторы разряжаются дольше. Это может показаться плюсом, но помните, что вы теряете часть своей емкости из-за холода. Это сделка с нулевой суммой. С другой стороны, холодные батареи также требуют больше времени для перезарядки.
Это сделка с нулевой суммой. С другой стороны, холодные батареи также требуют больше времени для перезарядки.
Примите во внимание, что чем ниже температура, тем дольше будут заряжаться залитые батареи и тем меньше их емкость. Держите их как можно ближе к «сладкой точке» 80F (27C).
AGM, SLA и гелевые аккумуляторы.
Я объединяю аккумуляторы с абсорбированным газовым матом (AGM), герметичными свинцово-кислотными (SLA) и гелевыми элементами, потому что они являются родственниками друг друга и имеют схожие характеристики.
Тем не менее, найти достоверные данные о том, как эти батареи реагируют на холодную погоду, на удивление трудно. Я нашел одно исследование, в котором было установлено, что батареи AGM/геля могут терять до 76% своей емкости при -4F (-20C). Хорошей новостью является то, что если батареи физически не заморозить (что не происходит примерно до -75F или -60C), они восстановят свою полную емкость после того, как снова нагреются.
По большинству показателей аккумуляторы AGM/SLA/гелевые ненамного лучше работают в холодную погоду, чем залитые версии. Многие производители рекомендуют вообще не заряжать батарею, если она ниже 32F (0C). Это, конечно, огромная проблема для многих радиолюбителей. С другой стороны, небольшие AGM/SLA/гелевые батареи, обычно используемые радиолюбителями, относительно недороги. Если их нужно заменять каждый год или около того из-за неправильного обращения, это не большие финансовые затраты.
Многие производители рекомендуют вообще не заряжать батарею, если она ниже 32F (0C). Это, конечно, огромная проблема для многих радиолюбителей. С другой стороны, небольшие AGM/SLA/гелевые батареи, обычно используемые радиолюбителями, относительно недороги. Если их нужно заменять каждый год или около того из-за неправильного обращения, это не большие финансовые затраты.
Вот несколько советов по использованию вашей AGM/SLA/гелевой батареи в холодную погоду:
- Поддерживайте температуру выше 32F (0C) насколько это возможно.
- Избегайте зарядки при температуре ниже 32F (0C).
- Используйте зарядное устройство или контроллер заряда, предназначенные для аккумуляторов AGM/SLA/гелевых аккумуляторов. Многие солнечные контроллеры заряда имеют выбираемые пользователем настройки для различных типов батарей.
Литиевые батареи.
Как и в случае с другими, есть хорошие и плохие новости относительно литиевых батарей в холодную погоду.
Хорошей новостью является то, что они не демонстрируют потери емкости из-за холода, как другие типы.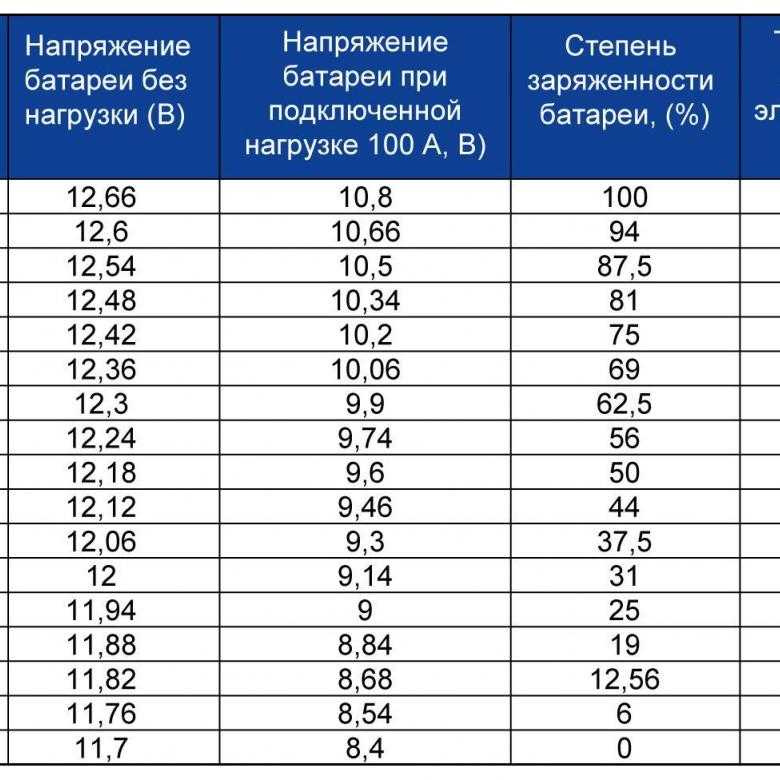 При 32F (0C) литиевая батарея обычно теряет около 17% своего заряда. При температуре -4F (-20C) обычная литиевая батарея будет иметь 70% своей емкости. В этом отношении литиевые батареи явно превосходят другие типы батарей даже при температуре выше 0°F (-17°C). Эти факторы, а также превосходная плотность энергии делают литиевые батареи фаворитом многих радиолюбителей.
При 32F (0C) литиевая батарея обычно теряет около 17% своего заряда. При температуре -4F (-20C) обычная литиевая батарея будет иметь 70% своей емкости. В этом отношении литиевые батареи явно превосходят другие типы батарей даже при температуре выше 0°F (-17°C). Эти факторы, а также превосходная плотность энергии делают литиевые батареи фаворитом многих радиолюбителей.
ГРАФИКА ПРЕДОСТАВЛЕНО SMARTBATTERY
Плохая новость заключается в том, что литиевые батареи очень легко повредить, если их заряжать при температуре ниже 32F (0C). Явление, известное как литиевое покрытие , может возникнуть во время процесса зарядки. Холод заставляет литий собираться на поверхности графитового анода, а не поглощаться им. Как только это происходит, это необратимо. Аккумулятор может быть безвозвратно испорчен, если зарядить его в холодном состоянии даже один раз.
Растворы для зарядки лития на морозе.
Что ты умеешь? Одна из возможностей — резко уменьшить зарядный ток. Хотя это звучит просто в теории, на практике это сложно. Если ваша электроника на аккумуляторе не может связываться с зарядным устройством и давать ему команды на снижение тока в зависимости от температуры, это не реальное решение. Тем не менее, технология существует для тех, кто хочет пойти по этому пути. Даже в этом случае у вас будет больше времени зарядки.
Хотя это звучит просто в теории, на практике это сложно. Если ваша электроника на аккумуляторе не может связываться с зарядным устройством и давать ему команды на снижение тока в зависимости от температуры, это не реальное решение. Тем не менее, технология существует для тех, кто хочет пойти по этому пути. Даже в этом случае у вас будет больше времени зарядки.
Менее сложный вариант — прогреть аккумулятор до температуры выше 32F (0C) перед зарядкой. Нагрейте аккумулятор в автомобиле, кемпере, палатке или даже теплом собственного тела, если он достаточно мал, чтобы носить его в кармане.
По моему собственному опыту, я обнаружил, что довольно легко не дать моим литиевым батареям переохладиться для зарядки. Я живу в районе Верхнего Среднего Запада/Великих озер США, и поверьте мне, у нас есть много возможностей проверить пределы нашего снаряжения в холодную погоду! Хотя температурные ограничения для литиевых аккумуляторов звучат очень обременительно, при небольшой предусмотрительности это не является большой проблемой.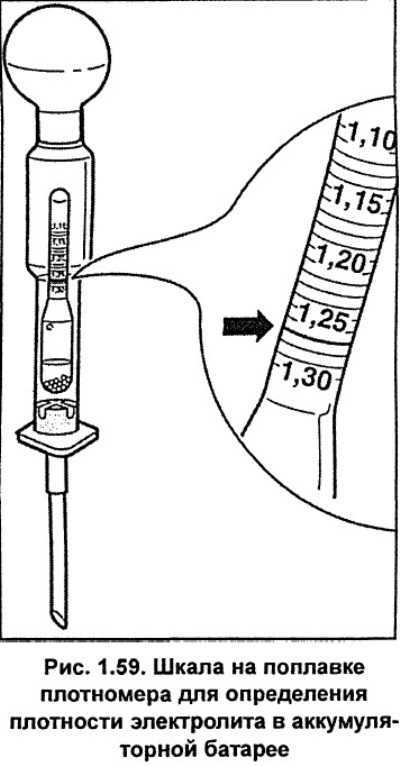
Что мы узнали сегодня.
- Радиооборудование обычно выдерживает низкие температуры, если оно остается сухим.
- Холодная погода негативно влияет на все батареи.
- Плотность электролита в залитых батареях имеет коэффициент температурной компенсации -0,004 на каждые десять градусов ниже 80F (62C).
- Температура замерзания электролита зависит от уровня заряда.
- Никогда не допускайте физического замерзания залитых аккумуляторов. Аккумуляторы
- AGM/SLA/гелевые имеют такую же потерю емкости при низких температурах, как и залитые аккумуляторы.
- Замораживание не приводит к долговременному повреждению аккумуляторов AGM/SLA/гелевых аккумуляторов.
- Низкие температуры не влияют на литиевые батареи так сильно, как на другие типы батарей.
- Зарядка литиевой батареи при температуре ниже 32F (0C) может привести к ее необратимому повреждению.
- Литиевое покрытие — это состояние, при котором литий связывается с поверхностью графитового анода.

Ресурсы.
Этот очень хороший одностраничный список от Canada Battery предлагает несколько отличных советов по аккумуляторам AGM.
НАСА выпустило очень увлекательный и подробный PDF-файл о литиевых покрытиях. Этому документу девять лет, и с тех пор появились новые разработки, но представленные основные концепции по-прежнему актуальны.
Вот несколько предыдущих статей Off Grid Ham , в которых содержится дополнительная информация:
Литиевые батареи
Аккумуляторы AGM
Уход и обслуживание залитых аккумуляторов.
Сколько батареи вам действительно нужно?
Нравится:
Нравится Загрузка…
Коррекция плотности электролита АКБ перед зимой
О доливке дистиллированной воды в АКБ, после двух лет эксплуатации без обслуживания.
После доливки до МАХ дистиллированной воды в каждую банку (0,5 л на 6 банок) и зарядки автоматическим зарядным устройством током от 2 А до 0,5 А в течение 20 часов, после суток работы измерил плотность электролита в банки.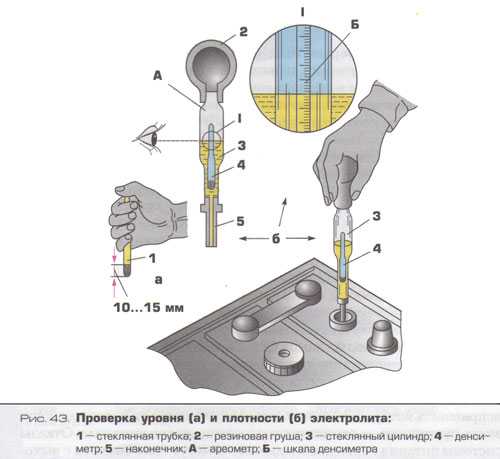
Оказалось, что в средних четырех банках плотность одинакова — 1,27, а в двух крайних банках (левом и правом) чувствительно меньше — 1,23; 1.24.
Погуглив, почитав разные статьи на эту тему, выяснил, что как бы не доделывали, неплохо бы позаботиться о продлении срока службы батареи 🙂
Если зарядка не помогла выровнять плотность электролита, необходимо выровнять с помощью концентрированного электролита плотностью 1,4.
Я по пути бросился в магазины по продаже аккумуляторов и автомагазины.
К моему удивлению, концентрированного электролита нигде не было.
В одном из магзиков консультант поделился, что плотность 1,4 запрещена и давно не производится, а стандартный корректирующий электролит плотностью 1,33 уже три месяца не поставляется, в связи с какими-то предстоящими изменения в законодательстве и скорее всего корректирующие будут меньшей плотности.
Правда или нет, но за что купил, за то и продаю:)
Заехал на авторынок, где много мелких магазинчиков-палаток и в одном из них не было проблем с коррекционным электролитом 1,33, для всего 70 рублей 🙂
Итак, что и сколько заливать/доливать. ..
..
Статьи в инете в основном старые, т.к. аккумулятор уже давно перешел в разряд расходников и мало кто обращается в сервис Это.
За основу расчетов взято
Суть коррекции плотности электролита в банке аккумуляторов заключается в следующем:
а) из банки берется некоторое количество электролита;
б) вместо этого в банку добавляют тот же объем либо дистиллированной воды (плотностью 1,00) — для понижения плотности электролита в банке, либо для корректировки электролита (обычно плотностью 1,40) — для увеличить плотность;
Равенство объемов забираемой и добавляемой жидкостей используется только для упрощения всей процедуры и упрощения логической интерпретации ее результатов.
По мере накопления опыта это равенство может нарушаться.
а) аккумулятор включается на 30 минут для заряда номинальным током для лучшего перемешивания электролита в результате газовыделения;
г) аккумулятор отключают от зарядного устройства и выдерживают в течение 0,5÷2 ч для выравнивания плотности электролита в объеме банок;
д) измеряется плотность электролита в каждой банке и его уровень, оба параметра нормируются.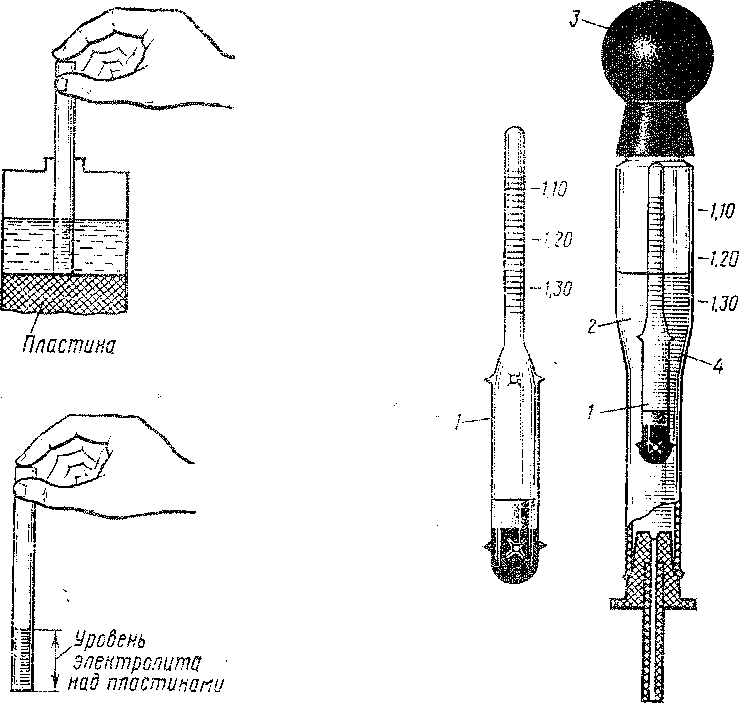
Тех. при необходимости повторяются все операции а) и д)
Ниже приведена формула, по которой можно применять корректирующий электролит с плотностью, отличной от 1,40
где:
Ve — объем удаленного электролита из банки, см3,
Вб — количество электролита в одной банке, см3,
ρн — начальная плотность электролита до доводки, г/см3,
ρк — конечная плотность, которую необходимо получить, г/см3,
ρd — плотность добавляемой жидкости, (вода — 1,00 г/см3 или электролит корректирующий — * г/см3)
Следует отметить, что при использовании данной формулы объемы удаляемого и добавляемого электролитов равны .
Итак теперь главный вопрос, какой объем электролита в нашей ISTA CALCIUM 12V 70А/ч?
Ответа на него я не нашел, но было решено, по аналогии с размерами наших российских аккумуляторов, за исходник взять объем 6СТ-55(60) — 3,8 л. В итоге выяснилось, что наверное в нашем аккумуляторе около 3,5 литров.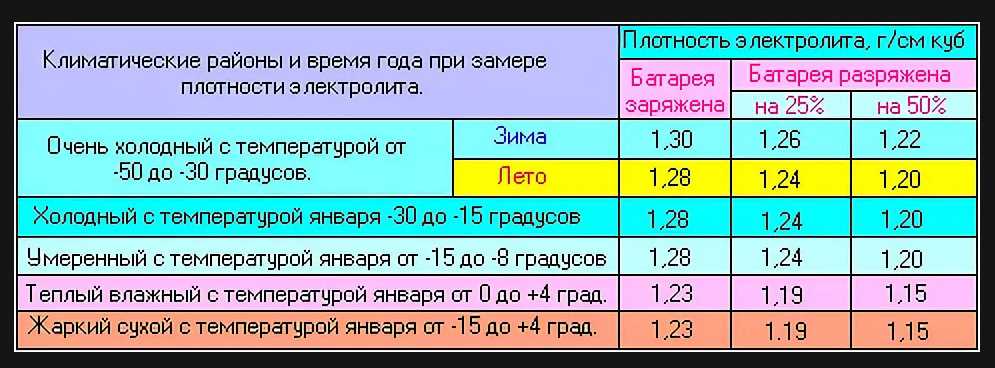
По расчетам при плотности 1,24 необходимо заменить 1,33, примерно 211 см3, на корректирующий электролит.
Чтобы не ошибиться, для начала из каждой крайней банки было отобрано четыре раза по 40 единиц указанного на колбе объема ареометра, итого по 160 штук 🙂
Соответственно, столько же и электролита залил 1.33
После смешивания вгляделся 🙂 плотность как раз оказалась 1.27
оставляю заряжаться на 10 часов током от 2 до 0,5 А (автоматическая зарядка) и утром плотность почти 1,32 в каждой банке.
Многовато, но это только сразу после отключения зарядки.
Через пару дней проверяю, что в каждой банке ровно 1.30, во всех шести.
Повторяю процедуру с подменой небольших объемов в каждую банку дистиллированной воды.
В этот раз я взяла по 60 см3 из каждой банки, залив вместо нее перегонку.
Полчаса подзарядил, день покатался и на проверку.
Ну а теперь о деле, во всех банках плотность электролита одинаковая — 1,26
для скоротечного лета в самый раз 🙂
срок службы батарей еще на три года, то в принципе не напрягает.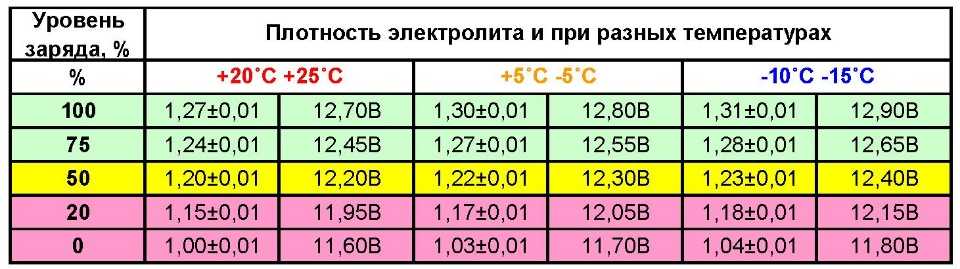
А когда знаешь, что мерить и доливать, то абсолютно все просто.
Следующая проверка в октябре/ноябре 🙂
PS : прошло более полутора лет с момента данной операции с корректирующим электролитом и после этого я читал много мнений что корректировать плотность таким способом нельзя, правильный вариант только полная зарядка аккумулятора стационарное зарядное устройство, у которого в итоге после полного заряда получается перекос по плотности в банках… НО , буквально на днях меня смутил полный заряд аккумулятора в несколько этапов и как в итоге в этих крайних банках плотность в конце заряда такая же как и в остальных — 1,27 все норм.
В этот раз вышла из строя только одна банка в середине, всего 1,27, и в одной 1,25 после полной зарядки.
КТС на АКБ держится, полная зарядка сделана, думаю ничего не терять, с одной средней можно повторю исполнение с корректирующим электролитом
Метка: 70 ₽ Пробег 32400 км
Периодичность
Каждые 15000 км проверяйте уровень и плотность электролита.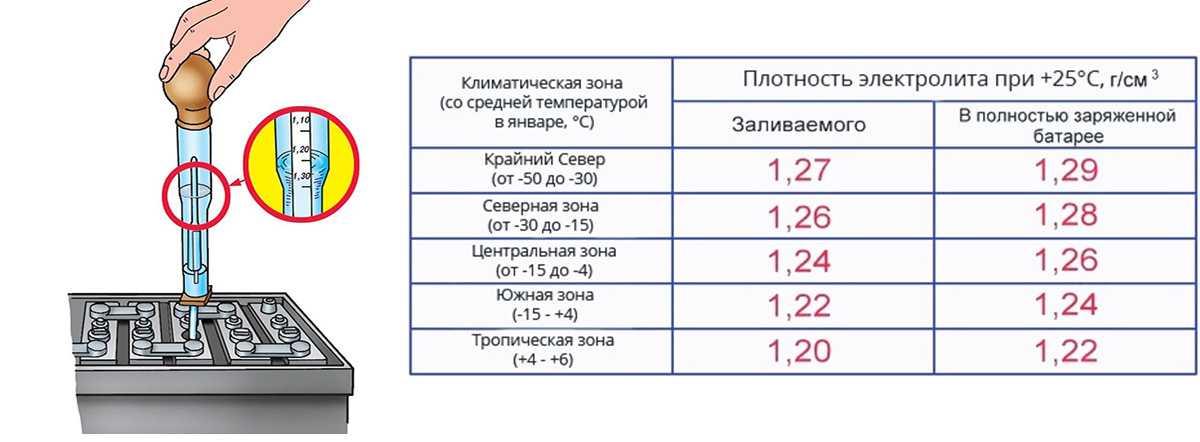
Регулярно очищайте аккумулятор от пыли и грязи. Если на корпусе есть трещины или вздутие верхней крышки, замените батарею.
Электролит должен быть прозрачным. Коричневый оттенок указывает на осыпание активной массы пластин – необходимо менять батарею.
Предупреждения
В процессе эксплуатации уровень электролита постепенно снижается из-за испарения воды, входящей в его состав. Для восстановления уровня доливайте в аккумулятор только дистиллированную воду.
При проверке плотности будьте внимательны: в состав электролита входит серная кислота! Капли электролита на детали автомобиля или на открытые участки тела немедленно смыть большим количеством воды.
Во время зарядки аккумулятора Не курите и не пользуйтесь открытым огнем.
Перед зарядкой снимите аккумулятор с автомобиля, иначе «закипевший» электролит может пролиться на кузов и детали автомобиля.
Таблица 1. Коррекция плотности электролита в зависимости
от температуры
Температура электролита, °С | Поправка, г/см 3 |
От -40 до -26 | |
От -25 до -11 | |
От -10 до +4 | |
от +5 до +19 | |
от +20 до +30 | |
+31 до +45 |
Таблица 2.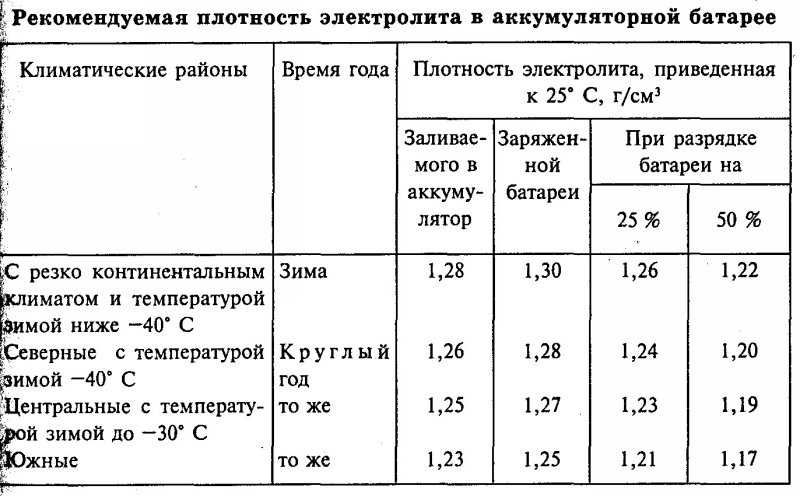 Плотность электролита при 25°С, г/см 3
Плотность электролита при 25°С, г/см 3
Климатический район (среднемесячная температура воздуха в январе, °С) | Сезон | Полностью заряженный аккумулятор | Аккумулятор заряжен | |
Очень холодный | Зима | |||
Холодный | Круглый год | |||
Умеренная | Круглый год | |||
Теплый влажный | Круглый год | |||
Горячесухое | Круглый год | |||
Таблица 3. Ориентировочные нормы регулировки плотности электролита
Ориентировочные нормы регулировки плотности электролита
Требуемая плотность электролита в аккумуляторе, г/см 3 | ||||
Реальная плотность электролита, г/см 3 | Объем электролита, удаленного из аккумулятора, см 3 | |||
ПОРЯДОК ВЫПОЛНЕНИЯ
| ||||||||||||||||||||||||||||
› Коррекция плотности электролита аккумулятора перед зимой!
Подготовка к регулировке.
Измерение уровня электролита.
Трубка для измерения уровня электролита.
Перед проверкой плотности электролита и в процессе ее регулировки необходимо следить за уровнем электролита в банках аккумуляторов. В автомобильных аккумуляторах нормальным считается уровень электролита на 10 ÷ 15 мм выше верхнего края пластин (сепараторов).
В батареях с индикатором (трубкой) электролит должен быть на одном уровне с ним или выше его на 5 мм.
Корректирующий электролит — электролит повышенной плотности (обычно 1,40 г/см3) для повышения плотности электролита аккумуляторной батареи или приготовления электролита нормальной плотности для зарядки аккумуляторной батареи.
Вода дистиллированная.
Добавляется в электролит для снижения его плотности.
Важные детали
1. В связи с тем, что кислота и вода имеют разную плотность, при разбавлении электролита или кислоты водой кислоту следует добавлять в воду, а не наоборот.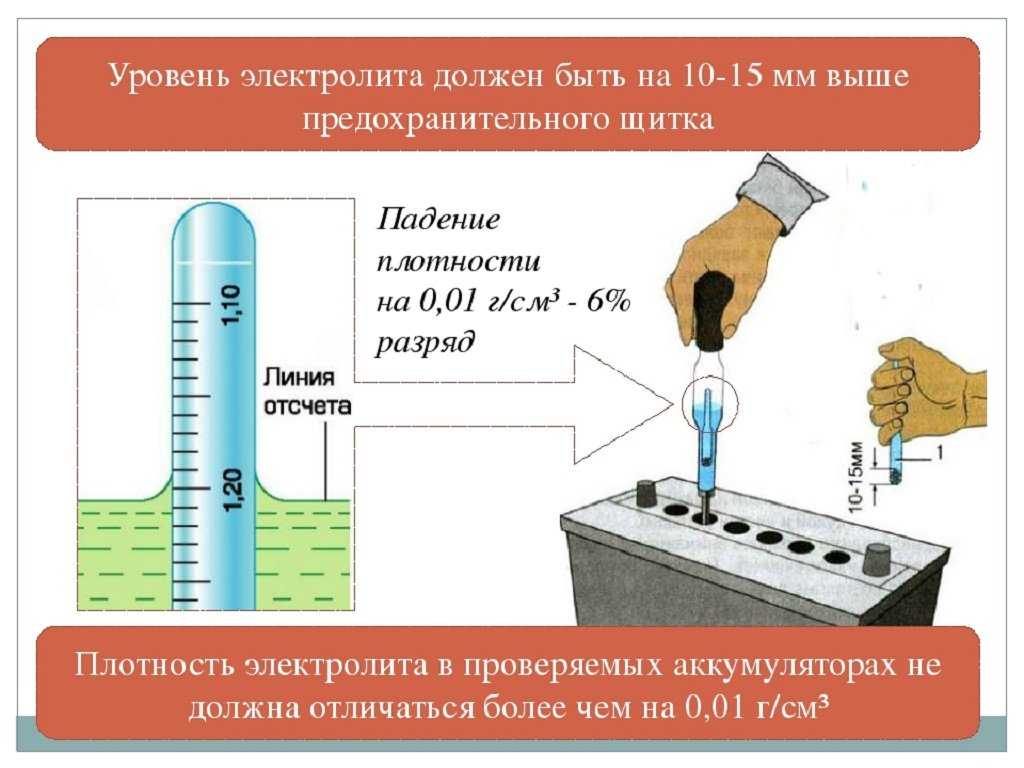
2. Обращайтесь с аккумулятором очень осторожно. Ни в коем случае нельзя его переворачивать. Это может привести к падению пластин и последующему выходу из строя батареи.
Определение требуемого значения плотности электролита полностью заряженного аккумулятора.
На протяжении всего срока службы батареи плотность электролита постоянно меняется. Есть обратимые изменения плотности — это нормальный заряд и разряд батареи. Интервал изменения плотности электролита при изменении состояния аккумулятора с полностью разряженного на полностью заряженный и наоборот обычно составляет для нового аккумулятора 0,15÷0,16 г/см3.
Но бывают и необратимые изменения, такие как электролиз воды (разложение на водород и кислород) при «кипении» электролита. Плотность электролита увеличивается.
При сульфатации пластин, когда их активная поверхность покрыта слоем нерастворимого сульфата свинца или осыпается активная масса пластин, что уменьшает площадь поверхности пластин, которая участвует в электрохимической реакции — восстановить первоначальную плотность электролита во время зарядки невозможно. Это приводит к необратимому снижению плотности электролита и, соответственно, сужает диапазон изменения плотности в диапазоне полный заряд — полный заряд (0,15 ÷ 0,16 г/см3 — для новой исправной батареи).
Это приводит к необратимому снижению плотности электролита и, соответственно, сужает диапазон изменения плотности в диапазоне полный заряд — полный заряд (0,15 ÷ 0,16 г/см3 — для новой исправной батареи).
Постоянно повышенная плотность электролита приводит к уменьшению срока службы батареи.
Стабильно заниженная плотность приводит к снижению ЭДС и затруднению запуска двигателя, а также к повышенному риску замерзания электролита в зимний период эксплуатации.
Для начала нужно определиться, какую плотность электролита мы хотим иметь в нашем аккумуляторе применительно к климатической зоне его эксплуатации.
В этой таблице указана температура замерзания электролита.
Например, для центральных районов России (Москва, Казань…) можно выбрать плотность электролита 1,25÷1,27 г/см3. Необходимо помнить, что на автомобиле аккумуляторная батарея в лучшем случае может быть заряжена до 80÷90% ее максимальной емкости (то есть плотность электролита будет несколько ниже, чем при полной зарядке). Поэтому плотность электролита, исходя из температуры его замерзания (таблица), выбирают несколько большей, чем необходимо для обеспечения гарантированного незамерзания при минимальной температуре воздуха в зимний период.
Поэтому плотность электролита, исходя из температуры его замерзания (таблица), выбирают несколько большей, чем необходимо для обеспечения гарантированного незамерзания при минимальной температуре воздуха в зимний период.
Полная зарядка аккумулятора.
Необходимо четко понимать и строго соблюдать правило:
Проверка плотности электролита, с целью определения необходимости его регулировки, проводится только при ПОЛНОСТЬЮ ЗАРЯЖЕННОЙ АККУМУЛЯТОРНОЙ БАТАРЕЕ.
Известно, что при исправном генераторном оборудовании автомобиля и его нормальном напряжении 14,0 ÷ 14,6 В возможна зарядка аккумуляторной батареи только на 80 ÷ 90% от ее максимальной емкости из-за неэффективности процесса зарядки аккумуляторной батареи на транспортном средстве. .
При выборе зарядного устройства следует избегать использования «автоматических зарядных устройств» без предварительного ознакомления с логикой его автоматики. Во многих из них автоматическое отключение режима заряда производится просто при достижении напряжения на клеммах аккумулятора 14,5÷14,6 В, а это не всегда обеспечивает полный заряд аккумулятора.
Признаком ПОЛНОГО заряда аккумулятора является постоянство плотности электролита и напряжения на его клеммах при продолжении зарядки в течение 2-х часов.
При достижении условий полного заряда батареи, то есть постоянства напряжения на клеммах и плотности электролита в течение двух часов при продолжении зарядки, ее останавливают и выдерживают батарею от 30 минут до двух часов в выключенном состоянии.
Рекомендуется производить отключение в выключенном состоянии от получаса до двух часов после зарядки (разрядки), заливки (регулировки плотности) электролита, регулировки уровня электролита. Это делается для выравнивания плотности электролита в объеме банок, для снижения температуры электролита, выхода пузырьков газа, образующихся при «закипании». В противном случае возможны недопустимые погрешности измерения плотности и уровня электролита, а также напряжения на клеммах аккумулятора.
Затем измеряется уровень электролита и его плотность в каждой банке. Если замечена значительная разница плотности электролита между банками (более 0,01 г/см3), следует попытаться провести дополнительную, так называемую уравнительную зарядку аккумулятора для выравнивания плотности между банками, при этом ток заряда можно снижается в 2 ÷ 3 раза по сравнению с номинальной, для уменьшения газообразования («кипения»).
Если подзарядка в течение нескольких часов не выравнивает плотность электролита в банках, очевидно, необходимо выровнять ее путем последующей коррекции.
По завершении данного этапа работ оформляется этикетка с указанием плотности и уровня электролита в каждой банке. Принимается решение, какие действия производить над каждой конкретной банкой. За основу взято соотношение плотности электролита, которое мы приняли как оптимальный вариант для нашей климатической зоны, и реального значения, измеренного после полной зарядки аккумулятора.
Коррекция плотности электролита.
Суть коррекции плотности электролита в банке аккумуляторов заключается в следующем:
а) из банки отбирается некоторое количество электролита;
б) вместо этого в банку добавляют такой же объем либо воды дистиллированной (плотность 1,00 г/см3) — для уменьшения плотности электролита в банке, либо корректирующего электролита (обычно плотностью 1,40 г/см3 ) — для увеличения плотности;
в) аккумулятор включают на 30 мин для заряда номинальным током для лучшего перемешивания электролита в результате газовыделения;
г) аккумуляторную батарею отключают от зарядного устройства и выдерживают в течение 0,5÷2 ч для выравнивания плотности электролита в объеме банок;
д) измеряли плотность электролита в каждой банке и его уровень, оба параметра нормированы. То есть при необходимости все операции а)÷д) повторяются.
То есть при необходимости все операции а)÷д) повторяются.
Приведу таблицу, в которой указано «…сколько повесить в граммах», то есть указать конкретное количество в см3 удаляемого электролита и соответствующее количество добавляемой жидкости (воды дистиллированной или корректирующей электролита в зависимости от направления изменения плотности).
Объем жидкости указан для корректировки 1 л электролита (1000 см3). Таким образом, чтобы скорректировать конкретный аккумулятор, нам необходимо знать количество электролита в одной банке этого аккумулятора в литрах. Полученные из таблицы значения необходимо умножить на объем электролита в литрах в одной банке регулируемого аккумулятора.
Количество электролита в одной банке:
6СТ-45 — 500 см3;
6СТ-55 — 633 см3.
Ориентировочные нормы в см3 регулировка плотности электролита в объеме 1 л.
В таблице предусмотрено использование корректирующего электролита плотностью всего 1,40 г/см3. Ниже приведена формула, по которой можно использовать корректирующий электролит с плотностью, отличной от 1,40 г/см3.
где
Ve — объем электролита, удаленного из банки, см3,
Vb — объем электролита в одной банке, см3,
для некоторых типов аккумуляторов, объем электролита в одной банке указывается чуть выше по тексту,
ρn — исходная плотность электролита до регулировки, г /см3,
ρк – конечная плотность, которую необходимо получить, г/см3,
ρд – плотность добавляемой жидкости, (вода – 1,00 г/см3 или корректирующий электролит – *г/см3)
Следует отмечено, что при использовании этой формулы объемы удаляемого и добавляемого электролитов равны.
Если таблицу трудно понять! Вы можете сделать это позже:
Выкачать большую часть жидкости из одной из банок. Эту операцию удобно выполнять с помощью «груши». Измерьте эвакуированный объем и добавьте около половины этого объема электролита. Аккуратно покачайте батарею в разные стороны, затем снова измерьте плотность. Если плотность не достигла необходимого значения, долить еще от объема, сдутого ранее с электролитом. Таким образом, необходимо доливать электролит, каждый раз уменьшая его количество вдвое.
Таким образом, необходимо доливать электролит, каждый раз уменьшая его количество вдвое.
Цена вопроса: 200 ₽
Аккумулятор — один из основных элементов автомобиля, отвечающий за запуск двигателя. Значение аккумулятора трудно переоценить, ведь без него невозможно запустить двигатель, а, следовательно, автомобиль своим ходом двигаться не может. Именно поэтому батарея требует особого внимания, исключающего возникновение неприятных ситуаций в виде невозможности совершить запланированную поездку. Стоит отметить, что для поддержания работоспособности этого важного источника питания не нужно предпринимать никаких сверх усилий, а достаточно провести лишь небольшой комплекс профилактических мероприятий.
Свинцовая аккумуляторная батарея представляет собой гальванический элемент, внутри которого химическая энергия преобразуется в электрическую в результате протекающих реакций. Этот процесс невозможен без электролита — раствора кислоты, обеспечивающего движение заряженных частиц между погруженными в него электродами. Как правило, электролит представляет собой водный раствор серной кислоты определенной плотности. Именно такой параметр, как плотность электролита, оказывает существенное влияние на работоспособность аккумулятора, поэтому периодически его необходимо контролировать.
Как правило, электролит представляет собой водный раствор серной кислоты определенной плотности. Именно такой параметр, как плотность электролита, оказывает существенное влияние на работоспособность аккумулятора, поэтому периодически его необходимо контролировать.
Измерение плотности электролита аккумулятора
Измерить плотность залитого в свинцовый аккумулятор электролита не так уж сложно, но есть определенные нюансы, связанные с особенностями устройства и принципом работы аккумулятора. Перечислим некоторые важные моменты, которые следует учитывать:
- Проводить процедуру измерения плотности получится только в случае так называемой обслуживаемой батареи, которая обеспечивает доступ к банкам (секциям) с электролитом через крышки заливочные отверстия. Именно через эти отверстия (обычно их количество равно шести, как и количество секций) берется состав для измерения плотности.
- В процессе своей работы автомобильный аккумулятор постоянно заряжается и разряжается.
 Разрядка происходит при прокручивании стартера, а заряд — когда двигатель уже работает от генератора. В зависимости от степени заряда меняется и плотность электролита. Значения могут варьироваться в пределах 0,15-0,16 г/см 3 . Важно учитывать, что автомобильный генератор не способен полностью зарядить аккумулятор. При нормальной работе на машине потенциал аккумулятора используется только на 80-90%. Полную зарядку может обеспечить только внешнее зарядное устройство, к которому обязательно придется прибегнуть перед измерением плотности электролита.
Разрядка происходит при прокручивании стартера, а заряд — когда двигатель уже работает от генератора. В зависимости от степени заряда меняется и плотность электролита. Значения могут варьироваться в пределах 0,15-0,16 г/см 3 . Важно учитывать, что автомобильный генератор не способен полностью зарядить аккумулятор. При нормальной работе на машине потенциал аккумулятора используется только на 80-90%. Полную зарядку может обеспечить только внешнее зарядное устройство, к которому обязательно придется прибегнуть перед измерением плотности электролита. - Плотность электролита зависит от его температуры. Обычно измеряется при температуре +25°С, в противном случае вносятся поправки.
Допустим, все вышеперечисленные условия учтены, и можно переходить непосредственно к измерению плотности. Для этого понадобится специальный прибор — плотномер, который состоит из ареометра, резиновой груши и стеклянной трубки с наконечником. Устройство вводят в аккумуляторную батарею через заливное отверстие, а затем резиновой грушей засасывают электролит. Это происходит до тех пор, пока не всплывет ареометр. Показания считываются после того, как колебания ареометра прекратятся и станет возможным определить точное значение. Показания отсчитывают по шкале, при этом смотреть следует на уровень поверхности жидкости.
Это происходит до тех пор, пока не всплывет ареометр. Показания считываются после того, как колебания ареометра прекратятся и станет возможным определить точное значение. Показания отсчитывают по шкале, при этом смотреть следует на уровень поверхности жидкости.
Полученное значение должно быть в пределах 1,25-1,27 г/см 3 , если автомобиль эксплуатируется в средней полосе. В зоне холодного климата (среднемесячная температура января ниже -15°С) показатель должен быть в пределах 1,27-1,29 г/см 3 . Проверяют плотность электролита на соответствие этим цифрам в каждом из шесть банок аккумулятора. Показания не должны отличаться более чем на 0,01 г/см 3 , иначе потребуется их корректировка.
Как мы уже говорили, плотность электролита зависит от температуры. Это означает, что зимой и летом жидкость в одном и том же полностью исправном аккумуляторе будет иметь разную плотность. Следующая таблица дает представление о том, насколько будут отличаться показания.
Зависимость температуры замерзания электролита от его плотности представлена в другой таблице. На основании этих данных можно установить оптимальную плотность электролита для конкретных климатических условий. Нижняя граница выбранного интервала должна обеспечивать, чтобы электролит не замерзал даже при самых сильных морозах и обеспечивать усилие, необходимое для проворачивания стартера. В то же время завышать плотность тоже нельзя, так как положительные электроды аккумулятора начинают ускорять коррозионные процессы, приводящие к сульфатации пластин.
На основании этих данных можно установить оптимальную плотность электролита для конкретных климатических условий. Нижняя граница выбранного интервала должна обеспечивать, чтобы электролит не замерзал даже при самых сильных морозах и обеспечивать усилие, необходимое для проворачивания стартера. В то же время завышать плотность тоже нельзя, так как положительные электроды аккумулятора начинают ускорять коррозионные процессы, приводящие к сульфатации пластин.
Причины изменения плотности электролита
Значения, зафиксированные в результате измерения плотности, не всегда соответствуют требуемым значениям. Расхождения могут касаться как отдельных банок аккумуляторов, так и всех вместе взятых. Если плотность слишком высокая, то нужно в первую очередь обратить внимание на уровень электролита. Низкий уровень в большинстве случаев является следствием электролиза, приводящего к разложению воды, содержащейся в электролите, на водород и кислород. Этот процесс выражается в появлении пузырьков на поверхности жидкости, что обычно происходит при зарядке аккумулятора. Частое «кипячение» может привести к уменьшению концентрации воды, и этот вопрос решается простым ее добавлением. Доливайте в аккумулятор только дистиллированную воду, контролируя уровень электролита. Подробнее о регулировке плотности электролита поговорим ниже.
Частое «кипячение» может привести к уменьшению концентрации воды, и этот вопрос решается простым ее добавлением. Доливайте в аккумулятор только дистиллированную воду, контролируя уровень электролита. Подробнее о регулировке плотности электролита поговорим ниже.
Если с повышенной плотностью все понятно, то с пониженной ситуация несколько сложнее. Теоретически одной из причин снижения плотности может быть то, что по какой-то причине уменьшилась доля серной кислоты в электролите. Однако на практике это маловероятно, так как сам по себе он имеет высокую температуру кипения, исключающую испарение даже при интенсивном нагреве, возникающем, например, при зарядке аккумулятора. Более распространенной причиной снижения плотности электролита является так называемая сульфатация пластин, заключающаяся в образовании на электродах сульфата свинца (PbSO4). На самом деле это естественный процесс, который происходит при каждой разрядке аккумулятора. Но дело в том, что при нормальной работе после разряда аккумулятора аккумулятор необходимо зарядить (на автомобиле аккумулятор постоянно подзаряжается от генератора). Заряд сопровождается обратным превращением сульфата свинца в свинец (на катоде) и диоксида свинца (на аноде) — в те активные вещества, которые составляют основу электродов и принимают непосредственное участие в химическом процессе внутри аккумулятора. Если аккумулятор находится длительное время в разряженном состоянии, сульфат свинца кристаллизуется, безвозвратно теряя способность участвовать в химических реакциях. Это очень неприятный процесс, в результате которого аккумулятор не сможет полностью зарядиться даже при использовании внешнего зарядного устройства из-за того, что в работе задействована не вся площадь пластин. Поскольку аккумулятор не заряжается до конца, плотность электролита не восстанавливается до исходных значений. На самом деле уже идет речь об устранении нарушений в нормальном функционировании аккумулятора.
Заряд сопровождается обратным превращением сульфата свинца в свинец (на катоде) и диоксида свинца (на аноде) — в те активные вещества, которые составляют основу электродов и принимают непосредственное участие в химическом процессе внутри аккумулятора. Если аккумулятор находится длительное время в разряженном состоянии, сульфат свинца кристаллизуется, безвозвратно теряя способность участвовать в химических реакциях. Это очень неприятный процесс, в результате которого аккумулятор не сможет полностью зарядиться даже при использовании внешнего зарядного устройства из-за того, что в работе задействована не вся площадь пластин. Поскольку аккумулятор не заряжается до конца, плотность электролита не восстанавливается до исходных значений. На самом деле уже идет речь об устранении нарушений в нормальном функционировании аккумулятора.
Частичную сульфатацию пластин можно устранить с помощью контрольно-тренировочных циклов, заключающихся в зарядке и последующей разрядке аккумулятора до определенного уровня. Эта функция есть у большинства современных зарядных устройств, поэтому есть смысл ею воспользоваться, особенно если аккумулятор по каким-то причинам долгое время находился в разряженном состоянии. Процедура десульфатации очень длительная и может занимать до нескольких дней. Если она не дает результата, то крайняя мера – увеличение плотности путем добавления корректирующего электролита (плотность около 1,40 г/см 3 ). Такой метод можно рассматривать лишь как временное решение проблемы, ведь причина как таковая не устраняется.
Эта функция есть у большинства современных зарядных устройств, поэтому есть смысл ею воспользоваться, особенно если аккумулятор по каким-то причинам долгое время находился в разряженном состоянии. Процедура десульфатации очень длительная и может занимать до нескольких дней. Если она не дает результата, то крайняя мера – увеличение плотности путем добавления корректирующего электролита (плотность около 1,40 г/см 3 ). Такой метод можно рассматривать лишь как временное решение проблемы, ведь причина как таковая не устраняется.
Как повысить плотность электролита
Уменьшить или увеличить плотность электролита в аккумуляторе можно, откачав определенное его количество и долив дистиллированной воды или электролита большей плотности (корректирующий) . Эта процедура занимает много времени, так как цикл откачки до заполнения может повторяться несколько раз, пока не будет достигнуто желаемое значение. После каждой регулировки нужно поставить аккумулятор на зарядку (не менее 30 минут), а затем дать постоять (0,5-2 часа). Эти действия необходимы для лучшего перемешивания электролита и выравнивания плотности в банках.
Эти действия необходимы для лучшего перемешивания электролита и выравнивания плотности в банках.
В процессе повышения (или понижения) плотности электролита не забывайте о контроле его уровня. Осуществляется стеклянной трубкой с двумя отверстиями по краям. Один край погружается в электролит до соприкосновения с защитной сеткой. Далее верхний конец закрывают пальцем, а саму трубку осторожно приподнимают вместе со столбиком жидкости внутри. Высота этого столбца указывает на расстояние от верхнего края пластин до поверхности залитого электролита. Он должен быть 10-15 мм. Если на аккумуляторе есть индикатор (трубка) или прозрачный корпус с отмеченными минимальными и максимальными отметками, то контролировать уровень намного проще.
Не забывайте, что все операции с электролитом необходимо производить осторожно, используя защитные перчатки и очки.
О доливке дистиллированной воды в аккумулятор, после двух лет эксплуатации без обслуживания.
После доливки до МАХ дистиллированной воды в каждую банку (0,5 л на 6 банок) и зарядки автоматическим зарядным устройством током от 2 А до 0,5 А в течение 20 часов, после суток работы измерил плотность электролита в банки.
Оказалось, что в средних четырех банках плотность одинакова — 1,27, а в двух крайних банках (левом и правом) чувствительно меньше — 1,23; 1.24.
Погуглив, почитав разные статьи на эту тему, выяснил, что как бы он ни был доработан, неплохо бы позаботиться о продлении срока службы батареи 🙂
Если зарядка не помогла выровнять плотность электролита, то необходимо выровнять с помощью концентрированного электролита плотностью 1,4.
Я по пути бросился в магазины по продаже аккумуляторов и автомагазины.
К моему удивлению, концентрированного электролита нигде не было.
В одном из магзиков консультант поделился, что плотность 1,4 запрещена и давно не производится, а стандартный корректирующий электролит плотностью 1,33 уже три месяца не поставляется, в связи с какими-то предстоящими изменения в законодательстве и скорее всего корректирующие будут меньшей плотности.
Правда или нет, но за что купил, за то и продаю:)
Заехал на авторынок, где много мелких магазинчиков-палаток и в одном из них не было проблем с коррекционным электролитом 1,33, для всего 70 рублей 🙂
Итак, что и сколько заливать/доливать. ..
..
Статьи в инете в основном старые, т.к. аккумулятор уже давно перешел в разряд расходников и мало кто обращается в сервис Это.
За основу расчетов взято
Суть коррекции плотности электролита в банке аккумуляторов заключается в следующем:
а) из банки берется некоторое количество электролита;
б) вместо этого в банку добавляют тот же объем либо дистиллированной воды (плотностью 1,00) — для понижения плотности электролита в банке, либо для корректировки электролита (обычно плотностью 1,40) — для увеличить плотность;
Равенство объемов забираемой и добавляемой жидкостей используется только для упрощения всей процедуры и упрощения логической интерпретации ее результатов.
По мере накопления опыта это равенство может нарушаться.
а) аккумулятор включается на 30 минут для заряда номинальным током для лучшего перемешивания электролита в результате газовыделения;
г) аккумулятор отключают от зарядного устройства и выдерживают в течение 0,5÷2 ч для выравнивания плотности электролита в объеме банок;
д) измеряется плотность электролита в каждой банке и его уровень, оба параметра нормируются.
Тех. при необходимости повторяются все операции а) и д)
Ниже приведена формула, по которой можно применять корректирующий электролит с плотностью, отличной от 1,40
где:
Ve — объем удаленного электролита из банки, см3,
Вб — количество электролита в одной банке, см3,
ρн — начальная плотность электролита до доводки, г/см3,
ρк — конечная плотность, которую необходимо получить, г/см3,
ρd — плотность добавляемой жидкости, (вода — 1,00 г/см3 или электролит корректирующий — * г/см3)
Следует отметить, что при использовании данной формулы объемы удаляемого и добавляемого электролитов равны .
Итак теперь главный вопрос, какой объем электролита в нашей ISTA CALCIUM 12V 70А/ч?
Ответа на него я не нашел, но было решено, по аналогии с размерами наших российских аккумуляторов, за исходник взять объем 6СТ-55(60) — 3,8 л. В итоге выяснилось, что наверное в нашем аккумуляторе около 3,5 литров.
По расчетам при плотности 1,24 необходимо заменить 1,33, примерно 211 см3, на корректирующий электролит.
Чтобы не ошибиться, для начала из каждой крайней банки было отобрано четыре раза по 40 единиц указанного на колбе объема ареометра, итого по 160 штук 🙂
Соответственно, столько же и электролита залил 1.33
После смешивания вгляделся 🙂 плотность как раз оказалась 1.27
оставляю заряжаться на 10 часов током от 2 до 0,5 А (автоматическая зарядка) и утром плотность почти 1,32 в каждой банке.
Многовато, но это только сразу после отключения зарядки.
Через пару дней проверяю, что в каждой банке ровно 1.30, во всех шести.
Повторяю процедуру с подменой небольших объемов в каждую банку дистиллированной воды.
В этот раз я взяла по 60 см3 из каждой банки, залив вместо нее перегонку.
Полчаса подзарядил, день покатался и на проверку.
Ну а теперь о деле, во всех банках плотность электролита одинаковая — 1,26
для скоротечного лета в самый раз 🙂
срок службы батарей еще на три года, то в принципе не напрягает.
А когда знаешь, что мерить и доливать, то абсолютно все просто.
Следующая проверка в октябре/ноябре 🙂
PS : прошло более полутора лет с момента данной операции с корректирующим электролитом, и после этого читал много мнений, что корректировать плотность таким способом нельзя, правильный вариант только полностью заряжать аккумулятор стационарным зарядным устройством, что в конечном итоге после полной зарядки приведет к перекосу плотности в банках… НО , буквально на днях меня смутил полный заряд аккумулятора в несколько этапов и как результат, в этих крайних банках плотность в конце заряда такая же как и в остальных — 1,27 все норм.
В этот раз вышла из строя только одна банка в середине, всего 1,27, и в одной 1,25 после полной зарядки.
КТК на АКБ держится, полный заряд произведен, думаю терять нечего, с одним средним можно повторить исполнение с корректирующим электролитом
Цена вопроса: 70 ₽ Пробег: 32400 км
что должно быть в норме (в зима и лето)
Каждый, кто имел дело с аккумуляторными батареями, знает, что их основными характеристиками являются номинальное напряжение и зарядная емкость. Но для поддержания работоспособности батареи не менее важным параметром является плотность батареи. Конечно, на самом деле речь идет о плотности электролита в аккумуляторе. Но часто используется именно это сленговое выражение. Контроль концентрации электролита так же необходим, как и регулярная зарядка источника тока.
Но для поддержания работоспособности батареи не менее важным параметром является плотность батареи. Конечно, на самом деле речь идет о плотности электролита в аккумуляторе. Но часто используется именно это сленговое выражение. Контроль концентрации электролита так же необходим, как и регулярная зарядка источника тока.
На что влияет плотность электролита
В большинстве аккумуляторов используются свинцовые пластины, а рабочей средой является серная кислота, разбавленная водой. Насыщенность раствора, измеряемая в граммах/см3, является характеристикой, влияющей на способность аккумулятора накапливать заряд для последующего использования.
Конструкция свинцово-кислотного аккумулятора
Концентрация кислоты в растворе электролита и характеристики аккумулятора напрямую связаны.
- При низкой плотности снижается и способность источника тока накапливать зарядную емкость, обеспечивающую его работоспособность. При малой плотности аккумулятор быстрее разряжается и не выдает установленный максимальный ток.

- Если значение этого параметра упадет ниже определенного значения, то в мороз вода в электролите может замерзнуть, и аккумулятор полностью выйдет из строя.
- Но при высокой плотности резко ускоряется процесс сульфатации свинцовых пластин. Это означает, что при слабом заряде аккумуляторов на них образуется сульфат свинца, который уже не преобразуется при повторном заряде в свинец. Это также приводит к снижению способности накапливать необходимый заряд, а со временем — к полному выходу из строя аккумулятора.
Поэтому важно поддерживать значение этого параметра в соответствии с установленными и проверенными стандартами. Значительное снижение или превышение нормативных значений не способствует продуктивной работе аккумулятора.
Холод, при котором содержимое батареи может замерзнуть, показаны на рисунке.
Температура замерзания водного раствора кислоты в зависимости от его плотности
Нормативные показатели электролитической плотности
Наверняка многим автомобилистам, знакомым с проблемами сохранения работоспособности аккумуляторов, известна цифра 1,27 г/см3. Такой считается оптимальная плотность, при которой кислотные аккумуляторы способны максимально раскрыть свои возможности.
Такой считается оптимальная плотность, при которой кислотные аккумуляторы способны максимально раскрыть свои возможности.
Но это значение справедливо не для всех. типы аккумуляторов и их рабочие назначения. Кроме того, оптимальная плотность варьируется для разных температур, при которых аккумулятору приходится работать. Поэтому оптимальные значения зимой и летом будут несколько отличаться.
Назначение аккумуляторов свинцово-кислотных
- Стартерные аккумуляторы предназначены для обеспечения максимально возможного тока при запуске различных двигателей. Это, в первую очередь, автомобильные аккумуляторы. Стандартное значение плотности для них составляет 1,26 – 1,28 г/см3.
- Тяговые батареи должны обеспечивать работу электродвигателей постоянного тока в течение длительного времени. Одно из их применений – электромобили и другие электродвижущие средства. Наилучшее значение плотности электролита для этих аккумуляторов также находится в пределах 1,26 – 1,28 г/см3.

- Стационарные батареи применяются для питания любых электрических цепей и устройств. Обычно располагаются в одном месте в помещении. Для них рекомендуется пониженное значение 1,22 — 1,24 г/см3.
Зависит от температуры
Изменяется температура окружающей среды — меняются и значения плотности водного раствора кислоты. При повышении температуры способность аккумулятора накапливать заряд увеличивается примерно на 1% с каждым градусом. С понижением температуры, конечно, эта способность снижается. Поэтому в холодную погоду рекомендуется держать аккумулятор на высоких значениях плотности, а в жару снижать эти показатели.
Работа батареи при различных температурах в зависимости от плотности
Конечно никто не будет заниматься сменой погоды при каждом скачке. Непосредственно перед наступлением холодов полезно немного увеличить плотность батареи, а перед летним сезоном — понизить. Кроме того, существуют нормы оптимальной плотности для районов с разным климатом. Предполагается, что эти нормативные значения будут соблюдаться круглый год, за редким исключением. Для разных регионов считается нормальным:
Предполагается, что эти нормативные значения будут соблюдаться круглый год, за редким исключением. Для разных регионов считается нормальным:
- В холодном климате 1,27 — 1,30 г/см3
- В средней полосе 1,25 — 1,28 г/см3
- В теплых районах 1,22 — 1,25 г/см3
Более подробно эти характеристики указаны в таблице.
Стандартные значения плотности электролита аккумулятора для различных температурных условий
Как проверить плотность электролита в кислотном аккумуляторе
Для проверки этой характеристики доступны простые измерители, называемые автомобильными ареометрами или денсиметрами. Их работа основана на применении закона Архимеда, то есть способности груза погружаться на разную глубину в зависимости от плотности жидкости. Конструктивно ареометр содержит:
- Стеклянная или пластиковая колба.
- Стеклянный поплавок с грузом и маркировкой на нем, соответствующей измеренным значениям.
- На одну сторону колбы надевается резиновая груша, предназначенная для забора электролита в колбу.

- С противоположной стороны находится резиновый патрубок, через который берется жидкость из заливного отверстия аккумулятора.
Измеряемое значение определяется той линией на поплавке, до которой доходит жидкость, собранная в ареометре.
Однопоплавковый автомобильный ареометр
Существуют более простые ареометры, в которых есть несколько небольших стержневых грузов с разным весом для каждого. На каждую гирю (или на колбу напротив нее) наносится соответствующее значение плотности. Результат измерения определяется максимальным значением всплывающих грузов. Такой ареометр дешевле, но не обладает достаточной точностью.
Многопоплавковый автомобильный ареометр
Само измерение ареометра осуществляется следующим образом:
- Носик ареометра вставляется в аккумулятор через заливное отверстие. Есть аппараты не с резиновым, а с пластиковым носиком. При этом погружать его в электролит нужно осторожно, чтобы не повредить свинцовые пластины.

- При помощи груши в колбу набирается электролит. Для ареометров с одним поплавком необходимо контролировать количество собранной жидкости. Его должно быть достаточно, чтобы поплавок свободно плавал внутри колбы. Но и много жидкости пить тоже нельзя. Тогда поплавок может упираться в верхний край колбы. Показания ареометра в этом случае будут недостоверными.
- Взяв жидкость, смотрим — наоборот, какие риски на поплавке — это ее уровень. Цифры рядом с риском будут обозначать значение плотности.
Для ареометров с несколькими поплавками значение плотности определяется по поплавкам. Плавающая гиря с максимальным числом просто показывает результат измерения.
Показания с помощью ареометра
Для аккумуляторных батарей из нескольких ячеек поверка проводится отдельно в каждой банке.
Обычная цена деления в аккумуляторных ареометрах 0,01 г/см3. Но доступны ареометры и с более точной шкалой.
После завершения измерений необходимо тщательно промыть ареометр дистиллированной водой.
Условия, при которых следует проводить измерения
Перед началом измерений концентрации электролита необходимо придерживаться простых правил. А в некоторых случаях придется корректировать показания ареометра в зависимости от условий, при которых они были получены.
Самое необходимое условие — поддержание необходимого уровня жидкости в самом аккумуляторе. Плотность будет измерена правильно, но для безопасной работы аккумулятора необходимо будет довести уровень до нормы. А это приведет к изменению плотности.
Уровень заряда аккумулятора
Плотность электролита изменяется при зарядке/разрядке аккумулятора. При разряде уменьшается, при заряде увеличивается. В зависимости от степени разрядки аккумулятора значения изменяются следующим образом.
Зависимость показаний ареометра от степени заряженности аккумулятора
Точно определить уровень разрядки вряд ли возможно. Поэтому нужно сначала полностью зарядить аккумулятор, подождать несколько часов и только потом проводить измерения.
Если проводились какие-либо действия с водно-кислотным раствором — добавлением дистиллированной воды или самой кислоты, то не следует измерять плотность сразу после них. Необходимо дождаться, пока добавленная жидкость полностью перемешается в аккумуляторе.
Температура при измерениях
Калибровка эталонных ареометров ориентируется на температуру +25°С. Для получения наиболее точных показаний измерения плотности электролита следует проводить при одной и той же температуре. Зимой проверяемый аккумулятор следует занести в теплое место и дать ему нагреться до нужной температуры. Но не стоит снимать мерки буквально дома. Кислотный раствор может случайно испортить мебель или одежду. Лучше использовать отапливаемое помещение, приспособленное для таких работ.
Если нет возможности провести измерения при рекомендуемой температуре 20 — 25°С, то можно провести измерения при любой температуре, а затем воспользоваться таблицей поправок:
Поправочные значения для измерений при разных температурах
Регулярные проверки плотности электролита в аккумуляторе позволят не только поддерживать его в оптимальных для работы условиях, но и своевременно выявлять возможные проблемы и неисправности.
Добавление воды в автомобильный аккумулятор
Автомобильные аккумуляторы могут выйти из строя, если уровень электролита не контролируется должным образом. Емкость аккумулятора резко упадет, а зимой велик шанс, что он полностью выйдет из строя. Итак, как мы можем позаботиться об уровне электролита в аккумуляторе?
Содержание
Почему важен уровень электролита в автомобильном аккумуляторе?
Электролит в батареях состоит из 65% воды и 35% серной кислоты. При работе аккумулятора при подзарядке электролит может закипеть, особенно при слишком высокой температуре наружного воздуха или под капотом, процесс ускоряется.
Будучи нелетучим, кислота почти не испаряется. Но вода быстро испаряется. В результате уровень электролита падает, соотношение воды и кислоты уже не в параметрах, а плотность электролита увеличивается.
Зачем добавлять воду в автомобильный аккумулятор?
Нормальная плотность уровня электролита составляет около 1,29 г/см³. При выкипании воды плотность и содержание кислоты увеличиваются. Если это произойдет, то пластины батареи будут изнашиваться гораздо быстрее, а если не доливать воду, то пластины просто повредятся.
При выкипании воды плотность и содержание кислоты увеличиваются. Если это произойдет, то пластины батареи будут изнашиваться гораздо быстрее, а если не доливать воду, то пластины просто повредятся.
Таким образом, добавление воды в автомобильный аккумулятор обеспечивает эффективность и производительность аккумулятора, когда уровень электролита находится на нормальном уровне.
Какой тип воды следует добавлять в автомобильный аккумулятор?
Единственный тип воды, который вам нужно добавить в аккумулятор, — это дистиллированная вода. Другие виды воды, такие как водопроводная вода и некоторые виды воды в бутылках, могут содержать минералы и другие вещества, вызывающие коррозию деталей аккумулятора. Дистиллированная вода содержит водород и кислород и не имеет лишних примесей
Когда доливать воду в автомобильный аккумулятор?
Есть несколько способов проверить правильный уровень электролита в аккумуляторе, но перед этим в первую очередь нужно внимательно посмотреть на сам аккумулятор.
Некоторые батареи имеют специальный индикатор. Он показывает несколько своих состояний:
- Нормальный, низкий уровень электролита. В этом случае нужно добавить воды.
- Низкая плотность электролита, здесь нужно зарядить аккумулятор.
Некоторые аккумуляторы имеют отметки «min» и «max». Эти батареи позволяют проверить уровень электролита, просто взглянув на него, благодаря относительной прозрачности корпуса.
Вы также можете проверить уровень заряда батареи, сняв ее и открыв небольшие крышки. На некоторых аккумуляторах вы найдете специальный индикатор, показывающий, что электролит должен покрывать только 0,5 см (0,196 дюйма) и не более. Если индикатора нет, то ориентироваться можно по погружению пластин в жидкость.
Проверять уровень электролита в аккумуляторе и его плотность следует только тогда, когда аккумулятор полностью заряжен на зарядном устройстве!
Каков нормальный уровень электролита в автомобильном аккумуляторе?
Нормальный уровень электролита должен быть на 15–20 миллиметров (0,59–0,78 дюйма) выше края пластин. Если пластины не покрыты, это указывает на низкий уровень электролита, который необходимо восстановить как можно быстрее.
Если пластины не покрыты, это указывает на низкий уровень электролита, который необходимо восстановить как можно быстрее.
Наилучшие испытания проводятся с помощью наиболее часто используемого ареометра и рефрактометра. Купить эти средства можно в большинстве магазинов автозапчастей и они пригодятся не только этой проверке, но и другим автомобильным жидкостям.
В то же время, измеряя уровень, вы также можете проверить состояние электролита, который должен быть прозрачным. Если жидкость не прозрачная или темная, значит аккумулятор вышел из строя и нужно купить новый.
Сколько воды добавляется в автомобильный аккумулятор?
Количество воды всегда будет зависеть от емкости аккумулятора, чем больше аккумулятор, тем больше в нем электролита. Причем объем зависит от конструкции аккумулятора и может отличаться от производителя к производителю. Ниже приведены оценки, основанные на разной емкости батареи:
| Battery capacity | Electrolyte level | Water level |
| 55 Ah | ~ 2. 6 L (0.68 gal) 6 L (0.68 gal) | ~ 1.64 L (0.43 gal) |
| 60 , 62 Ah | 2.7 L -3.1 L 0.71 – 0.81 gal | 1.77 – 1.95 L 0.46 – 0.51 gal |
| 65 Ah | ~ 3.6 l (0.95 gal) | ~ 2.29 L (0.60 gal) |
| 75 Ач | 3.7 – 4.1 L 0.977 – 1.08 gal | 2.41 – 2.60 L 0.63 – 0.68 gal |
| 90 Ah | 4.3 – 4.8 L 1.13 – 1.26 gal | 2.86 – 3.13 L 0.75 – 0.82 gal |
Как долить дистиллированную воду в автомобильный аккумулятор?
Чтобы правильно заполнить аккумулятор водой, выполните следующие простые действия.
- Очистите аккумулятор с поверхности, чтобы грязь и другие вещества не попали в аккумулятор при откручивании пробок. Перед этим оставьте батарею при комнатной температуре примерно на 7 часов;
- Выкрутите пробки и проверьте уровень электролита, как я описал выше;
- Если вам нужно добавить дистиллированную воду, добавляйте ее осторожно. Если вы добавили большее количество, удалите его с помощью шприца.
- Закрутите пробки и оставьте автомобильный аккумулятор не менее чем на 7 часов, т.к. смешивание воды с кислотой занимает некоторое время;
- Зарядить аккумулятор, но если вы видите, что электролит закипает, зарядку следует прекратить;
- Измерьте плотность электролита ареометром. Нормальный уровень должен быть 1,29 г/см3.
Заключение
Добавление воды в автомобильный аккумулятор — хороший способ сохранить его и продлить срок службы. Вы должны добавлять только дистиллированную воду, потому что другие типы воды содержат такие вещества, как кальций, магний, соль и другие примеси, которые могут вызывать химические реакции и ускорять разрушение пластин аккумулятора.
Будьте осторожны при выборе некоторых аккумуляторов, и они помечены как «необслуживаемые», поскольку большинство из них таковыми не являются. Их крышки спрятаны под наклейкой с этикеткой аккумулятора. Достаточно снять его и вы увидите крышки аккумуляторов.
Действительно есть аккумуляторы необслуживаемые, эти аккумуляторы не имеют крышек на поверхности и не требуют обслуживания, просто используйте их до полного износа.
Старайтесь не доливать в аккумулятор больше воды, чем необходимо, так как это отрицательно скажется на его работе. Плотность электролита уменьшится, а значит, уменьшится мощность аккумулятора. Также это снижает его устойчивость к отрицательным температурам, а зимой это может быть проблематично.
К счастью, избыток воды можно уменьшить очень простым способом, как я упоминал выше. Не беспокойтесь о смеси с серной кислотой, этот процесс очень медленный, и уменьшение сразу после добавления не повлияет на смесь.
youtube.com/embed/x0Nh4yR7LG0?feature=oembed» frameborder=»0″ allow=»accelerometer; autoplay; clipboard-write; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»»>Изображение: איתן טלEtan Tal, CC BY 3.0 https://creativecommons.org/licenses/by/3.0, через Wikimedia Commons
Эти наполненные энергией батареи хорошо работают в условиях экстремального холода и жары
Первый автор исследования Гуоруй Цай, исследователь наноинженерии из Калифорнийского университета в Сан-Диего, готовит аккумуляторную ячейку для испытаний при минусовой температуре. Фотографии Дэвида Байо / Калифорнийского университета в Сан-Диего, Школа инженерии Джейкобса
Инженеры Калифорнийского университета в Сан-Диего разработали литий-ионные аккумуляторы, которые хорошо работают при морозе и палящем зное, сохраняя при этом много энергии. Исследователи совершили этот подвиг, разработав электролит, который не только универсален и надежен в широком диапазоне температур, но также совместим с высокоэнергетическими анодом и катодом.
Термически устойчивые батареи описаны в статье, опубликованной 4 июля в Труды Национальной академии наук (PNAS) .
Такие аккумуляторы могут позволить электромобилям в холодном климате проехать большее расстояние без подзарядки; они также могут уменьшить потребность в системах охлаждения, чтобы аккумуляторы транспортных средств не перегревались в жарком климате, сказал Чжэн Чен, профессор наноинженерии в Инженерной школе Джейкобса Калифорнийского университета в Сан-Диего и старший автор исследования.
«Вам нужна высокотемпературная эксплуатация в районах, где температура окружающей среды может достигать трехзначных цифр, а на дорогах становится еще жарче. В электромобилях аккумуляторы обычно находятся под полом, недалеко от этих горячих дорог», — пояснил Чен, который также является преподавателем Центра устойчивой энергетики и энергетики Калифорнийского университета в Сан-Диего. «Кроме того, батареи нагреваются просто от того, что во время работы проходит ток. Если аккумуляторы не выдержат такой прогрев при высокой температуре, их производительность быстро ухудшится».
Если аккумуляторы не выдержат такой прогрев при высокой температуре, их производительность быстро ухудшится».
В ходе испытаний экспериментальные батареи сохранили 87,5 % и 115,9 % своей емкости при температуре -40 и 50 C (-40 и 122 F) соответственно. У них также был высокий кулоновский КПД 98,2% и 98,7% при этих температурах соответственно, что означает, что батареи могут подвергаться большему количеству циклов зарядки и разрядки, прежде чем они перестанут работать.
Проверка работоспособности аккумуляторных батарей при высоких температурах в печи, нагретой до 50°С.
Аккумуляторы, разработанные Ченом и его коллегами, устойчивы как к холоду, так и к жаре благодаря своему электролиту. Он изготовлен из жидкого раствора дибутилового эфира, смешанного с солью лития. Особенностью дибутилового эфира является то, что его молекулы слабо связываются с ионами лития. Другими словами, молекулы электролита могут легко отдавать ионы лития во время работы батареи. Это слабое молекулярное взаимодействие, как обнаружили исследователи в ходе предыдущего исследования, повышает производительность батареи при отрицательных температурах. Кроме того, дибутиловый эфир может легко выдерживать тепло, потому что он остается жидким при высоких температурах (его температура кипения составляет 141 C или 286 F).
Кроме того, дибутиловый эфир может легко выдерживать тепло, потому что он остается жидким при высоких температурах (его температура кипения составляет 141 C или 286 F).
Стабилизирующие литий-серные химические вещества
Особенностью этого электролита является то, что он совместим с литий-серной батареей, которая представляет собой тип перезаряжаемой батареи с анодом из металлического лития и катодом из серы. Литий-серные батареи являются неотъемлемой частью аккумуляторных технологий следующего поколения, поскольку они обещают более высокую плотность энергии и более низкую стоимость. Они могут хранить в два раза больше энергии на килограмм, чем современные литий-ионные батареи — это может удвоить запас хода электромобилей без увеличения веса аккумуляторной батареи. Кроме того, сера является более распространенной и менее проблематичной для получения, чем кобальт, используемый в катодах традиционных литий-ионных аккумуляторов.
Но есть проблемы с литий-серными батареями. И катод, и анод сверхреактивны. Серные катоды настолько реактивны, что растворяются во время работы батареи. Эта проблема усугубляется при высоких температурах. А литий-металлические аноды склонны к образованию игольчатых структур, называемых дендритами, которые могут пробивать части батареи, вызывая ее короткое замыкание. В результате литий-серные батареи работают только до десятков циклов.
И катод, и анод сверхреактивны. Серные катоды настолько реактивны, что растворяются во время работы батареи. Эта проблема усугубляется при высоких температурах. А литий-металлические аноды склонны к образованию игольчатых структур, называемых дендритами, которые могут пробивать части батареи, вызывая ее короткое замыкание. В результате литий-серные батареи работают только до десятков циклов.
Чжэн Чен, профессор наноинженерии Калифорнийского университета в Сан-Диего.
«Если вам нужна батарея с высокой плотностью энергии, вам, как правило, нужно использовать очень жесткую и сложную химию», — сказал Чен. «Высокая энергия означает, что происходит больше реакций, что означает меньшую стабильность, большую деградацию. Создание стабильной высокоэнергетической батареи само по себе является сложной задачей, а попытка сделать это в широком диапазоне температур еще сложнее».
Электролит на основе дибутилового эфира, разработанный командой Калифорнийского университета в Сан-Диего, предотвращает эти проблемы даже при высоких и низких температурах. Аккумуляторы, которые они тестировали, имели гораздо более длительный срок службы, чем обычные литий-серные аккумуляторы. «Наш электролит помогает улучшить как сторону катода, так и сторону анода, обеспечивая при этом высокую проводимость и межфазную стабильность», — сказал Чен.
Аккумуляторы, которые они тестировали, имели гораздо более длительный срок службы, чем обычные литий-серные аккумуляторы. «Наш электролит помогает улучшить как сторону катода, так и сторону анода, обеспечивая при этом высокую проводимость и межфазную стабильность», — сказал Чен.
Команда также разработала серный катод, чтобы сделать его более стабильным, привив его к полимеру. Это предотвращает растворение большего количества серы в электролите.
Следующие шаги включают масштабирование химического состава батареи, ее оптимизацию для работы при еще более высоких температурах и дальнейшее увеличение срока службы.
Бумага: «Критерии выбора растворителя для устойчивых к температуре литий-серных аккумуляторов». Соавторами являются Guorui Cai, John Holoubek, Mingqian Li, Hongpeng Gao, Yijie Yin, Sicen Yu, Haodong Liu, Tod A. Pascal и Ping Liu, все из Калифорнийского университета в Сан-Диего.
Эта работа была поддержана грантом факультета ранней карьеры в рамках Программы грантов для исследований космических технологий НАСА (ECF 80NSSC18K1512), Национального научного фонда через Центр материаловедения и инженерии Калифорнийского университета в Сан-Диего (MRSEC, грант DMR-2011924) и Управление транспортных технологий Министерства энергетики США в рамках Программы перспективных исследований аккумуляторных материалов (Battery500 Consortium, контракт DE-EE0007764). Эта работа была частично выполнена в Нанотехнологической инфраструктуре Сан-Диего (SDNI) в Калифорнийском университете в Сан-Диего, члене Национальной координируемой инфраструктуры нанотехнологий, которая поддерживается Национальным научным фондом (грант ECCS-1542148).
Эта работа была частично выполнена в Нанотехнологической инфраструктуре Сан-Диего (SDNI) в Калифорнийском университете в Сан-Диего, члене Национальной координируемой инфраструктуры нанотехнологий, которая поддерживается Национальным научным фондом (грант ECCS-1542148).
Лизель Лабиос , 858-246-1124, .(JavaScript должен быть включен для просмотра этого адреса электронной почты)
Studio Ten 300 Калифорнийского университета в Сан-Диего предлагает радио- и телевизионную связь для интервью с нашими преподавателями в СМИ, которые можно координировать через .(JavaScript должен быть включен для просмотра этого адреса электронной почты). Чтобы связаться с экспертом факультета Калифорнийского университета в Сан-Диего по актуальным вопросам и актуальным новостям, посетите https://ucsdnews.ucsd.edu/media-resources/faculty-experts.
Превышение размеров литий-металлических электродов в твердотельных батареях: значение для перенапряжения и, следовательно, производительности?
1. Placke T., Kloepsch R., Dühnen S., Winter M., J. Solid State Electrochem.
2017, 21, 1939–1964. [Google Scholar]
Placke T., Kloepsch R., Dühnen S., Winter M., J. Solid State Electrochem.
2017, 21, 1939–1964. [Google Scholar]
2. Касначев Ю., Вагнер Р., Винтер М., Чекич-Ласкович И., Вверх. Курс. хим. 2018, 376, 16. [Google Scholar]
3. Шнелл Дж., Гюнтер Т., Кнох Т., Вейдер К., Колер Л., Джаст А., Келлер М., Пассерини С., Рейнхарт Г., Дж. Источники питания. 2018, 382, 160–175. [Академия Google]
4. Дуань Х., Инь Ю.-С., Ши Ю., Ван П.-Ф., Чжан С.-Д., Ян С.-П., Ши Дж.-Л., Вэнь Р., Го Ю. -Г., Ван Л.-Дж., Дж. Ам. хим. соц. 2018, 140, 82–85. [PubMed] [Google Scholar]
5. Юнг К. Н., Шин Х. С., Пак М. С., Ли Дж. В., ChemElectroChem 2019, 6, 3842–3859. [Google Scholar]
6. Homann G., Meister P., Stolz L., Brinkmann J.P., Kulisch J., Adermann T., Winter M., Kasnatscheew J., ACS Appl. Матер. Интерфейсы 2020, 3, 3162–3168. [Google Scholar]
7. Винтер М., Барнетт Б., Сюй К., Chem. преп. 2018, 118, 11433–11456. [PubMed] [Академия Google]
8.
Цао Д., Сунь С. , Ли К., Натан А., Сян П., Чжу Х., Материя
2020, 3, 57–94. [Google Scholar]
, Ли К., Натан А., Сян П., Чжу Х., Материя
2020, 3, 57–94. [Google Scholar]
9. Brissot C., Rosso M., Chazalviel J.N., Lascaud S., J. Power Sources 1999, 81, 925–929. [Google Scholar]
10. Чоудхури С., Джоуль 2018, 2, 2201–2203. [Google Scholar]
11. Li Z., Lu W., Zhang N., Pan Q., Chen Y., Xu G., Zeng D., Zhang Y., Cai W., Yang M., Yang Z., Sun Y., Ke H ., Cheng H., J. Mater. хим. А 2018, 6, 14330–14338. [Академия Google]
12. Бай П., Ли Дж., Брашетт Ф. Р., Базант М. З., Energy Environ. науч. 2016, 9, 3221–3229. [Google Scholar]
13. Бикер Г., Винтер М., Бикер П., Phys. хим. хим. физ. 2015, 17, 8670–8679. [PubMed] [Google Scholar]
14. Janek J., Zeier W.G., Nat. Энергия 2016, 1, 16141. [Google Scholar]
15. Сюй К., хим. преп. 2004, 104, 4303–4417. [PubMed] [Google Scholar]
16. Сакуда А., Куратани К., Ямамото М., Такахаши М., Такеучи Т., Кобаяши Х., Дж. Электрохим. соц. 2017, 164, А2474-А2478. [Академия Google]
17. Нам Й.Дж., Чо С.Дж., О Д.Ю., Лим Дж.М., Ким С.Ю., Сонг Дж.Х., Ли Ю.Г., Ли С.Ю., Юнг Ю.С., Нано Летт.
2015, 15, 3317–3323. [PubMed] [Google Scholar]
Нам Й.Дж., Чо С.Дж., О Д.Ю., Лим Дж.М., Ким С.Ю., Сонг Дж.Х., Ли Ю.Г., Ли С.Ю., Юнг Ю.С., Нано Летт.
2015, 15, 3317–3323. [PubMed] [Google Scholar]
18. Wang Y., Richards W.D., Ong S.P., Miara L.J., Kim J.C., Mo Y.F., Ceder G., Nat. Матер. 2015, 14, 1026–1031. [PubMed] [Google Scholar]
19. Сюй Л., Тан С., Ченг Ю., Ван К., Лян Дж., Лю С., Цао Ю.-С., Вэй Ф., Май Л., Джоуль 2018, 2, 1991–2015. [Google Scholar]
20. Хань Ф., Юэ Дж., Чен С., Чжао Н., Фан С., Ма З., Гао Т., Ван Ф., Го С., Ван С., Джоуль 2018, 2, 497–508. [Google Scholar]
21. Камая Н., Хомма К., Ямакава Ю., Хираяма М., Канно Р., Ёнемура М., Камияма Т., Като Ю., Хама С., Кавамото К., Мицуи А., Нат. Матер. 2011, 10, 682–686. [PubMed] [Google Scholar]
22. Шин Х.С., Рю В.Г., Пак М.С., Юнг К.Н., Ким Х., Ли Дж.В., ChemSusChem 2018, 11, 3184–3190. [PubMed] [Google Scholar]
23. Сунь С., Лю Дж., Гонг Ю., Уилкинсон Д. П., Чжан Дж., Nano Energy 2017, 33, 363–386. [Google Scholar]
24. У Дж., Рао З., Ченг З., Юань Л., Ли З., Хуан Ю., Adv. Энергия Матер.
2019, 9, 17. [Google Scholar]
У Дж., Рао З., Ченг З., Юань Л., Ли З., Хуан Ю., Adv. Энергия Матер.
2019, 9, 17. [Google Scholar]
25. Кляйн С., Борзуцки К., Шнайдер П., Фромм О., Рейтер Дж., Фан К., Плакке Т., Винтер М., Каснатшеев Дж., Chem. Матер. 2020, 32, 6279–6284. [Google Scholar]
26. Оно С., Бернгес Т., Буххейм Дж., Дючардт М., Хац А.-К., Крафт М.А., Квак Х., Сантоша А.Л., Лю З., Минафра Н., Цудзи Ф., Сакуда А., Шлем R., Xiong S., Zhang Z., Adelhelm P., Chen H., Hayashi A., Jung Y.S., Lotsch B.V., Roling B., Vargas-Barbosa N.M., Zeier W.G. ACS Energy Lett. 2020, 5, 910–915. [Google Scholar]
27. У С., Пан К., Цзя М., Рен Ю., Хе Х., Чжан Л., Чжан С., Green Energy & Environ. 2019, 4, 360–374; Окружающая среда. 2019 , 4, 360–374. [Google Scholar]
28. Миндемарк Дж., Лейси М.Дж., Боуден Т., Бранделл Д., Prog. Полим. науч. 2018, 81, 114–143. [Google Scholar]
29.
Nair J.R., Imholt L., Brunklaus G., Winter M., Electrochem. соц. Интерфейс
2019, 28, 55–61. [Google Академия]
[Google Академия]
30. Штрейперт Б., Штольц Л., Хоманн Г., Янсен П., Чекич-Ласкович И., Винтер М., Каснатшеев Дж., ChemSusChem 2020, 13, 5301–5307. [Бесплатная статья PMC] [PubMed] [Google Scholar]
31. Kasnatscheew J., Evertz M., Streipert B., Wagner R., Nowak S., Cekic Laskovic I., Winter M., J. Phys. хим. С 2017, 121, 1521–1529. [Google Scholar]
32. Касначев Дж., Эвертц М., Стрейперт Б., Вагнер Р., Новак С., Чекич Ласкович И., Винтер М., Дж. Источники энергии 2017, 359, 458–467. [Google Scholar]
33. Kasnatscheew J., Röser S., Börner M., Winter M., ACS Appl. Матер. Интерфейсы 2019, 2, 7733–7737. [Google Scholar]
34. Kasnatscheew J., Evertz M., Kloepsch R., Streipert B., Wagner R., Cekic Laskovic I., Winter M., Energy Technol. 2017, 5, 1670–1679. [Google Scholar]
35. Homann G., Stolz L., Nair J., Laskovic I.C., Winter M., Kasnatscheew J., Sci. Респ. 2020, 10, 4390. [Бесплатная статья PMC] [PubMed] [Google Scholar]
36.
Homann G. , Stolz L., Winter M., Kasnatscheew J., iScience.
2020, 23, 101225. [Бесплатная статья PMC] [PubMed] [Google Scholar]
, Stolz L., Winter M., Kasnatscheew J., iScience.
2020, 23, 101225. [Бесплатная статья PMC] [PubMed] [Google Scholar]
37. Homann G., Stolz L., Neuhaus K., Winter M., Kasnatscheew J., Adv. Функц. Матер. 2020, 30, 2006289. [Google Scholar]
38. Zhang X., Yang Y., Zhou Z., Chem. соц. преп. 2020, 49, 3040–3071. [PubMed] [Google Scholar]
39. Фат Дж. П., Альшаймер Л., Сторч М., Стадлер Дж., Бандлоу Дж., Хан С., Ридель Р., Ветцель Т., Дж. Хранение энергии 2020, 29, 11. [Google Scholar]
40. Хуфнер Т., Ольденбургер М., Бедурфтиг Б., Груле А., Дж. Хранение энергии 2019, 24, 6. [Google Scholar]
41. Леверенц М., Фукс Г., Беккер Л., Зауэр Д. У., Дж. Хранение энергии 2018, 18, 149–159. [Google Scholar]
42. Леверенц М., Зауэр Д. У., Дж. Хранение энергии 2018, 18, 421–434. [Академия Google]
43. Даггер Т., Касначев Дж., Вортманн-Вестховен Б., Швитерс Т., Новак С., Винтер М., Шаппахер Ф. М., Дж. Источники питания 2018, 396, 519–526. [Google Scholar]
44.



 Если аккумулятор имеет полупрозрачный корпус, уровень электролита определяется визуально: он должен быть между отметками «MIN» и «MAX» на боковой стороне аккумулятора.
Если аккумулятор имеет полупрозрачный корпус, уровень электролита определяется визуально: он должен быть между отметками «MIN» и «MAX» на боковой стороне аккумулятора.
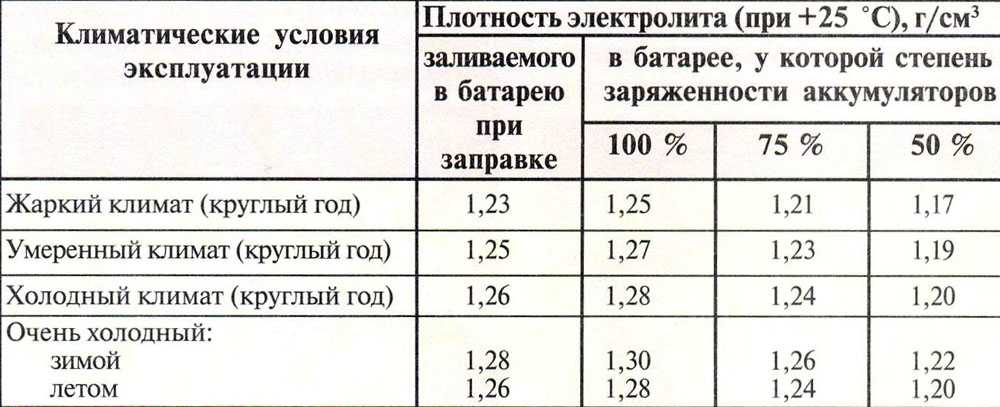 Слейте электролит из ареометра в аккумуляторную батарею.
Слейте электролит из ареометра в аккумуляторную батарею.