Что такое частота? | Fluke
Частота переменного тока (ac) — это количество синусоидальных колебаний переменного тока в секунду. Частота — это количество изменений направления тока за секунду. Для измерения частоты используется международная единица герц (Гц). 1 герц равен 1 колебанию в секунду.
- Герц (Гц) = 1 герц равен 1 колебанию в секунду.
- Колебание = Одна полная волна переменного тока или напряжения.
- Полупериод = Половина колебания.
- Период = Время, необходимое для выполнения одного полного колебания.
Частота отражает повторяемость процессов. С точки зрения электрического тока частота — это количество повторений синусоиды или, другими словами, полного колебания, которое включает положительную и отрицательную составляющие.
Чем больше колебаний происходит в секунду, тем выше частота.
Пример. Если известно, что частота переменного тока равна 5 Гц (см. схему ниже), это означает, что его форма сигнала повторяется 5 раз за 1 секунду.
Частота обычно используется для описания работы электрооборудования. Ниже приведены некоторые наиболее распространенные диапазоны частот:
- Частота линии питания (обычно 50 Гц или 60 Гц).
- Частотно-регулируемые приводы: обычно используют несущую частоту 1–20 кГц.
- Звуковой диапазон частот: от 15 Гц до 20 кГц (диапазон человеческого слуха).
- Радиочастота: от 30 до 300 кГц.
- Низкая частота: от 300 кГц до 3 МГц.
- Средняя частота: от 3 до 30 МГц.
- Высокая частота: от 30 до 300 кГц.
Обычно цепи и оборудование предназначены для работы с постоянной или переменной частотой. Оборудование, рассчитанное на работу с постоянной частотой, при изменении частоты начинает работать неправильно. Например, двигатель переменного тока, рассчитанный на работу при 60 Гц, работает медленнее при частоте ниже 60 Гц или быстрее при частоте выше 60 Гц. Для двигателей переменного тока любое изменение частоты приводит к пропорциональному изменению частоты вращения двигателя. Другим примером является снижение частоты вращения двигателя на 5 % при снижении частоты сети на 5 %.
Другим примером является снижение частоты вращения двигателя на 5 % при снижении частоты сети на 5 %.
Цифровой мультиметр с режимом частотомера может измерять частоту сигналов переменного тока со следующими функциями:
- регистрация МИН/МАКС значений, позволяющая записывать результаты измерений частоты за заданный интервал времени. Эта функция также применима к измерениям напряжения, тока и сопротивления.
- автоматический выбор диапазона, при котором прибор автоматически подбирает диапазон частот при условии, что частота измеряемого напряжения не выходит за пределы этого диапазона.
Параметры электросетей различаются в зависимости от страны. В США работа сети основана на высокостабильном сигнале с частотой 60 Гц, что соответствует 60 колебаниям в секунду.
Бытовые электросети в США получают питание от однофазного источника питания 120 В перем. тока. Напряжение в настенной розетке дома в США совершает синусоидальные колебания в диапазоне от 170 до −170 В, при этом истинное среднеквадратичное значение этого напряжения будет равно 120 вольт. Частота колебаний составляет 60 циклов в секунду.
Частота колебаний составляет 60 циклов в секунду.
Единица измерения получила название «герц» в честь немецкого физика Генриха Герца (1857–1894 гг.), который первым осуществил передачу и принятие радиоволн. Радиоволны распространяются с частотой одно колебание в секунду (1 Гц). (аналогично часы тикают с частотой 1 Гц)
Ссылка: Digital Multimeter Principles by Glen A. Mazur, American Technical Publishers.
Статьи на связанные темы:
- Порядок измерения частоты мультиметром
Как определить частоту сотовой связи с помощью смартфона
GSM-Репитеры.РУ » Как определить частоту сотовой связи с помощью смартфона
При выборе системы усиления крайне важно знать два параметра: поколение мобильной сети (2G, 3G или 4G), качество которой вы хотите улучшить, и частоту, на которой она функционирует.
Дело в том, что все основные компоненты систем усиления — антенны, репитеры, модемы и роутеры — создаются под определенные частотные диапазоны и очень редко поддерживают сразу все существующие в мире стандарты. Другими словами, вы можете приобрести комплект усиления «для 4G-интернета», но если в его составе будет антенна, рассчитанная на частотный диапазон, в котором не работает ваш оператор, деньги будут потрачены впустую.
Другими словами, вы можете приобрести комплект усиления «для 4G-интернета», но если в его составе будет антенна, рассчитанная на частотный диапазон, в котором не работает ваш оператор, деньги будут потрачены впустую.
Приведем пример. Чаще всего 4G-интернет предоставляется на частоте 2600 МГц, и большинство комплектов для усиления 4G рассчитаны именно на эту частоту. Тем не менее, все чаще отечественные операторы начинают использовать дополнительные частоты 1800 и 800 МГц. Если в вашем местоположении работает именно такая сеть, то комплект, рассчитанный на частоту 2600 МГц, будет бесполезен.
Итак, чтобы выбрать комплект, вам нужно знать, какие технологии вы хотите усилить и в каких частотных диапазонах они работают. Проще всего это сделать с помощью смартфона под управлением операционной системы Android или iOS (iPhone).
Определяем поколение сотовой сети
Определить поколение сотовой сети с помощью смартфона, как правило, очень легко. В большинстве современных операционных систем технология передачи данных указывается в строке состояния рядом с уровнем сотового сигнала. Технология может быть указана непосредственно (2G, 3G или 4G) или с помощью одной из аббревиатур. Чаще всего встречаются следующие обозначения:
В большинстве современных операционных систем технология передачи данных указывается в строке состояния рядом с уровнем сотового сигнала. Технология может быть указана непосредственно (2G, 3G или 4G) или с помощью одной из аббревиатур. Чаще всего встречаются следующие обозначения:
- 2G, GPRS (G), EDGE (E) — традиционная технология 2G, на которой работает стандартная голосовая GSM-связь и медленный мобильный интернет;
- 3G, UMTS, HSDPA (H), HSPA+ (H+) — третье поколение сотовой связи, используемое для звонков и доступа к широкополосному мобильному интернету;
- 4G, LTE (L) — четвертое поколение сотовой связи, в данный момент используемое отечественными операторами только для доступа к высокоскоростному мобильному интернету.
Например, на смартфонах Xiaomi с двумя SIM-картами строка состояния выглядит следующим образом:
Как легко определить, первая SIM-карта оператора МТС в данный момент работает в режиме 4G, а вторая SIM-карта Tele2 — в 3G.
На каких частотах работают операторы в России
Казалось бы, узнав, какие стандарты связи доступны в вашем местоположении, можно приступать к выбору комплекта усиления. Тем не менее, есть одна существенная проблема: одна и та же технология связи может работать на разных частотах.
Каждый стандарт связи (2G, 3G и 4G) содержит множество подстандартов. Чтобы система усиления работала корректно и усиливала именно тот частотный диапазон, на котором работает ваш оператор, предварительно этот частотный диапазон нужно узнать.
В данный момент в России встречаются следующие стандарты сотовой связи:
|
2G |
900 МГц |
GSM-900, EGSM, GSM-E900 |
|
1800 МГц |
GSM-1800, DCS-1800 |
|
|
3G |
900 МГц |
UMTS-900 |
|
2100 МГц |
UMTS-2100 |
|
|
4G |
800 МГц |
LTE800 |
|
1800 МГц |
|
|
|
2600 МГц |
LTE2600 |
К сожалению, узнать, на какой частоте работает ваш оператор, уже не так легко. Разработчики операционных систем Android и iOS посчитали, что эта информация не пригодится обычным пользователям, и спрятали ее в специальное сервисное меню. Ниже мы расскажем, как вызвать скрытое меню и узнать частоту, используемую оператором. Но перед этим — еще один важный шаг!
Разработчики операционных систем Android и iOS посчитали, что эта информация не пригодится обычным пользователям, и спрятали ее в специальное сервисное меню. Ниже мы расскажем, как вызвать скрытое меню и узнать частоту, используемую оператором. Но перед этим — еще один важный шаг!
Переводим смартфон в нужный стандарт
Если ваш смартфон по умолчанию использует ту сеть, которую вы хотите усилить, дополнительных действий не требуется. Но бывают ситуации, когда вам необходимо определить частотный диапазон другой сети. Например, вы хотите узнать частоту 2G, а смартфон автоматически подключается к 3G. Другой пример: вам необходимо усилить голосовую связь, а ваш телефон подключен к 4G-сети, в которой доступен только мобильный интернет. Чтобы измерить нужный стандарт, принудительно переведите смартфон в соответствующий режим.
Для этого на устройствах Android перейдите в Настройки > Другие сети > Мобильные сети > Режим сети и выберите необходимый стандарт связи. В зависимости от модели смартфона и версии операционной системы путь к разделу Режим сети может незначительно отличаться.
В зависимости от модели смартфона и версии операционной системы путь к разделу Режим сети может незначительно отличаться.
Смартфоны Apple, к сожалению, не поддерживают ручное переключение режимов. Таким образом, пользователи iPhone могут определить частоту только того стандарта, в котором смартфон работает автоматически.
Как узнать частоту сотовой связи
Как мы уже сказали выше, чтобы получить информацию о частоте, на которой ваш смартфон подключен к базовой станции, необходимо зайти в специальное сервисное меню. На устройствах Android оно обычно называется Service Mode, на смартфонах Apple — Field Test. Чтобы вызвать соответствующий экран, достаточно набрать с телефона определенный номер.
Важно! В зависимости от модели устройства и версии операционной системы приведенные в этой статье инструкции могут не работать. В таком случае ввод кода ни к чему не приведет. Также на некоторых смартфонах меню может выглядеть иначе, а информация о сети находиться в одном из подменю. Возможно, вам придется поискать в подразделах меню прежде, чем вы найдете нужную страницу с информацией о мобильном соединении!
Возможно, вам придется поискать в подразделах меню прежде, чем вы найдете нужную страницу с информацией о мобильном соединении!
Перед тем, как производить тестирование частоты, отключите WiFi-соединение. В случае, если в вашем телефоне установлено две SIM-карты, рекомендуется извлечь ненужную карту и оставить только ту, которую необходимо протестировать. Так вы сможете избежать лишней путаницы и точно получите информацию о текущем соединении.
Как вызвать сервисное меню на Android
В зависимости от версии Android сервисное меню открывается с помощью одного из следующих кодов:
- *#0011#
- *#*#4636#*#*
- *#*#197328640#*#*
После ввода последнего символа скрытое меню должно открыться автоматически, нажимать кнопку вызова не нужно. На смартфонах Samsung вы сразу попадете на экран с информацией о состоянии сети. На устройствах других производителей может потребоваться перейти в подраздел «Информация о телефоне» или другой, содержащий сведения о мобильном подключении.
На смартфонах Samsung для получения информации о сети достаточно набрать номер *#0011#
Для получения информации о сети на смартфонах Xiaomi необходимо набрать номер *#*#4636#*#*, перейти в раздел «Информация о телефоне» и прокрутить страницу вниз. На устройствах с двумя SIM-картами разделов «Информация о телефоне» будет два.
Как видите, скрытое меню предоставляет очень много технических данных. Большая часть этой информации нам не понадобится, а на что именно следует обратить внимание, мы расскажем чуть ниже.
Как вызвать сервисное меню на iPhone
На смартфонах Apple сервисное меню вызывается аналогичным образом, но с помощью другого кода. После ввода необходимо нажать кнопку вызова:
- *3001#12345#*
Чтобы получить информацию о сотовом подключении, вам потребуется найти нужный пункт подменю.
- для 2G: GSM Cell Environment > GSM Cell Info > Neighboring Cells > 0
- для 3G: UMTS Cell Environment > Neighbor Cells > UMTS Set > 0
- для 4G: Serving Cell Info
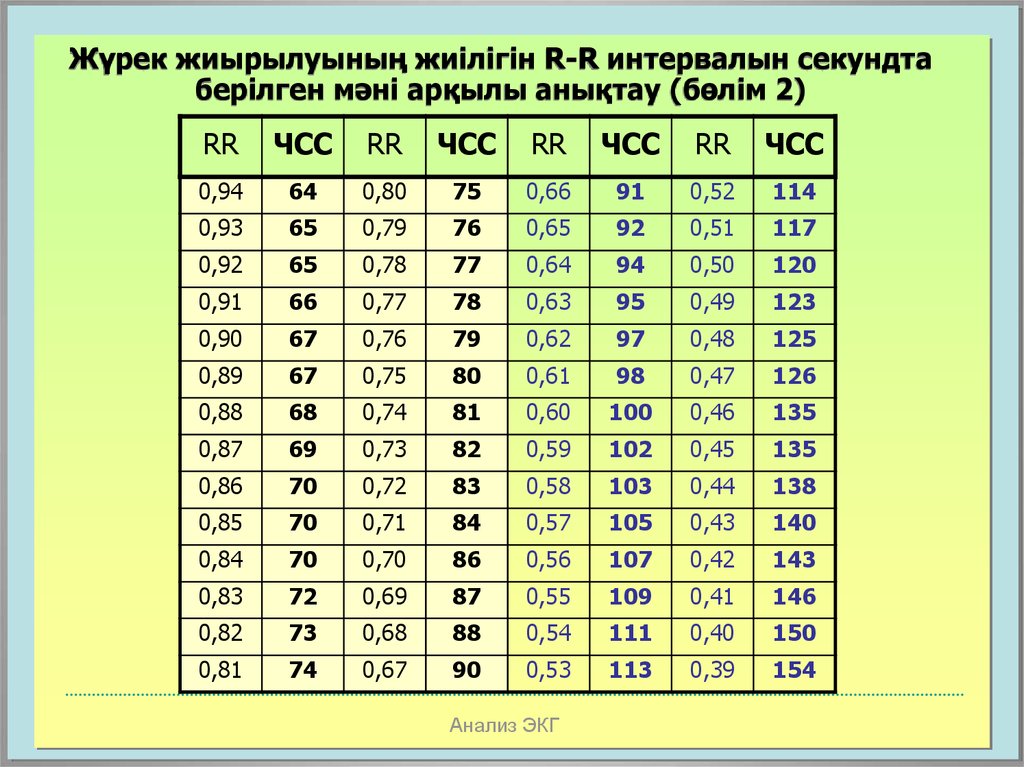
Определяем частоту 2G-сети (GSM)
Для определения частоты, на которой функционирует GSM-сеть, используется специальный радиочастотный номер канала — ARFCN. По сути, это идентификатор, указывающий, в каком радиочастотном диапазоне сейчас работает ваш смартфон. На странице сервисного меню идентификатор обычно указывается после обозначения
Реже смартфоны в режиме 2G показывают сразу название стандарта (например, GSM-900) или рабочую частоту.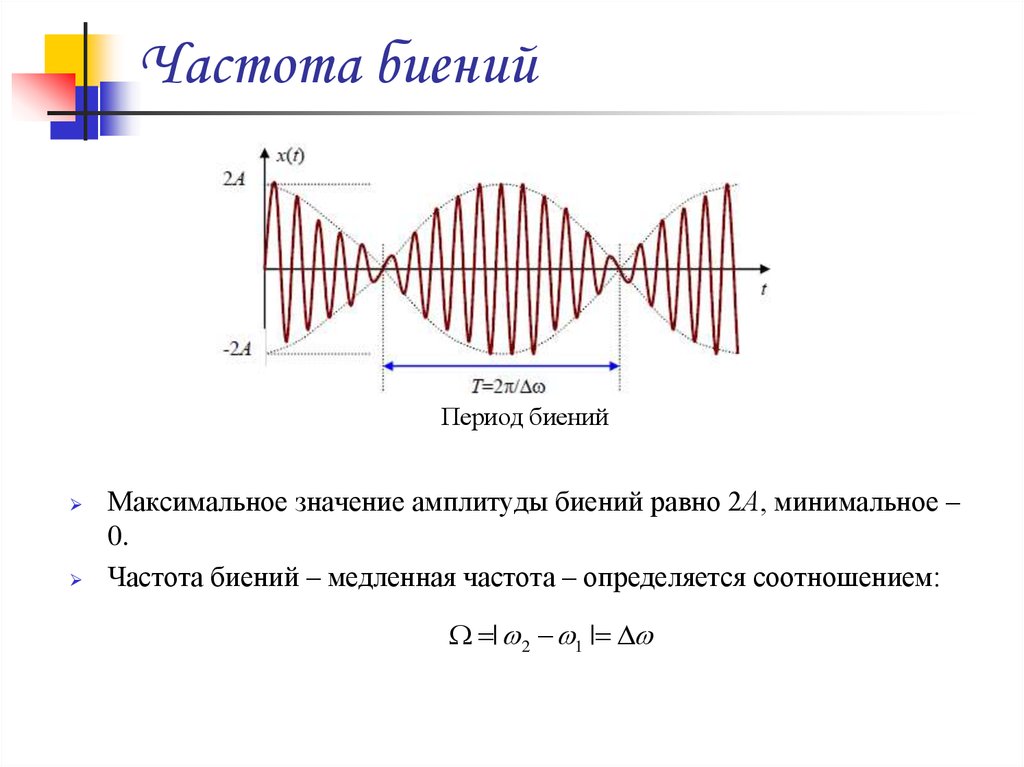 Если ваш смартфон отобразил название стандарта в готовом виде, считайте, что вам повезло. В противном случае определите, к какому стандарту относится указанный ARFCN, с помощью нижеприведенной таблицы.
Если ваш смартфон отобразил название стандарта в готовом виде, считайте, что вам повезло. В противном случае определите, к какому стандарту относится указанный ARFCN, с помощью нижеприведенной таблицы.
|
1–124 |
GSM-900 |
900 МГц |
|
0–124 |
EGSM (GSM-E900) |
900 МГц |
|
512–885 |
GSM-1800 (DCS) |
1800 МГц |
Например, так выглядит определение частоты GSM на смартфонах Samsung (слева) и iPhone (справа):
Если смартфон показывает несколько значений ARFCN, перечисленных столбиком, то активная сеть, как правило, первая в списке.
Определяем частоту 3G-сети
Аналогичным образом дело обстоит с определением частоты в 3G-сетях. Здесь идентификатор канала называется по-другому — UARFCN. В отличие от 2G-сетей, значений UARFCN может быть указано два: одно, позволяющее определить канал приема данных (DL), и другое, указывающее на канал отправки (UL). Также может быть указано название стандарта или его специальный порядковый номер — так называемый «бэнд» (от англ. band).
|
1 |
DL |
10562–10838 |
UMTS-2100 |
2100 МГц |
|
UL |
9612–9888 |
|||
|
8 |
DL |
2937–3088 |
UMTS-900 |
900 МГц |
|
UL |
2712–2863 |
Таким образом, в сервисном меню вы можете обнаружить либо значение UARFCN, либо порядковый номер «бэнда»: например, Band 1. UARFCN обычно указывается после таких аббревиатур, как RX, CH DL и других. На iPhone идентификатор частоты 3G называется Downlink Frequency или dl_freq.
UARFCN обычно указывается после таких аббревиатур, как RX, CH DL и других. На iPhone идентификатор частоты 3G называется Downlink Frequency или dl_freq.
Если смартфон показывает несколько значений UARFCN, перечисленных столбиком, то активная сеть, как правило, первая в списке.
Приведем пример определения UARFCN на современных смартфонах Xiaomi (слева) и Samsung (справа). В данном случае используется частота 2100 МГц:
Определяем частоту 4G-сети
Аналогичным образом дело обстоит и с 4G-сетями. Здесь может быть указан «бэнд» или идентификатор канала — EARFCN. На iPhone определить частоту 4G проще всего по «бэнду», указанному в пункте Freq Band Indicator или freq_band_ind. Если смартфон показывает несколько значений EARFCN, перечисленных столбиком, то активная сеть, как правило, первая в списке.
|
3 |
DL |
1200–1949 |
LTE1800 |
1800 МГц |
|
UL |
19200–19949 |
|||
|
7 |
DL |
2750–3449 |
LTE2600 FDD |
2600 МГц |
|
UL |
20750–21449 |
|||
|
20 |
DL |
6150–6449 |
LTE800 |
800 МГц |
|
UL |
24150–24449 |
|||
|
38 |
37750–38249 |
LTE2600 TDD |
2600 МГц |
|
Обратите внимание, что в последнем приведенном стандарте не указаны различные значения EARFCN для отправки и приема.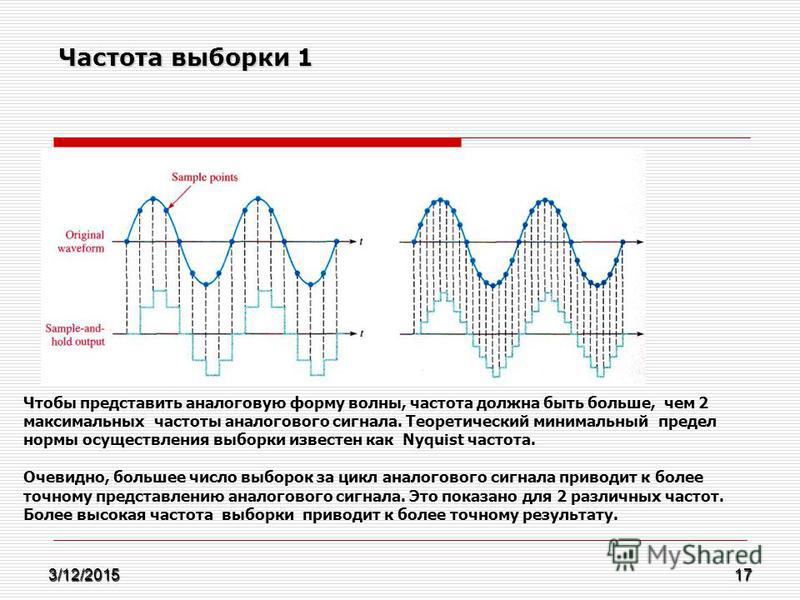 Это вовсе не случайно. Дело в том, что в стандарте LTE Band 38 прием и передача данных происходит в одном и том же частотном диапазоне, но попеременно (технология TDD). Для усиления этого стандарта может потребоваться специальный репитер.
Это вовсе не случайно. Дело в том, что в стандарте LTE Band 38 прием и передача данных происходит в одном и том же частотном диапазоне, но попеременно (технология TDD). Для усиления этого стандарта может потребоваться специальный репитер.
Ниже показан пример определения EARFCN на смартфонах Xiaomi (слева) и последних версиях iPhone (справа).
На устройствах Android определить частоту 4G можно и проще, воспользовавшись бесплатным приложением CellMapper. CellMapper отображает информацию о сотовой сети, в том числе текущий «бэнд». К сожалению, с его помощью нельзя определить частоту 2G- или 3G-сети.
Дополнительные рекомендации
Всегда определяйте частоту в той точке, в которой планируете устанавливать внешнюю антенну системы усиления. Если оператор использует несколько частотных диапазонов одновременно, смартфон может на улице использовать один стандарт, а в помещении — другой. Связано это с тем, что более низкие частоты проникают в помещения лучше и, как правило, именно им электронные устройства отдают предпочтение.
Например, если ваш оператор предоставляет 4G-интернет одновременно в частотных диапазонах 800 и 2600 МГц, то внутри помещения смартфон может выбрать более медленный, но лучше проникающий, стандарт LTE800, а на улице переключиться на более быстрый LTE2600.
Кроме того, следует учитывать, что одновременное использование двух 4G-диапазонов открывает перед оператором возможность агрегации частот. Агрегация — функция сетей LTE-Advanced, при которой абонентские устройства используют несколько частотных диапазонов для достижения максимальной скорости. Сегодня эта технология лишь начинает внедряться операторами сотовой связи, но в обозримом будущем она может существенно повысить производительность мобильного интернета.
Если вы определили, что в вашем местоположении оператор связи работает одновременно в двух «бэндах», имеет смысл задуматься о приобретении двухдиапазонной системы усиления.
Обнаружение низкочастотных вариантов ДНК путем целенаправленного секвенирования цепей Уотсона и Крика
- Письмо
- Опубликовано:
- Джошуа Д. Коэн ORCID: orcid.org/0000-0003-1158-5668 1,2,3,4,5 ,
- Кристофер Дувиль 1,2,3,4 ,
- Джонатан С. Дадли 1, 2, 3,4 ,
- Брайан Дж. Мог ORCID: orcid.org/0000-0001-9988-7147 1,2,3,4,5 ,
- Мария Пополи 1,2,3,4 ,
- Джанин Птак 1,2,3,4 ,
- Ли са Доббин 1, 2,3 ,
- Натали Силлиман 1,2,3,4 ,
- Джой Шефер 1,2,3 ,
- Жанна Ти 6,7,8,9 90 013 ,
- Питер Гиббс 6,8,9 ,
- Кристиан Томасетти 2,10 ,
- Николас Пападопулос ORCID: orcid.org/0000-0001-7135-7451 1,2,3 ,
- Кеннет В. Кинзлер 1,2,3 и
- …
- Берт Фогельштейн
ORCID: orcid.
 org/0000-0003-0766-3854 1,2,3,4
org/0000-0003-0766-3854 1,2,3,4
Природные биотехнологии том 39 , страницы 1220–1227 (2021)Цитировать эту статью
10 тыс. обращений
19 цитирований
158 Альтметрический
Сведения о показателях
Субъекты
- Биомаркеры
- Секвенирование ДНК
- Геномика
- Методы на основе ПЦР
Abstract
Идентификация и количественная оценка низкочастотных мутаций остаются сложной задачей, несмотря на улучшение базовой частоты ошибок технологий секвенирования следующего поколения. Здесь мы описываем метод, названный SaferSeqS, который решает эти проблемы за счет (1) эффективного введения идентичных молекулярных штрих-кодов в нити Уотсона и Крика матричных молекул и (2) обогащения целевых последовательностей с помощью специфичной для нити ПЦР. Метод обеспечивает высокую чувствительность и специфичность и позволяет обнаруживать варианты с частотой ниже 1 на 100 000 молекул ДНК-матрицы с частотой фоновых мутаций <5 × 10 –7 мутантов на пару оснований (п.н.). Мы демонстрируем, что он может оценивать мутации в одном ампликоне или одновременно в нескольких ампликонах, оценивать ограниченное количество бесклеточной ДНК с высокой степенью извлечения обеих цепей и снижать частоту ошибок существующих подходов молекулярного штрих-кодирования на основе ПЦР более чем в 100 раз.
Здесь мы описываем метод, названный SaferSeqS, который решает эти проблемы за счет (1) эффективного введения идентичных молекулярных штрих-кодов в нити Уотсона и Крика матричных молекул и (2) обогащения целевых последовательностей с помощью специфичной для нити ПЦР. Метод обеспечивает высокую чувствительность и специфичность и позволяет обнаруживать варианты с частотой ниже 1 на 100 000 молекул ДНК-матрицы с частотой фоновых мутаций <5 × 10 –7 мутантов на пару оснований (п.н.). Мы демонстрируем, что он может оценивать мутации в одном ампликоне или одновременно в нескольких ампликонах, оценивать ограниченное количество бесклеточной ДНК с высокой степенью извлечения обеих цепей и снижать частоту ошибок существующих подходов молекулярного штрих-кодирования на основе ПЦР более чем в 100 раз.
Это предварительный просмотр содержимого подписки, доступ через ваше учреждение
Соответствующие статьи
Статьи открытого доступа со ссылками на эту статью.
Сверхчувствительный мониторинг пациентов с лейкемией с использованием анализов обнаружения мутаций superRCA
- Лэй Чен
- , Анна Эрикссон
- … Ульф Ландегрен
Связь с природой Открытый доступ 12 июля 2022 г.

Продольное когортное исследование наблюдения и ожидания у пациентов с полным клиническим ответом после химиолучевой терапии локализованного рака прямой кишки: протокол исследования
- Сина Ватандоуст
- , Дэвид Ватчоу
- … Кристос С. Карапетис
Рак BMC Открытый доступ 01 марта 2022 г.
Количественный анализ NGS без калибровки мутаций ниже 0,01% VAF
- Пэн Дай
- , Лючия Руоцзя Ву
- … Дэвид Ю Чжан
Связь с природой Открытый доступ 21 октября 2021 г.

Варианты доступа
Подпишитесь на этот журнал
Получите 12 печатных выпусков и онлайн-доступ
209,00 € в год
всего 17,42 € за выпуск
Узнать больше
Взять напрокат или купить эту статью
Получите только эту статью до тех пор, пока она вам нужна
$39,95
Узнать больше
Цены могут облагаться местными налогами, которые рассчитываются при оформлении заказа
Рис. 1: Обзор SaferSeqS. Рис. 2: Обнаружение мутаций в образцах жидкой биопсии. Рис. 3: Мультиплексная панель для обнаружения мутаций гена, вызывающего рак. Рис. 4: Клиническое применение мультиплексной панели SaferSeqS.Доступность данных
Данные секвенирования, полученные в этом исследовании, можно получить из Европейского архива генома и фенома (инвентарный номер EGAS00001005048).
Доступность кода
Конвейер биоинформатики SaferSeqS реализован на языке Python. Исходный код доступен в репозитории Zenodo (https://doi.org/10.5281/zenodo.4588264).
Ссылки
Shendure, J. et al. Секвенирование ДНК в 40 лет: прошлое, настоящее и будущее. Природа 550 , 345–353 (2017).
Артикул КАС Google Scholar
McMahon, M.A. et al. Энтекавир, препарат от гепатита В, влияет на репликацию и резистентность ВИЧ-1. Н. англ. Дж. Мед. 356 , 2614–2621 (2007).
Артикул КАС Google Scholar
Robins, H.S. et al. Всесторонняя оценка разнообразия β-цепи Т-клеточного рецептора в αβ Т-клетках. Кровь 114 , 4099–4107 (2009).
Артикул КАС Google Scholar
- «>
Миллер В. и др. Секвенирование ядерного генома вымершего шерстистого мамонта. Природа 456 , 387–390 (2008).
Артикул КАС Google Scholar
Брюйнс, Б., Тиггелаар, Р. и Гарденьерс, Х. Массивно-параллельные методы секвенирования для криминалистики: обзор. Электрофорез 39 , 2642–2654 (2018).
Артикул КАС Google Scholar
Hoang, M.L. et al. Полногеномный количественный анализ редких соматических мутаций в нормальных тканях человека с использованием массового параллельного секвенирования. Проц. Натл акад. науч. США 113 , 9846–9851 (2016).
Артикул КАС Google Scholar
Chiu, R.W. et al. Неинвазивная пренатальная диагностика хромосомной анеуплоидии плода путем массивно-параллельного геномного секвенирования ДНК в материнской плазме.
 Проц. Натл акад. науч. США 105 , 20458–20463 (2008 г.).
Проц. Натл акад. науч. США 105 , 20458–20463 (2008 г.).Артикул КАС Google Scholar
Mattox, A.K. et al. Применение жидкой биопсии при раке. науч. Перевод Мед. 11 , eaay1984 (2019).
Newman, A.M. et al. Встроенное цифровое подавление ошибок для улучшенного обнаружения циркулирующей опухолевой ДНК. Нац. Биотехнолог. 34 , 547–555 (2016).
Артикул КАС Google Scholar
Доу, Ю. и др. Точное обнаружение вариантов мозаики в данных секвенирования без соответствующих контролей. Нац. Биотехнолог. 38 , 314–319 (2020).
Артикул КАС Google Scholar
Разави, П. и др. Высокоинтенсивное секвенирование выявляет источники бесклеточных вариантов ДНК, циркулирующих в плазме.
 Нац. Мед. 25 , 1928–1937 (2019).
Нац. Мед. 25 , 1928–1937 (2019).Артикул КАС Google Scholar
Мейнерт, А. М., Бикнелл, Л. С., Херлс, М. Э., Джексон, А. П. и Тейлор, М. С. Количественная оценка чувствительности обнаружения однонуклеотидных вариантов при секвенировании экзома. Биоинформатика BMC 14 , 195 (2013).
Артикул Google Scholar
Кинде И., Ву Дж., Пападопулос Н., Кинзлер К.В. и Фогельштейн Б. Обнаружение и количественная оценка редких мутаций с помощью массивно-параллельного секвенирования. Проц. Натл акад. науч. США 108 , 9530–9535 (2011).
Артикул Google Scholar
Bettegowda, C. et al. Обнаружение циркулирующей опухолевой ДНК на ранних и поздних стадиях злокачественных новообразований человека. Науч.
 Перевод Мед. 6 , 224ra224 (2014).
Перевод Мед. 6 , 224ra224 (2014).Артикул Google Scholar
Cohen, J.D. et al. Комбинированная жидкостная биопсия на основе циркулирующей опухолевой ДНК и белковых биомаркеров для более раннего выявления рака поджелудочной железы. Проц. Натл акад. науч. США 114 , 10202–10207 (2017).
Артикул КАС Google Scholar
Коэн, Дж. Д. и соавт. Обнаружение и локализация хирургически резектабельного рака с помощью мультианализа крови. Наука 359 , 926–930 (2018).
Артикул КАС Google Scholar
Phallen, J. et al. Прямое обнаружение рака на ранней стадии с использованием циркулирующей опухолевой ДНК. науч. Перевод Мед. 9 , eaan2415 (2017).
- «>
Springer, S. et al. Мультимодальный тест для лечения пациентов с кистой поджелудочной железы. Науч. Перевод Мед. 11 , eaav4772 (2019).
Springer, S. et al. Сочетание молекулярных маркеров и клинических признаков улучшает классификацию кист поджелудочной железы. Гастроэнтерология 149 , 1501–1510 (2015).
Артикул КАС Google Scholar
Tie, J. et al. Анализ ДНК циркулирующей опухоли выявляет минимальное остаточное заболевание и прогнозирует рецидив у пациентов с раком толстой кишки II стадии. Науч. Перевод Мед. 8 , 346ra392 (2016).
Артикул Google Scholar
Wang, Y. et al. Выявление соматических мутаций и ВПЧ в слюне и плазме больных плоскоклеточным раком головы и шеи. науч. Перевод Мед. 7 , 293ra104 (2015).

Артикул Google Scholar
Ван Ю. и др. Обнаружение опухолевой ДНК в спинномозговой жидкости больных первичными опухолями головного и спинного мозга. Проц. Натл акад. науч. США 112 , 9704–9709 (2015).
Артикул КАС Google Scholar
Wang, Y. et al. Диагностический потенциал опухолевой ДНК из жидкости кисты яичника. eLife 5 , e15175 (2016).
Springer, S.U. et al. Неинвазивное выявление уротелиального рака посредством анализа мутаций драйверного гена и анеуплоидии. eLife 7 , e32143 (2018).
Schmitt, M.W. et al. Обнаружение ультраредких мутаций с помощью секвенирования нового поколения. Проц. Натл акад. науч. США 109 , 14508–14513 (2012 г.).
Артикул КАС Google Scholar
- «>
Schmitt, M.W. et al. Секвенирование небольших геномных мишеней с высокой эффективностью и предельной точностью. Нац. Методы 12 , 423–425 (2015).
Артикул КАС Google Scholar
Самородницкий Е. и др. Оценка гибридизационного захвата по сравнению с методами на основе ампликона для секвенирования всего экзома. Гул. Мутат. 36 , 903–914 (2015).
Артикул КАС Google Scholar
Chabon, J.J. et al. Интеграция геномных особенностей для неинвазивного раннего выявления рака легких. Природа 580 , 245–251 (2020).
Артикул КАС Google Scholar
Zheng, Z. et al. Закрепленная мультиплексная ПЦР для целевого секвенирования следующего поколения. Нац. Мед. 20 , 1479–1484 (2014).

Артикул КАС Google Scholar
Макаров В. и Лалиберте Дж. Усовершенствованное лигирование адаптера. Патент США 10 208 338B2 (2019 г.).
Peng, Q. et al. Направленное секвенирование с обогащением одного праймера с помощью одноконцевого дуплекса-UMI. науч. Отчет 9 , 4810 (2019).
Артикул Google Scholar
Vogelstein, B. et al. Ландшафты генома рака. Наука 339 , 1546–1558 (2013).
Артикул КАС Google Scholar
Снайдер, М. В., Кирхер, М., Хилл, А. Дж., Даза, Р. М. и Шендуре, Дж. Бесклеточная ДНК содержит нуклеосомный след in vivo, который сообщает ткани ее происхождения. Cell 164 , 57–68 (2016).
Артикул КАС Google Scholar
- «>
Нахмансон, Д. и др. Целенаправленная фрагментация генома с помощью CRISPR/Cas9 обеспечивает быстрое и эффективное обогащение небольших геномных областей и сверхточное секвенирование с минимальными затратами ДНК (CRISPR-DS). Рез. генома. 28 , 1589–1599 (2018).
Артикул КАС Google Scholar
Kennedy, S. R. et al. Обнаружение ультранизкочастотных мутаций методом дуплексного секвенирования. Нац. протокол 9 , 2586–2606 (2014).
Артикул КАС Google Scholar
Rago, C. et al. Серийная оценка опухолевого бремени человека у мышей с помощью анализа циркулирующей ДНК. Рак Res. 67 , 9364–9370 (2007).
Артикул КАС Google Scholar
Lennon, A.M. et al. Возможность анализа крови в сочетании с ПЭТ-КТ для скрининга рака и направления вмешательства.
 Наука 369 , eabb9601 (2020).
Наука 369 , eabb9601 (2020).Li, H. Выравнивание считываний последовательностей, клонирование последовательностей и сборка контигов с помощью BWA-MEM. Препринт на https://arxiv.org/abs/1303.3997 (2013 г.).
Ли, Х. и др. Формат выравнивания/карты последовательностей и SAMtools. Биоинформатика 25 , 2078–2079(2009).
Артикул Google Scholar
Смит, Т., Хегер, А. и Садбери, И. Инструменты UMI: моделирование ошибок секвенирования в уникальных молекулярных идентификаторах для повышения точности количественного определения. Рез. генома. 27 , 491–499 (2017).
Артикул КАС Google Scholar
Jiang, P. et al. Обнаружение и характеристика зазубренных концов двухцепочечной ДНК в плазме. Рез. генома.
 30 , 1144–1153 (2020).
30 , 1144–1153 (2020).Артикул КАС Google Scholar
Скачать ссылки
Благодарности
Мы благодарим всех, кто участвовал в этом исследовании, за их мужество и щедрость. Мы также благодарим М. Хоанга, С. Сура, А. Маттокса, А. Перлмана и сотрудников Центра Людвига в Университете Джонса Хопкинса за проницательные и полезные научные обсуждения. Мы благодарны C. Blair и K. Judge за экспертную техническую и административную помощь и E. Cook за иллюстративную помощь. Эта работа была поддержана Фондом исследований рака поджелудочной железы Люстгартена, Фондом Маркуса, Вирджинией и Д.К. Фонд Людвига для исследований рака, Фонд Конрада Н. Хилтона, Фонд Джона Темплтона, Грант исследователя Фонда медицинских исследований будущего (APP1194970) и гранты Национального института здравоохранения (T32 GM007309, U01 CA230691-01, P50 CA228991, U01 CA200469, R37 CA230400-01 и U01 CA152753).
Информация об авторе
Авторы и организации
Людвиг Центр генетики и терапии рака, Медицинский факультет Университета Джона Хопкинса, Балтимор, Мэриленд, США
Джошуа Д.
 Коэн, Кристофер Дувилль, Джонатан С. Дадли, Брайан Дж. . Мог, Мария Пополи, Джанин Птак, Лиза Доббин, Натали Силлиман, Джой Шефер, Николас Пападопулос, Кеннет В. Кинцлер и Берт Фогельштейн
Коэн, Кристофер Дувилль, Джонатан С. Дадли, Брайан Дж. . Мог, Мария Пополи, Джанин Птак, Лиза Доббин, Натали Силлиман, Джой Шефер, Николас Пападопулос, Кеннет В. Кинцлер и Берт ФогельштейнКомплексный онкологический центр имени Сидни Киммела, Медицинский факультет Университета Джона Хопкинса, Балтимор, Мэриленд, США
Джошуа Д. Коэн, Кристофер Дувиль, Джонатан С. Дадли, Брайан Дж. Мог, Мария Пополи, Джанин Птак, Лиза Доббин , Натали Силлиман, Джой Шефер, Кристиан Томасетти, Николас Пападопулос, Кеннет В. Кинзлер и Берт Фогельштейн
Исследовательский центр рака поджелудочной железы Сола Голдмана, Медицинский факультет Университета Джона Хопкинса, Балтимор, Мэриленд, США
Джошуа Д. Коэн, Кристофер Дувиль, Джонатан С. Дадли, Брайан Дж. Мог, Мария Пополи, Джанин Птак, Лиза Доббин, Натали Силлиман, Джой Шефер, Николас Пападопулос, Кеннет В. Кинзлер и Берт Фогельштейн
Ховард Медицинский институт Хьюза, Балтимор, Мэриленд, США
Джошуа Д.
 Коэн, Кристофер Дувилль, Джонатан С. Дадли, Брайан Дж. Мог, Мария Пополи, Джанин Птак, Натали Силлиман и Берт Фогельштейн
Коэн, Кристофер Дувилль, Джонатан С. Дадли, Брайан Дж. Мог, Мария Пополи, Джанин Птак, Натали Силлиман и Берт ФогельштейнДепартамент биомедицинской инженерии, Джонс Университет Хопкинса, Балтимор, Мэриленд, США
Джошуа Д. Коэн и Брайан Дж. Мог
Отдел персонализированной онкологии, Институт медицинских исследований Уолтера и Элизы Холл, Парквилл, Виктория, Австралия
Джинн Тай и Питер Гиббс
- 90 082 Отделение медицинской онкологии, Онкологический центр Питера Маккаллума, Мельбурн, Виктория, Австралия
Жанна Тай
Департамент медицинской онкологии, Western Health, Мельбурн, Виктория, Австралия
Жанна Ти и Питер Гиббс
Факультет медицины, стоматологии и медицинских наук Мельбурнского университета, Мельбурн, Виктория, Австралия США
Кристиан Томасетти
Авторы
- Джошуа Д. Коэн
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Christopher Douville
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Jonathan C.
 Dudley
DudleyПросмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Brian J. Mog
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Мария Пополи
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Janine Ptak
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Lisa Dobbyn
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Натали Силлиман
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Joy Schaefer
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Jeanne Tie
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Peter Gibbs
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Cristian Tomasetti
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Николас Пападопулос
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Kenneth W.
 Kinzler
KinzlerПосмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Bert Vogelstein
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Взносы
J.D.C., N.P., K.W.K. и Б.В. разработали метод SaferSeqS. JDC, CD, JCD, BJM, NP, KWK и Б.В. внесли свой вклад в разработку дизайна исследования. JDC, MP, JP, LD, NS и Дж.С. проводил опыты. Дж.Т. и П.Г. набрали участников и приобрели образцы. J.D.C. разработали биоинформатический конвейер SaferSeqS и проанализировали данные. Математический и статистический анализы были проведены J.D.C. и К.Т. Н.П., К.В.К. и Б.В. руководили исследованием. J.D.C. и Б.В. написали рукопись, которая была отредактирована и одобрена всеми авторами.
Авторы переписки
Переписка с Николас Пападопулос, Кеннет В. Кинзлер или Берт Фогельштейн.
Декларации этики
Конкурирующие интересы
B. V., K.W.K. и Н.П. являются основателями Thrive и Personal Genome Diagnostics, а также собственным капиталом в Exact Sciences и Personal Genome Diagnostics. К.В.К. и Н.П. являются консультантами Thrive. К.В.К. и B.V. являются консультантами Sysmex и Eisai, а K.W.K., B.V. и N.P. являются консультантами CAGE Pharma. B.V. также является консультантом Catalio, а K.W.K., B.V. и N.P. являются консультантами Neophore. CD. является консультантом Thrive и получает компенсацию в виде дохода и капитала. Компании, упомянутые выше, а также другие компании, лицензировали ранее описанные технологии, связанные с работой, описанной в этой статье, от Университета Джона Хопкинса. JDC, CD, BV, KWK, C.T. и Н.П. являются изобретателями некоторых из этих технологий. Лицензии на эти технологии связаны или будут связаны с долевыми или лицензионными выплатами изобретателям, а также Университету Джона Хопкинса. Дополнительные патентные заявки на работу, описанную в этой статье, поданы Университетом Джона Хопкинса.
V., K.W.K. и Н.П. являются основателями Thrive и Personal Genome Diagnostics, а также собственным капиталом в Exact Sciences и Personal Genome Diagnostics. К.В.К. и Н.П. являются консультантами Thrive. К.В.К. и B.V. являются консультантами Sysmex и Eisai, а K.W.K., B.V. и N.P. являются консультантами CAGE Pharma. B.V. также является консультантом Catalio, а K.W.K., B.V. и N.P. являются консультантами Neophore. CD. является консультантом Thrive и получает компенсацию в виде дохода и капитала. Компании, упомянутые выше, а также другие компании, лицензировали ранее описанные технологии, связанные с работой, описанной в этой статье, от Университета Джона Хопкинса. JDC, CD, BV, KWK, C.T. и Н.П. являются изобретателями некоторых из этих технологий. Лицензии на эти технологии связаны или будут связаны с долевыми или лицензионными выплатами изобретателям, а также Университету Джона Хопкинса. Дополнительные патентные заявки на работу, описанную в этой статье, поданы Университетом Джона Хопкинса. Условия всех этих договоренностей регулируются Университетом Джонса Хопкинса в соответствии с его политикой в отношении конфликта интересов. Остальные авторы заявляют об отсутствии конкурирующих интересов.
Условия всех этих договоренностей регулируются Университетом Джонса Хопкинса в соответствии с его политикой в отношении конфликта интересов. Остальные авторы заявляют об отсутствии конкурирующих интересов.
Дополнительная информация
Информация о рецензировании Nature Biotechnology благодарит Пола Спеллмана и других анонимных рецензентов за их вклад в рецензирование этой работы.
Примечание издателя Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Дополнительная информация
Дополнительная информация
Дополнительная информация Рис. 1–9и Примечание.
Сводка отчетов
Дополнительные таблицы 1–7.
Права и разрешения
Перепечатка и разрешения
Об этой статье
Эта статья цитируется
Отслеживание ранней метастатической диссеминации рака легкого в TRACERx с использованием ctDNA
- Кристофер Аббош
- Александр М.
 Франкелл
Франкелл - Чарльз Суонтон
Природа (2023)
Продольное когортное исследование наблюдения и ожидания у пациентов с полным клиническим ответом после химиолучевой терапии локализованного рака прямой кишки: протокол исследования
- Сина Ватандоуст
- Дэвид Ватчоу
- Христос С. Карапетис
Рак BMC (2022)
Ограничения и возможности технологий анализа внеклеточной ДНК в диагностике рака
- Пинг Сонг
- Люсия Руоджиа Ву
- Дэвид Ю Чжан
Природа Биомедицинская инженерия (2022)
Сверхчувствительный мониторинг пациентов с лейкемией с использованием анализов обнаружения мутаций superRCA
- Лей Чен
- Анна Эрикссон
- Ульф Ландегрен
Nature Communications (2022)
Циркулирующие биомаркеры в диагностике и лечении гепатоцеллюлярной карциномы
- Филип Джонсон
- Цин Чжоу
- Ю.
 М. Деннис Ло
М. Деннис Ло
Nature Reviews Гастроэнтерология и гепатология (2022)
в Reaktor — ADSR
В этом уроке я расскажу об основном детекторе частоты в Reaktor. Я начну с самого простого частотного детектора, объясню его недостатки, а затем разработаю лучшую версию с небольшим количеством математики и дополнительной работы. Давайте приступим к делу!
ПРОСТОЕ ОБНАРУЖЕНИЕ ЧАСТОТЫ
Базовую модель можно собрать, используя только два модуля – триггер от А до Е и таймер. Просто соедините их вот так, и все готово:
Это очень простая конструкция. Каждый раз, когда входящий звук переключается с отрицательного значения на положительное, модуль A to E Trig отправляет выходной сигнал. Затем модуль таймера выводит частоту, определенную двумя последними полученными событиями.
Этот макрос возвращает достаточно точное представление о входящей частоте. Однако, к сожалению, у него есть погрешность, из-за которой он колеблется на несколько герц выше и ниже фактической частоты.
Однако, к сожалению, у него есть погрешность, из-за которой он колеблется на несколько герц выше и ниже фактической частоты.
Причина этой ошибки объясняется в первом руководстве по сглаживанию, которое можно найти здесь. Проще говоря, из-за цифровой дискретизации маловероятно, что входящий сигнал будет дискретизирован точно при пересечении нуля — вместо этого мы обычно оставляем немного положительное значение менее чем за один период дискретизации до пересечения нуля. Эта степень ошибки может вызвать проблемы в нашем алгоритме.
Давайте рассмотрим пример. Модуль A to E Trig выводит событие только в том случае, если предыдущее значение было отрицательным, а текущее значение положительным. Допустим, сигнал пересекает ноль и в следующей точке дискретизации принимает значение 0,005, запуская модуль от A до E. Затем сигнал повторяется, снова пересекает нулевую точку, и на этот раз дискретизируется равным 0,004. Опять же, сработает модуль от A до E, что даст нам приблизительную частоту.
Тем не менее, сам сигнал еще не завершил полный цикл с тех пор, как мы в последний раз запускали модуль таймера — он прошел путь от 0,005 до 0,004, до завершения полного цикла еще 0,001! В результате модуль таймера будет выводить частоту, немного превышающую фактическую частоту. Короче говоря, время, которое мы рассчитываем, всегда будет отличаться на долю периода выборки.
К счастью, эту проблему не так сложно решить, применив немного математики.
УЛУЧШЕННОЕ ОБНАРУЖЕНИЕ ЧАСТОТЫ
Чтобы сделать улучшенную версию базового частотного детектора, нам нужно немного больше информации о волновой форме, с которой мы работаем. Когда происходит пересечение нуля, нам, во-первых, нужно знать, как далеко продвинулась волна за последний период дискретизации, а во-вторых, нам нужно знать, где была форма волны в последний раз, когда произошло пересечение нуля.
Эти фрагменты информации легко доступны для нас:
Математический макрос
Модуль «T» представляет собой единичную задержку, которая просто задерживает сигнал на один период выборки. Мы можем найти расстояние, пройденное за последний период выборки, просто вычитая предыдущую выборку из текущей.
Мы можем найти расстояние, пройденное за последний период выборки, просто вычитая предыдущую выборку из текущей.
Вы также можете заметить, что я заменил вход «A» в модуль запуска от A до E на входящую волну. Таким образом, модуль выводит значение пересечения нуля, когда оно происходит.
Таким образом, мы можем найти значение последнего пересечения нуля, просто используя модуль Order для запуска модуля Value (содержащего последнее пересечение нуля), а затем сохраняя новое значение пересечения нуля для использования в следующий раз. Мы вычитаем текущее значение из предыдущего, чтобы получить представление о том, насколько далеко мы находимся от точного волнового цикла (если значения равны, это означает, что мы нашли точный волновой цикл; однако почти во всех случаях мы будем обнаружить, что мы немного больше или меньше, чем точный цикл).
Теперь мы знаем, как далеко мы прошли за последний период выборки и насколько близко мы подошли к точному волновому циклу. Когда мы делим, как мы это делаем в конце макроса, у нас остается число, которое представляет количество времени, оставшееся от полного цикла, в периодах выборки.