Что такое удельная теплоемкость вещества, характеристики полиметилсилоксана
Характеризует теплоусвояемость единицы массы физической системы при нагреве на 1 градус.
Размерность удельной теплоемкости, обозначаемой латинской буквой Ср, — Дж/(кг-К). Кроме того, различают объемную теплоемкость С„ (Дж/(м3-К)) и мольную теплоемкость См (Дж/(моль-К)). Зависимость удельной теплоемкости от температуры следует учитывать при проектировании нагревательных систем устройств для пластикации полимерных материалов.
Удельная теплоемкость вещества показывает количество энергии, которую необходимо сообщить / отобрать, для того, чтобы увеличить / уменьшить температуру одного килограмма вещества на один градус Кельвина.
То
есть в других словах, если например удельная теплоемкость воды
равняется 4,2 кДж/(кг*К) — это значит, что для того, чтобы нагреть один
кг воды на один градус, необходимо передать этому кг воды 4,2 кДж
энергии.
Удельная теплоемкость для любого вещества есть величина переменная, то есть она зависит от температуры и агрегатного состояния вещества. Если продолжать пример с водой, то ее удельная теплоемкость для 0°С равняется 4,218, а при 40°С 4,178 кДж/(кг*К). Для льда теплоемкость еще ниже — 2,11 кДж/(кг*К) для льда с температурой 0°С.
Что касается воды, необходимо отметить, что это жидкость с самым высоким значением удельной теплоемкости. Другими словами, чтобы обеспечить заданное количество температуры, вода должна поглотить или отдать количество тепла значительно больше, чем любое другое тело такой же массы.
В связи с этим становится понятным интерес к воде, когда нужно обеспечить искусственный теплообмен. Количество тепла, необходимое для повышения температуры с Т н до Т k тела массой m можно рассчитать по следующей формуле:
Q = C x ( Т н – Т k ) x m , кДжгде m — масса тела, кг; С — удельная теплоемкость, кДж/(кг*К)
Удельная теплоемкость различных твердых веществ при 20 °С
( если не указано другое значение температуры )
Название |
Cp ж |
Название |
Cp ж |
Асбест |
0,80 |
Мрамор |
0,80 |
Асбоцемент (плиты) |
0,96 |
Панели легкие строительные |
1,47. |
Асфальт |
0,92 |
Парафин |
2,19 |
Базальт |
0,84 |
Песчаник глиноизвестковый |
0,96 |
Бакелит |
1,59 |
Песчаник керамический |
0,75-0,84 |
Бетон |
1,00 |
Песчаник красный |
0,71 |
Бумага сухая |
1,34 |
Пластмасса |
1. |
Волокно минеральное |
0,84 |
Полистирол |
1,38 |
Гипс |
1,09 |
Полиуретан |
1,38 |
Глина |
0,88 |
Полихлорвинил |
1,00 |
Гранит |
0,75 |
Пробка |
1,26. |
Графит |
0,84 |
Пробка, крошка |
1,38 |
Грунт песчаный |
1.1…3.2 |
Резина твердая |
1,42 |
Дерево, дуб |
2,40 |
Сера ромбическая |
0,71 |
Дерево, пихта |
2,70 |
Слюда |
0,84 |
Древесно-волокнистая плита |
2,30 |
Солидол |
1,47 |
Земля влажная |
2,0 |
Соль каменистая |
2. |
Земля сухая |
0,84 |
Соль каменная |
0,92 |
Земля утрамбованная |
1,0-3,0 |
Соль поваренная |
0,88 |
Зола |
0,80 |
Стекло |
0,75-0,82 |
Известь |
0,84 |
Стекловолокно |
0,84 |
Кальцит |
0,80 |
Тело человека |
3,47 |
Камень |
0. |
Торф |
1,67…2,09 |
Каолин ( белая глина ) |
0,88 |
Уголь бурый ( 0…100 °С ) |
|
Картон сухой |
1,34 |
20% воды |
2,09 |
Кварц |
0,75 |
60% воды |
3,14 |
Кизельгур ( диатомит ) |
0,84 |
в брикетах |
1,51 |
Кирпич |
0,84 |
Уголь древесный |
0,75. |
Кирпичная стена |
0,84… 1,26 |
Уголь каменный ( 0…100 °С ) |
1,17… 1,26 |
Кожа |
1,51 |
Фарфор |
0,80 |
Кокс ( 0…100 °С ) |
0,84 |
Хлопок |
1,30 |
( 0. |
1,13 |
Целлюлоза |
1.55 |
Лед ( 0 °С ) |
2.11 |
Цемент |
0,80 |
( -10 °С) |
2,22 |
Чугун |
0,55 |
( -20 °С ) |
2,01 |
Шерсть |
1,80 |
( -60 °С ) |
1,64 |
Шифер |
0,75 |
Лед сухой (твердая CO 2 ) |
1,38 |
Щебень |
0,75. |
Удельная теплоемкость различных жидких веществ при 20 ° С
( если не указано другое значение температуры )
Название |
Cp ж |
Название |
Cp ж |
Ацетон |
2,22 |
Масло минеральное |
1,67…2,01 |
Бензин |
2,09 |
Масло смазочное |
1,67 |
Бензол ( 10 °С ) |
1,42 |
Метиленхлорид |
1,13 |
Бензол ( 40 °С ) |
1,77 |
Метил хлорид |
1,59 |
Вода чистая ( 0 °С ) |
4,218 |
Морская вода ( 18 °С ) |
|
Вода чистая ( 10 °С ) |
4,192 |
0,5 % соля |
4,10 |
Вода чистая ( 20 °С ) |
4,182 |
3 % соля |
3,93 |
Вода чистая ( 40 °С ) |
4,178 |
6 % соли |
3,78 |
Вода чистая ( 60 °С ) |
4,184 |
Нефть |
0,88 |
Вода чистая ( 80 °С ) |
4,196 |
Нитробензол |
1,47 |
Вода чистая ( 100 °С ) |
4,216 |
Парафин жидкий |
2,13 |
Глицерин |
2,43 |
Рассол ( -10 °С ) |
|
Гудрон |
2,09 |
20% соли |
3,06 |
Деготь каменноугольный |
2,09 |
30% соли |
2,64. |
Дифенил |
2,13 |
Ртуть |
0,138 |
Довтерм |
1,55 |
Скипидар |
1,80 |
Керосин бытовой |
1,88 |
Спирт метиловый ( метанол ) |
2,47 |
Керосин бытовой ( 100 °С ) |
2,01 |
Спирт нашатырный |
4,73 |
Керосин тяжелый |
2,09 |
Спирт этиловый ( этанол ) |
2,39 |
Кислота азотная 100%-я |
3,10 |
Толуол |
1. |
Кислота серная 100%-я |
1,34 |
Трихлорэтилен |
0,93 |
Кислота соляная 17%-я |
1,93 |
Хлороформ |
1,00 |
Кислота угольная ( -190 °С) |
0,88 |
Этиленгликоль |
2,30 |
Клей столярный |
4,19 |
Эфир кремниевой кислоты |
1,47 |
Что такое ТЕПЛОЁМКОСТЬ смотрите ЗДЕСЬ.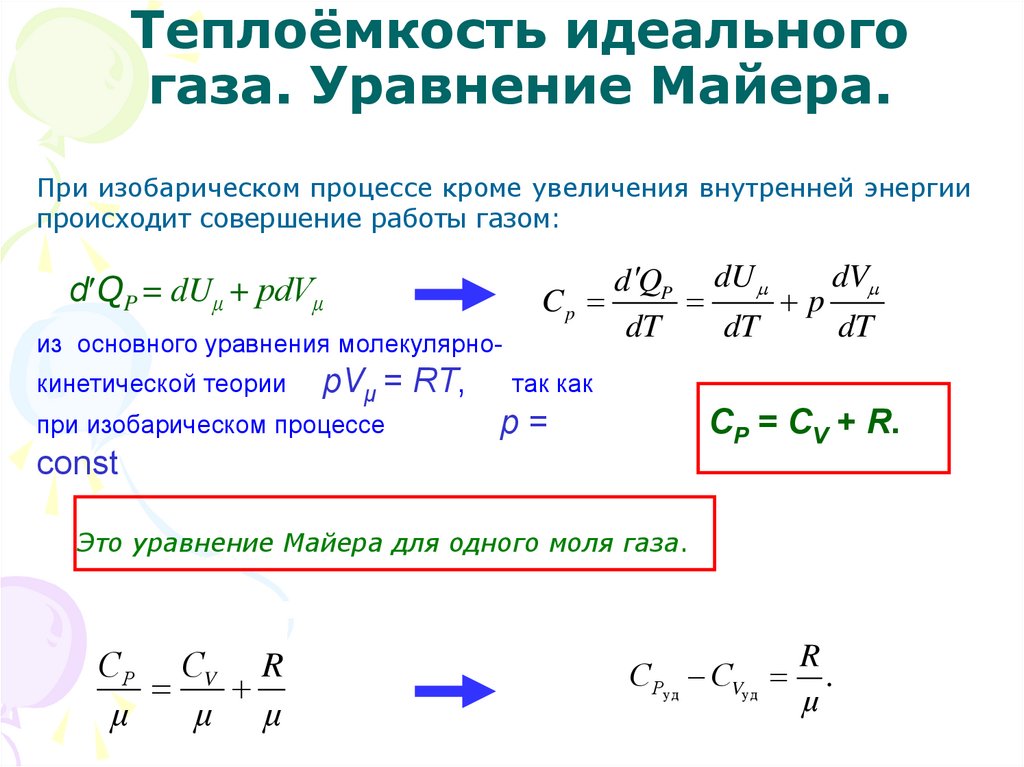
|
ОглавлениеОТ ИЗДАТЕЛЬСТВАИЗ ПРЕДИСЛОВИЯ К ПЕРВОМУ ИЗДАНИЮ ВВЕДЕНИЕ Глава I. Кинематика § 1. Движение тел § 2. Кинематика. Относительность движения и покоя. § 3. Траектория движения § 4. Поступательное и вращательное движения тела § 5. Движение точки § 6. Описание движения точки § 7. Измерение длины § 8. Измерение промежутков времени § 9. Равномерное прямолинейное движение и его скорость § 10. Знак скорости при прямолинейном движении § 11. Единицы скорости § 12. Графики зависимости пути от времени § 13. Графики зависимости скорости от времени § 14. Неравномерное прямолинейное движение § 15. Мгновенная скорость § 16. Ускорение при прямолинейном движении § 17.  Скорость прямолинейного равноускоренного движения Скорость прямолинейного равноускоренного движения§ 18. Знак ускорения при прямолинейном движении § 19. Графики скорости при прямолинейном равноускоренном движении § 20. Графики скорости при произвольном неравномерном движении § 21. Нахождение пути, пройденного при неравномерном движении, при помощи графика скорости § 22. Путь, пройденный при равнопеременном движении § 23. Векторы § 24. Разложение вектора на составляющие § 25. Криволинейное движение § 26. Скорость криволинейного движения § 27. Ускорение при криволинейном движении § 28. Движение относительно разных систем отсчета § 29. Кинематика космических движений Глава II. Динамика § 30. Задачи динамики § 31. Закон инерции § 32. Инерциальные системы отсчета § 33. Принцип относительности Галилея § 34. Силы § 35. Уравновешивающиеся силы. О покое тела и о движении по инерции § 36. Сила — вектор. Эталон силы § 37. Динамометры § 38. Точка приложения силы § 39.  Равнодействующая сила Равнодействующая сила§ 40. Сложение сил, направленных по одной прямой § 41. Сложение сил, направленных под углом друг к другу § 42. Связь между силой и ускорением § 43. Масса тела § 44. Второй закон Ньютона § 45. Единицы силы и массы § 46. Системы единиц § 47. Третий закон Ньютона § 48. Примеры применения третьего закона Ньютона § 49. Импульс тела § 50. Система тел. Закон сохранения импульса § 51. Применения закона сохранения импульса § 52. Свободное падение тел § 53. Ускорение свободного падения § 54. Падение тела без начальной скорости и движение тела, брошенного вертикально вверх § 55. Вес тела § 56. Масса и вес § 57. Плотность вещества § 58. Возникновение деформаций § 59. Деформации в покоящихся телах, вызванные действием только сил, возникающих при соприкосновении § 60. Деформации в покоящихся телах, вызванные силой тяжести § 61. Деформации тела, испытывающего ускорение § 62. Исчезновение деформаций при падении тел § 63.  Разрушение движущихся тел Разрушение движущихся тел§ 64. Силы трения § 65. Трение качения § 66. Роль сил трения § 67. Сопротивление среды § 68. Падение тел в воздухе Глава III. Статика § 69. Задачи статики § 70. Абсолютно твердое тело § 71. Перенос точки приложения силы, действующей на твердое тело § 72. Равновесие тела под действием трех сил § 73. Разложение сил на составляющие § 74. Проекции сил. Общие условия равновесия § 75. Связи. Силы реакции связей. Тело, закрепленное на оси § 76. Равновесие тела, закрепленного на оси § 77. Момент силы § 78. Измерение момента силы § 79. Пара сил § 80. Сложение параллельных сил. Центр тяжести § 81. Определение центра тяжести тел § 82. Различные случаи равновесия тела под действием силы тяжести § 83. Условия устойчивого равновесия под действием силы тяжести § 84. Простые машины § 85. Клин и винт Глава IV. Работа и энергия § 86. «Золотое правило» механики § 87. Применения «золотого правила» § 88.  Работа силы Работа силы§ 89. Работа при перемещении, перпендикулярном к направлению силы § 90. Работа силы, направленной под любым углом к перемещению § 91. Положительная и отрицательная работа § 92. Единица работы § 93. О движении по горизонтальной плоскости § 94. Работа силы тяжести при движении по наклонной плоскости § 95. Принцип сохранения работы § 96. Энергия § 97. Потенциальная энергия § 98. Потенциальная энергия упругой деформации § 99. Кинетическая энергия § 100. Выражение кинетической энергии через массу и скорость тела § 101. Полная энергия тела § 102. Закон сохранения энергии § 103. Силы трения и закон сохранения механической энергии § 104. Превращение механической энергии во внутреннюю энергию § 105. Всеобщий характер закона сохранения энергии § 106. Мощность § 107. Расчет мощности механизмов § 108. Мощность, быстроходность и размеры механизма § 109. Коэффициент полезного действия механизмов Глава V.  Криволинейное движение Криволинейное движение§ 110. Возникновение криволинейного движения § 111. Ускорение при криволинейном движении § 112. Движение тела, брошенного в горизонтальном направлении § 113. Движение тела, брошенного под углом к горизонту § 114. Полет пуль и снарядов § 115. Угловая скорость § 116. Силы при равномерном движении по окружности § 117. Возникновение силы, действующей на тело, движущееся по окружности § 118. Разрыв маховиков § 119. Деформация тела, движущегося по окружности § 120. «Американские горки» § 121. Движение на закруглениях пути § 122. Движение подвешенного тела по окружности § 123. Движение планет § 124. Закон всемирного тяготения § 125. Искусственные спутники Земли Глава VI. Движение в неинерциальных системах отсчета и силы инерции § 126. Роль системы отсчета § 127. Движение относительно разных инерциальных систем отсчета § 128. Движение относительно инерциальной и неинерциальной систем отсчета § 129.  Поступательно движущиеся неинерциальиые системы Поступательно движущиеся неинерциальиые системы§ 130. Силы инерции § 131. Эквивалентность сил инерции и сил тяготения § 132. Невесомость и перегрузки § 133. Является ли Земля инерциальиой системой отсчета? § 134. Вращающиеся системы отсчета § 135. Силы инерции при движении тела относительно вращающейся системы отсчета § 136. Доказательство вращения Земли § 137. Приливы Глава VII. Гидростатика § 138. Подвижность жидкости § 139. Силы давления § 140. Измерение сжимаемости жидкости § 141. «Несжимаемая» жидкость § 142. Силы давления в жидкости передаются во все стороны § 143. Направление сил давления § 144. Давление § 145. Мембранный манометр § 146. Независимость давления от ориентации площадки § 147. Единицы давления § 148. Определение сил давления по давлению § 149. Распределение давления внутри жидкости § 150. Закон Паскаля § 151. Гидравлический пресс § 152. Жидкость под действием силы тяжести § 153.  Сообщающиеся сосуды Сообщающиеся сосуды§ 154. Жидкостный манометр § 155. Устройство водопровода. Нагнетательный насос § 156. Сифон § 157. Сила давления на дно сосуда § 158. Давление воды в морских глубинах § 159. Прочность подводной лодки § 160. Закон Архимеда § 161. Измерение плотности тел на основании закона Архимеда § 162. Плавание тел § 163. Плавание несплошных тел § 164. Устойчивость плавания кораблей § 165. Всплывание пузырьков § 166. Тела, лежащие на дне сосуда Глава VIII. Аэростатика § 167. Механические свойства газов § 168. Атмосфера § 169. Давление атмосферы § 170. Другие опыты, показывающие существование атмосферного давления § 171. Разрежающие насосы § 172. Влияние атмосферного давления на уровень жидкости в трубке § 173. Максимальная высота столба жидкости § 174. Опыт Торричелли. Ртутный барометр и барометр-анероид § 175. Распределение атмосферного давления по высоте § 176. Физиологическое действие пониженного давления воздуха § 177.  Закон Архимеда для газов Закон Архимеда для газов§ 178. Воздушные шары и дирижабли § 179. Применение сжатого воздуха в технике Глава IX. Гидродинамика и аэродинамика § 180. Давление в движущейся жидкости § 181. Течение жидкости по трубам § 182. Закон Бернулли § 183. Жидкость в неинерциальных системах отсчета § 184. Реакция движущейся жидкости и ее использование § 185. Перемещение на воде § 186. Ракеты § 187. Реактивные двигатели § 188. Баллистические ракеты § 189. Взлет ракеты с Земли § 190. Сопротивление воздуха § 191. Эффект Магиуса и циркуляция § 192. Подъемная сила крыла и полет самолета § 193. Турбулентность в потоке жидкости или газа § 194. Ламинарное течение РАЗДЕЛ ВТОРОЙ. ТЕПЛОТА. МОЛЕКУЛЯРНАЯ ФИЗИКА Глава X. Тепловое расширение твердых и жидких тел § 195. Тепловое расширение твердых и жидких тел § 196. Термометры § 197. Формула линейного расширения § 198. Формула объемного расширения § 199. Связь между коэффициентами линейного и объемного расширения § 200.  Измерение коэффициента объемного расширения жидкостей Измерение коэффициента объемного расширения жидкостей§ 201. Особенности расширения воды Глава XI. Работа. Теплота. Закон сохранения энергии § 202. Изменения состояния тел § 203. Нагревание тел при совершении работы § 204. Изменение внутренней энергии тел при теплопередаче § 205. Единицы количества теплоты § 206. Зависимость внутренней энергии тела от его массы и вещества § 207. Теплоемкость тела § 208. Удельная теплоемкость § 209. Калориметр. Измерение теплоемкостей § 210. Закон сохранения энергии § 211. Невозможность «вечного двигателя» § 212. Различные виды процессов, при которых происходит передача теплоты Глава XII. Молекулярная теория § 213. Молекулы и атомы § 214. Размеры атомов и молекул § 215. Микромир § 216. Внутренняя энергия с точки зрения молекулярной теории § 217. Молекулярное движение § 218. Молекулярное движение в газах, жидкостях и твердых телах § 219. Броуновское движение § 220. Молекулярные силы Глава XIII.  Свойства газов Свойства газов§ 221. Давление газа § 222. Зависимость давления газа от температуры § 223. Формула, выражающая закон Шарля § 224. Закон Шарля с точки зрения молекулярной теории § 225. Изменение температуры газа при изменении его объема. Адиабатические и изотермические процессы § 226. Закон Бойля — Мариотта § 227. Формула, выражающая закон Бойля — Мариотта § 228. График, выражающий закон Бойля — Мариотта § 229. Зависимость между плотностью газа и его давлением § 230. Молекулярное толкование закона Бойля — Мариотта § 231. Изменение объема газа при изменении температуры § 232. Закон Гей-Люссака § 233. Графики, выражающие законы Шарля и Гей-Люссака § 234. Термодинамическая температура § 235. Газовый термометр § 236. Объем газа и термодинамическая температура § 237. Зависимость плотности газа от температуры § 238. Уравнение состояния газа § 239. Закон Дальтона § 240. Плотность газов § 241. Закон Авогадро § 242.  Моль. Постоянная Авогадро Моль. Постоянная Авогадро§ 243. Скорости молекул газа § 244. Об одном из способов измерения скоростей движения молекул газа (опыт Штерна) § 245. Удельные теплоемкости газов § 246. Молярные теплоемкости § 247. Закон Дюлонга и Пти Глава XIV. Свойства жидкостей § 248. Строение жидкостей § 249. Поверхностная энергия § 250. Поверхностное натяжение § 251. Жидкостные пленки § 252. Зависимость поверхностного натяжения от температуры § 253. Смачивание и несмачивание § 254. Расположение молекул у поверхности тел § 255. Значение кривизны свободной поверхности жидкости § 256. Капиллярные явления § 257. Высота поднятия жидкости в капиллярных трубках § 258. Адсорбция § 259. Флотация § 260. Растворение газов § 261. Взаимное растворение жидкостей § 262. Растворение твердых тел в жидкостях Глава XV. Свойства твердых тел. Переход тел из твердого состояния в жидкое § 263. Введение § 264. Кристаллические тела § 265.  Аморфные тела Аморфные тела§ 266. Кристаллическая решетка § 267. Кристаллизация § 268. Плавление и отвердевание § 269. Удельная теплота плавления § 270. Переохлаждение § 271. Изменение плотности веществ при плавлении § 272. Полимеры § 273. Сплавы § 274. Затвердевание растворов § 275. Охлаждающие смеси § 276. Изменения свойств твердого тела Глава XVI. Упругость и прочность § 277. Введение § 278. Упругие и пластические деформации § 279. Закон Гука § 280. Растяжение и сжатие § 281. Сдвиг § 282. Кручение § 283. Изгиб § 284. Прочность § 285. Твердость § 286. Что происходит при деформации тел § 287. Изменение энергии при деформации тел Глава XVII. Свойства паров § 288. Введение § 289. Пар насыщенный и ненасыщенный § 290. Что происходит при изменении объема жидкости и насыщенного пара § 291. Закон Дальтона для пара § 292. Молекулярная картина испарения § 293. Зависимость давления насыщенного пара от температуры § 294.  Кипение Кипение§ 295. Удельная теплота парообразования § 296. Охлаждение при испарении § 297. Изменение внутренней энергии при переходе вещества из жидкого состояния в парообразное § 298. Испарение при кривых поверхностях жидкости § 299. Перегревание жидкости § 300. Пересыщение паров § 301. Насыщение пара при возгонке § 302. Превращение газа в жидкость § 303. Критическая температура § 304. Сжижение газов в технике § 305. Вакуумная техника § 306. Водяной пар в атмосфере Глава XVIII. Физика атмосферы § 307. Атмосфера § 308. Тепловой баланс Земли § 309. Адиабатические процессы в атмосфере § 310. Облака § 311. Искусственные осадки § 312. Ветер § 313. Предсказание погоды Глава XIX. Тепловые машины § 314. Условия, необходимые для работы тепловых двигателей § 315. Паросиловая станция § 316. Паровой котел § 317. Паровая турбина § 318. Поршневая паровая машина § 319. Конденсатор § 320. Коэффициент полезного действия теплового двигателя § 321.  Коэффициент полезного действия паросиловой станции Коэффициент полезного действия паросиловой станции§ 322. Бензиновый двигатель внутреннего сгорания § 323. Коэффициент полезного действия двигателя внутреннего сгорания § 324. Двигатель Дизеля § 325. Реактивные двигатели § 326. Передача теплоты от холодного тела к горячему Ответы и решения к упражнениям Предметный указатель |
Различия между «теплоемкостью» и «удельной теплоемкостью»
Энергия может существовать во многих структурах, и теплота является одной из самых интересных. Жара регулярно скрывается, поскольку она может существовать в пути и перемещается различными, особенно различными способами. Тепловое движение связывается с каждой частью нашей жизни и помогает нам понять, как работают возможности Вселенной. Это объясняет холод, который мы чувствуем в достаточно ветреный вечер, или почему центр Земли до сих пор не может остыть.
Теплоемкость
Теплоемкость – это физическое свойство материи, определяемое как количество тепла, которое должно быть сообщено объекту для получения единичного изменения его температуры. Теплоемкостью называют также теплоемкостью.
Теплоемкостью называют также теплоемкостью.
Для понимания теплоемкости в первую очередь мы хотим получить тепло. Теплота — это своего рода энергия, которая переходит от объектов с более высокой температурой к объектам с более низкой температурой. Например, если мы коснемся горячей чашки эспрессо, нам будет жарко в свете того факта, что чашка передает свою энергию (тепло) в наше тело. Опять же, если мы соприкасаемся со стаканом холодной воды, тепловая энергия переходит от нашего тела к стеклу, заставляя его чувствовать себя холодным. Кроме того, единицей СИ для теплоты является джоуль (Дж). Кроме того, это отмечено как Q в ситуации.
Формула для теплоемкости
емкость (с) вещества – это теплоемкость иллюстрации вещества, деленная на массу модели. Удельную теплоемкость также иногда называют массовой теплоемкостью.Тепловая энергия = Q/∆T
Где ‘Q’ – количество теплоты
‘∆T’ удельная теплоемкость
7
 Небрежно, сколько теплоты должно быть добавлено к одной единице массы вещества, чтобы вызвать добавление одной единицы температуры.
Небрежно, сколько теплоты должно быть добавлено к одной единице массы вещества, чтобы вызвать добавление одной единицы температуры.Для общего понимания, когда люди находятся близко к морю, они видят, что вода холодная, а песок горячий. Солнце там сравнимо, откуда такая разница в температуре? они, наверное, подумали! Температура твердой и жидкой части повышается, когда мы подводим к ней тепло. Если принять, что мы передали сравнимую долю тепла двум разным видам твердых тел, то в этот момент температурное расширение может быть разным для обоих твердых тел. В соответствии с этим, в зависимости от возможности твердого тела, повышение температуры изменяется для различных видов твердых тел. Эта характеристика известна как удельная теплоемкость.
Формула удельной теплоемкости
Удельная теплоемкость (с) = Q/м∆T
Где ‘Q’ – количество теплоты
‘∆T’удельное относится к температуре
‘м
‘ stands for mass
Difference between Heat Capacity and Specific Heat Capacity
Heat Capacity | Specific heat capacity |
|
|
|
|
|
|
Где Q – количество тепла. ‘∆T’ конкретно относится к температуре.
|
Где Q — количество тепла. «∆T» относится к температуре. ‘m’ означает массу. |
Заключение
Основное различие между теплоемкостью и удельной теплоемкостью заключается в разнице в массе при расчете.
Оба они определяются как количество энергии, необходимой для повышения температуры, но в удельной теплоемкости емкость рассчитывается на единицу массы вещества.
Примеры задач
Задача 1: Кусок железа массой 135 г имеет удельную теплоемкость 0,43 Дж/г°C. Кроме того, он нагревается от 100°C до 350°C. Итак, подсчитайте, сколько тепловой энергии требуется?
Решение:
Масса (m) = 135 г
Удельная теплоемкость железа, (c) = 0,35 Дж/г°C
Изменение температуры (ΔT) = 350 – 100 = 250°C
Расчет,
Q = mc ΔT
Q = (135 г) (0,35 Дж/г°C) (250°C)
Q = 11 812,5 Дж
Итак, теплоемкость 135 г железа равна 11 8125,5 Дж.
Задача 2: Чтобы нагреть 75 граммов меди от 35 °С до 65 °С, требуется 427,5 Дж. Чему равна удельная теплоемкость в джоулях/г°С?
Решение:
Масса (M) = 427,5 J
Тепло медного Q = 75 г
Изменение температуры (ΔT) = 65 — 35 = 30 ° C
Расчет
Q = MCΔT
Подставляя числа в уравнение, мы получаем:
427,5 Дж = (75 г)c(30°C)
Решите для c,
c = 427,5 Дж/(75 г)(30°C)
c = 0,19 Дж/г·°C
Удельная теплоемкость меди 0,19 Дж/г·°С.

Задача 3: Кусок меди массой 85 г имеет удельную теплоемкость = 0,13 Дж/г°C. Точно так же он нагревается от 70°C до 150°C. Таким образом, установить, сколько тепловой энергии требуется?
Решение:
Масса (m) = 85 г
Удельная теплоемкость железа, (c) = 0,13 Дж/г°C
Изменение температуры (ΔT) = 70 – 150 = 80°C
Расчет
Q = mc ΔT
Q = (85 г) (0,13 Дж/г°C) (80°C)
Q = 884 Дж
Итак, теплоемкость 85 г меди равна 884 Дж.
Задача 4: Чтобы нагреть 55 граммов железа от 25°С до 40°С, требуется 420,5 Дж. Чему равна удельная теплоемкость в джоулях/г°С?
Решение:
Масса (m) = 420,5 г
Теплота меди Q = 55 г
Изменение температуры (ΔT) = 25 – 40 = 15°C
Расчет
Q = mcΔT
Подставляя числа в уравнение, получаем:
420,5 Дж = (55 г)c(15°C)
Решите для c,
c = 420,5 Дж/(55 г)(15°C)
c = 0,50 Дж/г°C
Удельная теплоемкость железа 0,50 Дж/г°C.

Задача 5. Если для повышения температуры 150 г вещества на 15°С (без фазового перехода) требуется 600 Дж тепловой энергии, рассчитайте удельную теплоемкость вещества. 9
Температура = 15 °C 15°C)
= 0,266 Джг°C
Следовательно, удельная теплоемкость вещества равна 0,266 Джг°C
Задача 6. Кубик свинца массой 600 г нагревается с 30°C до 80°C . Какое количество энергии потребовалось для нагревания свинца? Удельная теплоемкость свинца составляет 0,22 Дж/г°С.
Раствор:
m = 600 грамм
c = 0,22 Дж/г°C
ΔT = (T конечная – T начальная) = (80°C – 30°C) = 50°C
Подставьте эти значения в приведенное выше уравнение теплоемкости.
Q = mcΔT
Q = (600 грамм)·(0,22 Дж/г°C) × (50°C)
Q = 6600 Дж
Для нагрева свинцового кубика из от 25°С до 75°С.
термодинамика — Зависит ли удельная теплоемкость от температуры вещества?
$\begingroup$
Веществу при температуре 200 градусов Цельсия дается некоторое количество тепла, чтобы поднять его температуру на один градус Цельсия, и этому же веществу при температуре -200 градусов Цельсия дается некоторое количество тепла, чтобы увеличить его температуру до -199 градусов Цельсия. Одинаково ли количество теплоты, необходимое для обоих процессов?
Одинаково ли количество теплоты, необходимое для обоих процессов?
- термодинамика
- теплопроводность
$\endgroup$
2
$\begingroup$
В общем случае теплоемкость зависит от температуры, поэтому ответ — нет, количество разное. Однако из-за теоремы о равнораспределении при достаточно высокой температуре (по сравнению с типичной температурной шкалой, заданной квантовой механикой) температурная зависимость выравнивается. Известно, что это приводит к закону Дюлонга-Пти для твердых тел или постоянной теплоемкости идеальных газов, которые вы, должно быть, видели. Вот почему, чтобы наблюдать температурную зависимость, вам нужно перейти к низкой температуре (возьмем, например, теплоемкость Дебая для твердых тел) или включить много степеней свободы (возьмем излучение черного тела). Как следствие 3-го закона термодинамики или, в более общем смысле, конечного значения остаточной энтропии, вам также необходимо иметь нулевое значение теплоемкости при низкой температуре.

 ..1,88
..1,88 67…2.09
67…2.09 ..2,51
..2,51 1…3.0
1…3.0 84..1,26
84..1,26 .. 1,17
.. 1,17 ..1000 °C )
..1000 °C ) ..1,00
..1,00 ..2,72
..2,72 72
72
