Устройство автомобильной аккумуляторной батареи.
Рассмотрим несколько популярных на нашем рынке технологий.
Самая на данный момент популярная Свинцово-кислотная Сурьмянистая батарея — в пластины начали добавлять такой металл как СУРЬМА «Sb», они стали намного прочнее, теперь температурные перепады им были не страшны. НО минусами можно назвать кипение при 100% заряде (проходит интенсивный процесс электролиза, теряется большая часть воды из электролита). А также интенсивный саморазряд. В таких батареях обычный электролит представляет собой смесь дистиллированной воды и серной кислоты. Свинцово-кислотный аккумулятор представляет собой чередующиеся отрицательные и положительные электроды, к которым подключена активная масса. В свою очередь батарея состоит из 6 аккумуляторов, последовательно соединенных и находящихся в одном корпусе. Для изготовления корпуса применяется материал пропилен, он не способен проводить ток и одновременно с этим легко противостоит разъедающим свойствам кислоты.
Для создания электродов применяют свинцовый сплав. В большинстве современных аккумуляторов для создания электродов применяют свинцово-кальциевый сплав. Благодаря этому такие аккумуляторные батареи очень медленно саморазряжаются — за 18 месяцев теряют 50% емкости, а также имеют малый расход воды — 1 г/Ач. Из этого следует, что во время эксплуатации такой батареи можно обойтись без добавления воды.
Кальциевая аккумуляторная батарея — в наши дни набирающая популярность. Это батарея в которой свинцовые решетки легированы небольшим количеством кальция (Ca), около 0,07 — 0,1% от общего веса (в современных типах может быть немного больше). На корпусе можно видеть такие надписи — Ca/Ca (говорит о том что обе пластины и «плюсовая», и «минусовая» легированы этой добавкой). Для чего добавлен кальций в пластины? Причин здесь много, но основных всего две — это уменьшение саморазряда (к слову он уменьшился в 6 раз), а также снизить потерю воды из электролита (здесь этот процесс не такой интенсивный, а поэтому батарею можно сделать почти необслуживаемой)
Гибридная – это что-то среднее между кальцием и сурьмой, здесь одна пластина с добавками кальция, а другая сурьмы, обозначение «Sb/Ca» или «Ca+». Этот вид впитал в себя достоинства одной и другой технологий.
Этот вид впитал в себя достоинства одной и другой технологий.
Пластины с положительным зарядом у гибридного аккумулятора производится из свинца с добавкой сурьмы. Отрицательный электрод производится из сплава свинца с кальцием.
В результате совмещаются преимущества двух технологий и устраняются их недостатки. Положительный электрод из свинцово-сурьмянистого сплава даёт устойчивость к глубокому разряду, а отрицательный электрод с кальцием снижает саморазряд и выкипание воды из электролита.
При производстве отрицательного электрода была использована технология ExMET (Expanded Metal) данная технология даёт возможность выпускать электроды меньшей толщины и массы. Благодаря отсутствию перегрева увеличилась прочность пластин. Она обеспечивает более жёсткую структуру пластин, снижает коррозию и обеспечивает высокие эксплуатационные характеристики гибридных аккумуляторов.
Кальциевые и гибридные аккумуляторы ещё не настолько сильно распространены, как сурьмянистые, но постепенно они завоёвывают место на рынке.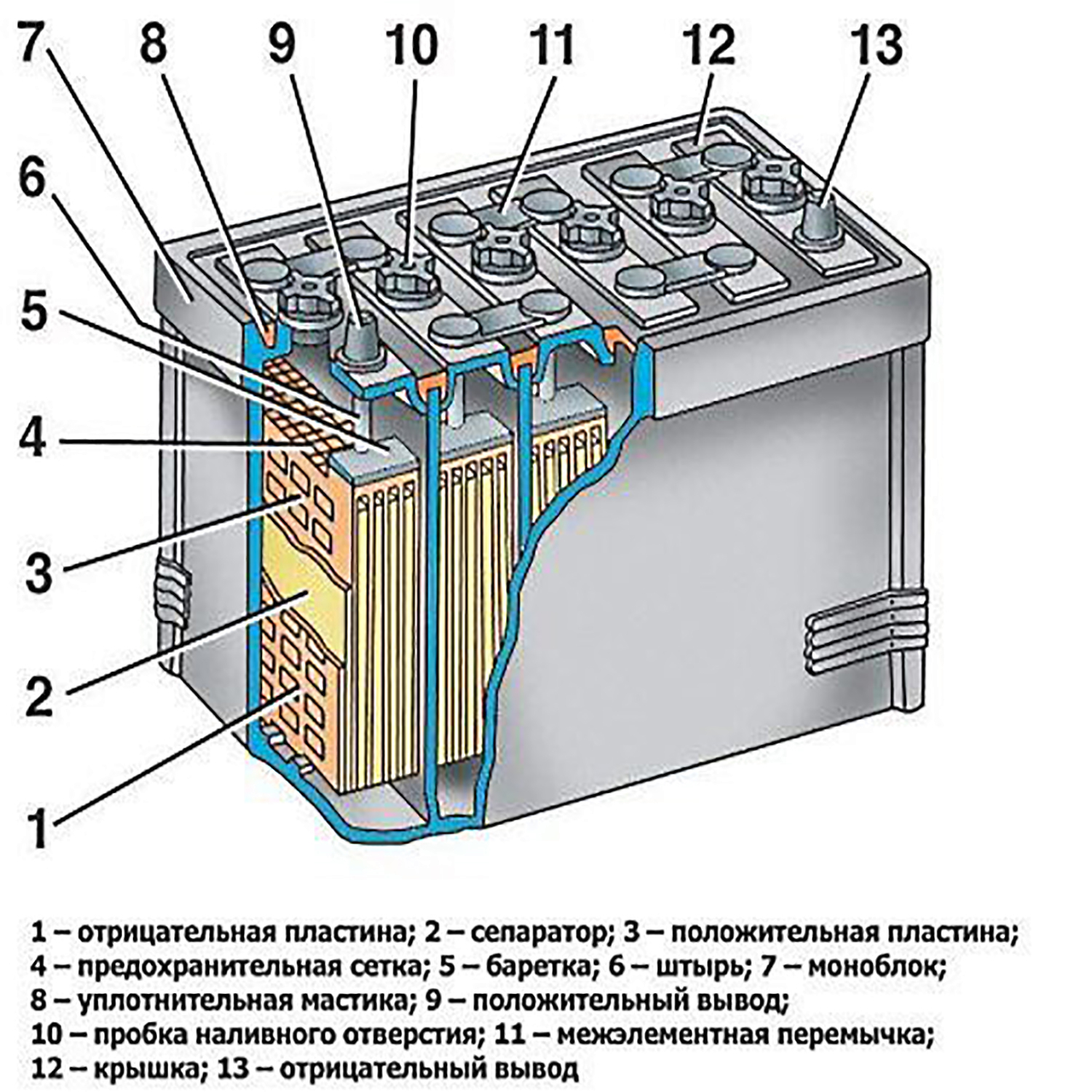 Пока их массовое использование тормозится достаточно высоким ценником.
Пока их массовое использование тормозится достаточно высоким ценником.
И на конец самая усовершенствованная на данный момент свинцово-кислотная технология абсорбирующего стекловолокна (AGM)
Выбирая AGM на основе самой совершенной технологии Absorbent Glass Mat (абсорбирующее стекловолокно), Вы получаете исключительно качественный аккумулятор, который способен удовлетворить потребности в энергии самых требовательных автомобилей и оборудования. Аккумулятор AGM безопасен и герметичен даже в случае поломки. Технология AGM обеспечивает в три раза больший срок службы в циклах по сравнению с обычными аккумуляторами, что идеально подходит для усовершенствованных систем Start-Stop, в которых аккумулятор нужно быстро подзаряжать энергией рекуперативного торможения.
Аккумуляторы Powersports AGM спроектированы с учетом работы в суровых условиях. Благодаря усовершенствованной технологии AGM этот сложный продукт обеспечивает максимальную мощность в течение длительного времени и не требует обслуживания.
Впитывающий стекломат (AGM)
Специальный стекловолоконный сепаратор впитывает весь электролит в аккумуляторе и обеспечивает высокую устойчивость к циклированию. Это позволяет аккумулятору выдерживать многочисленные циклы заряда-разряда без потери производительности.
Узнать больше о технологии AGM
Автомобильный аккумулятор (АКБ). Общее устройство аккумулятора
Неотъемлемой частью каждого автомобиля является аккумуляторная батарея, которая предназначена для питания электрических цепей управления и сервиса бортовой сети, когда двигатель автомобиля не работает. Но самое главное,- приводить в действие стартер, во время заводки авто. Аккумуляторная батарея включается в буфер с автомобильным генератором и во время движения, или просто работы двигателя, является нагрузкой для генератора. Но как только вся совокупная электрическая нагрузка превысит мощность выдаваемую генератором, в действие «вступает» аккумулятор и поддерживает напряжение бортовой сети на уровне 12 вольт.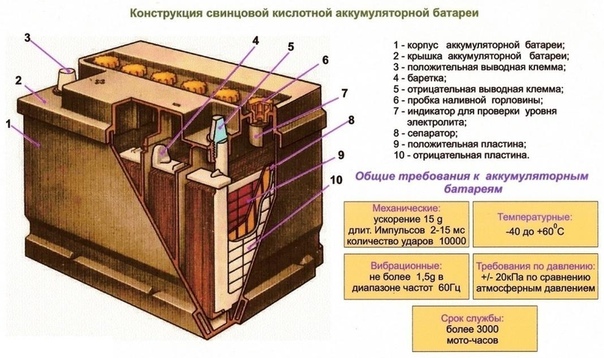
Обычно для автомобилей применяются кислотно-свинцовые аккумуляторы, которые имеют напряжение 12 вольт и различаются только по емкости заряда. Автомобильный аккумулятор должен обладать несколькими важными параметрами.
- Иметь малое внутренне падение напряжения
- Иметь небольшой саморазряд во время эксплуатации
- Иметь способность выдавать большие токи
- Иметь небольшие габариты и минимальное обслуживание.
Всем этим параметрам и соответствует кислотно-свинцовый аккумулятор, об устройстве которого поговорим ниже.
Устройство аккумулятора автомобиля
Аккумулятор, с номинальным напряжением в 12 вольт состоит из (обычно 6) независимых друг от друга аккумуляторов (банок) меньшего напряжения (2 вольта), собранных в одном корпусе и соединенных последовательно между собой.
- Банка аккумулятора представляет собой набор разно полюсных пластин, которые изолированы друг от друга кислотоупорными сепараторами.

- Корпус аккумулятора изготавливается из кислотоупорных пластмасс или эбонита. В корпусе имеется отсеки для установки банок аккумулятора.
- Полюсная пластина изготавливается из свинца и имеет вид решетки, в ячейки решетки впрессовывается специальный состав (активное вещество) пористой структуры, для увеличения площади соприкосновения с электролитом. Активное вещество изготавливается из свинцового порошка, с добавлением серной кислоты. В отрицательные пластины добавляется еще сернокислый барий. Во время формирования аккумулятора пластины заряжаются, и активное вещество в плюсовых пластинах превращается в диоксид свинца, а в отрицательных – в губчатый свинец.
- Электролит заливается в банки аккумулятора и служит для движения заряженных частиц от полюса к полюсу. Изготавливается из серной кислоты и очищенной воды (дистиллированной).
Принцип работы аккумуляторной батареи
Физика процесса работы аккумулятора очень проста, при подключении нагрузки, в аккумуляторе начинается движение заряженных частиц, что приводит к появлению тока. В условиях заряда от генератора или зарядного устройства, напряжение заряда превышает номинальное значение напряжения аккумулятора, и движение частиц происходит в обратном направлении.
В условиях заряда от генератора или зарядного устройства, напряжение заряда превышает номинальное значение напряжения аккумулятора, и движение частиц происходит в обратном направлении.
|
РЕКОМЕНДУЕМ ТАКЖЕ ПРОЧИТАТЬ:
|
Устройство аккумуляторной батареи
На легковых машинах в качестве стартерных используются свинцово-кислотные автомобильные аккумуляторы. Строение аккумуляторных батарей постоянно меняется и становится лучше.
Схема аккумуляторной батареи
 Пластмассовый сепаратор изолирует пластины противоположной полярности.
Пластмассовый сепаратор изолирует пластины противоположной полярности.Электроды производят из свинцового сплава. В нынешних аккумуляторных батареях электроды «+» и «-«производятся из свинцово-кальциевого сплава. У такого типа АКБ низкий уровень саморазряда, и самый небольшой расход воды (1 г/Ач). Это дает возможность совсем не добавлять воду за время использования – это необслуживаемый аккумулятор.
Редко можно встретить более недорогую конструкцию, так называемую гибридную аккумуляторную батарею
. В ней электроды со знаком»+» свинцово-сурмяные, а со знаком «-» – свинцово-кальциевые. В таких акб расходуется воды в 1,5-2 раза больше кальциевой батареи, но им также не нужно обслуживание.Чтобы увеличить стойкость электродов не подвергаться ржавчине в свинцово-кальциевый сплав может добавляться серебро и олово.
Электроды выглядят в виде решетки. Технологии производства электродов с разными полюсами различны. Решетка отрицательных электродов по технологии Expanded metal изготавливается путем просечки свинцового листа со следующей растяжкой.
При изготовлении положительных электродов могут применять несколько технологий. Самая лучшая технология Power Frame. Каждый электрод Power Frame имеет специальную опорную раму и внутренние жилки особой направленности, в итоге получается высокая жесткость и самое малое линейное расширение. Самые несложные электроды, произведенные по технологии Power Pass и Chess Plate.
Электроды помещены в специальный электролит, в качестве которого применяют раствор серной кислоты. У электролита особую плотность, которая меняется в зависимости от того насколько заряжен АКБ. В зависимости от физического состояния электролита разделяют два вида акб: с жидким электролитом и с пропитавшим специальный материал электролитом. На сегодняшний день, самые известные аккумуляторы используют с жидким электролитом. Новые системы автомобиля, такие как система стоп-старт, система особого рекуперативного торможения, предъявляют самые высокие требования к аккумулятору- повышенный пусковой ток, стойкость к значительному разряду, значительный срок службы. Этим требованиям отвечают аккумуляторы AGM (Absorbed Glass Material), в которых электролит остается в материале с микропорами. Материал способен впитывать электролит. Данная технология повышает эффективность активной массы за счет улучшенного поглощения кислоты.
В будущем аккумуляторы типа AGM и EFB на 100% заменят свинцово-кальциевые батареи с жидким электролитом. На данный момент они считаются дорогими АКБ.
Зарядка аккумулятора сопровождается газообразованием. Отвод газов от АКБ проводится через систему вентиляции. Центральная система вентиляции объединяет каждый отдельно взятый аккумулятор в составе батареи с атмосферой. Герметичной она считается из-за предохранительных клапанов. Клапан устанавливается в пробке акб и начинает работать при определенном лишним давлении. Система названа Valve Regulated Lead Acid Battery или VRLA батарея. Кислород и водород, которые образуются при заряде, не выходят с аккумулятора, а работают между собой с образованием воды. Выходят они только при значительном напряжении заряда.
Выходят они только при значительном напряжении заряда.
Подключение аккумулятора к электрической сети производится через два свинцовых вывода. Вывод «+» всегда толще «-«, что исключает ошибку при включении батареи. Полярность (расположение) выводов делят на прямой или обратный. При прямой полярности плюсовой вывод батареи можно найти слева, при обратной полярности справа.
Автомобильные аккумуляторы оборудуются специальным индикатором заряженности батареи, некоторым «глазком». Плотность электролита можно оценить по цвету «глазка» («зеленый» –заряженная батарея, «черный» – неполный заряд, «желтый» – невысокий уровень электролита).
На автомобиле АКБ прочно закрепляются через специальное крепление, которая предупреждает повреждения и разлив электролита. Крепление бывает верхним и нижним. Для батарей в основной части или багажнике автомобиля предусматривается особый аварийный размыкатель автомобильной батареи.
АКБ и зарядное устройство для него можно купить в магазинах «Интерком», заказать товар с доставкой можно в нашем интернет магазине. Приезжайте в наши магазины, делайте заявки и получайте товары с заводской гарантией.
Приезжайте в наши магазины, делайте заявки и получайте товары с заводской гарантией.
Принцип работы аккумуляторной батареи (АКБ)
Важной частью каждого автомобиля является аккумуляторная батарея (АКБ).
Автомоби́льный аккумуля́тор — это тип аккумулятора, который применяется на автомобильном или мототранспорте. Используется в качестве источника электроэнергии для работы бортовой сети автомобиля при неработающем двигателе или для запуска двигателя.
АКБ служит для электрического питания цепей управления и бортовой сети, когда двигатель не работает. Но самое главное его предназначение – пуск двигателя. АКБ приводит в действие стартер, во время заводки двигателя автомобиля.
В последнее время на автомобилях применяют кислотно-свинцовые аккумуляторы, с напряжением 12 В. Они хорошо зарекомендовали себя и имеют долгий срок эксплуатации. Но если ваш аккумулятор сдох, можно попытаться реанимировать АКБ.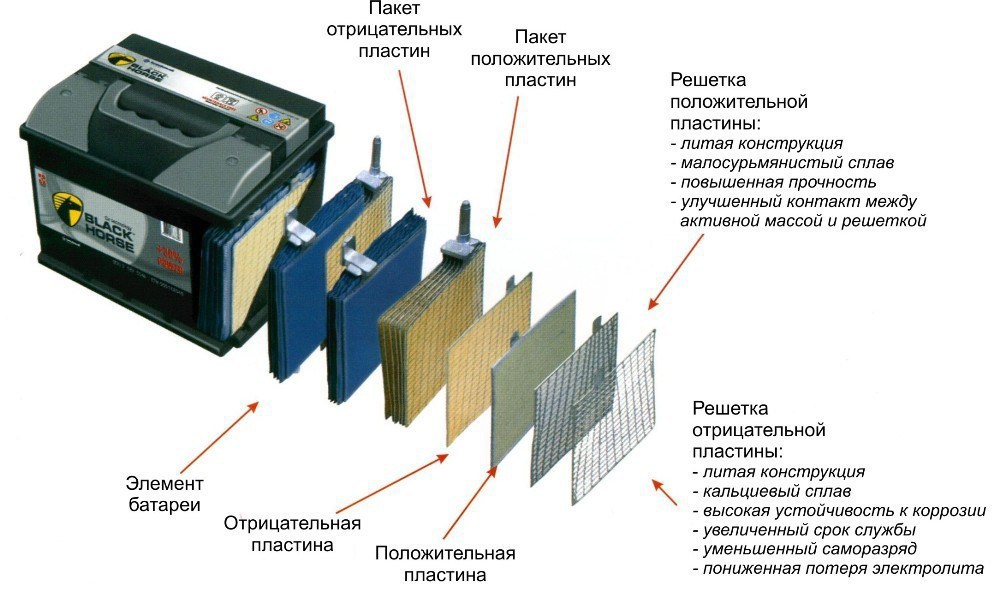
Основные параметры автомобильного аккумулятора, которыми он должен обладать
- Не большое внутреннее падение напряжения;
- Медленный саморазряд во время эксплуатации;
- Способность выдавать большие токи;
- Удобные габариты и простое обслуживание.
Кислотно-свинцовый автомобильный аккумулятор соответствует этим требованиям.
Устройство аккумуляторной батареи (АКБ)
Аккумулятор 12В состоит из нескольких независимых друг от друга банок — аккумуляторов по 2 В. каждый. Аккумуляторы последовательно собираются и соединяются между собой в одном корпусе.
- Банка аккумулятора состоит из полюсных пластин, изолированных друг от друга кислотоупорными сепараторами.
- Корпус аккумулятора изготовлен из специальной кислотоупорной пластмассы или эбонита. В корпусе вылиты специальные отсеки для установки банок аккумулятора.

- Полюсная пластина представляет собой решетку с ячейками, изготавливаемую из свинца. В каждую ячейку решетки впрессовано активное вещество пористой структуры, что обеспечивает увеличение площади соприкосновения с электролитом.
В состав активного веществавходит свинцовый порошок с добавлением серной кислоты. В отрицательных пластинах размещается сернокислый барий. Во время формировки АКБ пластины заряжаются, и активное вещество превращается в диоксид свинца, а в отрицательных – в губчатый свинец.
Электролит – специальная жидкость, которая заливается в банки аккумулятора и служит для движения заряженных частиц от полюса к полюсу. Электролит состоит из серной кислоты и очищенной дистиллированной воды.
Принцип работы аккумуляторной батареи (АКБ)
В процессе работы в АКБ происходит движение заряженных частиц, вследствие чего появляется ток.
Обслуживание АКБ
АКБ необходимо обслуживать и заряжать. Если вы настоящий автомобилист или водитель вам следует знать как заряжать АКБ. Если вы столкнулись с проблемой пуска двигателя зимой, скорее всего вам придется запустить двигатель от АКБ другого автомобиля.
Как устроен автомобильный аккумулятор — типы современных АКБ, принцип их работы, конструктивные особенности
- Все статьи
- Как устроен автомобильный аккумулятор — типы современных АКБ, принцип их работы, конструктивные особенности
Автомобильный аккумулятор выполняет три функции. Основанная функция АКБ – это запуск двигателя. Также, батарея питает бортовые электрические устройства – при неработающем двигателе. Вторая важная функция – возможность аварийного питания, источником которого аккумулятор выступает в случае поломки генератора. Третья функция – это достижение баланса напряжения, которое поступает от генератора. Эта функция характерна для инжекторных двигателей.
Третья функция – это достижение баланса напряжения, которое поступает от генератора. Эта функция характерна для инжекторных двигателей.
Устройство аккумулятора автомобиля существенно не меняется уже много десятилетий. Хотя развитие технологий и появление новых материалов более высокого качества способствует более надежной конструкции и работе АКБ.
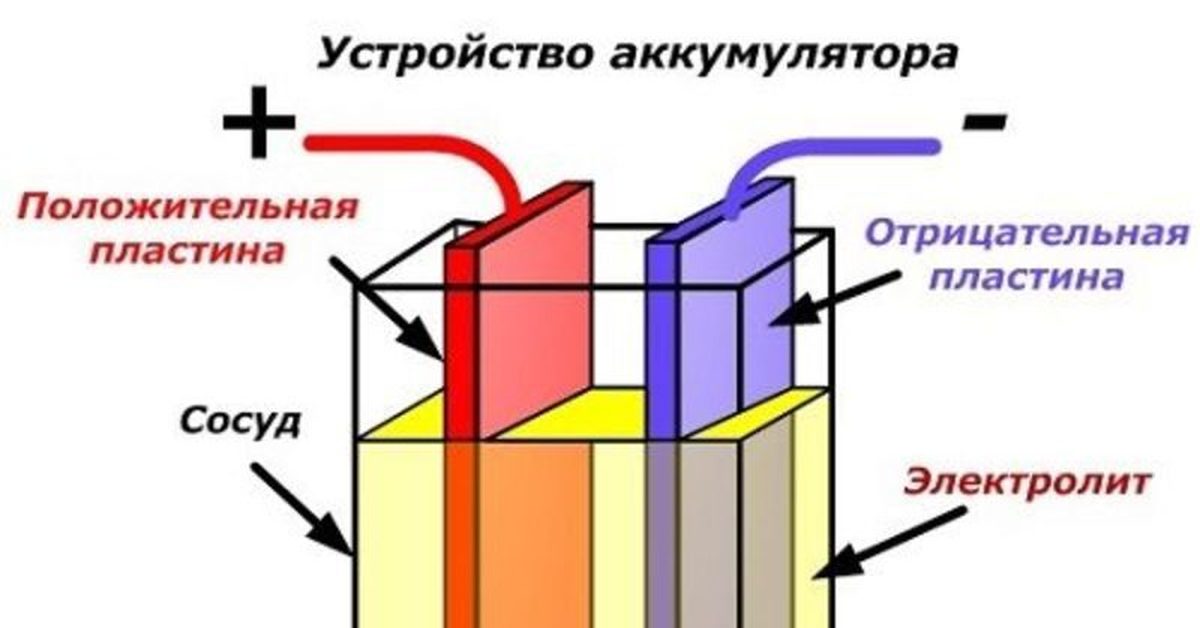
Основу работы аккумулятора составляет принцип возникновения разности потенциалов – то есть, напряжения. Оно возникает между пластинами, которые погружены в раствор электролита.
АКБ – устройство, которое, в зависимости от типа и производителя, имеет определенные конструктивно-технологические различия. Но общий принцип – одинаков: все аккумуляторные батареи содержат электроды, разделенные сепараторами, и помещенные в пространство, заполненное электролитом.
Корпус
Корпус аккумулятора состоит из двух частей: основной глубокой емкости и закрывающей крышки. Она может быть оснащена горловинами с пробками или системой, при помощи которой стабилизируется давление внутри батареи, и отводится образующийся газ.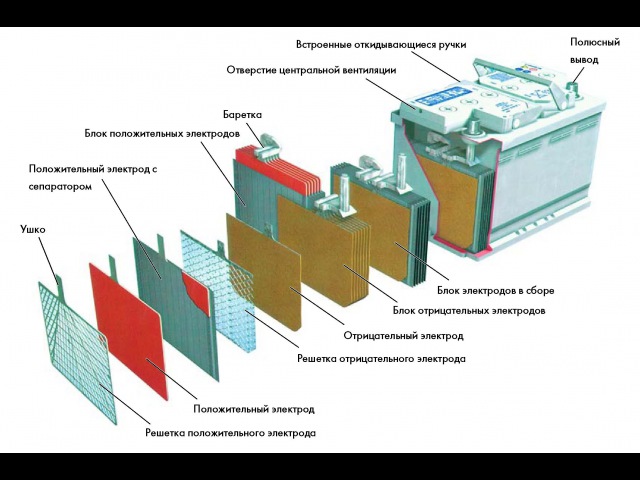 Конструкция корпуса зависит от типа АКБ.
Конструкция корпуса зависит от типа АКБ.
Сам корпус изготовлен из материала, к которому предъявляются большие требования прочности и безопасности. Он должен быть устойчив к воздействию агрессивных химических реагентов, переносить колебания температуры и сильную вибрацию. В большинстве современных аккумуляторов корпус сделан из полипропилена.
Внутренние отсеки
Стандартное устройство аккумуляторной батареи представляет собой контейнер, состоящий из шести секций (или, как их называют, «банок»). Каждая секция – это отдельный источник питания. Она вырабатывает порядка 2 – 2,1 В. Стандартная АКБ рассчитана на 12 В.
В каждой из ячеек находится набор (или пакет) из отдельных пластин с чередующейся полярностью. То есть, одна пластина положительная, другая отрицательная. Причем, пластины отделены друг от друга. Пластины сделаны из свинца и имеют решетчатую структуру в виде прямоугольных сот. Это облегчает нанесение них активной массы – основного рабочего реагента.
Пластины
Для увеличения прочности пластин в них добавляют сурьму. У этой технологии есть и свои недостатки: присутствие сурьмы способствует выкипанию воды из электролита. Это – основная причина, по которой практически во все типы АКБ необходимо доливать воду. Но технологии не стоят на месте. Устройство автомобильных аккумуляторов совершенствуется. Количество сурьмы в свинцовых пластинах значительно уменьшилось, благодаря чему появились малообслуживаемые и гибридные аккумуляторы.
На положительный электрод наносится двуокись свинца, на отрицательный – губчатый свинец. Внутрь заливается электролит, который является водным раствором серной кислоты.
Каждая чередующаяся пластина является электродом, имеющим противоположную полярность. Таким образом, с целью предотвращения замыкания, между каждой парой пластин располагается сепаратор. Он изготовлен из пористого пластика и не создает препятствий для циркуляции электролита внутри ячейки.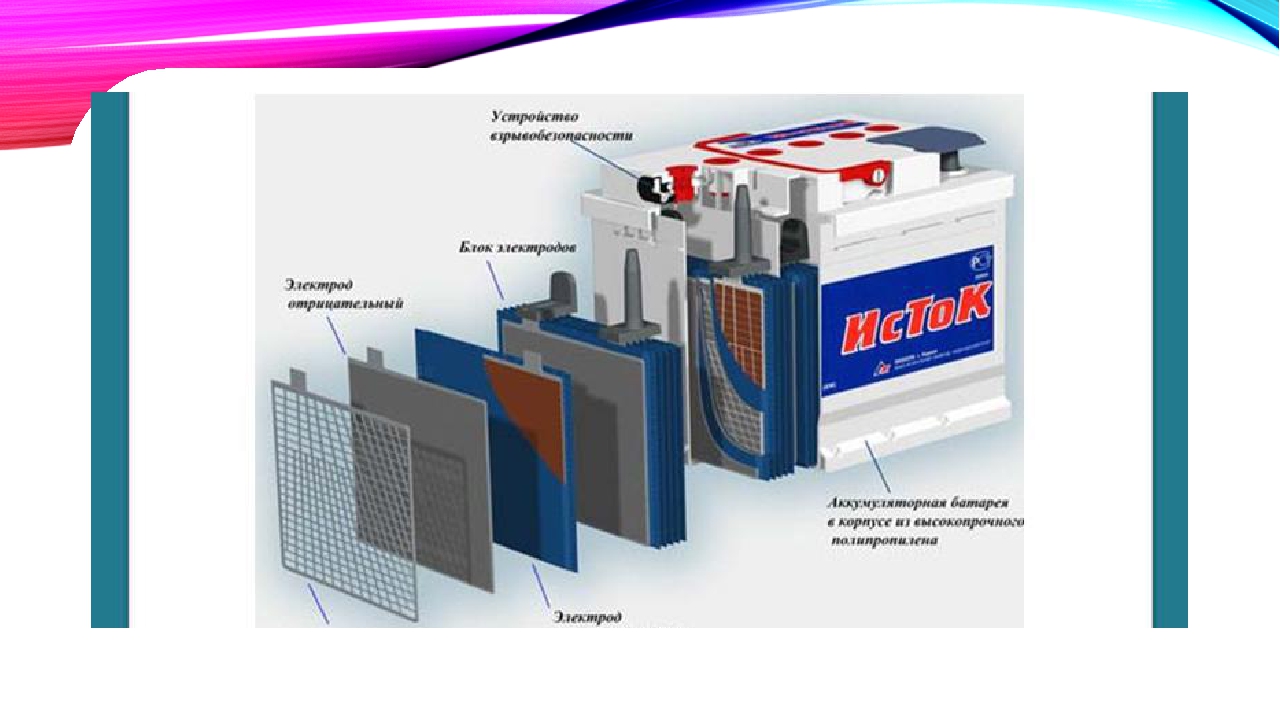
Пластин с отрицательной полярностью больше на 1 единицу, так как каждая пластина с положительным зарядом помещена между двумя отрицательными (минусовыми).
Пакет с пластинами надежно фиксируется, чтобы предотвратить смещение и деформацию. Фиксация осуществляется при помощи специального бандажа. Токовыводы пластин (плюсовые и минусовые) объединены в пары. Концентрация энергии происходит при помощи токосборников – на выводные борны аккумулятора. К ним токоприемные клеммы.
Устройство АКБ обеспечивает максимальную надежность. Современные аккумуляторы – это качественные устройства, выступающие источниками питания даже для самых мощных автомобилей.
Виды современных аккумуляторов
Современные АКБ подразделяются на два основных вида: классические и необслуживаемые. Классические существуют уже больше ста лет и описаны выше. Необслуживаемые аккумуляторные батареи были созданы всего несколько десятилетий назад. Они эффективно работают в любом, даже перевернутом, положении.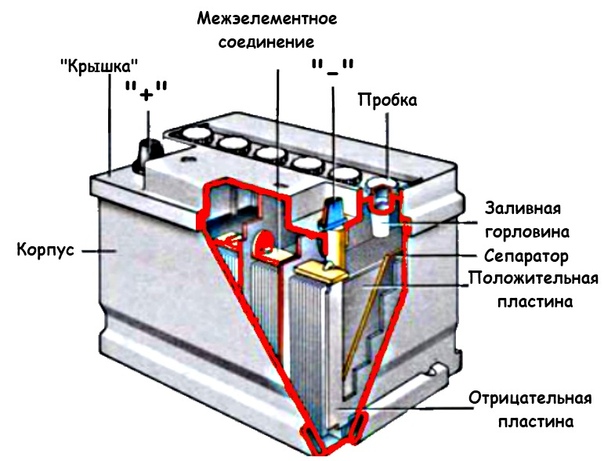 Вместо жидкого электролита в них применяется гелиевый, или адсорбированный сепараторами. Устройство автомобильного аккумулятора, который является необслуживаемым, подразумевает максимальную герметичность. Для отвода газов, которые выделяются при заряде и разряде, предусмотрен специальный клапан.
Вместо жидкого электролита в них применяется гелиевый, или адсорбированный сепараторами. Устройство автомобильного аккумулятора, который является необслуживаемым, подразумевает максимальную герметичность. Для отвода газов, которые выделяются при заряде и разряде, предусмотрен специальный клапан.
Главное различие необслуживаемых АКБ от классических – в более низких разрядных и зарядных токах. Причина – в конструкции необслуживаемых батарей. При больших токах классическая АКБ активно выделяет газ и «закипает». У необслуживаемых и герметизированных батарей этого нет.
2.3. Устройство стартерных аккумуляторных батарей
Стартерные аккумуляторные батареи состоят из отдельных аккумуляторов, соединенных между собой последовательно с помощью перемычек.
Каждый аккумулятор состоит из чередующихся отрицательных и положительных электродов, разделенных сепараторами и собранных в блок.
Блоки электродов каждого аккумулятора помещаются либо в отдельных ячейках моноблока, либо в отдельных баках из эбонита, устанавливаемых в деревянном ящике или в стеклопластиковом корпусе. Каждый аккумулятор закрывается отдельной крышкой, которая при сборке аккумуляторной батареи герметизируется с помощью специальной заливочной битумной мастики.
Для танковых аккумуляторных батарей кроме заливочной мастики для уплотнения крышек применяются резиновые уплотнительные прокладки (рамки).
Различные типы аккумуляторных батарей имеют свои конструктивные особенности, однако в их устройстве много принципиально общего. Устройство танковой аккумуляторной батареи показано на рис. 4, а устройство автомобильной аккумуляторной батареи — на рис. 5.
|
4. Устройство танковой аккумуляторной батареи |
Устройство танковой аккумуляторной батареи
|
|
5. 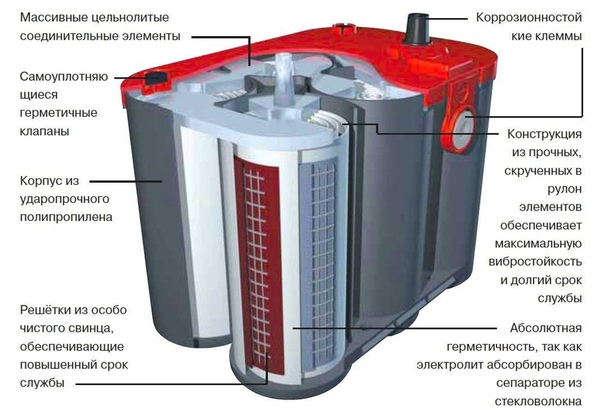 Устройство автомобильной аккумуляторной батареи Устройство автомобильной аккумуляторной батареи
|
Устройство автомобильной аккумуляторной батареи
|
Электрод каждой полярности состоит из токоотвода и активной массы. Токоотводы электродов стартерных аккумуляторов отливают из свинцово-сурьмянистого сплава.
Для токоотводов положительных электродов некоторых типов батарей применяется свинцово-сурьмянистый сплав с небольшой добавкой мышьяка, что увеличивает коррозионную стойкость токоотводов.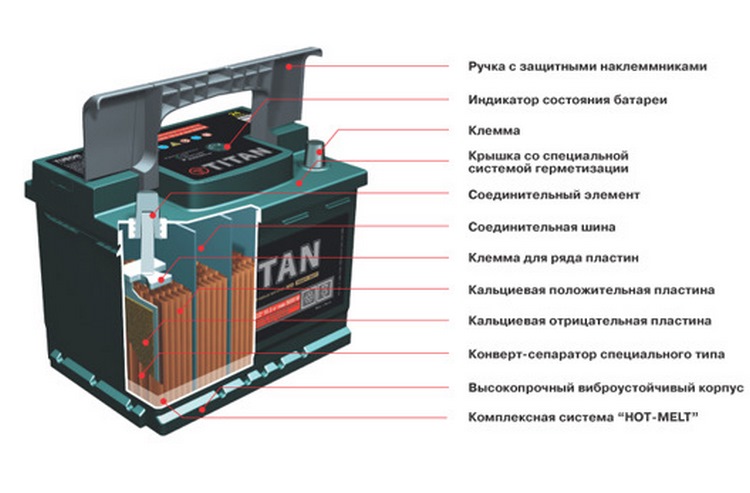 При изготовлении электродов ячейки токоотводов заполняются специальной пастой, которая после электрохимической обработки (формирования) превращается в пористую активную массу.
При изготовлении электродов ячейки токоотводов заполняются специальной пастой, которая после электрохимической обработки (формирования) превращается в пористую активную массу.
Электроды одной полярности о определенным зазором свариваются между собой в полублоки посредством свинцового мостика, к которому приваривается борн (рис. 6).
|
6. Блок электродов аккумуляторной батареи |
|
Полублоки положительных и отрицательных электродов собираются в блок электродов так, что положительные и отрицательные электроды чередуются. В собранном аккумуляторе крайние электроды, как правило, являются отрицательными. Поэтому полублок отрицательных электродов имеет на один электрод больше, чем полублок положительных электродов.
Блок электродов опирается выступами («ножками») электродов на опорные призмы, имеющиеся на дне каждой ячейки моноблока или отдельного эбонитового бака. Таким образом, между нижними кромками электродов и дном имеется свободное пространство, необходимое для накапливания шлама (осадка, образующегося с течением времени из активной массы). Тем самым предотвращаются короткие замыкания разноименных электродов выпадающим шламом.
При сборке блока положительные и отрицательные электроды отделяются друг от друга микропористыми прокладками, которые называются сепараторами.
Сепараторы предохраняют разноименные электроды от коротких замыканий и обеспечивают необходимый запас электролита между электродами.
Сепараторы изготавливаются в виде тонких листов из мипора (микропористого эбонита на основе натурального каучука) или из мипласта (микропористого полихлорвинила) и имеют с одной стороны гладкую, а с другой ребристую поверхность (рис. 7). Ребристая поверхность сепаратора обращена к положительному электроду для лучшего доступа к нему электролита.
7). Ребристая поверхность сепаратора обращена к положительному электроду для лучшего доступа к нему электролита.
|
7. Сепаратор |
Размеры сепараторов несколько больше, чем размеры электродов, что предотвращает замыкания между кромками разноименных электродов. Для повышения срока службы положительных электродов в некоторых типах автомобильных и мотоциклетных батарей применяются комбинированные сепараторы — мипор или мипласт со стекловолокном. При этом сепаратор стекловолокном устанавливается к положительному электроду. Прилегая плотно к его поверхности, он предохраняет активную массу от оплывания.
Для предохранения верхних кромок сепараторов от механических повреждений (при измерении температуры, плотности и уровня электролита) сверху над сепараторами устанавливается перфорированный предохранительный щиток.
Каждый аккумулятор закрывается крышкой (рис.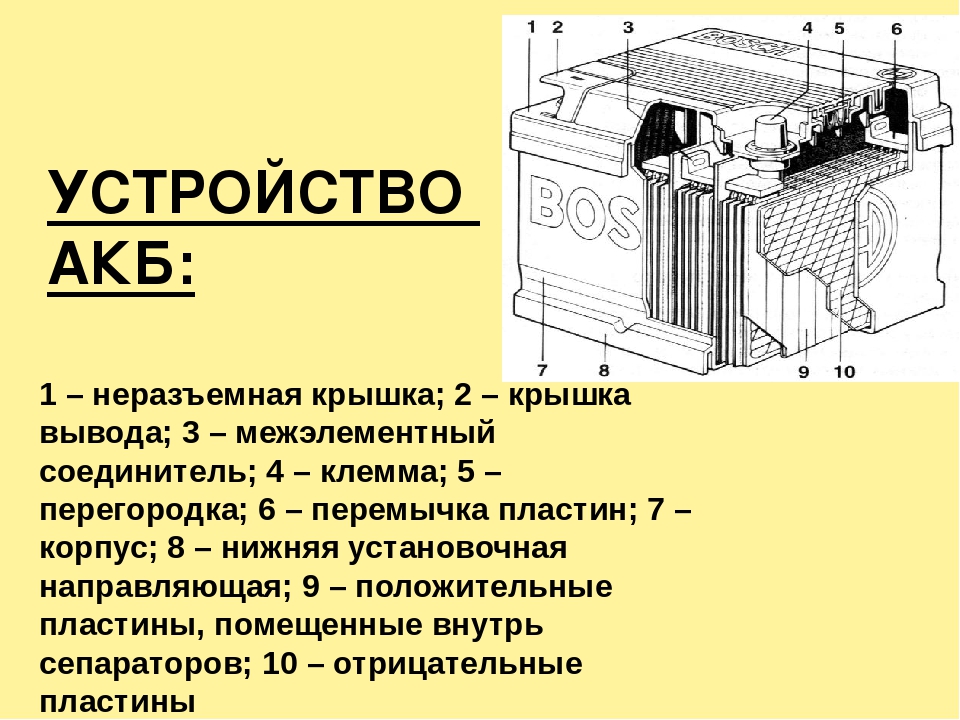 8), изготовленной из эбонита или пластмассы. В двух крайних отверстиях для выводных борнов блоков электродов запрессованы свинцовые втулки, которые затем свариваются с борнами и перемычками, что создает надежное уплотнение. Среднее отверстие для заливки электролита закрывается резиновой пробкой, имеющей вентиляционное отверстие для выхода газа. Однако применяются также крышки (рис. 9) с автоматическим ограничением уровня электролита и отдельными вентиляционными отверстиями. Такие крышки закрываются глухой пробкой (без вентиляционного отверстия).
8), изготовленной из эбонита или пластмассы. В двух крайних отверстиях для выводных борнов блоков электродов запрессованы свинцовые втулки, которые затем свариваются с борнами и перемычками, что создает надежное уплотнение. Среднее отверстие для заливки электролита закрывается резиновой пробкой, имеющей вентиляционное отверстие для выхода газа. Однако применяются также крышки (рис. 9) с автоматическим ограничением уровня электролита и отдельными вентиляционными отверстиями. Такие крышки закрываются глухой пробкой (без вентиляционного отверстия).
|
8. Крышка аккумулятора |
Крышка аккумулятора
|
|
9. 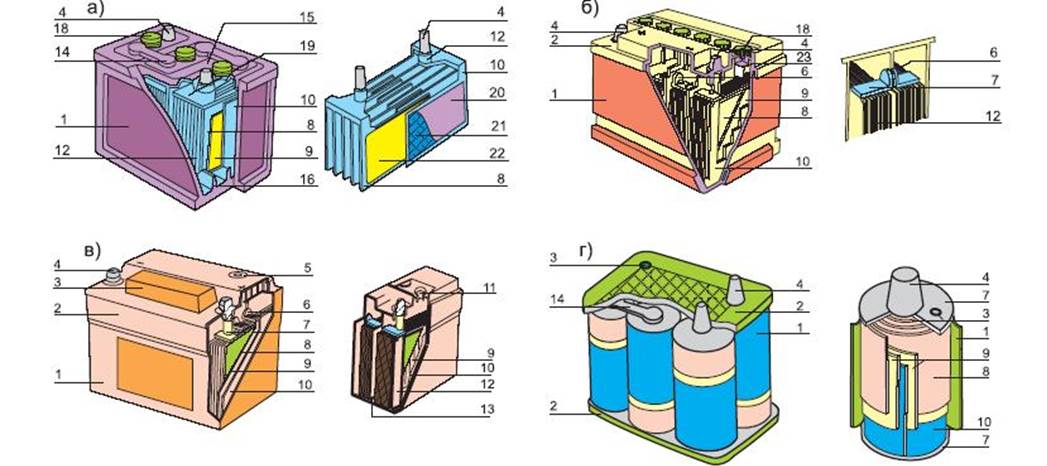 Крышка аккумулятора с автоматическим ограничением уровня электролита Крышка аккумулятора с автоматическим ограничением уровня электролита
|
Крышка аккумулятора с автоматическим ограничением уровня электролита
|
Для автомобильных аккумуляторных батарей, устанавливаемых на машинах, преодолевающих глубокие броды, применяются гидростатические пробки (рис. 10), предотвращающие попадание забортной воды в аккумуляторы.
|
10. Гидростатическая пробка |
Гидростатическая пробка
|
При сборке батарей на заводе под пробки заливных отверстий подкладываются уплотнительные резиновые диски, создающие герметичность, необходимую при хранении батарей в сухом виде. У некоторых типов батарей герметичность обеспечивается за счет применения полиэтиленовых пробок с глухими выступами (рис. 11) на месте вентиляционного отверстия или с помощью заклейки вентиляционного отверстия пленкой.
У некоторых типов батарей герметичность обеспечивается за счет применения полиэтиленовых пробок с глухими выступами (рис. 11) на месте вентиляционного отверстия или с помощью заклейки вентиляционного отверстия пленкой.
При приведении аккумуляторных батарей в рабочее состояние глухие выступы над вентиляционными отверстиями срезаются, уплотнительные резиновые диски и пленки удаляются.
|
11. Полиэтиленовая пробка с глухим выступом |
Полиэтиленовая пробка с глухим выступом
|
Выводные борны отдельных аккумуляторов последовательно соединяются между собой посредством перемычек (рис. 12) способом сварки. Борны, перемычки и выводы танковых, а также автомобильных (ЗСТ-215, 6СТ-182, 6СТ-190) батарей, рассчитанных на большие величины стартерных токов, имеют внутренние медные вкладыши, снижающие падение напряжения на перемычках. К выводным борнам крайних аккумуляторов навариваются полюсные выводы. В зависимости от назначения батарей применяются полюсные выводы в виде конусов или в виде проушин с отверстиями под болт.
К выводным борнам крайних аккумуляторов навариваются полюсные выводы. В зависимости от назначения батарей применяются полюсные выводы в виде конусов или в виде проушин с отверстиями под болт.
|
12. Перемычки |
Полюсные выводы батарей обозначаются знаками «+» (положительный) и «—» (отрицательный), такие же знаки ставятся на стенках моноблока (ящика) у полюсных выводов.
Танковые аккумуляторные батареи 6СТЭН-140М и 6СТ-140Р собираются из шести отдельных аккумуляторов, помещенных в общий деревянный корпус (ящик). Танковые батареи 12СТ-70М, 12СТ-70 и 12СТ-85Р собираются из двенадцати аккумуляторов. Каждые четыре аккумулятора собраны в четырехкамерный бак и три таких бака помещены в деревянный ящик или корпус из стеклопластика. Для повышения прочности деревянный ящик стянут двумя стальными лентами, проходящими между эбонитовыми баками батареи. Батареи 12СТ-85Р собраны в корпусе из стеклопластика (рис. 13). Полюсные выводы батарей в виде проушин с отверстиями под болт выведены на переднюю стенку корпуса и привернуты к нему двумя винтами. Полюсные выводы закрываются защитным кожухом, который крепится болтом к передней стенке корпуса батареи. Деревянные ящики батарей покрываются кислотостойким лаком БТ-783. Батареи закрываются деревянной прессованной крышкой (в батарее 12СТ-85Р крышка из стеклопластика).
13). Полюсные выводы батарей в виде проушин с отверстиями под болт выведены на переднюю стенку корпуса и привернуты к нему двумя винтами. Полюсные выводы закрываются защитным кожухом, который крепится болтом к передней стенке корпуса батареи. Деревянные ящики батарей покрываются кислотостойким лаком БТ-783. Батареи закрываются деревянной прессованной крышкой (в батарее 12СТ-85Р крышка из стеклопластика).
|
13. Танковая аккумуляторная батарея 12СТ-85Р в корпусе из пресс-материала ДСВ-К-1 (стеклопластика) |
Автомобильные аккумуляторные батареи (рис. 14… 25) собираются в моноблоках из эбонита или пластмассы с внутренними перегородками, образующими ячейки для каждого аккумулятора.
Мотоциклетные батареи (рис. 26 и 27) собираются в моноблоках из эбонита, полиэтилена и холодостойкого полипропилена.
|
26. Мотоциклетная аккумуляторная батарея 3МТ-8. 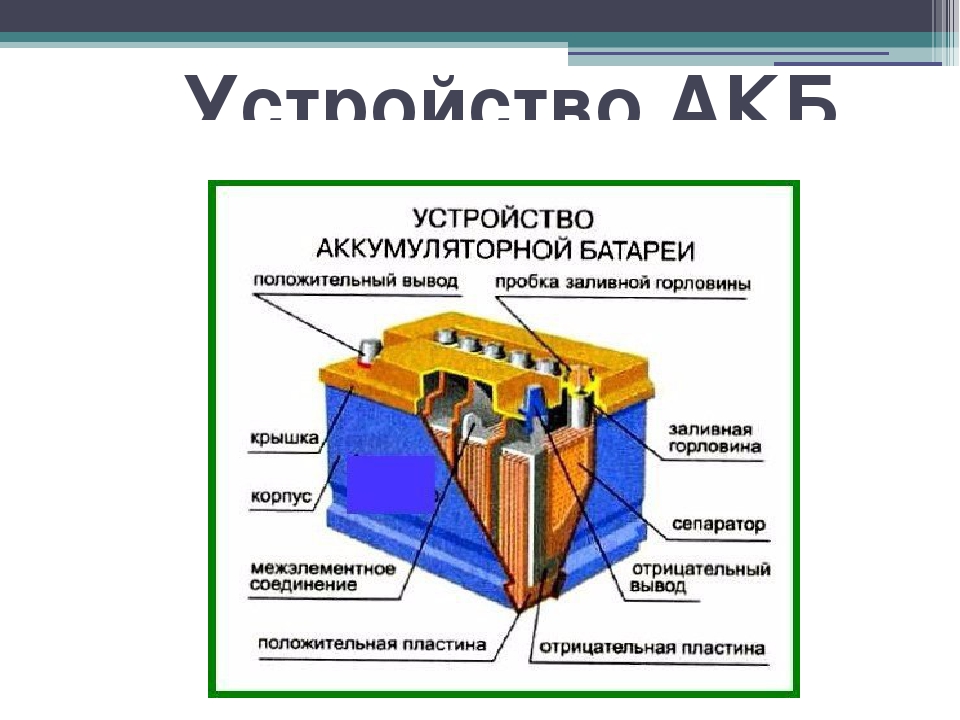 Общий вид Общий вид
|
27. Мотоциклетная аккумуляторная батарея 6МТС-9. Общий вид |
Все аккумуляторные батареи большой емкости, имеющие массу более 30 кг, снабжены ручками для удобства переноски, снятия и установки на машину.
Для обеспечения работоспособности системы электрического пуска дизельных двигателей колесных машин и гусеничных транспортеров-тягачей при низких температурах окружающего воздуха разработана стартерная аккумуляторная батарея 6СТ-190ТРН с внутренним электрообогревом. По габаритным и присоединительным размерам батарея на колесных машинах и гусеничных тягачах взаимозаменяема с серийными батареями 6СТЭН-140М, 6СТЭ-128 и 12СТ-70. Общий вид и устройство аккумуляторной батареи 6СТ-190ТРН показаны на рис. 28 и 29.
|
28. Автомобильная аккумуляторная батарея 6СТ-190ТРН с внутренним электрообогревом. Общий вид |
Батарея собрана на тонких унифицированных электродах с увеличенным количеством активной массы. В сплав, из которого изготовлены токоотводы электродов, введена добавка мышьяка, позволившая увеличить срок их службы.
В сплав, из которого изготовлены токоотводы электродов, введена добавка мышьяка, позволившая увеличить срок их службы.
|
29. Устройство аккумуляторной батареи 6СТ-190ТРН с внутренним электрообогревом |
Устройство аккумуляторной батареи 6СТ-190ТРН с внутренним электрообогревом
|
В активную массу отрицательных электродов введен эффективный расширитель, позволивший повысить отдачу батареи в стартерном режиме разряда при низких температурах. В состав активной массы отрицательного электрода введен также ингибитор окисления свинца, что обеспечивает сохранение сухозаряженности батареи в течение одного года.
Для сокращения потерь энергии уменьшены зазоры между сепараторами и электродами, использованы сепараторы из мипора с высокой пористостью, перемычки и борны армированы медными вкладышами.
Моноблок батареи выполнен из полиэтилена низкого давления с наполнителем.
Каждый аккумулятор батареи 6СТ-190ТРН оборудован отдельным нагревательным элементом типа ЭНА-100 (электрический нагреватель аккумуляторный номинальной мощностью 100 Вт). Нагревательный элемент выполнен из графитированного шнура на основе вискозного кордного волокна в изоляции из фторопласта.
Нагреватели расположены в придонном пространстве под блоком электродов (рис. 30).
|
|
Устройство аккумуляторной батареи 6СТ-190ТРН с внутренним электрообогревом
|
Система обогрева батарей имеет два основных эксплуатационных режима:

Номинальная мощность системы обогрева батареи составляет 600 Вт в режиме форсированного разогрева и 125 Вт в режиме длительного подогрева.
Управление режимами обогрева осуществляется с помощью несложного коммутационного устройства, устанавливаемого вне батареи.
Для предотвращения перегрева батареи внутри нее встроено температурное реле, отключающее нагревательные элементы от источника питания при достижении температуры электролита 15±5 °С.
Питание системы обогрева аккумуляторных батарей предусматривается в движении от собственной генераторной установки машины, а на стоянке — от внешнего источника электроэнергии постоянного или переменного тока с номинальным напряжением 28.0 В.
Особенности эксплуатации системы внутреннего электрообогрева аккумуляторных батарей 6СТ-190ТРН и основные рекомендации по применению режимов электрообогрева в условиях эксплуатации батарей на машинах приведены в других статьях раздела.
Устройство аккумуляторов | Эко Технологии
Устройство стартерных аккумуляторов
О стартерных аккумуляторах
Стартерные аккумуляторные батареи представляют собой вторичный источник электроэнергии. Поэтому купить стартерные аккумуляторы означает получить батареи, способные полностью восстанавливаться после нового электрического заряда. Как правило, заказать стартерные аккумуляторы автолюбители стремятся для использования главной функции данных аппаратов – обеспечение запуска двигателей. Однако подобрать стартерный аккумулятор можно и для реализации его второй функции: это прекрасный аварийный источник питания при выходе из строя генератора.
Современная промышленность позволяет купить стартерные аккумуляторы, которые работают по принципу превращения при заряде электрической энергии в химическую и при разряде обратного превращения – из химической энергии в электрическую. В результате, можно заказать стартерные аккумуляторы, в которых активная масса как отрицательного, так и положительного электродов преобразуется в сульфат свинца.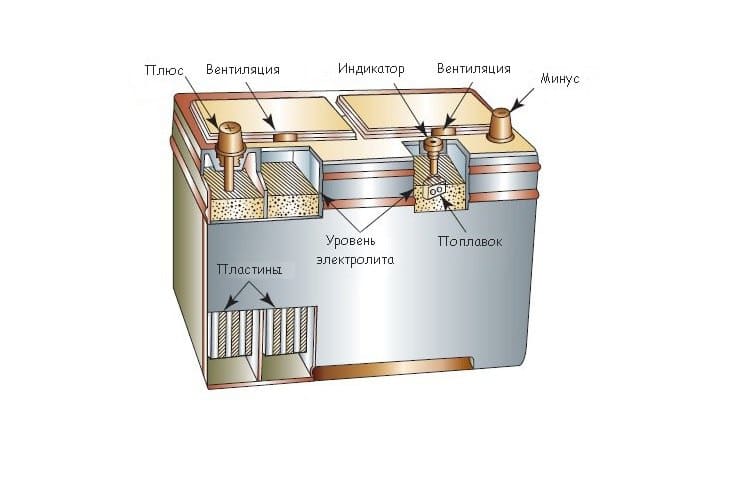 При этом сегодня потребитель имеет возможность подобрать стартерные аккумуляторы емкостью от 36 до 225 А/ч.
При этом сегодня потребитель имеет возможность подобрать стартерные аккумуляторы емкостью от 36 до 225 А/ч.
Конструкция аккумулятора
Аккумулятор — химический источник тока, который преобразует химическую энергию в электрическую и накапливает ее.
Стандартная 12-вольтовая автомобильная аккумуляторная батарея выполнена из шести последовательно соединенных между собой блоков разноименно заряженных пластин, каждый из которых и представляет собой простейший аккумулятор с выходным напряжением около 2 вольт. Положительно заряженная пластина (электрод) представляет собой свинцовую решетку с активной массой из двуокиси свинца (PbO2), а электрод со знаком минус — решетку с активной массой из губчатого свинца (Pb). Полублоки разноименно заряженных пластин вставляются друг в друга. Во избежание возникновения короткого замыкания между пластинами, их разделяют пористыми сепараторами из изоляционного материала. Собранные блоки помещаются в корпус и заливаются электролитом (раствором серной кислоты плотностью 1.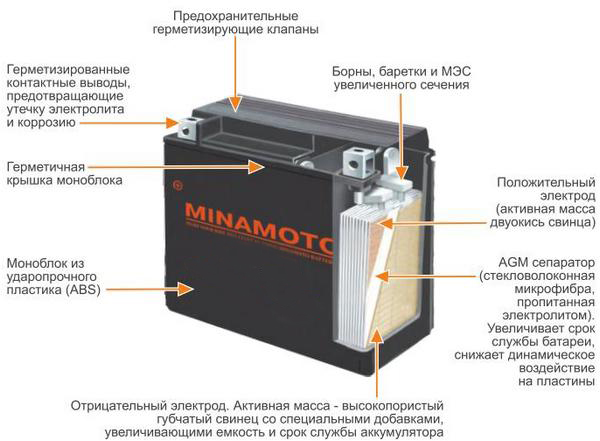 27-1.29 г/см3). Полюса (баретки) крайних элементов соединяются с расположенными снаружи корпуса контактными выводами — борнами.
27-1.29 г/см3). Полюса (баретки) крайних элементов соединяются с расположенными снаружи корпуса контактными выводами — борнами.
Аккумулятор состоит из следующих основных частей:
- Моноблок — это корпус аккумулятора, служащий резервуаром для электролита. Современные аккумуляторы и аккумуляторные батареи имеют полипропиленовые или эбонитовые корпуса. Эбонитовый корпус характерен для аккумуляторов российского производства. Внутри моноблок любой аккумуляторной батареи разделен на ячейки (три или шесть, в зависимости от напряжения батареи- 6 В либо 12 В) для отдельных блоков пластин.
- Крышка — закрывает межэлементные соединения аккумулятора и приваривается к корпусу. В обслуживаемых и малообслуживаемых аккумуляторах в крышке могут располагаться индикатор уровня плотности электролита (косвенно свидетельствующий о степени заряженности того аккумулятора, в банке которого индикатор установлен) и отверстия для контроля уровня и доливки электролита, закрываемые пробками.
 Для того, чтобы избежать повышения давления внутри закрытого корпуса в крышке (или в пробках) выполнены специальные газоотводные каналы. В современных аккумуляторах газоотводные каналы имеют форму лабиринта, позволяющего задержать внутри корпуса капли электролита, уносимые газом, и возвратить их в электролит. Тем самым с одной стороны устраняется выход во внешнюю среду вредных кислотных испарений, а с другой — предотвращается потеря электролита. В аккумуляторах с эбонитовыми корпусами общая крышка отсутствует, ее роль выполняет мастика, которой заливаются межэлементные перемычки.
Для того, чтобы избежать повышения давления внутри закрытого корпуса в крышке (или в пробках) выполнены специальные газоотводные каналы. В современных аккумуляторах газоотводные каналы имеют форму лабиринта, позволяющего задержать внутри корпуса капли электролита, уносимые газом, и возвратить их в электролит. Тем самым с одной стороны устраняется выход во внешнюю среду вредных кислотных испарений, а с другой — предотвращается потеря электролита. В аккумуляторах с эбонитовыми корпусами общая крышка отсутствует, ее роль выполняет мастика, которой заливаются межэлементные перемычки. - Пластины — представляют собой свинцовые решетки с нанесенной на них активной массой. Химическая реакция между активной массой и электролитом аккумулятора происходит на поверхности частиц активной массы, поэтому ее делают пористой, чтобы материал хорошо пропитывался электролитом, и в реакции участвовал его максимальный объем.
- Сепараторы – диэлектрическая прослойка в аккумуляторе, необходимая для предотвращения короткого замыкания между разноименно заряженными пластинами.
 Современные сепараторы изготавливают из микропористой пластмассы (мипласта) в виде конверта.
Современные сепараторы изготавливают из микропористой пластмассы (мипласта) в виде конверта.
Преимущества конверт-сепаратора
- повышает надежность аккумуляторных батарей, так как стекающая активная масса остается внутри конверта;
- небольшие габаритные размеры, так как пластины установлены на дне моноблока.
- Соединительные выводы (борны) – выходящие наружу аккумулятора электрические контакты, сделанные из свинца и имеющие стандартные размеры.
По технологии изготовления аккумуляторы бывают:
- Малосурьмянистые (Pb) аккумуляторы – электролит жидкий.
- Кальцивые – в положительные и отрицательные пластины добавляется кальций, электролит жидкий.
- Кальцево-серебряные (Са/Аg9) – в пластины добавляют серебро и кальций, электролит жидкий.
- AGM (гелевые) – аккумуляторные пластины находятся не в жидком электролите, в загустевшем электролите — геле.
Стандарты производителей
- Европейский стандарт аккумуляторов DIN(EN) — обычные клеммы – А или плоские клеммы – D.
- Азиатский стандарт аккумуляторов JIS — обычные клеммы расположены на крышке – А или тонкие клеммы – В.
- Американский стандарт аккумуляторов ССА — клеммы вкручивающиеся – G.
Основные типы конструкций аккумуляторных батарей
Обслуживаемые аккумуляторы – из-за добавления в пластины таких аккумуляторов сурьмы, происходит разложение электролита при низком напряжении, вода испаряется и возникает необходимость ее доливать. Долив воды в аккумулятор осуществляется в отверстия на крышке, закрытые пробками.
Малообслуживаемые аккумуляторы – в пластины аккумуляторов вместо сурьмы добавляется кальций, что снижает газовыделение в аккумуляторах, а следовательно и скорость выкипания воды.
Необслуживаемые аккумуляторы – конструктивно сделаны так, чтобы срок выкипания воды превышал срок службы самой батареи. В результате, необслуживаемым аккумуляторам не требуется контроль уровня электролита, что делает ее самой легкой в эксплуатации.
В результате, необслуживаемым аккумуляторам не требуется контроль уровня электролита, что делает ее самой легкой в эксплуатации.
Вот 5 лучших аккумуляторов для устройств с высоким энергопотреблением | Оптовые цены
Тип батареи, которую вы выбираете, важнее, чем вы можете себе представить — и мы не говорим о AA, AAA и т. Д. Ваши устройства потребляют энергию с разной скоростью, поэтому вам следует выбрать батарею, которая лучше всего подходит для нее. уникальный расход. Устройства, которые потребляют много энергии за короткие периоды времени, называются «устройствами с высоким энергопотреблением». Например:
- Цифровые фотоаппараты
- Сотовые телефоны
- Портативные видеоигры
- Портативные устройства Bluetooth
- Радиоуправляемые игрушки
Хороший способ определить, потребляет ли устройство много энергии, — это то, как часто вам нужно заряжать его.Если полного заряда хватит на день или два, значит, это устройство с высоким энергопотреблением.
Эти устройства не подходят для работы от тех же батарей, что и устройства с низким уровнем заряда. Вам не захочется заводить вола в Дерби или использовать скаковую лошадь, чтобы вспахивать поля. Вот почему вам обычно следует использовать щелочные батареи для устройств с низким энергопотреблением и литий-ионные батареи для устройств с высоким уровнем потребления.
Следует отметить, что высокий сток и низкий сток представляют две стороны спектра.Большинство устройств находятся где-то посередине. Если ваше устройство находится ближе к середине, есть щелочные батареи с высоким разрядом, которые справятся со своей задачей. Вы должны рассматривать только литиево-ионные батареи, поскольку они почти не потребляют много энергии, потому что они специально разработаны для быстрых и мощных всплесков энергии. Вот почему они идеально подходят для вспышек фотоаппаратов, нескольких часов игры или музыкального вечера.
Вот некоторые из лучших батарей для ваших устройств с высоким энергопотреблением:
Цена: $ 3. 2.38 $ / каждый 95
95
Известные как батареи №1 с длительным сроком службы на рынке, литиевые батареи Energizer Ultimate AAA предназначены для работы в тяжелых условиях, дома и в играх. Отлично подходит для любого устройства AAA.
Цена: 31,95 $ 17,70 $ / шт.
No AA щелочная батарея работает дольше согласно тестам ANSI средней производительности. Это означает более длительное время автономной работы таких мощных устройств, как динамики Bluetooth, игровые контроллеры, цифровые камеры и многое другое.
Цена: 2,95 доллара 1,50 доллара за штуку
Щелочные батареи Duracell Procell 9V идеально подходят для устройств со средней скоростью разряда. Если ваше устройство не является экстремальным по спектру скорости разряда, эта щелочная батарея может быть лучшим вариантом для его питания.
Цена: 3.95 $ 2.38 $ / штука
Литиевая батарея L91 Energizer Ultimate AA была занесена в Книгу рекордов Гиннеса ™ как самая долговечная батарея AA в мире после тщательных испытаний цифровых камер, пультов дистанционного управления и переносных фонарей у конкурентов.
Цена: 3.95 $ 2.39 $ / штука
Energizer Photo обеспечивают надежное питание фонарей, цифровых фотоаппаратов, цифровых видеокамер, устройств умного дома, вспышек, лазеров и многого другого. Идеально для любого семейного или профессионального фотографа.
| 1 | ADBMS6817 | Монитор многоячеечной батареи | 11 | 50 | — | Многофункциональный: диапазон напряжения элементов: от 0 В до 5 В | — | — | — | |||||||||||||||
| 2 | ADBMS1818 | Multicell Battery Monitor | — | 5″> 112.5 | — | Мультихимия: Диапазон напряжения ячеек: от 0 В до 5 В | 100 ячеек | Монитор батареи | 7,43 долл. США (ADBMS1818ASWZ) | |||||||||||||||
| 3 | LT8253A | — | — | — | — | — | — | |||||||||||||||||
| 4 | LT8253 | — | 4 | 40 | — | — | — | — | — | — | — | — | — | 5 | LTC4126-ADJ | Зарядное устройство | 7″> 2.7 | 5,5 | 50 м | Li-Ion | 1 | Линейный | 2,65 долл. США (LTC4126EV-ADJ # TRMPBF) | |
| 6 | LT8491 | Зарядное устройство | 1210 | 9093 9093Свинцово-кислотный, LiFePO4, литий-ионный, литий-полимерный | Плавающее напряжение от 1,3 до 80 В | Переключение | $ 10,35 (LT8491EUKJ # PBF) 75 | — | Мультихимия: диапазон напряжения ячейки: от 0 В до 5 В | — | — | — | ||||||||||||
| 8 | LT8228 | — | 6 | 100 | 40 | Свинец , LiFePO4, Li-Ion, Li-Polymer | — | Переключение | 6″> $ 6.60 (LT8228EFE # PBF) | |||||||||||||||
| 9 | LTC2949 | Датчик уровня заряда батареи, монитор уровня заряда батареи | 4,5 | 14 | — | Li-Ion, Li-Poly | — | — | (LTC2949ILXE # 3ZZPBF) | |||||||||||||||
| 10 | LTC4124 | — | 2,7 | 5,5 | 100 м | Li-Ion | 1 | линейный | 900EV| LTC6812-1 | Монитор многоклеточных батарей | 16 | 75″> 93.75 | — | Мультихимический режим: диапазон напряжения элемента: от 0 В до 5 В | > 1000 В составных литий-ионных элементов | — | — | | ||||||
| 12 | ADP5360 | Зарядное устройство, датчик уровня заряда аккумулятора, Предел тока, программатор напряжения VID | 4,1 | 6,8 | 320 м | Li-Ion, Li-Poly, Li-Polymer | 1, 1 (Li) | Газовый манометр, I2C, линейный | $ 1,71 (ADP5360ACBZ- 1-R7) | |||||||||||||||
| 13 | LTC6810-2 | Монитор многоячеечной батареи | 5 | 5″> 37.5 | — | Мультихимический режим: диапазон напряжения элемента: от 0 В до 5 В | — | — | $ 5,92 (LTC6810IG-2 # 3ZZPBF) | |||||||||||||||
| 14 | LTC6810-1 | Multicell Battery Monitor | 5 | 37,5 | — | Мультихимия: Диапазон напряжения ячейки: от 0 В до 5 В | — | — | 5,92 долл. США (LTC6810IG-1 # 3ZZPBF) | |||||||||||||||
| 15 | LTC6806 | 3 Топливный элемент4.75 | 150 | — | Топливный элемент | — | — | $ 26,00 (LTC6806ILW # 3ZZPBF) | ||||||||||||||||
| 16 | LTC4126-10 | Зарядное устройство для аккумулятора | 7″> 2,7 | Зарядное устройство | 2,7 | 93 Li-Ion | 1 | Linear | 2,65 $ (LTC4126EV-10 # TRMPBF) | |||||||||||||||
| 17 | LTC4126 | Зарядное устройство | 2,7 | 5,5 | 7.5 м | Li-Ion | 1 | Линейный | 2,65 долл. США (LTC4126EV # TRMPBF) | |||||||||||||||
| 18 | LT8708-1 | Резервная батарея, двунаправленная | 2,8 | 80 | 202 LiFePO4, литий-ионный, литий-полимерный | — | Buck-Boost | 6″> $ 6,60 (LT8708EUHG-1 # PBF) | ||||||||||||||||
| 19 | LT8708 | Резервная батарея, двунаправленная 9093 | 10 2,8 | Свинцово-кислотный, LiFePO4, литий-ионный, литий-полимерный | — | Buck-Boost | $ 6.60 (LT8708EUHG # PBF) | |||||||||||||||||
| 20 | LTC6813-1 | Монитор многоячеечной батареи | 16 | 112,5 | — | Мультихимический режим: диапазон напряжения ячеек: от 0 В до 5 В | 100 ячеек | 90 Монитор батареи— | ||||||||||||||||
| 21 | LTC4162-S | Зарядное устройство | 5″> 4,5 | 35 | 3,2 | Свинцово-кислотный | Свинцово-кислотный до 24 В | Переключение | $ 2.55 (LTC4162EUFD-SAD # PBF) | |||||||||||||||
| 22 | LTC4162-L | Зарядное устройство | 4,5 | 35 | 3,2 | Li-Ion, Li-Poly | 1 до 8 | Переключение | 2,55 долл. США (LTC4162EUFD-L40 # PBF) | |||||||||||||||
| 23 | LTC4162-F | Зарядное устройство | 4,5 | 35 | 3,2 | LiFePO4 | —1–9 | Переключение 5 | PBF) | |||||||||||||||
| 24 | AD8452 | Battery Test | -26 | 36 | — | Li-Ion | — | — | 85″> $ 5.85 (AD8452ASTZ) | |||||||||||||||
| 25 | LTC4091 | Зарядное устройство, PowerPath, импульсный регулятор | 6 | 36 | 2 | Li-Ion, Li-Polymer | 1 | Linear | J$ #PBF) | |||||||||||||||
| 26 | LTC2944 | Датчик уровня заряда батареи | 3,6 | 60 | — | Свинцово-кислотный, LiFeO2, литий-ионный, литий-полимерный, NiCd, NiMH | Напряжение аккумулятора до 60 В | Счетчик кулонов | 85″> $ 2.85 (LTC2944CDD # PBF) | |||||||||||||||
| 27 | ADP5350 | Зарядное устройство, PowerPath, импульсный регулятор | 4 | 5,38 | 650 м | Li-Ion | 1 | Switching | B (ADP) 3,45 -R7)||||||||||||||||
| 28 | LTC6811-2 | Multicell Battery Monitor | 11 | 75 | — | Мультихимия: диапазон напряжения элементов: от 0 В до 5 В | — | — | $ 8.19 (LTC6811IG-2 # PBF) | |||||||||||||||
| 29 | LTC6811-1 | Монитор многоячеечной батареи | 11 | 75 | — | Мультихимия: диапазон напряжения ячеек: от 0 В до 5 В | — | — | 19″> 8,19 долл. США (LTC6811IG-1 # PBF) | |||||||||||||||
| 30 | LTC4013 | Зарядное устройство | 4,5 | 60 | 20 | Свинцово-кислотный, LiFePO4, Li-Ion, Li-Polymer (медленный, NiCd заряда), NiMH (медленная зарядка) | Напряжение аккумулятора до 60 В | Переключение | 3 $.95 (LTC4013EUFD # PBF) | |||||||||||||||
| 31 | ADP5092 | Зарядное устройство | 80 м | 3,3 | 150 м | Li-Ion | 1 | Коммутация | 49″>AC R 9001,99 (ADP50 -9292AC 900) | |||||||||||||||
| 32 | ADP5091 | Зарядное устройство для аккумулятора | 80 м | 3,3 | 150 м | Li-Ion | 1 | Коммутация | $ 2,49 (ADP5091ACPZ-1-R7) | |||||||||||||||
| 800 uModule Regulator | 6 | 58 | 6 | Свинцово-кислотный, LiFePO4, Li-Ion, Li-Polymer | Напряжение холостого хода до 36 В | Переключение | $ 16.50 (LTM8064EY # PBF) | |||||||||||||||||
| 34 | LTC2943-1 | Датчик уровня заряда аккумулятора | 6″> 3,6 | 20 | — | Свинцово-кислотный, LiFeO2, литий-ионный, литий-полимерный, NiCd, NiMH | 908 04.01.2018 12:00:00 AMСчетчик кулонов | 2,70 $ (LTC2943CDD-1 # PBF) | ||||||||||||||||
| 35 | LTM8054 | uModule Regulator | 5 | 36 | 5,4 | Свинцово-кислотный , LiFePO4, Li-Ion, Li-Polymer | Напряжение холостого хода до 36 В | Переключение | $ 15.95 (LTM8054EY # PBF) | |||||||||||||||
| 36 | LTC4125 | Беспроводная передача энергии | 3 | 5″> 5,5 | — | LiFePO4, Li-Ion | 1 | Resonant | PBF 4,00 $ | |||||||||||||||
| 37 | LTC3335 | Датчик уровня заряда батареи, импульсный регулятор | 1,8 | 5,5 | 50 м | — | — | — | 3,35 доллара США (LTC3335EUDC # PBF3)06 | Зарядное устройство, PowerPath, импульсный регулятор | 850 м | 5.1 | 300 м | Li-Ion, Li-Poly, NiMH (медленная зарядка) | 1 | Линейный | 94″> 2,94 доллара США (LTC3106EUDC # PBF) | |||||||
| 39 | LTC4040 | Резервная батарея | 34 3,5 900 | 34 3,5 900 5.5 | 2,5 | LiFePO4, Li-Ion, Li-Poly | 1 | Переключение | 2,90 долл. США (LTC4040EUFD # PBF) | |||||||||||||||
| 40 | LTC4015 | Зарядное устройство | 40 4,5 | Свинцово-кислотный, LiFePO4, литий-ионный, литий-полимерный | Напряжение аккумулятора до 35 В | Переключение | $ 5.10 (LTC4015EUHF # PBF) | |||||||||||||||||
| 41 | LT3761 | Драйвер светодиода | 5″> 4,5 | 60 | 20 | Свинцово-кислотный, литий-ионный, литий-полимерный, NiCd (медленная зарядка), NiMH (медленная зарядка ) | Устанавливается внешним зарядным устройством IC | Переключение | 3,20 доллара США (LT3761EMSE # PBF) | |||||||||||||||
| 42 | LTC3305 | Балансировщик аккумуляторных элементов | 12 | 64 | Четыре10 | Свинцово-кислотный 900 Acid | Battery Balancer | 6 долларов США.95 (LTC3305EFE # PBF) | ||||||||||||||||
| 43 | LTC4123 | Зарядное устройство | 2″> 2,2 | 5 | 25 м | NiMH (медленная зарядка) | 1 | Линейный | 123ED $ 2,65 (LTC TRC | Линейный | ||||||||||||||
| 44 | LTC4121-4.2 | Зарядное устройство | 4,4 | 40 | 400 м | Li-Ion, Li-Polymer | 1 | Switching | 2,60 $ (LTC4121EUD-4.2 # PBF) | |||||||||||||||
| 45 | LTC4121 | Зарядное устройство | 4,4 | 40 | 400 м | Свинцово-кислотная, LiFePO4, литий-ионная, литий-полимерная | Напряжение батареи до 18 В | Переключение | 6″> 2,60 долл. США (LTC4121EUD # PBF) | |||||||||||||||
| 46 | LTC4079 | Зарядное устройство | 2,7 | 60 | 250 м | Свинцово-кислотный, LiFePO4, Li-Ion, Li-Polymer6, NiMH93 (90 Напряжение батареи до 60 В | Линейное | $ 2.35 (LTC4079EDD # PBF) | ||||||||||||||||
| 47 | ADP5090 | Зарядное устройство | 80 м | 3,3 | 150 м | Li-Ion | 1 | Переключение | 9001,99 R (ADP 15090-ACP) | |||||||||||||||
| 48 | LT8490 | Зарядное устройство | 6 | 80 | 10 | Свинцово-кислотный, LiFePO4, литий-ионный, литий-полимерный | 3V to 80V Float Voltage»> От 1,3 до 80 В, плавающее напряжение | Переключение | $ 10.35 (LT8490EUKJ # PBF) | |||||||||||||||
| 49 | AD8451 | Зарядное устройство | -31 | 36 | — | Li-Ion | 1 | Линейный | 9009,40 (AD84511200) | LTM8056 | uModule Regulator | 5 | 58 | 5,4 | Свинцово-кислотный, LiFePO4, литий-ионный, литий-полимерный | Напряжение холостого хода до 48 В | Переключение | $ 22. 00 (LTM8056EY # PBF) 00 (LTM8056EY # PBF) | ||||||
Студенты, выпускники «заряжаются» с новым аккумуляторным устройством для телефона | Pittwire
Многие люди оставляют свои телефоны заряжаться на ночь — в конце концов, почему бы не проснуться после напряженного дня с телефоном на 100%?
Но если вы будете делать это по привычке, со временем аккумулятор телефона станет слабее. Эта деградация — это то, что группа новаторов из Университета Питтсбурга надеется решить с помощью своего продукта Canal Battery Guard.
«Каждый сталкивается с этой проблемой: вы получаете новый телефон, и батареи хватает на целый день, но через год или два они не работают так долго», — сказал Николас Кшатри, пятый курс биоинженерии в школе Pitt’s Swanson School. инженеров и соучредитель Canal.
Защита аккумулятора действует как посредник между телефоном и зарядным устройством. Меньше, чем полдолларовая монета, защитный кожух подключается к порту зарядки телефона с одной стороны и имеет собственный порт с другой стороны для кабеля зарядки. Затем пользователи связывают устройство с приложением Canal, чтобы обнаружить изменения.
Затем пользователи связывают устройство с приложением Canal, чтобы обнаружить изменения.
Отсюда охранник обнаруживает изменения температуры и использует алгоритм зарядки, который дает батарее телефона периоды отдыха, чтобы минимизировать перегрев, основной фактор деградации батареи.
«Несколько компаний придумали устройства, которые работают аналогично, но все, что они делают, это чувствуют, когда телефоны заряжаются, а затем отключают заряд», — сказал Кшатри. «Наше устройство обеспечивает периоды отдыха».
Кшатри вместе с недавними выпускниками инженерных специальностей Мохамедом Морси (ENGR ’20) и Мэтью Розенблаттом (ENGR ’20) работали над защитой батареи в течение последних трех с половиной лет, начиная с того времени, когда они были студентами первого курса. Идея пришла от Морси, представившего ее в курсе, преподаваемом в Swanson School, «Искусство создания: введение в практическое проектирование и проектирование систем».”
«В то время я мало что знал о проблеме, которую нам предстоит решить, но я подумал, что есть способ продлить срок службы батареи смартфона, изменив способ ее зарядки», — сказал Морси. «Я особо не думал об этом, пока не пошел в класс, где у меня была возможность представить свою недоработанную идею и сформировать вокруг нее команду».
«Я особо не думал об этом, пока не пошел в класс, где у меня была возможность представить свою недоработанную идею и сформировать вокруг нее команду».
Курс вел Джозеф Самоски, доцент кафедры биоинженерии. Для студентов-первокурсников, таких как команда Canal, этот класс предлагается как курс с отличием по инновациям, дизайнерскому мышлению и ориентированному на пользователя дизайну.Студентам предлагается изучить неудовлетворенные потребности и разработать темы проектов по своему выбору, а затем применить экспериментальный процесс проектного мышления для создания и прототипирования инновационных решений.
«Мы хотим, чтобы наши ученики имели возможность видеть проблемы с точки зрения своих пользователей, а затем разрабатывать решения, которые были бы творческими и эффективными в удовлетворении потребностей людей», — сказал Самоски, который продолжает преподавать в классе. «Я восхищаюсь агентурностью и преданностью команды Canal и с нетерпением жду результатов их постоянных испытаний и исследований. Мы невероятно гордимся способностью нашей команды, особенно в этом году, успешно построить стартап для разработки этого продукта ».
Мы невероятно гордимся способностью нашей команды, особенно в этом году, успешно построить стартап для разработки этого продукта ».
Завершив курс и решив больше работать вместе, команда провела дополнительные исследования причин деградации батарей и работала с Инновационным институтом Питта над коммерческими разработками. Охранник батареи участвовал в соревнованиях, таких как Конкурс больших идей семьи Рэндалл, где в 2020 году получил третье место. Команда также вошла в охрану доменной печи Питта.
По словам Кшатри, пандемия COVID-19 оказала «минимальное влияние» на развитие охраны.
«Возможно, вначале мы могли бы работать вместе в одном месте, но столь же продуктивно мы работали удаленно», — сказал он.
Команда ищет дополнительное финансирование, поскольку Canal продвигается к выводу на рынок защиты аккумулятора, а также к дальнейшим испытаниям.
Человек, который принес нам литий-ионную батарею в возрасте 57 лет, придумал новую батарею в возрасте 92 лет — Quartz
ОСТИН, ТЕХАС. Скорее всего, вы никогда не слышали о ней, пока не заглянули на эту страницу когда-либо видел — Джон Баннистер Гуденаф.Но вы знаете его работу. На самом деле, они у вас почти наверняка есть.
Скорее всего, вы никогда не слышали о ней, пока не заглянули на эту страницу когда-либо видел — Джон Баннистер Гуденаф.Но вы знаете его работу. На самом деле, они у вас почти наверняка есть.
Рассмотрим последние шесть или семь десятилетий технологических и научных достижений: вакцина от полиомиелита, космическая ракетная техника, Arpanet (предшественник Интернета). На этом фоне выделяются два изобретения с точки зрения социальных и экономических последствий, не говоря уже о чистой повсеместности, изобретения, без которых жизнь большинства населения мира — пересечение границ возраста и этнической принадлежности, религии, моральной основы, состояния здоровья, политического принадлежность, вкус, стиль, национальная принадлежность — были бы совсем другие.
Адаптированный отрывок из новой книги Стива Левина «Электростанция» («Викинг»). Первым из этих крупногабаритных изобретений является транзистор, созданный в 1947 году в Bell Labs, преобразовавший электронику, являющуюся основой мировой экономики и современной цивилизации. Второй — литий-ионный аккумулятор. Литий-ионный аккумулятор, коммерциализированный Sony в 1991 году, взял на себя неуклюжую электронику, обеспечиваемую транзистором, и сделал ее портативной.
Второй — литий-ионный аккумулятор. Литий-ионный аккумулятор, коммерциализированный Sony в 1991 году, взял на себя неуклюжую электронику, обеспечиваемую транзистором, и сделал ее портативной.
В отличие от транзистора, литий-ионный аккумулятор не получил Нобелевской премии.Но многие думают, что так и должно быть. Литий-ионный аккумулятор обеспечил транзистору доступность. Без него у нас не было бы смартфонов, планшетов или ноутбуков, в том числе устройства, которое вы читаете прямо сейчас. Не было бы Apple. Нет Самсунга. Нет Теслы.
В 1980 году Гуденаф, физик, которому тогда было 57 лет, изобрел литий-ионную нервную систему. Его детищем стал катод из оксида кобальта, самый важный компонент каждой литий-ионной батареи. От Могадишо до Паго-Паго, от Антарктиды до Гренландии и всех других земель между ними, катод Гуденафа содержится почти в каждом портативном электронном устройстве, когда-либо проданном.Другие пытались улучшить катод из оксида кобальта, но все безуспешно.
«Я хочу решить проблему, прежде чем бросить свои фишки. Мне всего 92 года. У меня еще есть время, чтобы пойти». — Джон Гуденаф
Мне всего 92 года. У меня еще есть время, чтобы пойти». — Джон Гуденаф
Сегодня, в 92 года, Гуденаф все еще ходит в свой небольшой офис каждый день по адресу: Техасский университет в Остине. По его словам, это потому, что он еще не закончил. Спустя тридцать пять лет после его блокбастера электромобиль все еще не может конкурировать с двигателем внутреннего сгорания по цене. Когда солнечная и ветровая энергия производят электричество, ее нужно либо использовать немедленно, либо потерять навсегда — экономичной стационарной батареи для хранения энергии не существует.Тем временем сгущаются грозовые тучи: нефть снова дешева, но, как и все товары с цикличным ростом, ее цена снова вырастет. Климат становится теплее и в целом становится более неспокойным.
Короче, миру нужна супер-батарея. Что, «или мне жаль, что мы собираемся вести войны, сражаясь за последние резервы того, того или другого, и у нас будет глобальное потепление сверх того, что мы можем вынести», — говорит Гудинаф.
Хорошая новость в том, что у Гуденафа есть последняя идея.Он работает над этим с еще одной группой постдокторантов. «Я хочу решить проблему, прежде чем бросить свои фишки», — говорит он. «Мне всего 92 года. У меня еще есть время пойти».
Сказав это, Гуденаф ухмыляется, возможно, это самый странный смех среди ученых на планете. Послушайте это здесь.
Аккумуляторная революция 1960-х годов
Аккумулятор — это в основном устройство, заставляющее электрически заряженные атомы, известные как ионы, перемещаться из одной точки в другую. Когда электрические заряды движутся, они создают электрический ток.Этот ток питает все, что подключено к батарее.
Следовательно, чтобы сделать батарею, вам понадобятся два электрода, между которыми ионы будут путешествовать. В середине вам понадобится вещество, через которое они смогут пройти, называемое электролитом. Один электрод заряжен отрицательно и называется анодом. Другой, положительно заряженный, — катод. Когда батарея разряжается, то есть когда она подключена к устройству, которое получает от нее энергию, положительно заряженные ионы перемещаются от анода к катоду, создавая ток. Если это перезаряжаемая батарея, подключение устройства к розетке — таким образом, возвращая в нее электричество — заставляет ионы возвращаться к аноду, где они хранятся до тех пор, пока не понадобятся снова.
Если это перезаряжаемая батарея, подключение устройства к розетке — таким образом, возвращая в нее электричество — заставляет ионы возвращаться к аноду, где они хранятся до тех пор, пока не понадобятся снова.
Практически все в конструкции батарей сводится к материалам, из которых сделаны анод, катод и электролит. Они определяют, сколько ионов может хранить аккумулятор и как быстро он может их откачать.
В начале двадцатого века электромобили, работающие от свинцово-кислотных аккумуляторов (свинец для электродов, серная кислота для электролита), казались превосходящими конкурентов с бензиновыми двигателями внутреннего сгорания.Свинцовая кислота не была новым изобретением — ее создал в 1859 году Гастон Планте. Но электрика была тихой и легкой в маневрировании по сравнению с шумными и грязными двигателями внутреннего сгорания с их раздражающими ручными кривошипами. Затем ряд изобретений, в том числе электрический стартер, дал преимущество горению. В течение десятилетий мало кто думал, что все должно быть по-другому.
Но в 1966 году Ford Motor, который с моделью T и сборочной линией сделал больше, чем любая другая компания, чтобы сделать процесс сжигания топлива массовым, попытался вернуть электромобиль.Заявлена батарея с серным катодом и натриевым анодом. Это был новый образ мышления — легкая батарея, которая могла хранить в том же пространстве в 15 раз больше энергии, чем свинцово-кислотная.
Были, конечно, минусы. Аккумулятор Ford работал при температуре около 300 ° C (570 ° F) по сравнению с примерно 90 ° C двигателя внутреннего сгорания. Натрий плавится при 98 ° C и может воспламениться при встрече с воздухом. Вы же не хотите ездить с горячим, взрывоопасным, расплавленным металлом под капотом. Реально аккумулятор годился только для стационарного хранения, для электростанций.
Однако поначалу и Форд, и общественность пренебрегли осторожностью. Обещав выпускать экологически чистые электромобили, Ford захватил воображение населения 1960-х годов, которое внезапно осознало, что его города окутывает смог.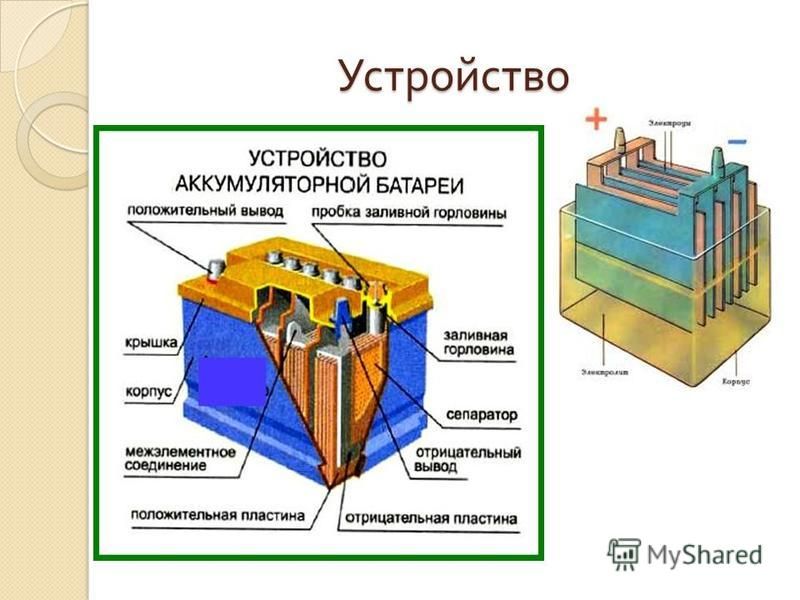 На начальных этапах электрические Ford, использующие свинцово-кислотные аккумуляторы, могли проехать 40 миль (64 км) с максимальной скоростью 40 миль в час. Форд утверждал, что с началом использования новых серно-натриевых батарей автомобили будут преодолевать 200 миль со скоростью шоссе. Вы могли бы зарядиться в течение часа, а затем проехать еще 200 миль.
На начальных этапах электрические Ford, использующие свинцово-кислотные аккумуляторы, могли проехать 40 миль (64 км) с максимальной скоростью 40 миль в час. Форд утверждал, что с началом использования новых серно-натриевых батарей автомобили будут преодолевать 200 миль со скоростью шоссе. Вы могли бы зарядиться в течение часа, а затем проехать еще 200 миль.
Такие разговоры вызвали ажиотаж, снова напоминающий коммерчески изобретательный XIX век. Во всем мире исследователи стремились подражать Ford и, если могли, лучше его. Гуденаф, в то время ученый из Массачусетского технологического института, сказал, что все внезапно изменилось. Батарейки уже не надоели. Безумие продолжалось и в следующее десятилетие, набирая обороты, сказал Гуденаф, благодаря сочетанию арабского нефтяного эмбарго 1973 года, всеобщего убеждения в том, что в мире заканчивается нефть, и стимулирования научных достижений по обе стороны Атлантики.
Как бы то ни было, электрика вроде вернулась. Теперь Гуденаф бросился в бой. За двадцатилетний период он либо сам произведет, либо примет участие в изобретении почти всех крупных достижений современных батарей.
За двадцатилетний период он либо сам произведет, либо примет участие в изобретении почти всех крупных достижений современных батарей.
Трудное воспитание Гуденаф
Джон Гуденаф вырос в большом доме недалеко от Нью-Хейвена, штат Коннектикут, где его отец Эрвин изучал историю религии в Йельском университете. Отношения его родителей «были катастрофой», — сказал он, — трения, переросшие в отчужденность по отношению к их детям.Гуденаф и его мать, Хелен, особенно «никогда не были связаны» — она не хотела Джона, который должен был стать ее вторым ребенком, но ее муж настоял на своем, и она навсегда отдалилась от него.
Когда Джону было 12, его отправили на стипендию в Гротон, частную школу-интернат в Массачусетсе, и он редко слышал об этом от родителей. Мать Джона написала всего один раз, когда он стал взрослым. В тонкой автобиографии, опубликованной самостоятельно, Гуденаф цитирует множество влияний: братьев и сестер, собаку по имени Мак, семейную горничную, давних соседей. Но он явно игнорирует своих родителей и никогда не называет их по имени. Их место в его жизни было исключительно биологическим.
Но он явно игнорирует своих родителей и никогда не называет их по имени. Их место в его жизни было исключительно биологическим.
Отрочество Гуденафа не предполагало прихода теплого, забавного и самоуверенного взрослого. Страдая от дислексии в то время, когда ее плохо понимали и не лечили, Гуденаф не мог читать в Гротоне, понимать его уроки или сидеть в часовне. Вместо этого он занялся исследованием леса, его животных и растений. Тем не менее, как-то все наконец сошлось.Он выиграл место и пакет помощи в Йельском университете и продолжил выпуск с отличием по математике.
«Разве вы не знаете, что кто-либо, кто когда-либо делал что-нибудь значимое в физике, уже сделал это к тому времени, когда он был в вашем возрасте?»
После Второй мировой войны Гуденаф, к тому времени 24-летний армейский капитан, находившийся на архипелаге Азорских островов у побережья Португалии, получил телекс с приказом отправиться в Вашингтон, округ Колумбия. Педагоги наткнулись на неизрасходованные бюджетные деньги и выступили за их использование для отправки 21 вернувшегося армейского офицера на учебу в аспирантуре по физике и математике. Гуденаф почти не принимал науку в качестве старшекурсника, но по причинам, скрытым временем, профессор математики Йельского университета добавил свое имя в группу.
Гуденаф почти не принимал науку в качестве старшекурсника, но по причинам, скрытым временем, профессор математики Йельского университета добавил свое имя в группу.
Так он оказался в Чикагском университете, обучаясь у некоторых ведущих физиков того времени, включая Эдварда Теллера и Энрико Ферми. Когда Гуденаф записался на предварительные курсы бакалавриата, необходимые для того, чтобы догнать остальных, профессор заметил: «Я не понимаю вас, ветераны. Разве вы не знаете, что кто-либо, кто когда-либо делал что-нибудь значимое в физике, уже сделал это к тому времени, когда он был в вашем возрасте? »
Но оказалось, что Гуденаф имел интуицию в физике.После получения докторской степени в 1952 году он пошел работать в лабораторию Линкольна Массачусетского технологического института, которую ВВС США профинансировали годом ранее для создания первой системы ПВО страны, известной как SAGE. Он присоединился к команде, которая работала над системой компьютерной памяти.
В то время компьютеры содержали достаточно электронных ламп, чтобы заполнить «пространство большого танцевального зала», по словам Гуденафа, и обладали адски медленной памятью. Вскоре после того, как Гуденаф присоединился к Массачусетскому технологическому институту, команда представила память на магнитных сердечниках — гораздо более быструю, надежную и компактную форму хранения.Помимо поддержки SAGE, он стал основой систем компьютерной памяти, пока полупроводники не вытеснили его в 1970-х годах. По мнению Гуденафа, последовали и другие достижения, в том числе «правила Гуденаф-Канамори», которые описывают, как магнетизм работает в различных материалах в атомном масштабе — еще один строительный блок компьютеров будущего.
Предоставлено Джоном Гуденаф
Джон Гуденаф (в первом ряду, второй слева) со своими коллегами в Оксфорде в 1982 году, через два года после создания катода из оксида кобальта. К середине 1970-х Гуденаф был зациклен на поиске научного ответа на энергетический кризис под руководством ОПЕК, который казался самой большой проблемой, с которой столкнулась страна. Но вмешалась политика: сенатор США Майк Мэнсфилд протолкнул закон, требующий, чтобы любые исследования, финансируемые ВВС США, которые финансировали лабораторию Массачусетского технологического института, были заявлены в ВВС..files/image009.png) По этому закону за энергию отвечали не ВВС, а национальные лаборатории.
По этому закону за энергию отвечали не ВВС, а национальные лаборатории.
Друг сообщил о возможности через Атлантику.Оксфордскому университету требовался профессор для преподавания и управления лабораторией неорганической химии. В 1976 году Гуденаф был удивлен, когда его выбрали; он не был химиком и закончил всего два курса химии в колледже. Ему повезло, что во второй раз его выбрали на должность, на которую он был недостаточно квалифицирован на бумаге.
Гуденаф был крутым профессором. Клэр Грей, его студентка в Оксфорде, вспомнила курс физики, который начался со 165 студентов. После строгой лекции Гуденафа она была одной из восьми, кто вернулся на второй урок.Он был столь же требователен в лаборатории. Но это произошло потому, что после Массачусетского технологического института он стремился к большим достижениям в химии твердого тела, области, известной созданием материалов, которые становятся коммерческими.
Первая литиевая батарея
Примерно в то время, когда Гуденаф отправился в Оксфорд, британский химик Стэн Уиттингем объявил о большом прорыве в области батарей. Вместе с коллегами из Стэнфордского университета он открыл способ сделать электрод из слоистого материала — такого, который мог бы хранить ионы лития внутри листов сульфида титана.Ионы лития могли перемещаться от одного электрода к другому, создавая перезаряжаемую батарею. И он работал бы при комнатной температуре. Заимствуя термин из химии, Виттингем назвал этот вид хранилища интеркаляцией , и он застрял .
Вместе с коллегами из Стэнфордского университета он открыл способ сделать электрод из слоистого материала — такого, который мог бы хранить ионы лития внутри листов сульфида титана.Ионы лития могли перемещаться от одного электрода к другому, создавая перезаряжаемую батарею. И он работал бы при комнатной температуре. Заимствуя термин из химии, Виттингем назвал этот вид хранилища интеркаляцией , и он застрял .
Новость привлекла широкое внимание. Нефтяной гигант Exxon в то время стремился бросить вызов Bell Labs (где был изобретен транзистор) как центру изобретений. Это привело к Уиттингему, который начал делать батарею, полагаясь на результаты исследований в Стэнфорде.Его работа шла в большой секретности. Наконец, в 1976 году компания Exxon подала заявку на патент на батарею на основе лития.
В течение шести десятилетий неперезаряжаемые цинк-углеродные батареи были стандартным химическим составом для бытовой электроники. (Он затмил свинцово-кислотный, который годился для автомобильных аккумуляторов, но был слишком громоздким и тяжелым для небольших устройств.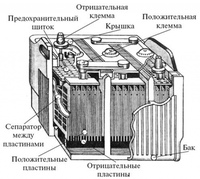 ) Также использовался никель-кадмиевый. Детище Уиттингема было на шаг впереди обоих. Мощный и легкий, он может питать гораздо меньшую портативную бытовую электронику (вспомните iPod, а не Walkman) — если бы он работал.
) Также использовался никель-кадмиевый. Детище Уиттингема было на шаг впереди обоих. Мощный и легкий, он может питать гораздо меньшую портативную бытовую электронику (вспомните iPod, а не Walkman) — если бы он работал.
Но фундаментальная физика помешала. Те же электрохимические реакции, которые позволили литиевым батареям, также заставили их взорваться. При перезарядке элемент может загореться, и прежде чем вы заметите это, батарея извергнет пламя. Но, похоже, вам не станет лучше, если вы будете осторожны и будете использовать другие элементы; вы обнаружите, что они медленно разваливаются при повторной зарядке и разрядке. Эти досадные проблемы — взрывающиеся лаборатории и разваливающиеся батареи — мешали работе Уиттингема.
Гуденаф думал, что сможет создать более мощную батарею, чем батарея Уиттингема, без неприемлемых недостатков.В мужской батарее Exxon катодным материалом, в котором хранился литий, был сульфид титана. Но в дни работы в Массачусетском технологическом институте Гудинаф познакомился с другим семейством соединений — оксидами металлов, комбинацией кислорода и различных металлических элементов. По его мнению, оксиды могут обеспечивать заряд и разряд при более высоком напряжении, чем создание Уиттингема, что, согласно законам физики, приведет к увеличению энергии. И он был бы гораздо менее изменчивым. Вот что он попробует.
По его мнению, оксиды могут обеспечивать заряд и разряд при более высоком напряжении, чем создание Уиттингема, что, согласно законам физики, приведет к увеличению энергии. И он был бы гораздо менее изменчивым. Вот что он попробует.
Также была возможная ловушка.Чем больше лития может храниться в электродах и затем перемещаться между ними, тем больше энергии будет производить батарея — но если литий составлял большую часть материала катода, и весь он уходил на путь к аноду, тогда Гуденаф рассуждал, что катод будет выдолблен и сам упадет. Так может ли какой-либо из оксидов металлов выдержать такое злоупотребление? И если да, то какой из них и в какой магической пропорции лития можно было извлечь?
Гуденаф направил двух ассистентов докторантуры методично прокладывать себе путь через структуры, содержащие группу оксидов.Он попросил их выяснить, при каком напряжении литий можно извлечь из оксидов — он ожидал, что оно будет намного выше, чем 2,2 вольта, которые использовал Уиттингем, — и сколько лития можно извлечь из атомной структуры.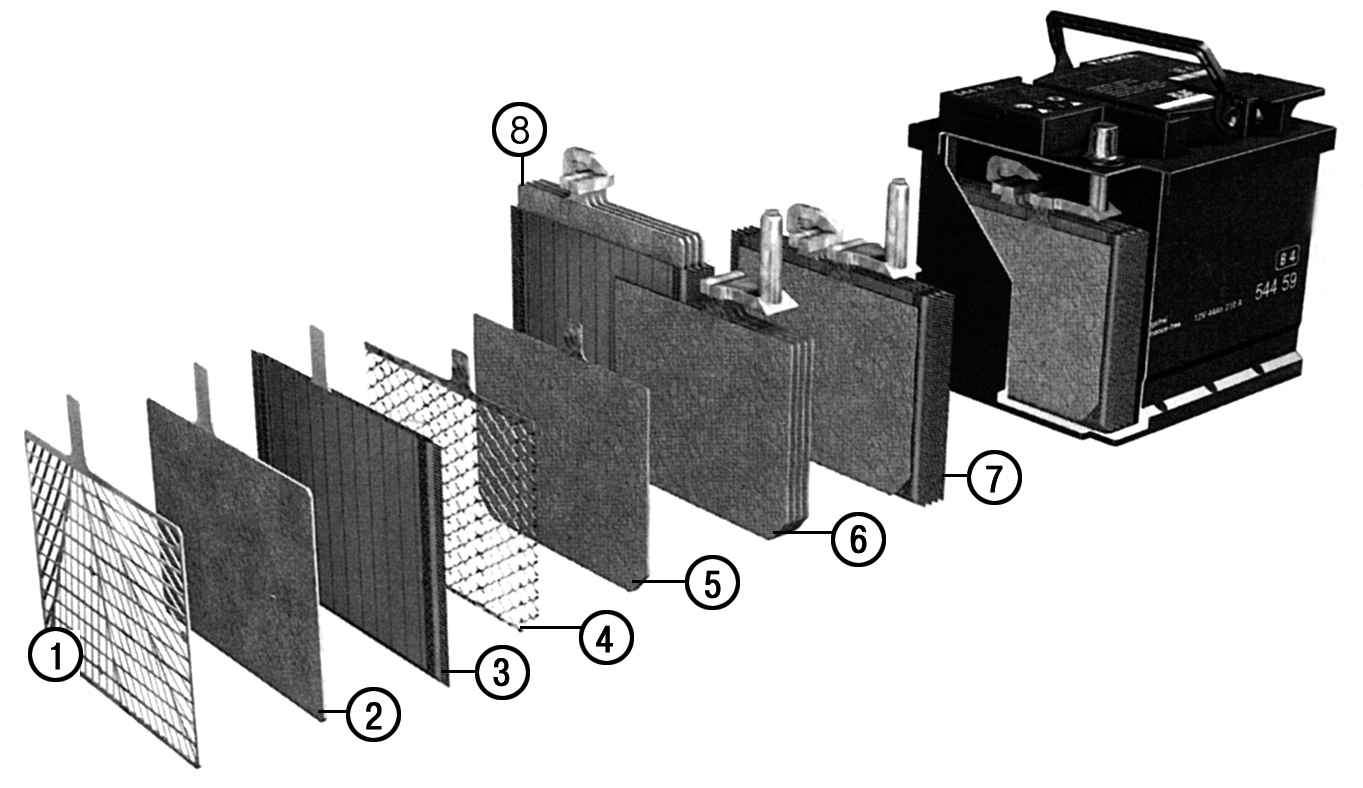
Их ответ заключался в том, что примерно половину лития можно было снять с катода при 4 вольтах, прежде чем он смялся. Этого было достаточно для мощной перезаряжаемой батареи. Из протестированных оксидов постдоки обнаружили, что кобальт является лучшим и наиболее стабильным для этой цели.
Построенный в 1980 году, через четыре года после того, как Гуденаф прибыл в Оксфорд, катод из оксида лития-кобальта стал прорывом даже в большей степени, чем натрий-серная конфигурация Форда. Это был первый литий-ионный катод, способный при установке в батарею питать как компактные, так и относительно большие устройства, качество, которое сделало бы его намного превосходящим все, что есть на рынке. В результате получилась бы батарея, в два-три раза превышающая энергию любой другой перезаряжаемой батареи, работающей при комнатной температуре, и, таким образом, ее можно было бы сделать намного меньше и обеспечить такую же или лучшую производительность.
В 1991 году Sony объединила катод Гуденаф и угольный анод в первую в мире коммерческую перезаряжаемую литий-ионную батарею. В результате получился мгновенный блокбастер. Помимо продажи батарей, Sony решила проблему с помощью одного из своих ведущих электронных продуктов — портативных видеокамер. Доступные ранее батареи были слишком громоздкими для портативного использования видео, но литий-ионные позволили Sony предложить новую, изящную версию камер, и они тоже стали очень продаваемыми.
В результате получился мгновенный блокбастер. Помимо продажи батарей, Sony решила проблему с помощью одного из своих ведущих электронных продуктов — портативных видеокамер. Доступные ранее батареи были слишком громоздкими для портативного использования видео, но литий-ионные позволили Sony предложить новую, изящную версию камер, и они тоже стали очень продаваемыми.
«Аккумулятор — это… уловка, сенсация, механизм обмана населения акционерными обществами.- Томас Эдисон
Rivals быстро выпустили аккумуляторы-подражатели и портативные камеры, а затем установили литий-ионные аккумуляторы в ноутбуки и сотовые телефоны, создав несколько многомиллиардных отраслей малой электроники. Цинк-углерод и никель-кадмий просто не могли соответствовать энергии литий-иона по отношению к массе, и первые не могли перезаряжаться. Прорыв Sony вызвал ажиотаж в лабораториях по всему миру, пытаясь найти еще более совершенные литий-ионные конфигурации, которые позволили бы собрать больше энергии в все меньшем и меньшем пространстве.
Тем не менее, несмотря на его центральную роль в создании первой коммерческой литий-ионной батареи, Гуденаф не получил гонорара. Оксфорд отказался запатентовать катод Гуденаф — университет, похоже, не видел никаких преимуществ в владении интеллектуальной собственностью. В конце концов, Гуденаф передал лицензионные права Исследовательскому учреждению по атомной энергии, британской правительственной лаборатории к югу от Оксфорда, рассудив, что, по крайней мере, его изобретение может выйти на рынок. Он никогда не понимал масштабов будущего рынка. Никто этого не сделал.
Но изобретение Гуденаф привело не только к эпохе современных мобильных телефонов и ноутбуков. Поскольку литий-ионный аккумулятор был относительно легким по сравнению с тем количеством заряда, которое он удерживал, он также открыл возможность создания экономичных электромобилей.
Технология, созданная для мошенников
Шарлатаны и торгаши процветают в эпоху изобретений, поскольку никто не может точно знать, что станет следующим золотым дном. Батареи были необычно отмечены преувеличением и откровенным мошенничеством: поскольку люди интуитивно понимают важность лучшей батареи и думают, что поэтому мир должен иметь такую батарею, они уязвимы для обмана.В 1883 году Томас Эдисон, слишком много раз вводившийся в заблуждение в процессе создания своей электронной империи, оценил аккумуляторные батареи как простую басню. Он написал:
Батареи были необычно отмечены преувеличением и откровенным мошенничеством: поскольку люди интуитивно понимают важность лучшей батареи и думают, что поэтому мир должен иметь такую батарею, они уязвимы для обмана.В 1883 году Томас Эдисон, слишком много раз вводившийся в заблуждение в процессе создания своей электронной империи, оценил аккумуляторные батареи как простую басню. Он написал:
Аккумулятор — это, на мой взгляд, уловка, сенсация, механизм для обмана населения акционерными обществами. Аккумуляторная батарея — одна из тех необычных вещей, которые поражают воображение, и мошенники на бирже не могли желать ничего более совершенного, чем та самая вещь. … Как только человек приступает к работе с аккумуляторной батареей, он обнаруживает скрытую способность лгать.
Сам Гуденаф вспоминает историю японского материаловеда по имени Сигето Окада. Окада прибыл в 1993 году в Техасский университет, куда Гуденаф переехал в предыдущем году из Оксфорда. Он прибыл из Nippon Telegraph and Telephone (NTT), японского телефонного гиганта, который запросил разрешения включить его в команду Гуденафа за счет компании. После обычных оговорок о конфиденциальности Гуденаф согласился. Он заставил Окаду работать рядом с индийским постдоком по имени Акшая Падхи.
Он прибыл из Nippon Telegraph and Telephone (NTT), японского телефонного гиганта, который запросил разрешения включить его в команду Гуденафа за счет компании. После обычных оговорок о конфиденциальности Гуденаф согласился. Он заставил Окаду работать рядом с индийским постдоком по имени Акшая Падхи.
Принимая таких исследователей, Гуденаф был частью особого мира материаловедов, которые в своих лучших проявлениях сочетают интуицию физики с скрупулезностью химии и прагматизмом инженерии. Их роль — придумать новый порядок из имеющихся перед ними частей. Падхи и Окада начали возиться, ища батарею с большей энергией и большей безопасностью, чем то, что уже было изобретено.
Они думали, что катод с кристаллической структурой, называемой шпинелью, может работать.В обычном катоде из кобальта атомы уложены слоями, поэтому ионы лития, хранящиеся в нем, могут перемещаться внутрь и наружу только по этим слоям. В шпинели расположение атомов позволяет ионам перемещаться в трех измерениях, поэтому они могут находить несколько путей внутрь и наружу электрода, что позволяет ему быстрее заряжаться и разряжаться.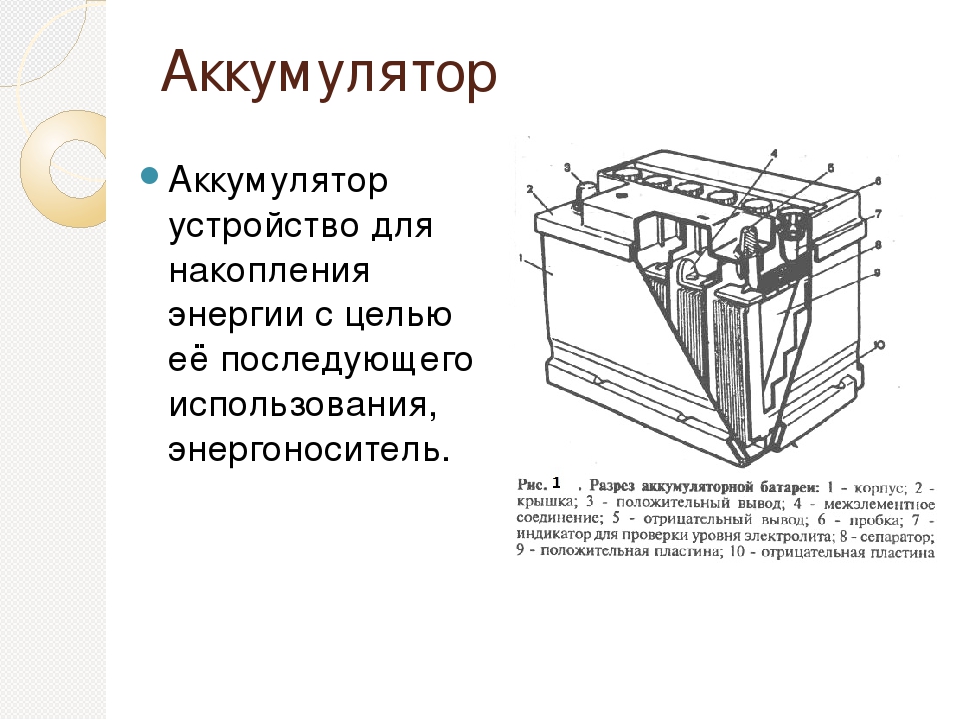 В 1982 году Майк Теккерей, научный сотрудник, работавший под руководством Гуденафа в Оксфорде, создал новаторский катод из марганцевой шпинели, который был дешевле и безопаснее, чем оксид кобальта Гуденаф, изобретенный чуть больше года назад.Возможно, Падхи и Окада смогут произвести шпинель еще лучше.
В 1982 году Майк Теккерей, научный сотрудник, работавший под руководством Гуденафа в Оксфорде, создал новаторский катод из марганцевой шпинели, который был дешевле и безопаснее, чем оксид кобальта Гуденаф, изобретенный чуть больше года назад.Возможно, Падхи и Окада смогут произвести шпинель еще лучше.
Они начали с методической замены металлов, чтобы посмотреть, достигли ли они цели своего учителя. Они пробовали кобальт, марганец и ванадий, но ни один из них не подошел. В конце концов, они отсеяли список до последнего варианта — комбинации железа и фосфора. Гуденаф скептически относился к тому, что у них получится шпинель, и сказал об этом Падхи. Потом старик уехал на летние каникулы.
График, показывающий заряжающие свойства оливина, кристаллическую структуру, обнаруженную в лаборатории Гуденаф. Гуденаф вернулся к новостям. Падхи сказал, что профессор прав — ему не удалось получить структуру шпинели. Вместо этого он создал другую, встречающуюся в природе кристаллическую структуру, названную оливином. И ему удалось извлечь литий из оливина и снова ввести его внутрь. При осмотре Гуденаф увидел, что результат был сенсационным. В третий раз — сначала с оксидом кобальта, затем с марганцевой шпинелью, а теперь и с фосфатом железа — лаборатория Гуденаф произвела большой литий-ионный катод с коммерческими возможностями.
И ему удалось извлечь литий из оливина и снова ввести его внутрь. При осмотре Гуденаф увидел, что результат был сенсационным. В третий раз — сначала с оксидом кобальта, затем с марганцевой шпинелью, а теперь и с фосфатом железа — лаборатория Гуденаф произвела большой литий-ионный катод с коммерческими возможностями.
Гуденаф узнал лишь намного позже, что Окада, японский исследователь, рассказал об открытии Падхи своему работодателю, который тайно разработал саму формулировку. В ноябре 1995 года NTT, используя методологию Падхи, незаметно подала заявку на патент и начала опрашивать японских производителей электроники, оценивая их интерес к новой литий-железо-фосфатной батарее.
Гуденаф уловил эту уловку только в следующем году. Он был недоверчив. «Падхи, ради бога, он был шпионом», — чуть не крикнул он своему постдоку.«Проснись и начни что-нибудь в записной книжке». Он имел в виду, что Падхи должен посвятить свою работу записи в лабораторную тетрадь; эта запись окажется решающей в случае битвы за интеллектуальную собственность.
«Извини», — ответил Пади Гуденафу. «Он мой друг.»
Вступила в гонку за приоритет. Японцы и американцы бросили конкурирующие бумаги и заявки на патенты. От имени лаборатории Гуденаф Техасский университет подал иск на 500 миллионов долларов против NTT.
Потом осложнения усугубились. Профессор Массачусетского технологического института по имени Йет-Мин Чан начал возиться с идеей Гуденафа и подал заявку на получение собственных патентов. Утверждая, что его улучшения позволили создать еще один новый материал, Чан и некоторые партнеры запустили A123, компанию по производству аккумуляторов из Массачусетса. Его заявленной целью было продать версию литий-железо-фосфатной батареи для использования в электроинструментах и, в конечном итоге, в автомобилях. Это создало еще одно правовое прикрытие для Гуденаф, поскольку компания Чанга пыталась убедить европейский суд отменить патенты старика, что в конечном итоге и сделала в 2008 году.
Результат был беспрепятственным, достигнув апогея в конце 2008 года, когда Уоррен Баффет потратил 230 миллионов долларов на покупку 10% BYD, китайской автомобильной компании, которая анонсировала новый электромобиль на литий-железо-фосфатном двигателе. . Никто не говорил об источнике батарей BYD, но после действий Чанга в отрасли сложилось впечатление, что изобретение лаборатории Гудинаф может появиться где угодно.
. Никто не говорил об источнике батарей BYD, но после действий Чанга в отрасли сложилось впечатление, что изобретение лаборатории Гудинаф может появиться где угодно.
В 2009 году A123 продала акции в ходе первичного публичного предложения. Харизма Чанга, имя Массачусетского технологического института и общий дух времени создали ауру шипения, и цена акций выросла на 50% в первый день торгов.Компания Чанга привлекла 587 миллионов долларов, что стало крупнейшим IPO года и огромной зарплатой для него и всех участников. Кроме Гуденафа.
В конце концов, Техасский университет заключил договор с NTT. Выплата школе составила 30 миллионов долларов вместе с долей прибыли от японских патентов. NTT не признала правонарушений. Гуденаф ничего не получил от A123.
В том, что произошло с тех пор, можно было увидеть некую поэтическую справедливость. В 2012 году — всего через три года после IPO — A123 обанкротилась.BYD еще не реализовал заявленный потенциал. Но Гуденаф все еще считал исход железо-фосфатного спора пародией. Юрист, нанятый университетом, был просто болтуном, слишком наивным против хитрых мошенников. Мир аккумуляторов полон преувеличений, и им нужно противостоять. «Им нужны деньги», — говорит он. «И некоторые хуже, чем другие».
Юрист, нанятый университетом, был просто болтуном, слишком наивным против хитрых мошенников. Мир аккумуляторов полон преувеличений, и им нужно противостоять. «Им нужны деньги», — говорит он. «И некоторые хуже, чем другие».
Последняя большая идея
Даррен Кэрролл
Гуденаф в своей лаборатории в Техасском университете в Остине.Жена Гуденаф, Ирен, страдает болезнью Альцгеймера, и в прошлом году он поместил ее на постоянное лечение в учреждение сестринского ухода.Его брат, Уорд, умер примерно в то же время, в возрасте 93 лет.
Когда вы являетесь великим изобретателем в свои 90 лет, это вызывает множество похвал. То же самое и с Гуденафом, который почти каждый год номинирован на Нобелевскую премию, часто вместе с Акирой Йошино, японским химиком, который решил объединить катод американца с угольным анодом, чтобы создать первую работающую литий-ионную батарею — Sony персонаж. В 2013 году Гуденаф получил Национальную медаль науки от президента Барака Обамы, а в 2009 году премию Энрико Ферми. Фактически, Гуденаф имеет свою собственную одноименную награду — с 2009 года Королевское химическое общество Великобритании присуждает ежегодную премию Джона Б. Гуденафа в области химии материалов.
Фактически, Гуденаф имеет свою собственную одноименную награду — с 2009 года Королевское химическое общество Великобритании присуждает ежегодную премию Джона Б. Гуденафа в области химии материалов.
Но Гуденаф, кажется, больше всего страстно желает завершить свою карьеру последним большим изобретением. Он, конечно же, пытается создать супер-батарею, которая сделает электромобили действительно конкурентоспособными по сравнению со сжиганием топлива, а также будет экономно хранить энергию ветра и солнца.
Но выбранный им путь связан с одной из самых сложных проблем в области аккумуляторных технологий — как сделать анод из чистого металлического лития или натрия.Если это удастся сделать, полученная батарея будет иметь на 60% больше энергии, чем существующие литий-ионные элементы. Это мгновенно катапультирует электромобили в новую гонку лицом к лицу со сгоранием. На протяжении многих лет многие ученые пытались и потерпели неудачу — например, именно металлический литий продолжал поджигать лабораторию Стэна Уиттингема в Exxon в 1970-х годах.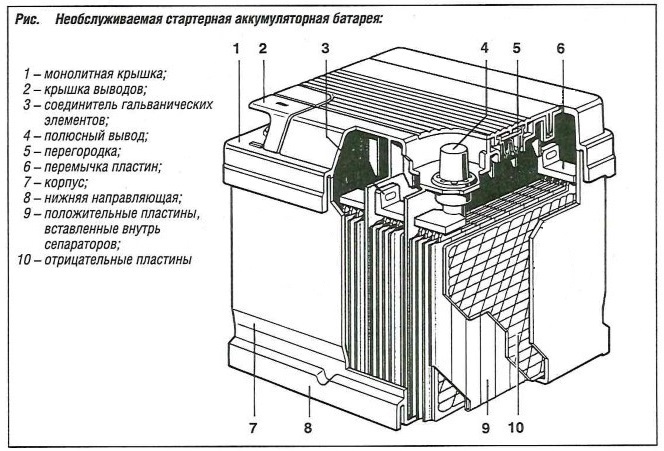
Хотя Гуденаф не будет излагать точную новую идею, он думает, что он что-то понял. И, благодаря его послужному списку, игроки знают, что кто-то будет безрассудно делать против него ставку.«Он все еще очень проницателен. Его разум все еще работает », — говорит Теккерей, южноафриканец, который изобрел марганцевую шпинель при Гуденафе, а сейчас работает в Аргоннской национальной лаборатории США. «Если и будет прорыв, то он будет левым. И Джон приходит из-за пределов коробки ».
Ставки высоки, и Гуденаф отвергает многие конкурирующие подходы, которые он видит — например, Илон Маск из Tesla, который, по его словам, доволен тем, что «продает свои автомобили богатым людям в Голливуде», ожидая, пока ученые создадут батарею. который будет приводить в действие электромобиль среднего класса.Это не совсем справедливо — Маск, очевидно, продает свои автомобили за 80 000–100 000 долларов в элитную нишу, но к 2018 году он клянется иметь модель за 35 000 долларов для более широкого сегмента рынка. Он добивается этого благодаря гибкой инженерии, которая позволила постепенно улучшить его аккумулятор.
Он добивается этого благодаря гибкой инженерии, которая позволила постепенно улучшить его аккумулятор.
Но Гуденаф не менее пренебрежительно относится к подобным ухищрениям и их ничтожным 7% или 8% в год дополнительной эффективности. «Вам нужно что-то, что даст вам немного шага, — говорит он, — а не шага.
Никто, включая его, не может с уверенностью сказать, что на этот раз Гуденаф добьется успеха. Только то, что он не сдался. Проблема супер-аккумулятора действительно сложна. Сам Гуденаф говорит, что все остальные тоже должны продолжать попытки совершить прыжок. Он считает, что у месторождения есть три десятилетия, чтобы преуспеть и коммерциализировать прорыв, прежде чем возникнут действительно серьезные проблемы с окружающей средой и нехваткой ресурсов. На это, думает он, должно быть достаточно времени. «Работает много людей, и никто из них не глуп», — говорит он.«Я не говорю, что я единственный, кто может решить эту проблему».
И снова он может быть.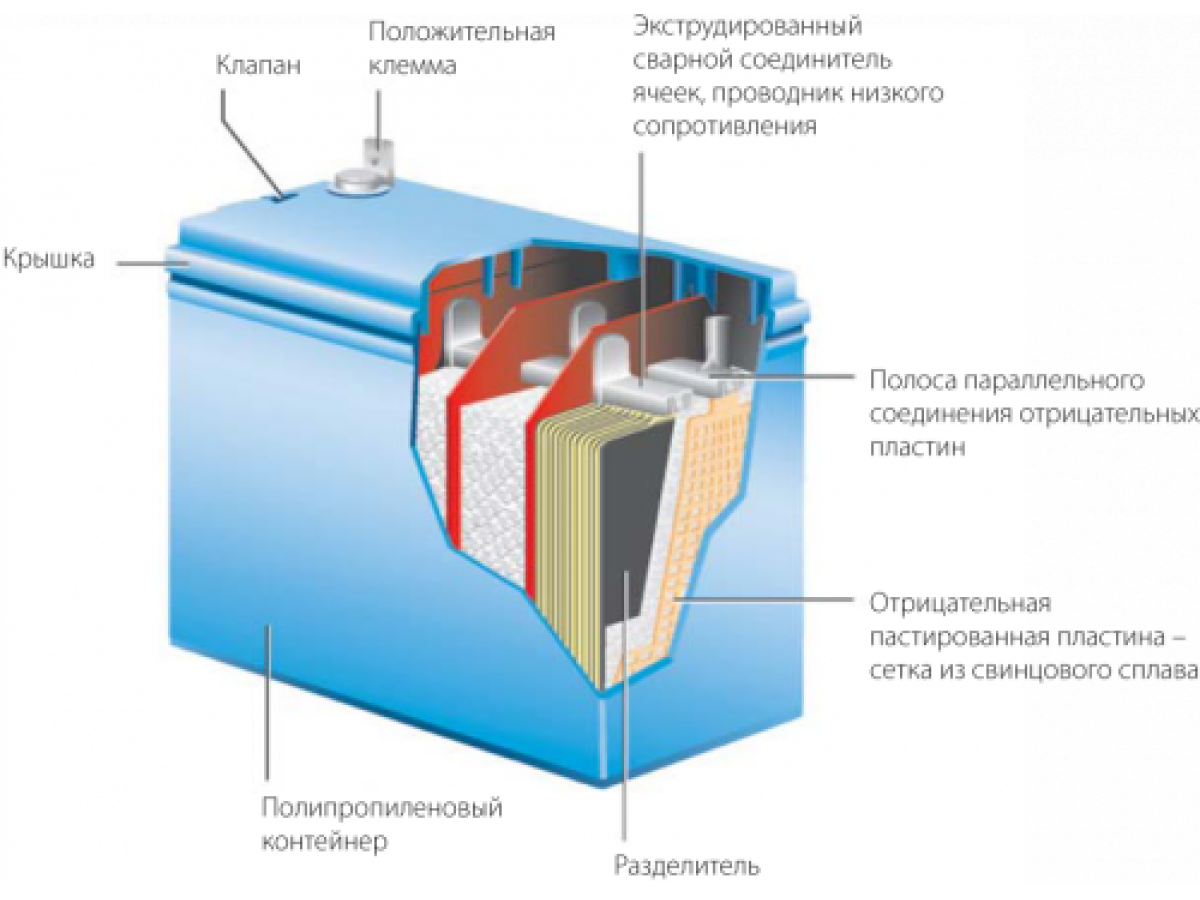 Вот почему многие люди — те, кто знает о нем, — пристально следят за Джоном Баннистером Гудинафом.
Вот почему многие люди — те, кто знает о нем, — пристально следят за Джоном Баннистером Гудинафом.
Адаптировано из The Powerhouse Стива Левина, поступит в продажу 5 февраля компанией Viking. Смотрите видео и веб-сайт здесь.
Батарея LVAD, CRT-D или CRT-P
Батарея LVAD, CRT-D или CRT-P | ЭбботтLVAD, CRT-D ИЛИ CRT-P СРОК БАТАРЕИ
Некоторые сердечные устройства, в том числе устройства для сердечной ресинхронизирующей терапии (CRT-P и CRT-D) и вспомогательные устройства для левого желудочка (LVAD), питаются от батареи.Батареи для этих типов устройств специально разработаны для работы в течение длительного времени — обычно от трех до шести лет, в зависимости от вашего устройства и его функций.
ЭЛТ-УСТРОЙСТВА
Когда батарея вашего ЭЛТ-устройства начинает разряжаться, он дает много предупреждений. Ваш врач сможет определить, что батарея разряжена, во время последующих осмотров с вашей удаленной системы или в кабинете вашего врача. Когда это произойдет, ваш врач, скорее всего, порекомендует вам заменить текущее устройство.
Когда это произойдет, ваш врач, скорее всего, порекомендует вам заменить текущее устройство.
Новое устройство необходимо для замены батарей CRT-P или CRT-D, потому что батареи нельзя перезаряжать или извлекать из этих устройств. Узнайте больше о замене устройства.
LVADS
УстройстваLVAD поставляются с блоком питания и батареями. Блок питания можно подключить к электрической розетке, чтобы обеспечить питание, пока вы находитесь в помещении, в состоянии покоя или во сне. Батареи являются перезаряжаемыми и могут использоваться, когда вы находитесь вдали от дома или источника питания.
Многие пациенты заряжают свои батареи на ночь и снова вставляют их утром перед тем, как пойти на работу или принять участие в своей повседневной деятельности. Батареи легкие и долговечные, обеспечивая много часов бесперебойной работы.
ВЫ ХОТИТЕ ПРОДОЛЖИТЬ И ВЫЙТИ CARDIOVASCULAR.ABBOTT?
СОДЕРЖАНИЕ САЙТА НЕ ПОД КОНТРОЛЕМ ABBOTT.
Меры предосторожности
Обязательно прочтите его.
Следующие страницы предназначены для медицинских работников и содержат информацию о правильном использовании продуктов (медицинских устройств и т. Д.) Abbott Medical Japan GK.
Информация, представленная здесь, не предназначена для предоставления информации пациентам и широкой общественности.
Вы медицинский работник?
Тест
да
Меры предосторожности
Обязательно прочтите его.
Следующие страницы предназначены для медицинских работников и содержат информацию о правильном использовании продуктов (медицинских устройств и т. Д.).) компании Abbott Medical Japan GK.
Информация, представленная здесь, не предназначена для предоставления информации пациентам и широкой общественности.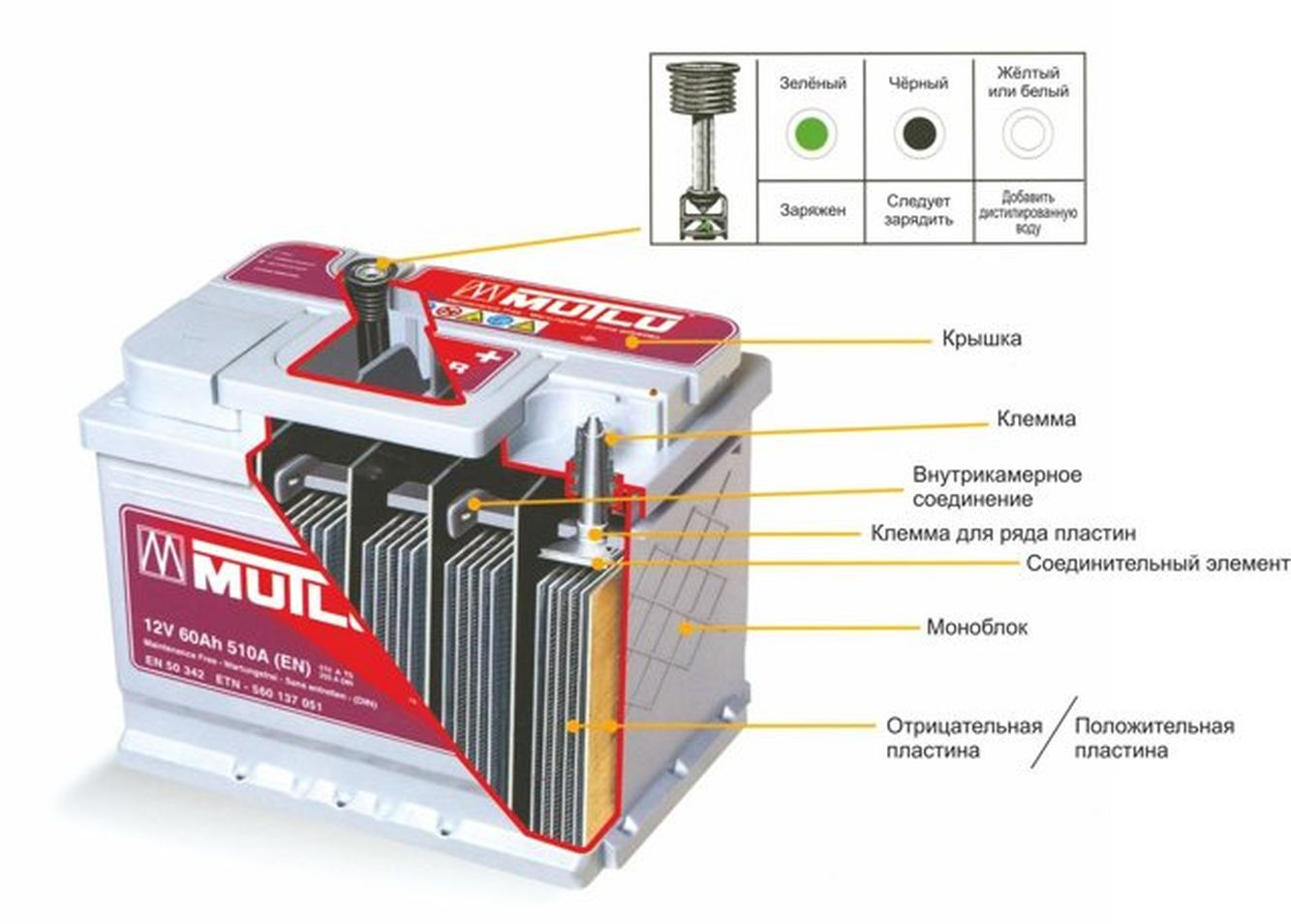
Вы медицинский работник?
Тест
[prod, crx3, samplecontent, publish, crx3tar]
ВЫ ХОТИТЕ ПРОДОЛЖИТЬ И ВЫЙТИ CARDIOVASCULAR.ABBOTT?
СОДЕРЖАНИЕ САЙТА НЕ ПОД КОНТРОЛЕМ ABBOTT.
https://vascular.abbott.com/,https://mri.merlin.net/,https://www.thelancet.com/,https://www.ahajournals.org/, https://www .onlinejacc.org /, https: //jamanetwork.com/, https://www.sciencedirect.com/, https: // onlinelibrary.wiley.com/,https://www.cms.gov/,https://www.novitas-solutions.com/,https://event.on24.com/,http://dx.doi.org/ , https: //www.myloopaccount.com/, https://www.invasivecardiology.com/, https://manuals.sjm.com/, https://www.cardiovascular.abbott
Ложь
доступность © 2019 Abbott. Все права защищены. Пожалуйста, прочтите официальное уведомление для получения более подробной информации.
Все права защищены. Пожалуйста, прочтите официальное уведомление для получения более подробной информации.
Если не указано иное, все названия продуктов и услуг, представленные на этом Интернет-сайте, являются товарными знаками, принадлежащими компании Abbott, ее дочерним или аффилированным компаниям или переданными по лицензии ей.Запрещается использование каких-либо товарных знаков, фирменных наименований или фирменного стиля Abbott на этом сайте без предварительного письменного разрешения Abbott, кроме как для идентификации продукта или услуг компании.
доступностьВЫ ХОТИТЕ ПРОДОЛЖИТЬ И ВЫЙТИ CARDIOVASCULAR.ABBOTT?
СОДЕРЖАНИЕ САЙТА НЕ ПОД КОНТРОЛЕМ ABBOTT.
доступность © 2019 Abbott. Все права защищены. Пожалуйста, прочтите официальное уведомление для получения более подробной информации.
Если не указано иное, все названия продуктов и услуг, представленные на этом Интернет-сайте, являются товарными знаками, принадлежащими компании Abbott, ее дочерним или аффилированным компаниям или переданными по лицензии ей.Запрещается использование каких-либо товарных знаков, фирменных наименований или фирменного стиля Abbott на этом сайте без предварительного письменного разрешения Abbott, кроме как для идентификации продукта или услуг компании.
доступностьМеры предосторожности
Обязательно прочтите его.
Следующие страницы предназначены для медицинских работников и содержат информацию о правильном использовании продуктов (медицинских устройств и т. Д.) Abbott Medical Japan GK.
Информация, представленная здесь, не предназначена для предоставления информации пациентам и широкой общественности.
Вы медицинский работник?
Тест
Этот сайт использует файлы cookie.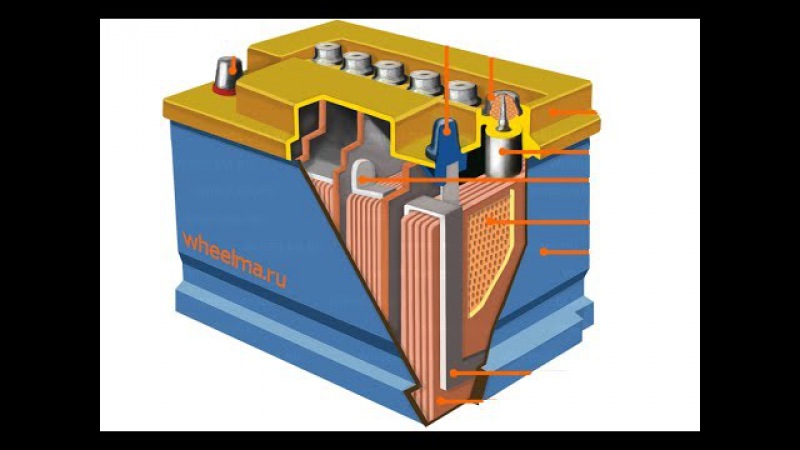 Используя этот сайт, вы соглашаетесь на размещение наших файлов cookie.Прочтите нашу политику конфиденциальности, чтобы узнать больше.
Используя этот сайт, вы соглашаетесь на размещение наших файлов cookie.Прочтите нашу политику конфиденциальности, чтобы узнать больше.
Холодная погода и дверные звонки на батарейках — Ring Help
Во многих частях света зима приносит холода, дождь, мокрый снег, снег, а иногда и очень низкие температуры. В результате на производительность кольцевых устройств может влиять холод. Эта статья расскажет вам, почему это происходит, и предложит несколько советов, что с этим делать.
Срок службы батареи и холода
Чрезвычайно холодная погода отрицательно сказывается на литий-ионных батареях, например, используемых в кольцевых устройствах. При понижении температуры у этих батарей возникают проблемы с удержанием заряда, а если становится достаточно холодно, они вообще перестают работать. В результате при определенных температурах батареи в устройстве Ring могут разрядиться быстрее, чем ожидалось, и, возможно, потребуется более частая подзарядка.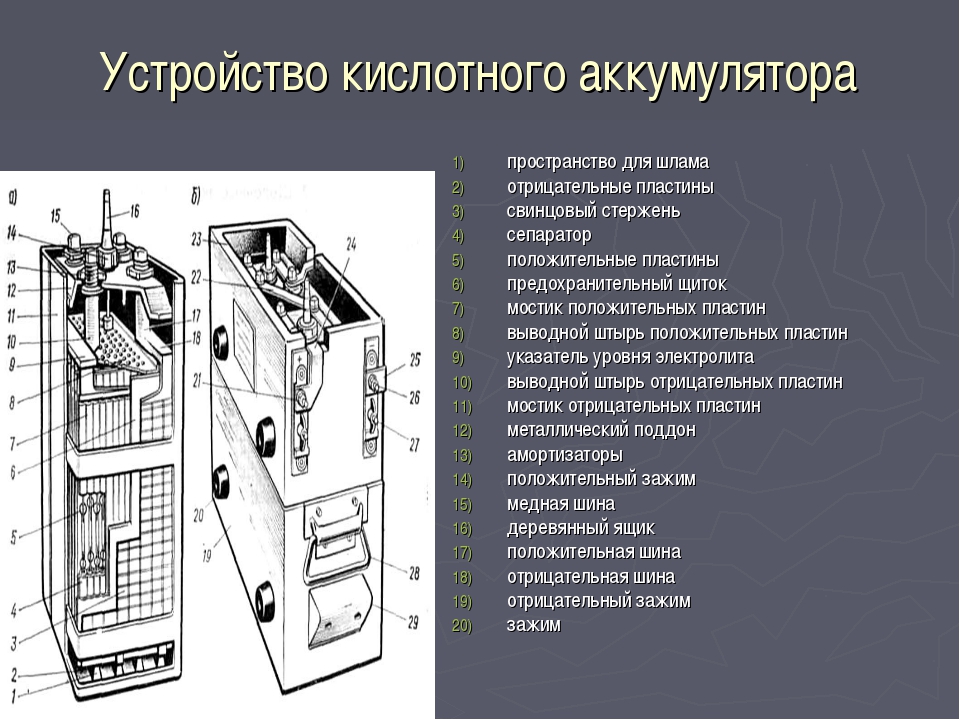
Еще одним важным фактором, влияющим на срок службы батареи Ring, является то, подключено ли оно к другому источнику питания, например, к существующему питанию дверного звонка.Устройства с кольцевым питанием от батарей работают от батарей, а не от внешнего источника питания. Внешние источники питания используются для подзарядки батарей и не могут обеспечивать питание устройства. Когда температура упадет ниже 0 градусов Цельсия, аккумулятор перестанет принимать внешний заряд и может разрядиться.
Важные температуры
Ниже приведены основные температуры, на которые следует обращать внимание при работе с аккумуляторами.
- 36 ° F (3 ° C): Батарея может не удерживать заряд так эффективно, что вам придется заряжать устройство чаще.
- 32 ° F (0 ° C): Батарея может вообще не заряжаться. Даже конфигурации с проводным подключением могут не заряжать аккумулятор.
- -5 ° F (-20,5 ° C): Аккумулятор может полностью перестать работать до тех пор, пока температура не повысится.

Что делать, когда становится холодно
- Перенесите устройство внутрь: когда станет холодно и аккумулятор вашего устройства разрядится, внесите все устройство внутрь и зарядите аккумулятор с помощью USB-кабеля. Это позволит вашему устройству нагреться во время зарядки аккумулятора.
- Убедитесь, что ваша батарея заряжена до 100%: при зарядке батареи убедитесь, что она достигла 100% перед повторной установкой устройства. Хотя батарея по-прежнему не будет такой эффективной, как при более высоких температурах, убедитесь, что батарея на 100%, и ваше устройство проработает как можно дольше.
- Контролируйте уровень заряда и температуру: пока температура колеблется в пределах указанных выше значений, у вас могут быть проблемы с зарядкой аккумулятора. Поэтому важно постоянно следить за временем автономной работы, когда становится холодно, чтобы убедиться, что ваше устройство всегда работает.
Я пытался зарядить аккумулятор в очень холодный или жаркий день, но аккумулятор не заряжался. В чем дело?
В чем дело?
Если аккумулятор слишком горячий или слишком холодный, встроенное программное обеспечение не дает ему заряжаться, чтобы не повредить аккумулятор. Поместите аккумулятор внутрь и дайте ему остыть до комнатной температуры, прежде чем пытаться зарядить аккумулятор.
Щелкните здесь, чтобы получить дополнительную информацию о сроке службы батареи.
Советы по уходу за аккумулятором и хранению аккумулятора
Помогает ли хранение батареи в холодильнике продлить срок ее службы? Узнайте несколько полезных советов о том, как лучше всего хранить, обращаться с аккумуляторами и ухаживать за ними, будь то дома или в дороге.Do’s
- Храните батарейки, особенно маленькие и литиевые батарейки типа «таблетка», а также устройства, в которых они используются, в недоступном для детей месте. При проглатывании плоские литиевые батарейки могут застрять в пищеводе ребенка и стать причиной серьезной травмы менее чем за два часа. Посетите страницу безопасности литиевых батарей для монет, чтобы узнать больше.

- Помогите Energizer повысить осведомленность о рисках, связанных с проглатыванием 20-миллиметровых литиевых батарей для монет.Посетите нашу страницу по технике безопасности для монетоприемных литиевых батарей или позвоните в службу поддержки клиентов Energizer (1-800-383-7323), чтобы узнать больше.
ЕСЛИ ВЫ ПОДОЗРИВАЕТЕ, ЧТО ВАШ РЕБЕНОК ПРОГЛАТИЛ ЛИТИЕВУЮ БАТАРЕЮ ДЛЯ МОНЕТ, НЕМЕДЛЕННО ОТведите ЕГО ИЛИ ЕЕ В АВАРИЙНУЮ ПОМОЩЬ И СЛЕДУЙТЕ ЭТИМ ДЕЙСТВИЯМ:- 1. Сообщите врачам и медсестрам, что это может быть литиевая батарейка.
- 2. Сообщите медицинской бригаде идентификационный номер из упаковки батареи, если это возможно.
- 3. Не позволяйте ребенку есть или пить до тех пор, пока рентген не определит наличие батареи.
- 4. Не вызывайте рвоту.
- ОБЯЗАТЕЛЬНО прочтите инструкции на своем устройстве перед установкой батарей.
 Используйте только батареи того размера и типа, которые указаны в инструкции.
Используйте только батареи того размера и типа, которые указаны в инструкции. - ОБЯЗАТЕЛЬНО вставляйте батареи правильно.Следуйте символам, показывающим правильный способ расположения положительного (+) и отрицательного (-) полюсов батарей.
- ОБЯЗАТЕЛЬНО поддерживайте чистоту контактных поверхностей аккумулятора, аккуратно протирая их чистым ластиком для карандашей или тканью.
- НЕМЕДЛЕННО извлекайте разряженные батареи из устройства и утилизируйте их надлежащим образом.
- НЕОБХОДИМО извлекать из устройства все батареи одновременно и заменять их новыми батареями того же размера и типа.
- ДЕЙСТВИТЕЛЬНО продлевает срок службы батареи, выключая устройство и извлекая батареи, когда оно не используется, и не предполагается, что оно будет использоваться в течение длительного периода времени.
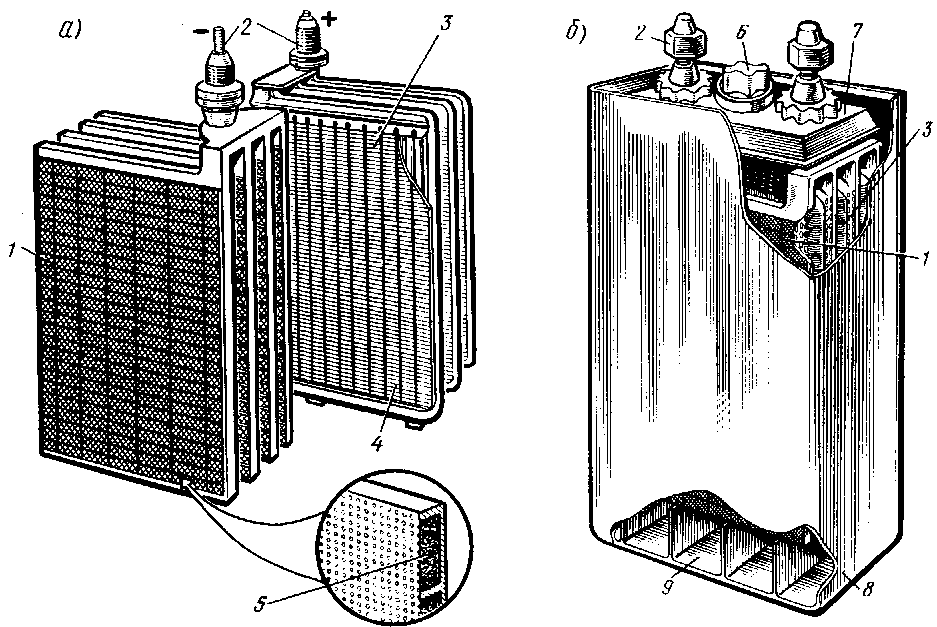
- НЕОБХОДИМО соблюдать правила хранения батарей, храня их в прохладном, сухом месте при нормальной комнатной температуре. Батареи не нужно хранить в холодильнике.
Нельзя
- НЕ бросайте батареи в огонь — они могут протечь или лопнуть.
- ЗАПРЕЩАЕТСЯ разбирать, разбивать, прокалывать или иным образом повредить аккумуляторы. Это может привести к утечке или разрыву.
- НЕ носите незакрепленные батареи в кармане или сумочке с металлическими предметами, такими как монеты, скрепки и т. Д. Это может вызвать короткое замыкание батареи, что приведет к перегреву или утечке.
- ЗАПРЕЩАЕТСЯ заряжать аккумулятор, если он специально не помечен как «аккумуляторный».
 «Попытка перезарядить неперезаряжаемую (первичную) батарею может привести к утечке или разрыву. Не используйте перезаряжаемые щелочные батареи в зарядных устройствах для никель-металлогидридных батарей.
«Попытка перезарядить неперезаряжаемую (первичную) батарею может привести к утечке или разрыву. Не используйте перезаряжаемые щелочные батареи в зарядных устройствах для никель-металлогидридных батарей. - ЗАПРЕЩАЕТСЯ хранить аккумуляторы или устройства с батарейным питанием в жарких местах — повышенные температуры могут привести к потере емкости, утечке или повреждению.
- НЕ используйте одновременно старые и новые батареи, а также батареи разных типов или производителей.Это может вызвать утечку или разрыв, что может привести к травмам или повреждению имущества.
- НЕ давайте батарейки маленьким детям.
Как правильная или неправильная зарядка или хранение влияют на срок службы аккумуляторных батарей? Изучите несколько полезных советов о том, как лучше всего хранить аккумуляторные батареи, обращаться с ними и ухаживать за ними, будь то дома, на работе или в игре.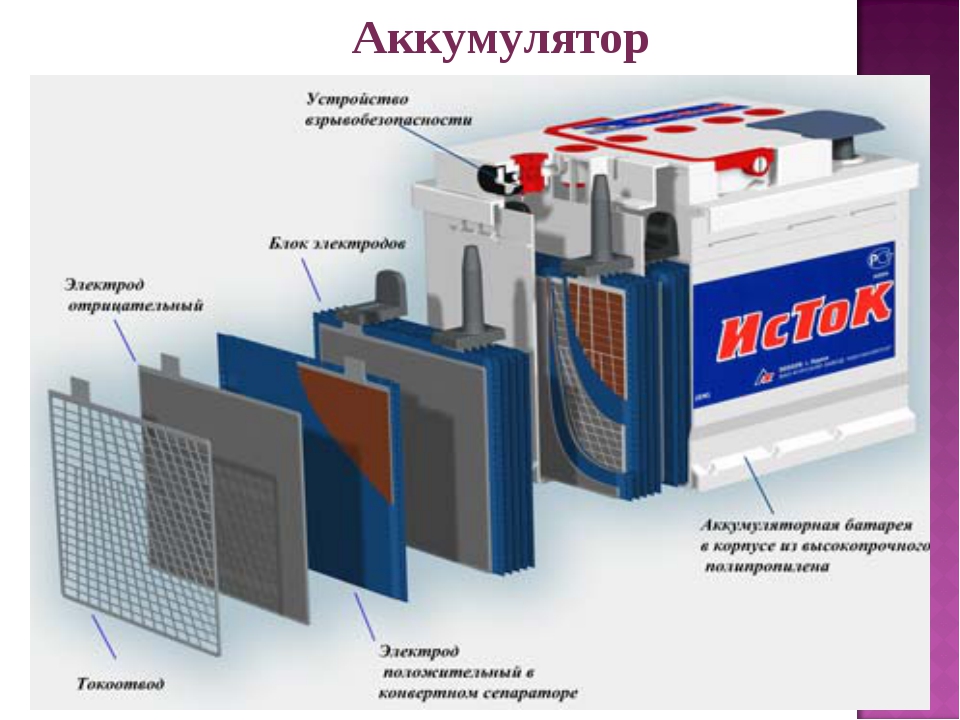
Dos
- ОБЯЗАТЕЛЬНО соблюдайте инструкции производителя по хранению и уходу за батареями и не перезаряжайте батареи.
- Заряжайте аккумулятор при комнатной температуре (от 68 ° F до 72 ° F), чтобы продлить срок его службы. Батареи нагреваются во время зарядки и использования — это нормально.В качестве меры предосторожности большинство аккумуляторов и зарядных устройств предназначены для защиты от перегрева.
- НЕ забудьте зарядить аккумулятор за несколько часов до того, как вы захотите его использовать. Аккумуляторные батареи теряют определенный процент заряда каждый день, если их не использовать для зарядки.
- ОБЯЗАТЕЛЬНО поддерживайте чистоту контактных поверхностей аккумулятора, аккуратно протирая их чистым ластиком для карандашей, тканью или спиртом.
 Грязные контактные точки являются основным источником проблем с зарядкой.
Грязные контактные точки являются основным источником проблем с зарядкой. - ОБЯЗАТЕЛЬНО используйте только зарядные устройства, предназначенные для вашего типа батарей. Если вы не уверены в совместимости, обратитесь к производителю продукта.
Нельзя
- НЕ оставляйте аккумуляторные батареи разряженными или неиспользуемыми в течение длительного времени.Чтобы продлить срок службы батарей, заряжайте их не реже, чем каждые 6-9 месяцев. ЗАПРЕЩАЕТСЯ заряжать аккумулятор, если он специально не помечен как «перезаряжаемый». Попытка перезарядить основную (неперезаряжаемую) батарею может привести к утечке или разрыву. НЕ используйте перезаряжаемые батареи в зарядных устройствах, которые не предназначены для определенного типа батарей.
Есть ли правильный и неправильный способ путешествовать с батареями? Получите несколько полезных советов о том, как лучше всего хранить, обращаться с батареями и ухаживать за ними во время путешествий.
Планируете поездку? Батареи не нужно оставлять дома. Батареи и устройства с батарейным питанием безопасны для полета, если вы будете следовать этим простым рекомендациям U.S. Департамент транспорта:
- Упакуйте запасные батареи в ручную кладь. В пассажирском салоне летные экипажи могут лучше контролировать условия безопасности, чтобы предотвратить инцидент, и могут получить доступ к огнетушителям, если инцидент все же произойдет.
- Храните запасные батареи в оригинальной розничной упаковке, чтобы предотвратить непреднамеренное включение или короткое замыкание.

- В случае незакрепленных батарей поместите полоску изоляционной ленты на контакты батареи или поместите каждую батарею в отдельный защитный футляр, пластиковый пакет или упаковку, чтобы защитить их от контакта с металлическими предметами, такими как монеты, ключи или украшения.
- Примите меры, чтобы предотвратить раздавливание, прокалывание или чрезмерное давление на аккумулятор, так как это может вызвать внутреннее короткое замыкание, что приведет к перегреву.
Согласно Министерству транспорта США, «батареи не представляют большой опасности в устройствах, которые они питают, и что извлечение батареи из устройства не повышает безопасность».
Для получения дополнительной информации и новейших технологий транспортировки аккумуляторов и устройств с батарейным питанием посетите веб-сайт http://safetravel.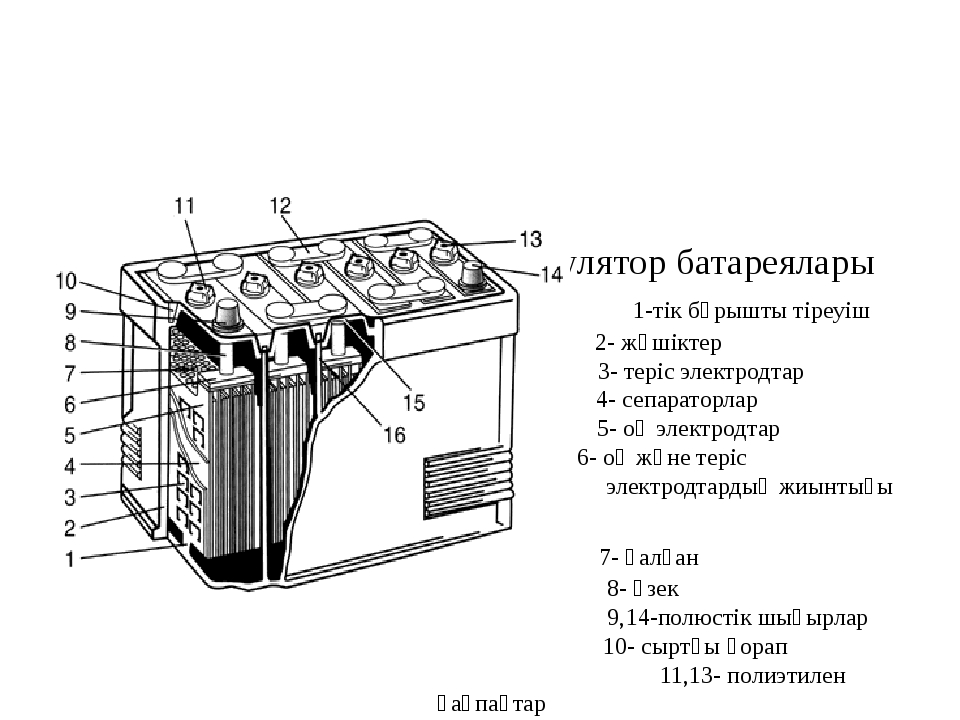 dot.gov/.
dot.gov/.
Хотя зачастую утилизировать использованные батареи в рамках обычного процесса утилизации отходов безопасно, компания Energizer призывает всех сдавать свои батареи на переработку — это просто ответственный поступок. Вот почему мы сотрудничаем с такими важными организациями, как Earth911, для получения информации об утилизации одноразовых батарей и перезаряжаемых батарей.
Утилизация в США.С.
В качестве первого шага определите тип имеющейся у вас батареи, а затем определите соответствующий метод утилизации. Обратите внимание, что правила могут различаться в вашем муниципалитете или штате, поэтому, пожалуйста, ознакомьтесь с местными правилами. Если вы занимаетесь утилизацией большого количества батареек-таблеток, обратитесь в службу поддержки клиентов Energizer по телефону 800-383-7323 или напишите нам по электронной почте.
Мы настоятельно рекомендуем вам посетить Earth911, чтобы узнать больше об утилизации одноразовых батарей, и Call2Recycle® для получения информации об утилизации аккумуляторных батарей.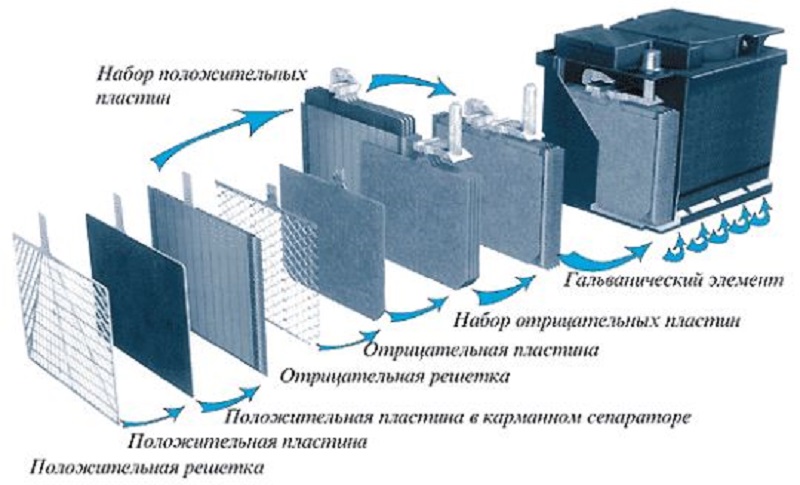
Ресурсы всегда под рукой
Посетите Earth911 на www.earth911.com
Посетите Call2Recycle ® на сайте www.call2recycle.org
Хотя зачастую утилизировать использованные батареи в рамках обычного процесса утилизации отходов безопасно, компания Energizer призывает всех утилизировать свои батареи — это просто ответственный поступок.Вот почему мы сотрудничаем с такими важными организациями, как Earth911, для получения информации об утилизации одноразовых батарей.
Мы рекомендуем вам утилизировать эти типы батарей в рамках программы Call2Recycle ® .
Утилизация — хорошая альтернатива.
Пожалуйста, сделайте ответственный поступок.
Компания Energizer настоятельно рекомендует надлежащую утилизацию и переработку всех батарей.
Для получения дополнительной информации о том, как безопасно и ответственно утилизировать использованные одноразовые и перезаряжаемые батареи, посетите две организации, с которыми компания Energizer гордится партнерством:
Земля 911 Земля 911
Call2Recycle

