Проверка НРЦ и плотности электролита
Главная / Информация покупателю / Ремонт, заряд, контроль и хранение АКБ / Проверка НРЦ и плотности электролита
Для того, чтобы замедлить старение АКБ, необходимо выполнять несколько основных требований по контролю за состоянием батареи и электрооборудования автомобиля. Проверка напряжения разомкнутой цепи (НРЦ) проводится через 6 – 8 часов после выключения двигателя (или зарядного тока при заряде от внешнего зарядного устройства). Напряжение на клеммах батареи измеряется с помощью вольтметра. Значение НРЦ в зависимости от степени заряженности батареи приведено в табл. 1. Степень заряженности также однозначно связана и с плотностью электролита АКБ
табл. 1 Зависимость напряжения разомкнутой цепи [ НРЦ ] АКБ при различных температурах электролита
Степень заряженности % | Равновесное напряжение разомкнутой цепи (НРЦ) В, при различных температурах | ||
+20…+25 С | +5…-5 С | -10…-15 С | |
100 | 12,70 – 12,90 | 12,80 – 13,00 | 12,90 – 13,10 |
75 | 12,55 – 12,65 | 12,55 – 12,75 | 12,65 – 12,85 |
Опасная зона | |||
50 | 12,20 – 12,30 | 12,30 – 12,40 | 12,40 – 12,50 |
25 | 11,95 – 12,10 | 12,10 – 12,20 | 12,20 – 12,30 |
0 | 11,60 – 11,80 | 11,70 – 11,90 | 11,80 – 12,00 |
При безотказной эксплуатации необслуживаемой батареи, которая не имеет пробок, достаточно один раз в 3 – 4 месяца проверять ее НРЦ с целью определения состояния заряженности в соответствии с табл. 1. Если же возникают трудности с пуском двигателя, необходимо проверить исправность электрооборудования.
1. Если же возникают трудности с пуском двигателя, необходимо проверить исправность электрооборудования.
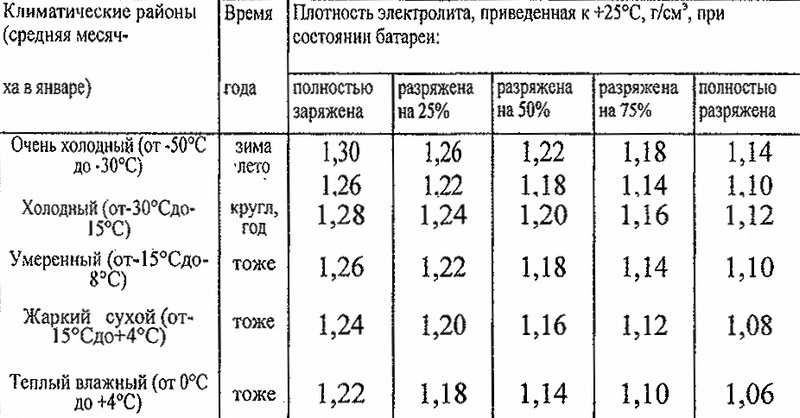
У полностью заряженной батареи плотность электролита составляет 1,28+0,01 г/см
Если значение плотности во всех аккумуляторах («банках») одинаково (с разбросом ±0,01 г/см3), это говорит об отсутствии внутренних замыканий. При наличии внутреннего короткого замыкания плотность электролита в дефектном аккумуляторе будет значительно ниже, чем в остальных ячейках.
Для измерения плотности применяют ареометры со сменными денсиметрами для измерения плотности различных жидкостей, например, антифриза с плотностью от 1,0 до 1,1 г/см3 или электролита с плотностью от 1,1 до 1,3 г/см3.
Одновременно необходимо замерить температуру электролита.
Если при измерении окажется, что НРЦ ниже 12,6 В, а плотность электролита ниже 1,24 г/см3, батарею необходимо подзарядить и проверить зарядное напряжение на ее клеммах при работающем двигателе.
табл. 2 Температурные поправки к показаниям денсиметра при приведении плотности электролита к +25 С
Температура электролита, С | Поправка, г/см3 | Температура электролита, С | Поправка, г/см3 |
-65..-50 | -0,06 | -4…+10 | -0,02 |
-49…-35 | -0,05 | +11…+24 | -0,01 |
-34…-20 | -0,04 | +26…+40 | +0,01 |
-19…-5 | -0,03 | +41…+55 | +0,02 |
Как проверить плотность электролита в аккумуляторе ареометром и без него в домашних условиях
Автор Акум Эксперт На чтение 7 мин Просмотров 8. 6к. Опубликовано Обновлено
6к. Опубликовано Обновлено
Аккумуляторная батарея постоянно работает в режиме разряда-заряда. Чтобы продлить время её эксплуатации, следует поддерживать её заряд на максимальном уровне. А для этого время от времени необходимо проверять уровень заряда АКБ. Сделать это можно разными способами, но самый надёжный — измерить плотность электролита. Поэтому многие водители задаются вопросом, как проверить плотность аккумулятора.
Ареометр в работеСодержание
- Что такое плотность и на что она влияет
- Как пользоваться ареометром — подробная инструкция
- Можно ли измерить без ареометра
- Можно ли проверить плотность в необслуживаемом аккумуляторе
Что такое плотность и на что она влияет
Обязательным элементом свинцово-кислотной батареи является электролит. Это серная кислота, разбавленная дистиллированной водой. Плотность воды составляет 1 грамм на миллилитр (г/мл). У серной кислоты она выше, чем у воды, и составляет 1,84 г/мл. Концентрированная кислота способна растворить многие металлы, в том числе и свинец, поэтому её следует разбавлять водой. Разбавленная водой кислота называется электролитом. Разбавляют её до пропорции, при которой она неспособна растворить свинец, но позволяет протекать химическому процессу, называемому электролитической диссоциацией (разновидность электролиза).
Плотность воды составляет 1 грамм на миллилитр (г/мл). У серной кислоты она выше, чем у воды, и составляет 1,84 г/мл. Концентрированная кислота способна растворить многие металлы, в том числе и свинец, поэтому её следует разбавлять водой. Разбавленная водой кислота называется электролитом. Разбавляют её до пропорции, при которой она неспособна растворить свинец, но позволяет протекать химическому процессу, называемому электролитической диссоциацией (разновидность электролиза).
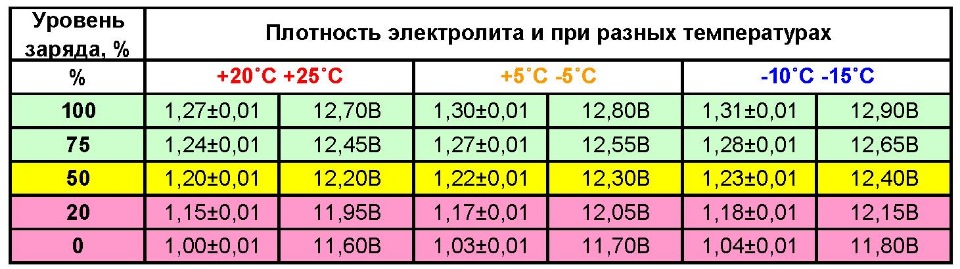
Чем выше плотность, тем сильнее электролиз, но тем быстрее идёт разрушение свинца. Наиболее оптимальная плотность для аккумуляторов 1,27 г/мл для районов умеренного климата со средней температурой от -20 до +30°С. Такую плотность имеет полностью (100 %) заряженный новый аккумулятор. Для северных регионов это значение составляет 1,29 г/мл, для южного жаркого климата — 1,25 г/мл.
Таблица с рекомендуемыми значениями плотности электролита для полностью заряженной батареиВ продажу поступает серная кислота уже в виде электролита плотностью 1,3 г/мл. С учётом условий эксплуатации аккумулятора её доводят до нужных параметров.
С учётом условий эксплуатации аккумулятора её доводят до нужных параметров.
Как уже отмечалось выше, чем больше плотность электролита, тем сильнее электролиз и тем выше потенциал на выводах батареи. Новая АКБ имеет плотность 1,27 г/мл и напряжение на клеммах 12,8 В. За время эксплуатации батареи при регулярном недозаряде на её свинцовых пластинах образуется нерастворимый сульфат свинца, соединение серной кислоты со свинцом. Называется это сульфатацией пластин. При заряде батареи уже не вся кислота высвобождается, и плотность электролита снижается. А следовательно, снижается и интенсивность электролиза. Напряжение на клеммах будет уже меньше 12,8 В. А попытка зарядить батарею до начального значения напряжения лишь приводит к кипению электролита — активному выделению пузырьков водорода и кислорода. Это процесс разложения воды. Потеря воды приводит к повышению плотности.
Мнение эксперта
Алексей Бартош
Специалист по ремонту, обслуживанию электрооборудования и промышленной электроники.
Задать вопрос
Слишком высокая или низкая плотность одинаково недопустимы и значительно снижают срок эксплуатации АКБ.
В условиях эксплуатации автомобиля с частыми пусками двигателя и коротким пробегом происходит ускоренная сульфатация пластин и снижение плотности электролита. При эксплуатации машин в дальних рейсах с длительной работой двигателя происходит перезаряд батареи и разложение воды на газы, а плотность электролита повышается. Напряжение на клеммах уже не отражает степень заряженности батареи. И чтобы точно узнать состояние аккумулятора, нужно произвести измерение плотности электролита. Для этого используют ареометр.
Наиболее популярный тип ареометраАреометр — прибор для измерения плотности жидкостей и твёрдых тел, принцип работы которого основан на Законе Архимеда.
Как пользоваться ареометром — подробная инструкция
Ареометр представляет собой стеклянную колбу (пипетку) с помещённым внутрь измерительным грузом-поплавком (ареометром), на котором нанесены деления с указанием величин от 1,1 в верхней точке поплавка до 1,3 и даже 1,32 г/мл внизу шкалы.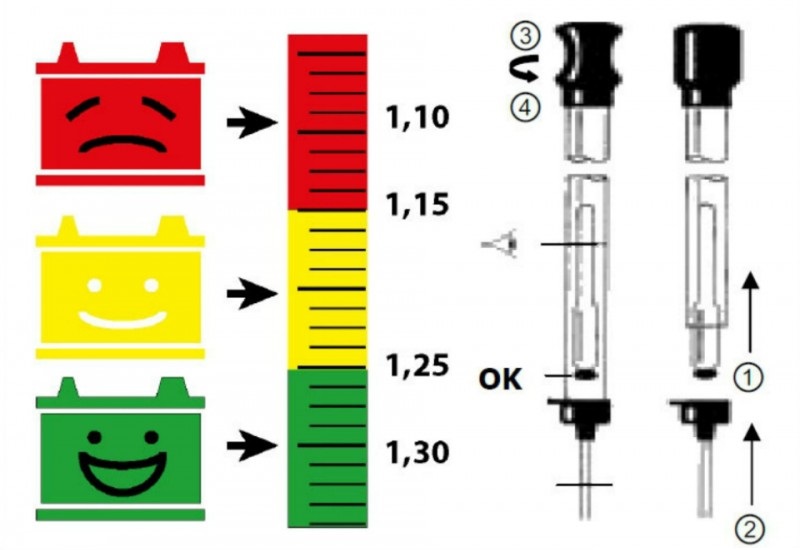 Нижняя часть колбы имеет тонкую трубку, которую легко можно опустить через отверстие аккумулятора в его банку для забора электролита. На верхнюю часть колбы надевается резиновая груша, которая применяется для всасывания раствора в колбу.
Нижняя часть колбы имеет тонкую трубку, которую легко можно опустить через отверстие аккумулятора в его банку для забора электролита. На верхнюю часть колбы надевается резиновая груша, которая применяется для всасывания раствора в колбу.
У некоторых ареометров несколько поплавков разного веса, которые всплывают при заполнении колбы. Плотность будет соответствовать поплавку, всплывшему частично или не всплывшему первому после всплывших. Встречаются дешёвые пластиковые изделия иной формы, но принцип их действия такой же.
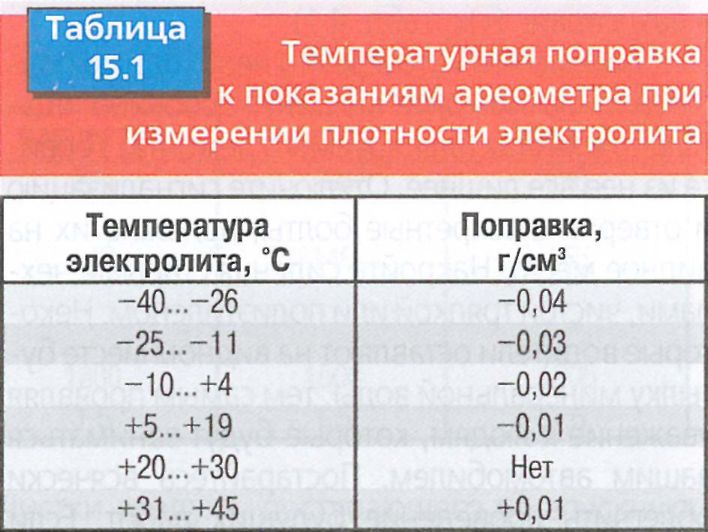
Другие разновидности ареометраИзмерение ареометром производят при температуре электролита +20 … +30°C. Если температура иная, то необходимо применять корректировочные поправки к показанию ареометра.
Поправки к показаниям ареометра при измерении электролита разной температурыПользование ареометром настолько простое, что даже можно проверить плотность электролита в домашних условиях. Чтобы проверить плотность аккумулятора, необходимо выполнить следующие действия:
- Подготовить ареометр, собрать прибор, если он находится в разобранном виде в футляре.
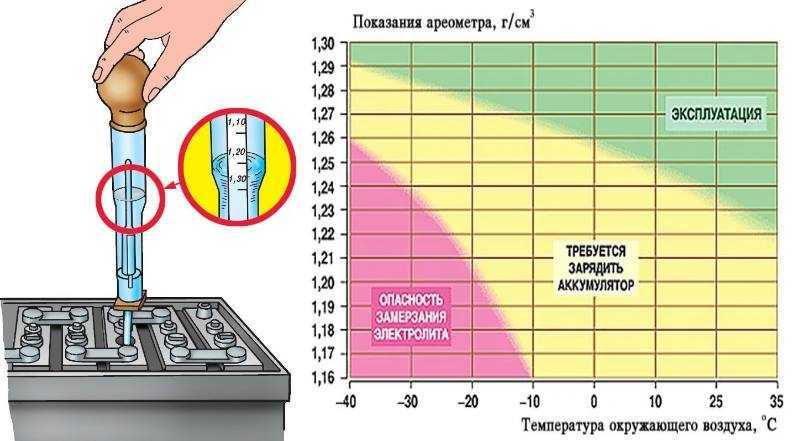
- Подготовить аккумулятор, выкрутить пробки из отверстий в крышках банок, либо снять общую планку с пробками на ней.
- Подготовить стеклянную банку или пластиковый сосуд с дистиллированной водой для промывки и продувки ареометра между замерами.
- Опустить носик прибора в банку аккумулятора до касания с пластинами сепаратора.
- Сжать грушу для выдавливания воздуха из колбы.
- Освободить грушу для принятия начальной формы и забора электролита из банки батареи в колбу.
- Наполнить колбу жидкостью так, чтобы поплавок всплыл.
- Отметить визуально уровень шкалы поплавка на границе поверхности электролита в колбе. Указанное на шкале значение соответствует плотности электролита.
- Выдавить жидкость обратно в банку батареи.
- Ареометр опустить в сосуд с дистиллированной водой и пару раз промыть остатки электролита в колбе путём нажатия и отпускания груши.
Следует добавить, что при помощи ареометра можно корректировать плотность электролита, добавляя дистиллированную воду или электролит плотностью 1,3 г/мл. по необходимости в банки и произведя измерения. Только для выравнивания плотности в банке требуется время после каждой добавки, а такую корректировку проводят на полностью заряженном аккумуляторе с температурой электролита около +25 °C.
по необходимости в банки и произведя измерения. Только для выравнивания плотности в банке требуется время после каждой добавки, а такую корректировку проводят на полностью заряженном аккумуляторе с температурой электролита около +25 °C.
Можно ли измерить без ареометра
Измерить плотность без ареометра не получится. Но можно изготовить ареометр самому, самым важным элементом которого является измерительный поплавок-грузик. Изготовить можно из полой пластиковой трубки, например соломинки для напитков, в которую помещается груз. Точность измерения будет зависеть от точности нанесения шкалы на грузик и известной плотности измеряемых эталонов жидкости. Сначала поплавок помещается в дистиллированную воду и отмечается линия окружности поверхности воды на поплавке. Эта линия соответствует 1,0 г/мл. Затем поплавок помещается в электролит, купленный в магазине с удельным весом, например, 1,3 г/мл. Линия поверхности электролита на поплавке будет соответствовать плотности 1,3 г/мл. Расстояние между двумя полученными значениями измеряется в мм и делится на разницу значений — 30. Теперь на поплавок можно нанести шкалу с любым шагом, но лучше для значений 1,27; 1,25; 1,23; 1,2; 1,15; 1,1.
Теперь на поплавок можно нанести шкалу с любым шагом, но лучше для значений 1,27; 1,25; 1,23; 1,2; 1,15; 1,1.
Отбор электролита можно произвести обычной резиновой грушей в стеклянный стакан, куда помещается изготовленный поплавок-грузик.
Самодельный ареометр из пластиковой трубки для соковМожно ли проверить плотность в необслуживаемом аккумуляторе
У необслуживаемых аккумуляторов нет откручиваемых пробок на банках. Однако при изготовлении батареи отверстия присутствуют. После заполнения электролитом эти отверстия закрываются одноразовыми пробками, иногда расположенными на общей планке, и запаиваются или заклеиваются. При необходимости можно аккуратно эти пробки снять, и аккумулятор превратится в обслуживаемую батарею. В некоторых случаях отверстия в месте расположения пробок выполняют при помощи сверла, что также позволяет произвести забор электролита и его корректировку.
Сверлятся отверстия 12 мм под резиновые пробки для аптечных пузырьковВажно в ходе таких действий заранее понимать, как после окончания обслуживания эти отверстия вновь надёжно закрыть. Это можно сделать с применением того же пластика, из которого изготовлен корпус батареи, или подобного. Пластик легко клеится, плавится и спаивается.
Это можно сделать с применением того же пластика, из которого изготовлен корпус батареи, или подобного. Пластик легко клеится, плавится и спаивается.
Если вскрыть необслуживаемую батарею удалось, то проверить плотность электролита в аккумуляторе можно так же, как описывалось выше.
Аккумулятор превратился в обслуживаемыйСейчас читают:
Способ определения плотности электролита свинцового аккумулятора
Использование: способ предназначен для определения плотности электролита свинцового аккумулятора. Сущность изобретения: при определении плотности учитывается отданная текущая емкость свинцового аккумулятора, коэффициент пропорциональности между приращением разрядной электрической емкости аккумулятора и приращением плотности электролита. Кроме того, учитывается уровень электролита, при ращение плотности электролита за счет самозаряда при 20 С. Текущую плотность электролита при разряде аккумулятора получают суммированием плотности электролига перед началом разряда и приращением плотности электролита за счет разряда и саморазряда аккумулятора.
СОЮЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИК (ф)5 Н 01 М 10/42
ОП И САН И Е ИЗО БР ЕТЕ Н И Я!К ABTOPCHOMY СВИДЕТЕЛЬСТВУ (Ю )>
ГОСУДАРСТВ Е Н Н ОЕ ПАТЕ НТНО Е
ВЕДОМСТВО СССР (ГОСПАТЕНТ СССР) (21) 4903277/07 (22) 18. 01.91 (46) 23 ° 11.92. Бюл. t,» 43 (72) 10.П.Найденко, М.Д.Маслаков и Ю.В.Скачков (56) Притулюк В.А. Химические источники тока в авиации. M,: Воениздат, 1976, с. 28-29.
Дасоян M.A, Химические источники тока, Л.: Энергия, 1969, с, 82, 83, 569.
Справочник химика, М.-Л.: Химия, 1964, с. 594.
Справочник по электрохимии./Под ред. Сухотина А.M. Л.: Химия, 1981, с. 115, Р
Сухотина А.M. Л.: Химия, 1981, с. 115, Р
Перельман В,И, Краткий справочник химика, M,: ГНТИ химической литературы, 1963, с. 405, Крайптон Т. Вторичные источники тока. M,: Мир, 1985, с, 175.
Устинов П.И, Стационарные аккумуляторные установки, M.: Энергия, 1970, с, 90.Изобретение относится к технике измерения, конкретно к способам измерения плотности свинцовых аккумуляторов (CA).
Известен способ определения плотности электролита СА с помощью ареометра (!).
Основными недостатками данного способа являются:
— низкая достоверность измерения, т,к. значения плотности электролита
„„5U „„1777190A1 (54) СПОСОБ ОПРЕДЕЛЕНИЯ ПЛОТНОСТИ
ЭЛЕКТРОЛИТА СВИНИОВОГО АККУМУЛЯТОРА (57) Использование: способ предназначен для определения плотности электролита свинцового аккумулятора. Сущность изобретения: при определении плотности учитывается отданная текущая емкость свинцового аккумулятора, коэффициент пропорциональности между приращением разрядной электрической емкости аккумулятора и приращением плотности электролита. Кроме того, учитывается уровень электролита, при ращение плотности электролита за счет о самозаряда при 20 С. Текущую плотность электролита при разряде аккумулятора получают суммированием плотности электролита перед началом разряда и приращением плотности электро. лита за счет разряда и саморазряда аккумулятора. 1 табл. в верхней части бака СА, откуда берут некоторое количество электролита для осуществления измерений, могут отличаться от значений плотности электролита, находящегося внутри &oка пластин СА, íà +0,05 г/смз в то время, как для практики требуется оценивать интегральную плотность электролита с большей точностью: — высокая трудоемкость, т,к. измерения осуществляются вручную, 1777190
Кроме того, учитывается уровень электролита, при ращение плотности электролита за счет о самозаряда при 20 С. Текущую плотность электролита при разряде аккумулятора получают суммированием плотности электролита перед началом разряда и приращением плотности электро. лита за счет разряда и саморазряда аккумулятора. 1 табл. в верхней части бака СА, откуда берут некоторое количество электролита для осуществления измерений, могут отличаться от значений плотности электролита, находящегося внутри &oка пластин СА, íà +0,05 г/смз в то время, как для практики требуется оценивать интегральную плотность электролита с большей точностью: — высокая трудоемкость, т,к. измерения осуществляются вручную, 1777190
Известен также способ определения плотности электролита при стоянке CA без тока, принятый в качестве прототипа, путем измерения установившегося значения ЭДС. E свинцового аккумулятора и определения плотности электролита по формуле (7):
d = E — 0,84 (г/смз) (1)
Пднако этот способ имеет методическую погрешность до 0,01 г/смз и не позволяет определять плотность электролита СА в процессе разряда, т,к, при разряде невозможно измерять
ЭДС, в то же время, контроль плотности электролита СА при разряде необходим, т,к. он позволяет оценивать состояние СА в процессе разряда, его остаточную емкость и выбирать оптимальный режим разряда.
он позволяет оценивать состояние СА в процессе разряда, его остаточную емкость и выбирать оптимальный режим разряда.
Целью изобретения является повышение точности, а также измерение плотности электролита в процессе разряда. 25
Сущность .изобретения состоит в том, что в режиме стоянки аккумулятора без тока измеряют его установившуюся ЭДС, но в отличие от прототипа, с целью повышения точности, а также измерения плотности электролита в процессе разряда, предваритель» но определяют:
— зависимость установившейся ЭпС
СА от плотности электролита, напри» мер, при 25 С, используя известную аналитическую зависимость (2), которая обеспечивает большую точность определения плотности электролита по установившейся ЭЛС, чем это достига- 4 ется в прототипе при использовании эмпирической формулы;
— изменение активности серной кис» лоты и воды в водных растворах электролитов при изменении температуры 45 на 10С
— коэффициенты пропорциональности между приращением, разрядной емкости аккумулятора и приращениями плотности электролита, а также поправку к ним, учитывающую влияние уровня электролита в аккумуляторе на указанные коэффициенты пропорциональности, — приращение плотности электролита о за счет саморазряда при 20 С, При измерении плотности, электролита в режиме стоянки аккумулятора без то» ка дополнительно измеряют температуру электролита, и, используя известные температурный коэффициент Э,пС (2, с, 83) и изменения активной серной кислоты и воды в водных растворах электролитов при изменении температуры на 1 С, вычисляют ЭРС аккумулятора при 25 С, после чего, используя зависимость установившейся ЭДС от плотности электролита при 25ОС, определяют плотность электролита при
25 С, а в процессе разряда измеря» ют ток разряда, время разряда, тем» пературу электролита, вычисляют от» данную аккумулятором емкость, прира -.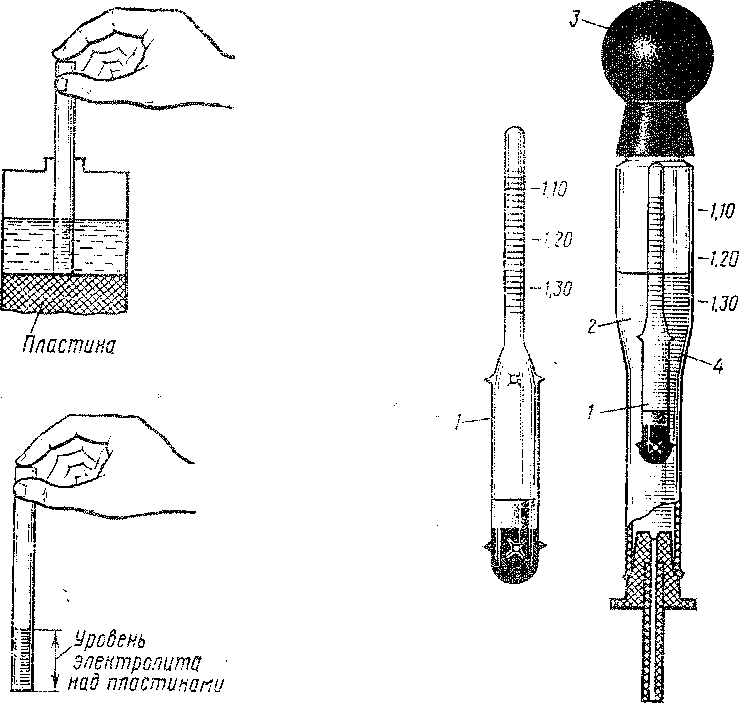 щение плотности электролита за счет .разряда аккумулятора, приращение плотности электролита за счет саморазряда при измеренной температуре, а текущую плотность электролита при разряде получают, суммируя плотность электролита перед началом разряда с приращениями плотности электролита за счет разряда и саморазряда.
щение плотности электролита за счет .разряда аккумулятора, приращение плотности электролита за счет саморазряда при измеренной температуре, а текущую плотность электролита при разряде получают, суммируя плотность электролита перед началом разряда с приращениями плотности электролита за счет разряда и саморазряда.
Для определения плотности электролита предложенным способом предварительно определяют зависимость установившейся ЭлС свинцового ак» кумулятора от плотности электролита, например, при 25 С, используя известную аналитическую зависимость, кото рая обеспечивает большую точность определения плотности электролита по установившейся ЭЛС
E=2,041+0,0591 lg — — — — — ) (2) а PaSO
a H O — активность воды в водных растворах электро» литов °
Из формулы (2) не просматривается связь между ЭДС и плотностью элект» ролита СА, Однако, такая связь существует, поскольку активности а Нз80 и а Н О зависят от концентрации и температуры электролита.
Таблицы, отражающие эти зависимости, приведены, например,,в ; (3) и в (4), а концентрация и температура ,однозначно определяют плотность электролита. В (3) с, 522 приводится таблица, связывающая концентра» цию с плотностью электролита при
В (3) с, 522 приводится таблица, связывающая концентра» цию с плотностью электролита при
20 С, в (5) даются поправки плотности в зависимости от температуры, Указанные данные в совокупности позволяют определить зависимость плот0 6
f000 P
m = — — — — -/
M(f00-P) 5 1777!9 ности электролита от установившейся
ЭДС .СА при известной температуре, Ниже приводится таблица, в которой по результатам анализа данных (л.3, 4, 5, 6) определена зависимость установившейся ЭЯС CA от плотности рао створа серной кислоты при 25 С.
Указанные в таблице эксперимено тальные значения ЭЛС Еахсп при 25 С и концентрации в массовых процентах взяты из,(л.3, с. 81), При этомконцентрация в массовых процентах пересчитана на мольную концентрацию (моль/1000 г растворителя) по изве- 15 стной (л. 4, с. 494) формуле: где тп — малярная концентрация! 20
P — концентрация в массовых процентах1
М вЂ” молекулярный вес растворен-. ного вещества (Н ЯО ), выполнены расчеты и получены остальные данные таблицы.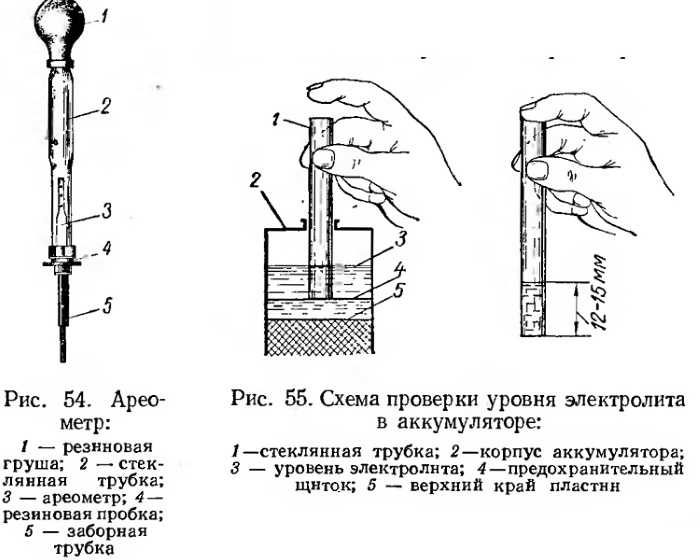 Если в таблице опустить первую строку, поскольку такие малые концентрации (плотности) в аккумуляторной практике не применяются, то погледний столбец указанной 30 таблицы показывает, что расчет плотности при стоянке CA без тока предложенным методом обеспечивает достаточно высокую точность, удовлетворяющую требованиям практики, 35
Если в таблице опустить первую строку, поскольку такие малые концентрации (плотности) в аккумуляторной практике не применяются, то погледний столбец указанной 30 таблицы показывает, что расчет плотности при стоянке CA без тока предложенным методом обеспечивает достаточно высокую точность, удовлетворяющую требованиям практики, 35
P предложенном способе предварительно определяют также. изменение активностей серной кислоты и воды в водных растворах электролитов при изменении температуры на 1 С. Это свя- 40 зано с предусмотренным в алгоритме, реализующем предложенный способ, пересчетом установившейся ЭДС с текущей
0 температуры на температуру 25 С. При разряде СА различными режимами от 45 одночасового до 75-часового плотность электролита d по окончании разряда изменяется в пределах от
1,210 до 1,029 г/смз при 25 С, что
— соответствует изменению молярной кон- 50 центрации m в пределах от 4,260 до
0,517 моль/1000 г, Как видно из (л.5.. с. 115) при концентрации 9,6
16 6 мас. 3, что соответствует m=1,08- .
3, что соответствует m=1,08- .
2,03 моль/1000 г, активность а Н О ц; в растворе серной кислоты практически не зависит от температуры. В диапазоне концентраций m = 4,260
0,517 моль/1000 r, которые имеют место по окончании разряда CA различными режимами, наиболее явно зависимость активности а Н О от температуры про»
2 о является при концентрации 28,3 мас.4 или 4,02 моль/1000 г, Такая концентрация электролита возможна после раз» ряда СА 1-часовым режимом. Но и в этом случае изменение активности а Н О на 1 С составляет менее 0,001, 2. что дает основание пренебречь им.
Таким образом, при разработке алгоритмов, реализующего предложенный способ, определения плотности электролита СА, принято допущение, что активность а Н О при тех концентрациях (плотностях) электролита, которые имеют место после окончания разряда различными режимами, не зависит от температуры.
Активность серной кислоты а Н БО при увеличении температуры уменьшается при всех концентрациях (плотностях), которые в практике эксплуатации СА имеет электролит (л. 4, с.594).
4, с.594).
Анализ изменения коэффициента активности у серной кислоты в функции температуры при тех концентрациях (плотностях) электролита, которые имеют место после разряда СА различными режимами, позволил установить, что для таких концентраций (плотнос» тей) при увеличении температуры на
1 С коэффициент активности серной кислоты уменьшается в 0,99 раз., Анализ изменения коэффициента активности серной кислоты в функции температуры в диапазоне концентраций (плотностей) электролита, которые имеют место в заряженном СА, позволил установить для таких концентраций (плотностей), что при увеличении температуры на 1 С уменьшается в о
0,98 раз.
Анализ изменения активности воды а Н О в функции температуры в диапазоне концентраций (плотностей) электролита, которые имеют место в заряженном СА позволил установить, что для таких концентраций (плотностей) при увеличении температуры на
1 С а Н О увеличивается в 0,9977раз.
Предложенный способ предусматривает также предварительное определение коэффициентов пропорциональности между приращениями разрядной емкости и приращениями плотности электролита.
Известно, что каждому ампер-часу количества электричества, отданному
С О где дд ñ
17771 о d сР если
1гв,1гР, к- к г о о
« К + t к-i., 2
t
Ip
6е
СА при разряде, соответствует расход
3,660 r серной кислоты и образование 0,672 г воды (л.2, с, 272-273), Однако получающееся при этом приращение плотности электролита, приведенное к одной температуре,, будет различаться в зависимости от начальной плотности электролита в момент начала разряда и его начального объема: чем больше начальная плотность электролита, тем меньше приращение плотности электролита.
Проведенные расчеты, например, для СА с площадью основания аккумуляторного бака внутри него, равной
2170 смг, с обьемом электролита 150 л, с измеряемым уровнем электролита над блоком пластин, равном 73 мм при 30 С, позволили получить следующие значе» ния коэффицяентов пропорциональности К: при d 25o 1 294, К = РР182 при 1,294 o d 25 f,246, К = 80833 при 1,246 > d 25 о. 1,208, К = 74615 25 при 1,208 ) d 25о 1,152, V = 89286: при 1,152 > д 25 = 1,089, К = 60625 при 1,089 ) d 25 K = 57059
1,208, К = 74615 25 при 1,208 ) d 25о 1,152, V = 89286: при 1,152 > д 25 = 1,089, К = 60625 при 1,089 ) d 25 K = 57059
На основе проведенных расчетов по-. лучено выражение для поправки P,ó÷è- 30 тывающей влияние высоты уровня электролита, как величины прямо пропорциональной обьему электролита на коэффициенты пропорциональности К указанных аккумуляторов: 35
P = (0 9982) 1 зо
rye h — высота уровня электролита, приведенная к температуре 30 С по из» 40 о вестной формуле:
h o = hg — 0,6(t- 30) мм, (6) где h — высота уровня электролита при температуре tС,, $5
t — измеренная температура, С.
Приращение плотности электролита за счет саморазряда определяется по результатам измерения плотности электролита в период стоянки СА без то- 5р ка, например, через каждые 24 ч и приводится к 20 С по формулам: о
2сг 4р 5 о о
d =gd — — — если t 730 С с. с о -20 о сР
20 ср 10
d =Ed с с t;-10 ср если 20 + с а 30 (á) о
tCf д5
d
d „, — плотность электролита о
У приведенная к 25 С, на конец предыдущих суток, — температура электролита на конец предыдущих суток.
Формулы (6) получены на основании (л,6, с. 175), где показано, что саморазряд СА после 20 С увеличива» о ется вдвое при каждом увеличении темо пературы на 10 С.
При определении плотности элект» ролита предложенным способом в период стоянки СА без тока измеряют установившуюся ЭДС, например, цифровым вольтметром, обеспечивающим измерение ЗДС, с четырьмя знаками после запятой, измеряют температуру электролита, например, с помощью термопреобразователя сопротивления, и, используя известный температурный коэффициент ЭДС,равный 0,00136 В/град (л.3, с. 83), а также предварительно полученные изменения активности серной кислоты и воды в водных растворах электролитов при изменении темпера» о туры на 1 С, вычисляют ЭРС аккумуляо тора при 25 С, после чего, используя предварительно полученную зависимость установившейся ЭДС от плотности электролита при 25 С (см, таблицу), определяют плотность электролита при
25 С, При определении плотности электролита в процессе разряда измеряют ток разряда, время разряда, температуру электролита, вычисляют отданную аккумулятором емкость по формулам:
СР IP ht, (7) приращение разрядной емкости, величина тока разряда, const — временной интервал измерения тока, 1777190
Л
C к (10) 30
1! у Cp d = d — > — у к
Š— 0,84, 35
5О ао (Мс
С,=КАС, (8) где С — отданная аккуиуляторои емP кость на текущий момент времени разряда. 5
5
Имея значения плотности электролита перед включением аккумулятора на разряд, выбирают в соответствии с нею коэффициент пропорциональности К, пересчитывают уровень электролита после последнего заряда, измеренный при температуре t на 30 С, по фор» муле (6), вычисляют поправку f5, учитывающую влияние уровня электролита в аккумуляторе на коэффициент пропор15 циональности К по формуле (5), вычисляют новое значение коэффициента
К пропорциональности К по фориуле
К =К (o) 20 вычисляют приращение плотности элек- тролита за счет разряда аккумулятора по формуле и текущую плотность электролита при
25 С по формуле: о где d — плотность электролита перед
1 началом разряда, измеренная при стоянке CA без тока.
Вычисляют приращение плотности электролита за счет саморазряда, для, чего предварительно вычисленное при-ращение плотности электролита за счет саморазряда при 20 С пересчитывают на текущую температуру по формулам: о йР t-20 о
Дс1 = ДЙ вЂ” — если t 730 С
С С
2оо t-10
Дй =Ad
10 если 20 (t
1о lgp0 о
Дс1с = hdс ecole t c 20 С вычисляют часовой саморазряд по формуле: после часа разряда опять вычисляют . 55 часовой саиоразряд для текущей температуры по формуле: о ц Лспо
55 часовой саиоразряд для текущей температуры по формуле: о ц Лспо
q — °
24 (14) По данным часового разряда для начала и по окончании каждого часа разряда вычисляют по формуле средний самора зряд за час
q = (q +q )/2 (15) и через каждый час разряда q сумми» руют и с плотностью электролита, по-. лученной по фориуле (11), Проведенная опытная проверка способа показала, что он обеспечивает высокую точность определения плотности электролита при стоянке СА без тока и в процессе разряда.
Использование предложенного способа повышает точность определения плот-: ности электролита СА при стоянке без тока и в процессе разряда, упрощает осуществление контроля плотности электролита СА, создает предпосылки для его автоматизации с использованием вычислительной техники.
Формула изобретения
Способ определения плотности элек» тролита свинцового аккумулятора в режиме стоянки его без тока путеи из» иерения установившегося значения ЭпС и вычисления плотности электролита по формуле где d — плотность электролита при
+15 С, E — установившееся значение ЭРС свинцового аккумулятора, отличающийся . теи, что, с целью повышения точности, а также измерения плотности электролита в процессе разряда, предварительно определяют зависимость установившейся
теи, что, с целью повышения точности, а также измерения плотности электролита в процессе разряда, предварительно определяют зависимость установившейся
ЭПС свинцового аккумулятора от плотности электролита при 25 С, изменение активности серноЙ кислоты и воды в водном растворе серной кислоо ты при изменении температуры на 1 С,. коэффициенты пропорциональности меж ду приращениями разрядной электрической емкости аккумулятора и приращениями плотности электролита, а также поправку к ним, учитывающую влияние уровня электролита на указанные коэффициенты пропорциональности, приращение плотности электролита за счет саиоразряда при 20 С, при определении плотности электролита измеряют установившуюся ЭДС ак11 1 кумулятора при стоянке его без тока, температуру электролита и, используя температурный коэффициент.3РО
0,00136 В/град и предварительно полученные изменения активностей серной кислоты и воды в водном растворе серной кислоты при изменении температуры на 1 С, вычисляют ЭДС аккумулятора при 25 С, после чего,используя зависимость установившейся
ЭДС от плотности электролита при
25 С, определяют плотность электро- лита при 25 С, а в процессе разряда измеряют ток разряда, время разряда, 777190 12 температуру электролита, вычисляют отданную аккумулятором электрическую емкость, приращение плотности электролита за счет разряда аккумулятора, приращение плотности электролита за счет саморазряда при измеренной (текущей) температуре, а текущую плотность электролита при разряде аккуму» лятора получают суммированием плотности электролита перед началом разряда и приращений плотности электролита за счет разряда и саморазряда аккумулятора, 15
1 р
r/сма при
25 С
P) г/сма при
29оС
М температура поправки плОТИОсти эмса
В
ЭДС расхождение с Е „ „, 2; моль/
1000 r раста.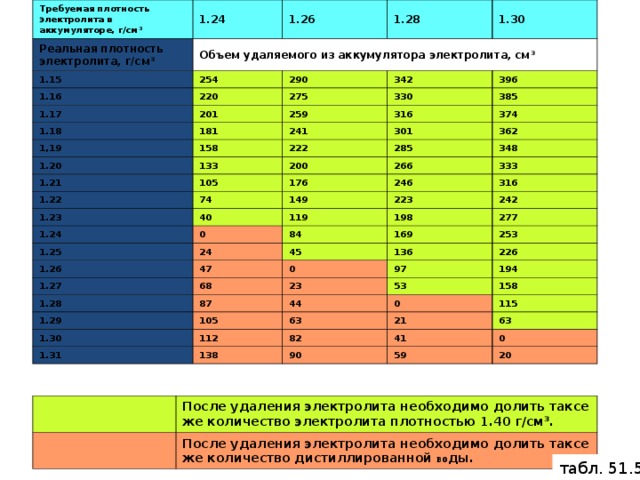 а Н,О
а Н,О
Ер ц у
В
ЭДС а l1 O 4 „,э;т+ при 25РС
1,281
7,61
0,00029 о,oo189
0,00903
0,06648
0,3086
1,2616
4, 5216
14,583
48,573
117,785
0,56
0,08
0,05
0,03
7519
0,01
0,01
0,06
0,02
0,04
0,09
0,04
Составитель И,Найденко
Редактор Т,Куркова Техред И,Моргентал Корректор й.Тупица
Заказ 11125 Тираж Подписное
ВНИИПЯ. Государственного комитета по изобретениям и открытиям при ГКНТ СССР
113035, Москва, Ж-35, Раушская наб., д. 4/5
Производственно-издательский комбинат «Патент», r.Óæãîðîä, ул. Гагарина, 101
090502
0,1006
0 1999 о 5
0,997
2,000
2>9939
4,004
5,006
5,9956
7,0077
8,0000
1, 0016
i 0o5
1,0112
l, O5P7
1,1124
1,1606
1,2038
1,2425
1, 2773
1,3090
1 3381
0,0002
0,0002
0,0002
0,00027
0,00036 о,ooo51
0,00062
0300068
0,00071
0,00073 о,ооо74
0 00076
1,0006
1,004
1,01
1,028
1,057
1,!1
1,15Р, 1, 200
l,239
1,274
1,305
1,334
0,9981
0,9963
0,9928
0,9819
0,9618
0,9126 о,Р516
0,7799
0,7032
0,6259
0,5509
0,4814
1, 7977 l, 8321
1,8805
1«9192
1,9738
2,0149
2э0533
2,0888
2, 1218
2 156
2, 1822
1,76183
1, 79625
1,83122
l,88102
1,91à45
1 97099
2 01370
2ю05289.
2,08974
2, 12368
2,15504
Копия смешивания электролитов на 360º — iQ International AG
iQ International — технологический лидер в области заливных стартерных аккумуляторов со смешиванием электролитов, единственное на рынке круговое смешивание электролитов на 360°. Эта отмеченная наградами технология является первым значительным достижением в области залитых стартерных аккумуляторов за последние десятилетия.
Инновационная технология предотвращает первую причину выхода из строя аккумуляторов: кислотное расслоение. Круговое смешивание электролитов на 360° предотвращает разрушительное расслоение кислоты в любой залитой стартерной батарее, обеспечивая однородный электролит, необходимый для долговременной работы батареи за счет более высокого коэффициента использования материала.
Преимущества технологии перемешивания 360° против расслоения
Двойной срок службы. Отсутствие потерь мощности (Ач) из-за вредного кислотного расслоения.
Отсутствие потерь мощности (Ач) из-за вредного кислотного расслоения.
Смешивание на 360° устраняет расслоение кислоты, обеспечивая при этом непрерывную производительность с высокой емкостью (Ач), которую мы называем Sustained Capacity™. Полное смешивание электролитов обеспечивает лучшую производительность стандартных залитых аккумуляторов и усовершенствованных залитых аккумуляторов (EFB), используемых в системах Start-Stop. Эти аккумуляторы отвечают растущим требованиям использования электроэнергии в современных автомобилях.
Смешивание на 360° обеспечивает:
Высокая способность перезарядки; Значительно меньше сульфатации; Значительно меньше износ. Смешивание на 360° идеально подходит для аккумуляторов, используемых в зонах с жарким и холодным климатом, для тяжелых условий эксплуатации в такси и автопарках, а также оптимален для аккумуляторов с большим сроком службы в транспортных средствах с функцией Start-Stop и другими микрогибридными технологиями.
Универсальный
Система смешивания 360° работает от автомобильных и грузовых аккумуляторов. Детали подходят для всех обычных аккумуляторных ящиков и аккумуляторных ящиков типа EFB, соответствующих всем отраслевым стандартам (например, DIN, JIS, BCI). Установка выполняется быстро и легко, а сборка на производственной линии может быть автоматизирована или выполняться вручную.
Действует
Смешивание на 360° — это пассивное устройство, функционирующее независимо от установки аккумулятора в транспортном средстве (спереди/сзади) и направления установки (продольно/поперечно). 30-минутной поездки достаточно для полной циркуляции объема электролита. Система работает даже при более низком уровне жидкости, вызванном разным потреблением воды в аккумуляторе.
Простота внедрения
Внедрение технологии смешивания 360° в любое предприятие по производству аккумуляторов может быть осуществлено с минимальными капиталовложениями. Благодаря своей универсальной конструкции компоненты смешивания 360° могут быть включены в любую залитую батарею и установлены на существующей сборочной линии производственного предприятия. Это обеспечивает гибкость для быстрого внедрения продуктов премиум-класса с двойным циклом и сроком службы или с сопоставимыми характеристиками по более низкой цене.
Это обеспечивает гибкость для быстрого внедрения продуктов премиум-класса с двойным циклом и сроком службы или с сопоставимыми характеристиками по более низкой цене.
Лучшее использование материалов
Смесительные батареи 360º обеспечивают более высокую устойчивую производительность и более длительный срок службы из того же количества сырья и природных ресурсов по сравнению с обычными или усовершенствованными залитыми батареями.
360° Смешивание электролитов работает без движущихся частей.
Запатентованная технология защиты от расслоения iQ International не имеет движущихся частей. Он использует силы, создаваемые движением автомобиля, для циркуляции электролита внутри аккумулятора. Кинетическая энергия от ускорения, торможения или прохождения поворотов создает гидростатическое давление (насос), которое обеспечивает полную циркуляцию электролита по всему аккумулятору.
Демонстрация циркуляции электролита на 360° с предшествующей системой смешивания.

На видео показана эффективность смешивания при вождении конструкции 360° ранней стадии (справа) по сравнению с поведением обычного элемента батареи (слева).
360° Electrolyte Mixing
Отмеченная наградами инновация
Наша технология 360° Electrolyte Mixing — инновация, отмеченная многочисленными наградами. Он был удостоен первой премии Франкфуртской премии Automechanika Innovation Award в 2010 году, а также стал обладателем золотой медали GreenTec Awards 2017 в Берлине. GreenTec — самая престижная европейская награда за экологические инновации.
Кислотное расслоение — причина № 1 преждевременного выхода батареи из строя.
С увеличением числа потребителей электроэнергии в транспортных средствах стало известно о явлении, которому до недавнего времени уделялось мало внимания: кислотное расслоение. Сегодня кислотное расслоение является причиной номер один преждевременного выхода аккумуляторов из строя.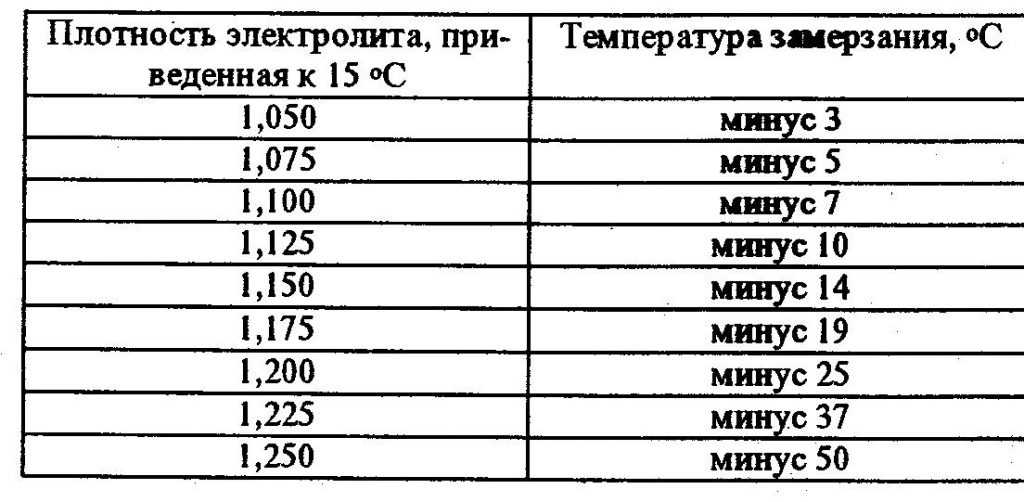
У полностью заряженного нового аккумулятора без расслоения плотность кислоты составляет от 1,26 кг/л до 1,28 кг/л в зависимости от климата и области применения. При разрядке серная кислота химически поглощается оксидом свинца пластин аккумулятора. Плотность падает, а более легкий электролит движется вверх. При перезарядке происходит обратный процесс: у поверхностей пластин выделяется концентрированная серная кислота до 1,80 кг/л. Поскольку плотность этой кислоты больше, она оседает на дно батареи, где со временем образует вертикальный градиент плотности в электролите.
Несбалансированность плотности электролита приводит к ранней потере емкости аккумулятора до 40% от номинального значения и, как следствие, к падению работоспособности аккумулятора и преждевременному выходу из строя аккумулятора. Внешние температуры (холод, жара) также сильно влияют на химический процесс и вызывают раннее утомление.
Запатентованная iQ International технология перемешивания электролитов на 360° устраняет эти серьезные недостатки.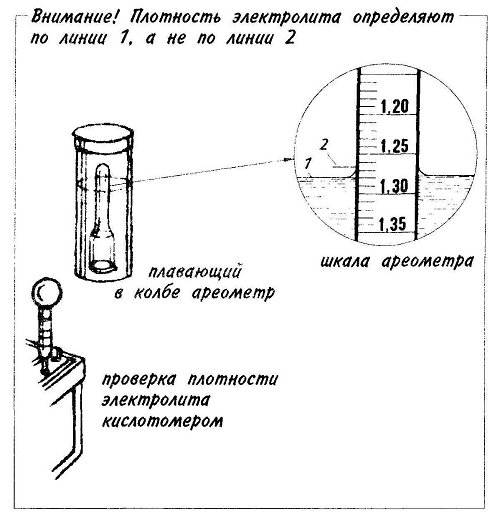
Замена обычных добавок к электролиту для аккумуляторов производными диоксолона для литий-ионных аккумуляторов с высокой плотностью энергии
. 2021 5 февраля; 12 (1): 838.
doi: 10.1038/s41467-021-21106-6.
Парк Севон 1 , Со Ён Чжон 2 , Тэ Гён Ли 1 3 , Пак Мин Ву 1 , Хён Ён Лим 1 , Джэкён Сон 1 , Джефил Чо 1 , Санг Гю Квак 4 , Сун Ю Хонг 5 , Нам-Сун Чой 6
Принадлежности
- 1 Школа энергетики и химической инженерии, Ульсанский национальный институт науки и технологий (UNIST), Ульсан, Республика Корея.

- 2 Химический факультет, Ульсанский национальный институт науки и технологий (UNIST), Ульсан, Республика Корея.
- 3 Отдел исследований фотогальваники, Корейский институт энергетических исследований (KIER), Тэджон, Республика Корея.
- 4 Школа энергетики и химического машиностроения, Ульсанский национальный институт науки и технологий (UNIST), Ульсан, Республика Корея. [email protected].
- 5 Химический факультет, Ульсанский национальный институт науки и технологий (UNIST), Ульсан, Республика Корея. [email protected].
- 6 Школа энергетики и химического машиностроения, Ульсанский национальный институт науки и технологий (UNIST), Ульсан, Республика Корея.
 [email protected].
[email protected].
- PMID: 33547320
- PMCID: PMC7864909
- DOI: 10.1038/с41467-021-21106-6
Бесплатная статья ЧВК
Севон Парк и др. Нац коммун. .
Бесплатная статья ЧВК
. 2021 5 февраля; 12 (1): 838.
doi: 10.1038/s41467-021-21106-6.
Авторы
Парк Севон 1 , Со Ён Чжон 2 , Тэ Гён Ли 1 3 , Пак Мин Ву 1 , Хён Ён Лим 1 , Джэкён Сон 1 , Джефил Чо 1 , Санг Гю Квак 4 , Сун Ю Хонг 5 , Нам-Сун Чой 6
Принадлежности
- 1 Школа энергетики и химической инженерии, Ульсанский национальный институт науки и технологий (UNIST), Ульсан, Республика Корея.

- 2 Химический факультет, Ульсанский национальный институт науки и технологий (UNIST), Ульсан, Республика Корея.
- 3 Отдел исследований фотогальваники, Корейский институт энергетических исследований (KIER), Тэджон, Республика Корея.
- 4 Школа энергетики и химического машиностроения, Ульсанский национальный институт науки и технологий (UNIST), Ульсан, Республика Корея. [email protected].
- 5 Химический факультет, Ульсанский национальный институт науки и технологий (UNIST), Ульсан, Республика Корея. [email protected].
- 6 Школа энергетики и химического машиностроения, Ульсанский национальный институт науки и технологий (UNIST), Ульсан, Республика Корея.
 [email protected].
[email protected].
- PMID: 33547320
- PMCID: PMC7864909
- DOI: 10.1038/с41467-021-21106-6
Абстрактный
Межфазные фазы твердого электролита, образованные с использованием добавок к электролиту, являются ключевыми для взаимодействия анод-электролит и увеличения срока службы литий-ионных аккумуляторов. Классические межфазные добавки к твердому электролиту, такие как виниленкарбонат и фторэтиленкарбонат, имеют ограниченный потенциал для одновременного достижения длительного срока службы и быстрой зарядки в литий-ионных батареях с высокой плотностью энергии (LIB). Здесь мы сообщаем о синтетическом аддитивном подходе следующего поколения, который позволяет формировать высокостабильную архитектуру интерфейса электрод-электролит из фторированных и силилированных добавок к электролиту; он выдерживает вызванное литированием объемное расширение кремниевых анодов и обеспечивает ионные каналы для легкого транспорта литий-иона, защищая при этом богатый никелем LiNi 0,8 Co 0,1 Mn 0,1 O 2 катоды. Ретросинтетически разработанные твердоэлектролитные межфазные присадки 5-метил-4-((трифторметокси)метил)-1,3-диоксол-2-он и 5-метил-4-((триметилсилилокси)метил)-1,3- диоксол-2-он обеспечивают пространственную гибкость межфазной поверхности твердого электролита, полученного из виниленкарбоната, за счет полимерного распространения с виниловой группой виниленкарбоната. Архитектура интерфейса из синтезированной добавки типа виниленкарбоната позволяет создавать ЛИА с высокой плотностью энергии с сохранением емкости 81,5% после 400 циклов при 1 °C и возможностью быстрой зарядки (1,9% снижения емкости после 100 циклов при 3°С).
Ретросинтетически разработанные твердоэлектролитные межфазные присадки 5-метил-4-((трифторметокси)метил)-1,3-диоксол-2-он и 5-метил-4-((триметилсилилокси)метил)-1,3- диоксол-2-он обеспечивают пространственную гибкость межфазной поверхности твердого электролита, полученного из виниленкарбоната, за счет полимерного распространения с виниловой группой виниленкарбоната. Архитектура интерфейса из синтезированной добавки типа виниленкарбоната позволяет создавать ЛИА с высокой плотностью энергии с сохранением емкости 81,5% после 400 циклов при 1 °C и возможностью быстрой зарядки (1,9% снижения емкости после 100 циклов при 3°С).
Заявление о конфликте интересов
Авторы заявляют об отсутствии конкурирующих интересов.
Цифры
Рис. 1. Синтез функциональных производных ВК…
1. Синтез функциональных производных ВК…
Рис. 1. Синтез функциональных производных ВК и превращение добавок в форму СЭИ на…
a Синтез DMVC-OTMS и DMVC-OCF 3 . b Электрохимические превращения производных ДМВК. одноэлектронный перенос SET, NBS N -бромсукцинимид, AIBN азобисизобутиронитрил, 1,2-DCE 1,2-дихлорэтан, TEA триметиламин, MeCN ацетонитрил; Этилацетат EtOAc. c Разработка деформируемого и стабильного SEI с использованием VC, DMVC-OCF 3 и DMVC-OTMS на аноде Si–C.
Рис. 2. Уникальные особенности DMVC-OCF 3…
Рис. 2. Уникальные возможности DMVC-OCF 3 , DMVC-OTMS и VC для построения стабильного интерфейса…
2. Уникальные возможности DMVC-OCF 3 , DMVC-OTMS и VC для построения стабильного интерфейса…
Регистрация…
Рис. 2. Уникальные возможности DMVC-OCF 3 , DMVC-OTMS и VC для построения стабильных межфазных слоев.Включение DMVC-OCF 3 и DMVC-OTMS в каркас VC приводит к созданию гибкого и прочного SEI на аноде Si-C. DMVC-OTMS поглощает HF и дезактивирует PF 5 , что приводит к стабильности состава и структуры межфазных слоев на электродах. Фрагмент Me (-CH 3 ), связанный с каркасом VC, обеспечивает ионные каналы, обеспечивая пространство для транспорта литий-иона в SEI.
Рис. 3. Энергетические уровни LUMO растворителя…
Рис. 3. Энергетические уровни НСМО растворителя и добавок и свободные энергии Гиббса для…
 3. Энергетические уровни НСМО растворителя и добавок и свободные энергии Гиббса для восстановления добавок и полимеризации добавок.
3. Энергетические уровни НСМО растворителя и добавок и свободные энергии Гиббса для восстановления добавок и полимеризации добавок. a Уровни энергии LUMO EC, VC, DMVC-OCF 3 и DMVC-OTMS. Обратите внимание, что изозначение орбитали составляет 0,02 e / Å 3 . b – d Пути реакции разложения ДМВХ-ОКФ 3 путем одноэлектронного восстановления ( b ), разложения аниона ОКФ 3 ( c ) и радикальной полимеризации ДМВХ с VC, DMVC-OCF 3 и DMVC-OTMS ( d ). Обратите внимание, что относительные свободные энергии Гиббса (Δ G ) рассчитаны при 1 атм и 298 К. ΔΔ G rxn в цветных прямоугольниках указывает на разницу в Δ G с между продуктом и реагентом тримеризации, которая представляет собой теплоту реакции при тримеризации. реакции радикала DMVC + димера VC с VC, DMVC-OCF 3 или DMVC-OTMS. Для молекулярных структур в цветных прямоугольниках атомы водорода опущены для ясности.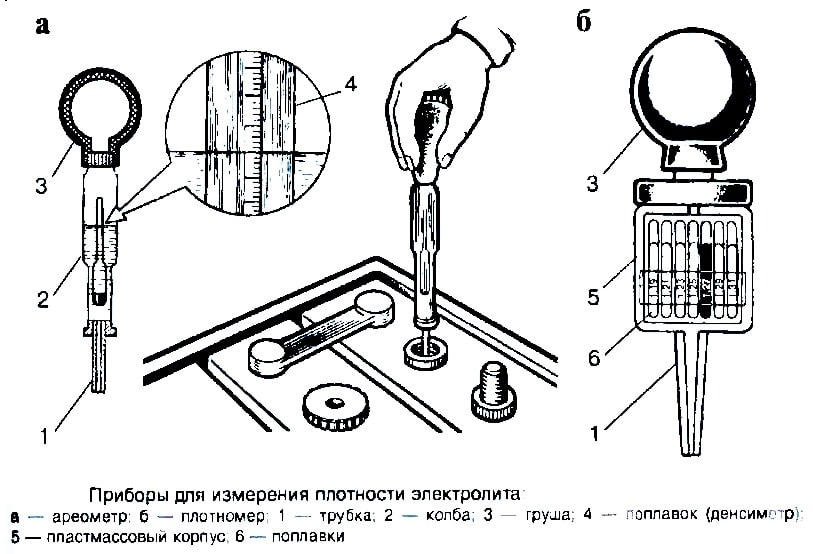
Рис. 4. Электрохимические характеристики синтезированных функциональных…
Рис. 4. Электрохимические характеристики синтезированных функциональных добавок и способность к быстрой зарядке.
a d Q…
Рис. 4. Электрохимические характеристики синтезированных функциональных добавок и способность к быстрой зарядке. a d Q /d V график полных элементов NCM811/Si-C. (Без добавок: 1,15 M LiPF 6 в EC/EMC (3/7, об./об.)) b Профили заряда GITT и ИК-падение полных элементов NCM811/Si–C. c Циклическая характеристика полных элементов NCM811/Si–C при 1 C и 25 °C. d – f Профили напряжения полных элементов NCM811/Si–C при температуре 1 C и 25 °C с электролитом, содержащим FEC ( d ), электролитом, содержащим VC ( e ), и VC + DMVC- ОКФ 3 + DMVC-OTMS, содержащий электролит ( f ) на 1-м, 300-м, 350-м и 400-м циклах.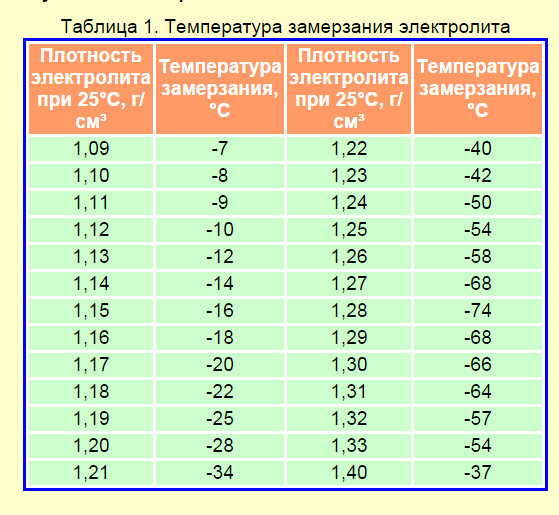 г Скорость заряда полных элементов NCM811/Si-C при скорости разряда 1 C. ч Цикл быстрой зарядки (1 C и 3 C) полных элементов NCM811/Si-C при скорости разряда 1 C при 25 °C. i Рентгенограммы и фотографии анодов Si-C, заряженных (литированных) при температуре 5 C.
г Скорость заряда полных элементов NCM811/Si-C при скорости разряда 1 C. ч Цикл быстрой зарядки (1 C и 3 C) полных элементов NCM811/Si-C при скорости разряда 1 C при 25 °C. i Рентгенограммы и фотографии анодов Si-C, заряженных (литированных) при температуре 5 C.
Рис. 5. ТЭМ-характеристика Si…
Рис. 5. ПЭМ-характеристика нанослоев Si анодов Si–C после предциклирования NCM811/Si–C…
a – c ПЭМ-изображения и результаты картирования ЭДС (розовый: кремний, зеленый: углерод и синий: кислород) нанослоя кремния исходного Si–C ( a ), Si–C, предварительно обработанный в электролите с добавлением VC ( b ), и VC + DMVC-OCF 3 + DMVC-OTMS с добавлением электролита ( c ). d – f Линейный EDS-взвешенный профиль чистого Si–C ( d ), Si–C, предварительно обработанного электролитом, содержащим VC ( e ), и VC + DMVC-OCF 3 + DMVC- OTMS, содержащий электролит ( f ). г Тенденция модуля Юнга нанослоя Si анода Si-C при циклировании полных ячеек NCM811/Si-C.
d – f Линейный EDS-взвешенный профиль чистого Si–C ( d ), Si–C, предварительно обработанного электролитом, содержащим VC ( e ), и VC + DMVC-OCF 3 + DMVC- OTMS, содержащий электролит ( f ). г Тенденция модуля Юнга нанослоя Si анода Si-C при циклировании полных ячеек NCM811/Si-C.
Рис. 6. РФЭС-спектры анодов Si–C…
Рис. 6. РФЭС-спектры анодов Si–C и катодов NCM811 после предциклирования.
и С 1…
Рис. 6. РФЭС-спектры анодов Si–C и катодов NCM811 после предциклирования. а С 1 с , О 1 s и F 1 s для анодов Si–C после предциклирования полных ячеек NCM811/Si–C с VC + DMVC-OCF 3 + DMVC-OTMS и VC. b , O 1 s , F 1 s , P 2 p для катодов NCM811, полученных из полных ячеек NCM811/Si-C после предциклирования в VC + DMVC-OCF 3 OTMS и ВК.
b , O 1 s , F 1 s , P 2 p для катодов NCM811, полученных из полных ячеек NCM811/Si-C после предциклирования в VC + DMVC-OCF 3 OTMS и ВК.
Рис. 7. СЭМ и ТЭМ характеристики…
Рис. 7. СЭМ и ПЭМ характеристики анодов Si–C после 400 циклов полного цикла NCM811/Si–C…
a – f Морфология поверхности исходного анода Si-C ( a ) и анодов Si-C, полученных из полных ячеек NCM811/Si-C, подвергнутых 400 циклам при 25 °C с VC ( b ) или VC + DMVC-OCF 3 + DMVC-OTMS ( c ), виды поперечного сечения исходного анода Si-C ( d ) и анодов Si-C из NCM811/Si-C полные клетки, подвергнутые циклу в течение 400 циклов при 25 °C с VC ( e ) или VC + DMVC-OCF 3 + DMVC-OTMS ( f ).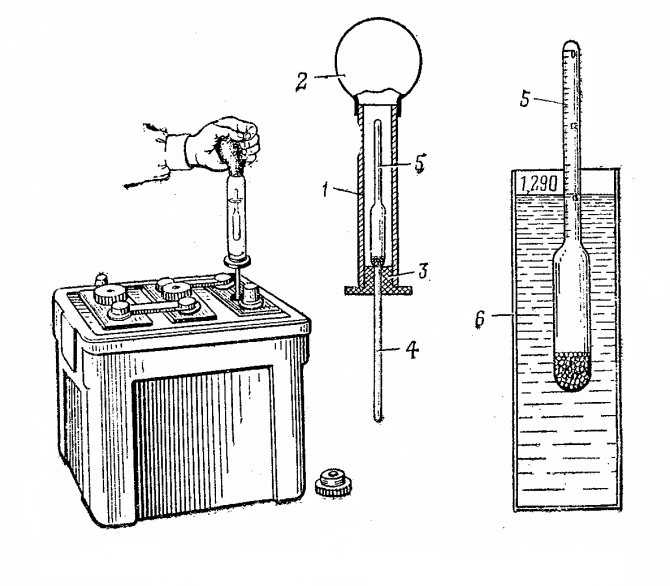 г – i Картирование ЭДС в ПЭМ исходного Si-C анода ( г ) и Si-C анодов после 400 циклов с ВК ( ч ) или ВК + ДМВХ-ОКФ 3 -+ ОТМС ( и ).
г – i Картирование ЭДС в ПЭМ исходного Si-C анода ( г ) и Si-C анодов после 400 циклов с ВК ( ч ) или ВК + ДМВХ-ОКФ 3 -+ ОТМС ( и ).
См. это изображение и информацию об авторских правах в PMC
Похожие статьи
Построение низкоимпедансного интерфейса на высоковольтном катоде LiNi 0,8 Co 0,1 Mn 0,1 O 2 с 2,4,6-трифенилбороксином в качестве пленкообразующей добавки к электролиту для литий-ионных аккумуляторов.
Ли Г., Ляо И., Ли З., Сюй Н., Лу И., Лан Г., Сунь Г., Ли В. Ли Г и др. Интерфейсы приложений ACS. 2020 авг 19;12(33):37013-37026. дои: 10.1021/acsami.0c05623. Epub 2020 10 августа. Интерфейсы приложений ACS. 2020. PMID: 32700895
Двухфункциональные добавки к электролиту для литий-ионных аккумуляторов с длительным циклом работы: экологически безопасные производные карбоната.

Хан Дж.Г., Хван Э., Ким И., Пак С., Ким К., Ро Д.Х., Гу М., Ли С.Х., Квон Т.Х., Ким И., Чой Н.С., Ким Б.С. Хан Дж.Г. и др. Интерфейсы приложений ACS. 2020 27 мая;12(21):24479-24487. дои: 10.1021/acsami.0c04372. Эпаб 2020 15 мая. Интерфейсы приложений ACS. 2020. PMID: 32368903
Микроразмерная сурьма в качестве стабильного анода во фторэтиленкарбонатсодержащих электролитах для перезаряжаемых литий-/натрий-ионных аккумуляторов.
Бянь Х, Донг И, Чжао Д, Ма Х, Цю М, Сюй Дж, Цзяо Л, Ченг Ф, Чжан Н. Биан X и др. Интерфейсы приложений ACS. 2020 22 января; 12 (3): 3554-3562. дои: 10.1021/acsami.9б18006. Epub 2020 10 января. Интерфейсы приложений ACS. 2020. PMID: 31886641
Регулирование электролита в отношении стабильных литий-металлических анодов в литий-серных батареях с сульфурированными катодами из полиакрилонитрила.

Chen WJ, Li BQ, Zhao CX, Zhao M, Yuan TQ, Sun RC, Huang JQ, Zhang Q. Чен В.Дж. и соавт. Angew Chem Int Ed Engl. 2020 26 июня; 59 (27): 10732-10745. doi: 10.1002/anie.201912701. Epub 2020 1 апр. Angew Chem Int Ed Engl. 2020. PMID: 31746521 Обзор.
Регулирование межфазного взаимодействия катод-электролит с помощью электролитных добавок в литий-ионных батареях.
Wang XT, Gu ZY, Li WH, Zhao XX, Guo JZ, Du KD, Luo XX, Wu XL. Ван XT и др. Chem Asian J. 2020, 15 сентября; 15 (18): 2803-2814. doi: 10.1002/asia.202000522. Epub 2020 7 июля. Химическая Азия Дж. 2020. PMID: 32543733 Обзор.
Посмотреть все похожие статьи
Цитируется
SiO x микронного размера — графитовое соединение в качестве анодных материалов для коммерческих литий-ионных аккумуляторов.
Джо М, Сим С, Ким Дж, О П, Сон Ю. Джо М и др. Наноматериалы (Базель). 2022 7 июня; 12 (12): 1956. doi: 10.3390/nano12121956. Наноматериалы (Базель). 2022. PMID: 35745295 Бесплатная статья ЧВК.
Si@MnO 2 @rGO, подобный морскому ежу, в качестве анодов для высокоэффективных литий-ионных аккумуляторов.
Лю Дж., Ван М., Ван Ц., Чжао С., Сун Ю., Чжао Т., Сунь Дж. Лю Дж. и др. Наноматериалы (Базель). 2022 17 января; 12 (2): 285. doi: 10.3390/nano12020285. Наноматериалы (Базель). 2022. PMID: 35055301 Бесплатная статья ЧВК.
использованная литература
- Goodenough JB, Kim Y. Проблемы литиевых перезаряжаемых батарей. хим. Матер. 2010; 22: 587–603. doi: 10.1021/cm2z.
 —
DOI
—
DOI
- Goodenough JB, Kim Y. Проблемы литиевых перезаряжаемых батарей. хим. Матер. 2010; 22: 587–603. doi: 10.1021/cm2z.
- Tarascon JM, Armand M. Проблемы и проблемы, с которыми сталкиваются перезаряжаемые литиевые батареи. Природа. 2001;414:359–367. дои: 10.1038/35104644. — DOI — пабмед
- Арико А.С., Брюс П., Скросати Б., Тараскон Дж.М., ван Шалквейк В. Наноструктурные материалы для передовых устройств преобразования и хранения энергии.
 Нац. Матер. 2005; 4: 366–377. DOI: 10.1038/nmat1368.
—
DOI
—
пабмед
Нац. Матер. 2005; 4: 366–377. DOI: 10.1038/nmat1368.
—
DOI
—
пабмед
- Арико А.С., Брюс П., Скросати Б., Тараскон Дж.М., ван Шалквейк В. Наноструктурные материалы для передовых устройств преобразования и хранения энергии.
- Лю С., Ли Ф., Ма Л.П., Ченг Х.М. Передовые материалы для хранения энергии. Доп. Матер. 2010;22:E28–E62. doi: 10.1002/adma.200
8. — DOI — пабмед
- Лю С., Ли Ф., Ма Л.П., Ченг Х.М. Передовые материалы для хранения энергии. Доп. Матер. 2010;22:E28–E62. doi: 10.1002/adma.200
- Че С.
 , Чой С.Х., Ким Н., Сун Дж., Чо Дж. Интеграция графитовых и кремниевых анодов для коммерциализации литий-ионных аккумуляторов высокой энергии. Ангью. хим. Междунар. Эд. 2019;58:2–28. doi: 10.1002/anie.201813331.
—
DOI
—
пабмед
, Чой С.Х., Ким Н., Сун Дж., Чо Дж. Интеграция графитовых и кремниевых анодов для коммерциализации литий-ионных аккумуляторов высокой энергии. Ангью. хим. Междунар. Эд. 2019;58:2–28. doi: 10.1002/anie.201813331.
—
DOI
—
пабмед
- Че С.
Грантовая поддержка
- 20172410100140/Министерство торговли, промышленности и энергетики (Министерство торговли, промышленности и энергетики Кореи)
- 2018M1A2A2063341/Национальный исследовательский фонд Кореи (NRF)
представляет собой смесь воды и воды — введение, раствор и соотношение.
 Аккумулятор Greenway
Аккумулятор Greenway0769-27282088
Сервисный центр
Dongguan Greenway Battery Co., Ltd.
ФАКС:(+86) 769 2229 0098
粤ICP备11070025号
Эл.
Аккумулятор вашего автомобиля не всегда может быть заправлен необходимым количеством электролита, которое необходимо для его правильного функционирования. Поэтому в некоторых случаях вам может потребоваться долить электролит в аккумулятор вашего автомобиля. Это может показаться легкой задачей, но на самом деле это не так просто, потому что это довольно сложная тема.
?Итак, если в аккумуляторе вашего автомобиля заканчивается электролит и у вас мало информации о том, что такое электролит или каково соотношение кислоты и воды в аккумуляторе, то вы попали на соответствующий веб-сайт, потому что мы у вас есть ответы на все ваши вопросы, касающиеся электролита батареи.
?Давайте начнем и познакомимся с «Электролитом батареи является смесь воды и — введение, раствор и соотношение»!
Из чего состоит аккумуляторный электролит? Если вы не знаете, из чего состоит электролит, то мы здесь, чтобы дать ответ! Большинство обычных батарей состоят из жидкости, которая широко известна как электролит. Этот электролит в аккумуляторе представляет собой смесь серной кислоты и воды. Пластины свинцово-кислотных аккумуляторов содержат активный материал, который всегда должен находиться в электролите, в то время как водород и кислород выделяются во время зарядки. Пока аккумулятор заряжается, плотность раствора электролита будет увеличиваться.
Этот электролит в аккумуляторе представляет собой смесь серной кислоты и воды. Пластины свинцово-кислотных аккумуляторов содержат активный материал, который всегда должен находиться в электролите, в то время как водород и кислород выделяются во время зарядки. Пока аккумулятор заряжается, плотность раствора электролита будет увеличиваться.
Электролиты в батарее служат катализатором, делающим батарею проводящей, инициируя движение ионов от катода к аноду при зарядке и наоборот при разрядке. В зависимости от степени, в которой электролит батареи может выделять ионы, электролит может быть либо сильным, либо слабым. К сильным электролитам относятся соединения, обладающие высокой степенью ионизации и проводящие мощный электрический ток. С другой стороны, слабые электролиты — это соединения, которые ионизируются в минимальной и незначительной степени и проводят небольшой электрический ток.
Теперь, если говорить о составе электролитов, то вам важно отметить, что в разных батареях в качестве электролита используются разные химические соединения. Некоторые из часто используемых соединений включают хлорид натрия, серную кислоту, азотную кислоту, хлорную кислоту, ацетат натрия и т. д. Таким образом, в зависимости от типа или марки батареи состав электролита батареи будет меняться от одной батареи к другой. Но в большинстве случаев электролиты в свинцово-кислотных батареях состоят из серной кислоты и воды.
Некоторые из часто используемых соединений включают хлорид натрия, серную кислоту, азотную кислоту, хлорную кислоту, ацетат натрия и т. д. Таким образом, в зависимости от типа или марки батареи состав электролита батареи будет меняться от одной батареи к другой. Но в большинстве случаев электролиты в свинцово-кислотных батареях состоят из серной кислоты и воды.
Что такое раствор электролита для аккумуляторов??Как вы прочитали выше, из чего состоит электролит, теперь давайте разберемся, что такое раствор электролита для аккумуляторов??
Каждая батарея состоит из катода, анода и электролита. Анод и катоды представляют собой электроды, полностью погруженные в раствор электролита и соединенные снаружи токопроводящей проволокой. Когда анод и катод растворяются в растворителе, раствор электролита высвобождает ионы. Ионы, разряжаемые электролитом, реагируют с анодом, высвобождая один или несколько электронов.
Проще говоря, мы можем сказать, что электролит – это среда, обеспечивающая транспортный механизм для ионов между катодом и анодом ячейки. Электролит часто рассматривается как жидкая смесь воды и других растворителей с растворенными кислотами, солями или щелочами, которые необходимы для ионной проводимости. Электролит позволяет двигаться только ионам. Для электролита батареи обычно используются материалы с высокой ионной проводимостью, чтобы ионы лития могли легко перемещаться вперед и назад. Все движение ионов лития обычно зависит от типа электролита; поэтому всегда должен использоваться тот электролит, который соответствует строгим условиям.
Электролит часто рассматривается как жидкая смесь воды и других растворителей с растворенными кислотами, солями или щелочами, которые необходимы для ионной проводимости. Электролит позволяет двигаться только ионам. Для электролита батареи обычно используются материалы с высокой ионной проводимостью, чтобы ионы лития могли легко перемещаться вперед и назад. Все движение ионов лития обычно зависит от типа электролита; поэтому всегда должен использоваться тот электролит, который соответствует строгим условиям.
Каково соотношение серной кислоты и воды в аккумуляторе? Когда дело доходит до аккумуляторного электролита, большинство людей обычно не понимают соотношения кислоты и воды в аккумуляторе! Если вы один из тех, кто запутался в одном и том же, то вам больше не нужно запутываться, потому что у нас есть ответ для вас!
Когда мы говорим об электролите, мы обычно говорим о растворе серной кислоты и воде. Этот раствор серной кислоты и воды заполняет ячейки свинцово-кислотных аккумуляторов, а синергия между свинцовыми пластинами и электролитом позволяет аккумулятору вашего автомобиля накапливать и высвобождать энергию.
Итак, всякий раз, когда в аккумуляторе вашего автомобиля заканчивается электролит, может возникнуть необходимость добавить в него дополнительный электролит. Но для этого вы должны быть уверены в процентном соотношении кислоты и воды в аккумуляторе! Всякий раз, когда вы ищете ответ на этот вопрос в Интернете, вы можете не найти соответствующих результатов ни на одном из веб-сайтов, но у нас есть подходящий ответ на ваш запрос».
Кислота, присутствующая в аккумуляторной батарее вашего автомобиля, обычно представляет собой серную кислоту, которую обычно разбавляют водой для достижения уровня концентрации 37%. Этот уровень концентрации батареи вашего автомобиля обычно варьируется от одной батареи к другой, в зависимости от марки. Идеальное соотношение кислоты и воды в аккумуляторе составляет 30,1 см3 кислоты: 100 см3 дистиллированной воды. Если это соотношение кислоты и воды не поддерживается должным образом, весь механизм электрохимии внутри аккумулятора может измениться.
