Как правильно добавить дистиллированную воду в аккумулятор
Как правильно добавить дистиллированную воду в аккумулятор При эксплуатации аккумуляторов уровень электролита в банках неизбежно снижается. С не обслуживаемыми АКБ проще уровень жидкости в отсеках практически не меняется на протяжении 5-6 лет. Что касается обслуживаемых аккумуляторов владельцам постоянно приходится контролировать уровень электролита и своевременно принимать меры. В статье расскажем, как долить дистиллированную воду в аккумулятор, сколько ее нужно и можно ли чем-то заменить.Где взять дистиллированную воду для аккумулятора Лет 20 назад у автомобилистов вопросов о приобретении дистиллированной воды не возникало она продавалась практически в каждой аптеке. Сейчас ситуация изменилась. Дело в том, что эта жидкость пригодна для использования в медицинских целях в течение трех суток, поэтому достать ее можно только в аптечном пункте, имеющем свой дистиллятор.
Современные альтернативные варианты: магазины авто запчастей автозаправочные станции, имеющие торговую точку; хозяйственные магазины (дистиллированная вода используется в утюгах и отпаривателях). Еще один вариант поиск воды в интернет-магазинах. Подойдет он тем, кто хочет сделать запас впрок. Срок доставки в зависимости от региона может быть несколько недель, для экстренной доливки жидкости в АКБ такой способ не походит. Некоторые автомобилисты не хотят тратить время на посещение магазинов, и задаются вопросом, можно ли заливать в аккумулятор простую или кипяченую воду. Первый вариант не подходит категорически. В воде из-под крана присутствуют посторонние вещества хлор, магний, фосфор и т.д. При зарядке аккумулятора они осядут на свинцовых пластинах. В лучшем случае это приведет к снижению емкости АКБ, в худшем к замыканию и выходу батареи из строя. Что касается кипяченой воды полноценно заменить дистиллированную она не сможет, в ней имеются соли металлов, пусть и в небольшом количестве. Такой вариант подойдет, если нужно срочно привести аккумулятор в боевую готовность, но затем придется промывать каждую банку и заливать новый электролит.
Такой вариант подойдет, если нужно срочно привести аккумулятор в боевую готовность, но затем придется промывать каждую банку и заливать новый электролит.
Попытка заменить дистиллированную воду кипяченой или какой-либо другой может привести к снижению емкости батареи, разрушению свинцовых пластин и другим неприятным последствиям. Как доливать дистиллированную воду в автомобильный аккумулятор правильно Если в вашем аккумуляторе увеличилась плотность электролита или вы заметили, что он не выдает нужного напряжения скорее всего причина в снижении количества дистиллированной воды. В норме ее должно быть 65 % на 35 % серной кислоты. Последовательность работ при доливке дистиллята в аккумулятор. Чтобы правильно долить жидкость в банки воспользуйтесь инструкцией. Уберите грязь и пыль с верхней части аккумулятора, особенно вокруг пробок. Протрите область вокруг горловин тряпкой, смоченной в содовом растворе, для нейтрализации серной кислоты, которая могла выплеснуться при зарядке.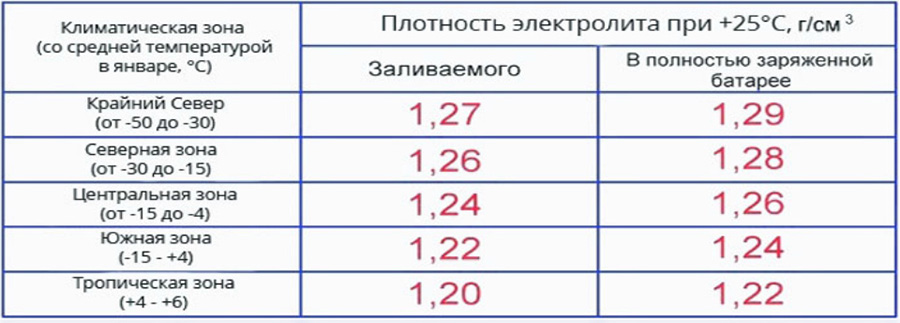
Доливка дистиллированной воды в аккумулятор должна проводиться на горизонтальной поверхности. В противном случае уровень жидкости в банках будет различный, поэтому вы или перельете воду, или не дольете. Рекомендуемая плотность электролита в аккумуляторе зависит от климатических условий вашего региона. Климатический пояс Плотность электролита (г/см3) 1,25 Средняя полоса 1,27 Север 1,29 Чтобы при измерении плотности электролита результат был точным держите ареометр вертикально, не допускайте касания поплавка его стенок. Набрав электролит в колбу, постепенно снижайте давление, чтобы поплавок свободно плавал.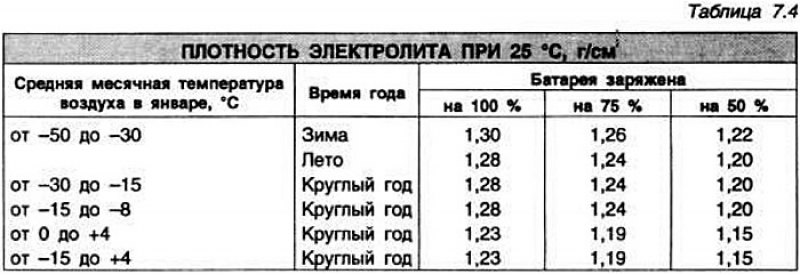 Если вы смогли этого достичь обратите внимание на место соприкосновения жидкости со шкалой. Это и будет плотность электролита в аккумуляторе. Проверьте плотность электролита после добавления дистиллированной воды в АКБ.
Если вы смогли этого достичь обратите внимание на место соприкосновения жидкости со шкалой. Это и будет плотность электролита в аккумуляторе. Проверьте плотность электролита после добавления дистиллированной воды в АКБ.
Сколько дистиллированной воды доливать в аккумуляторную батарею В современном аккумуляторе проще всего понять, сколько нужно заливать дистиллированной воды. Его корпус изготовлен из прозрачного пластика с нанесенной на нем шкалой. Достаточно следить, чтобы не был превышен рекомендуемый производителем уровень. В случае, если у вас аккумулятор другого типа, воспользуйтесь следующими советами. В некоторых АКБ чуть ниже горловины банки расположен металлический или пластмассовый язычок. Уровень электролита должен быть выше язычка на 5 мм. Если никаких отметок в банке нет доливайте дистиллированную воду так, чтобы уровень электролита был выше свинцовых пластин на 10-15 мм. Если вы не можете визуально определить, сколько электролита в банке возьмите стеклянную трубку, опустите ее в отсек, зажмите верхнюю часть пальцем и аккуратно извлеките.
 Дистиллированная вода имеет формулу h3O, то есть не содержит посторонних примесей. Как бы вы не старались, получить подобный результат дома практически невозможно незначительная часть солей металлов в воде останется.
Дистиллированная вода имеет формулу h3O, то есть не содержит посторонних примесей. Как бы вы не старались, получить подобный результат дома практически невозможно незначительная часть солей металлов в воде останется.
Если вам нужно срочно долить в аккумулятор воду наберите ее в пластмассовую бутылку и уберите в холодильник на 2-3 часа. Затем слейте не замерзшую воду в раковину, а лед растопите и пользуйтесь для заливки в банки. В этом случае ущерб для АКБ будет минимальным. Можно собирать в пластмассовую посуду дождевую воду, затем тщательно фильтровать и использовать по назначению. Важно, чтобы вода не соприкасалась с металлами. Например, та, что стекает с жестяных крыш, для заливки аккумулятора не подойдет. Подведем итоги Теперь вы знаете, как долить дистиллированную воду и при этом не испортить аккумулятор. Рекомендуем приобрести ареометр, чтобы контролировать плотность электролита в банках. Без этого прибора достичь нужной плотности невозможно, а ее изменение может вывести из строя вашу АКБ.
Электролит свинцово-кислотной аккумуляторной батареи.
Электролит
Для работы свинцово-кислотной аккумуляторной батареи необходим электролит – водный раствор серной кислоты, обладающий высокой ионной проводимостью. При погружении электродов аккумулятора в электролит и подключении к выводам электродов внешней нагрузки начинаются электрохимические реакции, описанные в предыдущей статье.
Электролит для заливки в аккумуляторную батарею готовят из серной кислоты (ГОСТ 667-73) и дистиллированной воды (ГОСТ 6709-72). При подготовке электролита следует пользоваться руководством по эксплуатации автомобиля. Для надежной работы аккумуляторных батарей необходима высокая степень чистоты электролита.
Нельзя применять техническую серную кислоту и недистиллированную воду, так как при этом ускоряется саморазрядка, сульфатация и разрушение пластин, и уменьшается емкость батареи.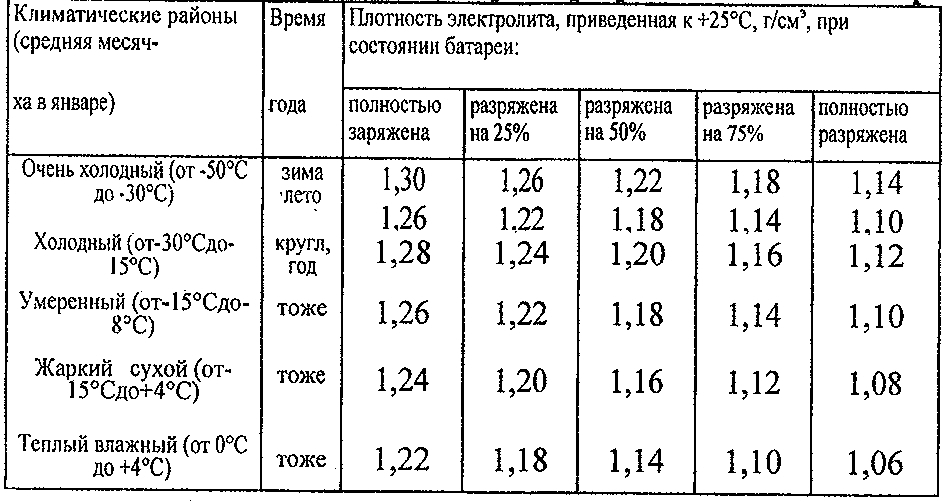
При приготовлении электролита кислоту льют тонкой струйкой в воду, одновременно помешивая раствор чистой стеклянной палочкой. Нельзя наливать воду в кислоту, так как при этом выделяется большое количество тепла в верхних слоях раствора, и электролит будет разбрызгиваться из емкости и при попадании на тело может вызвать ожоги.
Смешивать электролит следует в кислотостойкой эбонитовой, фарфоровой или освинцованной посуде.
Количество дистиллированной воды, серной кислоты или электролита при приготовлении 1 литра электролита необходимой плотности приведены в таблице 1.
Таблица 1. Количество дистиллированной воды, серной кислоты или электролита плотностью 1,4 г/см3 для приготовления 1 л электролита необходимой плотности при температуре 25 ˚С, л
Плотность |
Для серной кислоты |
Для электролита |
||
дистиллированная |
серная кислота |
дистиллированная |
электролит |
|
1,23 |
0,829 |
0,231 |
0,465 |
0,549 |
1,25 |
0,809 |
0,253 |
0,410 |
0,601 |
1,27 |
0,791 |
0,274 |
0,357 |
0,652 |
1,31 |
0,749 |
0,319 |
0,246 |
0,760 |
1,40 |
0,650 |
0,423 |
0 |
1 |
Плотность электролита определяют с помощью денсиметра или ареометра.
Новые аккумуляторные батареи заливают электролитом плотностью на 0,02 г/см3 меньше той, которая должна быть в конце зарядки.
***
Плотность электролита
Плотность электролита, как и любого другого вещества, определяется отношением массы к занимаемому этой массой объему. Для электролита плотность измеряется в граммах на кубический сантиметр (г/см3).
Поскольку плотность дистиллированной воды равна 1 г/см3, а серная кислота тяжелее воды (ее плотность при +20 ˚С составляет: 1,8312-1,8355 г/см3), то с добавлением серной кислоты в воду плотность электролита будет возрастать, а при добавлении в раствор (электролит) воды, его плотность будет уменьшаться. По этим же причинам плотность будет уменьшаться при сульфатации пластин и при сильной разрядке батареи, а увеличивается при испарении воды (например, в процессе интенсивной зарядки).
При понижении плотности электролита возрастает внутреннее сопротивление аккумуляторной батареи и уменьшается ее емкость. В морозное время года чрезмерное снижение плотности может привести к замерзанию электролита.
В морозное время года чрезмерное снижение плотности может привести к замерзанию электролита.
Повышение плотности электролита приводит к интенсивному разрушению пластин и их сульфатации, что снижает емкость аккумулятора и уменьшает срок его службы. Следует учитывать, что плотность электролита в аккумуляторах (банках) аккумуляторной батареи не должна отличаться более чем на 0,01 г/см3. В противном случае батарею необходимо полностью зарядить и произвести корректирование плотности электролита.
Если плотность выше нормы — доливают дистиллированную воду, если ниже — электролит плотностью 1,4 г/см3 (электролит можно доливать лишь в полностью заряженную аккумуляторную батарею). Корректировку плотности доливкой производят после предварительного отбора из аккумуляторов нужного количества электролита. После этого аккумуляторную батарею заряжают в течение 25…30 мин для полного перемешивания электролита и снова измеряют его плотность.
В процессе эксплуатации необходимо следить за состоянием аккумуляторной батареи. При нормальных эксплуатационных параметрах плотность электролита в аккумуляторах батареи является индикатором степени их разрядки. Снижение плотности электролита на 0,01 г/см3 соответствует разрядке аккумулятора на 6 %.
Если появляется необходимость в частой подзарядке батареи, следует выяснить причину и ее устранить, поскольку систематическая недозарядка аккумуляторной батареи значительной сокращает срок ее службы и отрицательно сказывается на пусковых качествах двигателя.
***
Определение степени зарядки аккумуляторной батареи
Степень зарядки аккумуляторной батареи проверяют измерением плотности электролита, приведенной к температуре +25 ˚С. В зависимости от климатических условий эксплуатации автомобиля и времени года используется электролит разной плотности (таблица 2).
Таблица 2. Плотность электролита в зависимости от климатических условий и времени года
Плотность электролита в зависимости от климатических условий и времени года
Макрокли- |
Климатический район (ГОСТ 16350-80) |
Средне- |
Время года |
Плотность электролита приведенная к температуре +25 ˚С, г/см3 |
|
Для новой аккумуляторной батареи |
Для заряженной аккумуляторной батареи |
||||
Холодный |
Очень холодный |
от -50 до -30 |
Зима |
1,28 |
1,30 |
Лето |
1,24 |
1,26 |
|||
Холодный |
от -30 до -15 |
Круглый год |
1,26 |
1,28 |
|
Умеренный |
Умеренный |
от -15 до -3 |
Круглый год |
1,24 |
1,26 |
Жаркий сухой |
от -15 до +4 |
1,22 |
1,24 |
||
Теплый влажный |
0 до +4 |
1,20 |
1,22 |
||
При определении плотности электролита необходимо учитывать его температуру, применяя соответствующие поправки, приведенные в таблице 3.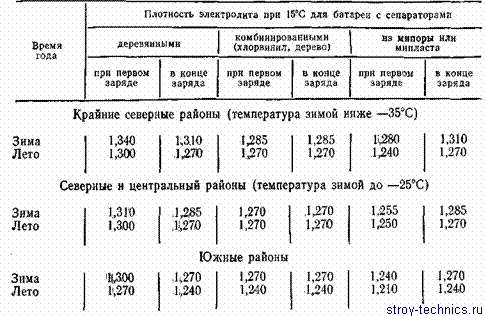
Таблица 3. Поправки при измерении плотности электролита (г/см3) в зависимости от его температуры
Температура электролита, |
+45 |
+30 |
+15 |
0 |
-30 |
-15 |
-45 |
Поправка плотности |
+0,02 |
+0,01 |
0 |
-0,01 |
-0,02 |
-0,03 |
-0,04 |
***
Проверка уровня электролита
Одним из важнейших условий надежной работы аккумуляторной батареи является поддержание необходимого уровня электролита в ее элементах. Уровень электролита в каждой секции моноблока (банках) должен быть на 10…15 мм выше предохранительного щитка, установленного над сепараторами.
Уровень электролита в каждой секции моноблока (банках) должен быть на 10…15 мм выше предохранительного щитка, установленного над сепараторами.
Для облегчения контроля уровня электролита у заливных горловин аккумуляторных батарей снизу имеются указатели – тубусы, входящие внутрь аккумуляторной батареи. Нижний срез тубуса находится на требуемом расстоянии от поверхности предохранительного щитка. Уровень электролита считается достаточным, если поверхность электролита касается нижнего торца тубуса горловины. При этом на поверхности электролита образуется четко видимый мениск. Если уровень электролита ниже указанного из-за выплескивания, следует долить дистиллированной воды.
Проверять уровень электролита рекомендуется на остывшей заряженной аккумуляторной батарее или после длительной поездки, так как в этом случае происходит «кипение» электролита, повышение его температуры и испарение дистиллированной воды.
В случае превышения уровня электролита в банках аккумуляторной батареи его следует уменьшить с помощью резиновой груши, так как выплескивание может привести к интенсивной коррозии деталей крепления и к окислению проводов.
***
Типы автомобильных аккумуляторов
Главная страница
Дистанционное образование
Специальности
Учебные дисциплины
Олимпиады и тесты
Паспорт и руководство по эксплуатации Delta GEL (33-55 Ач, 75-85 Ач)
%PDF-1.5 % 1 0 obj >/OCGs[13 0 R 207 0 R 394 0 R 583 0 R 699 0 R]>>/Pages 3 0 R/Type/Catalog>> endobj 2 0 obj >stream application/pdf
Эксплуатация аккумуляторной батареи КамАЗ | АвтоКАМ
При получении сухозаряженных аккумуляторных батарей их надо подготовить к работе на автомобиле: залить электролит и зарядить батарею на зарядной станции в соответствии с инструкцией по уходу за батареями.
При нормальной эксплуатации автомобиля батарея заряжается автоматически. Если аккумуляторная батарея постепенно разряжается или чрезмерно заряжается и электролит начинает «кипеть», необходимо проверить исправность генераторной установки.
Не следует допускать большого разрядного тока (при пуске холодного двигателя зимой), так как это приводит к короблению пластин, выпаданию активной массы и сокращению срока службы аккумуляторных батарей.
При эксплуатации батареи в центральных районах с температурой зимой до —30 °С в батарею следует заливать электролит плотностью 1,250 +- 0,01 г/см3.
Для районов Крайнего Севера с температурой зимой ниже —40 °С плотность заливаемого электролита должна быть 1,290 зимой и 1,250 летом, а для южных районов 1,230 (дана плотность, приведенная к температуре +15 °С)
Электролит готовят из аккумуляторной серной кислоты (ГОСТ 667—73) и дистиллированной воды (ГОСТ 6709—72) в керамической, эбонитовой или освинцованной посуде, в которую сначала наливают дистиллированную воду, а затем вливают тонкой струей серную кислоту.
Вливать воду в концентрированную серную кислоту запрещается во избежание несчастных случаев при разбрызгивании кислоты.
В аккумуляторы следует заливать электролит в таком порядке:
снять предохранительную коробку;
снять декоративную крышку;
вывернуть пробки и срезать выступы на них;
залить тонкой струйкой электролит; уровень электролита должен быть на уровне нижнего торца тубуса горловины.
Не ранее чем через 20 мин и не позднее чем через 2 ч после заливки электролита необходимо проверить его плотность и уровень. Если плотность электролита понизится не более чем на 0,03 г/см3 по сравнению с плотностью заливаемого электролита, то батарею можно устанавливать на автомобиле без подзаряда. Если плотность понизится более чем на 0,03 г/см3, то батарею следует зарядить.
Включать батарею на заряд разрешается, если температура электролита не превышает 30 °С. Заряд ведут током 19 А до обильного выделения газа во всех аккумуляторах и до стабилизации напряжения и плотности электролита в течение 2 ч. Во время заряда необходимо периодически проверять температуру электролита и следить за тем, чтобы она поднималась не выше 45 °С. В том случае, если температура окажется выше 45 °С, следует уменьшить зарядный ток наполовину или прервать заряд на время, необходимое для снижения температуры до 30—35 °С.
В конце заряда, если плотность электролита, замеренная с учетом температурной поправки, будет отличаться от плотности электролита, заливаемого ранее, то доливают либо дистиллированную воду (при плотности выше нормы), либо кислоту плотностью 1,400 г/см3 (при плотности ниже нормы).
После корректировки плотности продолжают заряд в течение 30 мин для полного перемешивания электролита.
Затем замеряют уровень электролита, который доводят до нормы (электролит должен касаться нижнего торца тубуса заливной горловины) добавлением электролита той же плотности при низком уровне или удалением с помощью резиновой груши избыточного количества электролита при его уровне выше нормы.
В процессе эксплуатации аккумуляторных батарей на автомобиле перед каждым его выездом из парка необходимо проверять надежность крепления батарей в гнезде и плотность контакта наконечников проводов с выводами батареи, а также очищать батареи от пыли и грязи. Электролит, попавший на поверхность батареи, нужно вытереть чистой ветошью, смоченной в 10 %-ном растворе нашатырного спирта или кальцинированной соды.
Периодически следует проверять уровень электролита и при необходимости доводить до нормы доливкой дистиллированной воды. В холодное время года во избежание замерзания воды ее следует добавлять непосредственно перед пуском двигателя. Доливать электролит или кислоту в аккумуляторные батареи запрещается, за исключением тех случаев, когда точно известно, что уровень электролита понизился в результате его выплескивания. При этом плотность доливаемого электролита должна быть такой же, как и электролита в аккумуляторной батарее.
Периодически следует проверять степень заряженности аккумуляторов по плотности электролита, руководствуясь данными, приведенными в табл. 6. При разряде батареи летом на 50% и зимой на 25% ее необходимо снять с автомобиля и отправить на полный заряд на зарядную станцию.
Один раз в год аккумуляторную батарею следует отправлять на зарядную станцию для проведения контрольно-тренировочного цикла.
Напряжение аккумуляторов для автомототехники
Работоспособность автомобильного или мотоциклетного аккумулятора очень сильно зависит от емкости и напряжения. Если батарея заряжена недостаточно, то вряд ли удастся запустить двигатель транспортного средства, поэтому нужно следить чтобы аккумулятор всегда был полностью заряжен. Для стандартных аккумуляторов на 12 Вольт напряжение полностью заряженной батареи должно составлять от 12,6 до 12,9 Вольт, некоторые показывают чуть больше 13 Вольт. Следует обязательно проверять напряжение хотя бы раз в 2 месяца, чтобы успеть вовремя защитить свой аккумулятор от поломки.
Минимальное и нормальное напряжение без нагрузки
Вообще напряжение в аккумуляторах бывает следующим:
- Номинальное. Оно обычно указано в технической литературе – 12 В. Крайне редко совпадает с фактическим, более того, при таком напряжении батарея явно нуждается в подзарядке.
- Фактическое. В состоянии покоя колеблется примерно от 12,4 В до 12,9 В.
- Под нагрузкой. Очень важный показатель работоспособности батареи, речь о нем пойдет чуть позже.
Проверять фактическое напряжение стоит не раньше, чем через час после полной зарядки аккумулятора, так как сразу после неё показатели будут завышены, могут превышать 13 В. Через час напряжение не должно быть ниже 12,6-12,7 В. Если оно опускается ниже, значит, батарея не держит заряд.
Если измерения показали напряжение 11,9-12 В, то батарея разряжена примерно наполовину, но её еще можно использовать для запуска двигателя. После того как мотор заведется, АКБ будет автоматически подзаряжаться от генератора. А вот если пользоваться автомобилем или мотоциклом вы не планировали, то аккумулятор срочно нужно заряжать, иначе будет происходить сульфатация свинцовых пластин АКБ, что крайне нежелательно. Дело в том, что постепенно снижая работоспособность батареи, сероватый налет сульфата свинца приводит к полному выходу её из строя,
В том случае, когда измерения показали вам всего 11,6 Вольт или ниже, ваш аккумулятор полностью разряжен, не стоит даже и пытаться его использовать, пока не зарядите и не проверите заново.
Итак, минимально возможное для запуска двигателя напряжение, измеряемое без нагрузки — 11,9 В. Нормальные рабочие показатели этого параметра – 12,4-12,9 Вольт. Фактически чаще всего заряд аккумулятора колеблется от 12,2 до 12,5 В, так как полный заряд АКБ бывает далеко не всегда.
А что будет под нагрузкой?
Чтобы определить, насколько работоспособна батарея, проверять её под нагрузкой обязательно, там будут совсем другие цифры. В состоянии покоя держать заряд может большинство аккумуляторов, даже непригодных к работе. Чтобы выявить «убитые» АКБ и нужна проверка под нагрузкой.
Как это происходит:
- К полностью заряженному аккумулятору на 3-4 секунды при помощи нагрузочной вилки подключают нагрузку, которая превышает емкость батареи в 2 раза.
- Снимают показатели напряжения в процессе работы АКБ под нагрузкой, они не должны быть ниже 9 В. Если этот параметр меньше 6, то либо вы не зарядили батарею перед проверкой, либо аккумулятор совершенно непригоден к работе.
- Отключив нагрузку, через 5-6 секунд снова нужно снять показатели. Напряжение должно полностью восстановиться до нормы, хотя бы до 12,3-12,5 В.
Когда показатели при проверке были значительно ниже нормы, зарядите батарею до конца и попробуйте произвести измерения еще раз. Если увидите тот же результат – надо купить аккумулятор, так как старый пора менять.
Как связаны напряжение АКБ и плотность электролита
Связь самая прямая. Чем выше один показатель, тем выше другой. При нормальном напряжении в 12,7 Вольт плотность электролита в большинстве аккумуляторов составляет 1,27 г/куб. см. При снижении заряда аккумулятора уменьшается плотность электролита, так как при этом процессе расходуется кислота. Когда АКБ начинает заряжаться, расходуется вода и образуется кислота, что приводит к повышению плотности содержимого электролитических батарей.
Зимой если заряд аккумулятора достаточно высокий, то плотность электролита растет, значит, растет и напряжение. Выходит, что для хорошо заряженного аккумулятора мороз не страшен. А вот если батарея разряжена, то на морозе плотность электролита будет снижаться и напряжение падать, в этом случае и возникают проблемы при запуске мотора.
ᐅ Как подготовить автомобильный аккумулятор к зиме — Основные правила
share.in Facebook share.in Telegram share.in Viber share.in Twitter
Содержание:
Тема зимнего использования АКБ (аккумуляторно-кислотных батарей) очень популярна среди автолюбителей. Дело в том, что любой аккумулятор чувствителен к колебаниям окружающей среды. Если оставить аккумулятор на морозе, он начнет быстро разряжаться. В какой-то момент может оказаться, что машина не заводится — владельцам авто приходится искать нестандартные способы зарядки АКБ и запуска транспортного средства. Иногда это приводит к выходу батареи из строя.
Если знать, как правильно подготовить аккумулятор к зиме, и познакомиться с его правильной эксплуатацией, можно облегчить себе жизнь. В этой статье мы расскажем о правилах подготовки АКБ к холодам и его хранении.
Подготовка аккумулятора к зиме
Чтобы в холодное время года с аккумулятором автомобиля не возникло никаких неприятностей, нужно заранее позаботиться о его состоянии. Есть несколько этапов подготовки батареи, которые включают в себя устранение неисправностей, восстановление плотности электролита и теплоизоляцию аккумулятора.
Поиск и исправление неисправностей
Первое, что нужно знать: чтобы можно было эффективно использовать аккумулятор, вся электрическая система авто должна быть исправной. Самые важные части — проводка и генератор. Проверьте проводку на наличие повреждений, через которые электричество может утекать наружу. В условиях холода это может привести к полной разрядке АКБ и сокращению срока службы аккумулятора.
Клеммы батареи нужно почистить, убрав с них грязь, следы коррозии и окислы. После обработки мелкой наждачкой нужно покрыть клеммы литолом или консистентной смазкой, которая может проводить электроэнергию.
Осмотр генератора
Чтобы аккумулятор работал нормально, генератор должен выдавать 14,5 В, хотя минимальным значением считается 13,8 В. Если напряжение еще ниже, это с большой вероятностью приведет к тому, что батарея не сможет зарядиться. Еще один фактор, который ухудшает процесс зарядки — проскальзывание ремня на генераторе. Если на корпусе генератора есть следы перегрева, это говорит о скором выходе устройства из строя, что также отразится на аккумуляторе.
Проверка плотности электролита
Несоответствие уровня плотности электролита в батарее норме повлияет на емкость и ресурс аккумулятора. По мнению специалистов, оптимальный показатель — 1,27 г/см3 (летом он может быть немного меньше). Если вы измерили плотность и обнаружили, что она слишком низкая, нужно долить электролит повышенной плотности. Если же показатели выше нормы, нужно разбавить электролит дистиллированной водой.
Теплоизоляция аккумулятора
Если температура окружающей среды может опускаться до очень низких температур, лучше заранее теплоизолировать батарею от холода. Нужно выбрать негорючий материал, который не проводит электричество — он не станет причиной замыкания или возгорания.
Хороший вариант — стеклоткань, уложенная в тонкие маты. Ею можно обернуть аккумулятор, сформировав дополнительный слой защиты от холода. Клеммы должны оставаться открытыми. Также существуют специальные готовые термочехлы для батарей (в том числе, с подогревом).
Советы по использованию АКБ зимой
Может случиться так, что у вас не получится поднять плотность электролита. В этом случае постарайтесь ограничить нагрузку на батарею. После запуска автомобиля не включайте приборы в первые 5 минут. Помните, что заряд аккумулятора начинается только тогда, когда машина уже на ходу.
Читайте также: Зарядка автомобильного аккумулятора: делаем это правильно
Чем зарядить аккумулятор авто?
Наиболее простой и эффективный вариант — купить специальное зарядное устройство (ЗУ) с возможностью автоматической зарядки АКБ. Вам нужно будет всего лишь правильно подсоединить кабели устройства к клеммам батареи, а затем подключить батарею к электросети. Если зарядное устройство для зарядки аккумулятора авто качественное и современное, все остальное оно сделает само.
Как хранить аккумулятор зимой
Что делать, если вы не собираетесь пользоваться автомобилем зимой? Нужно создать правильные условия для хранения аккумулятора. Если это необслуживаемый АКБ, то ему подойдет хранение в гараже без какой-либо особой подготовки. А вот с обслуживаемыми все немного сложнее — их лучше снимать, чтобы хранить в тепле.
При хранении аккумулятора нужно соблюдать несколько правил:
- Перед хранением нужно дозаправить АКБ электролитом и зарядить его.
- Если храните батарею в жилом здании, лучше подготовить для нее проветриваемое помещение.
- Температура воздуха должна быть не выше 25 °C. Не оставляйте батарею возле радиаторов отопления.
- Нельзя хранить АКБ во влажной среде.
Наилучшее место для аккумуляторной батареи — отапливаемый гараж, закрытый балкон, лоджия, терраса или веранда.
Советы по хранению аккумулятора в зимний период
Если вы будете хранить батарею отдельно от автомобиля, придерживайтесь следующих советов:
- Используйте при перезаправке готовый электролит или дистиллированную воду. Воду из-под крана использовать нельзя — она разрушит батарею.
- Если в доме высокий уровень влажности, нужно обработать клеммы литолом. После этого их рекомендуется закрыть специальными колпачками или укутать в промасленную бумагу.
- После того как установили АКБ в автомобиль, пусть авто полчаса поработает вхолостую. На протяжении одного дня постарайтесь минимально использовать электроприборы.
- В случае потери батареей своих свойств, можно попробовать перезаправить ее и снова зарядить. Однако наилучший способ — профессиональная диагностика.
- Осадок на дне банки, который появляется в результате разрушения электродов, говорит о необходимости заменить батарею.
Заключение
Соблюдая все эти правила и рекомендации, вы продлите термин эксплуатации своего авто и сохраните его работоспособность после зимы. Единственное условие — батарея должна изначально быть работоспособной. Чтобы убедиться в этом, стоит провести диагностику еще осенью.
Самый лучший способ подзарядки аккумулятора — зарядные устройства. Они автоматически регулируют ток заряда и уменьшают его по мере необходимости. Приобретя такое устройство, вы избавитесь от многих проблем, связанных с АКБ.
В крайних банках ниже плотность электролита. Как поднимать плотность электролита в аккумуляторе в домашних условиях
Вам понадобится
- Ареометр, «груша»-клизма, мерный стакан, электролит, аккумуляторная кислота, дистиллированная вода, раствор пищевой соды, дрель, паяльник.
Инструкция
Первое, с чего следует начать, это замерить плотность электролита в каждой в отдельности. Плотность должна быть в пределе от 1,25 до 1,29 – меньший показатель для южных районов с теплой , больший – для северных районов с холодным , а разброс показаний по банкам не должен быть 0,01. Если замер плотности показал, что ее значение находится в пределе 1,18-1,20, то вполне можно обойтись доливом электролита с плотностью 1,27. Сначала доведите плотность до нужной в одной банке. Откачайте электролит с помощью «груши», откачивайте по возможности большее количество, замерьте объем, долейте свежий электролит в половине объема от выкаченного. Покачайте из стороны в сторону и замерьте плотность. Если плотность не достигла нужного параметра, долейте еще электролита в четрверти объема от выкаченного. При дальнейших доливах объем снижайте вдвое, до достижения нужной плотности. А при достижении нужной плотности остаток долейте дистиллированной водой.
Если плотность упала ниже предела 1,18, то электролит здесь не поможет, нужна аккумуляторная кислота. Ее плотность значительно выше, ведь электролит готовится из нее путем смешивания с дистиллированной водой. Работы проводите в том же порядке, как и при добавлении электролита, но в данном случае процедуру, возможно, придется провести повторно, если после первого этапа разбавления плотность не достигнет нужного показателя.
Еще один способ подразумевает полную замену электролита в аккумуляторе. Для этого нужно, откачать максимальный объем электролита с помощью «груши», герметично закрыть вентиляционные отверстия пробок банок аккумулятора, положить батарею на бок и в дне аккумулятора, сверлом на 3-3,5, просверлить отверстия, поочередно в каждой банке, не забывая при этом сливать электролит. Затем промываем аккумулятор внутри дистиллированной водой. Просверленные отверстия запаиваем кислотостойкой пластмассой, лучше пробкой от другого аккумулятора. И заливаем свежий электролит, лучше приготовить его самому с плотностью несколько большей, чем положена для вашей климатической зоны.
Обратите внимание
При работе с электролитом и, особенно с кислотой будьте осторожны, работайте в резиновых перчатках и очках.
При разведении электролита самостоятельно помните: добавлять нужно кислоту в воду, а не наоборот, это обусловлено разной плотностью кислоты и воды.
Аккумулятор нельзя переворачивать к верху дном, это может привести к осыпанию активной массы пластин и последующему короткому замыканию.
При полной замене электролита не надейтесь на долгую службу аккумулятора, готовьтесь к покупке нового.
Полезный совет
Плотность аккумулятора нужно замерять при 20 градусах Цельсия.
Заранее подготовьте емкости под сливаемый электролит и для разведения свежего.
При зарядке аккумулятора плотность электролита повышается.
При запайке высверленных отверстий, проверьте устойчивость пластмассы на реакцию с электролитом.
Плотность электролита снижается при разрядке аккумулятора, куда он заливается. Чтобы поднять его плотность, попытайтесь зарядить аккумулятор до кипения в банках. Если после этого плотность электролита не поднялась до нужного показателя, освободите в нем место и долейте серную кислоту.
Вам понадобится
- ареометр, серная кислота или концентрированный электролит, зарядное устройство.
Инструкция
Поднятие плотности электролита без доливания кислотыПервым признаком падения плотности электролита является разрядка . Для того чтобы определить плотность, используйте ареометр. Для этого с его помощью оттяните некоторое количество электролита и по всплывающим поплавкам определите его плотность. Она должна составлять 1,27 г/см3, она может быть чуть выше. Если плотность электролита меньше нормы, подсоедините аккумулятор к зарядному устройству и заряжайте его до тех пор, пока в банках не закипит. Затем разрядите его с помощью лампочки, за это время измерьте ток разрядки и ее время. Перемножив эти значения, узнайте емкость аккумулятора и сравните ее с паспортной. Если она более чем на 30% меньше, то перезарядка не поможет. В обратном случае снова зарядите аккумулятор и замерьте плотность электролита. Она должна прийти в норму.
Поднятие плотности электролита доливанием кислотыВ том случае, если первый метод не , электролита остается менее 1,27 г/см3, долейте кислоту. Для этого ареометром оттяните некоторое количество электролита и залейте серную кислоту. Учтите, что ее плотность составляет 1,83 г/см3, и это очень едкое вещество. В автомагазинах продается концентрат электролита плотностью 1,4 г/см3 — он более безопасен, поэтому лучше используйте его. Доливайте концентрат, пока плотность не увеличится до нужного значения. После этого поставьте аккумулятор на зарядку с небольшим током (не более 2 А) на полчаса. За это время электролит полностью перемешается. Снова проверьте плотность во всех банках. Она должна быть одинаковой и соответствовать нормам. Если плотность все еще мала, повторите операцию снова.
Особую осторожность соблюдайте при работе с серной кислотой. Не допускайте ее попадания на кожу или одежду. Если это произошло, смойте электролит большим количеством воды и обработайте это место раствором соды, которая нейтрализует кислоту. При оттягивании раствора ни в коем случае не переворачивайте аккумулятор, потому что шлам от пластин может закоротить батарею, и она испортится.
Уменьшение плотности электролита происходит в основном при полной разрядке аккумулятора. При этом увеличивается внутреннее сопротивление аккумулятора и уменьшается его емкость, что приводит к сложностям при попытке запустить двигатель из-за снижения мощности стартера. Рассмотрим, как можно повысить плотность электролита.
Вам понадобится
Инструкция
Откройте пробки в верхней части и с помощью специального прибора, ареометра, измерьте плотность . Для этого в стеклянную трубку, которой поплавок, наберите электролит и по делению на поплавке определите его плотность. Если плотность меньше, чем 1.12, то ее уже вряд ли получится.
Полностью зарядите аккумулятор до того, пока не закипит электролит в банках. При этом значение плотности должно подняться до 1.26-1.28. Желательно осуществить несколько полных циклов зарядки-разрядки, для этого зарядите аккумулятор при помощи малых токов, после чего разрядите до 10.8 вольт, подключив на несколько часов сопротивление в 50 Ом или лампочку на 20-30 Ватт.
После этого перемножьте ток на время, в течение которого разряжался аккумулятор — таким образом, вы рассчитаете значение реальной емкости. Повторите весь цикл еще раз. После этих манипуляций емкость и плотность должны увеличиться. Снова измерьте плотность ареометром.
Если после всех причисленных действий плотность электролита составляет менее 1.26, то откорректируйте ее с помощью добавления электролита плотностью 1.40. Для этого грушей удалите часть электролита из аккумулятора, а вместо нее добавьте новый электролит с высокой плотностью, пока плотность результирующего состава не достигнет требуемого значения.
После этого опять зарядите аккумулятор малым током, не более 2-х Ампер в течение получаса для того, чтобы дать перемешаться электролиту. Опять проверьте плотность и если она меньше нормы, снова добавьте электролит.
Говоря о необходимости повысить плотность аккумулятора, мы, конечно же, имеем в виду плотность электролита в аккумуляторных батареях. Повернул ключ два-три раза, и все – стартер не крутит. Особенно если зажигание не отрегулировано.
Вам понадобится
- — ареометр,
- — электролит,
- — зарядное устройство
Инструкция
В подобных случаях, прежде всего, проверьте, достаточно ли заряжен ваш .
Если он долго стоял на хранении, снятый с автомобиля, вполне возможно АКБ потеряла свой . Это явление саморазрядом. Потеря заряда АКБ может быть и на эксплуатируемом автомобиле при определенном режиме движения.
С понижением заряда падает и электролита. Эти два показателя тесно взаимосвязаны. Поставьте аккумулятор на зарядку, и вы повысите плотность. Не забудьте открыть пробки.
Учтите, чем меньшим током вы будете заряжать вашу батарею, тем полнее и глубже вы зарядите аккумулятор. Для «55-го», например, оптимальным будет ток 2.75 А.
Проверьте плотность заряженной батареи. Если по истечении 10-12 часов ее плотность не достигла показаний 1.27 – 1.28 г/куб. см, вы не наблюдали кипения и выделения газов из банок АКБ – переходите к повышению плотности доливом свежего электролита.
Для этого с соблюдением всех мер предосторожности резиновой грушей или тем же ареометром поочередно из каждой банки забирайте электролит и сливайте в какую-нибудь стеклянную посудину. Чтобы не переводить впустую свежий электролит, заберите и вылейте, в зависимости от потери плотности, из банки сразу несколько всасываний.
Наверняка большинство автомобилистов сталкивались с ситуацией, когда оставленная на некоторое время машина перестает заводиться. При этом стартер может вообще не подавать каких-либо признаков жизни. Основной причиной этому, скорее всего, является аккумуляторная батарея, что за несколько дней полностью разрядился. Попытка зарядить ее в этом случае не приведет к положительному результату. Подобная проблема является результатом снижения плотности электролита, что залит в банки батареи …
Ведь эта жидкость, по сути является катализатором электрохимического процесса, без нее аккумулятор это набор и пластика, который работать не будет. Как мы с вами знаем, состоит от из (примерно 65%) и (35%), у этой жидкости есть определенная плотность, которая может понижаться и повышаться, в зависимости от заряженности.
Почему снижается плотность электролита?
Чаще всего с целью поддерживать на требуемом уровне количество жидкости внутри автомобильной батареи владельцы машины доливают туда дистиллированную воду. При этом редко проверяется плотность получившегося раствора. Вместе с тем, когда количество дистиллированной воды будет достаточно большим, при подзарядке вместе с этой жидкостью будет выкипать и электролит, что и приводит к снижению его плотности.
Рано или поздно этот показатель упадет ниже критического уровня, и завести транспортное средство уже не получиться.
В таком случае возникает необходимость повысить этот параметр раствора в аккумуляторе, что вернет его работоспособность.
Подготовка к восстановлению батареи
Перед тем, как своими силами повышать уровень плотности аккумуляторной батареи, к этому процессу следует тщательно подготовиться. В первую очередь:
- Замеряется этот основной показатель автомобильной батареи при температуре около 22 градусов. Сделать этом можно при помощи специального прибора – ареометра. При этом работать можно только в перчатках и защитных очках, чтобы избежать возможных ожогов.
- При приготовлении нового электролита кислота добавляется в воду. Если же сделать наоборот, жидкость , что может привести к кислотным ожогам.
- Переворачивать аккумулятор при работе с ним категорически запрещено, поскольку при этом могут посыпаться его пластины, что приведет к выходу прибора из строя.
- Наперед следует подготовить емкости, в которые будет сливаться старая жидкость и готовиться новая.
- Потребуются точные расчеты необходимого объема кислоты, поскольку в процессе зарядки плотность жидкости в АКБ возрастет.
Повышение плотности электролита
В АКБ есть несколько банок, электролитический раствор есть в каждой из них. Проверять и при необходимости повышать уровень плотности необходимо в каждой банке.
Нормальный уровень данного показателя зависит от нескольких факторов, в первую очередь – от температуры воздуха. Нормальным считается значение 1,25-1,29г/см3. Разница таких показателей между банками не должна превышать 0,1.
Если измерение этого показателя является ниже нормы, нужно повысить плотность электролита в аккумуляторе.
При помощи спринцовки из каждой банки выкачивается раствор. При этом набирать нужно как можно большее количество жидкости, измеряя ее объем, чтобы затем долить точно такое же количество свежего электролита.
Залив столько же свежего раствора, сколько было извлечено старого, АКБ хорошенько прокачивается с целью размешивания нового и старого электролита.
После этого снова проводиться измерение этого показателя: если он все еще находиться ниже нормы, все действия повторяются до достижения нужного значения плотности. По завершению при необходимости в банки автомобильной батареи добавляется дистиллированная вода.
Плотность ниже минимального значения
Бывают такие случаи, когда уровень этого показателя опускается ниже отметки 1,18. В таком случае вышеописанный способ ничем не поможет.
Чтобы восстановить работоспособность аккумуляторной батареи, вместо электролитического раствора нужно использовать кислоту, плотность которой выше, чему у электролита. При этом все действия проводятся точно так же, как и в предыдущем случае до того времени, пока показатель не придет в норму.
Можно ли повысить минимальную плотность?
Если уровень плотности раствора, что проводит ток в АКБ автомобиля упал намного ниже 1,18 г/см3, поднимать ее нет никакого смысла. В таком случае необходимо слить весь раствор, заменив его свежим.
Сначала с банок откачивается с помощью спринцовки как можно больше электролита. Далее батарея помещается в большую емкость, аккуратно переворачивается на бок, в дне каждой банки просверливается небольшое отверстие. Перевернув прибор, с него сливаются все излишки оставшейся жидкости.
Сделав это, в АКБ заливается свежий раствор, после чего прибор будет готов к использованию. Недостатком подобного способа является то, что в конечном результате снижается срок службы устройства, но некоторое время оно все еще поработает до покупки нового.
Как повысить при помощи зарядного устройстваТут также все просто, нам нужно заряжать аккумулятор на слабом токе, длительный промежуток времени. Суть такова, при достижении полного заряда, электролит начнет кипеть, пойдут пузырьки, это распадается и испаряется вода. Для повышения плотности нам нужно чтобы лишняя вода испарилась, а кислота осталась. Конечно, будет понижаться уровень в батареи – но вместо ушедшего уровня, добавляем нужный плотности электролит. Процесс этот долгий и муторный (выкипание — добавление), но примерно через пару суток можно догнать уже до плотности в 1,27 – 1,29 г/см3, что уже нормально.
Многим автовладельцам наверняка приходилось сталкиваться с проблемой некорректной работы аккумулятора. Бывает так, что машина простояла всего сутки, а завести ее после этого становится невозможно. При этом даже длительная зарядка батареи не помогает. Подобные симптомы свидетельствуют о снижении О том, какая должна быть плотность в аккумуляторе, почему она падает, и как ее поднять до нужного уровня, мы и поговорим в этой статье.
Электролит и его плотность
Электролит — это раствор, состоящий из серной кислоты и дистиллированной воды. Эти компоненты содержатся в примерно равных частях: вода — 1 часть, серная кислота — 1,25 части. Показатель 1,25 — это и есть плотность аккумулятора АКБ напрямую зависят от этого показателя — чем он выше,
тем ниже у нее температура замерзания, а сама она находится в удовлетворительном рабочем состоянии. Зная, какая должна быть плотность в аккумуляторе, можно судить о реальном состоянии своего устройства.
Замер плотности АКБ
Перед тем как проверить плотность аккумулятора, следует обзавестись специальным прибором под названием ареометр. Он представляет собой устройство, состоящее из нескольких резиновых и стеклянных элементов.
Т.к. электролит является опасным химическим соединением, перед замером его плотности необходимо позаботиться о мерах предосторожности, а именно работы проводить в резиновых перчатках, избегая попадания жидкости на кожу и одежду. Категорически запрещается курить!
Откройте горловину банки, вставьте в нее наконечник устройства и с помощью груши наберите немного электролита так, чтобы поплавок ареометра свободно плавал в корпусе, не задевая дно, боковые стенки и верх. Подождите, пока жидкость в приборе успокоится, и, держа его на уровне глаз, визуально считайте показания. Данную процедуру проведите со всеми банками. Если разница плотности будет превышать 0,01 г на куб. см, то обязательно долейте дистиллированную воду либо поставьте АКБ на выравнивающую зарядку. При снижении плотности до показателя 1,24 г на куб. см или ниже аккумулятор следует подзарядить.
Важно знать не только, как проверить плотность аккумулятора с помощью ареометра,
но и правила внесения поправок к показанию прибора в конкретных температурных условиях. Оптимальная температура электролита для измерения его плотности составляет +15 — +25˚С, но если приходится выполнять эту процедуру при более высокой или низкой температуре, то показания необходимо корректировать.
Температура электролита (˚С) | Поправка к показаниям ареометра |
Не следует выяснять, какая плотность в аккумуляторе, после того как туда недавно
была долита вода, или после неоднократных попыток запуска стартера. После выполнения всех процедур тщательно промойте ареометр водой.
Как поднять плотность в аккумуляторе?
Самым простым способом поддержания необходимого уровня электролита в АКБ является долив Однако большинство автовладельцев забывают или не знают о том, что периодически необходимо замерять плотность аккумулятора, т.к. вода со временем выкипает, а вместе с ней и электролит, что влечет снижение плотности, иногда до критической отметки. Когда аккумулятор совсем
отказывается работать, то тут же возникает животрепещущий вопрос: «Как поднять плотность в аккумуляторе?»
Используя нижеизложенную инструкцию, вы сможете самостоятельно продлить жизнь АКБ. Однако помните, что эта процедура требует особого внимания и аккуратности.
Меры предосторожности
Соблюдайте максимальную осторожность при работе с электролитом: все действия выполняйте в защитных очках и резиновых перчатках.
. При самостоятельном разведении электролита обязательно следует добавлять кислоту в воду, но не наоборот! Эти жидкости имеют разную плотность, и результатом ошибки могут стать серьезные ожоги.
. Запрещено переворачивать АКБ вверх дном, т.к. вследствие этого активная поверхность пластин может осыпаться и вызвать короткое замыкание.
. Заранее подготовьте емкости для слива старого электролита и приготовления новой смеси.
. Предварительно проверьте пластмассу, которую будете использовать для запайки отверстий, на стойкость к электролиту.
. Помните, что заряженный аккумулятор будет иметь большую плотность.
Подготовительный этап
Для того чтобы поднять плотность электролита аккумуляторе, потребуются:
. ареометр;
. мерная емкость;
. клизма-груша;
. паяльник;
. дрель;
. электролит;
. аккумуляторная кислота;
. дистиллированная вода.
Как поднять плотность электролита в аккумуляторе: подробная инструкция
Производим замеры плотности электролита в каждой банке. Помня, какая должна быть
плотность в аккумуляторе, сопоставляем свои реальные показатели. Итак, если плотность составляет 1,25-1,28, а разброс значений в каждой банке не превышает 0,01, то аккумулятор вполне работоспособен, и каких-либо процедур ему не требуется. Если же показатели варьируются на уровне 1,18-1,20, то единственным вариантом будет долив электролита с плотностью 1,27.
Из одной банки откачайте с помощью клизмы-груши максимальное количество старого электролита и замеряйте его объем.
. Долейте свежий раствор в количестве, составляющем половину от откачанного.
. Активно, но аккуратно покачайте аккумулятор, чтобы перемешались жидкости.
. Замеряйте плотность. Если значение не такое, какая должна быть плотность в аккумуляторе, долейте еще ½ электролита от оставшегося количества. Операцию следует повторять, пока не получите требуемые показатели.
. Остаток долейте дистиллированной водой.
Что делать при критическом уровне плотности
Если показатель плотности ниже 1,18, то данную проблему решить доливом электролита не получится. В этом случае потребуется аккумуляторная кислота, имеющая существенно большую плотность. Данный процесс производится аналогично схеме добавления электролита. Если с одного раза не удалось достичь нужных результатов, повторяйте процедуру необходимое количество раз.
Если в аккумуляторе плотность даже ниже 1,18, то необходимо прибегнуть к процедуре полной замены электролита. Для этого сразу надо откачать с помощью груши максимальное количество раствора. Затем на аккумуляторных банках герметично закройте вентиляционные отверстия пробок. Поставьте АКБ набок и поочередно просверлите 3-3,5-миллиметровые отверстия в дне каждой из банок. Перед тем как проделывать очередное отверстие, из предыдущего сливайте остатки электролита.
Далее необходимо тщательно промыть дистиллированной водой. После этого запаяйте высверленные отверстия кислотостойкой пластмассой (к примеру, для этого можно использовать пробки с ненужного аккумулятора).
Проделав все подготовительные процедуры, можете приступать к заливке свежего электролита. В этом случае рекомендуется использовать раствор, приготовленный самостоятельно, плотность которого будет несколько выше, чем предусмотрена для вашего климатического пояса. При этом следует учесть, что даже полная замена электролита в старом аккумуляторе не сможет обеспечить ему такой же срок службы, как у новой АКБ.
Совет: если вы хотите, чтобы аккумулятор служил вам как можно дольше, не забывайте его вовремя заряжать и проверяйте периодически его плотность.
Аккумуляторная батарея – один из основных элементов автомобиля, отвечающих за пуск двигателя. Значение аккумулятора сложно переоценить, ведь без него невозможно завести мотор, а, значит, машина своим ходом передвигаться не сможет. Именно поэтому АКБ требует к себе особого внимания, исключающего возникновение неприятных ситуаций в виде невозможности совершить запланированную поездку. При этом стоит отметить, что для поддержания работоспособности это важного источника питания не требуется предпринимать каких-то сверхусилий, а достаточно выполнять лишь небольшой комплекс профилактических мер.
Свинцовая аккумуляторная батарея представляет собой гальванический элемент, внутри которого химическая энергия в результате протекающих реакций преобразуется в электрическую. Этот процесс невозможен без электролита – раствора кислоты, обеспечивающего движение заряженных частиц между погруженными в него электродами. Как правило, электролит представляет собой водный раствор серной кислоты определенной плотности. Именно такой параметр как плотность электролита оказывает значительное влияние на работоспособность аккумулятора, поэтому периодически его нужно контролировать.
Измерение плотности электролита в аккумуляторе
Измерить плотность залитого в свинцовый аккумулятор электролита не так уж сложно, однако есть определенные нюансы, связанные с особенностями устройства и принципом работы АКБ. Перечислим некоторые важные моменты, которые надо учесть:
- Осуществить процедуру измерения плотности получится только в случае с так называемым обслуживаемым аккумулятором, который предоставляет доступ к банкам (секциям) с электролитом посредством закрытых крышками заливных отверстий. Как раз через эти отверстия (обычно их число равно шести, как и количество секций) и осуществляется забор состава для замера плотности.
- В процессе своей работы автомобильная аккумуляторная батарея постоянно заряжается и разряжается. Разряд происходит при прокручивании стартера, а заряд – при уже заведенном двигателе от генератора. В зависимости от степени заряженности меняется и плотность электролита. Значения могут колебаться в пределах 0.15-0.16 г/см 3 . Важно отметить, что автомобильный генератор не способен полностью зарядить аккумуляторную батарею. При штатной работе на машине потенциал АКБ используется только на 80-90%. Полный заряд может обеспечить только внешнее зарядное устройство, к которому обязательно придется прибегнуть перед осуществлением замера плотности электролита.
- Плотность электролита зависит от его температуры. Обычно замер производится при температуре +25 °С, в противном случае делаются поправки.
Допустим, все вышеперечисленные условия приняты во внимание, и есть возможность приступить непосредственно к замеру плотности. Для этого понадобится специальный прибор – денсиметр, который состоит из ареометра, резиновой груши и стеклянной трубки с наконечником. Прибор вводится в банку аккумулятора через заливное отверстие, а затем осуществляется засасывание электролита с помощью резиновой груши. Оно происходит до тех пор, пока ареометр не всплывет. Показания считываются после того, как прекратятся колебания ареометра и появится возможность определения точного значения. Отсчет показаний производится по шкале, при этом взгляд должен находиться на уровне поверхности жидкости.
Полученное значение должно входить в диапазон 1.25-1.27 г/см 3 , если автомобиль эксплуатируется в средней полосе. В холодной климатической зоне (средняя месячная температура января ниже -15 °С) показатель должен находиться в интервале 1.27-1.29 г/см 3 . Проверять плотность электролита на соответствие этим числам нужно в каждой из шести банок аккумулятора. Показания не должны отличаться более чем на 0.01 г/см 3 , иначе потребуется их корректировка.
Как мы уже говорили, плотность электролита изменяется в зависимости от температуры. Это значит, что зимой и летом жидкость в одном и том же полностью исправном аккумуляторе будет иметь разную плотность. О том, насколько будут разниться показания, дает представление приведенная ниже таблица.
Зависимость температуры замерзания электролита от его плотности демонстрирует еще одна таблица. На основе этих данных можно установить оптимальную плотность электролита для конкретных климатических условий. Нижняя граница подобранного интервала должна гарантировать, что электролит не замерзнет даже при самых сильных холодах и обеспечит требуемое для прокручивания стартера усилие. В то же время чрезмерно завышать плотность тоже нельзя, так как на положительных электродах аккумулятора начинают ускоряться коррозионные процессы, приводящие к сульфатации пластин.
| Температура замерзания, °С | Плотность электролита при 25 °С, г/см 3 | Температура замерзания, °С | |
|---|---|---|---|
| 1.09 | -7 | 1.22 | -40 |
| 1.10 | -8 | 1.23 | -42 |
| 1.11 | -9 | 1.24 | -50 |
| 1.12 | -10 | 1.25 | -54 |
| 1.13 | -12 | 1.26 | -58 |
| 1.14 | -14 | 1.27 | -68 |
| 1.15 | -16 | 1.28 | -74 |
| 1.16 | -18 | 1.29 | -68 |
| 1.17 | -20 | 1.30 | -66 |
| 1.18 | -22 | 1.31 | -64 |
| 1.19 | -25 | 1.32 | -57 |
| 1.20 | -28 | 1.33 | -54 |
| 1.21 | -34 | 1.40 | -37 |
Причины изменения плотности электролита
Зафиксированные в результате измерения плотности значения не всегда соответствуют требуемым показателям. Расхождения могут касаться как отдельных банок аккумулятора, так и всех вместе. Если плотность завышена, то нужно обратить в первую очередь внимание на уровень электролита. Низкий уровень в большинстве случае является последствием электролиза, приводящего к разложению входящей в состав электролита воды на водород и кислород. Этот процесс выражается в появлении на поверхности жидкости пузырьков, что обычно происходит при зарядке аккумулятора. Частое «кипение» может приводить к снижению концентрации воды, и этот вопрос решается ее простым добавлением. Доливать в аккумулятор стоит только дистиллированную воду, контролируя при этом уровень электролита. Подробнее о корректировке плотности электролита поговорим ниже.
Если с повышенной плотностью все ясно, то с пониженной ситуация несколько сложнее. В теории, одной из причин понижения плотности, может быть то, что по какой-то причине в электролите уменьшилась доля серной кислоты. Однако на практике это маловероятно, так как сама по себе она обладает высокой температурой кипения, исключающей испарение даже при интенсивном нагреве, который происходит, например, при зарядке аккумуляторной батареи. Более распространенной причиной снижения плотности электролита является так называемая сульфатация пластин, заключающаяся в образовании на электродах сульфата свинца (PbSO4). На самом деле, это естественный процесс, происходящий при каждом разряде АКБ. Но дело в том, что при нормальном режиме работы после разряда аккумулятора обязательно происходит его заряд (на автомобиле аккумулятор постоянно подзаряжается от генератора). Заряд сопровождается обратным преобразованием сульфата свинца в свинец (на катоде) и двуокись свинца (на аноде) – в те активные вещества, которые составляют основу электродов и непосредственно участвуют в химическом процессе внутри аккумуляторной батареи. Если АКБ находится длительное время в разряженном состоянии, сульфат свинца кристаллизуется, безвозвратно теряя способность участвовать в химических реакциях. Это очень неприятный процесс, в результате которого аккумулятор уже не получится зарядить полностью даже при использовании внешнего зарядного устройства ввиду того, что не вся площадь пластин задействована в работе. Так как аккумулятор не заряжается до конца, то и плотность электролита не восстанавливается до своих исходных значений. По сути, здесь уже идет разговор об устранении нарушений в нормальном функционировании аккумулятора.
Частичную сульфатацию пластин можно устранить с помощью контрольно-тренировочных циклов, заключающихся в заряде и последующем разряде батареи до определенного уровня. Большинство современных зарядных устройств имеют такую функцию, поэтому имеет смысл ей воспользоваться, особенно если аккумулятор по какой-то причине долго находился в разряженном состоянии. Процедура десульфатации весьма длительная и может занять до нескольких дней. Если она не принесла результата, то крайней мерой является увеличение плотности с помощью добавления корректирующего электролита (плотность около 1.40 г/см 3). Такой способ можно рассматривать только как временное решение проблемы, потому что причина как таковая не устраняется.
Как поднять плотность электролита
Понизить или повысить плотность электролита в аккумуляторе можно путем откачивания его определенного количества, и долива взамен дистиллированной воды или электролита с повышенной плотностью (корректирующего). Данная процедура требует больших временных затрат, так как цикл откачки-долива может повторяться несколько раз, пока не будет достигнуто требуемое значение. После каждой корректировки необходимо поставить аккумулятор на зарядку (минимум на 30 минут), а затем дать ему постоять (0.5-2 часа). Эти действия необходимы для лучшего перемешивания электролита и выравнивания плотности в банках.
В процессе поднятия (или понижения) плотности электролита не стоит забывать и о контроле его уровня. Он осуществляется стеклянной трубкой с двумя отверстиями по краям. Один край погружается в электролит до тех пор, пока не упрется в предохранительную сетку. Далее верхний конец закрывается пальцем, а сама трубка осторожно поднимается вместе со столбиком жидкости внутри. Высота этого столбика указывает на расстояние от верхней кромки пластин до поверхности залитого электролита. Оно должно составлять 10-15 мм. Если аккумулятор имеет индикатор (тубус) или прозрачный корпус с нанесенными метками минимума и максимума, то контролировать уровень значительно проще.
Не стоит забывать, что все операции с электролитом необходимо выполнять осторожно, используя защитные перчатки и очки.
ЭффективностьАч — обзор
Помимо катастрофических отказов, срок службы LAB определяется факторами непрерывного старения, такими как коррозия сети, деградация активной массы (в основном сульфатирование или потеря целостности), деградация сепаратора и / или высыхание . Влияние этих факторов на срок службы батареи зависит от конструкции элемента (например, толщины пластины) и рабочих параметров (например, зарядных / разрядных токов, состояния заряда (SoC), температуры).
Глубина разряда и динамическое принятие заряда
Реакции заряда / разряда LAB происходят через стадии растворения и осаждения с большими изменениями объема между реагентами и продуктами, что приводит к внутреннему механическому напряжению, которое приводит к частичному разложению исходного материала. структура и увеличение внутреннего сопротивления.Этот эффект тем больше, чем глубже глубина разряда (DoD). Срок службы сокращается с увеличением DoD, как показано на рисунке 5.7.
Рисунок 5.7. Цикл жизни в сравнении с DoD спиральной батареи RLS-Exide (Rand and Moseley, 2009).
Воспроизведено с разрешения Elsevier.Для достижения долгого срока службы DoD должно быть ограничено настолько, насколько позволяет приложение.
Диапазон SoC, используемых в различных приложениях, схематично показан на рисунке 5.8.
Рисунок 5.8. Диапазоны заряда, используемые в различных приложениях.
Обычная батарея SLI обычно остается в диапазоне SoC выше 80%. Если бы аккумулятор SLI, рассчитанный на высокую мощность и низкую стоимость, был настроен на выполнение полных циклов, то его срок службы был бы всего около 50 циклов.
Для электромобилей (EV) и промышленных приложений (стационарные накопители энергии) аккумулятор предназначен для глубокого разряда, с более толстыми пластинами и / или положительными электродами трубчатого типа (см. Рисунок 5.1).
Особая проблема возникает в приложениях с полным или мягким гибридным электромобилем (HEV), которые до сих пор были областью применения NiMH и литий-ионных аккумуляторов. В обоих приложениях рабочее окно SoC обычно находится между примерно 70% (выше этого уровня даже мощные батареи теряют способность к быстрой зарядке, что обеспечивает полную функциональность рекуперативного торможения) и примерно 40% (ниже этого уровня мощность разряда и, следовательно, движущая сила). функциональность, а также долговечность из-за процессов старения, которым способствует глубокая разрядка).Таким образом, аккумулятор HEV обычно не работает в почти полностью заряженном состоянии. Когда обычные LAB подвергаются этому режиму частичного состояния заряда (PSoC), они быстро выходят из строя в результате сульфатирования отрицательной пластины. Кроме того, если аккумулятор оставить на PSoC в течение значительного периода времени, кристаллы сульфата свинца имеют возможность постепенно расти в процессе созревания Оствальда.
Восстановление первичной мелкокристаллической структуры активной массы, которая необходима для поддержания оптимальной емкости, зависит от того, насколько батарея доведена до полной SoC.Если, однако, полная SoC никогда не будет достигнута, часть продукта разряда PbSO 4 останется, и размер его кристалла увеличится. Во время высокоскоростной работы (HEV требуют кратковременных зарядов со скоростью до ~ 30 раз превышающей 1-часовую скорость) эти большие кристаллы PbSO 4 сначала образуют слои на поверхности электрода (см. Рисунок 5.9, 1735 циклов). С увеличением времени работы слой будет расширяться до внутренних областей электрода (см. Рисунок 5.9, 3191 цикл). Поскольку зарядный ток не может быть приспособлен к реакции, которая восстанавливает PbSO 4 до Pb, отрицательный потенциал пластины смещается к более отрицательному значению, и выделение водорода увеличивается.
Рисунок 5.9. Потенциал отрицательного электрода в зависимости от количества циклов во время циклирования HEV (50 ± 3% SoC) и изображения серы EMP, связанные с содержанием PbSO 4 при 1735 и 3191 циклах.
Предоставлено ALABC, Северная Каролина, США.Этот результат высокоскоростной работы PSoC, то есть сниженного приема заряда, приводит к быстрой потере емкости и короткому сроку службы при использовании обычных LAB.
Влияние этого режима работы может быть уменьшено, если электрохимические реакции (заряд / разряд) распределены по всей толщине электрода и по всей площади пластины однородно, а не на поверхности пластины и около наконечника отвода тока. .Более однородное распределение тока может быть достигнуто за счет оптимальной конструкции сетки и включения определенных форм дополнительного углерода на отрицательную пластину.
Система хранения в микрогибридных транспортных средствах должна поддерживать все функции батареи SLI, включая холодный запуск и резервное питание для парковки и потенциального отказа генератора. Тем не менее, рекуперация энергии торможения должна быть активирована при работе PSoC. Следовательно, рабочее окно SoC для аккумуляторов micro-HEV смещено вверх до диапазона от 75% до 90% (на самом деле даже меньше для данного транспортного средства, температуры и, возможно, других условий использования, которые стратегия регулирования генератора переменного тока автопроизводителя может учитывать. ).Этот рабочий диапазон соответствует значительно более низкому соотношению мощности / энергии, необходимому для неглубоких циклических профилей, вызванных остановкой / запуском и рекуперацией в микрогибридах, по сравнению с мягкими и полными гибридами. Например, при отключении или восстановлении в течение 36 с при 60 А для батареи на 60 Ач произойдет только 1% оборота энергии. Оба параметра, приведенные в приведенном выше примере, превышают типичную продолжительность и токи остановки нагрузки или рекуперации, соответственно (то есть типичный DoD в микрогибридах значительно ниже 1%).Как следствие, циклический износ не сильно ускоряется и по-прежнему позволяет использовать (улучшенные) залитые батареи в большинстве микрогибридных автомобилей, но сульфатирование из-за прогрессирующей недозарядки может стать серьезной проблемой. Такая недозарядка, как правило, не приводит к раннему отказу с точки зрения производительности или мощности проворачивания, но ограничивает реальную экономию топлива за счет рекуперативного торможения, задерживает восстановление SoC после событий остановки / запуска или разрядки при выключении ключа и снижает доступность функция остановки / запуска.Эти эффекты наблюдались как для залитых автомобильных аккумуляторов, так и для автомобильных аккумуляторов типа AGM и иногда называются феноменом ленивых аккумуляторов .
И в мягких, и в микрогибридных приложениях, или с точки зрения аккумуляторов, в приложениях с частичным циклом, способность аккумулятора надежно поглощать высокие зарядные токи стала решающей. Было предложено назвать этот атрибут производительности динамическим принятием заряда (DCA; Karden et al., 2005), и впервые он станет частью стандарта батарей в новой европейской норме для микрогибридных батарей 12 В (Разработка стандартов, 2014).Следует подчеркнуть, что медлительность и непоследовательность (сильная зависимость от краткосрочной истории цикличности) DCA является технологической проблемой LAB, независимо от того, затоплены ли они или регулируются клапанами, но редко встречаются с другими технологиями хранения. Механически это можно объяснить тем, что растворение сульфата свинца является этапом, определяющим скорость реакции зарядки, которая не зависит от приложенного потенциала (Sauer et al., 2007) и усугубляется кислотным расслоением в затопленных батареях (Ebner et al. al., 2013). Модификации отрицательного электрода, макроскопически или микроскопически, позволяют существенно улучшить DCA и будут обсуждаться ниже.
Создание безопасных литий-ионных батарей для электромобилей: обзор
Уиттингем, М.С.: Литиевые батареи и катодные материалы. Chem. Ред. 104 , 4271–4302 (2004). https://doi.org/10.1021/cr020731c
CAS Статья PubMed Google ученый
Чжоу, Л.М., Чжан, К., Ху, З. и др .: Последние разработки и перспективы электродных материалов с иерархической структурой для литий-ионных аккумуляторов. Adv. Energy Mater. 8 , 1701415 (2018). https://doi.org/10.1002/aenm.201701415
CAS Статья Google ученый
Wei, Q.L., Xiong, F.Y., Tan, S.S., et al .: Накопление энергии: пористые одномерные наноматериалы: дизайн, изготовление и применение в электрохимическом накоплении энергии.Adv. Матер. 29 , 1602300 (2017). https://doi.org/10.1002/adma.201770134
CAS Статья Google ученый
Хао, Х., Ченг, X., Лю, З.У. и др.: Дорожная карта технологии тяговых аккумуляторных батарей в Китае: цели, воздействия и проблемы. Энергетическая политика 108 , 355–358 (2017). https://doi.org/10.1016/j.enpol.2017.06.011
Артикул Google ученый
Дин, Ю.Л., Кано, З.П., Ю., А.П. и др.: Автомобильные литий-ионные аккумуляторы: текущее состояние и перспективы на будущее. Электрохим. Energ. Ред. 2 , 1–28 (2019). https://doi.org/10.1007/s41918-018-0022-z
CAS Статья Google ученый
Wu, H.L., Zhang, Y.B., Deng, Y.Q., и др .: Легкая трехмерная структурированная матрица на основе углеродных нановолокон с высоким уровнем легирования азотом для анодов металлического лития. Sci. China Mater. 62 , 87–94 (2019). https://doi.org/10.1007/s40843-018-9298-x
CAS Статья Google ученый
Ли С., Цзян М. В., Се Ю. и др.: Разработка высокоэффективного металлического литиевого анода в жидких электролитах: проблемы и прогресс. Adv. Матер. 30 , 1706375 (2018). https://doi.org/10.1002/adma.201706375
CAS Статья Google ученый
Ли У.Д., Лю X.M., Селио Х. и др.: Mn по сравнению с Al в слоистых оксидных катодах в литий-ионных батареях: всесторонняя оценка длительной циклируемости. Adv. Energy Mater. 8 , 1703154 (2018). https://doi.org/10.1002/aenm.201703154
CAS Статья Google ученый
Li, Y., Li, X.H., Wang, Z.X. и др .: Путь созревания Оствальда к богатому никелем слоистому катодному материалу с богатой кобальтом поверхностью для литий-ионных аккумуляторов.Sci. China Mater. 61 , 719–727 (2018). https://doi.org/10.1007/s40843-017-9162-3
CAS Статья Google ученый
Лю, З.Х., Ю, К., Чжао, Ю.Л. и др .: Оксиды кремния: многообещающее семейство анодных материалов для литий-ионных аккумуляторов. Chem. Soc. Ред. 48 , 285–309 (2019). https://doi.org/10.1039/c8cs00441b
CAS Статья PubMed Google ученый
Дин, X.L., Лю, X.X., Хуанг, Y.Y. и др.: Повышенные электрохимические характеристики, которым способствуют однослойный графен и пустоты в кремниевых композитных анодных материалах. Nano Energy 27 , 647–657 (2016). https://doi.org/10.1016/j.nanoen.2016.07.031
CAS Статья Google ученый
Но, Х.Дж., Юн, С., Юн, С.С. и др .: Сравнение структурных и электрохимических свойств слоистого Li [Ni x Co y Mnz] O 2 ( x = 1/3, 0.5, 0,6, 0,7, 0,8 и 0,85) катодный материал для литий-ионных аккумуляторов. J. Источники энергии 233 , 121–130 (2013). https://doi.org/10.1016/j.jpowsour.2013.01.063
CAS Статья Google ученый
Цао, Г.З .: Синергия сольвента и соли предлагает безопасный путь к созданию высоковольтных литий-ионных аккумуляторов нового поколения. Sci. China Mater. 61 , 1360–1362 (2018). https://doi.org/10.1007/s40843-018-9296-y
CAS Статья Google ученый
Пэн П., Цзян Ф.М .: Тепловая безопасность литий-ионных батарей с различными катодными материалами: численное исследование. Int. J. Heat Mass Transf. 103 , 1008–1016 (2016). https://doi.org/10.1016/j.ijheatmasstransfer.2016.07.088
CAS Статья Google ученый
Рен, Д.С., Фенг, X.N., Лу, Л.Г., и др .: Модель литий-ионного аккумулятора с электрохимико-термической связью перезаряда и теплового разгона. J. Источники энергии 364 , 328–340 (2017).https://doi.org/10.1016/j.jpowsour.2017.08.035
CAS Статья Google ученый
Ши, Дж. Л., Фанг, Л. Ф., Ли, Х. и др .: Улучшенные термические и электрохимические характеристики каркаса сепаратора из модифицированного ПММА PE, полученного с помощью инициированного допамином ATRP для литий-ионных батарей. J. Membr. Sci. 437 , 160–168 (2013). https://doi.org/10.1016/j.memsci.2013.03.006
CAS Статья Google ученый
Равдель Б., Абрахам К.М., Гитценданнер Р. и др.: Термическая стабильность электролитов литий-ионных аккумуляторов. J. Источники энергии 119 (120/121), 805–810 (2003). https://doi.org/10.1016/s0378-7753(03)00257-x
Артикул Google ученый
Ли, Дж. К., Ма, К., Чи, М. Ф. и др .: Твердый электролит: ключ к высоковольтным литиевым батареям. Adv. Energy Mater. 5 , 1401408 (2015). https://doi.org/10.1002 / aenm.201401408
CAS Статья Google ученый
Джу, С.Ю., Ван, Ю.В., Шу, К.М. и др .: Опасность теплового взрыва на литий-ионных батареях 18650 с адиабатическим калориметром VSP2. J. Hazard. Матер. 192 , 99–107 (2011). https://doi.org/10.1016/j.jhazmat.2011.04.097
CAS Статья PubMed Google ученый
Фенг, Х.Н., Фанг, М., Хе, X.M. и др .: Характеристики теплового разгона крупноформатной призматической литий-ионной батареи с использованием калориметрии с увеличенной скоростью ускорения. J. Источники энергии 255 , 294–301 (2014). https://doi.org/10.1016/j.jpowsour.2014.01.005
CAS Статья Google ученый
Park, S., Jung, D .: Расположение аккумуляторных элементов и влияние теплоносителя на паразитное энергопотребление и распределение температуры элементов в гибридном электромобиле.J. Источники энергии 227 , 191–198 (2013). https://doi.org/10.1016/j.jpowsour.2012.11.039
CAS Статья Google ученый
Zhu, L.T., Sun, Z.C., Dai, H.F., et al .: Новая методология моделирования гистерезиса напряжения холостого хода для LiFePO 4 батарей, основанная на адаптивной дискретной модели Preisach. Прил. Энергетика 155 , 91–109 (2015). https://doi.org/10.1016/j.apenergy.2015.05.103
CAS Статья Google ученый
Ван, X.Y., Вэй, X.Z., Дай, Х.Ф .: Оценка состояния литий-ионных батарей на основе сопротивления переносу заряда с учетом различных температур и степени заряда. J. Хранение энергии 21 , 618–631 (2019). https://doi.org/10.1016/j.est.2018.11.020
Артикул Google ученый
Венгер М., Валлер Р., Лоренц В. Р. Х. и др.: Исследование газового зондирования в больших литий-ионных аккумуляторных системах для раннего обнаружения неисправностей и повышения безопасности.В: IECON 2014—40-я ежегодная конференция Общества промышленной электроники IEEE 29 октября — 1 ноября 2014 г. IEEE, Даллас, Техас, США. Нью-Йорк, США. https://doi.org/10.1109/iecon.2014.7049366
Wandt, J., Marino, C., Gasteiger, H.A., и др .: Электронная парамагнитная резонансная спектроскопия Operando — образование замшелого лития на литиевых анодах во время циклического заряда-разряда. Energy Environ. Sci. 8 , 1358–1367 (2015). https://doi.org/10.1039/c4ee02730b
CAS Статья Google ученый
Шей, А.Г., Бхадра, С., Герцберг, Б.Дж., и др.: Электрохимико-акустическое время полета: в действующей корреляции физической динамики с зарядом аккумулятора и здоровьем. Energy Environ. Sci. 8 , 1569–1577 (2015). https://doi.org/10.1039/c5ee00111k
CAS Статья Google ученый
Шарма, Н., Петерсон, В.К., Элкомб, М.М. и др .: Структурные изменения в коммерческой литий-ионной батарее во время электрохимического циклирования: исследование нейтронной дифракции на месте.J. Источники энергии 195 , 8258–8266 (2010). https://doi.org/10.1016/j.jpowsour.2010.06.114
CAS Статья Google ученый
Скросати, Б .: История литиевых батарей. J. Solid State Electrochem. 15 , 1623–1630 (2011). https://doi.org/10.1007/s10008-011-1386-8
CAS Статья Google ученый
Ли, X.Y., Wang, Z.П .: Новый метод диагностики неисправностей литий-ионных аккумуляторных батарей электромобилей. Измерение 116 , 402–411 (2018). https://doi.org/10.1016/j.measurement.2017.11.034
Артикул Google ученый
Ван, Й., Гао, К., Ван, Г. Х. и др .: Обзор состояния исследований и ключевых технологий управления температурным режимом аккумуляторной батареи и ее повышенной безопасности. Int. J. Energy Res. 42 , 4008–4033 (2018). https: // doi.org / 10.1002 / er.4158
Артикул Google ученый
Голубков, А.В., Фукс, Д .: Термический сбой: причины и последствия на клеточном уровне. В: Thaler, A., Watzenig, D. (eds.) Automotive Battery Technology, стр. 37–51. Спрингер, Чам (2014). https://doi.org/10.1007/978-3-319-02523-0_3
Глава Google ученый
Вен, Дж. У., Ю. Ю., Чен, К. Х .: Обзор вопросов безопасности литий-ионных батарей: существующие проблемы и возможные решения.Матер. Экспресс 2 , 197–212 (2012). https://doi.org/10.1166/mex.2012.1075
CAS Статья Google ученый
Чжан, Р., Чжэн, Ю., Дуань, Дж. И др .: Аккумуляторы для электромобилей: возможности и проблемы. Наука 358 , 10–13 (2017). (спецвыпуск)
Артикул Google ученый
Мингао, О., Рен, Д.С., Лу, LG и др .: Анализ замирания емкости из-за перезаряда для литий-ионных аккумуляторов большого формата с Li y Ni 1/3 Co 1/3 Mn 1/3 O 2 + Li y Mn 2 O 4 композитный катод. J. Источники энергии 279 , 626–635 (2015). https://doi.org/10.1016/j.jpowsour.2015.01.051
CAS Статья Google ученый
Цзэн Ю.К., Ву К., Ван Д.Ю. и др.: Исследование перезарядки литий-ионных полимерных батарей. J. Источники энергии 160 , 1302–1307 (2006). https://doi.org/10.1016/j.jpowsour.2006.02.009
CAS Статья Google ученый
Ирияма, Ю., Йокояма, М., Яда, С. и др.: Получение тонких пленок LiFePO 4 методом импульсного лазерного осаждения и их электрохимические свойства. Электрохим. Solid-State Lett. 7 , A340 (2004). https://doi.org/10.1149/1.17
CAS Статья Google ученый
Осаки Т., Киши Т., Кубоки Т. и др .: Реакция перезаряда литий-ионных аккумуляторов. J. Источники энергии 146 , 97–100 (2005). https://doi.org/10.1016/j.jpowsour.2005.03.105
CAS Статья Google ученый
Ву, Л.Дж., Нам, К.W., Wang, X.J. и др .: Структурное происхождение термической нестабильности, вызванной перезарядкой Ni-содержащих слоистых катодов для литиевых батарей с высокой плотностью энергии. Chem. Матер. 23 , 3953–3960 (2011). https://doi.org/10.1021/cm201452q
CAS Статья Google ученый
Wang, HY, Tang, AD, Huang, KL: выделение кислорода в перезаряженном Li x Ni 1/3 Co 1/3 Mn 1/3 O 2 электрод и кинетика его термического анализа.Подбородок. J. Chem. 29 , 1583–1588 (2011). https://doi.org/10.1002/cjoc.201180284
CAS Статья Google ученый
Юань, Q.F., Zhao, F.G., Wang, W.D., и др .: Исследование отказов перезаряда литий-ионных батарей. Электрохим. Acta 178 , 682–688 (2015). https://doi.org/10.1016/j.electacta.2015.07.147
CAS Статья Google ученый
Zheng, HH, Sun, QN, Liu, G., et al .: Корреляция между поведением растворения и характеристиками электрохимического цикла для LiNi 1/3 Co 1/3 Mn 1/3 O 2 — на основе ячеек. J. Источники энергии 207 , 134–140 (2012). https://doi.org/10.1016/j.jpowsour.2012.01.122
CAS Статья Google ученый
Wu, X.W., Wang, Z.X., Li, X.H. и др .: Влияние дифтор (оксалато) бората лития и гептаметилдисилазана с различными концентрациями на циклические характеристики LiMn 2 O 4 .J. Источники энергии 204 , 133–138 (2012). https://doi.org/10.1016/j.jpowsour.2011.12.012
CAS Статья Google ученый
Abraham, D.P., Spila, T., Furczon, M.M., et al .: Доказательства накопления переходных металлов на состаренных графитовых анодах с помощью SIMS. Электрохим. Solid-State Lett. 11 , А226 (2008). https://doi.org/10.1149/1.2987680
CAS Статья Google ученый
Шарма, Н., Петерсон, В.К .: Избыточная зарядка литий-ионной батареи: влияние на отрицательный электрод Li x C6, определенное методом дифракции нейтронов на месте. J. Источники энергии 244 , 695–701 (2013). https://doi.org/10.1016/j.jpowsour.2012.12.019
CAS Статья Google ученый
Li, Z., Huang, J., Yann Liaw, B., et al .: Обзор осаждения лития в литий-ионных и литий-металлических вторичных батареях.J. Источники энергии 254 , 168–182 (2014). https://doi.org/10.1016/j.jpowsour.2013.12.099
CAS Статья Google ученый
Abraham, D.P., Roth, E.P., Kostecki, R., et al .: Диагностическое обследование подвергшихся термическому износу мощных литий-ионных элементов. J. Источники энергии 161 , 648–657 (2006). https://doi.org/10.1016/j.jpowsour.2006.04.088
CAS Статья Google ученый
Зинт, В., фон Людерс, К., Хофманн, М. и др.: Литиевые покрытия в литий-ионных батареях при температурах ниже окружающей среды исследованы методом нейтронографии на месте. J. Источники энергии 271 , 152–159 (2014). https://doi.org/10.1016/j.jpowsour.2014.07.168
CAS Статья Google ученый
Ли, Х.Ф., Гао, Дж.К., Чжан, С.Л .: Влияние переразряда на набухание и характеристики перезарядки литий-ионных элементов.Подбородок. J. Chem. 26 , 1585–1588 (2008). https://doi.org/10.1002/cjoc.2008
CAS Статья Google ученый
Чжан Л.Л., Ма, Ю.Л., Ченг, X.Q. и др.: Механизм уменьшения емкости во время длительного цикла переразряженной батареи LiCoO 2 / мезоуглеродных микрогранул. J. Источники энергии 293 , 1006–1015 (2015). https://doi.org/10.1016/j.jpowsour.2015.06.040
CAS Статья Google ученый
Чжао, М.С., Кариуки, С., Девальд, Х.Д. и др.: Электрохимическая стабильность меди в электролитах литий-ионных аккумуляторов. J. Electrochem. Soc. 147 , 2874 (2000). https://doi.org/10.1149/1.13
CAS Статья Google ученый
Гуо Р., Лу Л.Г., Оуян М.Г. и др .: Механизм всего процесса переразряда и внутреннего короткого замыкания, вызванного переразрядкой, в литий-ионных батареях. Sci. Rep. 6 , 30248 (2016). https://doi.org/10.1038/srep30248
CAS Статья PubMed PubMed Central Google ученый
Шу, Дж., Шуй, М., Сюй, Д. и др.: Сравнительное исследование поведения катодных материалов для литий-ионных батарей при переразрядке. J. Solid State Electrochem. 16 , 819–824 (2012). https://doi.org/10.1007/s10008-011-1484-7
CAS Статья Google ученый
Шу Дж., Шуй М., Хуанг Ф. Т. и др.: Новый взгляд на оксид лития-кобальта в широком диапазоне напряжений для литий-ионных аккумуляторов. J. Phys. Chem. C 114 , 3323–3328 (2010). https://doi.org/10.1021/jp
CAS Статья Google ученый
Перамунаж, Д .: Получение и электрохимическая характеристика сверхлитированной шпинели LiMn 2 O 4 . J. Electrochem. Soc. 145 , 1131 (1998).https://doi.org/10.1149/1.1838428
CAS Статья Google ученый
Чжу, Дж. Г., Сан, З. К., Вэй, X. З. и др .: Экспериментальные исследования метода импульсного нагрева переменного тока для автомобильных литий-ионных аккумуляторов большой мощности при отрицательных температурах. J. Источники энергии 367 , 145–157 (2017). https://doi.org/10.1016/j.jpowsour.2017.09.063
CAS Статья Google ученый
Jiang, J.C., Ruan, H.J., Sun, B.X. и др.: Уменьшенная низкотемпературная электротермическая модель для литий-ионных аккумуляторов. Прил. Энергия 177 , 804–816 (2016). https://doi.org/10.1016/j.apenergy.2016.05.153
CAS Статья Google ученый
Чжан, С.С., Сюй, К., Джоу, Т.Р .: Исследование электрохимического импеданса при низких температурах литий-ионных аккумуляторов. Электрохим. Acta 49 , 1057–1061 (2004).https://doi.org/10.1016/j.electacta.2003.10.016
CAS Статья Google ученый
Эррейр С., Хюше О., Баруссо С. и др.: Новые литий-ионные электролиты для низкотемпературных применений. J. Источники энергии 97 (98), 576–580 (2001). https://doi.org/10.1016/s0378-7753(01)00670-x
Артикул Google ученый
Zhu, J.G., Sun, Z.К., Вей, X.Z. и др .: Метод нагрева литий-ионных аккумуляторов переменным током от отрицательных температур. Int. J. Energy Res. 40 , 1869–1883 (2016). https://doi.org/10.1002/er.3576
CAS Статья Google ученый
Смарт, М.С., Ратнакумар, Б.В., Уитканак, Л.Д., и др .: Улучшенные низкотемпературные характеристики литий-ионных элементов с электролитами на основе четвертичных карбонатов. J. Источники энергии 119 (120/121), 349–358 (2003).https://doi.org/10.1016/s0378-7753(03)00154-x
Артикул Google ученый
Сенишин, А., Мюльбауэр, М.Дж., Долотко, О. и др .: Низкотемпературные характеристики литий-ионных аккумуляторов: поведение литированного графита. J. Источники энергии 282 , 235–240 (2015). https://doi.org/10.1016/j.jpowsour.2015.02.008
CAS Статья Google ученый
Орсини, Ф., дю Паскье, А., Бодуан, Б. и др .: Наблюдение с помощью сканирующей электронной микроскопии (СЭМ) на границе раздела в пластиковых литиевых батареях. J. Источники энергии 76 , 19–29 (1998). https://doi.org/10.1016/s0378-7753(98)00128-1
CAS Статья Google ученый
Ким, Г.Х., Песаран, А., Спотниц, Р .: Трехмерная модель термического воздействия для литий-ионных элементов. J. Источники энергии 170 , 476–489 (2007).https://doi.org/10.1016/j.jpowsour.2007.04.018
CAS Статья Google ученый
Малеки, Х .: Исследования термостабильности литий-ионных элементов и компонентов. J. Electrochem. Soc. 146 , 3224 (1999). https://doi.org/10.1149/1.13
CAS Статья Google ученый
Чжао, Р., Чжан, С.Дж., Лю, Дж. И др .: Обзор методов улучшения тепловых характеристик литий-ионной батареи: модификация электродов и система терморегулирования.J. Источники энергии 299 , 557–577 (2015). https://doi.org/10.1016/j.jpowsour.2015.09.001
CAS Статья Google ученый
Лю, штаб-квартира, Вэй, З.Б., Хе, В.Д. и др .: Тепловые проблемы литий-ионных аккумуляторов и недавний прогресс в системах управления температурным режимом аккумуляторов: обзор. Energy Convers. Manag. 150 , 304–330 (2017). https://doi.org/10.1016/j.enconman.2017.08.016
CAS Статья Google ученый
Фэн X.N., Оуян М.Г., Лю X. и др.: Механизм теплового разгона литий-ионной батареи для электромобилей: обзор. Материя хранения энергии. 10 , 246–267 (2018). https://doi.org/10.1016/j.ensm.2017.05.013
Артикул Google ученый
Даути, Д.Х., Крафтс, К.К .: FreedomCAR: руководство по испытаниям на злоупотребление системой накопления электроэнергии для электрических и гибридных электромобилей. Выключенный. Sci. Tech.Инф. (2006). https://doi.org/10.2172/889934
Артикул Google ученый
Myung, S.T., Maglia, F., Park, K.J., et al .: Богатые никелем слоистые катодные материалы для автомобильных литий-ионных аккумуляторов: достижения и перспективы. ACS Energy Lett. 2 , 196–223 (2017). https://doi.org/10.1021/acsenergylett.6b00594
CAS Статья Google ученый
Jiang, J., Dahn, J.R .: ARC-исследования термической стабильности трех различных катодных материалов: LiCoO 2 ; Li [Ni 0,1 Co 0,8 Mn 0,1 ] O 2 ; и LiFePO 4 , в электролитах LiPF6 и LiBoB EC / DEC. Электрохим. Commun. 6 , 39–43 (2004). https://doi.org/10.1016/j.elecom.2003.10.011
CAS Статья Google ученый
Андерссон, А.: Извлечение / введение лития в LiFePO 4 : исследование дифракции рентгеновских лучей и мессбауэровской спектроскопии. Ионика твердого тела 130 , 41–52 (2000). https://doi.org/10.1016/s0167-2738(00)00311-8
CAS Статья Google ученый
Рёдер П., Баба Н., Фридрих К.А. и др .: Влияние делитированного Li 0 FePO 4 на разложение электролита на основе LiPF 6 исследовано с ускорением. калориметрия.J. Источники энергии 236 , 151–157 (2013). https://doi.org/10.1016/j.jpowsour.2013.02.044
CAS Статья Google ученый
Дан, Дж., Фуллер, Э., Обровац, М. и др .: Термическая стабильность Li x CoO 2 , Li x NiO 2 и λ-MnO 2 и последствия для безопасности литий-ионных элементов. Ионика твердого тела 69 , 265–270 (1994).https://doi.org/10.1016/0167-2738(94)
-4
CAS Статья Google ученый
Цао, Х., Ся, Б.Дж., Сюй, Н.Х. и др .: Структурные и электрохимические характеристики катодных материалов никелата лития, легированных Co и Al, для литий-ионных аккумуляторов. J. Alloy. Compd. 376 , 282–286 (2004). https://doi.org/10.1016/j.jallcom.2004.01.008
CAS Статья Google ученый
Yabuuchi, N., Ohzuku, T.: Новый литиевый вставной материал из LiCo 1/3 Ni 1/3 Mn 1/3 O 2 для усовершенствованных литий-ионных батарей. J. Источники энергии 119 (120/121), 171–174 (2003). https://doi.org/10.1016/S0378-7753(03)00173-3
CAS Статья Google ученый
Bak, SM, Hu, EY, Zhou, YN и др .: Структурные изменения и термическая стабильность заряженного LiNi x Mn y Co z O 2 катод материалы изучены с помощью комбинированной in situ рентгеновской дифрактометрии и масс-спектроскопии с временным разрешением.ACS Appl. Матер. Интерфейсы. 6 , 22594–22601 (2014). https://doi.org/10.1021/am506712c
CAS Статья PubMed Google ученый
Лян, К.П., Конг, Ф.Т., Лонго, Р.К. и др .: Выявление причин нестабильности в Ni-Ni-Ni 1-2 x Co x Mn x O 2 (NCM) катодные материалы. J. Phys. Chem. C 120 , 6383–6393 (2016).https://doi.org/10.1021/acs.jpcc.6b00369
CAS Статья Google ученый
Ван, Ю. Д., Цзян, Дж. У., Дан, Дж. Р.: Реакционная способность делитированного Li (Ni 1/3 Co 1/3 Mn 1/3 ) O 2 , Li ( Ni 0,8 Co 0,15 Al 0,05 ) O 2 или LiCoO 2 с неводным электролитом. Электрохим. Commun. 9 , 2534–2540 (2007). https: // doi.org / 10.1016 / j.elecom.2007.07.033
CAS Статья Google ученый
Хванг, С., Ким, С. М., Бак, С. М. и др .: Исследование локальной деградации и термической стабильности заряженных катодных материалов на основе никеля с помощью электронной микроскопии в реальном времени. ACS Appl. Матер. Интерфейсы. 6 , 15140–15147 (2014). https://doi.org/10.1021/am503278f
CAS Статья PubMed Google ученый
Bang, HJ, Joachin, H., Yang, H., et al .: Вклад структурных изменений LiNi 0,8 Co 0,15 Al 0,05 O 2 катодов на экзотермические реакции в Li-ion клетки. J. Electrochem. Soc. 153 , A731 (2006). https://doi.org/10.1149/1.2171828
CAS Статья Google ученый
Belharouak, I., Lu, W.Q., Liu, J., et al .: Температурное поведение делитированного Li (Ni 0.8 Co 0,15 Al 0,05 ) O 2 и Li 1,1 (Ni 1/3 Co 1/3 Mn 1/3 ) 0,9 O 2 порошки. J. Источники энергии 174 , 905–909 (2007). https://doi.org/10.1016/j.jpowsour.2007.06.092
CAS Статья Google ученый
Hua, WB, Schwarz, B., Knapp, M., et al .: (Де) механизм литирования иерархически слоистого LiNi 1/3 Co 1/3 Mn 1/3 O 2 катодов при высоковольтном циклировании.J. Electrochem. Soc. 166 , A5025 – A5032 (2019). https://doi.org/10.1149/2.0051903jes
CAS Статья Google ученый
Чен, Ж., Рен, Ю., Ли, Э. и др .: Исследование термического разложения Li 1- x (Ni 1/3 Mn 1/3 Co 1/3 ) 0,9 O 2 с использованием дифракции рентгеновских лучей высоких энергий in situ. Adv. Energy Mater. 3 , 729–736 (2013).https://doi.org/10.1002/aenm.201201059
CAS Статья Google ученый
Миллер Д.Дж., Профф К., Вен Дж.Г. и др.: Наблюдение за эволюцией микроструктуры в частицах катодного оксида литиевых батарей с помощью in situ электронной микроскопии. Adv. Energy Mater. 3 , 1098–1103 (2013). https://doi.org/10.1002/aenm.201300015
CAS Статья Google ученый
Кондраков, А.О., Шмидт, А., Сюй, Дж. И др .: Анизотропная деформация решетки и механическая деградация катодных материалов NCM с высоким и низким содержанием никеля для литий-ионных аккумуляторов. J. Phys. Chem. С 121 , 3286–3294 (2017). https://doi.org/10.1021/acs.jpcc.6b12885
CAS Статья Google ученый
Дин, Ю., Му, Д. Б., Ву, Б. Р. и др .: Последние достижения в области материалов положительных электродов из слоистого оксида с высоким содержанием никеля, используемых в литий-ионных батареях для электромобилей.Прил. Энергия 195 , 586–599 (2017). https://doi.org/10.1016/j.apenergy.2017.03.074
CAS Статья Google ученый
Луо, В.Б., Чжоу, Ф., Чжао, XM и др .: Синтез, характеристика и термическая стабильность LiNi 1/3 Mn 1/3 Co 1/3 — z Mg z O 2 , LiNi 1 / 3- z Mn 1/3 Co 1/3 Mg z O 2 и LiNi 1/3 Mn 1 / 3- z Co 1/3 Mg z O 2 .Chem. Матер. 22 , 1164–1172 (2010). https://doi.org/10.1021/cm
CAS Статья Google ученый
Сан Ю.К., Ким Д.Х., Юн К.С. и др.: Новый катодный материал с градиентом концентрации для высокоэнергетических и безопасных литий-ионных батарей. Adv. Функц. Матер. 20 , 485–491 (2010). https://doi.org/10.1002/adfm.200
CAS Статья Google ученый
Цзэн, X.Q., Чжан, К., Лу, Дж. И др .: Стабилизация мощного и мощного катода на никелевой основе для литий-ионных аккумуляторов. Chem 4 , 690–704 (2018). https://doi.org/10.1016/j.chempr.2017.12.027
CAS Статья Google ученый
Кам, К.С., Дофф, М.М .: Алиовалентное замещение титана в слоистых смешанных оксидах Li – Ni – Mn – Co для литиевых аккумуляторов. J. Mater. Chem. 21 , 9991 (2011).https://doi.org/10.1039/c0jm04193a
CAS Статья Google ученый
Liu, WM, Hu, GR, Peng, ZD и др .: Синтез сферического LiNi 0,8 Co 0,15 Al 0,05 O 2 катодных материалов для литий-ионных аккумуляторов метод кристаллизации, контролируемый совместным окислением. Подбородок. Chem. Lett. 22 , 1099–1102 (2011). https://doi.org/10.1016/j.cclet.2011.01.041
CAS Статья Google ученый
Li, X., Xie, Z.W., Liu, W.J. и др .: Влияние легирования фтором на структуру, химию поверхности и электрохимические характеристики LiNi 0,8 Co 0,15 Al 0,05 O 2 . Электрохим. Acta 174 , 1122–1130 (2015). https://doi.org/10.1016/j.electacta.2015.06.099
CAS Статья Google ученый
Ван, Ю., Гу, Х. Т., Сонг, Дж.J. Phys. Chem. C 122 , 27836–27842 (2018). https://doi.org/10.1021/acs.jpcc.8b08669
CAS Статья Google ученый
Растгоо-Дейлами, М., Джаванбахт, М., Омидвар, Х .: Повышенные характеристики слоистого Li 1,2 Mn 0,54 Ni 0,13 Co 0,13 O 2 катодный материал в Литий-ионные аккумуляторы с наноразмерным покрытием поверхности анатазом, легированным фтором TiO 2 .Ионика твердого тела 331 , 74–88 (2019). https://doi.org/10.1016/j.ssi.2018.12.025
CAS Статья Google ученый
Dai, GL, Du, HJ, Wang, SS и др .: Улучшенные электрохимические характеристики LiNi 0,8 Co 0,15 Al 0,05 O 2 с ультратонким и контролируемым по толщине TiO 2 с помощью технологии атомно-слоистого осаждения. RSC Adv. 6 , 100841–100848 (2016).https://doi.org/10.1039/c6ra21903a
CAS Статья Google ученый
Мюнг, С.Т., Изуми, К., Комаба, С. и др .: Роль покрытия оксидом алюминия на частицах Li – Ni – Co – Mn – O в качестве материала положительного электрода для литий-ионных аккумуляторов. Chem. Матер. 17 , 3695–3704 (2005). https://doi.org/10.1021/cm050566s
CAS Статья Google ученый
Yoon, WS, Nam, KW, Jang, D., и др .: Структурное исследование влияния покрытия на термическую стабильность заряженного покрытого MgO LiNi 0,8 Co 0,2 O 2 катодов, исследованных in situ XRD. J. Источники энергии 217 , 128–134 (2012). https://doi.org/10.1016/j.jpowsour.2012.05.028
CAS Статья Google ученый
Ли С.М., О, С.Х., Ан, Дж.П. и др .: Электрохимические свойства LiNi с покрытием ZrO 2 0.8 Co 0,2 O 2 катодные материалы. J. Источники энергии 159 , 1334–1339 (2006). https://doi.org/10.1016/j.jpowsour.2005.12.035
CAS Статья Google ученый
Мэн, X.B., Ян, X.Q., Sun, X.L .: Новые применения осаждения атомных слоев для исследований литий-ионных аккумуляторов. Adv. Матер. 24 , 3589–3615 (2012). https://doi.org/10.1002/adma.201200397
CAS Статья PubMed Google ученый
Ян П.Ф., Чжэн Дж.М., Чжан Х.Ф. и др.: Исследование функциональных возможностей слоя покрытия Al 2 O 3 на катоде для улучшения характеристик батареи на атомном и наноразмерном уровнях. Chem. Матер. 28 , 857–863 (2016). https://doi.org/10.1021/acs.chemmater.5b04301
CAS Статья Google ученый
Лю В., О, П., Лю, X.E. и др.: Богатый никелем слоистый оксид переходного металла лития для высокоэнергетических литий-ионных батарей.Энгью. Chem. Int. Эд. 54 , 4440–4457 (2015). https://doi.org/10.1002/anie.201409262
CAS Статья Google ученый
Manthiram, A., Knight, J.C., Myung, S.T. и др .: Катоды из слоистого оксида с высоким содержанием никеля и лития: прогресс и перспективы. Adv. Energy Mater. 6 , 1501010 (2016). https://doi.org/10.1002/aenm.201501010
CAS Статья Google ученый
Sun, YK, Myung, ST, Shin, HS и др .: Новый Li [(Ni 0,8 Co 0,2 ) со структурой ядро-оболочка 0,8 (Ni 0,5 Mn 0,5 ) 0,2 ] O 2 через соосаждение в качестве материала положительного электрода для литиевых вторичных батарей. J. Phys. Chem. B 110 , 6810–6815 (2006). https://doi.org/10.1021/jp0571473
CAS Статья PubMed Google ученый
Sun, Y.K., Bae, Y.C., Myung, S.T .: Синтез и электрохимические свойства слоистого LiNi 1/2 Mn 1/2 O 2 , полученного соосаждением. J. Appl. Электрохим. 35 , 151–156 (2005). https://doi.org/10.1007/s10800-004-6197-5
CAS Статья Google ученый
Сан Ю.К., Мён С.Т., Парк Б.С. и др .: Синтез сферических нано- и микромасштабных частиц ядро-оболочка Li [(Ni 0.8 Co 0,1 Mn 0,1 ) 1- x (Ni 0,5 Mn 0,5 ) x ] O 2 и их применения в литиевых батареях. Chem. Матер. 18 , 5159–5163 (2006). https://doi.org/10.1021/cm061746k
CAS Статья Google ученый
Сан, Ю.К., Чен, З.Х., Но, Х.Дж. и др.: Наноструктурированные высокоэнергетические катодные материалы для усовершенствованных литиевых батарей.Nat. Матер. 11 , 942–947 (2012). https://doi.org/10.1038/nmat3435
CAS Статья Google ученый
Park, KJ, Choi, MJ, Maglia, F., et al .: Высокопроизводительный градиент концентрации Li [Ni 0,865 Co 0,120 Al 0,015 ] O 2 катод для лития -ионовые батареи. Adv. Energy Mater. 8 , 1703612 (2018). https://doi.org/10.1002/aenm.201703612
CAS Статья Google ученый
Лу, Дж., Ву, Т.П., Амин, К .: Современные методы определения характеристик передовых литий-ионных аккумуляторов. Nat. Энергетика 2 , 17011 (2017). https://doi.org/10.1038/nenergy.2017.11
CAS Статья Google ученый
Ким, Х., Ким, М.Г., Чжон, Х.Й. и др .: Новый метод покрытия для уменьшения деградации поверхности LiNi 0,6 Co 0,2 Mn 0,2 O 2 Катодный материал : наноразмерная обработка поверхности первичных частиц.Nano Lett. 15 , 2111–2119 (2015). https://doi.org/10.1021/acs.nanolett.5b00045
CAS Статья PubMed PubMed Central Google ученый
Xu, X., Huo, H., Jian, JY, et al .: Литий-ионные батареи: радиально ориентированные монокристаллические первичные нанолисты обеспечивают сверхвысокую скорость и циклические свойства LiNi 0,8 Co 0,1 Mn 0,1 O 2 Катодный материал для литий-ионных аккумуляторов.Adv. Energy Mater. 9 , 1970051 (2019). https://doi.org/10.1002/aenm.201970051
Артикул Google ученый
Но, Х.Дж., Чен, З.Х., Юн, К.С. и др.: Катодный материал с наностержневой структурой: применение для усовершенствованных высокоэнергетических и безопасных литиевых батарей. Chem. Матер. 25 , 2109–2115 (2013). https://doi.org/10.1021/cm4006772
CAS Статья Google ученый
Лу, Дж., Чен, З.У., Пан, Ф. и др.: Высокоэффективные анодные материалы для литий-ионных аккумуляторных батарей. Электрохим. Energ. Ред. 1 , 35–53 (2018). https://doi.org/10.1007/s41918-018-0001-4
CAS Статья Google ученый
Таками, Н., Хосина, К., Инагаки, Х .: Диффузия лития в частицах Li 4/3 Ti 5/3 O 4 во время введения и извлечения. J. Electrochem.Soc. 158 , A725 (2011). https://doi.org/10.1149/1.3574037
CAS Статья Google ученый
Ву К., Янг Дж., Чжан Ю. и др.: Исследование Li 4 Ti 5 O 12 аккумуляторов, разработанных для гибридных электромобилей. J. Appl. Электрохим. 42 , 989–995 (2012). https://doi.org/10.1007/s10800-012-0442-0
CAS Статья Google ученый
Li, P.H., Wang, W., Gong, S. и др .: Hydrogenated Na 2 Ti 3 O 7 , эпитаксиально выращенный на гибкой углеродной губке с примесью азота для калий-ионных аккумуляторов. ACS Appl. Матер. Интерфейсы. 10 , 37974–37980 (2018). https://doi.org/10.1021/acsami.8b11354
CAS Статья PubMed Google ученый
Доу, Ф., Ши, Л.Й., Чен, Г.Р., и др .: Кремний / углеродные композитные анодные материалы для литий-ионных аккумуляторов.Электрохим. Energ. Ред. 2 , 149–198 (2019). https://doi.org/10.1007/s41918-018-00028-w
CAS Статья Google ученый
Веттер, Дж., Новак, П., Вагнер, М.Р. и др .: Механизмы старения в литий-ионных батареях. J. Источники энергии 147 , 269–281 (2005). https://doi.org/10.1016/j.jpowsour.2005.01.006
CAS Статья Google ученый
Chen, Z.H., Qin, Y., Ren, Y., et al .: Многоуровневое исследование термической стабильности литированного графита. Energy Environ. Sci. 4 , 4023 (2011). https://doi.org/10.1039/c1ee01786a
CAS Статья Google ученый
Барре, А., Дегилхем, Б., Гролло, С. и др .: Обзор механизмов старения литий-ионных аккумуляторов и оценок для автомобильных приложений. J. Источники энергии 241 , 680–689 (2013).https://doi.org/10.1016/j.jpowsour.2013.05.040
CAS Статья Google ученый
Xu, K .: Неводные жидкие электролиты для литиевых аккумуляторных батарей. Chem. Ред. 104 , 4303–4418 (2004). https://doi.org/10.1021/cr030203g
CAS Статья PubMed Google ученый
Zhao, L.W., Watanabe, I., Doi, T., et al.: ТГ-МС анализ межфазной границы твердого электролита (SEI) на графитовом отрицательном электроде в литий-ионных батареях. J. Источники энергии 161 , 1275–1280 (2006). https://doi.org/10.1016/j.jpowsour.2006.05.045
CAS Статья Google ученый
Waldmann, T., Hogg, B.I., Wohlfahrt-Mehrens, M .: Li-покрытие как нежелательная побочная реакция в коммерческих литий-ионных элементах — обзор. J. Источники энергии 384 , 107–124 (2018).https://doi.org/10.1016/j.jpowsour.2018.02.063
CAS Статья Google ученый
Ван, К.С., Сан, Дж. Х., Яо, X. Л. и др .: Температурное поведение литиированного графита с электролитом в литий-ионных батареях. J. Electrochem. Soc. 153 , A329 (2006). https://doi.org/10.1149/1.2139955
CAS Статья Google ученый
Аурбах, Д., Забан, А., Эйн-Эли, Ю. и др .: Недавние исследования корреляции между химией поверхности, морфологией, трехмерными структурами и характеристиками интеркаляционных анодов Li и Li-C в нескольких важных электролитных системах. J. Источники энергии 68 , 91–98 (1997). https://doi.org/10.1016/s0378-7753(97)02575-5
CAS Статья Google ученый
Спотниц, Р., Франклин, Дж .: Злоупотребление мощными литий-ионными элементами.J. Источники энергии 113 , 81–100 (2003). https://doi.org/10.1016/s0378-7753(02)00488-3
CAS Статья Google ученый
Юнг, Ю.С., Кавана, А.С., Райли, Л.А. и др.: Ультратонкое прямое атомное осаждение слоев на композитных электродах для высокопрочных и безопасных литий-ионных аккумуляторов. Adv. Матер. 22 , 2172–2176 (2010). https://doi.org/10.1002/adma.2001
CAS Статья PubMed Google ученый
Chen, Z., Hsu, P.C., Lopez, J., et al .: Быстрые и обратимые термочувствительные полимерные коммутационные материалы для более безопасных батарей. Nat. Энергетика 1 , 15009 (2016). https://doi.org/10.1038/nenergy.2015.9
CAS Статья Google ученый
Чжан С.С .: Обзор электролитных добавок для литий-ионных аккумуляторов. J. Источники энергии 162 , 1379–1394 (2006). https://doi.org/10.1016/j.jpowsour.2006.07.074
CAS Статья Google ученый
Чанг, Ю.С., Ю, С.Х., Ким, К.К .: Повышение температуры плавления полиэтилен-литий-ионного аккумуляторного сепаратора за счет покрытия поверхности полимерами, имеющими высокую термостойкость. Ind. Eng. Chem. Res. 48 , 4346–4351 (2009). https://doi.org/10.1021/ie
6zCAS Статья Google ученый
Орендорф, К.Дж .: Роль сепараторов в безопасности литий-ионных элементов. Электрохим. Soc. Интерфейс 21 , 61–65 (2012). https://doi.org/10.1149/2.f07122if
CAS Статья Google ученый
Ван, К.С., Сан, Дж. Х .: Повышение безопасности литий-ионных батарей с помощью 4-изопропилфенилдифенилфосфата. Матер. Lett. 61 , 3338–3340 (2007). https://doi.org/10.1016/j.matlet.2006.11.060
CAS Статья Google ученый
Ро, С.С., Сонг, К.В., Ким, К.К .: Влияние нерастворителя молекулярной структуры и его содержания на формирование макропористого полиарилатного слоя, нанесенного на полиэтиленовый сепаратор. Ind. Eng. Chem. Res. 50 , 12596–12605 (2011). https://doi.org/10.1021/ie201716m
CAS Статья Google ученый
Hu, S.Y., Lin, S.D., Tu, Y.Y., et al .: Новые полипропиленовые сепараторы с покрытием из арамидного нановолокна для литий-ионных батарей.J. Mater. Chem. А 4 , 3513–3526 (2016). https://doi.org/10.1039/c5ta08694a
CAS Статья Google ученый
Ли, Б.П., Мессерсмит, П.Б., Израэлачвили, Дж. Н. и др.: Клеи и покрытия на основе мидий. Анну. Rev. Mater. Res. 41 , 99–132 (2011). https://doi.org/10.1146/annurev-matsci-062910-100429
CAS Статья PubMed PubMed Central Google ученый
Уэйт, Дж. Х .: Сила мидий. Nat. Матер. 7 , 8–9 (2008). https://doi.org/10.1038/nmat2087
CAS Статья PubMed Google ученый
Lv, X., Li, H., Zhang, Z.Q., et al .: УФ-прививка полиэтиленового сепаратора для литий-ионной батареи. Phys. Процедуры 25 , 227–232 (2012). https://doi.org/10.1016/j.phpro.2012.03.076
CAS Статья Google ученый
Ямамото К., Танака Х., Сакагучи М. и др.: Четко определенный полиметилметакрилат, привитый к полиэтилену с помощью радикальной полимеризации с обратным переносом атома, инициированной пероксидами. Полимер 44 , 7661–7669 (2003). https://doi.org/10.1016/j.polymer.2003.10.006
CAS Статья Google ученый
Ко, Дж. М., Мин, Б. Г., Ким, Д. У. и др .: Литий-ионный аккумулятор тонкопленочного типа, в котором используется полиэтиленовый сепаратор с привитым глицидилметакрилатом.Электрохим. Acta 50 , 367–370 (2004). https://doi.org/10.1016/j.electacta.2004.01.127
CAS Статья Google ученый
Ли, Дж. Ю., Ли, Ю. М., Бхаттачарья, Б. и др .: Сепаратор, привитый силоксаном с помощью облучения электронным пучком для литиевых вторичных батарей. Электрохим. Acta 54 , 4312–4315 (2009). https://doi.org/10.1016/j.electacta.2009.02.088
CAS Статья Google ученый
Zhu, X.M., Jiang, X.Y., Ai, X.P., et al .: TiO 2 Сепараторы из полиэтилена с привитой керамикой для повышения термостабильности и электрохимических характеристик литий-ионных аккумуляторов. J. Membr. Sci. 504 , 97–103 (2016). https://doi.org/10.1016/j.memsci.2015.12.059
CAS Статья Google ученый
Xiang, Y.Y., Li, J.S., Lei, J.H., et al .: Усовершенствованные сепараторы для литий-ионных и литий-серных батарей: обзор последних достижений.Chemsuschem 9 , 3023–3039 (2016). https://doi.org/10.1002/cssc.201600943
CAS Статья PubMed Google ученый
Ли, Й., Ли, Х., Ли, Т. и др.: Синергетическая термостабилизация полипропиленовых сепараторов с керамическим / сополиимидным покрытием для литий-ионных аккумуляторов. J. Источники энергии 294 , 537–544 (2015). https://doi.org/10.1016/j.jpowsour.2015.06.106
CAS Статья Google ученый
Wang, J., Hu, Z.Y., Yin, X.N., et al .: Керамическая полипропиленовая разделительная пленка из глинозема / фенолфталеина и полиэфиркетона из керамического полипропилена для ионно-литиевых аккумуляторных батарей. Электрохим. Acta 159 , 61–65 (2015). https://doi.org/10.1016/j.electacta.2015.01.208
CAS Статья Google ученый
Чжу, X.M., Jiang, X.Y., Ai, X.P. и др .: высокотермостабильный микропористый полиэтиленовый сепаратор с привитой керамикой для более безопасных литий-ионных батарей.ACS Appl. Матер. Интерфейсы. 7 , 24119–24126 (2015). https://doi.org/10.1021/acsami.5b07230
CAS Статья PubMed Google ученый
Nho, Y.C., Sohn, J.Y., Shin, J., et al .: Получение нанокомпозита γ-Al 2 O 3 / полиэтиленовый сепаратор, сшитый облучением электронным пучком для литиевой вторичной батареи. Radiat. Phys. Chem. 132 , 65–70 (2017). https: // doi.org / 10.1016 / j.radphyschem.2016.12.002
CAS Статья Google ученый
Чен, Х., Линь, Q., Сюй, Q., и др .: Активация плазмой и осаждение атомного слоя TiO 2 на полипропиленовых мембранах для улучшения характеристик литий-ионных батарей. J. Membr. Sci. 458 , 217–224 (2014). https://doi.org/10.1016/j.memsci.2014.02.004
CAS Статья Google ученый
Пенг, К., Ван, Б., Ли, Ю.М. и др.: Осаждение частиц TiO 2 методом магнетронного распыления на полипропиленовых сепараторах для литий-ионных аккумуляторов. RSC Adv. 5 , 81468–81473 (2015). https://doi.org/10.1039/c5ra18171b
CAS Статья Google ученый
Ши К., Чжан П., Хуанг С.Х. и др .: Функциональный разделитель состоял из полиимидных нетканых материалов и слоя полиэтиленового покрытия для литий-ионных аккумуляторов.J. Источники энергии 298 , 158–165 (2015). https://doi.org/10.1016/j.jpowsour.2015.08.008
CAS Статья Google ученый
Wang, Z.H., Xiang, H.F., Wang, L.J., et al .: Неорганический композитный сепаратор на бумажной основе для литий-ионных аккумуляторов с высокой безопасностью. J. Membr. Sci. 553 , 10–16 (2018). https://doi.org/10.1016/j.memsci.2018.02.040
CAS Статья Google ученый
Гонг В.З., Вей С.Ю., Руан С.Л. и др.: Коаксиальные волокнистые мембраны из ППЭСК / ПВДФ из электропряденого волокна со свойством теплового отключения, используемые для литий-ионных аккумуляторов. Матер. Lett. 244 , 126–129 (2019). https://doi.org/10.1016/j.matlet.2019.02.009
CAS Статья Google ученый
Zhang, H., Zhang, Y., Xu, T.G., et al .: Сепаратор из поли (м-фениленизофталамида) для повышения термостойкости и удельной мощности литий-ионных аккумуляторов.J. Источники энергии 329 , 8–16 (2016). https://doi.org/10.1016/j.jpowsour.2016.08.036
CAS Статья Google ученый
Ли, Дж. Р., Вон, Дж. Х., Ким, Дж. Х. и др .: Самособирающиеся нанопористые нанопористые частицы с участием коллоидных частиц диоксида кремния, вызванные испарением, нетканых композитных сепараторов из полиэтилентерефталата для обеспечения высокой безопасности. высокопроизводительные литий-ионные аккумуляторы. J. Источники энергии 216 , 42–47 (2012).https://doi.org/10.1016/j.jpowsour.2012.05.052
CAS Статья Google ученый
Чжай, Ю.Ю., Ван, Н., Мао, X. и др .: Нановолоконные сепараторы из ПВдФ / ПММА / ПВдФ с сэндвич-структурой с высокой механической прочностью и термической стабильностью для литий-ионных аккумуляторов. J. Mater. Chem. А 2 , 14511–14518 (2014). https://doi.org/10.1039/c4ta02151g
CAS Статья Google ученый
Jeon, K.S., Nirmala, R., Navamathavan, R., et al .: Исследование эффективности Al 2 O 3 покрытых каплями мета-арамидных нановолокон с капельным покрытием в качестве разделительной мембраны в литий-ионных вторичных батареях. Матер. Lett. 132 , 384–388 (2014). https://doi.org/10.1016/j.matlet.2014.06.117
CAS Статья Google ученый
Ли, Дж., Ли, К.Л., Парк, К. и др .: Синтез мата из полиимидного нановолокна с покрытием из Al 2 O 3 и его электрохимические характеристики в качестве сепаратора для ионов лития батареи.J. Источники энергии 248 , 1211–1217 (2014). https://doi.org/10.1016/j.jpowsour.2013.10.056
CAS Статья Google ученый
Jiang, F.J., Yin, L., Yu, Q.C. и др .: Нановолоконная мембрана из бактериальной целлюлозы в качестве термостабильного сепаратора для литий-ионных аккумуляторов. J. Источники энергии 279 , 21–27 (2015). https://doi.org/10.1016/j.jpowsour.2014.12.090
CAS Статья Google ученый
Крол, Л.Ф., Беневенти, Д., Аллоин, Ф. и др .: Микрофибриллированная целлюлоза-SiO 2 композитные нанобумаги, полученные методом напыления. J. Mater. Sci. 50 , 4095–4103 (2015). https://doi.org/10.1007/s10853-015-8965-5
CAS Статья Google ученый
Chun, S.J., Choi, E.S., Lee, E.H., et al .: Экологически чистые мембраны из целлюлозного нановолокна из бумажных материалов с настраиваемыми сетевыми нанопористыми каналами для литий-ионных аккумуляторов.J. Mater. Chem. 22 , 16618 (2012). https://doi.org/10.1039/c2jm32415f
CAS Статья Google ученый
Сян, Х.Ф., Чен, Дж. Дж., Ли, З. и др .: Неорганическая мембрана в качестве разделителя для литий-ионной батареи. J. Источники энергии 196 , 8651–8655 (2011). https://doi.org/10.1016/j.jpowsour.2011.06.055
CAS Статья Google ученый
Chen, J.J., Wang, S.Q., Cai, D.D., et al .: Пористый SiO 2 в качестве сепаратора для улучшения электрохимических характеристик шпинели LiMn 2 O 4 катода. J. Membr. Sci. 449 , 169–175 (2014). https://doi.org/10.1016/j.memsci.2013.08.028
CAS Статья Google ученый
Раджа М., Ангулакшми Н., Томас С. и др.: Тонкие, гибкие и термостойкие керамические мембраны в качестве разделителя для литий-ионных батарей.J. Membr. Sci. 471 , 103–109 (2014). https://doi.org/10.1016/j.memsci.2014.07.058
CAS Статья Google ученый
Чжан, Ю.К., Ван, З.Х., Сян, Х.Ф. и др .: Тонкий неорганический композитный сепаратор для литий-ионных батарей. J. Membr. Sci. 509 , 19–26 (2016). https://doi.org/10.1016/j.memsci.2016.02.047
CAS Статья Google ученый
He, M.N., Zhang, X.J., Jiang, K.Y., et al .: Чистый неорганический сепаратор для литий-ионных батарей. ACS Appl. Матер. Интерфейсы. 7 , 738–742 (2015). https://doi.org/10.1021/am507145h
CAS Статья PubMed Google ученый
Шим, Э.Г., Нам, Т.Х., Ким, Дж. Г. и др .: Электрохимические характеристики литий-ионных батарей с трифенилфосфатом в качестве огнезащитной добавки. J. Источники энергии 172 , 919–924 (2007).https://doi.org/10.1016/j.jpowsour.2007.04.088
CAS Статья Google ученый
Йим, Т., Парк, М.С., Ву, С.Г., и др .: Самозатухающие литий-ионные батареи на основе встроенных внутри микрокапсул пожаротушения с чувствительностью к температуре. Nano Lett. 15 , 5059–5067 (2015). https://doi.org/10.1021/acs.nanolett.5b01167
CAS Статья PubMed Google ученый
Лю К., Лю В., Цю Ю.К. и др.: Сепаратор из микроволокна с электропрядением «ядро-оболочка» с термостойкими огнестойкими свойствами для литий-ионных аккумуляторов. Sci. Adv. 3 , e1601978 (2017). https://doi.org/10.1126/sciadv.1601978
CAS Статья PubMed PubMed Central Google ученый
Чжан, Х.Й., Цао, Ю.Л., Ян, Х.Х. и др.: Простое приготовление и электрохимическая характеристика модифицированного поли (4-метокситрифениламином) сепаратора в качестве самоактивируемого переключателя потенциала для литий-ионных батарей.Электрохим. Acta 108 , 191–195 (2013). https://doi.org/10.1016/j.electacta.2013.06.116
CAS Статья Google ученый
Ким, С.Ю., Хонг, Дж., Палмор, Г.Т.Р .: Целлюлоза, декорированная полипирролом, для аккумулирования энергии. Synth. Встретились. 162 , 1478–1481 (2012). https://doi.org/10.1016/j.synthmet.2012.06.003
CAS Статья Google ученый
Li, S.L., Xia, L., Zhang, H.Y. и др .: Сепаратор, модифицированный поли (3-децилтиофен), с самодействующим механизмом защиты от перезарядки для литий-ионных аккумуляторов на основе LiFePO 4 . J. Источники энергии 196 , 7021–7024 (2011). https://doi.org/10.1016/j.jpowsour.2010.09.111
CAS Статья Google ученый
Зив Б., Леви Н., Боргель В. и др.: Связывание марганца и увеличение срока службы литий-ионных аккумуляторов полимерными 18-краун-6 эфирами.J. Electrochem. Soc. 161 , A1213 – A1217 (2014). https://doi.org/10.1149/2.00jes
CAS Статья Google ученый
Banerjee, A., Ziv, B., Shilina, Y., et al .: Многофункциональный сепаратор для улавливания ионов марганца и удаления фтористоводородной кислоты для литий-ионных аккумуляторов на основе дилития из поли (этилен-альтернат-малеиновая кислота). поваренная соль. Adv. Energy Mater. 7 , 1601556 (2017). https://doi.org/10.1002 / aenm.201601556
CAS Статья Google ученый
Ли, З. К., Паурик, А. Д., Говард, Г. J. Источники энергии 272 , 1134–1141 (2014). https://doi.org/10.1016/j.jpowsour.2014.04.073
CAS Статья Google ученый
Banerjee, A., Ziv, B., Luski, S., и др .: Повышение срока службы литий-ионных аккумуляторов с помощью материалов, улавливающих ионы марганца с азотной функциональностью. J. Источники энергии 341 , 457–465 (2017). https://doi.org/10.1016/j.jpowsour.2016.12.036
CAS Статья Google ученый
Ниши Ю. Литий-ионные аккумуляторные батареи; последние 10 лет и будущее. J. Источники энергии 100 , 101–106 (2001).https://doi.org/10.1016/s0378-7753(01)00887-4
CAS Статья Google ученый
Калхофф, Дж., Эшету, Г.Г., Брессер, Д. и др.: Более безопасные электролиты для литий-ионных батарей: современное состояние и перспективы. Chemsuschem 8 , 2154–2175 (2015). https://doi.org/10.1002/cssc.201500284
CAS Статья PubMed Google ученый
Сюй, К .: Электролиты и межфазные границы в литий-ионных батареях и других устройствах. Chem. Ред. 114 , 11503–11618 (2014). https://doi.org/10.1021/cr500003w
CAS Статья PubMed Google ученый
Цзян, Дж. У., Дан, Дж. Р.: Влияние растворителей и солей на термическую стабильность LiC6. Электрохим. Acta 49 , 4599–4604 (2004). https://doi.org/10.1016/j.electacta.2004.05.014
CAS Статья Google ученый
Haregewoin, A.M., Wotango, A.S., Hwang, B.J .: Электролитные добавки для электродов литий-ионных аккумуляторов: прогресс и перспективы. Energy Environ. Sci. 9 , 1955–1988 (2016). https://doi.org/10.1039/c6ee00123h
CAS Статья Google ученый
Moumouzias, G., Ritzoulis, G., Siapkas, D., et al .: Сравнительное исследование LiBF 4 , LiAsF6, LiPF6 и LiClO 4 в качестве электролитов в пропиленкарбонат-диэтилкарбонате Растворы для Li / LiMn 2 O 4 элементов.J. Источники энергии 122 , 57–66 (2003). https://doi.org/10.1016/S0378-7753(03)00348-3
CAS Статья Google ученый
Ferrari, S., Quartarone, E., Mustarelli, P. и др .: бинарная ионно-жидкая система, состоящая из N -метоксиэтил- N -метилпирролидиния бис (трифторметансульфонил) -имида и бис (трифторметансульфонил) имид лития: новый многообещающий электролит для литиевых батарей.J. Источники энергии 194 , 45–50 (2009). https://doi.org/10.1016/j.jpowsour.2008.12.013
CAS Статья Google ученый
Хан, Х.Б., Чжоу, С.С., Чжан, Д.Дж., и др .: Бис (фторсульфонил) имид лития (LiFSI) в качестве проводящей соли для неводных жидких электролитов литий-ионных аккумуляторов: физико-химические и электрохимические свойства. J. Источники энергии 196 , 3623–3632 (2011). https://doi.org/10.1016 / j.jpowsour.2010.12.040
CAS Статья Google ученый
Зуо, X.X., Фан, С.Дж., Лю, Дж.С. и др .: Тетрафторборат лития в качестве добавки к электролиту для улучшения характеристик высокого напряжения литий-ионной батареи. J. Electrochem. Soc. 160 , A1199 – A1204 (2013). https://doi.org/10.1149/2.066308jes
CAS Статья Google ученый
Ларуш-Асраф, Л., Битон, М., Теллер, Х. и др.: Об электрохимическом и термическом поведении растворов бис (оксалато) бората лития (LiBOB). J. Источники энергии 174 , 400–407 (2007). https://doi.org/10.1016/j.jpowsour.2007.06.171
CAS Статья Google ученый
Wu, F., Zhu, Q.Z., Chen, R.J., et al .: Ионные жидкие электролиты с защитным дифтор (оксалат) боратом лития для высоковольтных литий-ионных батарей.Nano Energy 13 , 546–553 (2015). https://doi.org/10.1016/j.nanoen.2015.03.042
CAS Статья Google ученый
Окуока, С.И., Огасавара, Ю., Суга, Ю., и др .: Новая герметичная литий-пероксидная батарея с совместно легированным катодом Li 2 O в сверхконцентрированном литий-бис (фторсульфонил) амидный электролит. Sci. Отчетность 4 , 5684 (2015). https://doi.org/10.1038/srep05684
CAS Статья Google ученый
Wang, Q.S., Ping, P., Zhao, X.J., и др.: Разгон по температуре вызвал возгорание и взрыв литий-ионной батареи. J. Источники энергии 208 , 210–224 (2012). https://doi.org/10.1016/j.jpowsour.2012.02.038
CAS Статья Google ученый
Макнейл Д.Д., Дан Дж.Р .: Реакция заряженных катодов с неводными растворителями и электролитами: I. Li 0,5 CoO 2 . J. Electrochem. Soc. 148 , A1205 (2001).https://doi.org/10.1149/1.1407245
CAS Статья Google ученый
Шлоуп, С.Э., Керр, Дж. Б., Киношита, К.: Роль реакционной способности электролита литий-ионного аккумулятора в снижении производительности и саморазрядке. J. Источники энергии 119 (120/121), 330–337 (2003). https://doi.org/10.1016/s0378-7753(03)00149-6
Артикул Google ученый
Кавамура, Т., Кимура, А., Эгашира, М. и др.: Термическая стабильность алкилкарбонатных электролитов со смешанными растворителями для литий-ионных элементов. J. Источники энергии 104 , 260–264 (2002). https://doi.org/10.1016/S0378-7753(01)00960-0
CAS Статья Google ученый
Шлоуп С.Е., Пью Дж.К., Ван С. и др.: Химическая реакционная способность PF 5 и LiPF 6 в растворах этиленкарбоната / диметилкарбоната.Электрохим. Solid-State Lett. 4 , А42 (2001). https://doi.org/10.1149/1.1353158
CAS Статья Google ученый
Шмидт М., Хейдер У., Кюнер А. и др.: Фторалкилфосфаты лития: новый класс проводящих солей для электролитов для высокоэнергетических литий-ионных аккумуляторов. J. Источники энергии 97 (98), 557–560 (2001). https://doi.org/10.1016/s0378-7753(01)00640-1
Артикул Google ученый
Гнанарадж, Дж. С., Зиниград, Э., Асраф, Л. и др .: Об использовании LiPF 3 (CF 2 CF 3 ) 3 (LiFAP) растворов для литий-ионных аккумуляторов. электрохимические и термические исследования. Электрохим. Commun. 5 , 946–951 (2003). https://doi.org/10.1016/j.elecom.2003.08.020
CAS Статья Google ученый
Сюй М.К., Сяо А., Ли, В.С. и др.: Исследование тетрафтороксалатофосфата лития в качестве электролита литий-ионной батареи.Электрохим. Solid-State Lett. 12 , А155 (2009 г.). https://doi.org/10.1149/1.3134462
CAS Статья Google ученый
Цинь, Ю., Чен, З.Х., Лю, Дж. И др .: Тетрафтороксалатофосфат лития в качестве добавки к электролиту для литий-ионных элементов. Электрохим. Solid-State Lett. 13 , А11 (2010). https://doi.org/10.1149/1.3261738
CAS Статья Google ученый
Хуанг, Дж.Й., Лю, X.J., Кан, X.L. и др .: Исследование γ-бутиролактона для электролитов на основе LiBOB. J. Источники энергии 189 , 458–461 (2009). https://doi.org/10.1016/j.jpowsour.2008.12.088
CAS Статья Google ученый
Сюй, М.К., Чжоу, Л., Хао, Л.С. и др .: Исследование и применение дифтор (оксалат) бората лития (LiDFOB) в качестве добавки для улучшения термической стабильности электролита для литий-ионных аккумуляторов. .J. Источники энергии 196 , 6794–6801 (2011). https://doi.org/10.1016/j.jpowsour.2010.10.050
CAS Статья Google ученый
Younesi, R., Veith, G.M., Johansson, P., et al .: Литиевые соли для современных литиевых батарей: Li-Metal, Li-O 2 и Li-S. Energy Environ. Sci. 8 , 1905–1922 (2015). https://doi.org/10.1039/c5ee01215e
CAS Статья Google ученый
Янг, Л., Чжан, Х.Дж., Дрисколл, П.Ф. и др.: Литиевые соли на основе шестичленого кольца малонатобората в качестве электролитов для литий-ионных батарей. ECS, Лас-Вегас, Невада (2011). https://doi.org/10.1149/1.3589921
Книга Google ученый
Макмиллан, Р., Слегр, Х., Шу, З.Х. и др.: Фторэтиленкарбонатный электролит и его использование в литий-ионных батареях с графитовыми анодами. J. Источники энергии 81 (82), 20–26 (1999).https://doi.org/10.1016/s0378-7753(98)00201-8
Артикул Google ученый
Корепп К., Керн В., Ланцер Е.А. и др.: 4-бромбензилизоцианат по сравнению с бензилизоцианатом: новые пленкообразующие добавки к электролиту и добавки для защиты от перезаряда для литий-ионных батарей. J. Источники энергии 174 , 637–642 (2007). https://doi.org/10.1016/j.jpowsour.2007.06.142
CAS Статья Google ученый
Li, Z.D., Zhang, Y.C., Xiang, H.F., et al .: Триметилфосфит в качестве добавки к электролиту для высоковольтных литий-ионных батарей с использованием катода из слоистого оксида с высоким содержанием лития. J. Источники энергии 240 , 471–475 (2013). https://doi.org/10.1016/j.jpowsour.2013.04.038
CAS Статья Google ученый
Чандрасекаран, Р., Кох, М., Ожава, Ю. и др.: Исследования электрохимических ячеек на фторированном природном графите в пропиленкарбонатном электролите с добавкой дифторметилацетата (MFA) для низкотемпературных литиевых батарей.J. Chem. Sci. 121 , 339–346 (2009). https://doi.org/10.1007/s12039-009-0039-2
CAS Статья Google ученый
Xia, L., Xia, Y.G., Wang, C.S. и др .: 5 электролитов класса V на основе фторированных растворителей для литий-ионных аккумуляторов с отличной циклируемостью. ХимЭлектроХим 2 , 1707–1712 (2015). https://doi.org/10.1002/celc.201500286
CAS Статья Google ученый
Ли, Ю.М., Нам, К.М., Хван, Э.Х. и др .: Межфазное происхождение улучшения характеристик и затухания для 4,6 В LiNi 0,5 Co 0,2 Mn 0,3 O 2 аккумуляторных катода. J. Phys. Chem. С 118 , 10631–10639 (2014). https://doi.org/10.1021/jp501670g
CAS Статья Google ученый
Xiang, H.F., Xu, H.Y., Wang, Z.Z. и др .: Диметилметилфосфонат (DMMP) как эффективная огнезащитная добавка для электролитов литий-ионных аккумуляторов.J. Источники энергии 173 , 562–564 (2007). https://doi.org/10.1016/j.jpowsour.2007.05.001
CAS Статья Google ученый
Левчик С.В., Вейль Е.Д .: Обзор последних достижений в области антипиренов на основе фосфора. J. Fire Sci. 24 , 345–364 (2006). https://doi.org/10.1177/0734
6068426CAS Статья Google ученый
Ту, W.Q., Ся, П., Чжэн, X.W., и др .: Понимание взаимодействия между слоистым оксидом, богатым литием, и электролитом, содержащим добавки. J. Источники энергии 341 , 348–356 (2017). https://doi.org/10.1016/j.jpowsour.2016.12.012
CAS Статья Google ученый
Nam, TH, Shim, EG, Kim, JG и др .: Дифенилоктилфосфат и трис (2,2,2-трифторэтил) фосфит в качестве огнезащитных добавок для электролитов литий-ионных элементов при повышенной температуре. .J. Источники энергии 180 , 561–567 (2008). https://doi.org/10.1016/j.jpowsour.2008.01.061
CAS Статья Google ученый
Ван, X.M., Ясукава, Э., Касуя, С .: Негорючие триметилфосфатные электролиты для литий-ионных батарей, содержащие растворитель: I. Основные свойства. J. Electrochem. Soc. 148 , A1058 (2001). https://doi.org/10.1149/1.1397773
CAS Статья Google ученый
Сюй К., Дин М.С., Чжан С.С. и др.: Попытка составить негорючие электролиты на основе ионов лития с алкилфосфатами и фосфазенами. J. Electrochem. Soc. 149 , A622 (2002). https://doi.org/10.1149/1.1467946
CAS Статья Google ученый
Юн, У.С., Хаас, О., Мухаммад, С. и др .: Мягкое XAS-исследование на месте слоистого катодного материала на основе никеля при повышенных температурах: новый подход к изучению термической стабильности.Sci. Отчет 4 , 6827 (2015). https://doi.org/10.1038/srep06827
CAS Статья Google ученый
Лю, Дж. У., Сонг, X., Чжоу, Л. и др .: Фторированное производное фосфазена — многообещающая добавка к электролиту для высоковольтных литий-ионных батарей: от электрохимических характеристик до механизма коррозии. Nano Energy 46 , 404–414 (2018). https://doi.org/10.1016/j.nanoen.2018.02.029
CAS Статья Google ученый
Ихара М., Ханг Б.Т., Сато К. и др.: Свойства угольных анодов и термическая стабильность в электролите LiPF 6 / метилдифторацетат. J. Electrochem. Soc. 150 , A1476 (2003). https://doi.org/10.1149/1.1614269
CAS Статья Google ученый
Ли, Х.Х., Ван, Й.Й., Ван, К.С. и др .: Функция виниленкарбоната как термической добавки к электролиту в литиевых батареях.J. Appl. Электрохим. 35 , 615–623 (2005). https://doi.org/10.1007/s10800-005-2700-x
CAS Статья Google ученый
Ота, Х., Саката, Ю., Иноуэ, А. и др.: Анализ слоев SEI, полученных из виниленкарбоната, на графитовом аноде. J. Electrochem. Soc. 151 , A1659 (2004). https://doi.org/10.1149/1.1785795
CAS Статья Google ученый
Воллмер, Дж. М., Кертисс, Л. А., Виссерс, Д. Р. и др .: Механизмы восстановления этилена, пропилена и винилэтиленкарбонатов. J. Electrochem. Soc. 151 , A178 (2004). https://doi.org/10.1149/1.1633765
CAS Статья Google ученый
Чен, З.Х., Цинь, Ю., Амин, К.: Редокс-шаттлы для более безопасных литий-ионных батарей. Электрохим. Acta 54 , 5605–5613 (2009). https://doi.org/10.1016/j.electacta.2009.05.017
CAS Статья Google ученый
Сяо, Л.Ф., Ай, X.P., Цао, Ю.Л. и др.: Электрохимическое поведение бифенила как полимеризуемой добавки для защиты от перезаряда литий-ионных аккумуляторов. Электрохим. Acta 49 , 4189–4196 (2004). https://doi.org/10.1016/j.electacta.2004.04.013
CAS Статья Google ученый
Элиа, Г.А., Улисси, У., Чон, С. и др.: Исключительная долговечность литий-ионных батарей с использованием электролитов на основе ионной жидкости. Energy Environ. Sci. 9 , 3210–3220 (2016). https://doi.org/10.1039/c6ee01295g
CAS Статья Google ученый
Bhatt, AI, Best, AS, Huang, JH, et al .: Применение N -пропил- N -метилпирролидиния бис (фторсульфонил) имида RTIL, содержащего бис (фторсульфонил) лития. имид в литиевых батареях на основе ионной жидкости.J. Electrochem. Soc. 157 , A66 (2010). https://doi.org/10.1149/1.3257978
CAS Статья Google ученый
Мун, Дж., Йим, Т., Юнг, С. и др .: Возможность использования ионного жидкого растворителя на основе пирролидиния для неграфитовых углеродных электродов. Электрохим. Commun. 13 , 1256–1259 (2011). https://doi.org/10.1016/j.elecom.2011.08.030
CAS Статья Google ученый
Левандовски, А., Швидерска-Мочек, А .: Ионные жидкости как электролиты для литий-ионных аккумуляторов: обзор электрохимических исследований. J. Источники энергии 194 , 601–609 (2009). https://doi.org/10.1016/j.jpowsour.2009.06.089
CAS Статья Google ученый
Ферникола А., Кроче Ф., Скросати Б. и др.: LiTFSI-BEPyTFSI как улучшенный ионно-жидкий электролит для литиевых аккумуляторных батарей. J. Источники энергии 174 , 342–348 (2007).https://doi.org/10.1016/j.jpowsour.2007.09.013
CAS Статья Google ученый
Патри, Г., Романьи, А., Мартине, С., и др .: Моделирование затрат на литий-ионные аккумуляторные элементы для автомобильных приложений. Energy Sci. Англ. 3 , 71–82 (2015). https://doi.org/10.1002/ese3.47
Артикул Google ученый
Блидберг, А., Густафссон, Т., Tengstedt, C., et al .: Мониторинг фазового распределения Li x FeSO 4 F ( x = 1, 0,5, 0) для определения однородности реакции в пористых электродах батареи. Chem. Матер. 29 , 7159–7169 (2017). https://doi.org/10.1021/acs.chemmater.7b01019
CAS Статья Google ученый
Харрис С.Дж., Тиммонс А., Бейкер Д.Chem. Phys. Lett. 485 , 265–274 (2010). https://doi.org/10.1016/j.cplett.2009.12.033
CAS Статья Google ученый
Сандер, Дж. С., Эрб, Р. М., Ли, Л. и др.: Электроды аккумуляторных батарей с высокими рабочими характеристиками с помощью магнитного шаблона. Nat. Энергетика 1 , 16099 (2016). https://doi.org/10.1038/nenergy.2016.99
CAS Статья Google ученый
Эбнер М., Чанг Д. В., Гарсия Р. Э. и др.: Электроды: анизотропия извилистости в электродах литий-ионных аккумуляторов. Adv. Energy Mater. 4 , 1301278 (2014). https://doi.org/10.1002/aenm.201470024
Артикул Google ученый
Чен, К.Дж., Чжан, Ю., Ли, Ю.Дж. и др .: Высокопроводящие, легкие, малые извилистые углеродные каркасы в качестве сверхтолстых трехмерных токоприемников. Adv. Energy Mater. 7 , 1700595 (2017).https://doi.org/10.1002/aenm.201700595
CAS Статья Google ученый
Вилке, С., Швейцер, Б., Хатиб, С. и др .: Предотвращение распространения теплового разгона в литий-ионных аккумуляторных батареях с использованием композитного материала с фазовым переходом: экспериментальное исследование. J. Источники энергии 340 , 51–59 (2017). https://doi.org/10.1016/j.jpowsour.2016.11.018
CAS Статья Google ученый
Финеган, Д.П., Шил, М., Робинсон, Дж. Б. и др.: Быстрая томография литий-ионных аккумуляторов во время теплового разгона в рабочем режиме. Nat. Commun. 6 , 6924 (2015). https://doi.org/10.1038/ncomms7924
CAS Статья PubMed PubMed Central Google ученый
Чжун, Х., Конг, К., Чжан, Х. и др .: Безопасный композитный катод с положительным температурным коэффициентом для литий-ионной батареи. J. Источники энергии 216 , 273–280 (2012).https://doi.org/10.1016/j.jpowsour.2012.05.015
CAS Статья Google ученый
Feng, X.M., Ai, X.P., Yang, H.X .: Электрод с положительным температурным коэффициентом и механизмом отключения по температуре для использования в перезаряжаемых литиевых батареях. Электрохим. Commun. 6 , 1021–1024 (2004). https://doi.org/10.1016/j.elecom.2004.07.021
CAS Статья Google ученый
Zhang, H.Y., Pang, J., Ai, X.P., et al .: Электроды с положительным температурным коэффициентом на основе поли (3-бутилтиофена) для более безопасных литий-ионных батарей. Электрохим. Acta 187 , 173–178 (2016). https://doi.org/10.1016/j.electacta.2015.11.036
CAS Статья Google ученый
Янг, Х., Леоу, W.R., Чен, X.D .: Термочувствительные полимеры для повышения безопасности электрохимических накопителей. Adv. Матер. 30 , 1704347 (2018). https://doi.org/10.1002/adma.201704347
CAS Статья Google ученый
Кисе, М., Йошиока, С., Хамано, К. и др .: Разработка нового безопасного электрода для литиевой аккумуляторной батареи. J. Источники энергии 146 , 775–778 (2005). https://doi.org/10.1016/j.jpowsour.2005.03.158
CAS Статья Google ученый
Кисе, М., Йошиока, С., Хамано, К., и др .: Поведение импеданса при переменном токе и устойчивость литий-ионных аккумуляторов к перезаряду с использованием катодов с положительным температурным коэффициентом. J. Electrochem. Soc. 153 , A1004 (2006). https://doi.org/10.1149/1.2189262
CAS Статья Google ученый
Abada, S., Marlair, G., Lecocq, A., et al .: Моделирование литий-ионных батарей, ориентированное на безопасность: обзор.J. Источники энергии 306 , 178–192 (2016). https://doi.org/10.1016/j.jpowsour.2015.11.100
CAS Статья Google ученый
Xia, L., Li, S.L., Ai, X.P. и др .: Термочувствительные катодные материалы для более безопасных литий-ионных батарей. Energy Environ. Sci. 4 , 2845 (2011). https://doi.org/10.1039/c0ee00590h
CAS Статья Google ученый
Май, Л.К., Ян, М.Ю., Чжао, Ю.Л .: Отслеживание разряда батарей в реальном времени. Природа 546 , 469–470 (2017). https://doi.org/10.1038/546469a
CAS Статья PubMed Google ученый
Mutyala, M.S.K., Zhao, J.Z., Li, J.Y., et al .: Измерение температуры в ионно-литиевой батарее с помощью переносных гибких тонкопленочных термопар. J. Источники энергии 260 , 43–49 (2014). https: // doi.org / 10.1016 / j.jpowsour.2014.03.004
CAS Статья Google ученый
Форгез, К., Винь До, Д., Фридрих, Г. и др .: Тепловое моделирование цилиндрической литий-ионной батареи LiFePO 4 / графит. J. Источники энергии 195 , 2961–2968 (2010). https://doi.org/10.1016/j.jpowsour.2009.10.105
CAS Статья Google ученый
Zhu, J.G., Sun, Z.C., Wei, X.Z., и др .: Оценка внутренней температуры батареи для LiFePO 4 батареи на основе сдвига фазы импеданса в рабочих условиях. Энергии 10 , 60 (2017). https://doi.org/10.3390/en10010060
Артикул Google ученый
Ли С.Ю., Чуанг С.М., Ли С.Дж. и др.: Гибкий микродатчик для мониторинга температуры и напряжения плоских элементов на месте. Sens. Actuat.Физ. 232 , 214–222 (2015). https://doi.org/10.1016/j.sna.2015.06.004
CAS Статья Google ученый
Ли С.Ю., Ли С.Дж., Хунг Ю.М. и др.: Встроенный микродатчик для микроскопического мониторинга в реальном времени локальной температуры, напряжения и тока внутри литий-ионного аккумулятора. Sens. Actuat. Физ. 253 , 59–68 (2017). https://doi.org/10.1016/j.sna.2016.10.011
CAS Статья Google ученый
Ghannoum, A., Nieva, P., Yu, A.P., et al .: Разработка встроенных волоконно-оптических датчиков затухающих волн для оптических характеристик графитовых анодов в литий-ионных батареях. ACS Appl. Матер. Интерфейсы. 9 , 41284–41290 (2017). https://doi.org/10.1021/acsami.7b13464
CAS Статья PubMed Google ученый
Насименто, М., Феррейра, М.С., Пинто, Дж. Л .: Тепловой мониторинг литиевых батарей в реальном времени с помощью волоконных датчиков и термопар: сравнительное исследование.Измерение 111 , 260–263 (2017). https://doi.org/10.1016/j.measurement.2017.07.049
Артикул Google ученый
Nascimento, M., Novais, S., Ding, M.S., и др .: Внутренняя деформация и температурная дискриминация с оптоволоконными гибридными датчиками в литий-ионных батареях. J. Источники энергии 410 (411), 1–9 (2019). https://doi.org/10.1016/j.jpowsour.2018.10.096
CAS Статья Google ученый
Зоммер, Л.В., Кизель, П., Гангули, А. и др.: Быстрые и медленные процессы диффузии ионов в литиево-ионных ячейках во время цикла, наблюдаемые с помощью оптоволоконных датчиков деформации. J. Источники энергии 296 , 46–52 (2015). https://doi.org/10.1016/j.jpowsour.2015.07.025
CAS Статья Google ученый
Новаис, С., Насименто, М., Гранде, Л. и др.: Контроль внутренней и внешней температуры литий-ионной батареи с помощью датчиков с оптоволоконной решеткой Брэгга.Датчики 16 , 1394 (2016). https://doi.org/10.3390/s160
CAS Статья Google ученый
Суреш П., Шукла А.К., Муничандрайя Н .: Исследования температурной зависимости переменного тока. импеданс литий-ионных аккумуляторов. J. Appl. Электрохим. 32 , 267–273 (2002)
CAS Статья Google ученый
Чжу, Дж. Г., Сунь, З.C., Wei, X.Z. и др.: Новый метод онлайн-оценки внутренней температуры литий-ионной батареи, основанный на измерении спектроскопии электрохимического импеданса. J. Источники энергии 274 , 990–1004 (2015). https://doi.org/10.1016/j.jpowsour.2014.10.182
CAS Статья Google ученый
Сринивасан, Р., Демирев, П.А., Кархафф, Б.Г .: Быстрый мониторинг фазовых сдвигов импеданса в литий-ионных батареях для предотвращения опасностей.J. Источники энергии 405 , 30–36 (2018). https://doi.org/10.1016/j.jpowsour.2018.10.014
CAS Статья Google ученый
Wu, M.S., Chiang, P.C.J., Lin, J.C .: Электрохимические исследования современных литий-ионных аккумуляторов с помощью трехэлектродных измерений. J. Electrochem. Soc. 152 , А47 (2005). https://doi.org/10.1149/1.1825385
CAS Статья Google ученый
Сринивасан, Р., Кархафф, Б.Г., Батлер, М.Х., и др .: Мгновенное измерение внутренней температуры в литий-ионных перезаряжаемых элементах. Электрохим. Acta 56 , 6198–6204 (2011). https://doi.org/10.1016/j.electacta.2011.03.136
CAS Статья Google ученый
An, S.J., Li, J.L., Daniel, C., et al .: Разработка и демонстрация трехэлектродных карманных ячеек для литий-ионных аккумуляторов. J. Electrochem.Soc. 164 , A1755 – A1764 (2017). https://doi.org/10.1149/2.0031709jes
CAS Статья Google ученый
Янг, X.G., Ge, S.H., Лю, Т. и др .: Анализ сигнала плато напряжения для обнаружения и количественной оценки литиевого покрытия в литий-ионных элементах. J. Источники энергии 395 , 251–261 (2018). https://doi.org/10.1016/j.jpowsour.2018.05.073
CAS Статья Google ученый
Янсен, А.Н., Дис, Д.У., Абрахам, Д.П. и др.: Низкотемпературное исследование литий-ионных элементов с использованием электрода сравнения Li y S n . J. Источники энергии 174 , 373–379 (2007). https://doi.org/10.1016/j.jpowsour.2007.06.235
CAS Статья Google ученый
Ла Мантиа, Ф., Уэсселс, К.Д., Дешазер, Х.Д. и др .: Надежные электроды сравнения для литий-ионных батарей.Электрохим. Commun. 31 , 141–144 (2013). https://doi.org/10.1016/j.elecom.2013.03.015
CAS Статья Google ученый
Лю, Q.Q., Du, C.Y., Shen, B., и др .: Понимание нежелательных проблем с литиевым покрытием анода в литий-ионных батареях. RSC Adv. 6 , 88683–88700 (2016). https://doi.org/10.1039/c6ra19482f
CAS Статья Google ученый
Ву, Х., Чжуо, Д., Конг, Д.С. и др.: Повышение безопасности аккумуляторной батареи за счет раннего обнаружения внутреннего короткого замыкания с помощью бифункционального разделителя. Nat. Commun. 5 , 5193 (2014). https://doi.org/10.1038/ncomms6193
CAS Статья PubMed Google ученый
Бернс, Дж. К., Стивенс, Д. А., Дан, Дж. Р.: обнаружение литиевого покрытия на месте с использованием высокоточной кулонометрии. J. Electrochem. Soc. 162 , A959 – A964 (2015).https://doi.org/10.1149/2.0621506jes
CAS Статья Google ученый
Bitzer, B., Gruhle, A .: Новый метод обнаружения литиевого покрытия путем измерения толщины элемента. J. Источники энергии 262 , 297–302 (2014). https://doi.org/10.1016/j.jpowsour.2014.03.142
CAS Статья Google ученый
Ригер, Б., Шустер, С.Ф., Эрхард С.В. и др.: Многонаправленное лазерное сканирование как инновационный метод обнаружения локального повреждения клеток во время быстрой зарядки литий-ионных элементов. J. Хранение энергии 8 , 1–5 (2016). https://doi.org/10.1016/j.est.2016.09.002
Артикул Google ученый
Гримсманн, Ф., Герберт, Т., Браухле, Ф. и др .: Определение максимальных зарядных токов литий-ионных элементов для малых зарядов. J. Источники энергии 365 , 12–16 (2017).https://doi.org/10.1016/j.jpowsour.2017.08.044
CAS Статья Google ученый
Ульманн, К., Иллиг, Дж., Эндер, М. и др .: Обнаружение на месте металлического лития на графите в экспериментальных ячейках. J. Источники энергии 279 , 428–438 (2015). https://doi.org/10.1016/j.jpowsour.2015.01.046
CAS Статья Google ученый
Смарт, М.С., Ратнакумар, Б.В .: Влияние состава электролита на литиевое покрытие в литий-ионных элементах. J. Electrochem. Soc. 158 , A379 (2011). https://doi.org/10.1149/1.3544439
CAS Статья Google ученый
Петцл М., Данцер М.А .: Неразрушающее обнаружение, определение характеристик и количественная оценка литиевого покрытия в коммерческих литий-ионных батареях. J. Источники энергии 254 , 80–87 (2014).https://doi.org/10.1016/j.jpowsour.2013.12.060
CAS Статья Google ученый
фон Людерс, К., Цинт, В., Эрхард, С.В., и др .: Литиевое покрытие в литий-ионных батареях исследовано с помощью релаксации напряжения и дифракции нейтронов на месте. J. Источники энергии 342 , 17–23 (2017). https://doi.org/10.1016/j.jpowsour.2016.12.032
CAS Статья Google ученый
Шиндлер, С., Бауэр, М., Петцл, М. и др.: Релаксация напряжения и спектроскопия импеданса как оперативные методы обнаружения литиевого покрытия на графитовых анодах в коммерческих литий-ионных элементах. J. Источники энергии 304 , 170–180 (2016). https://doi.org/10.1016/j.jpowsour.2015.11.044
CAS Статья Google ученый
Гуо, З.С., Чжу, Дж. Й., Фэн, Дж. М. и др .: Прямое наблюдение на месте и объяснение дендрита лития промышленных графитовых электродов.RSC Adv. 5 , 69514–69521 (2015). https://doi.org/10.1039/c5ra13289d
CAS Статья Google ученый
Мехди, Б.Л., Цянь, Дж., Насыбулин, Э. и др.: Наблюдение и количественная оценка наноразмерных процессов в литиевых батареях с помощью операндно-электрохимического (S) ТЕМ. Nano Lett. 15 , 2168–2173 (2015). https://doi.org/10.1021/acs.nanolett.5b00175
CAS Статья PubMed PubMed Central Google ученый
Сагане, Ф., Симокава, Р., Сано, Х. и др.: Наблюдения с помощью сканирующей электронной микроскопии in-situ за реакциями осаждения лития и отрывом на границе стеклянный электролит из оксинитрида лития и фосфора / Cu. J. Источники энергии 225 , 245–250 (2013). https://doi.org/10.1016/j.jpowsour.2012.10.026
CAS Статья Google ученый
Вандт, Дж., Джейкс, П., Гранвер, Дж. И др.: Количественное и временное обнаружение литиевого покрытия на графитовых анодах в литий-ионных батареях.Матер. Сегодня 21 , 231–240 (2018). https://doi.org/10.1016/j.mattod.2017.11.001
CAS Статья Google ученый
Gotoh, K., Izuka, M., Arai, J., et al .: Исследование ядерного магнитного резонанса In situ 7Li релаксационного эффекта в практических ионно-литиевых батареях. Углерод 79 , 380–387 (2014). https://doi.org/10.1016/j.carbon.2014.07.080
CAS Статья Google ученый
Финеган Д.П., Дарси Э., Кейзер М. и др.: Температурный разгон: определение причины разрушения литий-ионных батарей во время теплового разгона. Adv. Sci. 5 , 1870003 (2018). https://doi.org/10.1002/advs.201870003
Артикул Google ученый
Сан, Дж., Ли, Дж. Г., Чжоу, Т. и др .: Токсичность, серьезная проблема теплового разгона коммерческой литий-ионной батареи. Nano Energy 27 , 313–319 (2016).https://doi.org/10.1016/j.nanoen.2016.06.031
CAS Статья Google ученый
Фернандес, Ю., Брай, А., де Персис, С.: Идентификация и количественная оценка газов, выделяемых во время испытаний на злоупотребление путем перезарядки коммерческой литий-ионной батареи. J. Источники энергии 389 , 106–119 (2018). https://doi.org/10.1016/j.jpowsour.2018.03.034
CAS Статья Google ученый
Характеристики электролитзависимого суперконденсатора на пористом биоуглероде, легированном азотом, из желатина
Abstract
Сверхемкость углерода сильно зависит от природы электролита, но четкая взаимосвязь между структурой и характеристиками остается неуловимой.Здесь серия биоуглеродов с постепенно изменяющейся структурой пор и химией поверхности получается с использованием нового протокола солевого шаблона (с экологически безвредным KNO 3 в качестве шаблона, активатора и порогена и дешевого желатина в качестве предшественника углерода) , и используются в качестве модельных систем для исследования зависимости электрохимического механизма таких наноуглеродов от двух типичных электролитов (KOH и EMIBF 4 ). Изменяя только дозировку KNO 3 , два основных показателя качества биочара — многомасштабная пористость и функционализация поверхности — были точно модулированы для создания двойных электрических слоев.Электрохимические данные проясняют, что комбинированные эффекты пористости и легирования способствуют увеличению сверхемкости, но только один из двух факторов играет ведущую роль в различных электролитах. Кинетический анализ подтверждает тот факт, что обильное легирование гетероатомом может эффективно компенсировать емкость за счет интенсивного поверхностного окислительно-восстановительного внедрения в KOH, в то время как подходящая дисперсия размера пор играет преобладающую роль в самоусилении разделения ионов и, таким образом, диктует хорошее разделение зарядов в EMIBF 4 .Квазиколичественная модель релевантности характеристики и структуры в EMIBF 4 обоснованно предполагает намек на превосходную совместимость между ионами и размерами пор, в которой двух- и однослойное взаимодействие удержания ионов в интегрированных одиночных и двойных ионных размерах Установлено, что поры более полезны для обуздания пресловутых эффектов чрезмерного экранирования и для изменения координационного числа, кулоновского упорядочения и фазовой конформации EMIBF 4 в нанопорах размером несколько нанометров. Этот уникальный способ накопления энергии в порах, согласованных с ионами, повышает плотность энергии оптимальных образцов до нового уровня — 88.3 Вт · ч кг −1 при 1 кВт · кг −1 , что составляет конкуренцию подавляющему большинству зарегистрированных углеродных материалов. Короче говоря, сравнительный пример здесь показывает ценную взаимосвязь добротности углерода и типа электролита, которая может выступать в качестве жизненно важного руля направления для разработки современных материалов суперконденсаторов, зависящих от электролита.
Ключевые слова: суперконденсатор , электролит, углеродные материалы, ионная жидкость, желатин, высокая плотность энергии
1. Введение
Благодаря высокой скорости заряда-разряда, большой удельной мощности, а также длительному сроку службы суперконденсаторы получили признание широко рассматриваются как одни из самых перспективных устройств хранения энергии [1,2,3,4].Суперконденсаторы (SC) в принципе обладают превосходной экологичностью и менее дороги, чем нынешние инициативы на основе батарей, потому что системы суперконденсаторов не зависят от редких металлов, благородных металлов или элементов лития, а вместо этого зависят от материалов электродов и других органических или водных электролиты. Суперконденсаторы можно разделить на электрохимические двухслойные конденсаторы (EDLC) и псевдоконденсаторы на основе механизмов накопления энергии. EDLC накапливают электричество за счет обратимого электропоглощения ионов на поверхностях электродов, в то время как псевдоконденсаторы доставляют энергию в зависимости от обратимых окислительно-восстановительных реакций на поверхностях активных материалов.В последнее время различные материалы (включая оксиды и гидроксиды металлов, углеродные материалы, проводящие полимеры и гибридные композиты) были тщательно изучены в качестве электродных материалов суперконденсаторов. Из них углеродные материалы считаются лучшими потенциальными кандидатами на роль SC, учитывая их общие достоинства: большая удельная поверхность (SSA), богатая пористость, легко изменяемые свойства (такие как наноструктурирование и функционализация), благоприятная химическая и термическая стабильность, экологичность. , низкая стоимость, доступность прекурсора и отличная проводимость.Поскольку такие тесно связанные углеродные SCs могут экономить электричество за счет быстрой адсорбции и десорбции противоположно заряженных ионов электролита через двойные электрические слои, сформированные вокруг областей границы электролит-электрод, их электрохимические свойства в значительной степени зависят от свободных электроактивных центров, к которым легко доступны ионы электролита. В этом контексте разработка функционализированных углеродных материалов идет полным ходом [5,6,7]. Однако их довольно небольшая удельная энергия (3–5 Вт · ч · кг -1 ) сильно ограничила их широкое применение, особенно по сравнению с литий-ионными (> 150 Вт · ч · кг -1 ) и свинцово-кислотными (~ 30 Вт · ч. кг −1 ) батарей [8].Теоретически плотность энергии EDLC может быть увеличена за счет увеличения как окна напряжения, так и емкости в соответствии с уравнением E = 0,5 CV 2 [9,10]. Квадратная зависимость плотности энергии от используемого электрохимического окна показывает, что использование электролитов с более высокими диапазонами рабочего напряжения и стабильностью оказывает гораздо более сильное влияние на улучшение плотности энергии. Таким образом, внедрение различных электролитов в качестве энергоносителей рабочей жидкости для SC не может просто управлять окнами рабочего напряжения и, следовательно, уровнем энергии, но также позволяет использовать новый метод накопления энергии и эффективность, связанные с электрохимическими событиями, происходящими в нанопорах размером несколько нм. функционализированных электродов.Таким образом, высоковольтные ионные жидкие электролиты (ИЖ) (такие как EMIBF 4 ,> 3,5 В) будут иметь более заметные преимущества по сравнению с водными электролитами (такими как КОН, <1,23 В), поскольку реакции расщепления воды будут происходить при низких температурах. потенциальные диапазоны [11,12,13]. К сожалению, свойства суперконденсатора ИЖ все еще плохо изучены по сравнению со свойствами водных электролитов. Улучшение поведения легко сталкивается с более острой проблемой, заключающейся в том, что ИЖ обладают гораздо большими размерами ионов и вязкостью и, следовательно, значительно более низкой ионной проводимостью и медленной диффузией ионов (особенно в сильно ограниченных пространственных средах).Например, ионная проводимость составляет всего ~ 2 мСм см -1 в ИЖ, но достигает ~ 1 См см -1 в водных электролитах [5,9]. Что еще более важно, подверженность электрохимического поведения ИЖ некоторым центральным факторам (например, взаимодействию между ионами электролита и электродными материалами [14,15], влиянию размера пор [16,17] и эффекту легирования гетероатомами [17, 18]). 18]) до сих пор не поддается однозначному описанию, что сбивает исследователей с толку относительно того, какие свойства углеродных материалов следует выделить, чтобы они соответствовали ИЖ.Соответственно, далеко идущими являются исследования зависимости структуры от характеристик в зависимости от электролита и углеродных электродных материалов.
Было признано, что несколько важных факторов, включая текстурные особенности (удельная поверхность (SSA), объем пор, распределение пор по ширине), химию поверхности и легирование гетероатомами (B, N, O, P) и внутренние атрибуты (такие как степень графитации [19], отношение C / O), следует учитывать при разработке высокоэффективных материалов EDLC.В этом отношении многочисленные аллотропы углерода (такие как упорядоченный мезопористый углерод с примесью азота, пористый углерод, полученный из биомассы [20,21,22] и восстановленный оксид графена) показали рекомендуемые электрохимические характеристики в водных электролитах. Тем не менее, их поведение в ИЖ отсутствует, что препятствует глубокому пониманию несоответствий между водными и ИЖ электролитами в суперконденсаторах, а также первостепенных факторов, влияющих на конечные характеристики. В свете различной природы водных и IL-электролитов, хорошо идентифицированная релевантность структуры и рабочих характеристик и обоснование манипуляций в водных системах, как было доказано, не переносятся механически в системы IL / углерод.
С учетом вышеперечисленных перспектив и для достижения более конкурентоспособных плотностей энергии в электролитах KOH и EMIBF 4 разработан и оценен ряд пористых углеродов, легированных азотом, с заданными свойствами, в надежде предложить один возможный технический критерий. относительно типа электролита и параметра углерода в области применения СК. Целевые угли могут быть получены одновременно с постепенно изменяющимся уровнем легирования азотом и распределением пор по размерам, используя модифицированный шаблонный рецепт с мягким KNO 3 как в качестве шаблона макропор, так и порогена в виде нанопор.В зависимости от типа электролита такие тщательно продуманные углеродные материалы демонстрируют отличные характеристики суперконденсатора, причины которых связаны с одним определенным критическим фактором качества углеродных материалов. Кинетический анализ проясняет, что емкость и скорость обработки критически зависят не от размера пор для EMIBF 4 , а от содержания примеси азота в электролите КОН, хотя оба эффекта способствуют усилению электрохимического поведения. Чрезвычайная плотность энергии 88.3 Вт · ч кг -1 , что сопоставимо с большинством современных углеродных материалов, может быть получено для образца оптимального размера в EMIBF 4 . Для EMIBF 4 предлагается квазиколичественная модель взаимосвязи структура-характеристики для выявления хорошей совместимости по размеру пор и ионов. Модель показывает, что объединение одиночных и двойных пор размером с ион более полезно для изменения кулоновского упорядочения, координационного числа и фазовой структуры ИЖ в нанопорах размером нм в электродах.Это позволяет этим SC, возможно, превосходить свойства некоторых типов батарей, а также открывает неизведанную возможность для химиков-материаловедов достичь превосходной доставки энергии, концентрируясь на формулировании или разработке как многомасштабных ионно-согласованных пор, так и уровней легирования (а не непрерывных микропор и поверхности областей) при поиске альтернативных электролитов с множеством жидких конформаций и составов. Наше текущее сравнительное исследование водных и ионно-ионных электролитов предварительно проливает свет на правдоподобный принцип конструкции, зависящий от электролита, чтобы дать инструкции по синтезу исключительных углеродных материалов для SC.
2. Материалы и методы
2.1. Подготовка материалов
Четыре этапа, включая золь-гель, лиофилизацию, отжиг и промывку водой, были задействованы в синтезе пористого биоуглерода. Обычно C-0,75 синтезировали следующим образом. Сначала 1 г желатина и 0,75 г KNO 3 растворяли в 20 мл горячей воды при 80 ° C с образованием прозрачного золя. После охлаждения до комнатной температуры золь помещали в холодильник при 4 ° C на 12 часов, а затем переносили при -20 ° C на дополнительные 12 часов.Затем замороженный гель помещали в жидкий азот примерно на 30 с с последующей сушкой вымораживанием в лиофилизаторе при -80 ° C и 1 Па в течение 36 часов с получением легкого аэрогеля. После этого процесс отжига проводился при 800 ° C в течение 1 ч в чистом газообразном аргоне со скоростью потока 300 мл / мин и скоростью нагрева 5 ° C / мин. Конечный продукт получали прямой промывкой водой и сушкой при 60 ° C в течение 24 часов. Образцы, синтезированные с различными дозировками соли KNO 3 (0,25, 0,5, 0,75 г), прокаленные при 800 ° C, также были получены с помощью вышеуказанного процесса и обозначены как C-0.25, С-0,5 и С-0,75 соответственно. Следы выбросов NO x во время карбонизации можно легко удалить с помощью метода прямой адсорбции воды. Все реагенты использовали в качестве аналитических реагентов и были приобретены у Guoyao Chemical Co., Ltd. (Шанхай, Китай). Все химические вещества использовались в том виде, в котором они были получены, без дополнительной обработки.
2.2. Характеристика материалов
Морфология и структура образцов были охарактеризованы с помощью сканирующего электронного микроскопа (SEM, JSM 7401F, JEOL Ltd., Токио, Япония) работал при 3,0 кВ, а просвечивающий электронный микроскоп (TEM, JEM 2010, JEOL Ltd., Токио, Япония) работал при 120,0 кВ. Измерения с помощью рентгеновской фотоэлектронной спектроскопии (XPS) проводили на Escalab 250xi (Waltham, MA, USA). Все спектры XPS были откалиброваны при 284,8 эВ с использованием линии C 1s, а необработанные данные были подогнаны с помощью программы XPSPEAK (XPS Peak 4.1, Тайвань). Изотерму адсорбции / десорбции N 2 контролировали с помощью системы Autosorb-IQ2-MP-C (Boynton Beach, FL, USA). Удельная поверхность (SSA) была получена с использованием многоточечного метода Брунауэра – Эммета – Теллера (BET), а распределение пор по размерам (PSD) было получено с помощью теории функции плотности закаленного твердого тела (QSDFT) и модели равновесия.Детектирование с помощью дифракции рентгеновских лучей (XRD) осуществляли на дифрактометре (Bruker D8 Advance, Блерика, Массачусетс, США) с излучением Cu-Kα при 40,0 кВ и 120 мА. Рамановские спектры регистрировали с использованием рамановского спектрофотометра (Horiba Jobin Yvon LabRAM HR800, Париж, Франция) с возбуждением гелий-неоновым лазером на длине волны 633 нм.
2.3. Электрохимическая оценка
Электродную суспензию готовили путем смешивания 80 мас.% Активных материалов, 10 мас.% Ацетиленовой сажи и 10 мас.% Связующего ПВДФ в растворителе N-метилпирролидон (NMP).Затем суспензию загружали на пенопласт Ni с круглым диском (толщиной 1 мм, диаметром 1,1 см) с массовой загрузкой около 3 мг / см 2 . После вакуумной сушки и сжатия под давлением 10 МПа в течение 30 с рабочие электроды были получены.
Испытание в 6 M KOH электролите: Трехэлектродная система была сначала оценена в 6 M KOH, используя графит в качестве противоэлектрода и Hg / HgO в качестве электрода сравнения. Циклическую вольтамперометрию (CV), гальваностатический заряд-разряд (GCD) и спектроскопию электрохимического импеданса (EIS) всех ячеек оценивали на электрохимической рабочей станции (EC Lab, Claix, Франция).Кривые циклической вольтамперометрии (CV) и гальваностатического заряда-разряда (GCD) записывались в окне напряжения -1-0 В. Спектроскопию электрохимического импеданса (EIS) контролировали при напряжении холостого хода с амплитудой 10 мВ в диапазоне 10 — От 2 до 10 5 Гц. Для двухэлектродной конфигурации две части рабочих электродов с одинаковой массовой нагрузкой были собраны в асимметричный конденсатор. Профили CV и CD были проверены в диапазоне 0–1 В.
Эксперимент с электролитом EMIBF 4 : симметричный двухэлектродный монетный элемент был сконструирован в перчаточных боксах из чистого аргона с концентрациями кислорода и влаги ниже, чем у 0.1 промилле. Мембрана Whatman (толщиной 680 мкм), изготовленная из стеклянного микроволокна (тип: GF / D1823-047), была помещена между двумя листами электродов с одинаковой нагрузкой, и все они были сжаты вместе и запечатаны в монетном элементе типа 2025. Были исследованы электрохимические характеристики, включая циклическую вольтамперометрию, гальваностатический заряд-разряд и спектроскопию электрохимического импеданса. Диапазон напряжения составлял 0–4 В в тесте CV, с различными скоростями сканирования от 20 до 200 мВ · с -1 .Детектирование GCD при различных плотностях тока 0,5–10 Ag −1 также выполнялось в диапазоне от 0 до 4 В. Измерения спектроскопии электрохимического импеданса оценивались с помощью электрохимического анализатора в диапазоне частот 10 5 –0,01 Гц.
Удельная емкость ( C , электрод , F g -1 ) для каждого электрода была рассчитана по формуле:
где I , Δ t , m и V — постоянный ток (мА), время разряда (с), общая масса активных материалов в обоих угольных электродах (мг) и напряжение window (V) соответственно.
Плотность энергии ( E , Вт · ч кг −1 ) оценивалась по формуле:
E = C ячейка V 2 / 7,2 = C электрод В 2 /28,8
(2)
Плотность мощности ( P , Вт кг −1 ) была получена в соответствии с выражением:
3. Результаты
Пористый элемент, легированный азотом. углерод был изготовлен с использованием экономически эффективной и экологически чистой стратегии KNO 3 солевой шаблон, основанной на дешевой желатиновой биомассе.Желатин имеет много азота и кислородсодержащих групп (COOH — , OH — , NH 2 ), которые могут напрямую вводить богатые гетероатомы в конечные углеродные продукты [7]. Насколько нам известно, более мягкая и менее коррозионная соль KNO 3 еще не нашла широкого применения при получении многофункциональных углеродных материалов. Вообще говоря, многие дизайнерские углеродные материалы в литературных исследованиях должны быть выполнены с помощью громоздкого многоступенчатого процесса, который объединяет шаблоны (обычно NaCl, металл, оксид металла или супермолекулы), активирующие агенты (обычно сильно коррозионные сильные щелочи КОН и NaOH) и кислотным выщелачиванием.В нашей работе KNO 3 непосредственно смешивался с золем желатина в горячей воде и служил как солевым шаблоном, так и активирующим агентом в легком гибридном биополимерном аэрогеле. Кроме того, водорастворимая и нейтральная соль KNO 3 обладает превосходной биосовместимостью с желатином. Полностью ионизированные частицы KNO 3 в воде не изменяют заметно кислотность или щелочность раствора, полностью подавляя неблагоприятный протеолиз желатина, происходящий в ненейтральной среде.Таким образом, этот эффект обеспечивает не только долгосрочное выживание однородно комплексного ионного гидрогеля, но и его последующую успешную перекристаллизацию в трехмерные аддукты соль-желатин. Следует отметить, что, поскольку кристаллы соли KNO 3 были гомогенно заключены внутри сетки желатинового аэрогеля после сублимационной сушки, эффективность карбонизации и активации во время процесса термоотжига была значительно повышена. Наконец, остаточные частицы от терморазложения солей KNO 3 могут быть легко удалены простой промывкой водой, в отличие от кислотного и основного выщелачивания традиционных темплатов (металл, оксид металла) и активирующих агентов (КОН и NaOH). .Различное массовое отношение KNO 3 / желатин в диапазоне от 0,25 до 0,75 (соответствующие образцы в дальнейшем обозначаются как C-0,25, C-0,5 и C-0,75 соответственно) использовали для настройки соответствующих физико-химических свойств. Электронная микроскопия была проведена для обеспечения микроскопического понимания материалов () . Картирование энергодисперсионной рентгеновской спектроскопии (DES) (d – g) демонстрирует успешный синтез углеродных материалов, легированных азотом, с однородным распределением элементов азота по образцам в масштабе микроразрешения.Дозировка солей KNO 3 оказывает большое влияние на микроструктуру. При меньшем количестве KNO 3 , равном 0,25, толстые пластинчатые углеродные фрагменты размером 100–200 нм располагались так дискретно и беспорядочно, что не собирались в очевидные каркасы с регулярными порами (a, h). При более высоком содержании KNO 3 , равном 0,5 (b и вставка i) и 0,75 (c и вставка j), чешуйчатая структура в конечном итоге превратилась в макропористый, взаимопроникающий и взаимосвязанный каркас (аналогично иерархической архитектуре сот или яичной коробки) , со средним размером макропор менее 1 мкм.Боковая стенка из макропор полна отверстий, щелей или отверстий, демонстрирующих исключительную пространственную связь. Эти хорошо развитые макропоры могут действовать как подходящие каналы для улучшения массовой диффузии электролитов во время связанных электрохимических процессов, в то время как очень прерывистые и дискретные внутренние структуры C-0,25 делают его хрупким с плохой способностью сопротивляться разрушению и усиливают транспортировку. эффекты. Важно отметить, что тщательный осмотр показывает, что многочисленные мезопоры небольшого размера с графитированными и изогнутыми боковыми стенками толщиной до атома изобилуют C-0.75 (j), но над двумя другими образцами (h, i) видимых мезопор не наблюдается. Примечательно, что некоторые хорошо идентифицированные крошечные микродомены с очевидными муаровыми полосами решетки встроены в углеродный скелет в C-0,75, что указывает на локальную графитовую структуру. Эта графитовая структура может значительно улучшить химическую стабильность, электронную проводимость и механическую прочность. Такие заметные морфологические различия между образцами ясно показывают, что дозировка соли KNO 3 оказывает существенное влияние на механизм карбонизации и структурной эволюции.
( a — c ) Изображения пористого углерода, полученные с помощью сканирующего электронного микроскопа (СЭМ). ( d — g ) Энергодисперсионная рентгеновская спектроскопия EDS) картирование C-0.75 с элементами C, N и O. ( ч — j ) Изображения, полученные с помощью просвечивающего электронного микроскопа (ПЭМ).
Кристаллографическая структура и степень графитизации углеродных материалов были определены с помощью спектров комбинационного рассеяния, которые широко считаются надежным методом для характеристики структуры графитовых углеродных материалов.Обычно спектр комбинационного рассеяния графитового углеродного материала включает типичные D- и G-полосы. Первый (1330–1340 см, −1 ) может относиться к дефектным или активированным беспорядком режимам дыхания шестичленных углеродных колец, а последний (1580–1600 см −1 ) типичен для фононов E 2g в центре зоны Бриллюэна [23]. Для всех образцов характерная полоса G на ~ 1580 см -1 и полоса D на ~ 1320 см -1 хорошо идентифицированы (а). Кристалличность, количественно определяемая отношением интенсивностей полос G к D ( I G / I D ), составляет 0.82, 0,90 и 0,95 для C-0,25, C-0,5 и C-0,75 соответственно, демонстрируя постепенное увеличение степени графита с более высокой дозировкой KNO 3 и постепенное снижение плотности дефектов в углероде. Приращение I G / I D поясняет, что в нашем методе увеличенная дозировка KNO 3 кажется неразрушающей, но способствует формированию графитовой структуры. Повышенная графитизация может происходить из-за того, что большое количество тепловыделений из-за жестких реакций восстановления углерода может генерировать высокотемпературную зону, локализованную на периферии вновь образованных пор, для консолидации ароматизации и расслоения объемных углеродных слоев внутренними слоями углерода. образующиеся на месте формы K (во время восстановления углерода).Кристалличность и фазы образцов дополнительно проверяли с помощью измерения дифракции рентгеновских лучей (XRD) (b). На картинах видны два дифракционных пика, относящиеся к плоскостям (002) и (100) графита (JCPDS № 41-1487) [7]. Очевидно, характерное уширение пиков подтверждает неупорядоченную структуру полученных пористых углеродных материалов. В сочетании с данными рамановского и просвечивающего электронного микроскопа (ПЭМ) можно сделать вывод, что пористый биоуголь, легированный азотом, особенно C-0,75, имеет аморфную, но упорядоченную структуру на коротких расстояниях.
( a ) комбинационного рассеяния и ( b ) рентгеновских дифрактограмм (XRD) всех пористых углеродов.
N 2 экспериментов по адсорбции были проведены для исследования текстурных свойств каждого материала. На изотермах адсорбции-десорбции представлены кривые I-типа без гистерезиса, а ветвь адсорбции компактно накладывается на ветвь десорбции, что означает, что микропоры доминируют в материалах. Удельная поверхность (SSA), определенная многоточечным методом Бруннера – Эммета – Теллера (БЭТ), составляет 1084.2, 2050,3 и 2744,6 м 2 г -1 для C-0,25, C-0,5 и C-0,75 соответственно. Примечательно, что все углеродные продукты демонстрируют узкое распределение пор по размерам (PSD), но отчетливые вариации (b). Поры в C-0,25 расположены в зоне микропор в диапазоне 0,5–1 нм и преимущественно сосредоточены на 0,5 нм. Объемы SSA и пор, вносимые мезопорами (определяемыми как S мезо и V мезо ), составляют всего 45,5 м 2 г −1 и 0.001 см 3 г −1 (). Эти данные показывают, что C-0,25 в действительности можно рассматривать как полностью ультрамикропористый материал. В случае C-0,5 СПМ положительно сдвигается в область 0,5–2 нм, подавляющее большинство из которых сосредоточено около 0,8 нм. Это ясно показывает, что большее количество соли KNO 3 может увеличить размер микропор до 0,8 нм. Увеличение размера пор происходит из-за эффекта расширения, вызываемого большим количеством пиролитических газов во время реакций восстановления углерода.Между тем, SSA и объем пор, происходящих из микропор, могут достигать 1770,1 м 2 г -1 и 0,718 см 3 г -1 соответственно. Что касается C-0,75, размер пор дополнительно увеличивается, в то время как доля удельной площади поверхности и объема мезопор составляет 32,1% и 36,8% соответственно. Это совпадает с хорошо наблюдаемыми мезопорами на изображениях ПЭМ (j), что указывает на большой объемный вклад мезопор небольшого размера (2–3 нм). Это явление полностью отличается от картины, согласно которой микропоры вносят вклад только в объем пор C-0.25 и С-0,5. В сочетании с PSD можно сделать вывод, что C-0,75 практически имеет двухмодовую конфигурацию пор с преобладающей шириной пор 0,8 и 1,5 нм.
Характеристика химических свойств поверхности и структур пористой текстуры. ( a ) N 2 кривые изотермы адсорбции-десорбции, ( b ) распределение пор по размерам и ( c ) совокупный объем пор. ( d ) Полномасштабная рентгеновская фотоэлектронная спектроскопия (XPS) pectra.( e ) Гистограмма изменения содержания элементов C, N и O при изменении соотношений KNO 3 / желатин. ( f ) Спектры N1s высокого разрешения.
Таблица 1
Текстурные и композиционные свойства всех образцов.
| Образцы | S всего (м 2 г −1 ) a | S мезо (м 2 г −1 ) | (S micro м 2 г −1 ) b | V всего (см 3 г −1 ) c | V мезо (см 3 g −1 ) | V micro (см 3 г −1 ) b | Содержание азота (ат.%) d |
|---|---|---|---|---|---|---|---|
| C-0.25 | 1084,3 | 45,5 | 1038,8 | 0,403 | 0,001 | 0,402 | 9,45 |
| C-0,5 | 2050,3 | 113 9,3113 | 0,7113 | ||||
| C-0,75 | 2744,6 | 880,5 | 1864,1 | 1,304 | 0,478 | 0,826 | 1.68 |
).Обзорные спектры (d) показывают, что элементы C, N и O присутствуют в каждой выборке. Атомный процент показывает, что C-0,25 обладает наивысшим уровнем легирования гетероатомами (т.е. доля азота 9,45%), в отличие от минимального содержания N 1,68% по сравнению с C-0,75 (e). Нисходящая тенденция эволюции легирующих добавок показывает тот факт, что возрастающая дозировка KNO 3 вредна для легирования азотом. Фактически, места соединения C и N-C также меняются с дозировкой KNO 3 . Спектры N1s высокого разрешения (f) могут быть далее деконволютированы на пиридиновый N (N-6, 398.3 эВ), пирролиновый N (N-5, 400,1 эВ) и графитовый N (NQ, 401,5 эВ) [24,25,26], а гораздо более сильная пиковая интенсивность C-0,25 также иллюстрирует его более высокий уровень легирования азотом. . По мере увеличения дозировки KNO 3 с 0,25 до 0,75 количество замещений азота вокруг «обычных» графитовых позиций (NQ), а не дефектных ситуаций (N-5 и N-6) постепенно увеличивается, в соответствии с I G / I D Эволюция отношения в спектрах КР. Другими словами, более высокая дозировка KNO 3 может привести к заметному преобразованию менее устойчивых конфигураций N-5 и N-6 без уменьшения относительного процента более устойчивых структур N-Q.Связь N-C и эволюция локализации в углеродном каркасе, скорее всего, коррелируют с процессом активационного травления. Этот процесс начинается с химически более активных дефектных участков азота и распространяется в основных плоскостях углеродных решеток, создавая все более крупные поры с увеличением дозировки KNO 3 , как ясно показали исследования ПЭМ и комбинационного рассеяния света в и. Взятые вместе, данные сравнения, несомненно, показывают, что C-0,25 не был полностью активирован KNO 3 во время пиролиза, вызывая, таким образом, неразвитые поры и каркас, незаметные мезопоры и низкую SSA; на удивление, он все еще может сохранить более богатый элемент N из сырья, чем C-0.5 и С-0,75. Как общепризнано, свойства текстуры как высокой SSA, так и соответствующей ширины пор в значительной степени способствуют усилению емкости EDLC, в то время как легирование гетероатомом способно дополнительно повысить производительность за счет реакций Фарадика или псевдоемкости. Однако в этом отчете мы обнаружили, что влияние этих двух факторов на емкость сильно зависит от используемых электролитов.
Электрохимические характеристики оценивались в двух типичных электролитах, 6 M KOH и EMIBF 4 IL, которые имеют окна рабочего напряжения 1 В и 4 В соответственно.Сначала мы оценили производительность трех электродов в 6 М КОН (). Все кривые CV в водном растворе отклоняются от стандартного прямоугольника из-за искажения формы (широкая выпуклость при низких потенциалах), что свидетельствует об отклонении от идеального поведения EDLC. При использовании одного электрода площадь кривой CV для C-0,75 немного превышает площадь C-0,25 и C-0,5. Емкости при 0,5, 1, 2, 5, 10 и 20 A g -1 вычисляются последовательно и составляют 215,6, 208,8, 204,2, 192,6, 182,8 и 169.2 F g -1 для C-0,75; 205,8, 191,8, 182,1, 169,6, 158,5 и 142,1 F g -1 для C-0,5; и 180,5, 173,4, 158,7, 145,4, 133,2 и 116,9 F g -1 для C-0,25. Соответствующее сохранение электрической емкости составляет 78,5% для C-0,75, 69,0% для C-0,5 и 64,8% для C-0,25. Возможность скорости замирания может тесно коррелировать с уменьшающимся размером поры. Следует подчеркнуть, что емкостной разрыв между этими образцами весьма нюансирован. Например, емкость C-0,75 всего на 35 Ф · г -1 больше, чем у C-0.25 при 0,5 A г -1 , тогда как SSA и объем пор C-0,75 в ~ 2,5 и ~ 2,1 раза больше, чем у C-0,25, соответственно. Если рассматривать исключительно вклад микропор в построение эффективной структуры EDLC, S micro для C-0,75 также в ~ 1,8 раза выше, чем для C-0,25, что, теоретически, должно было по крайней мере привести к увеличение емкости примерно в 1,8 раза вместо экспериментально аналогичных значений. Следовательно, резкое различие в текстурных свойствах (SSA и объемах пор) вообще не лежит в основе тонких вариаций электрической емкости.Что еще более важно, такое тонкое несоответствие будет в дальнейшем устранено в двухэлектродных оценочных системах, поскольку электрическая емкость теоретически будет в четверть от емкости трехэлектродной системы. Это может быть дополнительно продемонстрировано следующими данными, испытанными в двухэлектродной системе. Можно видеть, что кривые CV (a) частично накладываются друг на друга, а кривые CD (b) почти перекрываются друг с другом, намекая на очень аналогичную электрическую емкость среди трех образцов. Количественная электрическая емкость, основанная на двухэлектродной конфигурации, приближается к примерно 40 Ф · г -1 для всех электродов, что в итоге дает одноэлектродное значение (пунктирные линии) ~ 150-170 Ф · г -1 при 0.5 A g −1 (в). Таким образом, большое противоречие между одинаковой электрической емкостью и различными текстурными параметрами может быть интерпретировано только с учетом огромного несоответствия в легировании гетероатомами. В дополнение к EDLC, высокий уровень легирования C-0,25 может способствовать дополнительной электрической емкости и заполнить промежутки по сравнению с электродами C-0,5 и C-0,75 с высокими SSA и объемами пор. С другой стороны, вышеупомянутые исследования показывают, что трехэлектродная электрическая емкость ряда биочагов, легированных азотом, не поддается прямому преобразованию в электрохимические ячейки.Фактически, вещества на основе углерода являются своеобразными, потому что они могут функционировать либо как отрицательные электроды, либо как положительные электроды в симметричных электрохимических системах, с теоретической удельной электрической емкостью каждого электрода, почти идентичной аналогам, оцененным трехэлектродным методом. анализ. Напротив, как широко сообщается в литературе, псевдоемкостные вещества, обладающие ощутимыми выпуклостями (обычно окислительно-восстановительными сигналами), обычно могут иметь обратный эффект для симметричных систем суперконденсаторов, потому что их две дифференциальные электрические емкости на катодах и анодах, обозначаемые как C 1 и C 2. , становятся неравными [27,28].В общем случае, если один угольный электрод имеет правильное напряжение в направлении основных выступов кривых CV и, следовательно, большую дифференциальную электрическую емкость, другой углеродный электрод должен испытывать напряжение вдали от этих основных выступов, тем самым вызывая гораздо более низкий дифференциал. электрическая мощность. Поскольку симметричный суперконденсатор считается электронно эквивалентным двум последовательным конденсаторам, их общая электрическая емкость C 1 C 2 / (C 1 + C 2 ) не может превышать наибольшее теоретическое значение, которое может составлять к 1 / 2C 1 = 1 / 2C 2 при условии C 1 = C 2 .Не должно быть никаких шансов на насыщение оптимальной электрической емкости при любом напряжении, если только формы CV не должны оставаться идеально симметричными. Фактически, из-за значительного вклада окислительно-восстановительных реакций, пористые углеродные электроды, легированные азотом, демонстрируют несколько искаженные кривые ВАХ (а). Другими словами, во время трехэлектродной оценки имеет место переменная дифференциальная электрическая емкость. Как следствие, их двухэлектродная система, по прогнозам, не сможет соответствовать C 1 = C 2 , тем самым вызывая симметричную электрическую емкость, отличную от той, которая была получена из трехэлектродного анализа.Двухэлектродные CV-диаграммы (a) также сохраняют искаженные ортогоны с низкой регулярностью и приводят к увеличению электрической емкости на каждый электрод 150-170 Ф · г -1 при 0,5 А · г -1 в диапазоне потери 16,9–17,4% трехэлектродной электрической емкости 180,5–215,6 Ф г –1 . Другими словами, все углеродные электроды, легированные азотом, каждый из которых демонстрирует явную деформацию в пределах CV-профилей, испытывают явное ухудшение электрической емкости при применении в двухэлектродных испытаниях.В целом, заметно варьирующаяся дифференциальная электрическая емкость, о чем свидетельствует очевидное несоответствие или неравенство между двухэлектродными и трехэлектродными оценками, действительно подтверждает существование заметной псевдоемкости в пористых углеродах, легированных азотом, в водном растворе КОН. решение.
Трехэлектродные характеристики в водных электролитах 6 M KOH. ( a ) Циклическая вольтамперометрия (CV), ( b ) гальваностатический заряд-разряд (GCD) и ( c ) скоростная способность.
Электрохимические характеристики двухэлектродного симметричного суперконденсатора в ( a — c ) 6 M KOH электролите и ( d — f ) EMIBF 4 ионных жидких электролитах (IL). ( a , d ) Кривые циклической вольтамперометрии (CV), полученные при 20 мВ с −1 , ( b , e ) кривые гальваностатического заряда-разряда (GCD), полученные при 0,5 A g −1 и ( c , f ) диапазон скоростей от 0.От 5 до 10 A g -1 для трех образцов с различным распределением пор по размерам (PSD) и уровнями легирования.
Мы также проверили электрохимические характеристики пористого углерода с примесью азота в электролите EMIBF 4 IL. Интересно, что в резком контрасте с результатами для KOH, CV-площадь C-0,25 (d) значительно ниже, чем C-0,5 и C-0,75, вместе с кривыми CD (e). Их электрическая емкость КД на основе одного электрода при плотности тока 0,5 А г -1 достигает 158.9 F g -1 для C-0,75, в отличие от меньших значений 54,7 F g -1 для C-0,5 и 4,8 F g -1 для C-0,25, поразительное увеличение в три раза и соответственно более чем на один порядок (е). Сохранение электрической емкости может достигать 1,7 (35,0%), 22,4 (41,0%) и 85,9 F g -1 (54%) при 10 A g -1 по C-0,25, C-0,5 и C- 0,75, соответственно, что свидетельствует о резком увеличении скорости обработки при более высокой дозировке KNO 3 .Эти данные ясно показывают, что C-0,25 почти не способен накапливать энергию, в то время как C-0,75 может обеспечивать высокую электрическую емкость, даже сравнимую с самыми передовыми материалами на основе углерода в электролитах IL. Интересно, что эволюция емкости с дозировкой KNO 3 в EMIBF 4 кажется совершенно не похожей на тенденцию изменения KOH, которая в природе показывает, что решающий фактор или режим накопления энергии различен в двух электролитах. Учитывая, что последовательность повышения электрической емкости (с 4.8 F g -1 для C-0,25 до 54,7 F g -1 для C-0,5 и 158,9 F g -1 для C-0,75) соответствует порядку снижения уровня легирования с 9,45% для C-0,25 до 5,52% для C-0,5 и до 1,68% для C-0,75, значительное повышение электрической емкости с C-0,25 до C-0,75 не может быть объяснено легированием гетероатомами как ведущим фактором (как было проанализировано ранее в KOH электролиты, потому что легирование N / O в C-0,75 самое низкое). В этом случае, а не легирование, структурные свойства, в частности размер пор, имеют решающее влияние на настройку емкости в электролите EMIBF 4 IL, которая противоположна таковой в электролите KOH.
Тем не менее, массовая диффузия и способность скорости сильно зависели от размера пор, независимо от использования KOH или EMIBF 4 . Чтобы исследовать влияние текстурных характеристик на кинетику переноса, на всех образцах была проведена спектроскопия электрохимического импеданса (EIS) (). Все графики Найквиста показывают полупериод на высоких частотах, наклон 45 ° в среднем частотном сегменте между 5 и 100 Гц и почти прямые линии на частотах ниже 1 Гц. Такие характеристики подразумевают типичные емкостные процессы углеродных материалов.Емкостные процессы могут быть дополнительно подтверждены аналитически с помощью эквивалентной схемы для пористых электродов (вставка). Проекция наклонных линий 45 ° на абсциссу обозначает ионное сопротивление электролитов (заполненных поры пористых электродных структур), которое может служить центральным указателем, указывающим на процесс диффузии ионов и способность пористого N- электроды из легированного биоугля во время зарядки и разрядки. Независимо от типа электролита, постепенное уменьшение проектных значений длины от C-0.25 до C-0,75 показывает падение ионного сопротивления. Эта тенденция к снижению состоит из увеличения ширины пор в пористом каркасе биочага, легированного азотом. Прямые линии на низких частотах почти вертикальны для C-0,75, но довольно перекошены как для C-0,5, так и, в частности, для C-0,25, показывая гораздо более быструю диффузию ионов с увеличением размера пор. Что касается диффузно оптимизированной пористой архитектуры (C-0,75), ионное сопротивление ( R с ), экстраполированное из интервала x , составляет всего ~ 0.4 Ом в электролите КОН, что на одну величину меньше, чем в EMIBF 4 (~ 1,6 Ом). Сопротивление переноса заряда ( R c ) (подразумевается опущенным высокочастотным полукругом) также составляет ~ 0,2 Ом в КОН, в отличие от ~ 1,7 Ом в EMIBF 4 . Эти различные значения должны быть результатом заметных различий в размерах и вязкости ионов, что по существу отражает изменяющуюся динамику переноса различных ионов электролита в одних и тех же структурах пор.
Спектры спектроскопии электрохимического импеданса (EIS) образцов, испытанных в ( a ) 6 M KOH и ( b ) EMIBF 4 IL.
Сравнение спектров ЭИС C-0,75 в 6 KOH и EMIBF 4 ИЖ.
Чтобы глубже изучить причины электрохимических различий в KOH и EMIBF 4 , вклад емкости за счет обратимого емкостного поведения или поведения контролируемой диффузией вставки (реакции Фарада) изучается на основе взаимосвязи между током ( i ) и скорость сканирования ( v ) [29,30,31]
Это уравнение показывает, что электрохимический процесс контролируется диффузией (или вводится по Фарадею), когда b = 0.5 (он может описывать как процесс переноса ионов, так и окислительно-восстановительную реакцию), или быстрый емкостной процесс, когда b = 1.
Уравнение (1) также может быть выражено в другой форме:
где k 1 v представляет собой ток емкостного эффекта, а k 2 v 1/2 — ток, управляемый диффузией, выраженный как:
i (В) / v 1 / 2 = k 1 v 1/2 + k 2
(6)
На этом этапе может быть реализована линейная подгонка вольтамперометрических токов на каждом потенциале, а коэффициенты k 1 и k 2 также могут быть определены для расчета k 1 v и k 2 v 1/2 .Затем можно определить долю контролируемого диффузией тока или емкостного тока. Результаты подгонки при плотности тока 200 мВ · с −1 представлены на рис. Затененные области представляют собой контролируемый диффузией процесс, который отражает псевдоемкость от легирования гетероатомом через межфазную окислительно-восстановительную реакцию. Примечательно, что вклад псевдоемкости в 6 M KOH составляет 47,3% для C-0,25, но 24,1% для C-0,5 и 16,0% для C-0,75. Однако общая площадь CV этих трех образцов почти равна друг другу, что еще раз подтверждает важную роль легирования в увеличении общей емкости.Доля псевдоемкости находится в хорошем соответствии с соответствующим уровнем легирования, а именно, чем больше легирующая добавка, тем больше псевдоемкость. Это однозначно проливает свет на то, почему C-0,25, имеющий гораздо меньшую SSA и объем пор, может обеспечивать емкость, сравнимую с C-0,75, у которого гораздо больше SSA и объем пор (215,6 против 180,5 F g −1 при 0,5 A г -1 ). Это важное открытие может служить технической нормой для рационального проектирования углеродных материалов для SC в водных системах; то есть вместо бесконечных поисков оптимизации текстуры, в частности, включая огромную удельную поверхность и высоко иерархическую пористость, соответствующее содержание легирующей примеси азота может более эффективно повысить сверх емкостное поведение.Это главным образом связано с тем, что практическое применение высокоиерархических пористых углеродов с большими площадями поверхности всегда ограничивалось их небольшой плотностью отводов (которая очень пагубно сказывалась на объемных характеристиках) в результате наличия пустого пространства и других топологических проблем. Что еще хуже, защита пустых пространств лишает материалы жизненно важных факторов во время строгого календаря, потому что большинство пустых пустот могут подвергнуться полному разрушению. Эти соображения могут дополнительно подчеркнуть превосходство правильного легирования над высокой пористостью суперконденсаторов (SC) в водных системах.
Кривые CV ( a , d ) C-0,25, ( b , e ) C-0,5 и ( c , f ) C-0,75 в двух видах электролитов ( 6 M KOH и EMIBF 4 IL), испытанные в двухэлектродной системе при 200 мВ · с -1 . Затененные области представляют вклад, контролируемый диффузией.
Интересно, что в EMIBF 4 процесс, контролируемый диффузией, для всех угольных электродов составляет ~ 28%. Несмотря на огромную разницу в содержании примеси азота в образцах (9.45% для C-0,25, 5,52% для C-0,5 и 1,68% для C-0,75), есть только тривиальное изменение, касающееся вклада окислительно-восстановительных реакций. Это независимое от легирования или нечувствительное явление здесь показывает, что легирование азотом не является критическим фактором в повышении емкости углерода в высоковольтных ионных жидкостях. Результаты также подтверждают, что события накопления энергии должны в значительной степени зависеть от адсорбции и десорбции, а не от реакции внедрения или окислительно-восстановительной реакции, относящейся к легирующему азоту, при использовании EMIBF 4 в качестве электролита.Это в первую очередь потому, что КОН, как тип протонного электролита, в воде может быть хорошей реакционной средой для окислительно-восстановительных реакций гетероатомов. Напротив, поскольку EMIBF 4 представляет собой чистую расплавленную соль с большим размером ионов и стерическими препятствиями, а также хорошей электрохимической стабильностью при теоретическом рабочем напряжении, ему очень трудно интенсивно взаимодействовать с функциональными группами на углеродных поверхностях. . Следовательно, обильное легирование C-0,25 не вызывает заметного улучшения емкости, как это происходит в KOH.Фактически, легирующая примесь азота, скорее всего, задействует хорошее смачивание углеродных поверхностей EMIBF 4 для увеличения ионной активности. Конечно, точная роль N-примесей в изменении сверхемкостного поведения EMIBF 4 на углеродных материалах требует исследования с помощью скоординированной комбинации передовых технологий определения характеристик in situ или in operando, что выходит за рамки наших исследований. здесь. Для ясности и краткости показаны все основные показатели для всех нанесенных образцов в обоих электролитах.
Таблица 2
Сводная информация по ключевым параметрам производительности, таким как удельная емкость, пропускная способность, удельная энергия-мощность и вклад процесса, контролируемого диффузией, в обоих электролитах.
| Образцы | C (F g −1 ) при 0,5 A g −1 | C (F g −1 ) при 10 A g −1 | Скорость подачи от 0,5 до 10 A г −1 | Плотность энергии (Вт · ч, кг −1 ) | Плотность энергии (Вт · ч, кг −1 ) | Процесс с контролируемой диффузией |
|---|---|---|---|---|---|---|
| C-0.25-EMIBF 4 | 4,8 | 1,7 | 35,0% | 2,7 при 1 кВт кг −1 | 0,94 при 20 кВт кг −1 | 47,3% |
| C- EMIBF 4 | 54,7 | 22,4 | 41,0% | 30,4 при 1 кВт кг −1 | 12,4 при 20 кВт кг −1 | 24,1% |
| C 4 | 158,9 | 85,9 | 54.0% | 88,3 при 1 кВт кг -1 | 47,7 при 20 кВт кг -1 | 16,0% |
| C-0,25-KOH | 180,5 | 133,2 | 73,8113 93,8 при 0,1 кВт кг −1 | 2,5 при 5 кВт кг −1 | 28,5% | |
| C-0,5-KOH | 205,8 | 158,5 | 77,0% | 5,663 при 0,1 кВт кг −1 | 3,1 при 5 кВт кг −1 | 28.3% |
| C-0,75-KOH | 215,6 | 182,8 | 84,79% | 6,0 при 0,1 кВт кг −1 | 3,8 при 5 кВт кг −1 | 16 273
Поскольку эффект легирования был полностью исключен, решающим фактором в данном случае является размер пор. Учитывая, что размер пор C-0,25 в основном сосредоточен на 0,5 нм (даже меньше, чем диаметр десольватированных ионов EMI + (~ 0,7 нм) [16]), многочисленные ультрамикропоры были недоступны для EMIBF . 4 ИЖ и микропористые интерфейсы не могут быть эффективно использованы (а).Однако в KOH обильные ультрамикропоры позволяют ионам OH — проходить через каналы из-за гораздо меньшего размера чистого OH — (~ 0,14 нм) (обратите внимание, что мы принимаем во внимание только чистый размер ионов электролита, потому что сольватированные ионы сначала десольватировались бы, если бы их диаметр был больше диаметра пор). То есть минимальный размер пор, которые могут образовывать двойной электрический слой для хранения энергии, составляет около 0,14 нм для электролита КОН, но в 5 раз больше для электролита EMIBF 4 .Следовательно, критический размер пор для передачи энергии составляет не менее 0,7 нм для EMIBF 4 . В этом случае поры в C-0,25 были «живыми» для OH —, но «мертвыми» для EMI + . В результате микропоры большего размера (0,8 нм), соединенные с частичными субмезопорами двойного размера (1,5 нм) в C-0,75, могут в значительной степени улучшить совместимость размера пор иона, что приведет к значительному увеличению емкости в EMIBF. 4 .
( a ) Предложены модели порозависимой ионной диффузии с использованием двух видов электролитов (KOH и EMIBF 4 ) с разными размерами ионов.( b ) График Рагона показывает соотношение плотности энергии и мощности двухэлектродного симметричного конденсатора, используемого в различных электролитах. ( c ) Иллюстрация собранного плоского элемента на 4 В с использованием C-0,75 в качестве материала электрода и ( d ) его практическая демонстрация при освещении светодиодов разными цветами и рабочими напряжениями или параллельно.
Вкратце, мы сравнили два распространенных электролита, KOH и EMIBF 4 IL, и их влияние на характеристики EDLC на пористых углеродных материалах, легированных азотом, с настраиваемыми текстурными свойствами и химией легирования поверхности.Из-за меньшего размера ионов электролита KOH сверхмалые микропоры все еще были доступны для C-0,25. Кроме того, дополнительная псевдоемкость от окислительно-восстановительных реакций богатого гетеродегирования C-0,25 дополнительно компенсирует емкостные промежутки по сравнению с C-0,75 и C-0,5, которые имеют относительно более высокие SSA и объемы пор. Однако меньший размер пор вызывает очень вялую диффузию ионов и снижение скоростной способности обоих электролитов. Для EMIBF 4 легирование не является определяющим предварительным условием, в то время как дисперсия размера пор оказывает большее влияние на характеристики емкости углерода.Хотя C-0,75 имеет самую высокую емкость как в KOH, так и в EMIBF 4 , результаты говорят нам, что легирование рассматривается как более плодотворный протокол для улучшения характеристик водных электролитов, в то время как поиск подходящего размера пор считается более полезным, чем легирование. для электролитов ИЖ. Это дает определенное направление для разумной подготовки электролитзависимых углеродных материалов для СЭ.
Энергия и плотности мощности приведены на графике Рагона (b). Наиболее важно то, что график Рагона показывает довольно параллельный график по координате x при увеличении от 1 кВт кг -1 до очень высокой удельной мощности 20 кВт кг -1 , что свидетельствует о превосходной энергии — номинальная удельная мощность.В частности, плотность энергии достигает 88,3 Втч кг −1 , полученная для C-0,75, 30,4 Втч кг −1 для C-0,5 и только 2,7 Втч кг −1 для C-0,25 при 1 кВт кг −1 . Чрезвычайная плотность энергии 47,7 Вт · ч −1 для C-0,75 все еще сохраняется на уровне 20 кВт · кг −1 , что существенно превосходит таковые для двух других образцов и значения в KOH (5,2 Вт · ч кг −1 при 0,1 кВт кг −1 и 2,5 Втч кг −1 при 5 кВт кг −1 ), обнаруживая удивительную черту сохранения энергии.Показатели удельной энергии и удельной мощности нашего оптимального образца могут соперничать с подавляющим большинством заявленных усовершенствованных углеродных материалов по сравнению с. [12,19,21,32,33,34,35,36,37,38,39,40,41,42,43,44,45,46,47,48,49,50,51,52] Такие результаты не только продвигают простую или эффективную концепцию созревания пористых наноуглеродов, легированных гетероатомами, получаемую из биомассы, но также преодолевают дисгармоничное столкновение энергии и плотности мощности за счет согласования хорошо спроектированных углеродных электродов с электролитами, которые имеют широкий диапазон рабочего потенциала .Чтобы дополнительно продемонстрировать практическое применение материалов, была сконфигурирована двухэлектродная плоская ячейка на 4 В, как показано на c. Он может зажигать светодиоды разных цветов (красный, желтый, зеленый и синий) в диапазоне рабочих напряжений 1,8–3,5 В (d). Кроме того, один монетный элемент может напрямую питать 27 светодиодов параллельно в форме сердца (d). Этот пример открывает привлекательную перспективу для использования в реальном мире.
Таблица 3
Сравнение плотности энергии нашего оптимального образца с аналогами некоторых ранее описанных усовершенствованных углеродных материалов.Все удельные плотности энергии, указанные здесь в качестве справочных, основаны на массе активных материалов ячейки.
| Тип углерода | Плотность энергии | Ионные жидкости | Удельная емкость (Ф / г) | Refs |
|---|---|---|---|---|
| C-0,75 | 88,3 кг / Втч / кг 4 (4 В) | 160 Ф / г при 0,5 А / г | Эта работа | |
| Углерод имбирной соломки с примесью азота | 37.8 Вт · ч / кг при 1 кВт / кг | EMIMBF 4 (3 В) | 122 Ф / г при 0,5 A / г | [32] |
| Иерархический нанопористый биоуглерод | 43,3 Вт / кг в виде улья 1 кВт / кг | EMIM-TFSI (3,5 В) | 146 Ф / г при 0,2 А / г | [21] |
| Макро-мезопористая углеродная сетка с перекрестными связями | 92 Втч / кг при 1 кВт / кг | EMIBF 4 (4 В) | 166 Ф / г при 0,5 А / г | [33] |
| Углеродные нановолоконные микросферы с примесью азота | 58.7 Втч / кг при 0,3 кВт / кг | EMIM-TFSI (3,5 В) | 113 Ф / г при 5 мВ / с | [34] |
| Графеновая сеть, функционализированная диамином / триамином | 51 Втч / кг при 0,552 кВт / кг | BMIMBF 4 (3,5 В) | 119 Ф / г при 10 мВ / с | [35] |
| Совместно легированные трехмерные иерархические пористые угли ONS | 107 Втч / кг при 0,9 кВт / кг | BMIMBF 4 (3,6 В) | 214 Ф / г при 1 А / г | [12] |
| Графен | 61 Вт · ч кг -1 при 1 кВт / кг | Бутиролактон / BMIMBF 4 (3.7 В) | 131 Ф / г при 0,1 Ф / г | [36] |
| Пористый биоуглерод, обогащенный азотом и серой | 77,8 Вт · ч / кг при 0,5 кВт / кг | NaClO 4 / EC / DMC (3V) | 249 F / g при 0,5 A / g | [37] |
| Взаимосвязанные углеродные нанолисты на основе конопли | 50 Втч / кг при 1 кВт / кг | BMPY TFS (3 V) | 122 Ф / г при 1 А / г | [38] |
| Бимодальный микромезопористый биоуглерод с большой площадью поверхности | 60 Втч / кг при 0.1 кВт / кг | EMIM TFSI / AN (3V) | 160 Ф / г при 1 А / г | [39] |
| Пористый углерод, полученный из пульпы целлюлозных заводов | 51 Втч / кг при 375 Вт / кг | TEABF 4 / AN (3V) | 163 Ф / г при 0,1 А / г | [40] |
| УНТ | 47 Втч / кг при 1 кВт / кг | EMIMBF 4 (3 В) | 150 Ф / г при 5 мВ / с | [41] |
| Графеноподобные нанолисты из биоуглерода, легированного азотом | 51 Вт · ч / кг при 362 Вт / кг | EMITFSI / EMIBF 4 (3 В) | 162 Ф / г при 0.5 A / g | [42] |
| Иерархические пористые биоуглеродные микросферы с высокой удельной поверхностью | 57 Вт · ч / кг при 60 Вт / кг | TEABF 4 / AN (2,3 В) | 308 F / г при 2 мВ / с | [43] |
| Углерод из высокопористой графитовой биомассы | 50,16 Вт · ч / кг при 0,3 кВт / кг | EMIM-TFSI (3V) | без | [19] |
| 24,3 Вт · ч / кг при 1 кВт / кг | PVA / PVP / EMIHSO 4 / HQ (1.2 В) | 485 Ф / г при 0,85 А / г | [44] | |
| Связанные между собой пористые углеродные нанолисты | 45,5 Вт / кг при 750 Вт / кг | EMIMBF 4 (3 В) | 147 F / g при 1A / g | [45] |
| Необычные взаимосвязанные графитированные углеродные нанолисты | 64,7 Вт · ч / кг при 1 кВт / кг | EMITFSI / EMIBF 4 (3,5 В) | 152 F / g при 1 A / g | [46] |
| Мезопористые наночешки графена | 32.8 Втч / кг при 0,7 кВт / кг | N + Et 4 TFSI / CH 3 C (3V) | 105 F / g при 0,5 A / g | [47] |
| Иерархический пористые биоуглероды | 72,3 Втч / кг при 1,4 кВт / кг | ПВА / LiCl (0,8 В) | 226,0 Ф / г при 0,5 А / г | [48] |
| Иерархический пористый углерод | 4,2 Втч / кг при 0,1 кВт / кг | KOH (1V) | 171 Ф / г при 1 А / г | [49] |
| Пористый углерод с примесью меди из загрязненного тяжелыми металлами осадка сточных вод | 7.6 Вт · ч · / кг при 0,3 Вт / кг | KOH (1,2 В) | 159 Ф / г при 0,5 A / г | [50] |
| Полипиррол / углеродное волокно | 5,87 Вт · ч / кг при 60,0 Вт / кг | PVA / H 3 PO 4 (1,2 В) | 308,2 Ф / г при 5 мВ / с | [51] |
| Шаблонный углерод с примесью азота | 76 Втч / кг при 1 кВт / кг | EMImBF 4 (3,5 В) | 178 Ф / г при 0,2 А / г | [52] |
Учитывая, что помимо электродов на углеродной основе, общая масса Фактическое устройство суперконденсатора включает в себя некоторые неактивные и пассивные компоненты, такие как токосъемники, сепараторы, связующие и упаковка, графики Рагона, построенные только на массе электроактивного материала, не могут обеспечить прагматическую оценку энергетических и энергетических характеристик.Поскольку на долю углерода приходится примерно 30% коммерческих суперконденсаторов в корпусе (типично для крупномасштабных суперконденсаторов на базе переменного тока), повсеместно принимается коэффициент от 3 до 4 для экстраполяции реальных значений энергии и мощности из поведения электроактивные вещества в упакованном элементе [53]. показаны оба графика Рагона для суперконденсатора на основе C-0.75 в EMIBF 4 и подробный контраст с другими коммерческими установками электрохимического накопления энергии. Практическая удельная энергия постулированных упакованных СЭ может, как ожидается, достигнуть высокого значения примерно 15.91–29,43 Вт · ч кг −1 , что значительно превосходит коммерческие суперконденсаторы на основе углерода (3 ~ 5 Вт · ч · кг −1 ), в два раза выше, чем указано для гибридных электрохимических устройств с оксидом углерода, и даже выходит за пределы диапазона, предлагаемого батареи. В частности, такие нормированные плотности энергии могут сильно конкурировать со свинцово-кислотными батареями и батареями из метагидрида никеля (Ni-MH) (). Нормализованная плотность мощности составляет 0,33–6,67 кВт · кг −1 , что на порядок превосходит обе Ni-MH батареи (), в то время как значения для промышленных углеродных суперконденсаторов имеют значения плотности энергии от 4 до 5 Вт · ч кг — 1 .Таким образом, наши устройства не уступают коммерческим накопителям энергии. Что еще более важно, «репрезентативное время» также показывает, что установка может выполнить цикл зарядки-разрядки всего за несколько секунд при максимальной управляемой мощности 20 кВт кг -1 (). Вышеупомянутые результаты явно означают, что суперконденсатор на основе C-0,75 в EMIBF 4 обладает огромным потенциалом в будущих реалистичных требованиях, которые могут преодолеть пропасть между суперконденсаторами и батареями по характеристикам и материалам.
Сравнение суперконденсатора в корпусе на основе C-0.75 в EMIBF 4 с другими коммерческими накопителями электроэнергии (данные адаптированы из [54]).
4. Обсуждение
На самом деле супер емкостное поведение EMIBF 4 на серии C-0,25, C-0,5 и C-0,75 интересно и заставляет задуматься. Такая впечатляющая емкостная функция должна инициироваться эффектами оптимальной структуры пор с точки зрения смешанных микро- / мезопор и возникновения уникальных электрохимических процессов.Это конкретное электрохимическое событие должно происходить в объемах ИЖ вместо поверхностной конденсации EDL, как будет кратко обсуждено ниже. Удивительно, но чисто ультрамикропористый C-0,25 обладает эмпирически рекомендуемыми текстурными параметрами с большой удельной поверхностью (1084,3 м 2 г -1 ) и объемом пор (0,403 см 3 г -1 ), но он почти неактивен с точки зрения накопления энергии (4,8 F g -1 при 0,5 A g -1 ).В отличие от этого, увеличение в 2–2,5 раза удельной поверхности (2744,6 м 2 г -1 ) и объема пор (1,304 см 3 г -1 ) может невероятно привести к 33-кратному увеличению увеличение емкости (158,9 Ф г -1 ). Эта аномалия кажется очень убедительной, но противоречащей здравому смыслу, она сильно отличается от того, как обычно ведет себя емкость для хорошо идентифицированных водных электролитов. Это, несомненно, показывает, что заданная пористость (а не «постоянно» искомая удельная площадь поверхности и функционализация гетероатома) служит основной предпосылкой для поддержания эффективного накопления заряда в углеродных СК, пропитанных ИЖ, с помощью специального рабочего механизма.Фактически, ширина пор чисто ультрамикропористого C-0,25 составляет примерно 0,5 нм, и она намного меньше кристаллографического диаметра десольватированных ионов EMI + (~ 0,7 нм). Таким образом, его богатые ультрамикропоры слишком узки для того, чтобы EMIBF 4 мог отобрать образцы для создания обильных EDL, даже во время стадии медленного разряда и заряда при 0,5 A g -1 . Из-за инверсии заряда ионные частицы из ИЖ должны адсорбироваться и периодически переориентироваться в форме упорядоченной многослойной (послойной) сборки из попеременно распределенных катионов и анионов вне заряженных ультрамикропористых поверхностей C- 0.25. Противоположно заряженные ионы в этой схеме почти приняли ту же структуру кулоновского упорядочения, что и объемная фаза ИЖ, и, таким образом, имели достаточно высокую дальнодействующую взаимность, чтобы сопрягать поляризацию самого верхнего адсорбционного слоя с поляризацией смежного слоя [55,56 ]. Это приводит к колебаниям плотности демпфирующего заряда, что означает, что первый уровень противоионов может достигать максимальной плотности, в то время как следующий богатый коионами слой имеет меньшую плотность (все еще превышающую объемные значения). То есть, чтобы обеспечить нейтральность заряда для всей системы, заряды первого адсорбционного слоя превышают заряды поверхностей электродов, но сразу же компенсируются вторым слоем.Такое поведение компенсации может распространяться за пределы нескольких уровней, так что крошечная часть абсорбентов эффективно используется при вводе и выводе электроэнергии. Наконец, возникают такие вредные эффекты насыщения решетки и чрезмерного экранирования, ведущие к C-0,25, который имеет большую площадь поверхности 1084,3 м 2 г -1 , чтобы обменивать только довольно небольшое количество энергии 4,8 F г -1 .
Поскольку поры в C-0.5 имеют диаметр 0,8 нм (почти идентичны размеру обнаженных ионов EMI + ), они могут вмещать только один слой электросорбированных ионов.Эти электросорбированные ионы могут попасть в микропоры за счет хорошей комбинации внешних потенциалов, капиллярных сил, электростатических взаимодействий иона со стенкой, сил изображения и так далее. Затем они будут претерпевать всевозможные локальные микросреды атомного масштаба внутри пор размером с ионы, чтобы разрушить чередующиеся кулоновские структуры анионов и катионов, при этом как в ближайших координационных оболочках вокруг центрального иона, так и в изображении будет происходить заметное спаривание коионов. встречные заряды, возникающие в боковых атомах углерода.В этом случае все заряды, переносимые первым адсорбционным слоем в порах, могут более точно уравновешивать изображения боковых стенок углеродных пор, что способствует гораздо большей эффективности; сродство ионов в первом слое к поверхностям боковых стенок не нейтрализуется хорошо собранным прилегающим коионным слоем, тем самым самоусиливая разделение ионов и заряд поверхности. Такое четкое расположение ионов в порах должно подавлять так называемые многослойные структуры, возникающие в C-0.25, изменение распределения ионов на микропоры размером с ионы и межфазные свойства ионных частиц [57,58]. В результате емкость в порах C-0,5 размером с ионы может увеличиваться до 54,7 Ф г -1 ; а именно, только 1,9-кратное увеличение удельной поверхности неожиданно приводит к увеличению емкости на один порядок по сравнению с C-0,25. Для C-0,5 его общая удельная поверхность составляет 2050,3 м 2 г -1 с вкладом микропористости до 1770.1 м 2 г −1 . Общий объем и микропористый объем равны 0,825 и 0,718 см 3 г -1 , соответственно. Учитывая очень узкое распределение пор по размерам, площадь поверхности и объемы пор должны в основном определяться размером пор размером с ионы (размером около 0,8 нм). Таким образом, очевидное увеличение емкости должно иметь тесную связь с уникальным разделением ионов при однослойном ограничении.
Интересно, что помимо микропор размером с ион (0.8 нм), определенная часть пор размером с двойной ион (1,5 нм) успешно создается в C-0.75. Что еще более важно, общая площадь поверхности и объем пор достигают 2744 м 2 г -1 и 1.304 см 3 г -1 соответственно; площадь и объем микропористой поверхности по-прежнему сохраняют значения 1864,1 м 2 г -1 и 0,826 см 3 г -1 , что очень похоже на аналоги C-0,5. Согласно изложенным выше механизмам накопления заряда С-0.5, увеличение удельной поверхности C-0,75 в 1,3 раза по сравнению с C-0,5 должно дать емкость около 92 Ф · г -1 , а не резкое увеличение до аномального экспериментального значения 158,9 Ф · г — 1 . В частности, должна была быть достигнута сопоставимая емкость между C-0,5 и C-0,75, потому что они оба имеют почти одинаковые площади поверхности и объем микропор. Количественно площадь поверхности 880,5 м 2 г -1 от мезопор (32.1%) составляет 42,1% от общей емкости. Это явление явно противоречит предыдущей точке зрения на эффект просеивания ионов, которая предполагает, что только тогда, когда ион идеально подстраивается под размер пор, чтобы минимизировать свободное пространство, максимальная емкость ИЖ внутри нанопор происходит при критическом соотношении размера пор / иона. из ≈ 1 [59,60]. На основании таких перспектив уникальный механизм разделения ионов для C-0,5 должен был быть скрыт для C-0,75, который имеет гораздо более широкую PSD в диапазоне от 0.От 8 до 1,5 нм, поскольку экспериментально измеренная емкость может быть усреднена по широкой ширине поры. Этот эффект затемнения или усреднения должен был значительно снизить общую емкость на C-0,75 вместо того, чтобы поразительно увеличиться до 158,9 Ф · г -1 . Фактически, моно- и двухслойные эффекты ограничения сосуществуют и надежно взаимодействуют в C-0.75. Это наблюдение убедительно подтверждает, что вновь созданные мезопоры размером 1,5 нм (удвоенный диаметр иона) действительно лежат в основе более эффективного, но отличного режима накопления энергии, что в основном приводит к увеличению емкости.Эффективность накопления энергии в порах 1,5 нм значительно превышает таковую внутри микропор 0,8 нм. Помимо удержания одного ионного слоя в порах размером с ионы размером 0,8 нм, поры 1,5 нм идеально удваивают размер иона и, следовательно, почти вмещают два противоионных слоя за счет более эффективной упаковки ионов, а не только за счет снижения доступности пор. По сути, аномальная модификация емкости должна происходить как из-за сильно усиленной степени удержания, так и из-за конструктивного перекрытия двойного электрического слоя адсорбентов внутри 1.Поры 5 нм, с помощью которых полностью подавляется вредное чрезмерное экранирование межионных сетей электростатической корреляции дальнего действия, что приводит к более усиленному разделению ионов (отличающемуся большей емкостью). За счет объединения обоих эффектов может также происходить более сильное электростатическое противодействие (за счет боковой стенки углеродной поры) кулоновским взаимодействиям отталкивания между ионами с одинаковым зарядом (а именно, более сильная суммарная поверхностная зарядка атомов углерода), что обеспечивает «геометрически ограниченное предпочтение». стэкинг ионов в углеродном нанопространстве.В частности, вызванный ограничением высокоэнергетический фазовый и конформационный переход ИЖ внутри нанополостей происходит, как было исследовано в предыдущих исследованиях [52,61,62,63,64]. В полной мере используя обнаруженные здесь новые эффекты, SC (обладающие благоприятными характеристиками стоимости, устойчивости, скорости и срока службы, несмотря на наличие основного недостатка, заключающегося в низкой удельной плотности энергии) могут быть улучшены для достижения характеристик батарей. Хотя представляется очень трудным предсказать эту перспективу, мы уверены, что как использование меньших или более координирующих ионных жидкостей, так и оптимизация взаимодействия углеродных боковых стенок и ионов для облегчения гладких электрохимических реакций в тонко модулированных нанопорах может позволить дальнейшее перекрытие пропасти между SC. и настоящие аккумуляторные решения.
В целом, разделение их соответствующих вкладов в материалы углеродных электродов с различной шириной пор и функционализацией гетероатомов несет большой потенциал для дальнейшего совершенствования устройств хранения энергии на основе углерода. Например, наше открытие доказывает, что включение определенных адсорбционных центров для усиления сродства углеродной боковой стенки к иону электролита и, таким образом, для стабилизации декорации высокоэнергетического электролита, представляет собой потенциальную стратегию для дальнейшего увеличения отношения плотности энергии к мощности суперконденсаторов, в отличие от к бесконечному поиску все более крупных микропор и площадей поверхности.В конце концов, раскрытые эффекты могут высвободить неизведанный потенциал для оптимизации режимов накопления энергии и эффективности в электролитзависимых СЭ посредством контролируемого регулирования компонентов электролита (например, путем введения следовых количеств неорганических солей или растворителей, или путем изменения ионов ИЖ. характер или тип).
Влияние структуры пор электродов и раствора
% PDF-1.7 % 1 0 объект > эндобдж 2 0 obj > поток 2019-09-06T11: 25: 20-07: 002019-09-06T11: 25: 20-07: 002019-09-06T11: 25: 20-07: 00Appligent AppendPDF Pro 5.5uuid: 21dc163f-ac69-11b2-0a00-782dad000000uuid: 21dc4e04-ac69-11b2-0a00-80efcefffe7fapplication / pdf
Роль кислородных вакансий, состава электролита, структуры решетки и плотности легирования на электрохимическую реакционную способность анодов TiO2 в фазе Магнели
Субстехиометрический TiO 2 (Ti n O 2 n −1 , 4 ≤ n ≤ 10) — перспективный и экономичный материал, который исследуется для многих приложений, таких как хранение информации, хранение и преобразование энергии, а также очистка воды.При расширенной анодной поляризации Ti n O 2 n -1 , как сообщается, страдает постепенной потерей проводимости и электрохимической реактивности. В этом исследовании механизмы дезактивации и реактивации поверхности были исследованы на монолитном электроде Ti n O 2 n −1 в трех различных растворах электролита (, т.е. , H 2 SO 4 , HClO 4 , HCl).Собственные электронные свойства, кинетика переноса заряда, кристаллическая структура и состав поверхности были экспериментально исследованы после анодной и катодной поляризаций. Статистически эквивалентные результаты были получены с помощью локальной сканирующей электрохимической микроскопии (SECM) и измерения объемной спектроскопии электрохимического импеданса, которые показывают, что данные SECM с пространственным разрешением точно характеризуют кинетику переноса заряда Ti n O 2 n — 1 электрод в микронном масштабе.Результаты показывают, что уменьшение проводимости и кинетики переноса заряда после анодной поляризации во всех трех электролитах в первую очередь связано с потерей носителей заряда, таких как разряд H + на Ti 3+ точечных донорных сайтах и процесс был обратимым во время катодной поляризации через интеркалирование H + . В электролите H 2 SO 4 также произошла обратимая пассивация поверхности, которую приписали образованию поверхностных частиц TiOSO 4 , присутствие которых подтверждено экспериментальными измерениями и расчетами теории функционала плотности.Также было установлено, что кристаллическая структура Ti n O 2 n −1 непосредственно влияет на скорость образования гидроксильных радикалов, причем наибольшая скорость наблюдается для Ti 4 O 7 , который также обладал наибольшей плотностью носителей заряда.
онлайн-курсов PDH. PDH для профессиональных инженеров. ПДХ Инжиниринг.
«Мне нравится широта ваших курсов по HVAC; не только экология или экономия энергии.
курсов.»
Russell Bailey, P.E.
Нью-Йорк
«Он укрепил мои текущие знания и научил меня еще нескольким новым вещам.
, чтобы познакомить меня с новыми источниками
информации.
Стивен Дедак, П.Е.
Нью-Джерси
«Материал был очень информативным и организованным.Я многому научился, и они были
очень быстро отвечает на вопросы.
Это было на высшем уровне. Будет использовать
снова. Спасибо. «
Blair Hayward, P.E.
Альберта, Канада
«Простой в использовании веб-сайт. Хорошо организованный. Я действительно воспользуюсь вашими услугами снова.
проеду по вашей компании
имя другим на работе.»
Roy Pfleiderer, P.E.
Нью-Йорк
«Справочные материалы были превосходными, и курс был очень информативным, особенно потому, что я думал, что я уже знаком с
с подробной информацией о Канзасе
Городская авария Хаятт «.
Майкл Морган, P.E.
Техас
«Мне очень нравится ваша бизнес-модель.Мне нравится просматривать текст перед покупкой. Нашел класс
информативно и полезно
в моей работе ».
Вильям Сенкевич, П.Е.
Флорида
«У вас большой выбор курсов, а статьи очень информативны. You
— лучшее, что я нашел ».
Рассел Смит, П.E.
Пенсильвания
«Я считаю, что такой подход позволяет работающему инженеру легко зарабатывать PDH, давая время на просмотр
материал «
Jesus Sierra, P.E.
Калифорния
«Спасибо, что позволили мне просмотреть неправильные ответы. На самом деле,
человек учится
от сбоев.»
John Scondras, P.E.
Пенсильвания
«Курс составлен хорошо, и использование тематических исследований является эффективным.
способ обучения «
Джек Лундберг, P.E.
Висконсин
«Я очень впечатлен тем, как вы представляете курсы, т.е. позволяете
студент для ознакомления с курсом
материалов до оплаты и
получает викторину.»
Арвин Свангер, П.Е.
Вирджиния
«Спасибо за то, что вы предложили все эти замечательные курсы. Я определенно выучил и
получил огромное удовольствие «.
Мехди Рахими, П.Е.
Нью-Йорк
«Я очень доволен предлагаемыми курсами, качеством материалов и простотой поиска.
на связи
курсов.»
Уильям Валериоти, P.E.
Техас
«Этот материал в значительной степени оправдал мои ожидания. По курсу было легко следовать. Фотографии в основном обеспечивали хорошее наглядное представление о
.обсуждаемых тем ».
Майкл Райан, P.E.
Пенсильвания
«Именно то, что я искал. Потребовался 1 балл по этике, и я нашел его здесь.»
Джеральд Нотт, П.Е.
Нью-Джерси
«Это был мой первый онлайн-опыт получения необходимых мне кредитов PDH. Это было
информативно, выгодно и экономично.
Я очень рекомендую
всем инженерам ».
Джеймс Шурелл, П.Е.
Огайо
«Я понимаю, что вопросы относятся к« реальному миру »и имеют отношение к моей практике, и
не на основании каких-то неясных раздел
законов, которые не применяются
по «нормальная» практика.»
Марк Каноник, П.Е.
Нью-Йорк
«Отличный опыт! Я многому научился, чтобы перенести его на свой медицинский прибор.
организация «
Иван Харлан, П.Е.
Теннесси
«Материалы курса имели хорошее содержание, не слишком математическое, с хорошим акцентом на практическое применение технологий».
Юджин Бойл, П.E.
Калифорния
«Это был очень приятный опыт. Тема была интересной и хорошо изложенной,
а онлайн-формат был очень
Доступно и просто
использовать. Большое спасибо «.
Патрисия Адамс, P.E.
Канзас
«Отличный способ добиться соответствия требованиям PE Continuing Education в рамках ограничений по времени лицензиата.»
Joseph Frissora, P.E.
Нью-Джерси
«Должен признаться, я действительно многому научился. Помогает иметь распечатанный тест во время
обзор текстового материала. Я
также оценил просмотр
фактических случаев «.
Жаклин Брукс, П.Е.
Флорида
«Документ» Общие ошибки ADA при проектировании объектов «очень полезен.
испытание потребовало исследований в
документ но ответы были
в наличии «
Гарольд Катлер, П.Е.
Массачусетс
«Я эффективно использовал свое время. Спасибо за широкий выбор вариантов.
в транспортной инженерии, что мне нужно
для выполнения требований
Сертификат ВОМ.»
Джозеф Гилрой, П.Е.
Иллинойс
«Очень удобный и доступный способ заработать CEU для моих требований PG в Делавэре».
Ричард Роудс, P.E.
Мэриленд
«Я многому научился с защитным заземлением. До сих пор все курсы, которые я прошел, были отличными.
Надеюсь увидеть больше 40%
курсов со скидкой.»
Кристина Николас, П.Е.
Нью-Йорк
«Только что сдал экзамен по радиологическим стандартам и с нетерпением жду возможности сдать дополнительный
курсов. Процесс прост, и
намного эффективнее, чем
в пути «.
Деннис Мейер, P.E.
Айдахо
«Услуги, предоставляемые CEDengineering, очень полезны для профессионалов.
Инженеры получат блоки PDH
в любое время.Очень удобно ».
Пол Абелла, P.E.
Аризона
«Пока все отлично! Поскольку я постоянно работаю матерью двоих детей, у меня мало
время исследовать где
получить мои кредиты от. «
Кристен Фаррелл, P.E.
Висконсин
«Это было очень познавательно и познавательно.Легко для понимания с иллюстрациями
и графики; определенно делает это
легче поглотить все
теорий. «
Виктор Окампо, P.Eng.
Альберта, Канада
«Хороший обзор принципов работы с полупроводниками. Мне понравилось пройти курс по
.мой собственный темп во время моего утром
до метро
на работу.»
Клиффорд Гринблатт, П.Е.
Мэриленд
«Просто найти интересные курсы, скачать документы и взять
викторина. Я бы очень рекомендовал
вам на любой PE, требующий
CE единиц. «
Марк Хардкасл, П.Е.
Миссури
«Очень хороший выбор тем из многих областей техники.»
Randall Dreiling, P.E.
Миссури
«Я заново узнал то, что забыл. Я также рад оказать финансовую помощь
по ваш промо-адрес электронной почты который
сниженная цена
на 40% «
Конрадо Казем, П.E.
Теннесси
«Отличный курс по разумной цене. Воспользуюсь вашими услугами в будущем».
Charles Fleischer, P.E.
Нью-Йорк
«Это был хороший тест и фактически подтвердил, что я прочитал профессиональную этику
кодов и Нью-Мексико
правил. «
Брун Гильберт, П.E.
Калифорния
«Мне очень понравились занятия. Они стоили потраченного времени и усилий.»
Дэвид Рейнольдс, P.E.
Канзас
«Очень доволен качеством тестовых документов. Буду использовать CEDengineerng
при необходимости дополнительно
сертификация. «
Томас Каппеллин, П.E.
Иллинойс
«У меня истек срок действия курса, но вы все же выполнили свое обязательство и дали
мне то, за что я заплатил — много
оценено! «
Джефф Ханслик, P.E.
Оклахома
«CEDengineering предлагает удобные, экономичные и актуальные курсы.
для инженера »
Майк Зайдл, П.E.
Небраска
«Курс был по разумной цене, а материалы были краткими, а
хорошо организовано. «
Глен Шварц, П.Е.
Нью-Джерси
«Вопросы подходили для уроков, а материал урока —
.хороший справочный материал
для деревянного дизайна. «
Брайан Адамс, П.E.
Миннесота
«Отлично, я смог получить полезные рекомендации по простому телефонному звонку.»
Роберт Велнер, P.E.
Нью-Йорк
«У меня был большой опыт работы в прибрежном строительстве — проектирование
Building курс и
очень рекомендую .»
Денис Солано, P.E.
Флорида
«Очень понятный, хорошо организованный веб-сайт. Материалы курса по этике в Нью-Джерси были очень хорошими.
хорошо подготовлены. »
Юджин Брэкбилл, P.E.
Коннектикут
«Очень хороший опыт. Мне нравится возможность загружать учебные материалы на
.обзор везде и
всякий раз, когда.»
Тим Чиддикс, P.E.
Колорадо
«Отлично! Поддерживаю широкий выбор тем на выбор».
Уильям Бараттино, P.E.
Вирджиния
«Процесс прямой, никакой ерунды. Хороший опыт».
Тайрон Бааш, П.E.
Иллинойс
«Вопросы на экзамене были зондирующими и демонстрировали понимание
материала. Полная
и всесторонний ».
Майкл Тобин, P.E.
Аризона
«Это мой второй курс, и мне понравилось то, что мне предлагали курс
поможет по моей линии
работ.»
Рики Хефлин, P.E.
Оклахома
«Очень быстро и легко ориентироваться. Я определенно буду использовать этот сайт снова».
Анджела Уотсон, П.Е.
Монтана
«Легко выполнить. Нет путаницы при подходе к сдаче теста или записи сертификата».
Кеннет Пейдж, П.E.
Мэриленд
«Это был отличный источник информации о солнечном нагреве воды. Информативный
и отличный освежитель ».
Луан Мане, П.Е.
Conneticut
«Мне нравится, как зарегистрироваться и читать материалы в автономном режиме, а затем
Вернуться, чтобы пройти викторину «
Алекс Млсна, П.E.
Индиана
«Я оценил объем информации, предоставленной для класса. Я знаю
это вся информация, которую я могу
использование в реальных жизненных ситуациях »
Натали Дерингер, P.E.
Южная Дакота
«Обзорные материалы и образец теста были достаточно подробными, чтобы позволить мне
успешно завершено
курс.»
Ира Бродская, П.Е.
Нью-Джерси
«Веб-сайтом легко пользоваться, вы можете скачать материал для изучения, а потом вернуться
и пройдите викторину. Очень
удобно а на моем
собственный график «
Майкл Гладд, P.E.
Грузия
«Спасибо за хорошие курсы на протяжении многих лет.»
Деннис Фундзак, П.Е.
Огайо
«Очень легко зарегистрироваться, получить доступ к курсу, пройти тест и распечатать PDH
сертификат. Спасибо за создание
процесс простой ».
Фред Шейбе, P.E.
Висконсин
«Положительный опыт.Быстро нашел курс, который соответствовал моим потребностям, и закончил
один час PDH в
один час. «
Стив Торкильдсон, P.E.
Южная Каролина
«Мне понравилось загружать документы для проверки содержания
и пригодность, до
имея для оплаты
материал .»
Ричард Вимеленберг, P.E.
Мэриленд
«Это хорошее напоминание об ЭЭ для инженеров, не занимающихся электричеством».
Дуглас Стаффорд, П.Е.
Техас
«Всегда есть возможности для улучшения, но я ничего не могу придумать в вашем
.процесс, которому требуется
улучшение.»
Thomas Stalcup, P.E.
Арканзас
«Мне очень нравится удобство участия в онлайн-викторине и получение сразу
сертификат. «
Марлен Делани, П.Е.
Иллинойс
«Учебные модули CEDengineering — очень удобный способ доступа к информации по номеру
.много различные технические зоны за пределами
по своей специализации без
приходится путешествовать.»
Гектор Герреро, П.Е.
Грузия
Триада спортсменок — Американский семейный врач
1. Американская психиатрическая ассоциация. Диагностическое и статистическое руководство по психическим расстройствам. 4-е изд. Вашингтон, округ Колумбия: Американская психиатрическая ассоциация, 1994: 539–50 ….
2. Розен Л.В., Хотя ДЕЙСТВИТЕЛЬНО. Патогенетическое поведение гимнасток колледжей по контролю веса. Физическая спортивная медицина . 1988. 16: 140–3.
3. Розен Л.В., McKeag DB, Hough DO, Керли В. Патогенное поведение, связанное с контролем веса у спортсменок. Физическая спортивная медицина . 1986; 14: 79–84.
4. Сундгот-Борген Дж. Факторы риска и триггеры развития расстройств пищевого поведения у спортсменок высокого уровня. Медико-спортивные упражнения . 1994; 26: 414–9.
5. Отис CL. Аменорея, связанная с физическими упражнениями. Clin Sports Med . 1992; 11: 351–62.
6. Шангольд М, Арматура RW, Венц А.С., Шифф И. Оценка и лечение менструальной дисфункции у спортсменов. ЯМА . 1990; 263: 1665–9.
7. Nattiv A, Агостини Р, Дринкуотер Б, Йегер К.К. Триада спортсменок. Взаимосвязь расстройства пищевого поведения, аменореи и остеопороза. Clin Sports Med . 1994; 13: 405–18.
8. Отис CL, Дринкуотер Б, Джонсон М, Loucks A, Уилмор Дж.Позиционный стенд Американского колледжа спортивной медицины. Триада спортсменок. Медико-спортивные упражнения . 1997; 29: i – ix.
9. Дринкуотер БЛ, Брумнер Б, Чеснут CH 3d. Менструальный анамнез как фактор, определяющий текущую плотность костной ткани у молодых спортсменов. ЯМА . 1990; 263: 545–8.
10. Сколник А.А. Риск «триады спортсменок» для женщин. ЯМА . 1993; 270: 921–3.
11. Кинингем РБ, Апгар Б.С., Schwenk TL.Оценка аменореи. Врач Фам . 1996; 53: 1185–94.
12. Ренкен М.Л., Чеснут СН 3д, Дринкуотер BL. Плотность костей на нескольких участках скелета у спортсменов с аменореей. ЯМА . 1996; 276: 238–40.
13. Myburgh KH, Хатчинс Дж., Фатар AB, Hough SF, Ноукс Т.Д. Низкая плотность костной ткани является этиологическим фактором стрессовых переломов у спортсменов. Энн Интерн Мед. .1990; 113: 754–9.
14. Мандельбаум Б.Р., Наттив А. Гимнастика. В: Reider B, ed. Спортивная медицина: спортсмен школьного возраста. 2-е изд. Филадельфия: Сондерс, 1996.
15. Маткович В., Елич Т, Wardlaw GM, Ильич Ю.З., Гоэль П.К., Райт Дж. К., и другие. Время пика костной массы у кавказских женщин и его значение для профилактики остеопороза. Вывод из поперечной модели. Дж. Клин Инвест . 1994; 93: 799–808.
16. Лу П.В., Бриоди Дж. Н., Огл Г.Д., Морли К., Хамфрис ИК, Аллен Дж. и другие. Минеральная плотность костной ткани всего тела, позвоночника и шейки бедра у детей и молодых людей: поперечное и продольное исследование. J Bone Miner Res . 1994; 9: 1451–8.
17. Вуори И. Пиковая костная масса и физическая активность: краткий обзор. Nutr Ред. . 1996; 54: S11–4.
18. Янг Д., Хоппер JL, Nowson CA, Зеленый РМ, Шервин А.Дж., Каймакчи Б, и другие.Детерминанты костной массы у женщин от 10 до 26 лет: двойное исследование. J Bone Miner Res . 1995; 10: 558–67.
19. Камминг, округ Колумбия. Аменорея, связанная с физическими упражнениями, низкая плотность костной ткани и заместительная терапия эстрогенами. Arch Intern Med . 1996; 156: 2193–5.
20. ДеЧерни А. Костосберегающие свойства оральных контрацептивов. Am J Obstet Gynecol . 1996. 174: 15–20.
21. Беннелл К.Л., Малькольм С.А., Томас С.А., Эбелинг PR, МакКрори PR, Wark JD.Факторы риска стрессовых переломов у легкоатлеток: ретроспективный анализ. Clin J Sport Med . 1995; 5: 229–35.
22. Fagan KM. Фармакологическое лечение спортивной аменореи. Clin Sports Med . 1998; 17: 327–41.
23. Конференция NIH Consensus. Оптимальное потребление кальция. Группа разработки консенсуса NIH по оптимальному потреблению кальция. ЯМА . 1994; 272: 1942–8.
24. Американский колледж акушеров и гинекологов.Образовательный бюллетень ACOG. Остеопороз. № 246, апрель 1998 г. (заменяет № 167, май 1992 г.). Int J Gynaecol Obstet . 1998. 62: 193–201.
25. переулок JM, Нидик М.
