Плотность электролита в аккумуляторе – проверка, измерение в разряженном состоянии + Видео » АвтоНоватор
Плотность электролита в аккумуляторе – головная боль автовладельцев, которые сделали выбор в пользу разборных АКБ. Эти батареи можно контролировать и перезаряжать, но для этого нужно освоить небольшую науку, чем мы с вами и займемся.
Содержание
1 Какие значения плотности электролита считают нормой?
2 Проверка плотности электролита – приборы и их действие
3 Как повысить плотность рабочего электролита?
Какие значения плотности электролита считают нормой?
Аккумуляторная батарея – химический источник тока, и происходящие в нем превращения носят обратимый характер. Конструкция подобных устройств несложная, они состоят из корпуса, где размещены электроды, сепаратора-конвертора и шины. Закрывается это все крышкой с выходными отверстиями и клеммами. Но аккумулятор не будет работать без электролита. В свинцово-кислотных батареях это раствор серной кислоты, плотность которого измеряется в г/см3. Она пропорциональна концентрации раствора, а обратная зависимость прослеживается относительно температуры жидкости. Проверка плотности щелочного электролита будет проводиться теми автовладельцами, в машине которых используются никель-кадмиевые или никель-железные батареи.
В свинцово-кислотных батареях это раствор серной кислоты, плотность которого измеряется в г/см3. Она пропорциональна концентрации раствора, а обратная зависимость прослеживается относительно температуры жидкости. Проверка плотности щелочного электролита будет проводиться теми автовладельцами, в машине которых используются никель-кадмиевые или никель-железные батареи.
Аккумуляторные батареи для авто
По плотности электролита автомобильного аккумулятора можно определить состояние батареи. Если значение понизилось, то, вероятнее всего, какая-то ячейка с дефектом, произошел обрыв цепи или глубокий разряд АКБ. Для последнего случая пониженная плотность будет во всех ячейках. Если батарея не держит заряд, то следует проверить состояние жидкости внутри нее. Во время работы АКБ вода постепенно испаряется, в результате электролит становится более концентрированным, что тоже негативно сказывается на состоянии агрегата. Эта характеристика влияет на емкость батареи и определяет ее эксплуатационный срок.
Определение плотности электролита автомобильного аккумулятора
Очень важно выдерживать оптимальные показатели плотности электролита в АКБ, которые во многом зависят от климатической зоны. В регионах с холодным макроклиматом плотность кислотного электролита лучше поддерживать в диапазоне 1,27–1,29 г/см3. В средней полосе эти цифры изменятся – 1,25–1,27 г/см3. В более теплых районах нормальная плотность составляет 1,23–1,25 г/см3. Причем при заливке электролита лучше готовить раствор по нижней границе указанных диапазонов. Для щелочного аккумулятора проверка плотности внутреннего содержимого должна показывать 1,19–1,21 г/см3. Перед приготовлением важно уточнять состав, бывают калиевые и натриевые электролиты, для каждого из них будут свои пропорции, чтобы добиться указанного значения.
Мнение эксперта
Руслан Константинов
Эксперт по автомобильной тематике. Окончил ИжГТУ имени М.Т. Калашникова по специальности «Эксплуатация транспортно-технологических машин и комплексов».
В большинстве случаев электролит представляет собой раствор из серной кислоты и дистиллированной воды примерно в пропорциях примерно 2/1 (60% воды и 40% кислоты). При таком соотношении пластины аккумулятора способны накапливать электрический заряд. Многие знают о плотности электролита, но немногие знают, почему этот параметр меняется от разрядов и зарядов. Когда аккумулятор заряжается, из электролита выводится вода, соответственно процентное соотношение начинает меняться в пользу кислоты. При разряде АКБ наоборот снижается концентрация кислоты, на пластинах она начинает оседать сульфатами. При глубоком разряде то пластины попросту зарастут сульфатами, которые при следующем заряде уже не будут разрушаться, происходит процесс так называемой сульфатации. Это явление опасно тем, что постепенно плотность сильно снизится и зарядка уже не поможет восстановить работоспособность аккумулятора из-за чрезмерной сульфатации.
Не стоит экспериментировать и с повышением плотности, некоторые считают, что проще вовсе использовать концентрированную серную кислоту, например, при эксплуатации автомобиля в условиях критически низких температур. Делать так нельзя, серная кислота является одним из самых мощных растворителей, она попросту может разъесть свинцовые пластины. Превышать плотность более чем на 1,35 г/см3 недопустимо.
Проверка плотности электролита – приборы и их действие
Многие автомобилисты сталкивались с ситуацией, когда после длительного перезаряда электролит закипает и испаряется, тогда мы заливаем дистиллированную воду. При этом очень редко измеряется плотность раствора, а зря. Ведь вместе с водой выкипает еще и сама кислота, а добавив только дистиллят, вы получите смесь с меньшей концентрацией, что негативно скажется на работоспособности устройства.
Заливание дистиллированной воды в АКБ
Для измерения плотности электролита в аккумуляторе понадобится специальный прибор – денсиметр. Он состоит из стеклянной трубки, в которую помещен ареометр, наконечника и резиновой груши. Находим у батареи заливное отверстие и погружаем в раствор наконечник измерительного устройства. Затем с помощью груши засасываем часть кислоты внутрь стеклянного корпуса. Аккуратно держим прибор на уровне глаз – ареометр должен находиться в состоянии покоя, плавать в жидкости, не касаясь стенок.
Измерения плотности электролита в аккумуляторе
Если нет специального прибора, то можно произвести проверку плотности электролита в аккумуляторе и с помощью вольтметра. Подключаем к клеммам аккумулятора автотестер и измеряем напряжение. Оно должно колебаться в пределах 11,9–12,5 В. Затем поворачиваем ключ в зажигании и набираем 2,5 тысячи оборотов. В этом случае напряжение должно достигнуть минимум 13,9 В, но не превышать 14,4 В. Если никаких изменений не произошло, значит, необходимо просто зарядить устройство.
Как повысить плотность рабочего электролита?
Что делать, когда в аккумуляторе упала плотность электролита? Конечно, необходимо ее восстановить до нужного значения. Существует несколько способов:
- перезарядить батарею;
- полностью заменить электролит новым;
- добавить более концентрированный электролит;
- добавить кислоту.
Заранее подготавливаем весь необходимый инвентарь: мерную емкость, грушу, паяльник и дрель. Все предметы должны быть чистыми и хорошо высушенными. Также нам понадобится дистиллированная вода и сам электролит.
Сначала всегда следует попробовать перезарядить аккумулятор. Проверяем напряжение АКБ. После набора оборотов его значение не изменилось? Тогда следует в течение 10 часов заряжать устройство током, который в десять раз меньше емкости. Например, если она равна 60 А*час, то достаточно тока 6 А. Затем понижают это значение вдвое и еще оставляют АКБ на подзарядке в течение 2 часов. Именно второй режим и выравнивает плотность электролита. А если напряжение при заведенном двигателе поднимается более 14,4 В, то нужно залить в аккумулятор воду. Потом поставить батарею на зарядку. Если после таких мероприятий АКБ все равно быстро разряжается, то нужно работать с электролитом.
Затем понижают это значение вдвое и еще оставляют АКБ на подзарядке в течение 2 часов. Именно второй режим и выравнивает плотность электролита. А если напряжение при заведенном двигателе поднимается более 14,4 В, то нужно залить в аккумулятор воду. Потом поставить батарею на зарядку. Если после таких мероприятий АКБ все равно быстро разряжается, то нужно работать с электролитом.
Проверка напряжения АКБ
Чтобы вернуть в норму значение плотности электролита в разряженном аккумуляторе, можно полностью заменить содержимое. Для этого следует максимально выкачать жидкость из каждой банки, а потом слить остатки. Чтобы это сделать, герметично закрываем все отверстия и переворачиваем агрегат набок. Просверливаем на дне дырочки со стороны каждой банки и сливаем электролит. Категорически запрещено ставить АКБ вверх дном, так как в таком положении может произойти короткое замыкание, а поверхность пластин осыпется. После того как раствора в устройстве уже не будет, тщательно промываем его очищенной водой.
Обычно плотность электролита в аккумуляторах можно повысить либо понизить, доливая концентрированный раствор или очищенную воду. В первую очередь проводится проверка качества токопроводящего вещества в каждой банке по отдельности. Если измерение показало плотность более 1,18 г/см3, тогда можно просто разбавить его более концентрированным раствором. Для этого отбираем максимально возможное количество электролита, половину его заменяем раствором с большей концентрацией, чем мы стремимся получить (например, нам надо 1,25 г/см3), и заливаем все это обратно. Болтаем батарею аккуратно, чтобы хорошо перемешать обновленный состав.
Более концентрированный электролит можно приготовить самим, тогда лучше сделать 1,40 г/см 3. Покупной, скорее всего, будет 1,27 г/см3, тогда процесс повышения плотности может немного затянуться.
Приготовление концентрированного электролита
После небольшой паузы проводится проверка плотности. Вы обнаружите, что она повысилась, но не достигла нужной цифры. Тогда повторяем процедуру снова, только шаг разбавления уменьшаем, чтобы не перескочить целевую отметку. На это раз заменить более концентрированным электролитом нужно только четверть выкачанной жидкости. После каждой процедуры измерение будет показывать, что мы все ближе к заветной отметке на приборе. Точно получить нормальную плотность электролита в аккумуляторе таким способом сложно, вероятно, вы проскочите нужную отметку, но к тому моменту достаточно будет добавить чуть-чуть чистой воды, ведь шаг разбавления станет уже совсем маленьким и цель будет достигнута.
Вы обнаружите, что она повысилась, но не достигла нужной цифры. Тогда повторяем процедуру снова, только шаг разбавления уменьшаем, чтобы не перескочить целевую отметку. На это раз заменить более концентрированным электролитом нужно только четверть выкачанной жидкости. После каждой процедуры измерение будет показывать, что мы все ближе к заветной отметке на приборе. Точно получить нормальную плотность электролита в аккумуляторе таким способом сложно, вероятно, вы проскочите нужную отметку, но к тому моменту достаточно будет добавить чуть-чуть чистой воды, ведь шаг разбавления станет уже совсем маленьким и цель будет достигнута.
Когда плотность электролита менее 1,18 г/см3, придется добавлять кислоту. Все операции проводим в том же порядке, как и в способе 3. Только шаг разбавления сразу стоит брать небольшой, потому что у кислоты очень высокая плотность (около 1,8 г/см3), перескочить нужную отметку можно уже с первого разбавления. Очень важно при приготовлении всех растворов вливать кислоту в воду, а не наоборот, чтобы не провоцировать разбрызгивание концентрата. Проводите работы в специальной робе, защищайте кожу и органы зрения. Если жидкость попала на тело, немедленно промойте пораженный участок чистой водой.
Проводите работы в специальной робе, защищайте кожу и органы зрения. Если жидкость попала на тело, немедленно промойте пораженный участок чистой водой.
- Автор: Михаил
- Распечатать
Оцените статью:
(1 голос, среднее: 5 из 5)
Поделитесь с друзьями!
Adblock
detector
Как проверить плотность электролита аккумулятора
Содержание:
- Что такое плотность?
- Какой она должна быть?
- Подготовительная работа
- Техника безопасности при проверке
- Ареометр — это?
- Как использовать для проверки ареометр?
- Можно ли обойтись без прибора?
- Измерение самодельным устройством
- Проверка плотности в необслуживаемом акб
- Типичные неисправности
- Какой ареометр купить в РФ?
- Заключение
Если у автомобиля неисправный аккумулятор, то ездить на нем не рекомендуется.
Что такое плотность?
Свинцовые батареи включают в себя несколько элементов, одним из которых является электролит. Он представлен в виде серной кислоты, в составе которой присутствует дистиллированная вода. Воду добавляют в электролит из-за того, что концентрированная кислота имеет свойство растворять металлы. Разбавляют ее до такого состояния, чтобы состав не смог разрушить свинец. Плотность кислоты и воды разная — 1,84 г\\Мл и 1 г/мл соответственно.
Электролиз проходит сильнее, если плотность высокая, при этом разрушение свинца проходит еще быстрее. Для аккумуляторов, эксплуатируемых в разных условиях, должна быть своя плотность в диапазоне от 1,25 г/мл и выше. Также электролит можно купить и довести до требуемых значений.
Также электролит можно купить и довести до требуемых значений.
В процессе эксплуатации акб и при постоянном недоразряде на пластинах формируется налет кислоты со свинцом. Иными словами происходит сульфация, которая негативно влияет на работоспособность батареи. Интенсивность электролиза становится низкой. При попытке подзарядить аккумулятор происходит кипение вещества.
Какой должна быть?
С точностью сказать, какой должна быть плотность акб нельзя, поскольку это значение зависит от климата. Если эксплуатация проходит в умеренном климате, то плотность электролита должна соответствовать 1,25-1,27. При работе в холодных регионах это значение должно быть выше на 0,01, а в жаркой местности — ниже на 0,01. Самой высокой должна быть плотность в аккумуляторе в регионах с экстремально низкими температурами (до – 50°С). Каждому автовладельцу стоит знать, что чем ниже плотность в заряженном акб, тем больше он проработает.
Как уже было выяснено, плотность электролита влияет на состояние батареи и на срок ее службы.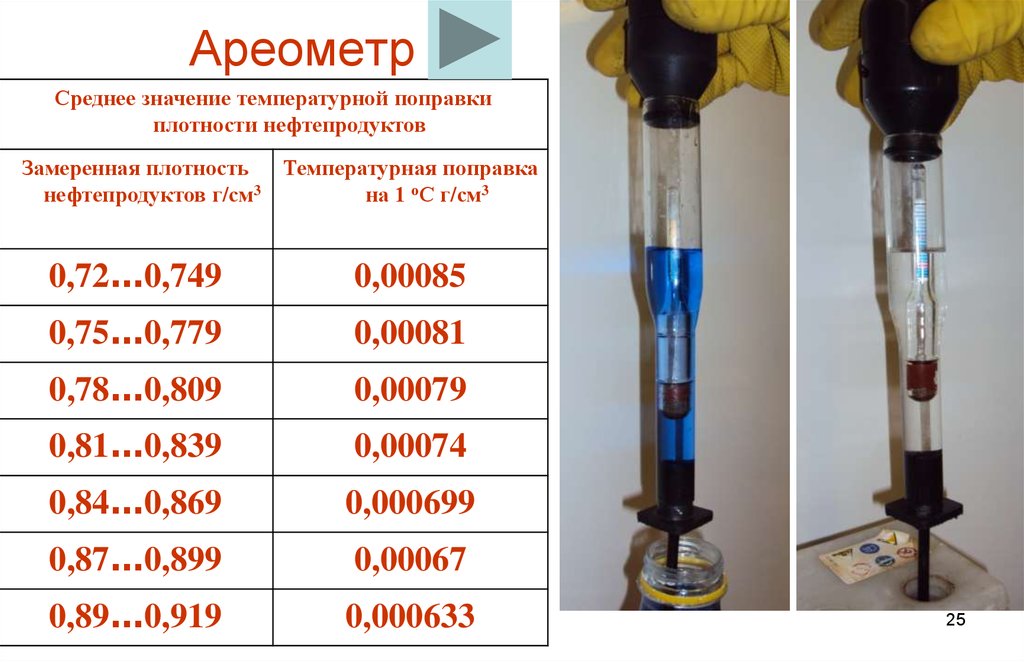 Если автолюбитель имеет обслуживаемую акб, то он может замерить значение с помощью специального прибора. Но поднимать параметры своими руками не стоит, иначе есть риск испортить пластины.
Если автолюбитель имеет обслуживаемую акб, то он может замерить значение с помощью специального прибора. Но поднимать параметры своими руками не стоит, иначе есть риск испортить пластины.
К примеру, многие автолюбители доливают кислоту, не зная, что ее молекулы находятся и в растворе, и на пластинах. После процедуры зарядки молекулы открепляются и восполняют недостаток кислоты в веществе. Если произвести долив, то кислоты станет чрезмерно много, что приведет к разрушению пластин.
Подготовительная работа
Прежде чем произвести измерение плотности электролита в аккумуляторе самостоятельно, необходимо подготовиться.
Водителю нужно знать следующие нюансы работы:
Для работы стоит использовать средства защиты.
Перед измерением следует убедиться, что раствор присутствует. Если его мало, то доливают воду.
Уровень плотности измеряют только после осмотра устройства со всех сторон.
Клеммы стоит очистить от грязевого налета с помощью наждачки, щетки.
Иногда требуется произвести демонтаж акб, отключить клеммы и фиксирующие пластины. Перед выключением акб нужно также деактивировать электроприборы и систему зажигания. Чтобы в банки не попала грязь, аккумулятор очищают тряпкой.
Техника безопасности при проверке
Во время проверки плотности идет работа с кислотой. При несоблюдении техники безопасности водитель может получить кожные ожоги. Чтобы провести процедуру правильно, необходимо следовать рекомендациям:
Работать в специальной одежде, которую не жалко выбросить.
Замеры производятся только в резиновых перчатках.
При приготовлении электролита возможно потребуются защитные очки.
Помещение желательно чтобы было вентилируемое.
Делая замеры, водителю не стоит курить, поскольку кислота взрывоопасна из-за содержания водорода.
Ареометр — это?
Ареометр — прибор, работа которого основывается на законе Архимеда. Иными словами, это устройство помогает исследовать плотность электролита после погружения его в жидкость. Что касается плотности, то она представляет собой удельный вес кислоты и воды по отношению к общему объему.
Что касается плотности, то она представляет собой удельный вес кислоты и воды по отношению к общему объему.
Ареометр различается по видам, водителю потребуется автомобильный вариант. Его конструкция включает в себя трубку, резиновую грушу, пипетку и сам прибор. Пипетка прикреплена к трубке так, чтобы она доставала до пластин. Внутри трубки — ареометр, который также состоит из трубки, на конце которой находится груз. Другой конец трубки превращается в узкую палочку с измерительной шкалой на поверхности. Резиновая груша прикреплена с другого конца корпуса.
Как использовать для проверки ареометр?
Водители, которых интересует, как замерить плотность электролита в аккумуляторе, должны знать некоторые условия для создания правильных измерений. Перед процедурой нужно убедиться, что аккумулятор заряжен полностью, но после подзарядки замерять плотность запрещено. Значения прибора придется корректировать, отталкиваясь от t электролитической жидкости. Самыми правильными параметрами будут те, что были выполнены при t раствора в +27°С.
Инструкция по измерению плотности прибором:
Для начала нужно собрать ареометр, то есть соединить корпус с пипеткой, туда же помещают денсимер и закрывают с обратного конца грушей.
Плотность замеряют в каждой банке. Пипетку устанавливают внутрь и в ареометр набирают кислоту. Для получения информации не потребуется много жидкости.
Показания прочитать можно, если взглянуть на шкалу прибора и место, где она пересекается с поверхностью жидкости.
Главное, разобраться, в каких измерениях на шкале отмечены значения. Бывают приборы с показаниями г/см3 и кг/см3.
Можно ли обойтись без прибора?
Если в наличии ареометра не оказалось, то проверку плотности осуществляют мультиметром. Сначала нужно собрать инструмент, подключив к корпусу провода с крокодилами. Тестер переключают на режим вольтметра, переводя переключатель на 20В. После этого прибор начнет демонстрировать значения ниже этого.
После этого кабеля присоединяют к выходам акб, то есть черный соединяют с отрицательной клеммой, а красный — с положительной.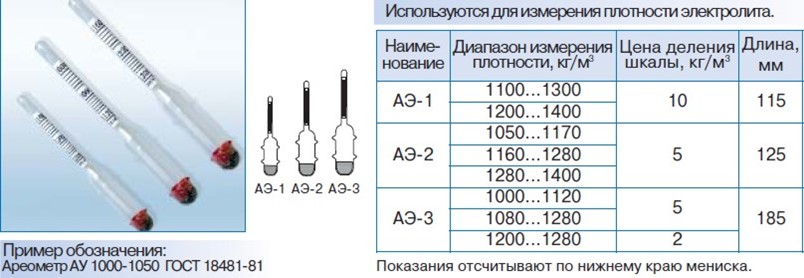 Далее нужно промониторить значения напряжения и сравнить информацию с «нормой». Заряженный аккумулятор покажет 12,7 вольт. Если значения ниже, то это говорит о том, что плотность ненормированная. В этой ситуации нужно дальнейшая диагностика акб или его замена.
Далее нужно промониторить значения напряжения и сравнить информацию с «нормой». Заряженный аккумулятор покажет 12,7 вольт. Если значения ниже, то это говорит о том, что плотность ненормированная. В этой ситуации нужно дальнейшая диагностика акб или его замена.
Измерение самодельным устройством
Если у водителя нет ни ареометра, ни мультиметра, ему стоит соорудить прибор самостоятельно. Главной деталью устройства в обоих случаях является поплавок. Вместо емкости часто используют пробирку. Ее наполняют крупой или сыпучей смесью, а в качестве груза берут свинцовый кусок металла.
Емкость помещают в воду и отмечают «1» место, где возникнет уровень. Цифра означает, что жидкость обладает плотностью 1. Для дальнейшей «разметки» потребуется провести замеры с жидкостью более высокой плотности.
В результате, для проверки плотности электролита в аккумуляторе потребуется провести те же самые действия, что и со специальными приборами.
Проверка плотности в необслуживаемом акб
Необслуживаемый аккумулятор представляет собой батарею, у которой нет пробок для залива растворов. Получается, что автовладелец не имеет возможности заполучить доступ к банкам. Однако существует один способ, как проверить плотность электролита в аккумуляторе, не открывая банки.
Получается, что автовладелец не имеет возможности заполучить доступ к банкам. Однако существует один способ, как проверить плотность электролита в аккумуляторе, не открывая банки.
Для начала водителю нужно открутить глазок индикатора жидкости, находящийся на крышке. Замер осуществляют через отверстие. Но полученные результаты будут соответствовать только одной банке. Из-за конструкции акб повысить плотность не получится никакими способами. Замеры в необслуживаемом аккумуляторе проводятся теми же самыми приборами.
Чаще всего повышение плотности осуществляют через ЗУ (зарядное устройство). Суть процедуры заключается в том, чтобы с помощью подачи минимального тока восстановить плотность электролитической жидкости. АКБ устанавливают на зарядку и ожидают до 3 суток. За это время излишки влаги выпарятся, увеличивая плотность.
Типичные неисправности
Прежде чем проверять значения плотности и повышать (понижать) ее, необходимо изучить типичные неисправности акб.
К ним относят:
Осыпание. Иногда пластины осыпаются. Об этом свидетельствует присутствие на дне хлопьев или кусков свинца. Восстановить устройство не получится. Требуется замена.
Иногда пластины осыпаются. Об этом свидетельствует присутствие на дне хлопьев или кусков свинца. Восстановить устройство не получится. Требуется замена.
Низкая плотность жидкости. При обнаружении низких показателей, необходимо повысить их всеми доступными способами, а затем оценить состояние акб.
Короткое замыкание. Если пластина внутри акб коснется дна, то батарея работать не будет. Обычно это происходит из-за большого количества осадка. Аккумулятор требует замены, поскольку выдать больше 10 вольт без нагрузки не сможет.
Всех этих проблем можно избежать, если правильно эксплуатировать батарею.
Какой ареометр купить в РФ?
Автомобильные ареометры также подразделяются на несколько видов по назначению. К примеру, с их помощью измеряют показатели антифриза. Рассмотрим, какие ареометры предназначены для определения плотности электролита.
Jonnesway AR030001 — тайваньское изобретение с трехцветной шкалой. Прибор устойчив к агрессивной среде, герметичен и имеет небольшой вес. Отличается высокой стоимостью.
Отличается высокой стоимостью.
Heyner PREMIUM 925 010 — качественный прибор с пластиковым корпусом, определяющий плотность при минимальном количестве электролита.
AUTOPROFI АКБ BAT/TST-118 — российская разработка с небольшим весом и простым управлением. На корпусе имеется цветная шкала. Разобраться в использовании сможет даже новичок. Долговечный прибор по мнению большинства пользователей.
JTC 1041 — тайваньское бюджетное устройство, определяющее степень зарядки и плотность электролита.
Вымпел АР-02 5002 — бюджетное российское изобретение. Его главным преимуществом является наличие стеклянной колбы. Способен проработать ни один десяток лет благодаря стеклу, которое не мутнеет.
Эксперты советуют покупать ареометры со стеклянной колбой, которая будет устойчива к органическим соединениям. Пластик также способен выдерживать агрессивную среду, но со временем он тускнеет. Для начинающих водителей понадобится прибор с цветной шкалой, для профессионалов — цифровая.
Заключение
Измерить плотность электролитической жидкости не так сложно, если использовать специальные инструменты. Во избежание получения ожогов, эксперты советуют надевать средства защиты, в том числе очки и перчатки. Если под рукой нет ареометра или мультиметра, то можно смастерить прибор самостоятельно. Однако для частых замеров лучше приобрести прибор отечественного или тайваньского производства. На рынке представлен широкий выбор моделей из разных ценовых категорий.
| Твитнуть |
Как проверить плотность электролита в аккумуляторе или поднять его
Вовсе не редкостью являются ситуации, когда двигатель не хочет заводиться и возникают проблемы с пуском. Довольно часто причина кроется именно в разряженном аккумуляторе. Это становится следствием изменения свойств содержащегося внутри электролита. Её необходимо поднять.
Её необходимо поднять.
Но прежде чем начинать мероприятия по изменению плотности, нужно понять причины, из-за которых такая ситуация возникла. Просто так качество раствора, состоящего из дистиллированной воды и серной кислоты, меняться не будет.
Определившись с причинами, удастся правильно провести ремонтно-восстановительные мероприятия, продлить срок службы АКБ и отложить покупку новой батареи. На практике повлиять на плотность вовсе не так сложно.
Содержание
- Причины снижения плотности
- В чём опасность высокой и низкой плотности
- Правильные показатели плотности
- Как проверить плотность
- Особенности повышения плотности
- Повышение с помощью ЗУ
Причины снижения плотности
Есть несколько факторов, влияющих на показатели плотности у электролита в аккумуляторах.
К ним можно отнести такие моменты:
- Разряд АКБ. Одна из главных причин, почему падает плотность электролита в автомобильном аккумуляторе.
 Параллельно со снижением заряда падают и показатели плотности. Заряжая АКБ, плотность постепенно повышается. Когда происходит потеря большой части ёмкости, это указывает на изменение концентрации состава в сторону уменьшения.
Параллельно со снижением заряда падают и показатели плотности. Заряжая АКБ, плотность постепенно повышается. Когда происходит потеря большой части ёмкости, это указывает на изменение концентрации состава в сторону уменьшения. - Эксплуатация. Со временем батарея изнашивается естественным путём, то есть длительная эксплуатация также влияет на кислоту.
- Хранение. Особенно опасным и вредным считается продолжительное хранение в условиях пониженной температуры.
- Выкипание. Электролит может выкипать при перезаряде. Это может произойти под влиянием зарядного устройства либо из-за неисправного генератора.
- Злоупотребление водой. Чтобы поддерживать уровень электролита, водители часто добавляют воду. Но забывают воспользоваться прибором для проверки плотности. Помимо воды, могут происходить и потери кислоты. Тем самым, добавляя воду, меняется плотность.
Если будет установлена точная причина, из-за которой плотность электролита в вашем аккумуляторе падает, вы сможете без особых сложностей её устранить. Но важно понимать, что не всегда ресурс АКБ зависит от плотности. Случается и так, что без замены батареи никак не обойтись.
Но важно понимать, что не всегда ресурс АКБ зависит от плотности. Случается и так, что без замены батареи никак не обойтись.
В чём опасность высокой и низкой плотности
Не всем автомобилистам известно, на что именно влияет плотность содержащегося в аккумуляторе раствора электролита, а как её изменение может повлиять на АКБ.
В действительности как низкая, так и высокая плотность, наблюдаемая у электролита, может поставить крест на аккумуляторе и привести к необходимости его замены.
Когда концентрация выше допустимой нормы, батарея раньше своего времени выходит из строя. Кислота постепенно начинает разрушать пластины.
В низкой концентрации тоже нет ничего хорошего. При этом протекают такие процессы:
- Сульфатация.
 Это процесс образования на пластинах из свинца белого твёрдого налёта. Из-за него АКБ попросту не может принимать заряд.
Это процесс образования на пластинах из свинца белого твёрдого налёта. Из-за него АКБ попросту не может принимать заряд. - Увеличивается порог замерзания. Если кислоты в составе мало, раствор может начать кристаллизоваться даже при -5 градусах Цельсия. Ледяная корка деформирует внутренние компоненты, может произойти короткое замыкание на пластинах.
- Нарушится пуск двигателя. Это будет проявляться в основном в зимний период.
Как видите, последствия изменения плотности разные, но все они ни к чему хорошему для автовладельца не ведут.
Правильные показатели плотности
Теперь закономерно спросить, какая же плотность тогда должна быть в аккумуляторе автомобиля.
Обычно не предусматривается существенное изменение плотности у электролита в аккумуляторах зимой и летом, ориентируясь только на период холодов.
Существуют специальные таблицы с параметрами плотности электролита в аккумуляторах, в зависимости от климатической зоны. То есть температура окружающей среды непосредственно связана с тем, какая концентрация смеси из кислоты и воды должна быть в АКБ.
Если говорить об эксплуатации аккумулятора под капотом автомобиля зимой, то плотность и его норма должны соответствовать таким значениям:
- При эксплуатации АКБ зимой, при отрицательной температуре, плотность заливаемого электролита должна составлять 1,27 г/см3.
- Если это крайний север с температурой от -30 до -50 градусов, при заливке должно быть 1,27, а при полном заряде АКБ 1,29.
- Для северного региона с температурой от -15 до -30 это 1,26 и 1,28 г/см3 для заливаемого электролита и при полностью заряженной батарее соответственно.
- Когда температура находится в пределах от -4 до -15 градусов, тогда таблица по плотности электролита в автомобильном аккумуляторе подсказывает о поддержании значений на уровне 1,24-1,26.
- Если это южный регион, когда температура редко падает ниже -10 градусов, хватит и 1,22-1,24 г/см3.
- В тропических регионах с положительной температурой даже зимой используют электролиты с плотностью 1,2-1,22 г/см3.
Да, плотность электролита, используемого в аккумуляторе зимой или летом, напрямую зависит от погодных условий.
Несколько корректировать плотность у электролита в автомобильном аккумуляторе летом нужно, если наблюдается сильная жара. Концентрация несколько снижается.
Главным условием поддержания работоспособности АКБ является не плотность электролита, а уровень заряда батареи.
Поэтому старайтесь всегда следить за степенью заряда, параллельно используя ареометр для проверки плотности.
Как проверить плотность
Далее следует рассказать о том, как можно проверить плотность в аккумуляторе и что для этого потребуется использовать.
Проверять плотность можно только в обслуживаемых и малообслуживаемых АКБ, где есть доступ к содержимому батареи.
Ведь закрытые виды батарей, которые считаются необслуживаемыми, не оснащены крышками банок. То есть их не получится открутить и специальным прибором оценить состояние рабочей жидкости.
То есть их не получится открутить и специальным прибором оценить состояние рабочей жидкости.
Если вы не знаете, как проверять параметры плотности электролита в аккумуляторах, ознакомьтесь со следующей инструкцией.
Для работы вам потребуется определённый набор. Состоит он из:
- защитных перчаток;
- закрытой одежды;
- очков;
- денсиметра.
Именно денсиметр позволяет измерить плотность содержащегося в аккумуляторе электролита.
Этот прибор для измерения плотности представляет собой стеклянную трубочку с грушей, а также встроенный ареометр. Фактически именно ареометр способен показать, какая концентрация электролита в вашем аккумуляторе.
Далее остаётся выполнить лишь несколько пошаговых действий.
Предлагаем инструкцию о том, как правильно проверить плотность у обслуживаемого автомобильного аккумулятора:
- Аккумулятор отключается от проводов, снимаются клеммы, устройство извлекается с посадочного места. Защитный кожух следует снять и открутить пробки подручным инструментом.

- Далее проверяется уровень раствора. Обычно он должен быть на 10-15 мм. выше уровня пластин.
- Если АКБ не заряжена, её следует подключить к зарядному устройству. По завершению зарядки нужно подождать около 5-7 часов.
- Если уровень жидкости нормальный, внутрь одной из банок погружается прибор, грушей выкачивается немного раствора.
- Ареометр должен оказаться погружённым в смесь, не касаться стенок колбы.
- Считываются данные на ареометре и записываются.
- Те же самые процедуры проводятся на остальных банках.
- Выполняется сравнение полученной информации с показателями нормы.
Проводить такие работы следует только при положительной температуре. Оптимально добиться диапазона 20-25 градусов Цельсия.
У необслуживаемых АКБ предусмотрен цветовой индикатор, позволяющий понять текущую плотность и состояние батареи.
В основном этот индикатор отражает степень заряда. Зелёный означает полный заряд, белый — около 50%, а чёрный — полную потерю заряда.
Особенности повышения плотности
Приняв во внимание все нюансы, стоит рассказать о том, как поднять плотность при изменении концентрации электролита в аккумуляторе.
Сделать это можно самостоятельно. Ведь чтобы поднять сниженную плотность у электролита, никаких отверстий в аккумуляторе обслуживаемого типа делать не придётся.
Нормой измерения при комнатной температуре считается 1,25-1,29 г/см3. Если показатели ниже, нужно поднимать плотность. Снижение параметров только в одной банке указывает на короткое замыкание.
Есть несколько рекомендаций для того, чтобы повысить плотность упавшего электролита в самом аккумуляторе. Для начала нужно сделать следующее:
- Полностью зарядить АКБ, поскольку проверять плотность при разряде проводить нельзя.
 Добавив электролит, концентрация резко увеличится и начнётся разрушение пластин.
Добавив электролит, концентрация резко увеличится и начнётся разрушение пластин. - Привести температуру жидкости в норму. Работать следует в диапазоне 20-25 градусов Цельсия.
- Убедиться, что уровень в каждой банке соответствует норме.
- Осмотреть АКБ на предмет повреждений и дефектов.
Далее проводится непосредственно сама корректировка параметров плотности с помощью электролита, чтобы в аккумуляторе восстановить рабочие характеристики.
Если уровень слишком низкий и упал ниже 1,18 г/см3, восстановлению такая АКБ уже не подлежит.
Если плотность выше этого порога, её требуется увеличить. Для этого нужно:
- разрядить АКБ, подключив её к какому-нибудь потребителю вроде лампочки;
- подготовить корректирующий электролит, продаваемый в магазинах;
- с помощью груши откачать небольшое количество смеси из каждой банки;
- добавить не более 50% от откаченного объёма новый электролит;
- поставить батарею на зарядку минут на 30, чтобы выровнять концентрацию во всех банках;
- дать постоять АКБ на ЗУ при минимальном зарядном токе;
- отключить батарею.

Примерно через 2-3 часа делается повторная проверка. Если концентрация ещё недостаточная, процедура повторяется.
Повышение с помощью ЗУ
Отдельного внимания заслуживает вопрос о том, как поднять упавшую плотность в своём аккумуляторе, воспользовавшись зарядным устройством.
Суть заключается в том, чтобы восстановить постепенно плотность залитого электролита путём подачи минимального тока. В необслуживаемом автомобильном аккумуляторе доступа к банкам нет. Тут единственным решением будет поставить АКБ на ЗУ и подождать 1-3 суток.
Это позволит постепенно испаряться лишней влаге, и тем самым плотность кислотно-водного раствора будет увеличиваться.
Процедура восстановления электролита не самая сложная, но при её выполнении важно соблюдать ряд рекомендаций.
Центр Аккумуляторных Батарей.
Skip to contentГлавная
Более 15 лет профессиональной работы в сфере продаж, обслуживания и ремонта аккумуляторных батарей и дополнительного оборудования.
Тяговые аккумуляторы
Стартерные аккумуляторы
Стационарные аккумуляторы
Тяговые аккумуляторы
Тяговые аккумуляторы предназначены для снабжения энергией электродвигателей транспортных средств разнообразного назначения, как промышленного и бытового использования, так и применяемых на железной дороге и метрополитене.
Мы предлагаем тяговые аккумуляторные батареи различной ёмкости и напряжения, используемые на погрузчиках, штабелерах, электротележках и другой технике с электродвигателями.
Стартерные аккумуляторы
Стартерные аккумуляторные батареи – предназначены для пуска различных двигателей. Все остальные функции электрификации техники, выполняет генераторная установка.
Наша компания может предложить Вам аккумуляторные батареи различной емкости и для разной техники, а также мы предоставляем услуги по обслуживанию и ремонту стартерных аккумуляторных батарей.
Стационарные аккумуляторы
Стационарный аккумулятор – это свинцово-кислотная аккумуляторная батарея, используемая в качестве источника постоянного тока в установках электропитания аппаратуры связи, промышленного оборудования и систем безопасности.
Наша компания предоставляет широкий выбор стационарных аккумуляторных батарей различных типов, а также полный спектр услуг по восстановлению и ремонту.
Трансформаторные зарядные устройства
Высокочастотные зарядные устройства
Трансформаторные зарядные устройства
Зарядные устройства трансформаторного типа, предназначенные для заряда тяговых аккумуляторных батарей большой ёмкости. Так же поставляются в комплекте с различной погрузочной техникой.
Трансформаторные зарядные устройства громоздки и имеют довольно тяжелый вес, но отличаются своей надежностью и неприхотливостью к условиям работы.
Высокочастотные зарядные устройства
Зарядные устройства без больших трансформаторов, устроенные на микропроцессорных схемах. На некоторых высокочастотных зарядных устройствах, присутствует возможность сменить напряжение, для заряда аккумуляторных батарей другого напряжения.
Благодаря программным модулям, существует множество универсальных зарядных устройств для проведения различных тренировочных зарядов и десульфатации. Наши специалисты помогут Вам подобрать необходимое оборудование.
Запчасти для аккумуляторов
Инструмент и оборудование
Спецодежда
Запчасти для аккумуляторов
В процессе эксплуатации тяговых аккумуляторов, иногда происходят различные поломки, такие как плохой контакт между элементами или сломалась крышка от банки и многое другое.
Мы рады предложить Вам самый большой на сегодняшний день выбор запчастей для аккумуляторных батарей различных типов и конструкций. Наши специалисты помогут подобрать и установить необходимые комплектующие в самые кратчайшие сроки.
Инструмент и оборудование
Всегда в наличии большой выбор инструментов и оборудования для диагностики и обслуживания свинцово-кислотных аккумуляторных батарей.Также, у нас, Вы можете приобрести различное оборудование для аккумуляторных мастерских, такое как: дистилляторы и деионизаторы, ёмкости для хранения электролита и других химических веществ, оборудование для транспортировки аккумуляторных батарей и многое другое.
Спецодежда
Спецодежда для различных специальностей. Кислотостойкая спецодежда, щелочестойкие фартуки и комплекты одежды.
Мы напрямую работаем с производителями различной спецодежды и средств персональной защиты.
Оплывание активной массы, оголение решеток электродов.

Электролит имеет темный цвет. Напряжение батареи при работе стартера быстро снижается.
Замерзание электролита при отрицательных температурах.
Вздутие стенок корпуса или его разрушение.
Взрыв смеси кислорода и водорода (гремучего газа).
Трещины на крышке и стенках аккумулятора или полное разрушение корпуса.
Коррозия решеток положительных электродов.
Быстро снижается напряжения батареи при работе стартера. Батарея плохо заряжается.
Короткое замыкание между электродами.
В дефектной банке плотность ниже, чем в остальных. При заряде дефектная банка не выделяет газ и не «кипит». При работе стартера в банке происходит интенсивное газовыделение.
Короткое замыкание между положительными и отрицательными электродами.

В дефектной банке плотность ниже, чем в остальных, а во время заряда аккумулятор совсем слабо “Кипит“. Обильное газовыделение появляется под нагрузкой.
Недоформованные пластины.
Полностью заряженная батарея не может обеспечить более 2-3 пусков двигателя, а при заряде и разряде интенсивно «кипит».
Разрыв электрической цепи внутри АКБ.
В этом случае, как правило, попытка включения любой нагрузки при обрыве цепи приводит к падению напряжения на выводах батареи до нуля.
Отрыв электродов от соединительных мостиков.
При работе стартера электролит в такой банке “кипит”. При бездействии батареи плотность электролита не снижается.
- Диагностика аккумулятора
- Долив воды
- Очистка корпуса батареи
- Очистка контактов от коррозии
- Протяжка болтов
Обслуживание аккумуляторной батареи – важнейшее действие при эксплуатации различных аккумуляторов. Своевременно проведенное обслуживание, помогает выявить все имеющиеся отклонения и исключить возникновение непредвиденных ситуаций.
Своевременно проведенное обслуживание, помогает выявить все имеющиеся отклонения и исключить возникновение непредвиденных ситуаций.
Наши специалисты предложат меры по немедленному устранению неисправностей, а также озвучат стоимость обслуживания. При предоставлении дополнительных сведений о марке, характеристиках, дате выпуска и состоянии аккумуляторной батареи, наши менеджеры смогут озвучить точную стоимость ремонта или замены со всеми нюансами.
Имя / Название компании *
Email *
Телефон
Напряжениебатареи *
Емкость батареи *
Габаритные размеры *
Имя
Отчество
Фамилия
Comment
Логин / Имя пользователя*
Фамилия
E-mail*
Пароль*
Подтвердить Пароль*
Поля со звездочкой (*) ОБЯЗАТЕЛЬНЫ к заполнению.
Only fill in if you are not human
Мы перезвоним через 5-10 минут!Имя
Фамилия
Message
Ваше имя, а так же, если Вы представитель компании, укажите её название. *
*
Представьтесь пожалуйста.
Укажите Ваш номер телефона и E-mail: *
Имя
Фамилия
Название оборудования: *
Чем больше информации Вы укажете, тем более точно Мы сможем указать стоимость работ.
Описание:
Если оборудование работает неправильно, напишите чем это выражается.
Name
Наш сайт использует файлы cookies, чтобы улучшить работу и повысить эффективность сайта. Продолжая работу с сайтом, вы соглашаетесь с использованием нами cookies и политикой конфиденциальности.
Принять
Какая должна быть плотность электролита в аккумуляторе
Всем привет, дорогие читатели, сегодня расскажу какая должна быть плотность электролита в аккумуляторе. Электролит – основной компонент аккумуляторной батареи, от его плотности зависит накопление и удержание батареей заряда. Низкая концентрация не позволяет АКБ нормально заряжаться, а разрядка наоборот происходит слишком быстро.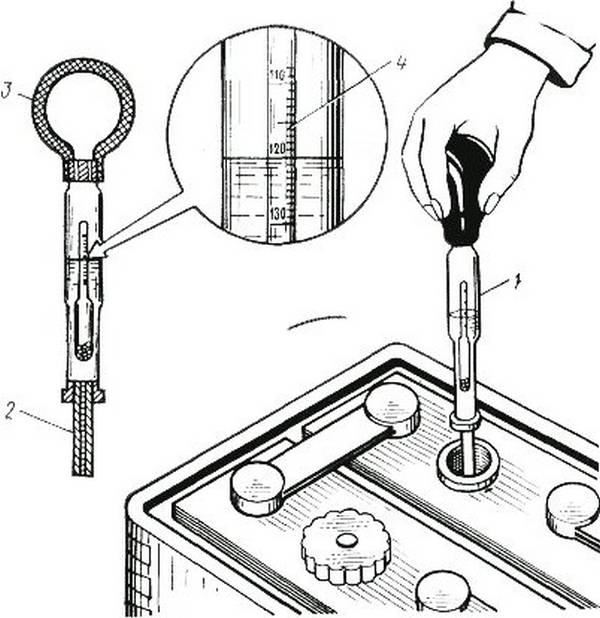 При низкой плотности машина плохо заводится с утра и может не завестись совсем, остановившись где-нибудь в поле. Неприятный момент, не правда ли? Чтобы его избежать, разберемся какая должна быть концентрация и как её повышать.
При низкой плотности машина плохо заводится с утра и может не завестись совсем, остановившись где-нибудь в поле. Неприятный момент, не правда ли? Чтобы его избежать, разберемся какая должна быть концентрация и как её повышать.
Содержание
- Причины и последствия
- К чему приводит безответственность
- Какая нужна плотность
- Повышаем плотность
- Техника безопасности
- Обслуживание батареи
Причины и последствия
Почему падает плотность электролита? Она понижается в результате испарения из секций батареи. Больше всего это происходит при закипании его при перезарядке. Постепенно испаряется электролит и вода естественным путем через дренажные отверстия. Есть такие в крышках банок АКБ, чтобы его не разорвало избытком газа или паров.
О необходимости доливать воду по уровню в обслуживаемых батареях знают многие владельцы машин. Но вот о том, что необходимо доливать и электролит, когда его концентрация низкая, знают далеко не все. Частично кислота выпаривается вместе с водой, частично разлагается, вступая в реакцию с веществом пластин АКБ.
Частично кислота выпаривается вместе с водой, частично разлагается, вступая в реакцию с веществом пластин АКБ.
Разумеется это происходит не быстро, поэтому проверять электролит ежедневно не имеет смысла. А вот ежемесячная проверка, для обслуживаемого аккумулятора будет не лишней.
Тем более что проверка дело быстрое и совсем не трудное. Для проверки нужно лишь снять АКБ. Открутить пробки и проверить ареометром все банки. После этого закрутить пробки обратно, и вернуть батарею на место. Займет не более 10 минут, даже если все делать не спеша.
К чему приводит безответственность
Когда водитель постоянно доливает по уровню лишь воду в батарею, нормальная плотность электролита падает, зимой такой аккумулятор просто разорвет льдом. Воды в нем больше чем кислоты, значит при понижении температуры она перейдет в лед. А лед, как известно расширяется, вот и происходит разрыв корпуса АКБ
Летом такая батарея быстро разряжается, не смотря на исправный генератор и постоянные стационарные подзарядки. С похолоданием, при температуре около нуля машина не заводится. Так как плотность снижается и от снижения температуры. Уровень заряда падает автоматически.
С похолоданием, при температуре около нуля машина не заводится. Так как плотность снижается и от снижения температуры. Уровень заряда падает автоматически.
Какая нужна плотность
Понятие летней и зимней плотности относительное, поддержание нужной концентрации необходимо и зимой и летом. В областях с более холодным климатом — плотность должна быть несколько выше, но все равно в определенных пределах. Поддерживать концентрацию помогает систематическая проверка. Вот график плотности и температур, который поможет вам сориентироваться, нужно ли повышать плотность электролита в вашей батарее.
Из графика видно, что даже при относительно нормальной плотности летом, с наступлением холодов все равно возникнут проблемы. Если электролит в аккумуляторе помутнел или почернел, лучше его заменить полностью, отрегулировав плотность в процессе замены. Как правильно это сделать сейчас расскажу.
Повышаем плотность
Начнем с того, что для этого необходимо:
- Ареометр – прибор для измерения плотности.

- Резиновая груша.
- Мерная колба или стакан.
- Емкость, куда сливать электролит.
- Бутылка с электролитом для аккумуляторов.
- Бутылка дистиллята.
Техника безопасности
Техника безопасности тоже на первом месте, вы же не хотите остаться слепыми? Я точно этого не хочу. Поэтому работайте в плотных резиновых перчатках, для защиты глаз приобретите специальные защитные очки, закрытые со всех сторон.
Если приходится разводить электролит своими руками, тогда помните: сначала в сосуд наливается вода, а потом в воду постепенно доливается кислота. Если сделать наоборот, происходит мгновенный нагрев жидкости и кипение. Сосуд может лопнуть, и тогда точно получите ожоги. А вам ведь это не нужно?
Если полностью менять электролит, нужно слить из АКБ старый раствор. При этом запрещено сильно наклонять или переворачивать корпус АКБ. Это может привести к осыпанию материала пластин и замыканию их. Тогда батарею можно выбросить.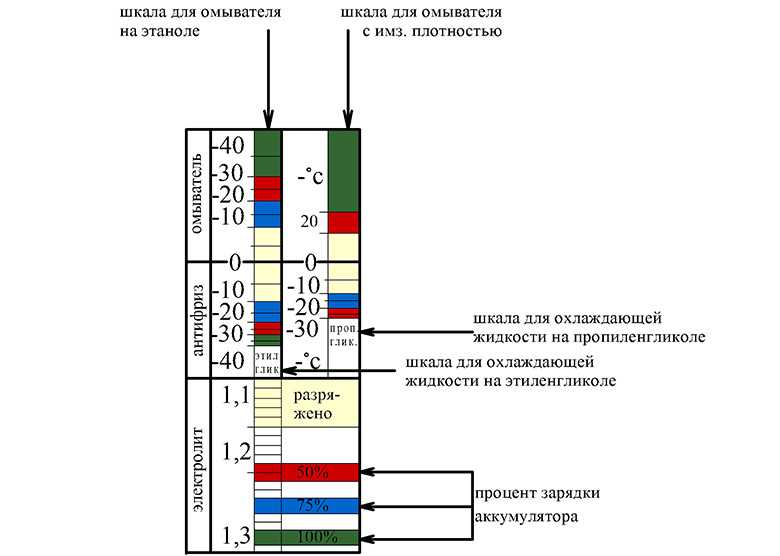
Замеры плотности выполняют при температуре в помещении 20 градусов, или чуть выше. Когда на улице мороз, батарею нужно принести в отапливаемое помещение. Дайте ей постоять и согреться. Учтите, что чем сильнее разряжена батарея, тем ниже её концентрация электролита. Поэтому перед замерами необходимо будет зарядить АКБ на максимум.
Как поднять плотность в не обслуживаемой батарее, я рассматривать не буду, лучше её просто сдать на свинец. Все манипуляции с такой батареей вы будете делать на собственный страх и риск, потому что её конструкция не позволяет выполнять обслуживание. Если вы любите риск и советы «очумельцев», помешать я вам не смогу, однако все же не советую.
Емкость для старого электролита лучше брать стеклянную или резиновую. Выливать его на землю или в водоем запрещено категорически. В канализацию тоже не рекомендуется. Лучше сдать на утилизацию, во избежание неприятностей, чем утилизировать самому, тем более что сейчас это сделать просто. В Интернете множество фирм, которые этим занимаются.
Обслуживание батареи
Процесс повышения плотности объясню на примере кислотной АКБ, как более распространенной. Показатели для щелочного типа будут отличаться, от приведенных мной.
Плотность для электролита приводится в граммах на кубический сантиметр (г/см3). Измеряется она ареометром, поочередно во всех банках. Допустимая плотность 1,25-1,29.Допустимый разброс между измерениями в банках 0,01. Как выровнять в банках уровень плотности? Конечно же не водой.
Когда показатель 1,20 или ниже, тогда нужно повышать концентрацию добавлением электролита. Добавляемый электролит должен быть с плотностью 1,27.
Действуйте следующим образом:
- Сначала, при помощи резиновой груши выкачиваете из одной банки старый электролит, как можно больше, и сливаете в мерный стаканчик, чтобы измерить его количество.
- После этого заливаете в ту же банку новый электролит, только ½ откачанного объема.
- Теперь нужно покачать батарею, не переворачивая, и сильно не наклоняя, чтобы старый электролит перемешался с новым.

- Затем снова замеряете плотность, если её не хватает, доливаете вторую половину откачанного объема.
- Так поступаете поочередно со всеми банками, пока не получите нужную плотность.
- Как увеличить плотность, если показатели ниже 1.18? Рекомендуется доливать уже не электролит, а кислоту аккумуляторную по описанной выше схеме. Пока не получим нужную концентрацию. Превышение плотности не желательно, будут быстрее разлагаться пластины аккумулятора и снижаться его ресурс.
- После достижения нужной концентрации, заряжаете АКБ.
- После зарядки снова измеряете концентрацию и выравниваете по необходимости дистиллятом или электролитом.
В общем, как повысить плотность электролита вы теперь знаете, работа это кропотливая. Зато АКБ потом отлично работает в течение года, а может и дольше, если избегать закипаний и замыканий. Если рассыпались пластины хотя бы одной банки, тогда поможет только замена АКБ.
Спасибо всем, подписывайтесь на обновления и делитесь с друзьями, будет еще много познавательного. До встречи.
До встречи.
Плотность электролита в аккумуляторе
Автомобильная батарея, известная как аккумулятор, отвечает за системы запуска, освещения и зажигания в машине. Как правило, автомобильные аккумуляторы являются свинцово-кислотными, состоят из гальванических элементов, обеспечивающих 12-вольтовую систему. Каждая из ячеек создает 2,1 В при полной зарядке. Плотность электролита – контролируемое свойство водно-кислотного раствора, обеспечивающее нормальную работу батарей.
Состав свинцово-кислотной батареи
Электролит свинцово-кислотной аккумуляторной батареи представляет собой раствор серной кислоты и дистиллированной воды. Удельный вес чистой серной кислоты составляет около 1,84 г/см3, и эту чистую кислоту разбавляют дистиллированной водой до тех пор, пока удельный вес раствора не станет равным 1,2-1,23 г/см3.
Хотя в некоторых случаях плотность электролита в аккумуляторе рекомендуется в зависимости от типа батареи, сезонного и климатического состояния. Удельный вес полностью заряженной батареи по промышленному стандарту в России — 1,25-1,27 г/см3 летом и для суровых зим- 1,27-1,29 г/см3.
Удельный вес полностью заряженной батареи по промышленному стандарту в России — 1,25-1,27 г/см3 летом и для суровых зим- 1,27-1,29 г/см3.
Удельный вес электролита
Одним из основных параметров работы батареи является удельный вес электролита. Это отношение веса раствора (серной кислоты) к весу равного объема воды при определенной температуре. Обычно измеряется с помощью ареометра. Плотность электролита используется в качестве индикатора состояния заряда ячейки или батареи, однако не может характеризовать емкость аккумулятора. Во время разгрузки удельный вес уменьшается линейно.
Учитывая это, нужно уточнить размер допустимой плотности. Электролит в батарее не должен превышать 1,44 г/см3. Плотность может составлять от 1,07 до 1,3 г/см3. Температура смеси при этом будет составлять около +15 С.
Электролит повышенной плотности в чистом виде характеризуется довольно высокой величиной этого показателя. Его плотность составляет 1,6 г/см3.
Степень заряженности
При полностью заряженном стационарном режиме и при разряде измерение удельного веса электролита дает приблизительное указание на состояние заряда ячейки. Удельный вес = напряжение разомкнутой цепи — 0,845.
Пример: 2,13 В — 0,845 = 1,285 г/см3.
Удельный вес уменьшается при разрядке батареи до уровня, близкого к значению чистой воды, и увеличивается во время перезарядки. Аккумулятор считается полностью заряженным, когда плотность электролита в аккумуляторе достигает максимально возможного значения. Удельный вес зависит от температуры и количества электролита в ячейке. Когда электролит находится вблизи нижней отметки, удельный вес выше, чем номинальный, он падает, и воду добавляют в ячейку, чтобы довести электролит до требуемого уровня.
Объем электролита расширяется, когда температура поднимается, и сжимается с понижением температуры, что влияет на плотность или удельное значение силы тяжести. По мере расширения объема электролита показания снижаются и, наоборот, удельный вес увеличивается при более низких температурах.
Перед тем как поднять плотность электролита в аккумуляторе, необходимо выполнить замеры и расчеты. Удельный вес для батареи определяется приложением, в котором он будет использоваться, с учетом рабочей температуры и срока службы батареи.
% Серная кислота | % Вода | Удельный вес (20 ° С) |
37,52 | 62,48 | 1,285 |
48 | 52 | 1,380 |
50 | 50 | 1,400 |
60 | 40 | +1,500 |
68,74 | 31,26 | 1,600 |
70 | 30 | 1,616 |
77,67 | 22,33 | 1,705 |
93 | 7 | 1,835 |
Химическая реакция в аккумуляторах
Как только нагрузка подключается через клеммы аккумулятора, разрядный ток начинает течь через нагрузку, и аккумулятор начинает разряжаться. Во время процесса разрядки кислотность раствора электролита уменьшается и приводит к образованию сульфатных отложений как на положительных, так и на отрицательных пластинах. В этом процессе разряда количество воды в растворе электролита увеличивается, что уменьшает его удельный вес.
Во время процесса разрядки кислотность раствора электролита уменьшается и приводит к образованию сульфатных отложений как на положительных, так и на отрицательных пластинах. В этом процессе разряда количество воды в растворе электролита увеличивается, что уменьшает его удельный вес.
Ячейки аккумуляторной батареи могут быть разряжены до заданного минимального напряжения и удельного веса. Полностью заряженная свинцово-кислотная аккумуляторная батарея имеет напряжение и удельный вес, 2,2 В и 1,250 г/см3 соответственно, и эта ячейка обычно может разряжаться до тех пор, пока соответствующие значения не достигнут 1,8 В и 1,1 г/см3.
Состав электролита
Электролит содержит смесь серной кислоты и дистиллированной воды. Данные не будут точными при замерах, если водитель только что добавил воду. Нужно подождать некоторое время, чтобы свежая вода успела смешаться с существующим раствором. Перед тем как поднять плотность электролита, нужно помнить: чем больше концентрация серной кислоты, тем плотнее становится электролит. Чем выше плотность, тем выше уровень заряда.
Чем выше плотность, тем выше уровень заряда.
Для раствора электролита наилучшим выбором является дистиллированная вода. Это минимизирует возможные загрязнения в растворе. Некоторые загрязняющие вещества могут вызывать реакцию с ионами электролита. Например, если смешивать раствор с солями NaCl, получится осадок, что изменит качество раствора.
Влияние температуры на емкость
Какая плотность электролита — это будет зависеть от температуры внутри батарей. Руководство пользователя для конкретных батарей уточняет, какая коррекция должна применяться. Например, в руководстве Surrette/Rolls для температур в диапазоне от -17,8 до -54,4оC при температуре ниже 21оC, снимается 0,04 для каждых 6 градусов.
Многие инверторы или контроллеры заряда имеют датчик температуры батареи, который прикрепляется к аккумулятору. У них обычно есть ЖК-дисплей. Указание инфракрасного термометра также даст необходимую информацию.
Прибор для измерения плотности
Ареометр плотности электролита используется для измерения удельного веса раствора электролита в каждой ячейке. Кислотная аккумуляторная батарея полностью заряжена с удельным весом 1,255 г/см3 при 26оС. Удельный вес — это измерение жидкости, которая сравнивается с базовой. Это вода, которой присваивается базовое число 1.000 г/см3.
Кислотная аккумуляторная батарея полностью заряжена с удельным весом 1,255 г/см3 при 26оС. Удельный вес — это измерение жидкости, которая сравнивается с базовой. Это вода, которой присваивается базовое число 1.000 г/см3.
Концентрация серной кислоты в воде в новой аккумуляторной батарее составляет 1.280 г/см3, это означает, что электролит весит в 1.280 г/см3 раз больше веса того же объема воды. Полностью заряженная батарея будет тестироваться на уровне до 1.280 г/см3, в то время как разряженная будет учитываться в диапазоне от 1.100 г/см3.
Процедура проверки ареометром
Температура считывания ареометра должна быть скорректирована до температуры 27оC, особенно в отношении плотности электролита зимой. Высококачественные ареометры оснащены внутренним термометром, который будет измерять температуру электролита, и включают шкалу преобразования для коррекции показаний поплавка. Важно признать, что температура значительно отличается от показателей окружающей среды, если автомобиль эксплуатируется. Порядок измерения:
Порядок измерения:
- Несколько раз набрать резиновой грушей электролит в ареометр, чтобы термометр мог отрегулировать температуру электролита и замерить показания.
- Изучить цвет электролита. Коричневая или серая окраска указывает на проблему с батареей и является признаком того, что она приближается к концу своего срока службы.
- Набрать минимальное количество электролита в ареометр, чтобы поплавок свободно плавал без контакта с верхней или нижней частью измерительного цилиндра.
- Удерживать ареометр в вертикальном положении на уровне глаз и обратить внимание на показания, где электролит соответствует шкале на поплавке.
- Добавить или вычесть 0,004 доли единицы для показаний на каждые 6оC, при температуре электролита выше или ниже 27оC.
- Отрегулировать показания, например, если удельный вес 1.250 г/см3, а температура электролита составляет 32оC, значение 1.250 г/см3 дает скорректированное значение 1.
 254 г/см3. Аналогично, если температура составляла 21оC, вычесть значение 1.246 г/см3. Четыре балла (0.004) от 1.250 г/см3.
254 г/см3. Аналогично, если температура составляла 21оC, вычесть значение 1.246 г/см3. Четыре балла (0.004) от 1.250 г/см3. - Протестировать каждую ячейку и отметить показания, скорректированные до 27оC, перед тем как проверить плотность электролита.
Примеры измерения заряда
Пример 1:
- Показания ареометра — 1.333 г/см3.
- Температура 17 градусов, что на 10 градусов ниже рекомендуемого.
- Вычитаем 0,007 с 1,333 г/см3.
- Результат равен 1.263 г/см3, поэтому состояние заряда составляет около 100 процентов.
Пример 2:
- Данные плотности — 1,178 г/см3.
- Температура электролита — 43 градусов С, что на 16 градусов больше нормы.
- Добавляем 0,016 до 1,178 г/см3.
- Результат равен 1,194 г/см3, зарядка 50 процентов.
СОСТОЯНИЕ ЗАРЯДА | УДЕЛЬНЫЙ ВЕС г / см3 |
100% | 1,265 |
75% | 1,225 |
50% | 1,190 |
25% | 1,155 |
0% | 1,120 |
Таблица плотности электролита
Нижеследующая таблица температурной коррекции является одним из способов объяснить резкие изменения значений плотности электролита при различных температурах.
Чтобы использовать эту таблицу, нужно знать температуру электролита. Если измерение по каким-то причинам невозможно, то лучше использовать температуру окружающего воздуха.
Таблица плотности электролита приводится ниже. Это данные в зависимости от температуры:
| % | 100 | 75 | 50 | 25 | 0 |
| -18 | 1,297 | 1,257 | 1,222 | 1,187 | 1,152 |
| -12 | 1,293 | 1,253 | 1,218 | 1,183 | 1,148 |
| -6 | 1,289 | 1,249 | 1,214 | 1,179 | 1,144 |
| -1 | 1,285 | 1,245 | 1,21 | 1,175 | 1,14 |
| 4 | 1,281 | 1,241 | 1,206 | 1,171 | 1,136 |
| 10 | 1,277 | 1,237 | 1,202 | 1,167 | 1,132 |
| 16 | 1,273 | 1,233 | 1,198 | 1,163 | 1,128 |
| 22 | 1,269 | 1,229 | 1,194 | 1,159 | 1,124 |
| 27 | 1,265 | 1,225 | 1,19 | 1,155 | 1,12 |
| 32 | 1,261 | 1,221 | 1,186 | 1,151 | 1,116 |
| 38 | 1,257 | 1,217 | 1,182 | 1,147 | 1,112 |
| 43 | 1,253 | 1,213 | 1,178 | 1,143 | 1,108 |
| 49 | 1,249 | 1,209 | 1,174 | 1,139 | 1,104 |
| 54 | 1,245 | 1,205 | 1,17 | 1,135 | 1,1 |
Как видно из этой таблицы, плотность электролита в аккумуляторе зимой намного выше, чем в теплое время года.
Техническое обслуживание аккумуляторной батареи
Эти батареи содержат серную кислоту. При работе с ними всегда нужно использовать защитные очки и резиновые перчатки.
Если ячейки перегружены, физические свойства сульфата свинца постепенно изменяются, и они разрушаются, из-за чего нарушается процесс зарядки. Следовательно, плотность электролита уменьшается из-за низкой скорости химической реакции.
Качество серной кислоты должно быть высоким. В противном случае батарея может быстро стать неработоспособной. Низкий уровень электролита помогает высушить внутренние пластины устройства, после чего будет невозможно восстановить аккумулятор.
Сульфированные батареи можно легко распознать, просмотрев измененный цвет пластин. Цвет сульфатированной пластины становится светлее, а его поверхность становится желтой. Такие ячейки и демонстрируют снижение мощности. Если сульфирование происходит в течение длительного времени, наступают необратимые процессы.
Чтобы избежать этой ситуации, рекомендуется заряжать свинцово-кислотные аккумуляторные батареи в течение длительного времени при низкой скорости зарядного тока.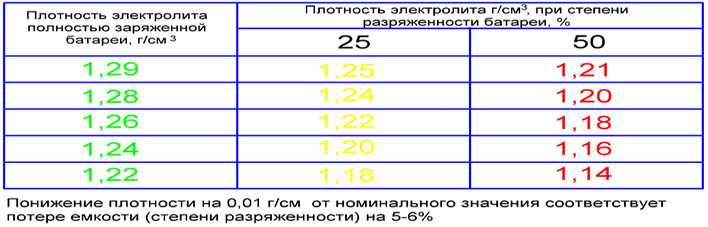
Всегда существует высокая вероятность повреждения клеммных колодок батарейных ячеек. Коррозия в основном поражает болтовые соединение между ячейками. Этого можно легко избежать, если обеспечить герметичность каждого болта с покрытием тонким слоем специальной смазки.
Во время зарядки аккумулятора существует высокая вероятность кислотного распыления и газов. Они могут загрязнять атмосферу вокруг батареи. Следовательно, около батарейного отсека нужна хорошая вентиляция.
Эти газы взрывоопасны, следовательно, открытое пламя не должно попадать внутрь пространства, где заряжаются свинцовые аккумуляторы.
Чтобы предотвратить взрыв батареи, который может привести к серьезным травмам или смерти, нельзя вставлять металлический термометр в аккумулятор. Нужно использовать ареометр со встроенным термометром, который предназначен для тестирования батарей.
Срок службы источника тока
Производительность батареи ухудшается с течением времени, независимо от того, используется она или нет, она также ухудшается при частых циклах заряда-разряда. Срок службы — это время, когда неактивная батарея может быть сохранена до того, как она станет непригодной для применения. Обычно считается, что это около 80% от ее первоначальной емкости.
Срок службы — это время, когда неактивная батарея может быть сохранена до того, как она станет непригодной для применения. Обычно считается, что это около 80% от ее первоначальной емкости.
Существует несколько факторов, которые существенно влияют на срок службы батареи:
- Циклическая жизнь. Время автономной работы определяется в основном циклами использования батареи. Обычно срок службы от 300 до 700 циклов при нормальном использовании.
- Эффект глубины разряда (DOD). Отказ от более высокой производительности приведет к сокращению жизненного цикла.
- Температурный эффект. Это является основным фактором производительности батареи, срока годности, зарядки и контроля напряжения. При более высоких температурах в батарее происходит большая химическая активность, чем при более низких температурах. Для большинства батарей рекомендуется использовать температурный диапазон -17 до 35оС.
- Напряжение и скорость перезарядки. Все свинцово-кислотные батареи выделяют водород из отрицательной пластины и кислород из положительной во время зарядки.
 Аккумулятор может хранить только определенное количество электроэнергии. Как правило, батарея заряжается на 90% за 60% времени. А 10% оставшегося объема батареи заряжается около 40% общего времени.
Аккумулятор может хранить только определенное количество электроэнергии. Как правило, батарея заряжается на 90% за 60% времени. А 10% оставшегося объема батареи заряжается около 40% общего времени.
Хорошее время жизни батарей — от 500 до 1200 циклов. Фактический процесс старения приводит к постепенному снижению емкости. Когда ячейка достигает определенного срока службы, она не перестает работать внезапно, этот процесс растянут во времени, за ним нужно следить, чтобы своевременно подготовиться к замене аккумулятора.
Заметное влияние плотности на динамику неводных электролитов
- Список журналов
- Научные отчеты
- PMC5402255
науч. респ. 2017; 7: 46718.
Опубликовано в сети 24 апреля 2017 г. doi: 10.1038/srep46718
doi: 10.1038/srep46718
Информация об авторе Примечания к статье Информация об авторских правах и лицензии Отказ от ответственности
Подвижность и сольватация ионов лития в электролитах имеют решающее значение для работы и безопасности ионно-литиевых батарей. Известно, что один и тот же растворитель не может одновременно удовлетворять требованиям подвижности и сольватации электролитов. Поэтому для оптимизации обоих свойств использовались сложные смеси растворителей. Здесь мы представляем влияние плотности на динамику и сольватацию органических жидких электролитов с помощью обширного моделирования молекулярной динамики. Наше исследование показывает, что небольшое изменение плотности может оказывать значительное влияние на подвижность электролитов, но не влияет на структуру сольватации иона лития. Оказывается, регулирование плотности электролитов может обеспечить более эффективный способ повышения подвижности, чем регулирование соотношения электролитов в смеси растворителей.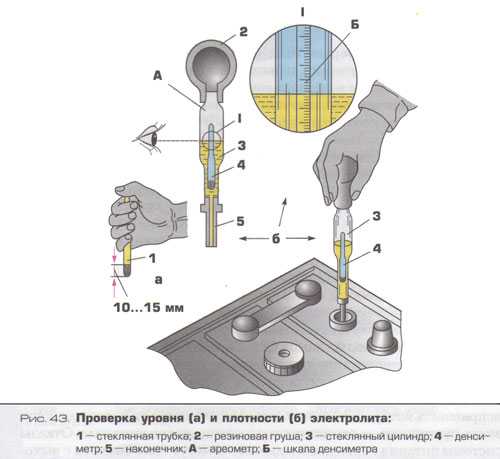 Наше исследование показывает, что изменение плотности электролитов в большей степени влияет на время пребывания растворителей в первой сольватной оболочке иона лития, чем на изменение структуры сольватной оболочки. Наконец, наши результаты предлагают интригующий момент для понимания и разработки электролитов литий-ионных аккумуляторов для повышения производительности и безопасности.
Наше исследование показывает, что изменение плотности электролитов в большей степени влияет на время пребывания растворителей в первой сольватной оболочке иона лития, чем на изменение структуры сольватной оболочки. Наконец, наши результаты предлагают интригующий момент для понимания и разработки электролитов литий-ионных аккумуляторов для повышения производительности и безопасности.
Поскольку в последние годы технологии и рынки портативных электронных устройств и электромобилей быстро растут, перезаряжаемые батареи, такие как ионно-литиевые батареи, стали одной из самых активных областей исследований и промышленных рынков 1 ,2 ,3 ,4 ,5 . Среди компонентов батареи электролиты играют центральную роль в работе и безопасности ионно-литиевых батарей 1 ,2 ,4 ,5 ,6 ,7 ,8 ,9 ,10 . Они позволяют ионам лития проводить между катодом и анодом аккумуляторов и способствуют образованию межфазного слоя твердого электролита (SEI), который является ключевым элементом для защиты электродов от деградации ,10 ,11 ,12 .
Ионная проводимость λ – одно из основных свойств, характеризующих электролиты, количественно характеризующее подвижность ионов для электрохимических реакций 13 . Факторами, определяющими ионную проводимость, являются число ионов n ион , величина заряда Q ион , который несут ионы, и подвижность ионов μ ион , то есть9 0 19 0 1 . Таким образом, для заданных ионов стратегия увеличения ионной проводимости по существу включает улучшение как коэффициента диффузии, так и количества ионов, участвующих в переносе зарядов 14 . В то время как большая диффузия ионов, очевидно, увеличивает ионную проводимость, образование пары катиона и аниона не способствует ионной проводимости из-за ее нейтральности по заряду. Фактически образование пар катионов и анионов тесно связано с уменьшением коэффициента диффузии из-за увеличения размера ионных кластеров в дополнение к уменьшению числа ионов, вносящих вклад в ионную проводимость. Поэтому образование пар в конечном итоге связано с уменьшением ионной проводимости. Чтобы катионы и анионы не образовывали пары и даже кластеры, необходим процесс сольватации катионов растворителями. Принято считать, что растворители в электролитах должны одновременно повышать подвижность ионов и образовывать правильную сольватную оболочку катионов.
Поэтому образование пар в конечном итоге связано с уменьшением ионной проводимости. Чтобы катионы и анионы не образовывали пары и даже кластеры, необходим процесс сольватации катионов растворителями. Принято считать, что растворители в электролитах должны одновременно повышать подвижность ионов и образовывать правильную сольватную оболочку катионов.
Молекула с большой диэлектрической проницаемостью может служить хорошим растворителем с точки зрения ионного спаривания, но легко не повысить подвижность ионов из-за ее большой вязкости. Напротив, молекула с малой диэлектрической проницаемостью имеет меньшую вязкость для повышения подвижности, но ее выполнение в процессе сольватации не выполняется. Таким образом, современные электролиты, применяемые в современных литий-ионных батареях, вместо одного типа растворителя состоят из нескольких типов растворителей, что снижает оба свойства: подвижность и ионное сопряжение 9.0019 1 ,5 ,15 . Например, этиленкарбонат (ЭК) имеет большую диэлектрическую проницаемость ( ε ~ 90 при 40 °C), которая даже выше, чем у воды ( ε ~ 79 при 25 °C). Однако его высокая вязкость ( η ~ 1,9 сП при 40 °С), а также высокая температура плавления ( T m ~ 36,4 °С) не позволяют выбрать его в качестве единственного растворителя. Диметилкарбонат (ДМК) имеет низкую вязкость ( η ~ 0,59 сП при 20 °C), но малая диэлектрическая проницаемость ( ε ~ 3,1 при 25 °C). Таким образом, комбинация циклических и линейных карбонатов, таких как ЭК и ДМК, была предложена в качестве кандидата на роль эффективного электролита, удовлетворяющего двум важным свойствам 1 , 17 , 18 .
Однако его высокая вязкость ( η ~ 1,9 сП при 40 °С), а также высокая температура плавления ( T m ~ 36,4 °С) не позволяют выбрать его в качестве единственного растворителя. Диметилкарбонат (ДМК) имеет низкую вязкость ( η ~ 0,59 сП при 20 °C), но малая диэлектрическая проницаемость ( ε ~ 3,1 при 25 °C). Таким образом, комбинация циклических и линейных карбонатов, таких как ЭК и ДМК, была предложена в качестве кандидата на роль эффективного электролита, удовлетворяющего двум важным свойствам 1 , 17 , 18 .
В этой работе мы исследуем влияние плотности на динамику электролита, состоящего из соли гексафторфосфата лития (LiPF 6 ) в бинарной смеси растворителей ЭК и ДМК с соотношением смеси ЭК:ДМК = 50% :50% (в объемных %). Обратите внимание, что для простоты мы будем обозначать соотношение растворителей и электролитов в смеси только как соотношение EC на протяжении всей этой работы. Для сравнения мы также исследуем динамику для случая EC 20%.
Для сравнения мы также исследуем динамику для случая EC 20%.
Нашей отправной точкой являются две системы электролитов с плотностью ρ = 1,3446 г/см 3 для ЭК 50% и ρ = 1,2677 г/см 3 90% для ЭК, затем исследуем динамика для ЕС 50% в зависимости от ρ . Эти начальные плотности соответствуют суммарным плотностям бинарных смесей ЭК и ДМК с 1 M LiPF 6 , когда две системы имеют одинаковый объем без учета эффекта смешивания ЭК и ДМК. Как правило, общая плотность смешанной системы не следует простой сумме: ρ Всего ≠ ρ Простой = ( ρ EC V EC + ρ DMC V ) . ) . ) . ) . ) . . ) . . ) . ) . ) . ) . ) . ) 9. ( ). V DMC ), но следует учитывать эффект смешивания: ρ всего = ρ простой + ρ 3 4 4 4 3 3 Терм ρ смешанный порождается взаимодействием между ЭК и ДМК, и его трудно ρ смешанный подлежит количественному определению. Если учесть смешение ЭК и ДМК, общая плотность будет отличаться от плотности без него 19 . Например, известно, что экспериментальная плотность объемного электролита для 50% EC с 1 M LiPF 6 в условиях окружающей среды составляет около ρ = 1,30 г/см 3 20 ,20 ,20 900 Далее рассмотрим еще пять плотностей ρ = 1,3219, 1,3028, 1,2852, 1,2709, 1,2568 г/см 3 для системы ЭК 50% для исследования влияния плотности на динамические свойства электролитов. Заметим, что это отличается от многих исследований влияния солей на динамику электролитов, поскольку в нашем исследовании исходная концентрация соли фиксирована, а объем системы изменен.
Если учесть смешение ЭК и ДМК, общая плотность будет отличаться от плотности без него 19 . Например, известно, что экспериментальная плотность объемного электролита для 50% EC с 1 M LiPF 6 в условиях окружающей среды составляет около ρ = 1,30 г/см 3 20 ,20 ,20 900 Далее рассмотрим еще пять плотностей ρ = 1,3219, 1,3028, 1,2852, 1,2709, 1,2568 г/см 3 для системы ЭК 50% для исследования влияния плотности на динамические свойства электролитов. Заметим, что это отличается от многих исследований влияния солей на динамику электролитов, поскольку в нашем исследовании исходная концентрация соли фиксирована, а объем системы изменен.
Динамика
Чтобы изучить влияние плотности ρ на подвижность электролитов, мы сначала рассмотрим константу диффузии D с использованием соотношения Эйнштейна, которое характеризуется среднеквадратичным смещением (СКО), определяемым как 22 ,23
где d — размерность системы, представляющая среднее значение по ансамблю. В вычислим D каждого компонента электролита как функцию ρ для ЭК 50%. Для всех компонентов D очень чувствителен к ρ по сравнению с другими жидкими системами 22 . При ρ уменьшается на Δ ρ = 0,0878 г/см 3 от ρ = 1,3446 г/см 3 до 1,2568 г/см 3 , D иона Li + показывает увеличение в 5,140 и 2,672 раза при Тл = 300 К и 400 К соответственно. Аналогичные возрастания D мы наблюдаем и для других компонентов: 4,554 и 2,715 для иона PF 6 − , 4,007 и 2,661 для EC, 3,959 и 2,853 для DMC при K 4 0= 0 К соответственно. Это означает, что небольшое изменение плотности может оказать большое влияние на диффузионную способность электролитов. Как T увеличивается, влияние ρ на D становится слабее.
В вычислим D каждого компонента электролита как функцию ρ для ЭК 50%. Для всех компонентов D очень чувствителен к ρ по сравнению с другими жидкими системами 22 . При ρ уменьшается на Δ ρ = 0,0878 г/см 3 от ρ = 1,3446 г/см 3 до 1,2568 г/см 3 , D иона Li + показывает увеличение в 5,140 и 2,672 раза при Тл = 300 К и 400 К соответственно. Аналогичные возрастания D мы наблюдаем и для других компонентов: 4,554 и 2,715 для иона PF 6 − , 4,007 и 2,661 для EC, 3,959 и 2,853 для DMC при K 4 0= 0 К соответственно. Это означает, что небольшое изменение плотности может оказать большое влияние на диффузионную способность электролитов. Как T увеличивается, влияние ρ на D становится слабее.
Открыть в отдельном окне
Коэффициент диффузии электролита.
Показаны константы диффузии D каждого компонента электролита, ( a ) a Li + ион, ( b ) a PF 6 — ион 6 EC и ( d ) DMC, как функция плотности ρ при температурах Т = 300 К и 400 К для соотношения смеси растворителей EC 50%. Для сравнения также приводим константу диффузии D каждого компонента электролита при соотношении смеси растворителей EC 20% при плотности ρ = 1,2677 г/см 3 . Результаты показывают, что D демонстрирует существенную зависимость ρ при фиксированном соотношении растворителей в смеси. Как для катиона, так и для аниона D для EC 20% показывает величину, сравнимую с D при ρ = 1,3219 г/см 3 ЭК 50% при обеих температурах Т = 300 К и 400 К. Например, для жидкого ацетонитрила экспериментальное исследование показало, что уменьшение ρ примерно на Δ ρ = 0,1 г/см 3 желательно для увеличения D в два раза при T 98= К 24 . Для воды показано, что уменьшение ρ приблизительно на Δ ρ = 0,2 г/см 3 желательно увеличить D в два раза при T = 300 K 20, 20, 22 Для органических жидких электролитов наши результаты показывают пятикратное увеличение D , когда ρ уменьшается менее чем на 0,1 г/см 3 при T = 300 K. относительно небольшая модификация ρ . Кроме того, D для EC 20% при ρ = 1,2677 г/см 3 показывает сопоставимую величину D для EC 50% при ρ = 1,3219 г/см9 3 Таким образом, наши результаты показывают, что для увеличения D корректировка ρ может быть лучшей стратегией, чем уменьшение доли ЕС. Последний, как известно, является традиционным методом, принятым для увеличения диффузионной способности (или уменьшения вязкости) электролитов. В наших результатах небольшое изменение в ρ , такие как Δ ρ от ρ = 1,3446 г/см 3 до 1,3219 г/см 3 показывает большее увеличение в D LI + Ion, чем изменение EC EC EC.
Для воды показано, что уменьшение ρ приблизительно на Δ ρ = 0,2 г/см 3 желательно увеличить D в два раза при T = 300 K 20, 20, 22 Для органических жидких электролитов наши результаты показывают пятикратное увеличение D , когда ρ уменьшается менее чем на 0,1 г/см 3 при T = 300 K. относительно небольшая модификация ρ . Кроме того, D для EC 20% при ρ = 1,2677 г/см 3 показывает сопоставимую величину D для EC 50% при ρ = 1,3219 г/см9 3 Таким образом, наши результаты показывают, что для увеличения D корректировка ρ может быть лучшей стратегией, чем уменьшение доли ЕС. Последний, как известно, является традиционным методом, принятым для увеличения диффузионной способности (или уменьшения вязкости) электролитов. В наших результатах небольшое изменение в ρ , такие как Δ ρ от ρ = 1,3446 г/см 3 до 1,3219 г/см 3 показывает большее увеличение в D LI + Ion, чем изменение EC EC EC. фракция от 50% до 20%. Эта ситуация аналогична для других компонентов и более высокой температуры. Обратите внимание, что небольшое изменение плотности на самом деле требует большого изменения давления. В нашем случае давление колеблется от менее 1 МПа до нескольких сотен МПа в соответствии с р . Для жидкого ацетонитрила был экспериментально исследован тот же диапазон давлений, и скорость изменения в D в нашем случае намного больше, чем в жидком ацетонитриле 24 .
фракция от 50% до 20%. Эта ситуация аналогична для других компонентов и более высокой температуры. Обратите внимание, что небольшое изменение плотности на самом деле требует большого изменения давления. В нашем случае давление колеблется от менее 1 МПа до нескольких сотен МПа в соответствии с р . Для жидкого ацетонитрила был экспериментально исследован тот же диапазон давлений, и скорость изменения в D в нашем случае намного больше, чем в жидком ацетонитриле 24 .
Чтобы увидеть, как ρ влияет на активационный барьер для диффузии, мы теперь исследуем температурную зависимость D для всех компонентов электролита для трех различных плотностей 19 , как показано на рис. На графике Аррениуса D хорошо вписывается в форму Аррениуса, D = D 0 Exp (- E A / K B T ), где D T ), где D T ), где D 9063 T. ). B – постоянная Больцмана. Мы находим, что абсолютная величина наклона подобранной линии уменьшается при уменьшении ρ . В вычислим энергию активации E a для диффузии по аррениусовской температурной зависимости Д 21 ,25 . Наши результаты показывают, что E A AT ρ = 1,3446 г/см 3 значительно больше, чем E A AT ρ = 1,2563 G/CM68. The ratio γ of E a at ρ = 1.3446 g/cm 3 to E a at ρ = 1.2568 g/cm 3 gives approximately γ = 1,34 для иона Li + , 1,33 для иона PF 6 − , 1,34 для ЭК и 1,37 для ДМК соответственно. По-видимому, E a увеличивается с одинаковой скоростью для всех компонентов электролита по мере увеличения ρ .
). B – постоянная Больцмана. Мы находим, что абсолютная величина наклона подобранной линии уменьшается при уменьшении ρ . В вычислим энергию активации E a для диффузии по аррениусовской температурной зависимости Д 21 ,25 . Наши результаты показывают, что E A AT ρ = 1,3446 г/см 3 значительно больше, чем E A AT ρ = 1,2563 G/CM68. The ratio γ of E a at ρ = 1.3446 g/cm 3 to E a at ρ = 1.2568 g/cm 3 gives approximately γ = 1,34 для иона Li + , 1,33 для иона PF 6 − , 1,34 для ЭК и 1,37 для ДМК соответственно. По-видимому, E a увеличивается с одинаковой скоростью для всех компонентов электролита по мере увеличения ρ . Наши результаты показывают, что уменьшение ρ приводит к значительному уменьшению E a для диффузии. Обратите внимание, что величины E a для всех компонентов показано Li + > PF 6 − > EC > DMC, и это объясняет, почему DMC является самым быстрым компонентом, а ион Li + 1 самым медленным 190,90.
Наши результаты показывают, что уменьшение ρ приводит к значительному уменьшению E a для диффузии. Обратите внимание, что величины E a для всех компонентов показано Li + > PF 6 − > EC > DMC, и это объясняет, почему DMC является самым быстрым компонентом, а ион Li + 1 самым медленным 190,90.
Открыть в отдельном окне
Температурная зависимость констант диффузии.
На графике Аррениуса показаны константы диффузии D каждого компонента электролита, ( a ) иона Li + , ( b ) a PF 6 − ion, ( c ) EC and ( d ) DMC, for EC 50% at three densities of ρ = 1.2568, 1.3028, and 1.3446 g/cm 3 . Все данные хорошо укладываются в форму Аррениуса, . Результаты показывают, что наклон аппроксимации увеличивается по мере увеличения ρ . Сплошные линии — ориентиры для глаз. ( e ) Энергии активации E a для диффузии иона Li + , a PF 6 − ион, EC и DMC как функция плотности ρ для EC 50%, которая рассчитывается по наклону графика Аррениуса. Ясно видно, что E a для всех компонентов электролита уменьшается по мере уменьшения ρ .
Сплошные линии — ориентиры для глаз. ( e ) Энергии активации E a для диффузии иона Li + , a PF 6 − ион, EC и DMC как функция плотности ρ для EC 50%, которая рассчитывается по наклону графика Аррениуса. Ясно видно, что E a для всех компонентов электролита уменьшается по мере уменьшения ρ .
В описании самодиффузии Цванциг интерпретировал диффузию как пересечение энергетического барьера от одного локального минимума энергии к одному из других локальных минимумов энергии в энергетическом ландшафте во всем фазовом пространстве 26 . Энергетический ландшафт системы создается заново в каждый момент обновленными координатами и импульсами систем. С точки зрения энергетического ландшафта уменьшение ρ может уменьшить энергетический барьер между локальными минимумами энергии, так что диффузия может быть усилена. По мере увеличения T влияние ρ будет уменьшаться, поскольку тепловая энергия становится достаточно большой для преодоления барьера.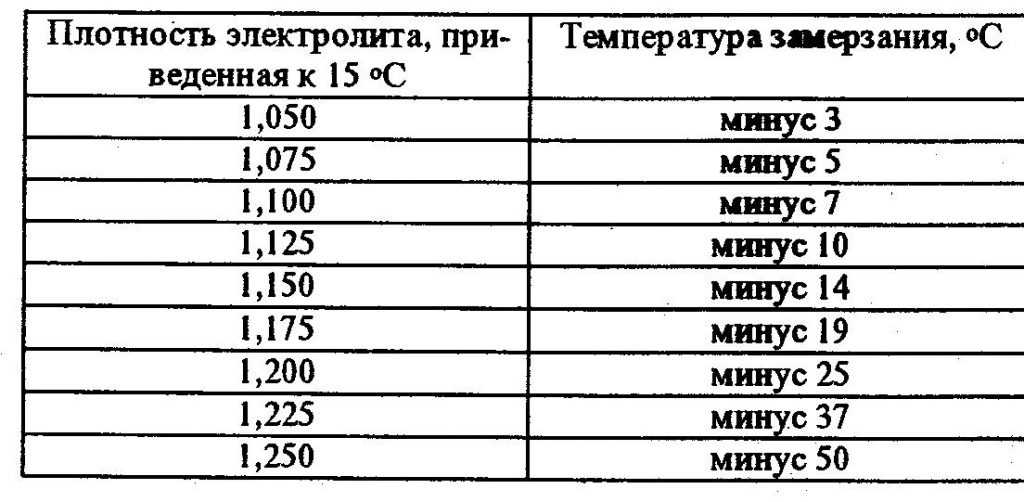 Наши результаты хорошо согласуются с интерпретацией Цванцига о диффузии.
Наши результаты хорошо согласуются с интерпретацией Цванцига о диффузии.
В дополнение к D мы рассчитываем ионную проводимость λ , определяемый как 13 , 17 , 27 , 28
, где Z является зарядкой Ion In Unit of Unit of the элементарный заряд e и представляет собой среднее значение по ансамблю. Суммирование ведется по всем ионам системы. Как показано на , λ для EC 50% существенно возрастает при уменьшении ρ . При ρ снижается до ρ = 1,2568 г/см 3 от 1,3446 г/см 3 , λ увеличивается почти в пять раз, что равно D . В сочетании с результатами D интересно, что λ также проявляет сильную чувствительность к ρ . Мы также обнаружили, что когда ρ становится 1,3028 г/см 3 , λ для EC 50% показывает ту же величину, что и для EC 20%. Из-за конкуренции между подвижностью и ионным спариванием известно, что оптимальная доля растворителя ЭЦ дает максимум за λ находится между 20% и 30% 1 .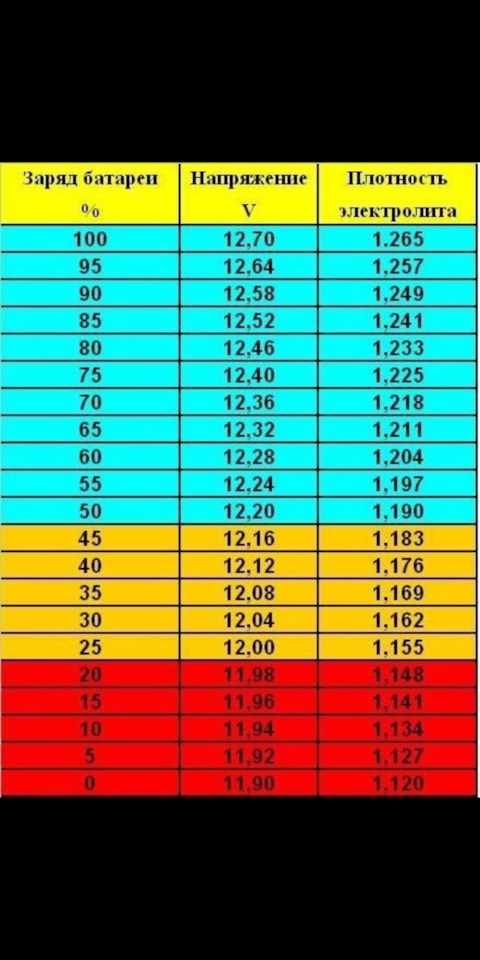 Наши результаты показывают, что существует альтернативный способ увеличения λ без изменения соотношения растворителей и электролитов в смеси. А именно, корректировка ρ оказывает более существенное влияние на D и λ , чем изменение соотношения электролитов в смесях растворителей. Предположительно, быстрый рост D при уменьшении ρ приводит к неожиданной чувствительности λ на ρ .
Наши результаты показывают, что существует альтернативный способ увеличения λ без изменения соотношения растворителей и электролитов в смеси. А именно, корректировка ρ оказывает более существенное влияние на D и λ , чем изменение соотношения электролитов в смесях растворителей. Предположительно, быстрый рост D при уменьшении ρ приводит к неожиданной чувствительности λ на ρ .
Открыть в отдельном окне
Ионная проводимость.
На графике в зависимости от плотности ρ показана ионная проводимость λ при температуре T = 300 K для соотношения растворителей в смеси EC 50%. Для сравнения также приводим λ для EC 20%. Подобно константе диффузии D, λ показывает существенную зависимость ρ. λ для EC 20% аналогично λ при ρ = 1,3219 г/см 3 для ЕС 50%.
Теперь остается вопрос, какие свойства могут быть связаны с чувствительностью D и λ на ρ .
Структура сольватации
Далее мы исследуем влияние плотности на структуру сольватации иона Li + . Мы вычисляем (кумулятивное) координационное число n ( r ), определяемое как 11 ,27 ,29 ,30 ,31 ,32 ,33
где g ( r ) функция радиального распределения (RDF). В , мы демонстрируем n ( r ) как функцию расстояния r от иона Li + для EC 50% и EC 20%. Как показано на рисунке, сольватная структура иона Li + сильно различается в зависимости от соотношения растворителей ЭК и ДМК 8 ,29 ,30 ,34 . Здесь следует отметить, что графики n ( r ) для всех исследованных нами плотностей EC 50% почти перекрываются друг с другом, что свидетельствует о том, что на сольватную структуру иона Li + изменение не влияет. из ρ . В , число сольватации N c в первой сольватной оболочке, определяемое как значение n ( r ) на первом плато в , остается постоянным как ρ варьируется. Количество каждого компонента в первой сольватной оболочке также одинаково для всех исследованных нами плотностей. Небольшое изменение ρ не вызывает реорганизации сольватной структуры иона Li + для данного соотношения растворителей электролитов.
из ρ . В , число сольватации N c в первой сольватной оболочке, определяемое как значение n ( r ) на первом плато в , остается постоянным как ρ варьируется. Количество каждого компонента в первой сольватной оболочке также одинаково для всех исследованных нами плотностей. Небольшое изменение ρ не вызывает реорганизации сольватной структуры иона Li + для данного соотношения растворителей электролитов.
Открыть в отдельном окне
Сольватационная структура иона Li + .
( a ) Совокупные координационные номера n ( r ) ОФ 6 − ион, ЕС и ДМК в зависимости от расстояния r от иона Li + при температуре T = 300 K для соотношения растворителей в смеси EC 50% при плотности ρ = 1,3446 г/см 3 и EC 20% при плотности ρ = 1,2677 г/см 3 .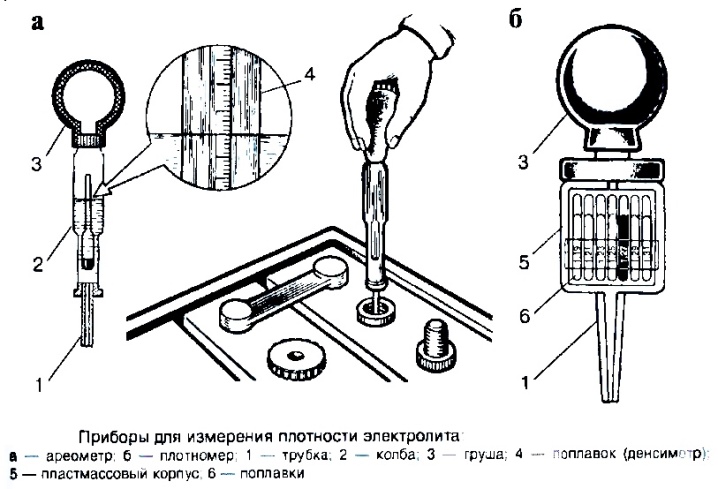 Сплошные и пунктирные линии обозначают случаи ЕС 50% и ЕС 20% соответственно. Обратите внимание, что мы вычисляем n ( r ) из позиций атома P для PF 6 — ион и карбонильный атом кислорода O как для EC, так и для DMC. ( b ) Число сольватации N c в первой сольватной оболочке иона Li + в зависимости от плотности ρ при температуре T 0= 0= символы обозначают случаи ЕС 50% и ЕС 20% соответственно. Далее мы представляем функции плотности вероятности P ( n ) иона Li + , которые представляют собой плотность вероятности для Li + ион иметь n соседей в первой сольватной оболочке для каждого соседа ( c ) общее число, ( d ) a PF 6 − ион, ( e )EC 9024 и ( ф ) ДМС.
Сплошные и пунктирные линии обозначают случаи ЕС 50% и ЕС 20% соответственно. Обратите внимание, что мы вычисляем n ( r ) из позиций атома P для PF 6 — ион и карбонильный атом кислорода O как для EC, так и для DMC. ( b ) Число сольватации N c в первой сольватной оболочке иона Li + в зависимости от плотности ρ при температуре T 0= 0= символы обозначают случаи ЕС 50% и ЕС 20% соответственно. Далее мы представляем функции плотности вероятности P ( n ) иона Li + , которые представляют собой плотность вероятности для Li + ион иметь n соседей в первой сольватной оболочке для каждого соседа ( c ) общее число, ( d ) a PF 6 − ион, ( e )EC 9024 и ( ф ) ДМС.
Далее мы исследуем функцию плотности вероятности P ( n ) для иона Li + иметь n соседей в первой сольватной оболочке. Он описывает, сколько ионов Li + имеют n соседей в сольватной оболочке. С n ( r ) и N c – значения, усредненные по общему числу ионов Li + , подробное описание распределения состава в сольватной оболочке полезно для лучшего понимания структура сольватации. В , мы демонстрируем P ( n ) для соседей общего числа, иона PF 6 − , EC и DMC соответственно. Следует отметить, что P ( n ) показывает одинаковое распределение для всех плотностей ЕС 50%, тогда как оно показывает большую разницу в отношении изменения доли ЕС. Как для EC 50%, так и для EC 20% большая часть Li 9Всего ионы 0019 + имеют 6 соседей в сольватной оболочке. В то время как один или два аниона находятся в первой сольватной оболочке при ЭК 20 %, при ЭК 50 % преобладают ионы Li + без анионов в оболочке. Процент ионов Li + является наибольшим при наличии одного или двух ЭК для ЭК 20% и четырех или пяти ЭК для ЭК 50%.
Он описывает, сколько ионов Li + имеют n соседей в сольватной оболочке. С n ( r ) и N c – значения, усредненные по общему числу ионов Li + , подробное описание распределения состава в сольватной оболочке полезно для лучшего понимания структура сольватации. В , мы демонстрируем P ( n ) для соседей общего числа, иона PF 6 − , EC и DMC соответственно. Следует отметить, что P ( n ) показывает одинаковое распределение для всех плотностей ЕС 50%, тогда как оно показывает большую разницу в отношении изменения доли ЕС. Как для EC 50%, так и для EC 20% большая часть Li 9Всего ионы 0019 + имеют 6 соседей в сольватной оболочке. В то время как один или два аниона находятся в первой сольватной оболочке при ЭК 20 %, при ЭК 50 % преобладают ионы Li + без анионов в оболочке. Процент ионов Li + является наибольшим при наличии одного или двух ЭК для ЭК 20% и четырех или пяти ЭК для ЭК 50%. Для ДМК P ( n ) показывает максимум при двух ДМК для ЕС 20%, тогда как заселенность ионов Li + с одним ДМК составляет большинство для ЕС 50%. Наши результаты показывают, что сольватная структура Li 9Ион 0019 + тесно зависит от соотношения растворителей в смеси, но не зависит от изменения ρ . Таким образом, существенное увеличение D и λ при уменьшении ρ не сопровождается изменением структуры сольватации. Это означает, что можно увеличить подвижность электролитов, регулируя ρ , не нарушая сольватной структуры иона Li + .
Для ДМК P ( n ) показывает максимум при двух ДМК для ЕС 20%, тогда как заселенность ионов Li + с одним ДМК составляет большинство для ЕС 50%. Наши результаты показывают, что сольватная структура Li 9Ион 0019 + тесно зависит от соотношения растворителей в смеси, но не зависит от изменения ρ . Таким образом, существенное увеличение D и λ при уменьшении ρ не сопровождается изменением структуры сольватации. Это означает, что можно увеличить подвижность электролитов, регулируя ρ , не нарушая сольватной структуры иона Li + .
Динамика сольватации
Теперь изучим динамические свойства в первой сольватной оболочке Li + ион. Распределение времени пребывания (RTD) R ( t ) описывает долговечность первой сольватной оболочки иона Li + . Мы определяем время пребывания как время выхода объекта из первой сольватной оболочки иона Li + в первый раз. Отметим, что по результатам n ( r ) в , мы используем определение первой сольватной оболочки иона Li + как окружность с центром в ионе Li + с радиусом 3,0 нм для карбонильный кислород EC и DMC. В представлены РДТ ЭК и ДМК на T = 300 K для различных плотностей EC 50%. На нем отчетливо видно, что RTD затухает быстрее при уменьшении ρ для обоих растворителей. Это означает, что растворители в первой сольватной оболочке легче замещаются другими для более низких ρ . Поскольку структура сольватации не зависит от небольшого изменения ρ , мы предполагаем, что растворитель того же типа заменит ранее существовавший. RTD для EC 50% плотности ниже ρ = 1,3446 г/см 3 распадается быстрее, чем один для EC 20% как для EC, так и для DMC, предполагая, что долговечность сольватной оболочки становится слабее для низких ρ в EC 50%, чем для EC 20%.
Отметим, что по результатам n ( r ) в , мы используем определение первой сольватной оболочки иона Li + как окружность с центром в ионе Li + с радиусом 3,0 нм для карбонильный кислород EC и DMC. В представлены РДТ ЭК и ДМК на T = 300 K для различных плотностей EC 50%. На нем отчетливо видно, что RTD затухает быстрее при уменьшении ρ для обоих растворителей. Это означает, что растворители в первой сольватной оболочке легче замещаются другими для более низких ρ . Поскольку структура сольватации не зависит от небольшого изменения ρ , мы предполагаем, что растворитель того же типа заменит ранее существовавший. RTD для EC 50% плотности ниже ρ = 1,3446 г/см 3 распадается быстрее, чем один для EC 20% как для EC, так и для DMC, предполагая, что долговечность сольватной оболочки становится слабее для низких ρ в EC 50%, чем для EC 20%.
Открыть в отдельном окне
Время пребывания в сольватной оболочке Li + .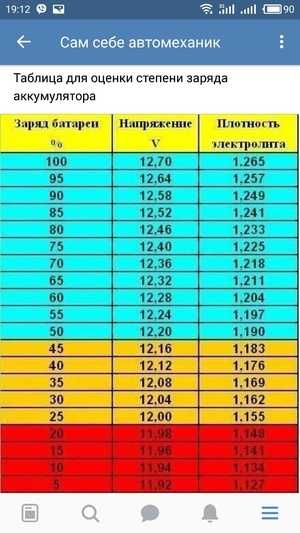
Распределения времени пребывания R ( t ) ( a ) ЭК и ( b ) ДМК в первой сольватной оболочке иона Li + при температуре T = 300 K. Сплошные линии обозначают случаи EC 50% для различных плотностей, а пунктирная линия представляет случай EC 20% при плотности ρ = 1,2677 г/см 3 . Далее приведены характерные времена пребывания τ R ( c ) ЭК и ( d ) ДМК в зависимости от плотности ρ при температурах T = 300 К и 40. Для сравнения. , мы также представляем τ R для EC 20%.
Поведение RTD можно понять по характерному времени пребывания τ R определено 35 AS
при T = 300 К, характерное время пребывания при ρ = 1,3446 г/см 3 для EC 50% — около 44,7 фунтов и 38,4 км для EC. и DMC соответственно, и снижается до 21,5 пс и 17,5 пс при уменьшении плотности до ρ = 1,2568 г/см 3 , как показано на рис. При T = 400 K τ R уменьшается с 15,0 пс и 13,2 пс до 9,7 пс и 8,2 пс для EC и DMC соответственно. Для обеих температур ? для диффузии.
При T = 400 K τ R уменьшается с 15,0 пс и 13,2 пс до 9,7 пс и 8,2 пс для EC и DMC соответственно. Для обеих температур ? для диффузии.
Поскольку РТД описывает быструю кинетику динамики сольватации 35 , мы теперь исследуем медленную кинетику длительности сольватной оболочки иона Li + . Чтобы охарактеризовать динамику сольватации в длительном временном масштабе, мы определяем функцию корреляции местонахождения (RCF) C ( T ) 17 , 35 AS
, где H ( T ) — единство, когда объект находится в пределах первой оболочки сольватации A LI + и H ( t ) в противном случае равен нулю. В то время как RTD представляет собой время непрерывного пребывания, в течение которого растворитель в сольватной оболочке постоянно остается неповрежденным, RCF описывает время прерывистого пребывания с учетом того, что растворитель в сольватной оболочке остается неповрежденным только в момент времени 9.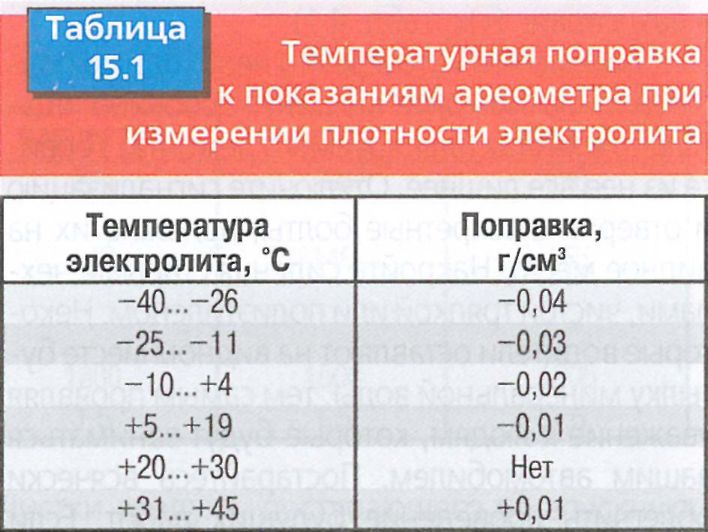 0063 t , учитывая, что он был цел в момент времени t = 0. В , мы представляем RCF EC и DMC при T = 300 K для различных плотностей EC 50%. RCF показывает аналогичное поведение RTD в отношении ρ . Это просто показывает, что RCF затухает быстрее для более низких ρ .
0063 t , учитывая, что он был цел в момент времени t = 0. В , мы представляем RCF EC и DMC при T = 300 K для различных плотностей EC 50%. RCF показывает аналогичное поведение RTD в отношении ρ . Это просто показывает, что RCF затухает быстрее для более низких ρ .
Открыть в отдельном окне
Время корреляции пребывания в сольватной оболочке Li + .
Корреляционные функции места жительства C ( t ) ЭК ( a ) и ( b ) ДМК в первой сольватной оболочке иона Li + при температуре T = 300 K. % для различных плотностей, а линия с кружками представляет случай ЕС 20% при плотности ρ = 1,2677 г/см 3 . Далее показаны характерные времена корреляции пребывания τ C ( c ) EC и ( d ) DMC в зависимости от плотности ρ при температурах T = 300 K и T = 400 K для EC 50%.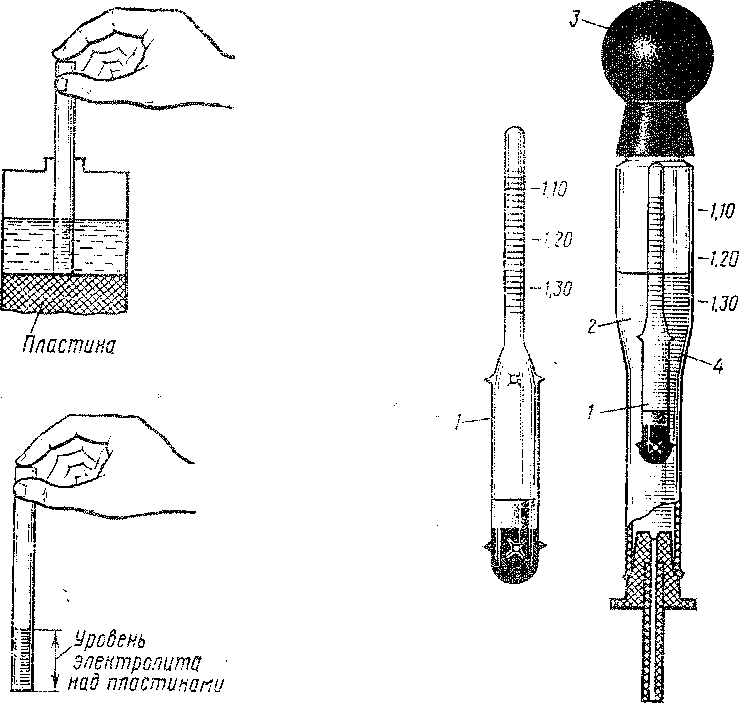 Для сравнения также приводим τ C для EC 20%.
Для сравнения также приводим τ C для EC 20%.
Теперь мы определяем время корреляции местонахождения τ C как время, необходимое для того, чтобы C ( t ) уменьшилось в e 35 раз. При T = 300 K время корреляции пребывания EC колеблется от 3 нс до 10 нс, а для DMC оно колеблется в половине значения τ C ЕС. При T = 300 К, время корреляции жительства EC уменьшается с τ C = 9,3 нс до 3,0 нс при уменьшении плотности с ρ = 1,3446 г/см 3 до 1,2568 ГМ = 1,3446 G/CM 3 до 1,2568 G/C. C/C./C. C/C/C/C. CM до 1,2568 G/CM до 1,2568 = 1,3446 G/CM 3 до 1,2568 G/CM до 1,2568 G/CM до 1,2568 = 1,3446 г/CM до 1.2568 = 1,3446 G/CM . 3 . При повышении температуры до T = 400 K τ C становится меньше 1 ns во всем исследованном нами диапазоне плотностей.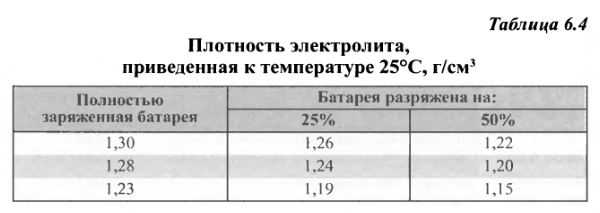 Для DMC поведение τ C по отношению к ρ такие же, как для EC, хотя τ C DMC меньше, чем τ 9006 EC для обеих температур. Уменьшение ? Поскольку медленная кинетика динамики сольватации тесно связана с диффузионной динамикой 35 , это свидетельствует о том, что чувствительность D к ρ связана с прочностью сольватной оболочки.
Для DMC поведение τ C по отношению к ρ такие же, как для EC, хотя τ C DMC меньше, чем τ 9006 EC для обеих температур. Уменьшение ? Поскольку медленная кинетика динамики сольватации тесно связана с диффузионной динамикой 35 , это свидетельствует о том, что чувствительность D к ρ связана с прочностью сольватной оболочки.
Увеличение подвижности электролитов имеет решающее значение для производительности батареи. Традиционным способом повышения подвижности при данной температуре является увеличение доли линейных карбонатов в бинарных растворителях электролитов 17 . Однако увеличение количества линейных растворителей ограничивается ионным связыванием солей, вызывающим снижение ионной проводимости. Поэтому представляет большой интерес найти оптимальное соотношение смесей растворителей, обеспечивающее максимальную ионную проводимость. В этом аспекте наши результаты показывают, что плотность электролитов может оказывать существенное влияние на динамику электролитов. Даже влияние плотности может иногда давать более впечатляющие результаты, чем соотношение смеси растворителей.
Даже влияние плотности может иногда давать более впечатляющие результаты, чем соотношение смеси растворителей.
Наше исследование фундаментальных свойств объемных электролитов показывает, что органические жидкие электролиты, состоящие из ЭЦ и ДМК, обладают большей чувствительностью диффузионной динамики к плотности, чем другие жидкости 22 ,24 ,36 . Хотя небольшое изменение плотности существенно изменяет энергию активации диффузии, оно не вызывает реорганизации сольватной структуры иона Li + . Скорее, уменьшение плотности вызывает более быструю динамику сольватации как в краткосрочном, так и в долгосрочном масштабе. Это указывает на то, что разрушение и восстановление сольватной оболочки Li 9Ионы 0019 + быстро возникают при уменьшении плотности. Уменьшение плотности, то есть увеличение молярного объема, дает больше возможностей для диффузии и больше шансов прервать сольватную оболочку растворителями, находящимися вне оболочки. Связывание растворителей с катионом обычно является одной из основных причин вязкости системы 37 ,38 ,39 . Таким образом, частая реформация сольватной оболочки будет способствовать повышению диффузионной способности. Это объясняет чувствительность коэффициента диффузии к плотности.
Связывание растворителей с катионом обычно является одной из основных причин вязкости системы 37 ,38 ,39 . Таким образом, частая реформация сольватной оболочки будет способствовать повышению диффузионной способности. Это объясняет чувствительность коэффициента диффузии к плотности.
Несмотря на то, что плотность может значительно повлиять на мобильность системы, мы хотели бы отметить, что это не приводит к непосредственному улучшению производительности батареи. Например, число переноса, доля общего тока, переносимого данным видом ионов, является одним из основных свойств, характеризующих эффективность электролитов 40 ,41 . В этом случае число переноса не увеличивается быстро при уменьшении плотности, так как константы диффузии как катионов, так и анионов увеличиваются с одинаковой скоростью. Наши результаты, однако, будут свидетельствовать о том, что плотность может играть роль в повышении мобильности. Наконец, наше фундаментальное исследование объемных электролитов предложит интригующую точку для понимания и разработки электролитов литий-ионных аккумуляторов.
Мы выполнили обширное моделирование молекулярной динамики (МД) неводных электролитов литий-ионных аккумуляторов, состоящих из раствора 1 M соли LiPF 6 в бинарной смеси растворителей EC и DMC. Мы провели все симуляции, используя пакет моделирования MD, LAMMPS 42 . Мы внедрили силовое поле OPLS/AA для описания молекулярного взаимодействия растворителей. Мы рассчитали дальнодействующие взаимодействия, используя алгоритм частица-частица-частица-сетка (PPPM). Моделирование выполняется в NVT ансамбль, где N, V и T — количество молекул, объем и температура соответственно. Линейный размер окна моделирования колеблется от L = 5,2672 нм до 5,3872 нм в зависимости от плотности. Во время моделирования мы поддерживали постоянную температуру с помощью термостата Ноуза-Гувера. Мы применили периодические граничные условия во всех трех направлениях окна моделирования. Мы использовали 1 фс в качестве временного шага моделирования.
Мы исследовали соотношение смеси растворителей EC:DMC = 50%:50% и 20%:80% (в об.%). Если две системы имеют одинаковый объем и не учитывается эффект смешивания двух систем, конечные плотности двух смесей растворителей основаны на индивидуальных плотностях EC и DMC 1 ,5 являются ρ = 1,3446 г/см 3 и 1,2677 г/см 3 (включая LiPF 20% и 0 соли EC соответственно) для 3 Поскольку смешанная плотность бинарных растворителей, используемых в экспериментах, оказывается ниже приведенной выше плотности 21 , мы выбрали еще пять случаев более низких плотностей ρ = 1,2568, 1,2709, 1,2852, 1,3028 и 1,3219 г/см 3 для EC 50%, чтобы исследовать, как плотность влияет на динамику системы, и сравнить с результатами смеси растворителей EC 20%.
Как цитировать эту статью : Han, S. Заметное влияние плотности на динамику неводных электролитов. Науч. Респ.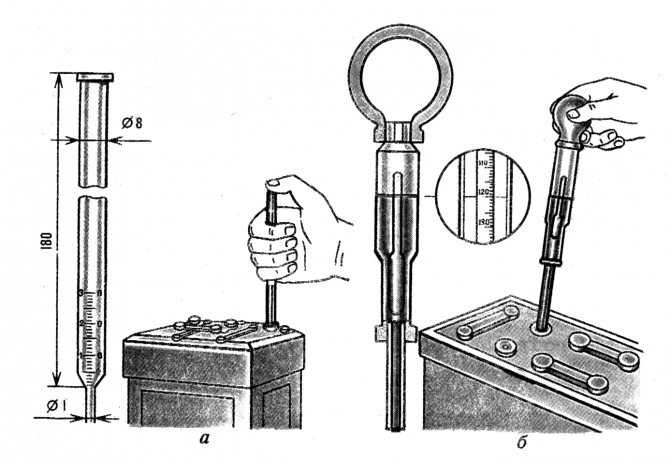 7 , 46718; doi: 10.1038/srep46718 (2017).
7 , 46718; doi: 10.1038/srep46718 (2017).
Примечание издателя: Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Авторы заявляют об отсутствии конкурирующих финансовых интересов.
Вклад авторов С.Х. разработал исследование; проведено моделирование; проанализировал данные и написал статью.
- Сюй К. Неводные жидкие электролиты для литиевых аккумуляторов. хим. преп. 104, 4303–4417 (2004). [PubMed] [Google Scholar]
- Аурбах Д. и другие. Дизайн растворов электролитов для Li и Li-ion аккумуляторов: обзор. Электрохим. Акта 50, 247–254 (2004). [Google Scholar]
- Goodenough J. B. & Kim Y. Проблемы перезаряжаемых литиевых батарей. хим. Матер. 22, 587–603 (2010). [Google Scholar]
- Этачери В.
и другие. Проблемы разработки перспективных литий-ионных аккумуляторов: обзор. Энергетическая среда.
 науч.
4, 3243–3262 (2011). [Академия Google]
науч.
4, 3243–3262 (2011). [Академия Google] - Сюй К. Электролиты и интерфазы в литий-ионных батареях и не только. хим. преп. 114, 11503–11618 (2014). [PubMed] [Google Scholar]
- Сюй К. и другие. Сольватационная оболочка Li + в неводных электролитах и ее влияние на химию интерфейса графит/электролит. Дж. Физ. хим. С 111, 7411–7421 (2007). [Google Scholar]
- Сюй К. Процесс переноса заряда на границе раздела графит/электролит и структура сольватной оболочки Li + в неводных электролитах. Дж. Электрохим. соц. 154, А162–А167 (2007). [Академия Google]
- фон Вальд Креше А., Бородин О. и Сюй К. Корреляция структуры сольватной оболочки Li + с межфазной химией на графите. Дж. Физ. хим. С 116, 26111–26117 (2012). [Google Scholar]
- Богл Х.
и другие. Понимание взаимодействия Li + с растворителем в неводном карбонатном электролите с помощью 17 O ЯМР. Дж. Физ. хим. лат.
4, 1664–1668 (2013).
 [PubMed] [Google Scholar]
[PubMed] [Google Scholar] - Ни М. и другие. Роль структуры раствора в формировании межфазной границы твердого электролита на графите с LiPF 6 в пропиленкарбонате. Дж. Физ. хим. С 117, 25381–25389 (2013). [Google Scholar]
- Йорн Р., Кумар Р., Абрахам Д. П. и Вот Г. А. Атомистическое моделирование границы электрод-электролит в литий-ионных системах накопления энергии: структурирование электролита. Дж. Физ. хим. С 117, 3747–3761 (2013). [Google Scholar]
- Бородин О., Бедров Д. Межфазная структура и динамика компонентов SEI алкилдикарбоната лития в контакте с электролитом литиевой батареи. Дж. Физ. хим. С 118, 18362–18371 (2014). [Академия Google]
- Тенни К. М. и Сайган Р. Т. Анализ молекулярных кластеров при моделировании электролитов литий-ионных аккумуляторов. Дж. Физ. хим. С 117, 24673–24684 (2013). [Google Scholar]
- Сео Д. М.
и другие. Роль смешанной сольватации и ионного спаривания в структуре растворов электролитов литий-ионных аккумуляторов.
 Дж. Физ. хим. С
119, 14038–14046 (2015). [Google Scholar]
Дж. Физ. хим. С
119, 14038–14046 (2015). [Google Scholar] - Мацуда Ю., Накашима Х., Морита М. и Такасу Ю. Поведение некоторых ионов в смешанных органических электролитах аккумуляторов с высокой плотностью энергии. Дж. Электрохим. Соц 128, 2552–2556 (1981). [Google Scholar]
- Soetens J.-C., Millot C., Maigret B. & Bakó I. Молекулярно-динамическое моделирование и рентгеноструктурные исследования этиленкарбоната, пропиленкарбоната и диметилкарбоната в жидкой фазе. Дж. Мол. жидкость 92, 201–216 (2001). [Google Scholar]
- Бородин О., Смит Г. Д. Квантово-химическое и молекулярно-динамическое моделирование диметилкарбоната: этиленкарбонатный электролит, легированный LiPF 6 . Дж. Физ. хим. Б 113, 1763–1776 (2009 г.)). [PubMed] [Google Scholar]
- Масия М., Пробст М. и Рей Р. Этиленкарбонат–Li + : теоретическое исследование структурных и колебательных свойств в газовой и жидкой фазах. Дж. Физ. хим. Б 108, 2016–2027 (2004). [Google Scholar]
- Хаямидзу К.
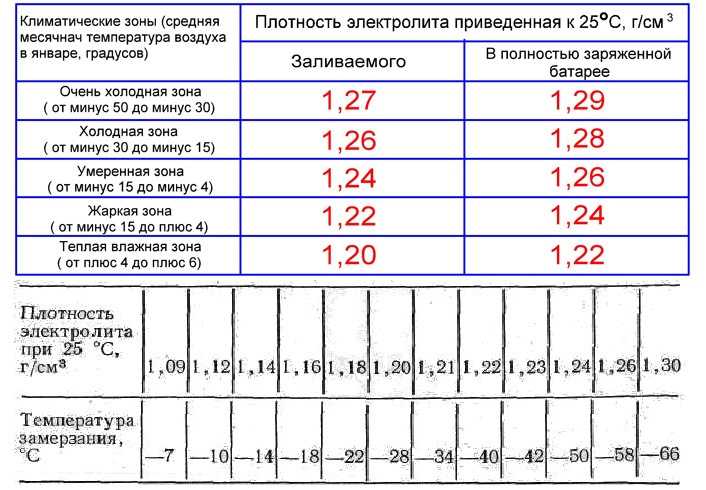 Температурная зависимость коэффициентов самодиффузии ионов и растворителей в одиночных растворах этиленкарбоната, пропиленкарбоната, диэтилкарбоната и бинарных растворах этиленкарбонат + диэтилкарбонат LiPF 6 изучен методом ЯМР. Дж. Хим. англ. Данные
57, 2012–2017 (2012). [Google Scholar]
Температурная зависимость коэффициентов самодиффузии ионов и растворителей в одиночных растворах этиленкарбоната, пропиленкарбоната, диэтилкарбоната и бинарных растворах этиленкарбонат + диэтилкарбонат LiPF 6 изучен методом ЯМР. Дж. Хим. англ. Данные
57, 2012–2017 (2012). [Google Scholar] - Сигма-Олдрич. www.sigmaaldrich.com/catalog/product/aldrich/746711.
- Порион П. и другие. Сравнительное исследование транспортных свойств LiFAP и LiPF 6 в алкилкарбонатах в качестве электролитов посредством измерений проводимости, вязкости и самодиффузии ЯМР. Электрохим. Акта 114, 95–104 (2013). [Google Scholar]
- Хан С., Кумар П. и Стэнли Х. Э. Отсутствие аномалии диффузии воды в направлении, перпендикулярном гидрофобным наноупорным стенкам. физ. Преподобный Е 77, 030201 (2008). [PubMed] [Академия Google]
- Хан С., Чой М. Ю., Кумар П. и Стэнли Х. Э. Фазовые переходы в замкнутых водных нанопленках. Нац. физ. 6, 685–689 (2010). [Google Scholar]
- Hurle R.
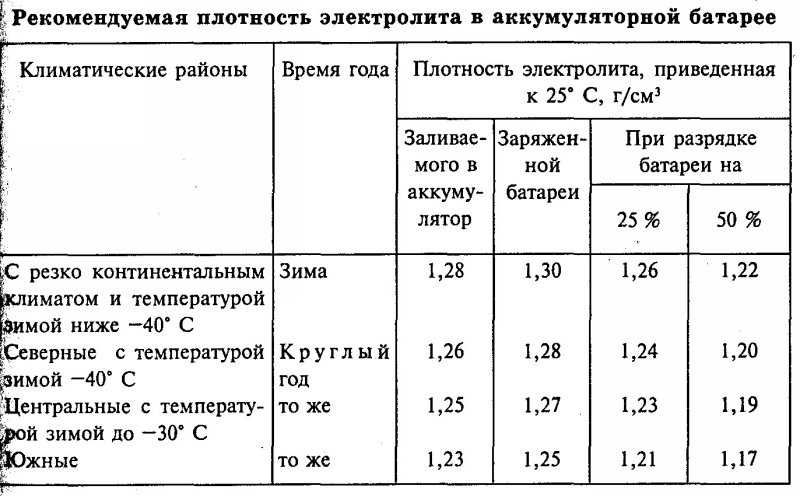 L. & Woolf L. A.
Самодиффузия в жидком ацетонитриле под давлением. Дж. Хим. Soc., Faraday Trans. 1.
78, 2233–2238 (1982). [Google Scholar]
L. & Woolf L. A.
Самодиффузия в жидком ацетонитриле под давлением. Дж. Хим. Soc., Faraday Trans. 1.
78, 2233–2238 (1982). [Google Scholar] - Окубо М. и другие. Определение энергии активации диффузии ионов Li в электродах. Дж. Физ. хим. Б 113, 2840–2847 (2009). [PubMed] [Google Scholar]
- Цванциг Р. О связи между самодиффузией и вязкостью жидкостей. Дж. Хим. физ. 79, 4507–4508 (1983). [Google Scholar]
- Кондо К. и другие. Электропроводность и сольватация ионов Li + LiPF 6 в растворах пропиленкарбоната. Дж. Физ. хим. Б 104, 5040–5044 (2000). [Google Scholar]
- Хаямидзу К., Айхара Ю., Араи С. и Мартинес К.Г. Импульсно-градиентное спиновое эхо 1 H, 7 Li и 19 F Измерения диффузии ЯМР и ионной проводимости 14 органических электролитов, содержащих LiN(SO 2 CF 3 ) 2 . Дж. Физ. хим. Б 103, 519–524 (1999). [PubMed] [Google Scholar]
- Бородин О.
и другие.
 Конкурентная сольватация литием линейных и циклических карбонатов из квантовой химии. физ. хим. хим. физ.
18, 164–175 (2016). [PubMed] [Google Scholar]
Конкурентная сольватация литием линейных и циклических карбонатов из квантовой химии. физ. хим. хим. физ.
18, 164–175 (2016). [PubMed] [Google Scholar] - Скармутсос И., Поннучами В., Ветере В. и Мосса С. Сольватация Li + в чистых, бинарных, тройных смесях органических карбонатных электролитов. Дж. Физ. хим. С 119, 4502–4515 (2015). [Академия Google]
- Джорджини М. Г. и другие. Структура сольватации вокруг иона Li + в смешанных циклических/линейных карбонатных растворах, раскрытая эффектом несовпадения комбинационного рассеяния. Дж. Физ. хим. лат. 6, 3296–3302 (2015). [Google Scholar]
- Камеда Ю. и другие. Структура сольватации Li + в концентрированных растворах LiPF 6 – пропиленкарбонат. Дж. Физ. хим. Б 111, 6104–6109 (2007). [PubMed] [Google Scholar]
- Ян Л., Сяо А. и Лучт Б. Л.
Исследование сольватации электролитов литий-ионных аккумуляторов методом ЯМР-спектроскопии. Дж. Мол. жидкость
154, 131–133 (2010).
 [Академия Google]
[Академия Google] - Ганеш П., Цзян Д. и Кент П. Р. К. Точные статические и динамические свойства жидких электролитов для литий-ионных аккумуляторов из молекулярной динамики ab initio. Дж. Физ. хим. Б 115, 3085–3090 (2011). [PubMed] [Google Scholar]
- Хан С., Кумар П. и Стэнли Х. Э. Динамика водородных связей воды в квазидвумерной гидрофобной щели нанопоры. физ. Преподобный Е 79, 041202 (2009). [PubMed] [Google Scholar]
- Хан С. Аномальное изменение динамики сверхкритического флюида. физ. Преподобный Е 84, 051204 (2011). [PubMed] [Академия Google]
- Поступна О. О., Колесник Ю. В., Калугин О. Н., Преждо О. В. Микроскопическая структура и динамика растворов LiBF 4 в циклических и линейных карбонатах. Дж. Физ. хим. Б 115, 14563–14571 (2011). [PubMed] [Google Scholar]
- Морита М., Асаи Ю., Йошимото Н. и Исикава М.
Спектроскопическое исследование комбинационного рассеяния растворов органических электролитов на основе бинарных систем растворителей этиленкарбоната с растворителями низкой вязкости, растворяющими различные соли лития.
 Дж. Хим. соц. Фарадей Транс.
94, 3451–3456 (1998). [Google Scholar]
Дж. Хим. соц. Фарадей Транс.
94, 3451–3456 (1998). [Google Scholar] - Онг М. Т. и другие. Сольватация и диффузия ионов лития в объемных органических электролитах из первопринципной и классической реактивной молекулярной динамики. Дж. Физ. хим. Б 119, 1535–1545 (2015). [PubMed] [Google Scholar]
- Lu Y. и другие. Стабильное циклирование литий-металлических аккумуляторов с использованием электролитов с высоким числом переноса. Доп. Энергия Матер. 5, 1402073 (2015). [Google Scholar]
- Ма Л. и другие. Высокопроводящие, сульфированные, сшитые под УФ-излучением сепараторы для Li-S аккумуляторов. хим. Мат. 28, 5147–5154 (2016). [Академия Google]
- Плимптон С. Дж. Быстрые параллельные алгоритмы для молекулярной динамики ближнего действия. Дж. Комп. физ. 117, 1–19 (1995). [Google Scholar]
Статьи из Scientific Reports предоставлены с разрешения Nature Publishing Group
Новый электролит поддерживает конструкцию перезаряжаемой батареи
Исследователи преодолевают трудности в разработке магниево-кальциевых батарей с помощью нового принципа конструкции.

ДЛЯ НЕМЕДЛЕННОГО ВЫПУСКА 8 октября 2021 г.
КОНТАКТЫ:
Кэти Холланд
301 405 0379
[email protected]
Аккумуляторные электролиты с использованием хелатообразователей на основе аминов, сольватирующих двухвалентные катионы, продемонстрировали стабильное и хорошо обратимое покрытие/удаление металлического Mg с изображениями сканирующей электронной микроскопии (СЭМ) зацикленного анода Mg, показанного слева, вместе с репрезентативной сольватной оболочкой катиона Mg2+ . Авторы и права: Нина Бородин, Сингюк Хоу, Сяо Цзи для UMD.
Образ выпуска
Энергия, содержащаяся в литий-ионных батареях, может изменить технологию поля боя будущего, создав мировой спрос на ключевые материалы для литий-ионных батарей, такие как литий, кобальт и никель, что создаст проблему с поставками для будущего производства.
Исследователи из Университета Мэриленда (UMD) и Командования по развитию боевых возможностей армии США, известного как DEVCOM, Армейская исследовательская лаборатория, разработали передовой аккумуляторный электролит, который может открыть новые возможности для многообещающих альтернатив, таких как перезаряжаемые магниево-металлические батареи. Подробное исследование этой новой аккумуляторной технологии было опубликовано в Science от 8 октября.
Подробное исследование этой новой аккумуляторной технологии было опубликовано в Science от 8 октября.
«Магния значительно больше, чем лития, что должно удовлетворить потребности постоянно растущего рынка аккумуляторов», — сказал Олег Бородин, армейский химик-вычислитель. «Низкий окислительно-восстановительный потенциал и большая емкость металлического магниевого анода также потенциально могут обеспечить плотность энергии, сравнимую или даже большую, чем у литий-ионных батарей в сочетании с высоковольтными оксидными катодами».
Бородин также пояснил, что по сравнению с литием магний образует меньше дендритов, что эксперты называют основной причиной проблем с безопасностью литий-ионных аккумуляторов.
Несмотря на эти преимущества, батареи из магниевого металла по-прежнему сталкиваются со многими проблемами, которые мешают их развитию. Одна из основных проблем связана с сильной реакцией магния на обычные электролиты во время работы батареи — оба электрода должны быть совместимы с электролитом, чтобы батарея достигла достаточной плотности энергии.
В качестве материала анода магний имеет тенденцию вызывать коррозию электролита и создавать толстое покрытие вокруг анода.
В то время как аналогичные покрытия в литий-ионных батареях обеспечивают диффузию ионов лития и защищают электролит от дальнейшего разложения, это покрытие блокирует магниевое покрытие и предотвращает протекание необходимых электрохимических реакций.
Пытаясь решить эту проблему, исследовательская группа UMD под руководством Чуншэна Вана, профессора химического машиностроения и директора Центра исследований экстремальных аккумуляторов, разработала новую стратегию проектирования, включающую новый класс растворителей.
К их удивлению, конструкция электролита не только предотвратила процесс коррозии, но и значительно увеличила кинетику реакции как анода, так и катода, повысив общую производительность батареи.
«Предыдущие электролиты могли покрывать магний, но у них было много недостатков, — сказал Ван. «Это исследование решило эту проблему с помощью нового электролита, который позволил наносить покрытие из металлического магния, а также использовать катоды с более высоким напряжением. Это первый раз, когда магниевая батарея теоретически достигла такой же плотности энергии, как литий-ионная батарея».
Это первый раз, когда магниевая батарея теоретически достигла такой же плотности энергии, как литий-ионная батарея».
Исследователи также обнаружили, что они могут применить тот же принцип проектирования к другим материалам, подпадающим под категорию двухвалентных металлов, а не только к магнию.
В своем эксперименте новая стратегия дизайна электролита позволила исследователям обойти часто встречающиеся проблемы как для перезаряжаемых батарей из магниевого металла, так и для перезаряжаемых батарей из кальциевого металла.
«Испытание с кальцием показывает, что эта конструкция электролита может быть распространена на другие типы мультивалентных батарей с низким потенциалом и расширяет выбор электродных материалов в целом», — сказал Сингюк Хоу, аспирант UMD и соавтор исследования. . «Люди особенно интересуются кальцием, потому что потенциал кальциевого анода даже ниже, чем у магниевого, а кальция в земной коре очень много».
Армейские исследователи в основном поддержали исследование с помощью расчетов теории функционала плотности (DFT), которые помогли команде понять, почему новый электролит привел к этим улучшениям, и направить поиск новых электролитов.
«Армия помогла нам понять механизм того, что именно произошло», — сказал Ван. «У нас есть знания об этом явлении, но предоставленные ими расчеты сыграли важную роль в демонстрации этой технологии и того, что мы должны сделать дальше, чтобы улучшить ее».
По словам Вана, команда планирует оптимизировать электролит, а затем преобразовать концепцию в крупномасштабный силовой элемент.
Бородин объяснил, что эта новая стратегия проектирования может означать настоящий прорыв для двухвалентных металлических батарей после двух десятилетий исследований, сопряженных с проблемами, связанными с недостаточной плотностью энергии, вызванной несовместимостью электрод-электролит. Это продвижение может изменить то, как армия в будущем снабжает энергией солдат на поле боя.
Перейдите по этой ссылке, чтобы подготовить исследование по науке.
О Инженерной школе им. А. Джеймса Кларка
Инженерная школа им. А. Джеймса Кларка Университета Мэриленда — ведущая программа, входящая в число 20 лучших в мире. Школа Кларка, расположенная всего в нескольких милях от Вашингтона, округ Колумбия, находится в центре созвездия высокотехнологичных компаний и федеральных лабораторий, предлагая студентам и преподавателям доступ к уникальным профессиональным возможностям.
Школа Кларка, расположенная всего в нескольких милях от Вашингтона, округ Колумбия, находится в центре созвездия высокотехнологичных компаний и федеральных лабораторий, предлагая студентам и преподавателям доступ к уникальным профессиональным возможностям.
Наш широкий спектр академических программ, включая единственную в мире аккредитованную программу бакалавриата по инженерной противопожарной защите, дополняется динамичной предпринимательской экосистемой, ранним практическим образовательным опытом и участием в национальных и международных конкурсах.
Школа Кларка занимается исследованиями в области аэрокосмической техники, биоинженерии, робототехники, нанотехнологий, устойчивости к стихийным бедствиям, энергетики и устойчивого развития, а также кибербезопасности. От универсального кода продукта до спутникового радио, SMS-сообщений и имплантируемой инсулиновой помпы — наши студенты, преподаватели и выпускники разрабатывают инновации, которые меняют жизни миллионов людей. Узнайте больше на www.eng.umd.edu.
Узнайте больше на www.eng.umd.edu.
Почему важна плотность энергии в батареях?
Плотность энергии батареи – это количество энергии, содержащейся в батарее, по сравнению с ее весом или размером. Мы называем это удельной плотностью энергии при сравнении с весом и объемной плотностью энергии при сравнении размеров.
Например, мы измеряем энергию батареи в ватт-часах (ватт в час, эквивалент использования одного ватта в течение одного часа). Затем мы можем разделить ватт-часы батареи (wh) на ее килограммы (вес) или объем (литры).
Таким образом, время, в течение которого аккумулятор может питать устройство по сравнению с его весом или размером, равно плотности энергии.
Почему важна плотность энергии батареи?
Плотность энергии батареи имеет решающее значение, поскольку чем выше плотность энергии, тем дольше батарея может излучать заряд по отношению к ее размеру. При этом батареи с высокой плотностью энергии могут быть полезны, когда для батареи не так много места, но вам нужно много выходной энергии. Смартфоны и другие портативные устройства являются прекрасными примерами этого.
Смартфоны и другие портативные устройства являются прекрасными примерами этого.
Давайте сформулируем преимущества плотности энергии в виде вопроса: что бы вы предпочли: небольшую и легкую батарею, которая излучает энергию в течение длительного времени, или тяжелую батарею, которая занимает много места и обеспечивает лишь небольшое количество энергии?
Почти все сказали бы, что первое. Вот почему высокая плотность энергии жизненно важна в нашем мире.
Плотность энергии в сравнении с плотностью мощности в батареях
Плотность энергии и плотность мощности легко спутать, потому что они в некотором роде похожи. Оба они измеряют электрические характеристики батареи по сравнению с ее весом.
Тем не менее, плотность энергии и плотность мощности различаются по одному важному признаку: в то время как плотность энергии батареи измеряется в ваттах часов (ватт-час) на килограмм (кг), плотность мощности измеряется в ваттах на выходе на килограмм.
Вот где сила против энергии вступает в игру. Плотность мощности измеряет, насколько быстро может быть доставлена энергия, а плотность энергии измеряет, сколько энергии удерживает батарея.
Каковы преимущества использования аккумуляторов с высокой плотностью энергии?
Аккумуляторы с высокой плотностью энергии изменили мобильный мир. Обладая большей энергией, мы можем разместить полезные батареи в небольших помещениях. Это позволяет использовать долговечные телефоны, ноутбуки, наушники или медицинские устройства.
Они также очень легкие по сравнению с прошлыми альтернативами. Могли бы вы представить, что носите с собой 5-фунтовый iPhone? Или 10-фунтовая таблетка?
Более высокая плотность энергии также означает, что мы можем упаковать много энергии в более крупные мобильные устройства, такие как автомобили, самолеты, строительное оборудование и роботы.
Каковы риски высокой плотности энергии?
Когда батарея накапливает больше энергии, она может высвободить больше энергии, если что-то пойдет не так.
Жидкие электролиты, содержащиеся в литий-ионных батареях, очень летучи и могут привести к возгоранию, что представляет опасность возгорания. Из-за этого в эти батареи встроены функции безопасности, которые ограничивают их легкий вес и компактность.
Следовательно, чем выше плотность энергии батареи, тем более опасной она может быть, что накладывает ограничения (и риски) на дальнейшее продвижение.
Какой аккумулятор в настоящее время имеет самую высокую плотность энергии?
Несомненно, литий-ионные аккумуляторы лидируют, когда речь идет о высокой плотности энергии. Они изменили наш мир благодаря достижениям в области энергопотребления и портативности. На самом деле плотность энергии литий-ионных аккумуляторов колеблется в пределах 260-270 Втч/кг, а свинцово-кислотных — в пределах 50-100 Втч/кг.
За последнее десятилетие в литий-ионных батареях было сделано много достижений, в частности, связанных с их химическим составом. Используя различные материалы для анода и катода, инженеры могут экспериментировать с электрохимией и изменять плотность энергии, плотность мощности и многое другое.
Литий-ионный аккумулятор с самой высокой плотностью энергии — это литий-кобальт-оксидный аккумулятор. В качестве катода используется оксид кобальта, а в качестве анода — графит. Из-за высокой плотности энергии он популярен для смартфонов, ноутбуков, часов, автомобилей и любых компактных устройств, которым необходимо излучать энергию в течение длительного времени.
→ Рекомендуемая литература: Анод и катод: в чем разница?
Преодолевая ограничения: твердотельные батареи
Итак, если мы достигаем пределов в развитии литий-ионных аккумуляторов, куда нам двигаться дальше? Будущее аккумуляторных технологий за твердотельными батареями.
Помните, что литий-ионные аккумуляторы имеют жидкий раствор электролита? Жидкое состояние этого раствора является фундаментальной проблемой. Он нестабилен, летуч при воздействии кислорода и может представлять значительный риск для безопасности. Это также ограничивает прогресс в размерах и плотности энергии из-за этих соображений безопасности.
Твердотельные батареи устраняют эти проблемы. Электролит в этих батареях является твердым, а не жидким, и поэтому имеет более высокую плотность энергии (в 2,5 раза больше), чем современные литий-ионные батареи. Они также имеют более быстрое время зарядки и меньше проблем с безопасностью, что делает батареи меньше и компактнее.
Хотя твердотельные батареи еще не доступны, они могут снова изменить наш мир.
Вот почему это важно
Плотность энергии аккумулятора имеет решающее значение, когда речь идет о его размере, продолжительности работы устройства и даже о безопасности аккумулятора. Фактически, это была ведущая тема совершенствования аккумуляторов и причина, по которой литий-ионные аккумуляторы так популярны.
Химики и инженеры постоянно стремятся создать безопасные, долговечные батареи с высокой плотностью энергии, и мы можем найти это идеальное решение в области химии твердотельных батарей. Будущее созрело для новых инноваций в литиевых батареях. Здесь, в Dragonfly Energy, мы совершаем революцию не только в достижениях в области твердотельных батарей, но и в производственном процессе.
Здесь, в Dragonfly Energy, мы совершаем революцию не только в достижениях в области твердотельных батарей, но и в производственном процессе.
У вас есть вопросы о плотности энергии и будущем батарей? Оставьте их в комментариях ниже!
Роль концентрации в растворах электролитов для неводных аккумуляторов на основе лития
Основные компоненты и, что особенно важно, концентрация неводного раствора электролита существенно не изменились с момента коммерциализации литий-ионных аккумуляторов в начало 1990-х. Однако поиски электрохимических систем накопления энергии с высоким содержанием энергии заставили исследователей пересмотреть пригодность «стандартной» одномолярной концентрации и обратить внимание на высококонцентрированные растворы электролитов. Однако взаимосвязь между фундаментальными свойствами электролита и характеристиками элемента не согласуется с тем, что можно было бы ожидать, основываясь только на ионной проводимости электролита. Здесь обсуждаются недавний прогресс и будущие перспективы корреляции между физико-химическими свойствами нестандартных растворов электролитов и их способностью улучшать характеристики накопления энергии в батареях на основе лития.
Основной
С момента коммерциализации Sony в 1991 году 1 многочисленные достижения в области неводных литий-ионных аккумуляторов привели к появлению множества продуктов 1,2 . Усилия по увеличению плотности энергии и удельной энергии привели к десятилетиям интенсивных исследований по улучшению электродных активных материалов. Следовательно, разработка электродных активных материалов намного опередила достижения в области химии электролитов. Состав раствора электролита, несмотря на его критическую роль в клетке как ионного проводника для переноса ионов лития между электродами, сегодня в основном такой же, как и в начале 19 века.90-е 1,2 . «Стандартный» состав электролита содержит смесь линейных и циклических карбонатных растворителей в виде 1-молярного (М) раствора соли, где солью обычно является гексафторфосфат лития (LiPF 6 ). Затем этот «стандартный» электролит приспосабливается к конкретному химическому составу элемента, прежде всего, путем изменения карбонатного растворителя и включения запатентованных смесей добавок 3 . Эти добавки, которые могут включать растворители, соли или другие молекулы, которые не считаются растворителями, обычно используются в небольших количествах по сравнению с количеством растворителя электролита (в обзоре Сюй произвольно установлено 10%, без указания массы). % или объемных %; кроме того, количества выше 10% считаются сорастворителями) 4 . Совсем недавно Solchenbach et al. предположил, что отношение добавки к активному материалу может иметь большее значение, чем конкретная концентрация 5 . Однако идеальное количество любой конкретной добавки, вероятно, зависит от ее функции в клетке и от количества, необходимого для получения желаемого эффекта без значительного негативного влияния на другие свойства, влияющие на производительность. Добавки выполняют множество функций в ячейке, например, в качестве пленкообразователей (т. е. расходуемых добавок) для образования межфазного слоя твердого электролита (SEI), межфазного слоя катод-электрод (CEI) или соединений для повышения безопасности системы (например, антипирены).
Эти добавки, которые могут включать растворители, соли или другие молекулы, которые не считаются растворителями, обычно используются в небольших количествах по сравнению с количеством растворителя электролита (в обзоре Сюй произвольно установлено 10%, без указания массы). % или объемных %; кроме того, количества выше 10% считаются сорастворителями) 4 . Совсем недавно Solchenbach et al. предположил, что отношение добавки к активному материалу может иметь большее значение, чем конкретная концентрация 5 . Однако идеальное количество любой конкретной добавки, вероятно, зависит от ее функции в клетке и от количества, необходимого для получения желаемого эффекта без значительного негативного влияния на другие свойства, влияющие на производительность. Добавки выполняют множество функций в ячейке, например, в качестве пленкообразователей (т. е. расходуемых добавок) для образования межфазного слоя твердого электролита (SEI), межфазного слоя катод-электрод (CEI) или соединений для повышения безопасности системы (например, антипирены). 3 . Например, количество добавки CEI, вероятно, будет ниже, чтобы избежать увеличения межфазного сопротивления, чем, например, количество антипирена, где требуется более высокое содержание, чтобы повлиять на время самозатухания.
3 . Например, количество добавки CEI, вероятно, будет ниже, чтобы избежать увеличения межфазного сопротивления, чем, например, количество антипирена, где требуется более высокое содержание, чтобы повлиять на время самозатухания.
Что касается основных компонентов раствора электролита, остается довольно большое игровое поле, которое только начали исследовать в последние годы (рис. 1). Например, концепция электролитов, не содержащих этиленкарбоната (ЭК), была исследована для улучшения работы при высоком напряжении 6 . Аспект концентрации соли является особенно интересным аспектом для изучения. Изменение концентрации напрямую влияет на сольватацию ионов Li + в растворе, а затем и на все остальные свойства электролита, в том числе на образование интерфаз (SEI и CEI). В этой статье с комментариями основное внимание будет уделено высококонцентрированным растворам электролитов (также известным как системы растворителей в соли 7 ) и рассмотрены аспекты, касающиеся будущей разработки электролитов и их применения в батареях на основе лития.
В середине рисунка описан стандартный раствор электролита для литий-ионных аккумуляторов. Этот стандартный электролит можно изменить (зеленое кольцо) не только путем изменения состава (например, растворителей или солевого аниона), но и путем изменения концентрации. Изменения в составе влияют на свойства электролита (синее кольцо), которые впоследствии влияют на работу элемента (оранжевое кольцо).
Полноразмерное изображение
Соответствующие транспортные свойства литий-иона необходимы для удовлетворительной гарантии характеристик электрохимического накопления энергии. Здравый смысл (т. е. понимание и объяснение свойств электролита, общепринятое специалистами в области растворов аккумуляторных электролитов) гласит, что это достигается за счет высокой электропроводности и малой вязкости электролита. В большинстве неводных растворов проводящих электролитов с ионами лития максимальная объемная проводимость достигается при концентрации соли примерно 1 М. Поэтому не случайно, что «стандартная» концентрация электролита составляет 1 М. Бородин и соавт. назвали это «наследием 1 моляра (M)» 8 . Эта максимальная проводимость является результатом компромисса между количеством носителей заряда и ионной подвижностью этих носителей заряда. Количество носителей заряда определяется диссоциацией соли, а ионная подвижность в первую очередь связана с вязкостью электролитной среды. В режиме концентрации 1 M ионы лития сольватируются «обычно используемыми» карбонатными растворителями, а анионы в основном считаются «свободными» (часто называемые ионными парами, разделенными растворителем, или SSIP) 9 . Строение сольватной оболочки, т. е. ионов лития и непосредственно координированных компонентов электролита, зависит как от природы растворителя, так и от солевого аниона. Кроме того, имеется значительное количество некоординированного растворителя, т. е. молекул растворителя за пределами первой сольватной оболочки. При высоких концентрациях соли (определение «высокой концентрации» обсуждается в следующем абзаце) координация ионов лития сильно отличается.
Поэтому не случайно, что «стандартная» концентрация электролита составляет 1 М. Бородин и соавт. назвали это «наследием 1 моляра (M)» 8 . Эта максимальная проводимость является результатом компромисса между количеством носителей заряда и ионной подвижностью этих носителей заряда. Количество носителей заряда определяется диссоциацией соли, а ионная подвижность в первую очередь связана с вязкостью электролитной среды. В режиме концентрации 1 M ионы лития сольватируются «обычно используемыми» карбонатными растворителями, а анионы в основном считаются «свободными» (часто называемые ионными парами, разделенными растворителем, или SSIP) 9 . Строение сольватной оболочки, т. е. ионов лития и непосредственно координированных компонентов электролита, зависит как от природы растворителя, так и от солевого аниона. Кроме того, имеется значительное количество некоординированного растворителя, т. е. молекул растворителя за пределами первой сольватной оболочки. При высоких концентрациях соли (определение «высокой концентрации» обсуждается в следующем абзаце) координация ионов лития сильно отличается. Ионы лития координируются как анионами, так и молекулами растворителя. Более того, свободных молекул растворителя, которые влияют не только на транспортные свойства электролита, но и на взаимодействие между электролитом и другими компонентами в ячейке, например, при образовании SEI/CEI, немного, если они вообще есть.
Ионы лития координируются как анионами, так и молекулами растворителя. Более того, свободных молекул растворителя, которые влияют не только на транспортные свойства электролита, но и на взаимодействие между электролитом и другими компонентами в ячейке, например, при образовании SEI/CEI, немного, если они вообще есть.
Сравнение растворов электролитов «1 M» и «высокой концентрации солей» приводит к вопросу, что такое «высокая концентрация»? К сожалению, на этот вопрос нет однозначного ответа, поскольку границы между различными режимами концентрации неводных растворов аккумуляторных электролитов сильно зависят от критериев определения. С точки зрения идеальности, из которой были выведены почти все классические уравнения, описывающие поведение электролита, все ионы в растворе должны быть полностью диссоциированы, участвовать в диффузии и миграции и двигаться независимо (т. е. не подвергаться влиянию других ионов). ионы) 10 . Однако растворы аккумуляторных электролитов отклоняются от идеальности уже при концентрациях ниже 0,1 M 11 ; таким образом, даже «стандартные» 1 М растворы электролитов можно считать концентрированными электролитами. Поэтому практическое определение «концентрированного электролита» существенно отличается от идеального определения, основанного на независимом движении ионов. В возможной попытке примирить эти различия в литературе появился термин «суперконцентрированный», который слабо ассоциируется с концентрациями выше примерно 3 M в апротонных растворителях 9.0019 8 .
Поэтому практическое определение «концентрированного электролита» существенно отличается от идеального определения, основанного на независимом движении ионов. В возможной попытке примирить эти различия в литературе появился термин «суперконцентрированный», который слабо ассоциируется с концентрациями выше примерно 3 M в апротонных растворителях 9.0019 8 .
Недавно было высказано предположение, что один из способов классификации практических электролитов (т. е. электролитов, используемых в технологически важных электрохимических накопителях энергии) по режимам концентрации может основываться на природе ионно-сольватной оболочки 8,10 . Как отмечалось выше, в высококонцентрированных электролитах (или «сверхконцентрированных» электролитах) свободных молекул растворителя мало, если они вообще есть, а анионы присутствуют в первой сольватной оболочке. Напротив, в электролитах с «низкой концентрацией» (т.е. менее 3 M на основе определения молярности, указанного выше) есть молекулы растворителя, которые не координируются напрямую с катионами в растворе и, таким образом, являются свободными.
Приведенные выше концентрации даны в молярных единицах (т. е. количество молей растворенного вещества на литр раствора), как это часто используется в литературе. Однако молярность не обязательно является наилучшей мерой концентрации для высококонцентрированных растворов электролитов, поскольку плотность значительно изменяется с концентрацией. Например, электролиты, содержащие бис(фторсульфонил)имид лития (LiFSI) в ЭК, увеличили плотность с 1,38 г см -3 при 0,63 М до 1,71 г см -3 при 5,67 М 12 . Следовательно, лучше подходят другие единицы для выражения концентрации, такие как моляльность (т.е. моли растворенного вещества на 1 кг растворителя) или молярное отношение (моли растворенного вещества:моли растворителя), особенно при сравнении электролитов в широком диапазоне концентраций.
В дополнение к общепринятому мнению, упомянутому выше, можно ожидать худших характеристик элемента при использовании электролитов с высокой концентрацией, когда объемная проводимость ниже, а вязкость увеличивается. Это предположение в значительной степени вытекает из картины при более низких концентрациях, когда транспортный механизм транспорта (т. е. когда ионы лития движутся через электролит с его сольватной оболочкой) вносит существенный вклад в проводимость ионов лития 8 . В этом случае «более низкая концентрация» зависит от растворителя и может считаться примерно до 3 М для карбонатов 8 . Изучение результатов исследований высококонцентрированных растворов электролитов приводит к вопросам относительно этого общепринятого мнения и, следовательно, полезности проводимости (объемного) электролита в качестве ключевого критерия оценки. Возможны ли другие транспортные механизмы, такие как структурная диффузия, при которой литий-ион транспортируется за счет обмена компонентами в первой сольватной оболочке (т.е. процессы ассоциации-диссоциации ионов) 8 , также эффективно транспортирует «достаточное количество» лития к электроду? Может ли высокая концентрация ионов лития свести к минимуму влияние градиентов концентрации в электролите? Основываясь на этих двух вопросах, необходимо ли изменение парадигмы в общепринятом понимании связи между транспортными свойствами и производительностью клетки? Кроме того, можно ли изменить электрохимическую стабильность отдельных компонентов электролита за счет координации и как координация влияет на образование межфазных границ? Эти вопросы рассматриваются в следующих разделах наряду с другими аспектами, важными для будущей разработки, оптимизации и внедрения высококонцентрированных электролитов в батареях на основе лития.
Это предположение в значительной степени вытекает из картины при более низких концентрациях, когда транспортный механизм транспорта (т. е. когда ионы лития движутся через электролит с его сольватной оболочкой) вносит существенный вклад в проводимость ионов лития 8 . В этом случае «более низкая концентрация» зависит от растворителя и может считаться примерно до 3 М для карбонатов 8 . Изучение результатов исследований высококонцентрированных растворов электролитов приводит к вопросам относительно этого общепринятого мнения и, следовательно, полезности проводимости (объемного) электролита в качестве ключевого критерия оценки. Возможны ли другие транспортные механизмы, такие как структурная диффузия, при которой литий-ион транспортируется за счет обмена компонентами в первой сольватной оболочке (т.е. процессы ассоциации-диссоциации ионов) 8 , также эффективно транспортирует «достаточное количество» лития к электроду? Может ли высокая концентрация ионов лития свести к минимуму влияние градиентов концентрации в электролите? Основываясь на этих двух вопросах, необходимо ли изменение парадигмы в общепринятом понимании связи между транспортными свойствами и производительностью клетки? Кроме того, можно ли изменить электрохимическую стабильность отдельных компонентов электролита за счет координации и как координация влияет на образование межфазных границ? Эти вопросы рассматриваются в следующих разделах наряду с другими аспектами, важными для будущей разработки, оптимизации и внедрения высококонцентрированных электролитов в батареях на основе лития.
Сравнение объемной проводимости или переноса лития как ключевого транспортного свойства
Объемная электролитная проводимость (собственная ионная проводимость материала, на которую не влияют какие-либо границы раздела, например, из-за заключения в пористой структуре) часто используется как ключевое транспортное свойство для оценки электролитов перед тестированием элементов. Ионная проводимость — это параметр, который можно относительно легко и надежно измерить с помощью стандартного оборудования, доступного в большинстве электрохимических лабораторий. Тем не менее, существуют определенные ограничения; в частности, высокая объемная электропроводность электролита не обязательно означает высокую электропроводность литий-иона 13 .
Вклад переноса ионов лития в общий ток известен как число переноса лития. Концепция числа переноса не уникальна для растворов жидких ионно-литиевых электролитов. Это общая концепция для описания вклада конкретных видов x в общую (т. е. объемную) проводимость (передаточное число x , T x , со значениями от 0 до 1) 14 . В «стандартных» электролитных системах это значение обычно низкое (между 0,2 и 0,4) 15 , что означает, что «свободные» анионы более подвижны, чем ионы лития с сольватной оболочкой растворителя. Таким образом, анионы, например PF 6 − «стандартный» электролит, как определено выше, вносят больший вклад в общий ток. Литий-ионная проводимость σ Li + в конкретном электролите может быть определена из произведения объемной электропроводности электролита σ и T Li + (т. е. σ Li + = σ ∙ T Li + ). В конечном счете, именно литий-ионная проводимость ограничивает плотность тока, которая может быть достигнута с данным электролитом в гальваническом элементе 10 .
е. объемную) проводимость (передаточное число x , T x , со значениями от 0 до 1) 14 . В «стандартных» электролитных системах это значение обычно низкое (между 0,2 и 0,4) 15 , что означает, что «свободные» анионы более подвижны, чем ионы лития с сольватной оболочкой растворителя. Таким образом, анионы, например PF 6 − «стандартный» электролит, как определено выше, вносят больший вклад в общий ток. Литий-ионная проводимость σ Li + в конкретном электролите может быть определена из произведения объемной электропроводности электролита σ и T Li + (т. е. σ Li + = σ ∙ T Li + ). В конечном счете, именно литий-ионная проводимость ограничивает плотность тока, которая может быть достигнута с данным электролитом в гальваническом элементе 10 .
Научные исследования с высококонцентрированными электролитами показали, что растворы электролитов с более низкой объемной проводимостью могут иметь улучшенные электрохимические характеристики накопления энергии по сравнению с их аналогами с более низкой концентрацией 12,16 . Этот изначально противоречащий здравому смыслу результат означает, что электролит с более низкой объемной проводимостью должен иметь более высокую литий-ионную проводимость, что может быть только в случае более высоких T Li + (т. е. если σ Li + [высокий] > σ Li + [низкий], как указано в характеристиках ячейки, и σ[высокий] < σ[низкий], то T Li + [высокий] > T Li + [низкий]). Когда значения T Li + приводились в рецензируемых отчетах, они были выше в высококонцентрированных электролитах, чем в более разбавленных «стандартных» растворах электролитов (например, T Li + 9).0020 = 0,42 для 1 M LiPF 6 в EC/DMC (3:7 по объему) по сравнению с T Li + = 0,58 для 4M LiTFSI + 0,5 10090M LiDFOB во фторэтиленовом карбонате Li + = 0,32 для 1M LiPF 6 в EC/DMC (1:2 по объему) по сравнению с T Li + = 0,57 для [LiFSI]:[ацетонитрилкарбонат]:[ацетонитрил] = 0,52:1:0,09 17 ).
Этот изначально противоречащий здравому смыслу результат означает, что электролит с более низкой объемной проводимостью должен иметь более высокую литий-ионную проводимость, что может быть только в случае более высоких T Li + (т. е. если σ Li + [высокий] > σ Li + [низкий], как указано в характеристиках ячейки, и σ[высокий] < σ[низкий], то T Li + [высокий] > T Li + [низкий]). Когда значения T Li + приводились в рецензируемых отчетах, они были выше в высококонцентрированных электролитах, чем в более разбавленных «стандартных» растворах электролитов (например, T Li + 9).0020 = 0,42 для 1 M LiPF 6 в EC/DMC (3:7 по объему) по сравнению с T Li + = 0,58 для 4M LiTFSI + 0,5 10090M LiDFOB во фторэтиленовом карбонате Li + = 0,32 для 1M LiPF 6 в EC/DMC (1:2 по объему) по сравнению с T Li + = 0,57 для [LiFSI]:[ацетонитрилкарбонат]:[ацетонитрил] = 0,52:1:0,09 17 ).
Более высокая проводимость ионов лития приводит к более высокой доступности ионов лития на электроде из-за образования более низкого градиента концентрации в электролите. В недавнем исследовании с использованием рамановской спектроскопии in situ изучалось количество ионов лития в электролите в фиксированном положении в ячейке после подачи тока. 17 Результаты показали значительное истощение ионов лития в «стандартном» растворе карбонатного электролита. Однако высококонцентрированный раствор электролита (т. е. 10 M) формировал значительно более низкий градиент концентрации. Дальнейшее исследование показало, что, хотя вязкость и ионная проводимость являются хорошими показателями производительности литий-ионных элементов с низкой массовой нагрузкой (например, 0,95 мАч см -2 ) и тонкими электродами (например, 22 мкм), электролиты с более высокой концентрацией (например, , 1,9M) может уменьшить истощение ионов лития в порах толстых электродов (например, массовая нагрузка 8,10 мАч см −2 и толщина 161 мкм) для улучшения характеристик электрохимического накопления энергии 18 . Важно отметить, что ионная проводимость объемного раствора электролита обычно выше, чем у электролита, заключенного в пористой структуре электродов или сепаратора 13 .
Важно отметить, что ионная проводимость объемного раствора электролита обычно выше, чем у электролита, заключенного в пористой структуре электродов или сепаратора 13 .
Было бы полезно использовать литий-ионную проводимость, полученную из числа переноса, в качестве ключевого параметра переноса для прогнозирования поведения растворов электролитов. Однако существуют значительные проблемы, связанные с точным измерением числа переноса. О значительных вариациях сообщает исх. 19в результатах, полученных электрохимическими методами (например, методом Брюса-Винсента) и в результатах, полученных из градиента импульсного поля ЯМР 19 . Каждый метод имеет определенные ограничения/допущения, которые необходимо учитывать. Таким образом, числа переноса вряд ли будут полезны в качестве универсального инструмента скрининга. Тем не менее, концепция переноса и его влияние на градиент концентрации ионов лития в аккумуляторной ячейке должны учитываться в исследовательских работах, посвященных электролитам.
Влияние вязкости
Высокая концентрация соли в растворе электролита достигается за счет высокой вязкости, которая значительно снижает подвижность ионов. Как отмечалось выше, количества растворителя при высоких концентрациях уже недостаточно для полного заполнения первой сольватной оболочки. Следовательно, анионы участвуют в координации ионов лития. Недостаточное количество растворителя также может привести к сценарию, при котором анионы координируются с более чем одним ионом лития, образуя то, что часто называют «агрегатами» 9.0019 8 . Образование агрегатов наряду с координацией анионов эффективно увеличивает ионный радиус сольватированных ионов лития. Поскольку подвижность обратно пропорциональна произведению вязкости и ионного радиуса 14 , оба из которых больше при высоких концентрациях, в результате подвижность комплексов на основе лития значительно снижается. Этот результат согласуется с классической картиной сил (электрических и сопротивления), действующих на заряженную частицу, движущуюся в электрическом поле 14 и описывает движение ионов на основе автомобильного механизма транспорта. Однако исследования показали, что при наличии агрегатов вклад структурной диффузии в общий перенос значителен (рис. 2А) 8 , что может помочь свести на нет другие эффекты высокой вязкости 20 .
Однако исследования показали, что при наличии агрегатов вклад структурной диффузии в общий перенос значителен (рис. 2А) 8 , что может помочь свести на нет другие эффекты высокой вязкости 20 .
A Параметры, влияющие на вклад транспортных и структурных диффузионных механизмов переноса катионов металлов в жидких электролитах (Перепечатано из ссылки 8 с разрешения Elsevier.) B XPS-анализ металлического лития, подвергнутого циклированию в концентрированном (10 M) и стандартном (1 M) LiFSI в растворе электролита EC:DMC (1:1 по объему). (Перепечатано из ссылки 27 с разрешения Elsevier). C Отбор материалов-кандидатов с использованием высокопроизводительных расчетов ключевых свойств для целенаправленных вычислительных исследований и/или синтеза и тестирования. (Воспроизведено из Crabtree, G. AIP Conference Proceedings 1652 , 112–128 (2015) 36 , с разрешения AIP Publishing).
AIP Conference Proceedings 1652 , 112–128 (2015) 36 , с разрешения AIP Publishing).
Изображение в натуральную величину
Вязкость электролита играет роль не только в транспортных свойствах литий-иона, но также и в аспектах, важных для производства и формирования клеток, а именно в наполнении электролитом и смачивании (хотя характер смачивания конкретного электролита, как определено контактный угол может играть более важную роль) 21 . Было показано, например, что емкость лабораторных ячеек с растворами электролитов на основе ионных жидкостей высокой вязкости увеличивается во время начального циклирования по мере того, как электроды постепенно смачиваются электролитом 20,22 . Можно использовать различные стратегии, чтобы понять и смягчить медленное смачивание. Например, в высококонцентрированные растворы электролитов можно добавлять растворители, используемые в качестве «разбавителей», которые не изменяют механизм локального транспорта и структуру сольватации, но снижают вязкость. Эта относительно новая концепция, описанная как локализованные высококонцентрированные электролиты (LHCE) 23 , кажется многообещающей. В дополнение к модификации электролитов можно использовать аналитические методы для лучшего понимания и отслеживания смачивания. Например, нейтронная радиография использовалась для оценки степени смачивания 24 , в то время как распространение ультразвука было предложено в качестве встроенного инструмента мониторинга 25 .
Эта относительно новая концепция, описанная как локализованные высококонцентрированные электролиты (LHCE) 23 , кажется многообещающей. В дополнение к модификации электролитов можно использовать аналитические методы для лучшего понимания и отслеживания смачивания. Например, нейтронная радиография использовалась для оценки степени смачивания 24 , в то время как распространение ультразвука было предложено в качестве встроенного инструмента мониторинга 25 .
Различные концентрации, различные межфазные фазы
Помимо транспортных свойств, электрохимическая стабильность электролита и межфазное образование являются критическими аспектами получения удовлетворительных характеристик батареи. В «стандартных» коммерческих электролитах образование SEI/CEI в значительной степени обусловлено добавками и растворителями электролита, которые присутствуют в избытке и в значительной степени не координируются ионами лития 4 . При высокой концентрации на электрохимическую стабильность электролита и, следовательно, на межфазные границы могут влиять различные факторы, например наличие анионов в первой сольватной оболочке и литиевая координация большей части растворителя 26 . В этом случае «высокая концентрация» не может быть сужена до определенного диапазона концентраций, а должна определяться на основе координации, как обсуждалось выше. В недавней рецензируемой статье дано подробное описание сложных взаимодействий, происходящих между катионами, анионами и растворителями в неводных растворах электролитов на основе лития 9.0019 26 . Интересным результатом ряда исследований является связь координации анионов с межфазным составом 17,27 . Природа межфазных фаз смещается от той, в которой преобладают растворители и продукты их разложения, к той, на которую в первую очередь влияют анионы и продукты их разложения, включая LiF (рис. 2B) 8,27 . Учитывая важность соли для интерфаз с высококонцентрированными электролитами, безусловно, интересно исследовать другие соли помимо LiPF 9.0103 6 и исследовать свойства сформированных SEI/CEI. LiFSI заинтересовался в этом отношении 17,27 . Другие варианты включают использование двухсолевых систем 28 или специальных сорастворителей (как в LHCE) 23 .
В этом случае «высокая концентрация» не может быть сужена до определенного диапазона концентраций, а должна определяться на основе координации, как обсуждалось выше. В недавней рецензируемой статье дано подробное описание сложных взаимодействий, происходящих между катионами, анионами и растворителями в неводных растворах электролитов на основе лития 9.0019 26 . Интересным результатом ряда исследований является связь координации анионов с межфазным составом 17,27 . Природа межфазных фаз смещается от той, в которой преобладают растворители и продукты их разложения, к той, на которую в первую очередь влияют анионы и продукты их разложения, включая LiF (рис. 2B) 8,27 . Учитывая важность соли для интерфаз с высококонцентрированными электролитами, безусловно, интересно исследовать другие соли помимо LiPF 9.0103 6 и исследовать свойства сформированных SEI/CEI. LiFSI заинтересовался в этом отношении 17,27 . Другие варианты включают использование двухсолевых систем 28 или специальных сорастворителей (как в LHCE) 23 . Подход с использованием смесей солей и/или растворителей позволяет использовать преимущества различных компонентов электролита для решения проблем, которые могут возникнуть в других компонентах элемента (например, коррозия алюминиевого токосъемника на положительном электроде) 16,23 .
Подход с использованием смесей солей и/или растворителей позволяет использовать преимущества различных компонентов электролита для решения проблем, которые могут возникнуть в других компонентах элемента (например, коррозия алюминиевого токосъемника на положительном электроде) 16,23 .
Разработка электролитов для литиевых аккумуляторов следующего поколения
Одним из факторов, стимулирующих исследования высококонцентрированных электролитов, является желание создать элементы, способные полностью использовать высоковольтные катодные материалы и литий-металлические аноды 12,17,23 . Материалы электродов с высокой емкостью или высоким напряжением, вероятно, необходимы для компенсации потерь энергоемкости (особенно удельной энергии) из-за повышенной плотности высококонцентрированных электролитов. Несмотря на то, что электролиты высокой концентрации использовались с графитовыми анодами (и, как правило, в паре с высоковольтными катодами), работы, посвященные металлическому литиевому электроду, безусловно, преобладают над работами, о которых сообщается в литературе 9. 0019 17,23,27,28 .
0019 17,23,27,28 .
Одной из основных проблем с анодами из металлического лития является необходимость контролировать морфологию осаждения, чтобы избежать мшистого или дендритного роста металлического лития. Высококонцентрированные растворы электролитов имеют в этом отношении существенное преимущество перед «стандартным» электролитом. Несколько исследований 17,23 показали, что высококонцентрированные электролиты (или также LHCE) позволяют наносить металлический литий с более плотной и округлой морфологией осажденного лития при плотности тока 1 мА см −2 . В аналогичных условиях игольчатые дендритные структуры осаждаются из «стандартных» 1 M растворов электролитов на основе карбонатов 17,23 . В этих примерах авторы связывают улучшенное поведение металлического лития с осаждением (и растворением) с изменениями в составе SEI, полученного из концентрированных электролитов (где SEI также зависит от состава исследуемого раствора электролита) 17,23 .
В дополнение к рассмотренным здесь неводным электролитам, другие нетрадиционные электролиты, такие как водно-солевые электролиты (WISE) 29 или гибридные водные неводные электролиты (HANE) 30 в последнее время вызывают интерес. WISE и HANE используют преимущества полной координации растворителей (как в высококонцентрированных электролитах, как определено выше), чтобы расширить окно электрохимической стабильности, типичное для водных электролитов в других технологиях хранения энергии, не основанных на литии. Тем не менее, все еще необходимы значительные исследования, чтобы эти системы могли конкурировать с неводными электролитами для батарей на основе лития 9.0019 29 .
Дальнейшая разработка новых компонентов и составов электролитов может выиграть от новых исследовательских подходов, включающих высокопроизводительные и автономные испытательные платформы в сочетании с машинным обучением. Вычислительный скрининг конкретных свойств может ограничить количество молекул, подлежащих углубленным исследованиям (рис. 2C) 31 . Автономные платформы, управляемые алгоритмами машинного обучения, могут использоваться для оптимизации составов, что может привести к неинтуитивным составам электролитов с определенными свойствами, как это уже было продемонстрировано с водными растворами электролитов 32 . Кроме того, использование передовых методов определения характеристик может привести к лучшему пониманию поведения электролита в ячейке во время работы. Например, рамановские характеристики in situ позволили непосредственно исследовать истощение ионов лития в электролите 18 . Сочетание инновационных исследовательских подходов с передовыми аналитическими методами, скорее всего, окажется особенно важным, учитывая многогранную роль электролита в аккумуляторе и его влияние на производительность и срок службы.
2C) 31 . Автономные платформы, управляемые алгоритмами машинного обучения, могут использоваться для оптимизации составов, что может привести к неинтуитивным составам электролитов с определенными свойствами, как это уже было продемонстрировано с водными растворами электролитов 32 . Кроме того, использование передовых методов определения характеристик может привести к лучшему пониманию поведения электролита в ячейке во время работы. Например, рамановские характеристики in situ позволили непосредственно исследовать истощение ионов лития в электролите 18 . Сочетание инновационных исследовательских подходов с передовыми аналитическими методами, скорее всего, окажется особенно важным, учитывая многогранную роль электролита в аккумуляторе и его влияние на производительность и срок службы.
Стоимость в конечном итоге станет движущим фактором при внедрении высококонцентрированных электролитов. Несмотря на то, что разница между стоимостью основных интересующих солей относительно невелика, разница между стоимостью растворителей-электролитов и солей 33 составляет ~10. В результате уменьшение количества растворителя и увеличение количества соли приводит к чистому увеличению стоимости состава электролита. Как недавно указал исх. 34, важно помнить, что «затраты» не всегда являются денежными, но также могут носить технический характер, особенно при рассмотрении возможности интеграции новых компонентов в существующие процессы производства клеток.
В результате уменьшение количества растворителя и увеличение количества соли приводит к чистому увеличению стоимости состава электролита. Как недавно указал исх. 34, важно помнить, что «затраты» не всегда являются денежными, но также могут носить технический характер, особенно при рассмотрении возможности интеграции новых компонентов в существующие процессы производства клеток.
Этап формирования и старения является наиболее затратным с точки зрения времени и денег этапом в процессе производства современных литий-ионных аккумуляторов 35 . Следовательно, экономия на этом производственном этапе была бы выгодной. Хотя известно, что природа и состав интерфаз меняются в высококонцентрированных электролитах, потенциальное влияние (с точки зрения времени и связанных с этим денежных затрат) на стадию формирования при производстве клеток до сих пор неизвестно. Вопрос стоимости гораздо сложнее, чем вопрос самих материалов. Таким образом, преимущества работы высококонцентрированных растворов электролитов, вероятно, должны быть значительными, чтобы перевесить затраты на текущие «стандартные» 1M растворы электролитов.
В обозримом будущем «стандартные» растворы электролита 1 M, вероятно, останутся самыми современными для текущего поколения литий-ионных аккумуляторов. Однако обнадеживающие экспериментальные результаты, полученные с использованием высококонцентрированных растворов электролитов, могут открыть альтернативный путь к будущим высоковольтным и высокоэнергетическим батареям на основе лития. Хотя объемная ионная проводимость останется доступным, надежным и экономически эффективным инструментом скрининга для разработки электролитов, важно помнить, что самая высокая объемная проводимость не обязательно приводит к «наилучшим» характеристикам элемента, особенно с точки зрения пропускной способности. Отказ от традиционной мудрости электролитов, чтобы сосредоточиться на таких аспектах, как проводимость литий-иона (т. е. перенос) и формирование градиентов концентрации в электролите (ведущее к истощению ионов лития), может вдохновить на новые направления в исследованиях электролитов с использованием концентраций выше стандартных. 1 М. Тем не менее нельзя забывать о важности понимания межфазной химии, поскольку использование высококонцентрированных электролитов меняет многое из того, что ученые знают о межфазном образовании.
1 М. Тем не менее нельзя забывать о важности понимания межфазной химии, поскольку использование высококонцентрированных электролитов меняет многое из того, что ученые знают о межфазном образовании.
Ссылки
Zhang, H. et al. От электродов с твердым раствором и концепции кресла-качалки до современных аккумуляторов. Анжю. хим. Междунар. Эд. 59 , 534–538 (2020).
КАС Статья Google ученый
Се, Дж. и Лу, Ю.-К. Ретроспектива литий-ионных аккумуляторов. Нац. коммун. 11 , 2499 (2020).
ОБЪЯВЛЕНИЕ КАС Статья Google ученый
Haregewoin, A.M., Wotango, A.S. & Hwang, B.-J. Электролитные добавки для электродов литий-ионных аккумуляторов: достижения и перспективы. Энергетика Окружающая среда.
 науч. 9 , 1955–1988 (2016).
науч. 9 , 1955–1988 (2016).КАС Статья Google ученый
Сюй, К. Электролиты и промежуточные фазы в литий-ионных батареях и не только. Хим. Ред. 114 , 11503–11618 (2014).
КАС Статья Google ученый
Solchenbach, S., Pritzl, D., Kong, E.J.Y., Landesfeind, J. & Gasteiger, H.A. Золотой микроэлектрод сравнения для измерения импеданса и потенциала в литий-ионных батареях. Дж. Электрохим. соц. 163 , A2265 (2016).
КАС Статья Google ученый
Zhang, T. & Paillard, E. Последние достижения в области высоковольтных, не содержащих электропроводов электролитов для литий-ионных аккумуляторов на основе графита. Фронт. хим. науч. англ. 12 , 577–591 (2018).
КАС Статья Google ученый
«>Бородин О., Селф Дж., Перссон К. А., Ван С. и Сюй К. Неизведанные воды: сверхконцентрированные электролиты. Джоуль 4 , 69–100 (2020).
КАС Статья Google ученый
Хендерсон, В. А., Брукс, Н. Р., Бреннессел, В. В. и Янг, В. Г. Структуры сольватов триглим-литий + катион: модели для аморфных концентрированных жидких и полимерных электролитов (I). Хим. Матер. 15 , 4679–4684 (2003).
КАС Статья Google ученый
Сюй К. Навигация по минному полю аккумуляторной литературы.
 Комм. Матер. 3 , 31 (2022).
Комм. Матер. 3 , 31 (2022).Артикул Google ученый
Валоен, Л. О. и Реймерс, Дж. Н. Транспортные свойства электролитов литий-ионных аккумуляторов на основе LiPF6. Дж. Электрохим. соц. 152 , А882 (2005 г.).
Артикул Google ученый
Wang, J. et al. Сверхконцентрированные электролиты для высоковольтной литий-ионной батареи. Нац. коммун. 7 , 12032 (2016).
ОБЪЯВЛЕНИЕ КАС Статья Google ученый
Raccichini, R., Furness, L., Dibden, J.W., Owen, J.R. & García-Araez, N. Характеристика импеданса транспортных свойств электролитов, содержащихся в пористых электродах и сепараторах, полезных для Li-S аккумуляторов. Дж. Электрохим. соц. 165 , A2741–A2749 (2018).
КАС Статья Google ученый
«>Сюй, К. Неводные жидкие электролиты для литиевых аккумуляторов. Хим. 104 , 4303–4418 (2004).
КАС Статья Google ученый
Wang, W. et al. Стабильное циклирование высоковольтных литий-металлических аккумуляторов благодаря высококонцентрированному электролиту на основе FEC. Приложение ACS Матер. Интер. 12 , 22901–22909 (2020).
КАС Статья Google ученый
Пэн З. и др. Мощные литий-металлические батареи на основе высококонцентрированных электролитов на основе ацетонитрила с добавкой виниленкарбоната. г. Доп. Функц. Матер. 30 , 2001285 (2020).
КАС Статья Google ученый
«>Zugmann, S. et al. Измерение чисел переноса для ионно-литиевых электролитов четырьмя различными методами, сравнительное исследование. Электрохим. Acta 56 , 3926–3933 (2011).
КАС Статья Google ученый
Giffin, G. A., Moretti, A., Jeong, S. & Passerini, S. Отделение эффективной проводимости ионов Li+ от вязкости электролита для улучшения характеристик элемента при комнатной температуре. J. Power Sources 342 , 335–341 (2017).
ОБЪЯВЛЕНИЕ КАС Статья Google ученый
Заутер, К.
 , Зан, Р. и Вуд, В. Понимание заполнения электролитом литий-ионных аккумуляторов. Дж. Электрохим. соц. 167 , 100546 (2020).
, Зан, Р. и Вуд, В. Понимание заполнения электролитом литий-ионных аккумуляторов. Дж. Электрохим. соц. 167 , 100546 (2020).ОБЪЯВЛЕНИЕ КАС Статья Google ученый
Ким, Г. Т. и др. Использование натуральных связующих и ионных жидких электролитов для более экологичных и безопасных литий-ионных аккумуляторов. J. Источники питания 196 , 2187–2194 (2011).
КАС Статья Google ученый
Чен, С. и др. Высоковольтные литий-металлические батареи с локализованными высококонцентрированными электролитами. Доп. Матер. 30 , 1706102 (2018).
Артикул Google ученый
Knoche, T. et al. Визуализация на месте процесса заливки растворителя электролита методом нейтронной радиографии. Дж.
 Источники питания 331 , 267–276 (2016).
Источники питания 331 , 267–276 (2016).ОБЪЯВЛЕНИЕ КАС Статья Google ученый
Денг З. и др. Ультразвуковое сканирование для наблюдения за смачиванием и «несмачиванием» в литий-ионном пакете. Клетки Джоуль 4 , 2017–2029 (2020).
КАС Статья Google ученый
Chen, X. & Zhang, Q. Атомное понимание фундаментальных взаимодействий в электролитах литиевых батарей. Акк. хим. Рез. 53 , 1992–2002 (2020).
КАС Статья Google ученый
Fan, X. et al. Высокофторированные межфазные переходы позволяют использовать высоковольтный литий-металл. Аккумуляторы. хим. 4 , 174–185 (2018).
КАС Google ученый
«>Дроге Л., Гримо А., Фонтейн О. и Тараскон Ж.-М. Водно-солевой электролит (WiSE) для аккумуляторов на водной основе: долгий путь к практичности. Доп. Энергия Матер. 10 , 2002440 (2020).
КАС Статья Google ученый
Ван, Ф. и др. Гибридный водный/неводный электролит для безопасных и высокоэнергетических литий-ионных аккумуляторов. Джоуль 2 , 927–937 (2018).
КАС Статья Google ученый
Cheng, L. et al. Ускорение поиска электролитов для хранения энергии с помощью высокопроизводительного скрининга.
 J. Phys. хим. лат. 6 , 283–291 (2015).
J. Phys. хим. лат. 6 , 283–291 (2015).КАС Статья Google ученый
Дэйв А. и др. Автономное открытие аккумуляторных электролитов с помощью роботизированных экспериментов и машинного обучения. Cell Rep. 1 , 100264 (2020).
КАС Google ученый
Zheng, H. et al. Двухсолевые электролиты низкой концентрации на основе дифторфосфата лития для литий-металлических аккумуляторов. Доп. Энергия Матер. 10 , 2001440 (2020).
КАС Статья Google ученый
Полманн, С. Показатели и методы перехода от исследований к инновациям в области накопления энергии. Нац. коммун. 13 , 1538 (2022).
ОБЪЯВЛЕНИЕ КАС Статья Google ученый
«>Crabtree, G. Объединенный центр исследований в области накопления энергии: новая парадигма исследований и разработок в области аккумуляторов. Конф. АИП. проц. 1652 , 112–128 (2015).
ОБЪЯВЛЕНИЕ Статья Google ученый
Суо, Л., Ху, Ю.-С., Ли, Х., Арманд, М. и Чен, Л. Новый класс электролитов на основе растворителя в соли для высокоэнергетических перезаряжаемых металлических литиевых батарей. Нац. коммун. 4 , 1481 (2013).
ОБЪЯВЛЕНИЕ Статья Google ученый
Бард, А. Дж. и Фолкнер, Л. Р. Электрохимические методы: основы и приложения (John Wiley & Sons, Inc., 2001).
Кремер Л.С. и др. Влияние концентрации соли в электролите на скоростную способность сверхтолстых электродов NCM 622. Аккумуляторы Supercaps 3 , 1172–1182 (2020 г.).
КАС Статья Google ученый
Beyene, T. T. et al. Концентрированный двухсолевой электролит для стабилизации металлического лития и увеличения срока службы безанодных литий-металлических аккумуляторов. Дж. Электрохим. соц. 166 , A1501–A1509 (2019).
КАС Статья Google ученый
Лю Ю., Чжан Р., Ван Дж. и Ван Ю. Текущее и будущее производство литий-ионных аккумуляторов. iScience 24 , 102332 (2021).
ОБЪЯВЛЕНИЕ КАС Статья Google ученый
Ссылки для скачивания
Литий-ионные аккумуляторы, Часть 5: Электролиты
Электролит часто является недооцененным компонентом литий-ионных (Li-ion) аккумуляторов. Они просто обеспечивают электрический путь между анодом и катодом, который поддерживает ток (на самом деле, ионный) поток. Но электролиты являются ключом к характеристикам аккумуляторов, и ожидается, что достижения в области химии электролитов станут важным событием, ведущим к созданию высокоэффективных, безопасных и недорогих литий-ионных аккумуляторов для будущих поколений электромобилей, хранения энергии в масштабе сети и другие крупные системы. В зависимости от конструкции аккумулятора это может быть жидкий или пастообразный материал. Твердые электролиты могли бы повысить плотность энергии и безопасность ионов лития, но они еще не готовы к коммерциализации. В этом разделе часто задаваемых вопросов рассматриваются электролиты, широко используемые в настоящее время, и рассматриваются усовершенствованные электролиты, находящиеся в стадии разработки, включая твердотельные и гибридные твердотельные электролиты.
В зависимости от конструкции аккумулятора это может быть жидкий или пастообразный материал. Твердые электролиты могли бы повысить плотность энергии и безопасность ионов лития, но они еще не готовы к коммерциализации. В этом разделе часто задаваемых вопросов рассматриваются электролиты, широко используемые в настоящее время, и рассматриваются усовершенствованные электролиты, находящиеся в стадии разработки, включая твердотельные и гибридные твердотельные электролиты.
Литий-ионные аккумуляторы состоят из анода и катода на основе различных окислительно-восстановительных химических пар с электролитом и сепаратором между ними. Электролит проводит ионы, а не электроны, через сепаратор и между анодом и катодом (рис. 1) . Электролиты могут принимать различные формы, причем растворенные соли являются наиболее распространенной формой. Растворитель является ключевым компонентом электролита. Водные электролиты имеют высокую проводимость (σ), обычно σ = ~1 Симен/см (См/см), но имеют относительно небольшие окна электрохимической стабильности около 1,25 В. Электролиты на основе неорганических растворителей имеют меньшую электропроводность с σ < 100 мСм/см, но предлагают более широкие окна стабильности 4 В и более. Кроме того, органические растворители более дороги по сравнению с водными растворами. Иногда используют твердый неорганический или полимерный электролит, но с гораздо меньшей электропроводностью; σ <0,1 мСм/см при комнатной температуре.
Электролиты на основе неорганических растворителей имеют меньшую электропроводность с σ < 100 мСм/см, но предлагают более широкие окна стабильности 4 В и более. Кроме того, органические растворители более дороги по сравнению с водными растворами. Иногда используют твердый неорганический или полимерный электролит, но с гораздо меньшей электропроводностью; σ <0,1 мСм/см при комнатной температуре.
Рисунок 1: Электролит переносит положительно заряженные ионы через сепаратор между катодом и анодом. (Изображение: Dragonfly Energy)
Различные химические составы первичных (неперезаряжаемых) и вторичных (перезаряжаемых) батарей основаны на разных электролитах. Серная кислота служит электролитом в большинстве свинцово-кислотных аккумуляторов. Обычные щелочные первичные элементы используют гидроксид калия в качестве электролита. Соли, такие как гексафторфосфат лития (LiPF6), обычно используются в качестве электролитов в литий-ионах.
Твердые электролиты для твердых литий-ионных аккумуляторов
Твердые электролиты, изготовленные из керамики, такой как оксиды лития и металла, обещают более высокую плотность энергии и не воспламеняются, что повышает безопасность по сравнению с жидкими электролитами. Помимо риска возгорания, жидкие электролиты могут быть очень реакционноспособными, что приводит к побочным реакциям с электродами, что приводит к снижению емкости батареи с течением времени, что называется снижением емкости. Ожидается, что батареи с твердотельными электролитами не будут испытывать снижения емкости. Также ожидается, что твердотельные электролиты позволят создать литий-металлический анод большой емкости, который значительно повысит удельную энергию и мощность, а также срок службы ионов лития. Разработка твердотельных электролитов сложна и требует материала с рядом эксплуатационных характеристик:
Помимо риска возгорания, жидкие электролиты могут быть очень реакционноспособными, что приводит к побочным реакциям с электродами, что приводит к снижению емкости батареи с течением времени, что называется снижением емкости. Ожидается, что батареи с твердотельными электролитами не будут испытывать снижения емкости. Также ожидается, что твердотельные электролиты позволят создать литий-металлический анод большой емкости, который значительно повысит удельную энергию и мощность, а также срок службы ионов лития. Разработка твердотельных электролитов сложна и требует материала с рядом эксплуатационных характеристик:
#1 Высокая ионная проводимость в сочетании с высокой устойчивостью к электронам
#2 Высокая способность переноса катионов для поддержки высоких уровней мощности
#3 Широкий диапазон электрохимической стабильности для надежной работы
#4 Высокая термическая стабильность и высокая механическая прочность
#5 Easy и низкая себестоимость производства
Коммерчески жизнеспособный материал еще предстоит разработать: Твердотельные электролиты на основе неорганических материалов обладают высокой ионной проводимостью и хорошей механической прочностью. Полимерные электролиты гибкие, их легче обрабатывать, они сохраняют хороший контакт с электродами, снижая межфазное сопротивление. Но у каждого подхода есть свои проблемы: неорганические твердотельные электролиты могут иметь плохой контакт с электродами (так называемое сопротивление границ зерен), не обладать химической и электрохимической стабильностью, иметь тенденцию быть относительно дорогими и хрупкими. Хрупкость представляет собой серьезную проблему, поскольку неорганические твердотельные электролиты не могут компенсировать изменения объема электродов во время заряда и разряда. Полимерные твердотельные электролиты могут устранить многие ограничения производительности неорганических твердотельных электролитов. Тем не менее, они имеют очень низкую ионную проводимость, что делает их неспособными поддерживать скорости заряда и разряда, необходимые для практических литий-ионных конструкций.
Полимерные электролиты гибкие, их легче обрабатывать, они сохраняют хороший контакт с электродами, снижая межфазное сопротивление. Но у каждого подхода есть свои проблемы: неорганические твердотельные электролиты могут иметь плохой контакт с электродами (так называемое сопротивление границ зерен), не обладать химической и электрохимической стабильностью, иметь тенденцию быть относительно дорогими и хрупкими. Хрупкость представляет собой серьезную проблему, поскольку неорганические твердотельные электролиты не могут компенсировать изменения объема электродов во время заряда и разряда. Полимерные твердотельные электролиты могут устранить многие ограничения производительности неорганических твердотельных электролитов. Тем не менее, они имеют очень низкую ионную проводимость, что делает их неспособными поддерживать скорости заряда и разряда, необходимые для практических литий-ионных конструкций.
Пока выбор лучшего твердотельного электролита не сужен; ведутся исследования десятков вариантов твердотельных электролитов, включая сульфиды, оксиды, фосфаты, полиэфиры, полиэфиры, полиуретаны и многие другие. В настоящее время полимеры легче обрабатывать, чем керамику, и их производство дешевле. Керамика может работать при более высоких температурах и больше подходит для суровых условий окружающей среды.
В настоящее время полимеры легче обрабатывать, чем керамику, и их производство дешевле. Керамика может работать при более высоких температурах и больше подходит для суровых условий окружающей среды.
Литий-ионы, использующие твердотельные электролиты, как ожидается, будут иметь очень низкую скорость саморазряда, что позволит хранить энергию в течение многих лет с незначительными потерями. Однако срок службы современных материалов составляет всего около трех лет, что делает их непрактичными практически во всех областях применения. Исследования продолжаются из-за большой выгоды, ожидаемой от разработки жизнеспособного твердотельного электролита:
Плотность энергии будет выше, поскольку твердотельные батареи более чем на 80% тоньше и имеют более высокое напряжение разложения, чем современные литий-ионные. Высокая плотность энергии позволила бы увеличить расстояние движения электромобилей (EV) и сократить количество зарядных станций, необходимых для поддержки работы EV.
Поскольку в твердотельных батареях нет жидкого электролита, который нагревается во время быстрой зарядки, то возможна более быстрая зарядка. Ожидается, что быстрая зарядка в сочетании с более высокой плотностью энергии повысит конкурентоспособность будущих поколений электромобилей.
Твердотельные электролиты обеспечивают безопасную работу . Современные жидкие электролиты легко воспламеняются и требуют многочисленных мер безопасности для обеспечения надежной работы. Твердотельные аккумуляторы по своей природе безопасны с очень низким риском возгорания, и их можно эксплуатировать при более высоких температурах по сравнению с литий-ионными на основе жидких электролитов.
Снижение стоимости возможно при использовании твердотельных аккумуляторов. Жидкие литий-ионные аккумуляторы стоят около 220 долларов за кВтч. Хотя ожидается, что она будет продолжать снижаться, темпы снижения затрат ограничены зависимостью от использования дефицитных материалов, таких как кобальт. Ожидается, что в твердотельных батареях не будут использоваться дефицитные или редкие материалы. Использование твердотельного электролита устранит компонент сепаратора, что еще больше упростит конструкцию аккумуляторов, снизит стоимость литий-ионных аккумуляторов и сделает их более привлекательными для использования в электромобилях и крупномасштабных системах хранения энергии.
Ожидается, что в твердотельных батареях не будут использоваться дефицитные или редкие материалы. Использование твердотельного электролита устранит компонент сепаратора, что еще больше упростит конструкцию аккумуляторов, снизит стоимость литий-ионных аккумуляторов и сделает их более привлекательными для использования в электромобилях и крупномасштабных системах хранения энергии.
Твердые варианты
Один многообещающий твердотельный электролит изготовлен из лития, скандия, индия и хлора (рис. 2) . Он имеет высокую ионную проводимость и низкую электронную проводимость. Он имеет окно с высокой электрохимической стабильностью, которое может поддерживать разработку твердотельного литий-иона, который может работать без значительной потери емкости в течение более ста циклов при высоком напряжении (выше 4 В) и тысяч циклов при более низком напряжении. Хлоридные характеристики этого электролита позволяют ему работать при напряжении более 4 В, что делает его пригодным для использования с наиболее распространенными катодными материалами, используемыми в современных литий-ионных конструкциях.
Рис. 2: Электролиты на основе хлора могут обеспечить улучшенные характеристики для твердотельных ионов лития. (Изображение: Аргоннская национальная лаборатория)
Большинство предыдущих разработок твердотельных электролитов были сосредоточены на сульфидах, с которыми легче работать, но они имеют более низкий диапазон электрохимической стабильности и разлагаются при напряжении выше 2,5 В. Для работы при более высоких напряжениях сульфиды требуют изолирующего покрытия. на катоде, что снижает проводимость системы. Замена сульфида хлоридом устраняет эту проблему.
В дополнение к оптимизации характеристик твердотельного электролита важным фактором является оптимизация интерфейса между электролитом и слоями анода и катода. Один из подходов заключается в использовании специальных покрытий, что увеличивает технологические процессы и стоимость.
Был предложен альтернативный метод, который требует удаления всего углекислого газа (CO2), присутствующего при спекании материалов батареи. Поскольку твердотельный электролит, анод и катод изготовлены из различных керамических материалов, присутствие даже небольшого количества СО2 может значительно снизить производительность интерфейсов между электролитом и анодом и катодом. Работа продолжается в различных аспектах составов и изготовления твердотельных электролитов. Гибридные электролиты могут стать краткосрочной альтернативой.
Поскольку твердотельный электролит, анод и катод изготовлены из различных керамических материалов, присутствие даже небольшого количества СО2 может значительно снизить производительность интерфейсов между электролитом и анодом и катодом. Работа продолжается в различных аспектах составов и изготовления твердотельных электролитов. Гибридные электролиты могут стать краткосрочной альтернативой.
Гибридные электролиты
Недавно предложенный способ устранения ограничений производительности неорганических и полимерных твердотельных электролитов заключается в гибридизации двух или более элементов. Разработка коммерчески жизнеспособного гибридного твердотельного электролита (HSE) могла бы преодолеть недостатки как неорганических, так и полимерных технологий, сочетая сильные стороны каждой технологии (рис. 3) .
Рисунок 3: Сравнение производительности полимерных, неорганических и гибридных твердых электролитов. (Изображение: Frontiers in Energy Research)
Как и в случае со всеми твердотельными электролитами, разработка HSE является сложной задачей, и коммерческое решение еще впереди. HSE имеют лучшую ионную проводимость, чем большинство полимерных электролитов, но она все же слишком низкая. Кроме того, HSE страдают плохой межфазной стабильностью (снижение надежности) и высоким межфазным сопротивлением (снижение скорости заряда/разряда), что значительно ограничивает производительность литий-ионных аккумуляторов на основе HSE.
HSE имеют лучшую ионную проводимость, чем большинство полимерных электролитов, но она все же слишком низкая. Кроме того, HSE страдают плохой межфазной стабильностью (снижение надежности) и высоким межфазным сопротивлением (снижение скорости заряда/разряда), что значительно ограничивает производительность литий-ионных аккумуляторов на основе HSE.
Краткое описание
Литий-ионные аккумуляторы с различными жидкими электролитами обеспечивают хорошее сочетание производительности и безопасности. Но стоят они относительно дорого. Новые типы электролитов потребуются для улучшения производительности литий-ионных аккумуляторов, снижения затрат и повышения безопасности. В настоящее время предпринимаются многочисленные усилия по разработке твердотельных электролитов, которые обещают литий-ионы с более высокой плотностью энергии, более быстрой зарядкой, более безопасной работой и более низкой стоимостью. Появление HSE обещает ускорить разработку твердотельных литий-ионных аккумуляторов.
Ссылки
Предотвращение выбросов CO2 повышает термическую стабильность на границе раздела электролита Li7La3Zr2O12 со слоистыми оксидными катодами, передовые энергетические материалы Разработки и вызовы в области гибридных твердых электролитов для литий-ионных аккумуляторов, передовые позиции в исследованиях в области энергетики
Ученые открыли новый электролит для твердотельных литий-ионных аккумуляторов, Аргоннская национальная лаборатория
Что такое аккумуляторный электролит и как он работает? Стрекоза Энергия
Ученые открыли новый электролит для твердотельных литий-ионных аккумуляторов
В поисках идеального аккумулятора ученые преследуют две основные цели: создать устройство, которое может хранить большое количество энергии и делать это безопасно. Многие батареи содержат жидкие электролиты, которые потенциально легко воспламеняются.
В результате твердотельные литий-ионные батареи, состоящие из полностью твердых компонентов, становятся все более привлекательными для ученых, поскольку они предлагают привлекательное сочетание более высокой безопасности и повышенной плотности энергии — именно столько энергии может хранить батарея. на заданный объем.
на заданный объем.
Исследователи из Университета Ватерлоо, Канада, которые являются членами Объединенного центра исследований в области хранения энергии (JCESR) со штаб-квартирой в Аргоннской национальной лаборатории Министерства энергетики США, обнаружили новый твердый электролит, который предлагает несколько важных преимущества.
Этот электролит, состоящий из лития, скандия, индия и хлора, хорошо проводит ионы лития, но плохо проводит электроны. Эта комбинация необходима для создания полностью твердотельной батареи, которая работает без существенной потери емкости в течение более ста циклов при высоком напряжении (выше 4 вольт) и тысяч циклов при промежуточном напряжении. Хлоридная природа электролита является ключом к его стабильности при рабочих условиях выше 4 вольт, что означает, что он подходит для типичных катодных материалов, которые составляют основу современных литий-ионных элементов.
«Главная привлекательность твердотельного электролита заключается в том, что он не может загореться и позволяет эффективно размещать его в аккумуляторной ячейке; мы были рады продемонстрировать стабильную работу при высоком напряжении», — сказала Линда Назар, заслуженный профессор химии Университета Ватерлоо и давний член JCESR.
Текущие версии твердотельных электролитов в значительной степени сосредоточены на сульфидах, которые окисляются и разлагаются при напряжении выше 2,5 вольт. Следовательно, они требуют включения изолирующего покрытия вокруг материала катода, которое работает при напряжении выше 4 вольт, что ухудшает способность электронов и ионов лития перемещаться из электролита в катод.
«С сульфидными электролитами у вас есть своего рода головоломка — вы хотите электронно изолировать электролит от катода, чтобы он не окислялся, но вам по-прежнему требуется электронная проводимость в материале катода», — сказал Назар.
Хотя группа Назара не была первой, кто изобрел хлоридный электролит, решение заменить половину индия на скандий, основанное на их предыдущей работе, оказалось выигрышным с точки зрения более низкой электронной и более высокой ионной проводимости. «Хлоридные электролиты становятся все более привлекательными, потому что они окисляются только при высоких напряжениях, а некоторые из них химически совместимы с лучшими катодами, которые у нас есть», — сказал Назар. «Недавно сообщалось о нескольких из них, но мы разработали один с явными преимуществами».
«Недавно сообщалось о нескольких из них, но мы разработали один с явными преимуществами».
Одним из химических ключей к ионной проводимости является пересекающаяся трехмерная структура материала, называемая шпинелью. Исследователи должны были сбалансировать два конкурирующих желания — загрузить шпинель как можно большим количеством ионов, несущих заряд, но также оставить участки открытыми для движения ионов. «Вы можете думать об этом, как о попытке устроить танец — вы хотите, чтобы люди пришли, но вы не хотите, чтобы было слишком много людей», — сказал Назар.
По словам Назар, идеальной ситуацией было бы, чтобы половина мест в структуре шпинели была занята литием, а другая половина оставалась открытой, но она объяснила, что создать такую ситуацию сложно.
В дополнение к хорошей ионной проводимости лития, Назар и ее коллеги должны были убедиться, что электроны не могут легко перемещаться через электролит, чтобы вызвать его разложение при высоком напряжении. «Представьте себе игру в классики», — сказала она. «Даже если вы просто пытаетесь перепрыгнуть с первого квадрата на второй, если вы можете создать стену, которая затрудняет перепрыгивание электронов, в нашем случае, это еще одно преимущество этого твердого электролита. ».
«Даже если вы просто пытаетесь перепрыгнуть с первого квадрата на второй, если вы можете создать стену, которая затрудняет перепрыгивание электронов, в нашем случае, это еще одно преимущество этого твердого электролита. ».
Назар сказал, что пока неясно, почему электронная проводимость ниже, чем у многих хлоридных электролитов, о которых сообщалось ранее, но это помогает установить чистую поверхность раздела между материалом катода и твердым электролитом, факт, который в значительной степени отвечает за стабильную работу даже при высоких температурах. количества активного вещества на катоде.
Статья, основанная на исследовании «Высокая емкость, длительный срок службы керамических полностью твердотельных литий-ионных аккумуляторов 4 В на основе хлоридных твердых электролитов», появилась в онлайн-издании Nature Energy 9 от 3 января.0063 .
Среди других авторов статьи Лайдонг Чжоу, аспирант Назара, член JCESR, ответственный за большую часть работы, а также Се Ён Ким, Чун Юэн Квок и Абдельджалил Ассуд, все из Университета Ватерлоо. Среди других авторов были Тонг-Тонг Зуо и профессор Юрген Янек из Университета Юстуса Либиха, Германия, и Цян Чжан из Окриджской национальной лаборатории Министерства энергетики.
Среди других авторов были Тонг-Тонг Зуо и профессор Юрген Янек из Университета Юстуса Либиха, Германия, и Цян Чжан из Окриджской национальной лаборатории Министерства энергетики.
Исследование финансировалось Управлением науки Министерства энергетики, Управлением фундаментальных энергетических наук при некоторой поддержке Канадского национального совета по науке и инженерным исследованиям.
Объединенный центр исследований в области хранения энергии (JCESR) , Центр инноваций в области энергетики Министерства энергетики США, представляет собой крупное партнерство, объединяющее исследователей из многих дисциплин для преодоления критических научных и технических барьеров и создания новой революционной технологии хранения энергии. В число партнеров, возглавляемых Аргоннской национальной лабораторией Министерства энергетики США, входят национальные лидеры в области науки и техники из академических кругов, частного сектора и национальных лабораторий.
