9 Определение коэффициента избытка воздуха
по газовому анализу продуктов сгорания.
Коэффициент избытка воздуха — есть отношение действительного количества воздуха Vд поданного в топочную камеру котла к теоретически необходимому для горения Vо
(16)
Величина зависит от состава и вида топлива, топочного режима, степени совершенства смешения топлива с воздухом и т.п. Если известен химический состав газов, получаемых при сгорании топлива, коэффициент избытка воздуха может быть определён по «азотной» формуле, которая для случая полного горения топлива записывается следующим образом:
. (17)
где N2 – содержание азота в сухих продуктах горения, %.
При наличии химической неполноты горения формула приобретает следующий вид:
. (18)
(18)
Если замерено содержание кислорода О2 в дымовых газах по кислородомеру, то величина может быть определена приближённо по «кислородной» формуле:
. (19)
Количество азота в продуктах сгорания может быть подсчитано по формуле:
, % (20)
В таком виде «азотная» формула справедлива для топлив, в которых содержится азота меньше 3%.
1) Потери тепла с уходящими газами определяются разницей энтальпий газов на выходе из последней поверхности нагрева котла и холодного воздуха, поступающего в котёл.
Величины энтальпий имогут быть определены в соответствии с рекомендациями нормативного расчета котельных агрегатов /1/.
, % (21)
2)
Потери тепла от химической неполноты
сгорания определяются суммарной теплотой
сгорания продуктов неполного горения,
остающихся в уходящих газах.
При наличии в продуктах сгорания потери тепла с химической неполнотой сгорания находят по формуле:
, кДж/кг (22)
где — объем сухих газов, м3/кг (м3/м3)
Эта потеря может быть выражена в % от располагаемого тепла
, % (23)
Величина может быть рассчитана по формуле:
Для жидкого топлива:
, м3/кг (24)
Для газового топлива:
,м3/м3 (25)
В
формулах (24) и (25) CO2,
SO2,
CO
– содержание в продуктах сгорания
двуокиси углерода, сернистого газа и
окиси углерода, %; — содержание в исходном топливе двуокиси
углерода, окиси углерода, сероводорода
и различных углеводородов, %.
Процентное содержание Н2, СО, СН4 определяется на хроматографе.
3) Потери тепла в окружающую среду за счет естественной конвекции и излучения наружными поверхностями агрегата изменяются в зависимости от тепловой нагрузки котла.
Экспериментальное определение потерь тепла от наружного охлаждения представляет значительные трудности. Для стационарных котлов величина q 5 принимается по данным рис. 5 для парового котла и рис.4 для водогрейного котла.
При нагрузках, отличающихся от номинальной более чем на 25 %, величина q5 уточняется по формуле:
, % (26)
При
испытании котлов на твердом топливе
необходимо производить дополнительные
замеры для определения потерь теплоты
от механического недожога q4 и физического тепла шлаков q6.
Балансовые испытания на различных нагрузках проводятся после выхода котлоагрегата из ремонта для выявления оптимальных эксплуатационных характеристик. Кроме того, по данным таких испытаний можно судить о качестве ремонта. Результаты измерений этих испытаний заносятся в специальную режимную карту (табл.3).
Таблица 3
РЕЖИМНАЯ КАРТА Котлоагрегата типа___ при сжигании ст№ | «Утверждаю» главный инженер» « | |||||||||||||||
Наименование величин | Разм. | 1 | 2 | 3 | 4 | 5 | 6 | |||||||||
Паропроизводительность | т/ч | |||||||||||||||
Перегретый пар | Давление | кг/см2 | ||||||||||||||
Температура | оС | |||||||||||||||
Топливо | Расход | |||||||||||||||
Давление | ||||||||||||||||
Температура | оС | |||||||||||||||
В О З ДУХ | Сопротивление воздухоподогревателя | ЛЕВ. | мм в.ст. | |||||||||||||
ПРАВ | -«- | |||||||||||||||
Давление воздуха | -«- | |||||||||||||||
Давление воздуха на горелки | -«- | |||||||||||||||
Температура воздуха за калорифером | оС | |||||||||||||||
Содержание О2 за | % | |||||||||||||||
Коэффициент избытка воздуха за | — | |||||||||||||||
Норма работающих горелок | 1 ярус | |||||||||||||||
2 ярус | ||||||||||||||||
| 3 ярус | ||||||||||||||||
Разряжение | В топке | мм
в. | ||||||||||||||
Перед дымососом | ЛЕВ. | -«- | ||||||||||||||
ПРАВ | -«- | |||||||||||||||
Температура дымовых газов | оС | |||||||||||||||
Уходящих | ЛЕВ. | оС | ||||||||||||||
ПРАВ | оС | |||||||||||||||
Температура питательной воды | оС | |||||||||||||||
Амперная загрузка и скорость вращения электродвигателей | ДС | А | а | |||||||||||||
Б | а | |||||||||||||||
ДВ | А | а | ||||||||||||||
Б | а | |||||||||||||||
УП Регулирующих клапанов | ДС | А | % | |||||||||||||
Б | % | |||||||||||||||
ДВ | А | % | ||||||||||||||
Б | % | |||||||||||||||
Примечания: Начальник Начальник ПТО службы наладки Начальник котельного цеха Руководитель Инженер группы режимов котельной группы Руководитель испытаний | ||||||||||||||||
Расчёт объёмов воздуха и продуктов сгорания.
 Определение расхода топлива, газов и воздуха на котёл ТПУ-35, страница 2
Определение расхода топлива, газов и воздуха на котёл ТПУ-35, страница 2Промышленность \ Котельные установки и парогенераторы
Теоретический объем водяных паров
Объем трехатомных газов
Полный объем продуктов сгорания определяется по формуле
а действительный объем водяных паров по формуле
Коэффициенты избытка воздуха.
Коэффициент избытка воздуха на выходе из топки с твердым шлакоудалением для котлов производительностью 35 т/ч и выше по таблице 4.2 методических указаний для каменных и бурых углей
.
Присосы воздуха в газоходах котла в соответствии с таблицей 4.3 методических указаний Δαi
Фестон, ширмовый пароперегреватель на выходе из топки ΔαФ | Конвективный пароперегреватель в горизонтальном газоходе или в верхней части опускной шахты (на весь пароперегреватель) ΔαПП | Водяной экономайзер из стальных труб (на каждую ступень) ΔαЭК | Воздухоподогреватель трубчатый (на каждую ступень) ΔαВЗП |
0,00 | 0,03 | 0,02 | 0,03 |
Коэффициент избытка воздуха за ширмовым пароперегревателем (фестоном)
Коэффициент избытка воздуха за конвективным пароперегревателем
Коэффициент избытка воздуха за водяным экономайзером
Коэффициент избытка воздуха за воздухоподогревателем
Объемы водяных паров.
Действительный объем водяных паров за ширмовым пароперегревателем (фестоном)
Действительный объем водяных паров за конвективным пароперегревателем
Действительный объем водяных паров за водяным экономайзером
Действительный объем водяных паров за воздухоподогревателем
Объемы дымовых газов.
Объем дымовых газов за ширмовым пароперегревателем (фестоном)
Объем дымовых газов за конвективным пароперегревателем
Объем дымовых газов за экономайзером
Объем дымовых газов за воздухоподогревателем
Объемные доли трехатомных газов.
Объемная доля трехатомных газов за фестоном
Объемная доля трехатомных газов за пароперегревателем
Объемная доля трехатомных газов за экономайзером
Объемная доля трехатомных газов за воздухоподогревателем
Объемные доли водяных паров.
Объемная доля водяных паров за фестоном
Объемная доля водяных паров за пароперегревателем
Объемная доля водяных паров за экономайзером
Объемная доля водяных паров за воздухоподогревателем
Суммарные доли трехатомных газов и водяных паров .
Суммарная доля трехатомных газов и водяных паров за фестоном
Суммарная доля трехатомных газов и водяных паров за пароперегревателем
Суммарная доля трехатомных газов и водяных паров за экономайзером
Суммарная доля трехатомных газов и водяных паров за воздухоподогревателем
Массы дымовых газов.
Масса дымовых газов за фестоном
Масса дымовых газов за пароперегревателем
Масса дымовых газов за экономайзером
Масса дымовых газов за воздухоподогревателем
Концентрации золы в дымовых газах .
Концентрация золы в дымовых газах за фестоном
Концентрация золы в дымовых газах за пароперегревателем
Концентрация золы в дымовых газах за экономайзером
Концентрация золы в дымовых газах за воздухоподогревателем
Средние объемные характеристики продуктов сгорания.
Расчетные формулы | Размерность | ||||
Газоходы котла | |||||
Топка, ширмы, фестон | Конвективный пароперегреватель | Водяной экономайзер | Воздухоподогреватель | ||
Коэффициент избытка воздуха за поверхностью нагрева | _ | 1,2 | 1,23 | 1,25 | 1,28 |
Коэффициент избытка воздуха, средний по газоходу | _ | 1,2 | 1,215 | 1,24 | 1,265 |
Объем водяных паров | 0,546 | 0,547 | 0,549 | 0,551 | |
Объем дымовых газов | 6,0206 | 6,091 | 6,21 | 6,33 | |
Объемная доля трехатомных газов | _ | 0,141 | 0,14 | 0,137 | 0,135 |
Объемная доля водяных паров | _ | 0,0907 | 0,09 | 0,088 | 0,087 |
Суммарная доля трехатомных газов и водяных паров | _ | 0,2317 | 0,23 | 0,225 | 0,222 |
Масса дымовых газов | 7,962 | 8,053 | 8,206 | 8,358 | |
Концентрация золы в дымовых газах | 0,0413 | 0,0408 | 0,0401 | 0,0393 | |
Энтальпии воздуха и
продуктов сгорания по газоходам.
Скачать файл
Выбери свой ВУЗ
- АлтГТУ 419
- АлтГУ 113
- АмПГУ 296
- АГТУ 267
- БИТТУ 794
- БГТУ «Военмех» 1191
- БГМУ 172
- БГТУ 603
- БГУ 155
- БГУИР 391
- БелГУТ 4908
- БГЭУ 963
- БНТУ 1070
- БТЭУ ПК 689
- БрГУ 179
- ВНТУ 120
- ВГУЭС 426
- ВлГУ 645
- ВМедА 611
- ВолгГТУ 235
- ВНУ им.
 Даля 166
Даля 166 - ВЗФЭИ 245
- ВятГСХА 101
- ВятГГУ 139
- ВятГУ 559
- ГГДСК 171
- ГомГМК 501
- ГГМУ 1966
- ГГТУ им. Сухого 4467
- ГГУ им. Скорины 1590
- ГМА им. Макарова 299
- ДГПУ 159
- ДальГАУ 279
- ДВГГУ 134
- ДВГМУ 408
- ДВГТУ 936
- ДВГУПС 305
- ДВФУ 949
- ДонГТУ 498
- ДИТМ МНТУ 109
- ИвГМА 488
- ИГХТУ 131
- ИжГТУ 145
- КемГППК 171
- КемГУ 508
- КГМТУ 270
- КировАТ 147
- КГКСЭП 407
- КГТА им.
 Дегтярева 174
Дегтярева 174 - КнАГТУ 2910
- КрасГАУ 345
- КрасГМУ 629
- КГПУ им. Астафьева 133
- КГТУ (СФУ) 567
- КГТЭИ (СФУ) 112
- КПК №2 177
- КубГТУ 138
- КубГУ 109
- КузГПА 182
- КузГТУ 789
- МГТУ им. Носова 369
- МГЭУ им. Сахарова 232
- МГЭК 249
- МГПУ 165
- МАИ 144
- МАДИ 151
- МГИУ 1179
- МГОУ 121
- МГСУ 331
- МГУ 273
- МГУКИ 101
- МГУПИ 225
- МГУПС (МИИТ) 637
- МГУТУ 122
- МТУСИ 179
- ХАИ 656
- ТПУ 455
- НИУ МЭИ 640
- НМСУ «Горный» 1701
- ХПИ 1534
- НТУУ «КПИ» 213
- НУК им.
 Макарова 543
Макарова 543 - НВ 1001
- НГАВТ 362
- НГАУ 411
- НГАСУ 817
- НГМУ 665
- НГПУ 214
- НГТУ 4610
- НГУ 1993
- НГУЭУ 499
- НИИ 201
- ОмГТУ 302
- ОмГУПС 230
- СПбПК №4 115
- ПГУПС 2489
- ПГПУ им. Короленко 296
- ПНТУ им. Кондратюка 120
- РАНХиГС 190
- РОАТ МИИТ 608
- РТА 245
- РГГМУ 117
- РГПУ им.
 Герцена 123
Герцена 123 - РГППУ 142
- РГСУ 162
- «МАТИ» — РГТУ 121
- РГУНиГ 260
- РЭУ им. Плеханова 123
- РГАТУ им. Соловьёва 219
- РязГМУ 125
- РГРТУ 666
- СамГТУ 131
- СПбГАСУ 315
- ИНЖЭКОН 328
- СПбГИПСР 136
- СПбГЛТУ им. Кирова 227
- СПбГМТУ 143
- СПбГПМУ 146
- СПбГПУ 1599
- СПбГТИ (ТУ) 293
- СПбГТУРП 236
- СПбГУ 578
- ГУАП 524
- СПбГУНиПТ 291
- СПбГУПТД 438
- СПбГУСЭ 226
- СПбГУТ 194
- СПГУТД 151
- СПбГУЭФ 145
- СПбГЭТУ «ЛЭТИ» 379
- ПИМаш 247
- НИУ ИТМО 531
- СГТУ им.
 Гагарина 114
Гагарина 114 - СахГУ 278
- СЗТУ 484
- СибАГС 249
- СибГАУ 462
- СибГИУ 1654
- СибГТУ 946
- СГУПС 1473
- СибГУТИ 2083
- СибУПК 377
- СФУ 2424
- СНАУ 567
- СумГУ 768
- ТРТУ 149
- ТОГУ 551
- ТГЭУ 325
- ТГУ (Томск) 276
- ТГПУ 181
- ТулГУ 553
- УкрГАЖТ 234
- УлГТУ 536
- УИПКПРО 123
- УрГПУ 195
- УГТУ-УПИ 758
- УГНТУ 570
- УГТУ 134
- ХГАЭП 138
- ХГАФК 110
- ХНАГХ 407
- ХНУВД 512
- ХНУ им.
 Каразина 305
Каразина 305 - ХНУРЭ 325
- ХНЭУ 495
- ЦПУ 157
- ЧитГУ 220
- ЮУрГУ 309
|
Навигация: Главная Случайная страница Обратная связь ТОП Интересно знать Избранные Топ: Марксистская теория происхождения государства: По мнению Маркса и Энгельса, в основе развития общества, происходящих в нем изменений лежит… Процедура выполнения команд. Рабочий цикл процессора: Функционирование процессора в основном состоит из повторяющихся рабочих циклов, каждый из которых соответствует… Проблема типологии научных революций: Глобальные научные революции и типы научной рациональности. Интересное: Подходы к решению темы фильма: Существует три основных типа исторического фильма, имеющих между собой много общего… Наиболее распространенные виды рака: Раковая опухоль — это самостоятельное новообразование, которое может возникнуть и от повышенного давления… Отражение на счетах бухгалтерского учета процесса приобретения: Процесс заготовления представляет систему экономических событий, включающих приобретение организацией у поставщиков сырья… Дисциплины: Автоматизация Антропология Археология Архитектура Аудит Биология Бухгалтерия Военная наука Генетика География Геология Демография Журналистика Зоология Иностранные языки Информатика Искусство История Кинематография Компьютеризация Кораблестроение Кулинария Культура Лексикология Лингвистика Литература Логика Маркетинг Математика Машиностроение Медицина Менеджмент Металлургия Метрология Механика Музыкология Науковедение Образование Охрана Труда Педагогика Политология Правоотношение Предпринимательство Приборостроение Программирование Производство Промышленность Психология Радиосвязь Религия Риторика Социология Спорт Стандартизация Статистика Строительство Теология Технологии Торговля Транспорт Фармакология Физика Физиология Философия Финансы Химия Хозяйство Черчение Экология Экономика Электроника Энергетика Юриспруденция |
⇐ ПредыдущаяСтр 13 из 120Следующая ⇒ Коэффициент избытка воздуха определяется газовым анализом проб продуктов сгорания, отбираемых из газоходов, с последующим расчетом по приводным ниже формулам. Коэффициент избытка воздуха указывает насколько больше количество подаваемого действительного объема воздуха, по сравнению с теоретически необходимым αт=Vв/V0. Азотная формула: α=1/(1–79/21*О2/N2). При прикидочных расчетах пользуются более простой приближенной формулой для определения α, легко получаемой из формулы азотной формулы. α=RO2 max/RO2 – углекислотная формула. Справедлива формула при отсутствии Q3, точность зависит от точности определения . При полном сгорании топлива объем подаваемого для горения воздуха приближенно можно считать равным объему сухих газов Vв= Vс.г., а процент неиспользованного кислорода — содержанию свободного кислорода в сухих газах О2 ΔVв= VО2. Тогда коэффициент избытка воздуха можно выразить как отношение процентного содержания кислорода в воздухе, подаваемом для горения, к проценту использованной части кислорода, что дает кислородную формулу в виде: α≈21/(21–О2). где О2 – процентное содержание кислорода в продуктах сгорания; 21 – процентное содержание кислорода в воздухе. Формула справедлива при полном сгорании тл. и без учета влажности тл. инче вводятся поправки.
Вопрос № 56 Коэффициент избытка воздуха и методы его определения В действительных условиях невозможно довести топливо до полного сгорания при теоретически необходимом объеме воздуха V0вследствие несовершенства перемешивания топлива с воздухом в большом топочном объеме за короткое время пребывания газов в нем (1—2 с). Поэтому для обеспечения достаточно полного сгорания топлива, удовлетворяющего экономическим показателям работы котлов, действительный объем воздуха всегда несколько больше теоретического. Отношение этих объемов называют коэффициентом избытка воздуха в продуктах сгорания: α=Vв/V°. Необходимый коэффициент избытка воздуха в топке αт зависит от сорта топлива, способа его сжигания и конструкции топочного устройства. Расчетный коэффициент αт устанавливается с учетом всех факторов согласно Нормам теплового расчета паровых котлов. Обычно его принимают для разных топлив в пределах: При сжигании твердых топлив……..1,15—1,25 При сжигании жидких топлив……..1,03—1,1 При сжигании газовых топлив. ……. 1,05—1,1 â избытка воздуха дает экономию расхода энергии на привод тягодутьевых машин и á КПД котла, однако его â ниже расчетного значения αт ведет к быстрому á недожога топлива и â экономичности котла. На электростанциях используют два метода определения этого показателя. Основным является метод прямого определения остаточного кислорода в потоке дымовых газов кислородомером. Пересчет процентного содержания кислорода на значение избытка воздуха производят по кислородной формуле. , где О2 – процентное содержание кислорода в продуктах сгорания; 21 – процентное содержание кислорода в воздухе. Эта формула справедлива, если отсутствует Q3 – химический недожог и минимальная влажность; Вторым достаточно широко применяемым методом определения избытка воздуха в продуктах сгорания является его расчет на основе нахождения процентного содержания сухих трехатомных газов RO2=CO2+SO2, где RO2=VRO2/Vс.г.*100. , где RO2 – текущий объем трехатомных газов; — объем трехатомных газов при α = 1, определяется на основе состава топлива. Справедлива формула при отсутствии Q3, точность зависит от точности определения Надежность определения коэффициента избытка воздуха а этим методом зависит от того, насколько точно известно для данного топлива значение RО2max (поскольку на электростанцию топливо поступает не всегда постоянного состава), а также от тщательности выполнения анализа отбираемых дымовых газов на содержание RO2. Азотная формула: α=1/(1–79/21*О2/N2).
Вопрос № 57 ⇐ Предыдущая891011121314151617Следующая ⇒ Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций… Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим… Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого… Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰)… |
Горение | ||||||||||||||||||||||
| Что такое горение? | ||||||||||||||||||||||
Горение происходит, когда топливо, чаще всего ископаемое, вступает в реакцию с кислородом воздуха с выделением тепла. Контролируя и регулируя некоторые газы в дымовой трубе или выхлопе, можно легко повысить эффективность сгорания, что экономит топливо и снижает расходы. Эффективность сгорания – это расчет того, насколько эффективно протекает процесс сгорания. Для достижения наивысшего уровня эффективности сгорания должно происходить полное сгорание. Полное сгорание происходит, когда вся энергия сжигаемого топлива извлекается и ни одно из соединений углерода и водорода не остается несгоревшим. Полное сгорание происходит, когда надлежащее количество топлива и воздуха (соотношение топливо/воздух) смешивается в течение необходимого времени при соответствующих условиях турбулентности и температуры. Хотя теоретически стехиометрическое сгорание обеспечивает идеальное соотношение топлива и воздуха, что снижает потери и извлекает всю энергию из топлива; в действительности стехиометрическое сгорание недостижимо из-за множества различных факторов. На практике для достижения полного сгорания необходимо увеличить количество воздуха, подаваемого в процесс горения, чтобы обеспечить сгорание всего топлива. Количество воздуха, которое необходимо добавить, чтобы обеспечить получение всей энергии, называется избыточным воздухом. В большинстве процессов горения во время реакций горения образуются некоторые дополнительные химические вещества. Некоторые из образующихся продуктов, таких как CO (монооксид углерода), NO (оксид азота), NO2 (диоксид азота), SO2 (диоксид серы), сажа и зола, должны быть сведены к минимуму и точно измерены. Агентство по охране окружающей среды установило специальные стандарты и правила для выбросов некоторых из этих продуктов, поскольку они вредны для окружающей среды. Анализ горения является жизненно важным шагом для правильной работы и управления любым процессом горения, чтобы получить максимальную эффективность сгорания с наименьшими выбросами загрязняющих веществ. | ||||||||||||||||||||||
| Цель сжигания | ||||||||||||||||||||||
Целью сжигания является получение энергии от сжигания топлива наиболее эффективным способом. Для достижения максимальной полноты сгорания необходимо сжигать весь топливный материал с наименьшими потерями. Чем эффективнее сжигается топливо и собирается энергия, тем дешевле становится процесс сжигания. | ||||||||||||||||||||||
Полное сгорание Полное сгорание происходит, когда извлекается 100% энергии топлива. Важно стремиться к полному сгоранию, чтобы сохранить топливо и повысить экономическую эффективность процесса сгорания. В камере сгорания должно быть достаточно воздуха для полного сгорания. Добавление избытка воздуха значительно снижает образование СО (окиси углерода), позволяя СО вступать в реакцию с О2. | ||||||||||||||||||||||
Стехиометрическое сжиганиеСтехиометрическое сгорание — это теоретическая точка, при которой соотношение топлива и воздуха идеально, так что происходит полное сгорание с идеальной эффективностью. Хотя стехиометрическое сжигание невозможно, во всех процессах сжигания стремятся максимизировать прибыль. Топливо В настоящее время в процессах сжигания топлива по всему миру используется множество видов топлива, наиболее распространенными из которых являются: уголь, масла (№ 2, № 4 и № 6), дизельное топливо, бензин, природный газ, пропан, коксовый газ и древесина. . Каждое топливо имеет различные химические характеристики, в том числе, среди прочего, уникальное соотношение C/h3 и теплотворную способность.
| ||||||||||||||||||||||
Эффект сжигания различных видов топливаУголь Существует множество разновидностей угля, используемых в процессах сжигания по всему миру; наиболее широко используются антрацит, битум, полубитум и бурый уголь. При сжигании угля образуется значительное количество двуокиси углерода, учитывая чрезвычайно высокое содержание углерода в угле; поскольку для сжигания углерода требуется больше кислорода, для сжигания угля требуется больше воздуха для горения, чем для сжигания других ископаемых видов топлива. В дополнение к выбросам двуокиси углерода при сжигании угля образуются некоторые другие загрязняющие вещества, включая NOx, двуокись серы (SO2), триоксид серы (SO3) и выбросы твердых частиц. Диоксид серы химически соединяется с водяным паром в воздухе, образуя слабую форму серной кислоты, которая является одной из основных причин кислотных дождей. МаслоНефтяное топливо в основном представляет собой смесь очень тяжелых углеводородов, содержание водорода в которых выше, чем в угле. В то же время нефть содержит меньше углерода, чем уголь, и поэтому для полного сгорания требуется меньше воздуха для горения. Следовательно, при сжигании нефти выделяется меньше углекислого газа, чем при сжигании угля, но больше углекислого газа, чем при сжигании природного газа. Большинство загрязняющих веществ, образующихся при сжигании угля, также являются побочным продуктом сжигания нефти. Природный газ Для сжигания природного газа требуется гораздо меньше воздуха из-за относительно низкого содержания углерода и большого количества водорода. При сжигании природного газа образуется меньше парниковых газов, которые считаются одним из основных источников глобального потепления. В эквивалентных количествах при сжигании природного газа образуется примерно на 30% меньше углекислого газа, чем при сжигании нефти, и на 45% меньше углекислого газа, чем при сжигании угля. В дополнение к выбросам двуокиси углерода при сжигании газа образуются выбросы NOx, тогда как выбросы двуокиси серы (SO2) и твердых частиц незначительны. Другие виды топлива, включая древесину, дизельное топливо, бензин, пропан, бутан, биотопливо, такое как этанол и т. д., обладают собственными свойствами горения, которые влияют на эффективность сгорания и выбросы в процессе.
| ||||||||||||||||||||||
Поток воздуха | ||||||||||||||||||||||
Поддержание надлежащего потока воздуха во время горения имеет основополагающее значение для обеспечения безопасного и полного сгорания. Общий воздушный поток включает воздух для горения, инфильтрационный воздух и разбавляющий воздух. Воздух для горения Время, температура и турбулентностьПроцесс горения сильно зависит от времени, температуры и турбулентности. Время важно для сгорания, потому что, если топливу не дать достаточно времени для сгорания, в топливе останется значительное количество энергии. С другой стороны, слишком долгое горение приведет к очень длинному пламени, что может быть следствием плохого смешивания. Правильный баланс времени и смешивания обеспечит полное сгорание, сведет к минимуму воздействие пламени (опасность обслуживания котла) и повысит безопасность горения. Кроме того, правильно контролируемый процесс сгорания направлен на обеспечение максимальной эффективности сгорания при сохранении низкого уровня выбросов вредных газов. Избыточный воздух Для обеспечения полного сгорания в камерах сгорания используется избыток воздуха. Расчет избытка воздуха Как обсуждалось ранее, в стехиометрических (теоретических) условиях количество кислорода в воздухе, используемом для горения, полностью расходуется в процессе горения. Для расчета избытка воздуха обычно используется следующая формула: | ||||||||||||||||||||||
| ||||||||||||||||||||||
Что такое черновик? Давление газов в дымовой трубе необходимо тщательно контролировать, чтобы гарантировать, что все газы сгорания удаляются из зоны сгорания с правильной скоростью. Контроль тяги важен не только для повышения эффективности сгорания, но и для поддержания безопасных условий. Низкое давление тяги создает накопление высокотоксичных газов, таких как окись углерода и взрывоопасные газы. Эти накопления могут происходить в камере сгорания или даже в помещении с вентиляцией, создавая риск травм и смерти. И наоборот, чрезвычайно высокое давление тяги может вызвать нежелательную турбулентность в системе, препятствующую полному сгоранию. Нежелательное высокое давление тяги имеет тенденцию повреждать камеру сгорания и материал теплообменника, вызывая удары пламени
| ||||||||||||||||||||||
Что такое котел? Котел представляет собой закрытый сосуд, в котором вода нагревается и циркулирует в виде горячей воды, пара или перегретого пара с целью нагревания, питания и/или производства электроэнергии. | ||||||||||||||||||||||
| ||||||||||||||||||||||
Конденсационные котлы Конденсационный котел сохраняет энергию за счет использования теплообменников, предназначенных для удаления дополнительной энергии из газов сгорания перед выходом из дымовой трубы. | ||||||||||||||||||||||
СЛЕДУЮЩИЙ>> | ||||||||||||||||||||||
air-fuel_ratio
Соотношение воздух-топливо ( AFR ) — это массовое отношение воздуха к топливу, присутствующее во время сгорания. Когда все топливо смешивается со всем свободным кислородом, как правило, в камере сгорания автомобиля,
смесь химически сбалансирована, и этот AFR называется стехиометрической смесью (часто сокращается до стоич ). AFR является важной мерой для предотвращения загрязнения окружающей среды и настройки производительности. Лямбда (λ) — это альтернативный способ представления AFR.
Лямбда (λ) — это альтернативный способ представления AFR.
В промышленных нагревателях, парогенераторах электростанций и больших газовых турбинах более распространенным термином является процентов избыточного воздуха для горения . Например, 15-процентный избыток воздуха для горения означает, что используется на 15 процентов больше требуемого стехиометрического количества воздуха.
Смесь – это рабочая точка, которую современные системы управления двигателем, использующие впрыск топлива, пытаются достичь в крейсерских ситуациях с малой нагрузкой. Для бензинового топлива стехиометрическая воздушно-топливная смесь примерно в 14,7 раз превышает массу воздуха в топливе. Любая смесь менее 14,7 к 1 считается богатой смесью, а более 14,7 к 1 — обедненной смесью при идеальном (идеальном) «испытательном» топливе (бензин, состоящий только из н-гептана и изооктана). На самом деле большинство видов топлива состоят из комбинации гептана, октана, нескольких других алканов, а также присадок, включая детергенты, и, возможно, оксигенаторов, таких как МТБЭ (метил-трет-бутиловый эфир) или этанол/метанол. Все эти соединения изменяют стехиометрическое соотношение, при этом большинство добавок снижают это соотношение (оксигенаторы привносят в процесс горения дополнительный кислород в жидкой форме, который высвобождается во время горения; для топлива с содержанием МТБЭ стехиометрическое соотношение может быть низким). как 14.1:1). Транспортные средства, использующие кислородный датчик (датчики) или другой контур обратной связи для управления соотношением топлива и воздуха (обычно путем управления объемом топлива), обычно автоматически компенсируют это изменение стехиометрического расхода топлива путем измерения состава выхлопных газов, в то время как транспортные средства без таких средств управления (например, большинство мотоциклов до недавнего времени и автомобили, выпущенные до середины 19-го века).80-х годов) могут возникнуть трудности с работой с некоторыми специализированными смесями топлива (особенно зимними видами топлива, используемыми в некоторых регионах), и может потребоваться повторная впрыскивание (или иное изменение коэффициента заправки), чтобы компенсировать использование специальных специализированных топливных смесей.
Все эти соединения изменяют стехиометрическое соотношение, при этом большинство добавок снижают это соотношение (оксигенаторы привносят в процесс горения дополнительный кислород в жидкой форме, который высвобождается во время горения; для топлива с содержанием МТБЭ стехиометрическое соотношение может быть низким). как 14.1:1). Транспортные средства, использующие кислородный датчик (датчики) или другой контур обратной связи для управления соотношением топлива и воздуха (обычно путем управления объемом топлива), обычно автоматически компенсируют это изменение стехиометрического расхода топлива путем измерения состава выхлопных газов, в то время как транспортные средства без таких средств управления (например, большинство мотоциклов до недавнего времени и автомобили, выпущенные до середины 19-го века).80-х годов) могут возникнуть трудности с работой с некоторыми специализированными смесями топлива (особенно зимними видами топлива, используемыми в некоторых регионах), и может потребоваться повторная впрыскивание (или иное изменение коэффициента заправки), чтобы компенсировать использование специальных специализированных топливных смесей.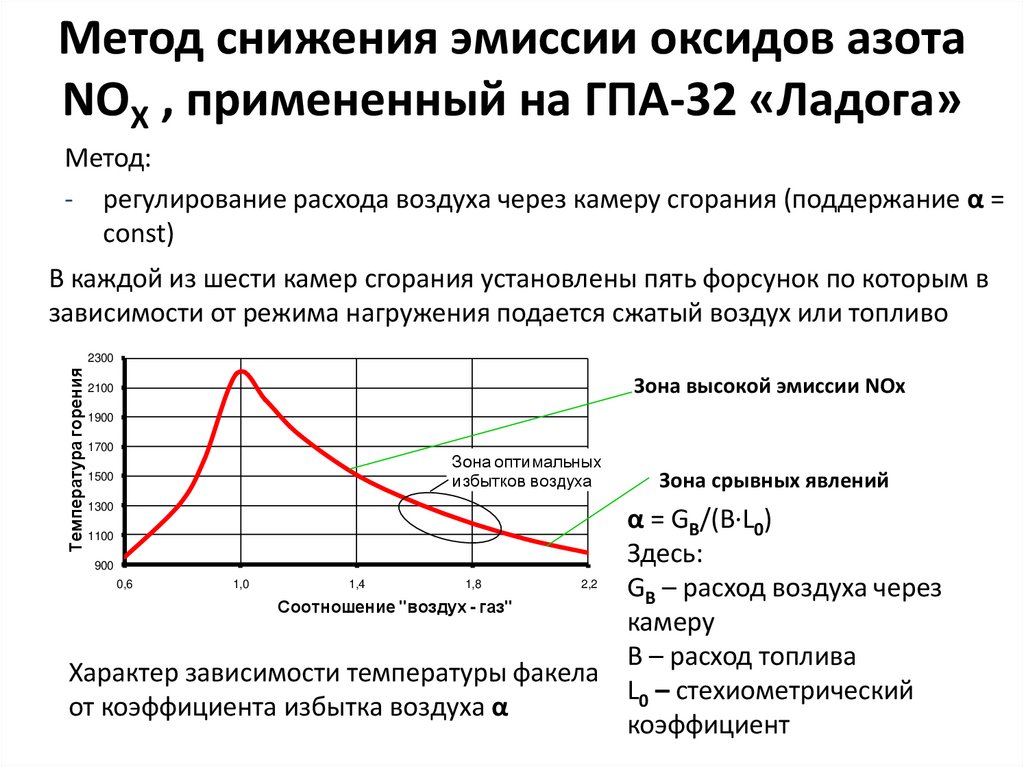 Производители транспортных средств не предоставляют средства изменения предопределенных топливных карт, что делает такие изменения невозможными без замены стандартного ЭБУ настраиваемой системой. Транспортные средства, использующие кислородные датчики, позволяют контролировать соотношение воздух-топливо с помощью измерителя соотношения воздух-топливо.
Производители транспортных средств не предоставляют средства изменения предопределенных топливных карт, что делает такие изменения невозможными без замены стандартного ЭБУ настраиваемой системой. Транспортные средства, использующие кислородные датчики, позволяют контролировать соотношение воздух-топливо с помощью измерителя соотношения воздух-топливо.
Бедные смеси производят более холодные дымовые газы, чем стехиометрические смеси, главным образом из-за чрезмерного разбавления неизрасходованным кислородом и связанным с ним азотом. Богатые смеси также производят более холодные газы сгорания, чем стехиометрическая смесь, в первую очередь из-за избыточного количества углерода, который окисляется с образованием монооксида углерода, а не диоксида углерода. Химическая реакция окисления углерода с образованием монооксида углерода выделяет значительно меньше тепла, чем аналогичная реакция с образованием диоксида углерода. (Окись углерода сохраняет значительную потенциальную химическую энергию.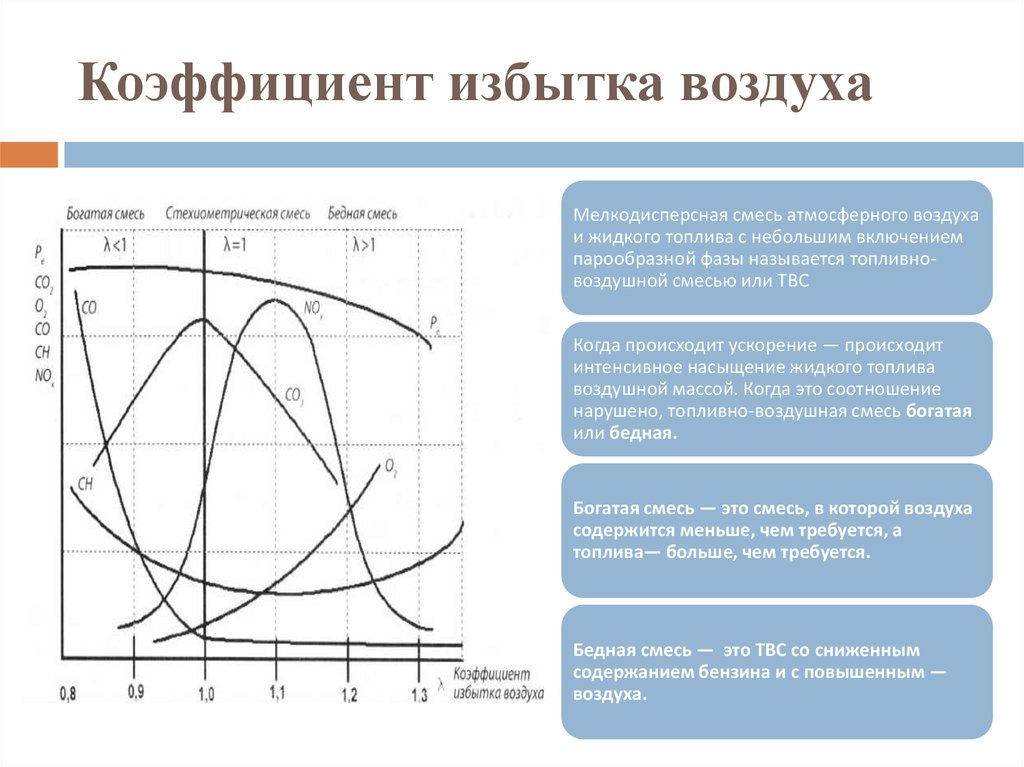 Она сама по себе является топливом, а двуокись углерода — нет.) Бедные и богатые смеси при потреблении в двигателе внутреннего сгорания производят меньше энергии, чем стехиометрическая смесь. Точно так же бедные смеси и богатые смеси дают более низкую эффективность использования топлива, чем лучшая смесь. (Смесь для наилучшей топливной экономичности немного отличается от стехиометрической смеси.)
Она сама по себе является топливом, а двуокись углерода — нет.) Бедные и богатые смеси при потреблении в двигателе внутреннего сгорания производят меньше энергии, чем стехиометрическая смесь. Точно так же бедные смеси и богатые смеси дают более низкую эффективность использования топлива, чем лучшая смесь. (Смесь для наилучшей топливной экономичности немного отличается от стехиометрической смеси.)
Дополнительные рекомендуемые знания
Содержимое
|
Сводка
Теоретически стехиометрическая смесь содержит достаточно воздуха, чтобы полностью сжечь доступное топливо. На практике это никогда полностью не достигается, в первую очередь из-за очень короткого времени, доступного в двигателе внутреннего сгорания для каждого цикла сгорания. Большая часть процесса сгорания завершается примерно за 4-5 миллисекунд при частоте вращения двигателя 6000 об/мин. Это время, которое проходит с момента зажигания искры до практически полного сгорания топливно-воздушной смеси после поворота коленчатого вала примерно на 80 градусов.
Большая часть процесса сгорания завершается примерно за 4-5 миллисекунд при частоте вращения двигателя 6000 об/мин. Это время, которое проходит с момента зажигания искры до практически полного сгорания топливно-воздушной смеси после поворота коленчатого вала примерно на 80 градусов.
Каталитические нейтрализаторы лучше всего работают, когда выхлопные газы, проходящие через них, показывают, что произошло почти идеальное сгорание.
Стехиометрическая смесь, к сожалению, очень сильно горит и может повредить компоненты двигателя, если двигатель находится под высокой нагрузкой на этой топливно-воздушной смеси. Из-за высоких температур этой смеси возможна детонация топливно-воздушной смеси вскоре после максимального давления в цилиндре при высокой нагрузке (так называемая детонация или стук). Детонация может привести к серьезному повреждению двигателя, так как неконтролируемое сгорание топливно-воздушной смеси может создать очень высокое давление в цилиндре. Как следствие, стехиометрические смеси используются только в условиях легкой нагрузки.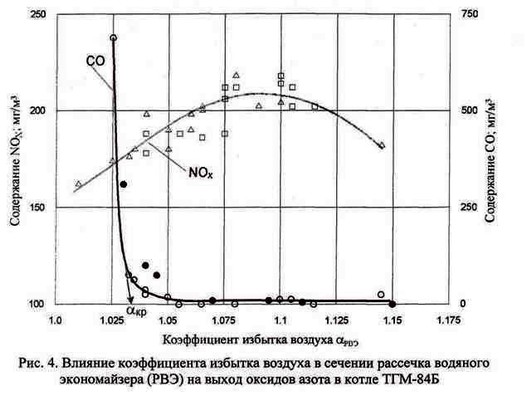 В условиях ускорения и высоких нагрузок используется более богатая смесь (более низкое соотношение воздух-топливо) для получения более холодных продуктов сгорания и тем самым предотвращения детонации и перегрева головки блока цилиндров.
В условиях ускорения и высоких нагрузок используется более богатая смесь (более низкое соотношение воздух-топливо) для получения более холодных продуктов сгорания и тем самым предотвращения детонации и перегрева головки блока цилиндров.
В типичной горелке для сжигания воздуха в природном газе используется стратегия двойного пересечения пределов для обеспечения контроля соотношения. (Этот метод использовался во время Второй мировой войны). Стратегия включает в себя добавление обратной связи по противоположному потоку в ограничивающее регулирование соответствующего газа (воздуха или топлива). Это обеспечивает регулирование соотношения в допустимых пределах.
Другие используемые термины
Существуют и другие термины, обычно используемые при обсуждении смеси воздуха и топлива в двигателях внутреннего сгорания. Однако слово «стоич» также известно как сленговое слово.
АФР
Соотношение воздух-топливо является наиболее распространенным справочным термином, используемым для смесей в двигателях внутреннего сгорания. Это отношение массы воздуха к массе топлива в топливно-воздушной смеси в любой момент времени.
Это отношение массы воздуха к массе топлива в топливно-воздушной смеси в любой момент времени.
Для чистого октана стехиометрическое соотношение смеси составляет примерно 14,7:1 или λ точно равно 1,00.
В безнаддувных двигателях с октановым числом максимальная мощность часто достигается при AFR в диапазоне от 12,5 до 13,3:1 или λ от 0,85 до 0,9.0.
ФАР
Соотношение топлива и воздуха часто используется в государственных исследованиях двигателей внутреннего сгорания и относится к соотношению топлива к воздуху, оно равно 1/AFR.
Лямбда
Большинство практичных устройств AFR фактически измеряют количество остаточного кислорода (для бедных смесей) или несгоревших углеводородов (для богатых смесей) в выхлопных газах. Лямбда (λ) — это мера того, насколько далека эта смесь от стехиометрии. Лямбда 1,0 соответствует стехиометрии, богатые смеси меньше 1,0, а бедные смеси больше 1,0.
Существует прямая связь между лямбдой и AFR. Чтобы рассчитать AFR по заданному значению лямбда, умножьте измеренное значение лямбда на стехиометрическое значение AFR для этого топлива. В качестве альтернативы, чтобы восстановить лямбда из AFR, разделите AFR на стехиометрический AFR для этого топлива. Это последнее уравнение часто используется в качестве определения лямбда:
Чтобы рассчитать AFR по заданному значению лямбда, умножьте измеренное значение лямбда на стехиометрическое значение AFR для этого топлива. В качестве альтернативы, чтобы восстановить лямбда из AFR, разделите AFR на стехиометрический AFR для этого топлива. Это последнее уравнение часто используется в качестве определения лямбда:
Поскольку состав распространенных видов топлива меняется в зависимости от сезона и поскольку многие современные автомобили могут работать на разных видах топлива, при настройке имеет смысл говорить о значениях лямбда, а не о AFR.
Коэффициент эквивалентности
Коэффициент эквивалентности системы определяется как отношение отношения топлива к окислителю к стехиометрическому соотношению топлива к окислителю. Математически,
где m представляет массу, n представляет количество молей, суффикс s t обозначает стехиометрические условия.
ТЛАЛИ
отношение топлива к окислителю заключается в том, что оно не имеет такой же зависимости, как отношение топлива к окислителю, от используемых агрегатов. Например, соотношение топлива и окислителя, основанное на массе топлива и окислителя, отличается от соотношения, определяемого на основе количества молей. Это не относится к коэффициенту эквивалентности. Следующий пример может помочь прояснить этот момент. Рассмотрим смесь одного моля этана ( C 2 H 6 ) и один моль кислорода ( O 2 ).
Например, соотношение топлива и окислителя, основанное на массе топлива и окислителя, отличается от соотношения, определяемого на основе количества молей. Это не относится к коэффициенту эквивалентности. Следующий пример может помочь прояснить этот момент. Рассмотрим смесь одного моля этана ( C 2 H 6 ) и один моль кислорода ( O 2 ).
- отношение топлива к окислителю в этой смеси в пересчете на массу топлива и воздуха равно
- отношение топлива к окислителю в этой смеси в пересчете на количество молей топлива и воздуха равно
Ясно, что эти два значения не равный. Чтобы сравнить его с коэффициентом эквивалентности, нам нужно определить соотношение топлива и окислителя смеси этана и кислорода. Для этого нужно рассмотреть стехиометрическую реакцию этана и кислорода,
Это дает,
Таким образом, мы можем определить коэффициент эквивалентности данной смеси как,
или аналогичный,
Другим преимуществом использования отношения эквивалентности является то, что отношения больше единицы всегда представляют избыток топлива в топливно-окислительной смеси, чем то, что требуется для полного сгорания (стехиометрическая реакция), независимо от используемых топлива и окислителя. . В то время как отношения менее 1 представляют собой дефицит топлива или, что эквивалентно, избыток окислителя в смеси. Это не так, если используется соотношение топлива и окислителя, которое будет принимать разные значения для разных смесей.
. В то время как отношения менее 1 представляют собой дефицит топлива или, что эквивалентно, избыток окислителя в смеси. Это не так, если используется соотношение топлива и окислителя, которое будет принимать разные значения для разных смесей.
Следует отметить, что коэффициент эквивалентности связан с λ (определено ранее) следующим образом:
См. также
- Адиабатическая температура пламени
- Кислородный датчик
- Измеритель соотношения воздух-топливо
- Датчик массового расхода воздуха
- Датчик массового расхода
- Расходомер воздуха
- Широкополосный O2
- Бережливое сжигание
Калькулятор AFR | Калькулятор соотношения воздух-топливо
Создано Габриэлой Диас
Отзыв от Ханны Памулы, кандидата наук и Стивена Вудинга
Последнее обновление: 03 октября 2022 г.
Содержание:- Что такое соотношение воздух-топливо (AFR)?
- Соотношение воздух-топливо обычных видов топлива
- Как рассчитать стехиометрическое соотношение воздух-топливо
- Как пользоваться калькулятором AFR?
Калькулятор AFR (соотношение воздух-топливо) даст вам соотношение воздуха к топливу и массу воздуха, необходимого для его полного сгорания .
Сгорание — это процесс, присутствующий в различных технологиях, таких как нагревательные устройства , двигатели внутреннего сгорания, газовые турбины, ракеты и т. д., где важным параметром является AFR.
Продолжайте читать, чтобы узнать о , что такое соотношение воздух-топливо , AFR некоторых видов топлива и , как рассчитать стехиометрическое соотношение воздух-топливо для ископаемого топлива.
Что такое соотношение воздух-топливо (AFR)?
Как выяснил Лавуазье, кислород является ключевым веществом в любом процессе горения, и оказывается, что для разных видов топлива количество необходимого кислорода тоже разное.
Эта конкретная потребность в кислороде выражается параметром, известным как соотношение воздух-топливо (AFR) , указывающим количество воздуха, необходимое для достижения полного сгорания заданного количества топлива 🔥.
AFR часто выражается в массе, как масса воздуха, деленная на массу топлива :
AFR=massairmassfuel\quad AFR= \dfrac{mass_{air}}{mass_{fuel}}AFR=massfuelmassair
Эта формула расчета соотношения воздух-топливо также может быть выражена в молярных единицах отношение и молярная масса каждого вещества как:
AFR=molesair×Mairmolesfuel×Mfuel\quad AFR= \dfrac{moles_{air}\times M_{air}}{moles_{fuel}\times M_{fuel}}AFR =molesfuel×Mfuelmolesair×Mair
или…
AFR=AFR‾×MairMfuel\quad AFR= \overline{AFR}\times \dfrac{M_{air}}{M_{fuel} }AFR=AFR×MfuelMair
где:
- AFRAFRAFR – соотношение воздух-топливо по массе;
- AFR‾\overline{AFR}AFR – соотношение воздух-топливо на молярной основе; и
- MairM_{air}Mair и MfuelM_{fuel}Mfuel – соответствующие молярные массы.
🙋 Если вы не совсем уверены, что такое молярное соотношение или как его рассчитать, мы рекомендуем проверить калькулятор молярного отношения , чтобы узнать больше об этом!
Соотношение воздух-топливо обычных видов топлива
От печи в наших домах до ракет, покидающих Землю, мы окружены различными приборами и оборудованием, которые включают процесс горения как часть своей функциональной системы, и все они используют определенное топливо . Например, природный газ , используемый в печах, системах отопления и электростанциях 🏭; бензин и дизель , в основном используются для автомобилей, автобусов и других транспортных средств 🚗,; авиационное турбинное топливо (ATF) для самолетов ✈ или жидкий водород в качестве ракетного топлива 🚀.
Например, природный газ , используемый в печах, системах отопления и электростанциях 🏭; бензин и дизель , в основном используются для автомобилей, автобусов и других транспортных средств 🚗,; авиационное турбинное топливо (ATF) для самолетов ✈ или жидкий водород в качестве ракетного топлива 🚀.
Вот некоторые соотношения воздух-топливо для наиболее распространенных углеводородов виды топлива :
Топливо | Формула | АФР (масса) | AFR (молярная) | Молярная масса (г/моль) |
|---|---|---|---|---|
Метан | Ч 4 | 17. | 9,52 | 16.04 |
Этан | С 2 Н 6 | 16,95 | 16,66 | 30.07 |
Пропан | С 3 Н 8 | 15,64 | 23,80 | 44.09 |
Бутан | С 4 Н 10 | 15,42 | 30,94 | 58.12 |
Пентан | С 5 Н 12 | 15,29 | 38. | 72,15 |
Октан | С 8 Н 18 | 15.09 | 59,50 | 114,23 |
Дизель | С 12 Н 23 | 14,6 | 84,49 | 167,31 |
Водород | Н 2 | 34,21 | 2,38 | 2,02 |
💡 Знаете ли вы, что природный газ в основном состоит из метана (CH 4 ) , примерно на 80-90%?
Как рассчитать стехиометрическое соотношение воздух-топливо
Минимальное количество воздуха, необходимое для полного сгорания, известно как теоретический или стехиометрический воздух . Это количество воздуха, используемого при расчете стехиометрического соотношения воздух-топливо.
Это количество воздуха, используемого при расчете стехиометрического соотношения воздух-топливо.
Общая формула полного сгорания углеводородного топлива с теоретическим воздухом:
CαHβ+a(O2+3,76N2)⟶bCO2+ch3O+dN2\text C_\alpha \text H_\beta + a(\text O_2 + 3.76 \text N_2) \longrightarrow b\text C\text O_2 + c\text H_2\text O + d\text N_2CαHβ+a(O2+3.76N2)⟶bCO2+ch3O+ дН2
На левой части реакции имеем:
- Реагенты горения, которыми являются углеводородное топливо и кислород .
- Общая формула углеводородного топлива представлена в виде CαHβ\text C_\alpha \text H_\betaCαHβ.
- Где нижние индексы α\alphaα и β\betaβ указывают на соответствующее число атомов углерода и водорода .
- Воздух для горения a(O2+3,76N2)a(\text O_2 + 3,76\text N_2)a(O2+3,76N2), при условии, что воздух состоит из 21% кислорода и 79% азота .

- Здесь коэффициент aaa представляет количество молей воздуха, необходимое для уравновешивания реакции горения.
А на правая часть реакции :
- Здесь находим продукты полного сгорания: углекислый газ (CO 2 ) , вода (H 2 O 1 и азот (N 2 ) . Обратите внимание, что для теоретического воздуха существует несвободного кислорода (O 2 ) .
- Коэффициенты продуктов сгорания bbb, ccc и ddd уравновешивают уравнение.
Коэффициенты , уравновешивающие химическую реакцию , можно получить через число атомов углерода (α\alphaα) и водорода (β\betaβ) конкретного топлива, присвоив следующие значения:
б=αб=\alphab=α
c=β2c=\dfrac{{\beta}}{2}c=2β
а=α+β4a=\alpha+\dfrac{{\beta}}{4}a=α+4β
d=3,76×(α+β4)d=3,76 \times \bigg(\alpha+\dfrac{{\beta}}{4}\bigg)d=3,76×(α+4β)
Вы можете проверить наш калькулятор реакции горения и узнать больше о том, как сбалансировать реакцию горения ⚗
Зная их, мы можем рассчитать количество молей воздуха для горения и молей топлива и соотнести их с помощью уравнения AFR показано ранее.
В определенных случаях, когда молекулярная формула топлива неизвестна, ее можно получить путем расчета анализа горения. Как только молекулярная формула известна, процедура балансировки реакции горения такая же, как указано выше.
Как пользоваться калькулятором AFR?
Чтобы использовать калькулятор AFR, выполните следующие действия:
Выберите одно из веществ из списка видов топлива .
После выбора калькулятор покажет соотношение воздух-топливо (AFR) для этого вещества.
Например, при выборе метана (CH 4 ) калькулятор покажет 17,19:1 , что означает, что для сгорания каждой единицы массы метана (т. е. 1 кг) требуется 17,19на его полное сгорание потребуется единица массы воздуха (т. е. 17,19 кг).
В разделе Масса воздуха и топлива введите массу топлива или воздуха, и калькулятор выдаст массу другого вещества.



 ст.
ст.
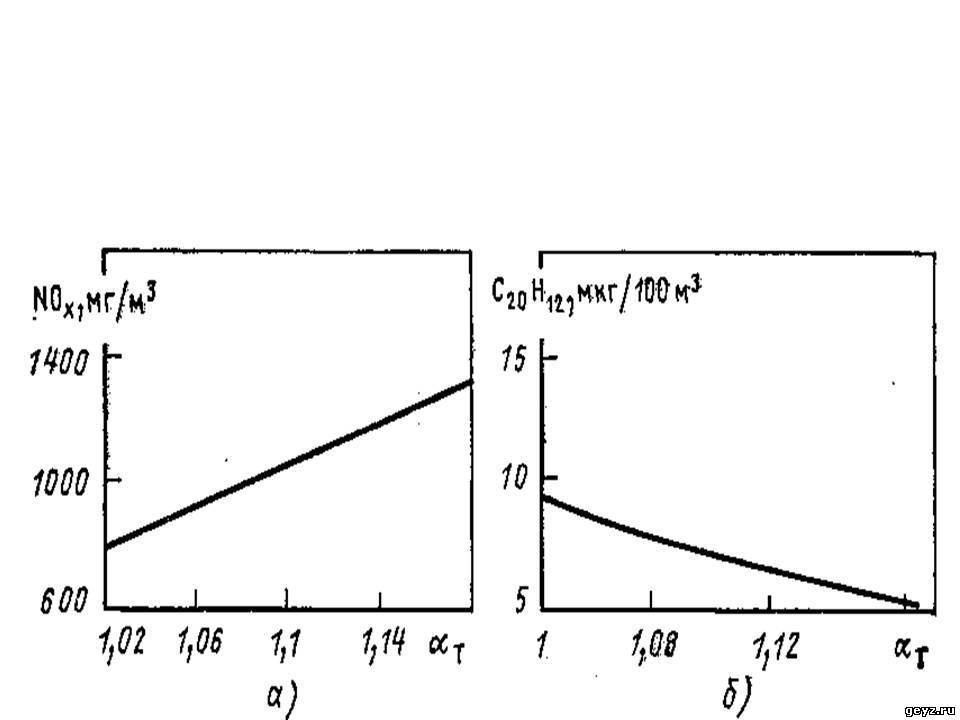 ..
..

 Высокореакционное твердое топливо, отличающееся большим выходом летучих веществ, легче воспламеняется и быстрее сгорает, поэтому нуждается в меньшем избытке воздуха, чем топливо с малым выходом летучих. Эффективное перемешивание топлива с воздухом достигается в газовоздушных смесях, поэтому сжигание мазута и газового топлива требует наименьшего избытка воздуха. Разный избыток воздуха нужен при сжигании одного и того же топлива, но в разных топочных устройствах (например, в прямоточной или вихревой топочной камере), отличающихся эффективностью перемешивания.
Высокореакционное твердое топливо, отличающееся большим выходом летучих веществ, легче воспламеняется и быстрее сгорает, поэтому нуждается в меньшем избытке воздуха, чем топливо с малым выходом летучих. Эффективное перемешивание топлива с воздухом достигается в газовоздушных смесях, поэтому сжигание мазута и газового топлива требует наименьшего избытка воздуха. Разный избыток воздуха нужен при сжигании одного и того же топлива, но в разных топочных устройствах (например, в прямоточной или вихревой топочной камере), отличающихся эффективностью перемешивания.

 Тепло, выделяемое при сжигании ископаемого топлива, используется в работе такого оборудования, как котлы, печи, печи и двигатели. Наряду с теплом в качестве побочных продуктов экзотермической реакции образуются CO2 (двуокись углерода) и h3O (вода).
Тепло, выделяемое при сжигании ископаемого топлива, используется в работе такого оборудования, как котлы, печи, печи и двигатели. Наряду с теплом в качестве побочных продуктов экзотермической реакции образуются CO2 (двуокись углерода) и h3O (вода).  Потери тепла неизбежны, что делает невозможным 100% КПД.
Потери тепла неизбежны, что делает невозможным 100% КПД.
 Чем меньше CO остается в дымовых газах, тем ближе к полному сгоранию становится реакция. Это связано с тем, что токсичный газ окись углерода (СО) по-прежнему содержит очень значительное количество энергии, которое необходимо полностью сжечь.
Чем меньше CO остается в дымовых газах, тем ближе к полному сгоранию становится реакция. Это связано с тем, что токсичный газ окись углерода (СО) по-прежнему содержит очень значительное количество энергии, которое необходимо полностью сжечь. Количество воздуха для горения, необходимое для полного сжигания конкретного топлива, будет зависеть от этих характеристик, особенно от отношения C/h3. Чем выше содержание углерода в топливе, тем больше воздуха требуется для полного сгорания. При контроле эффективности процесса горения важно знать, какое топливо сжигается, так как эта информация поможет не только определить оптимальные условия работы котла, но и максимизировать КПД котла.
Количество воздуха для горения, необходимое для полного сжигания конкретного топлива, будет зависеть от этих характеристик, особенно от отношения C/h3. Чем выше содержание углерода в топливе, тем больше воздуха требуется для полного сгорания. При контроле эффективности процесса горения важно знать, какое топливо сжигается, так как эта информация поможет не только определить оптимальные условия работы котла, но и максимизировать КПД котла.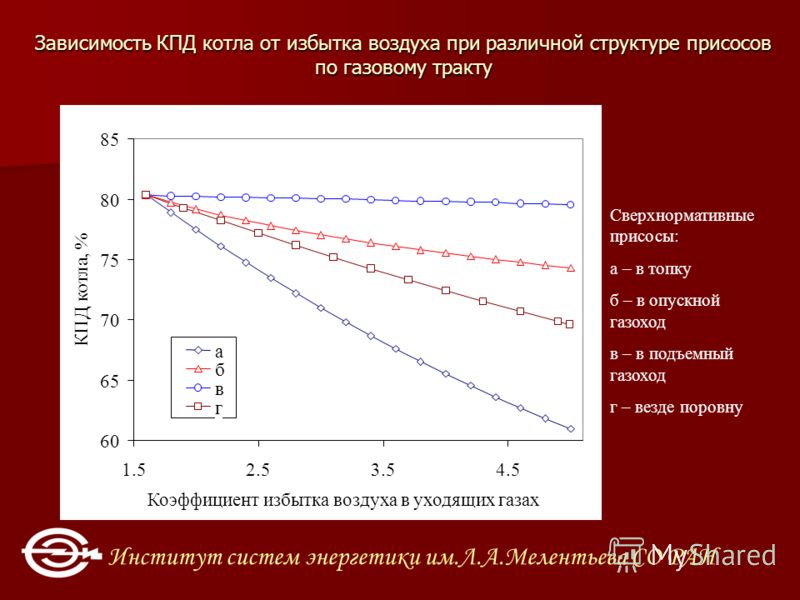
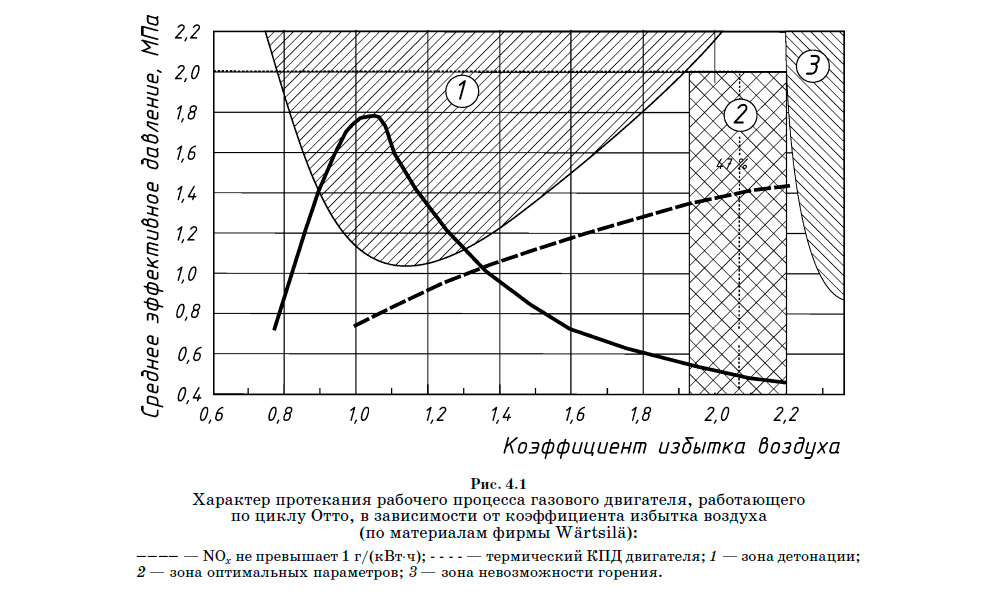 Сжигание природного газа чище, чем сжигание нефти и угля. Когда газ сжигается при недостаточном количестве воздуха для горения, могут образовываться некоторые летучие углеводороды, которые могут представлять угрозу безопасности; следует соблюдать осторожность, чтобы избежать опасных условий.
Сжигание природного газа чище, чем сжигание нефти и угля. Когда газ сжигается при недостаточном количестве воздуха для горения, могут образовываться некоторые летучие углеводороды, которые могут представлять угрозу безопасности; следует соблюдать осторожность, чтобы избежать опасных условий.
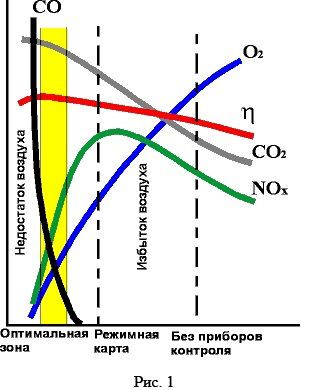 Различают два вида разбавления воздуха: естественное и индуцированное (искусственно созданное).
Различают два вида разбавления воздуха: естественное и индуцированное (искусственно созданное). Избыток воздуха увеличивает количество кислорода и азота, попадающих в пламя, увеличивая вероятность того, что кислород найдет топливо и прореагирует с ним. Добавление избыточного воздуха также увеличивает турбулентность, что увеличивает перемешивание в камере сгорания. Повышенное смешивание воздуха и топлива еще больше повысит эффективность сгорания, давая этим компонентам больше шансов вступить в реакцию. Чем больше избыточного воздуха поступает в камеру сгорания, тем больше топлива сгорает, пока, наконец, не достигнет полного сгорания. Большее количество избыточного воздуха создает меньшее количество CO, но также вызывает большие потери тепла. Поскольку уровни как CO, так и потерь тепла влияют на эффективность сгорания, важно контролировать и контролировать избыток воздуха и уровни CO, чтобы обеспечить максимально возможную эффективность сгорания.
Избыток воздуха увеличивает количество кислорода и азота, попадающих в пламя, увеличивая вероятность того, что кислород найдет топливо и прореагирует с ним. Добавление избыточного воздуха также увеличивает турбулентность, что увеличивает перемешивание в камере сгорания. Повышенное смешивание воздуха и топлива еще больше повысит эффективность сгорания, давая этим компонентам больше шансов вступить в реакцию. Чем больше избыточного воздуха поступает в камеру сгорания, тем больше топлива сгорает, пока, наконец, не достигнет полного сгорания. Большее количество избыточного воздуха создает меньшее количество CO, но также вызывает большие потери тепла. Поскольку уровни как CO, так и потерь тепла влияют на эффективность сгорания, важно контролировать и контролировать избыток воздуха и уровни CO, чтобы обеспечить максимально возможную эффективность сгорания.  Следовательно, измеряя количество кислорода в выхлопных газах, выходящих из дымовой трубы, мы должны быть в состоянии рассчитать процент избыточного воздуха, подаваемого в процесс.
Следовательно, измеряя количество кислорода в выхлопных газах, выходящих из дымовой трубы, мы должны быть в состоянии рассчитать процент избыточного воздуха, подаваемого в процесс. Это давление тяги может быть положительным или отрицательным в зависимости от конструкции котла; В промышленности чаще всего используются котлы с естественной тягой, уравновешивающей тягой и котлы с принудительной тягой.
Это давление тяги может быть положительным или отрицательным в зависимости от конструкции котла; В промышленности чаще всего используются котлы с естественной тягой, уравновешивающей тягой и котлы с принудительной тягой. Топка котла — это место, где топливо и воздух вводятся для сжигания; топливно-воздушные смеси обычно подаются в топку с помощью горелок, в которых образуется пламя. Образовавшиеся горячие газы проходят через серию теплообменников, где тепло передается воде, протекающей через них. В конечном итоге продукты сгорания выбрасываются в атмосферу через дымовую трубу выхлопной части котла.
Топка котла — это место, где топливо и воздух вводятся для сжигания; топливно-воздушные смеси обычно подаются в топку с помощью горелок, в которых образуется пламя. Образовавшиеся горячие газы проходят через серию теплообменников, где тепло передается воде, протекающей через них. В конечном итоге продукты сгорания выбрасываются в атмосферу через дымовую трубу выхлопной части котла. Дымовые газы, образующиеся в конденсационных котлах, имеют гораздо более низкую температуру, чем в неконденсационных котлах, поскольку водяной пар в дымовых газах конденсируется, высвобождая скрытую теплоту и повышая эффективность котла. Конденсационные котлы имеют КПД 9.5 % или более по сравнению с обычными 70–80 % для неконденсационных котлов.
Дымовые газы, образующиеся в конденсационных котлах, имеют гораздо более низкую температуру, чем в неконденсационных котлах, поскольку водяной пар в дымовых газах конденсируется, высвобождая скрытую теплоту и повышая эффективность котла. Конденсационные котлы имеют КПД 9.5 % или более по сравнению с обычными 70–80 % для неконденсационных котлов. 19
19 08
08