Проверка, корректировка плотности электролита в аккумуляторе, ЭДС
По плотности электролита судят о степени заряженности автомобильного аккумулятора. Чем ниже плотность электролита, тем более аккумулятор разряжен. Уменьшение плотности электролита на 0,01 г/см3 по сравнению с первоначальной означает, что аккумулятор разрядился примерно на 6%.
Проверка и корректировка плотности электролита в аккумуляторе, проверка ЭДС и напряжения автомобильного аккумулятора.
Информацию о плотности электролита, а значит и о степени заряженности аккумуляторной батареи, можно получить при проверке плотности электролита ареометром или плотномером. Трубку ареометра опустите в аккумулятор и грушей наберите в нее электролит до тех пор, пока поплавок не всплывет. Деление, до которого погрузился поплавок, покажет плотность электролита.
Старайтесь держать ареометр так, чтобы уровень электролита в нем совпадал с уровнем глаз. Желательно перед измерением плотности 2-3 раза набрать в ареометр электролит для смачивания стенок, чтобы избежать прилипания к ним поплавка. Если же прилипание случится, постучите легонько пальцем по колбе.
Если же прилипание случится, постучите легонько пальцем по колбе.
В последние годы автолюбители все чаще предпочитают измерять плотность не ареометром, а плотномером. Он удобнее потому, что в нем нет стеклянных деталей — корпус с трубкой и семь поплавков выполнены из пластмассы. Кроме этого, плотномером проще чем ареометром измерять плотность электролита. Поплавки плотнометра имеют различные массы, поэтому всплывают при различной плотности электролита.
Цифры, нанесенные на корпусе плотномера против каждого поплавка, указывают наименьшую плотность, при которой поплавок всплывает. Плотность электролита определяется по всплывшему поплавку с наибольшей цифрой. Если уровень электролита мал, то сначала долейте в аккумулятор дистиллированной воды и только через полтора-два часа, когда вода перемешается с электролитом, приступайте к измерению плотности.
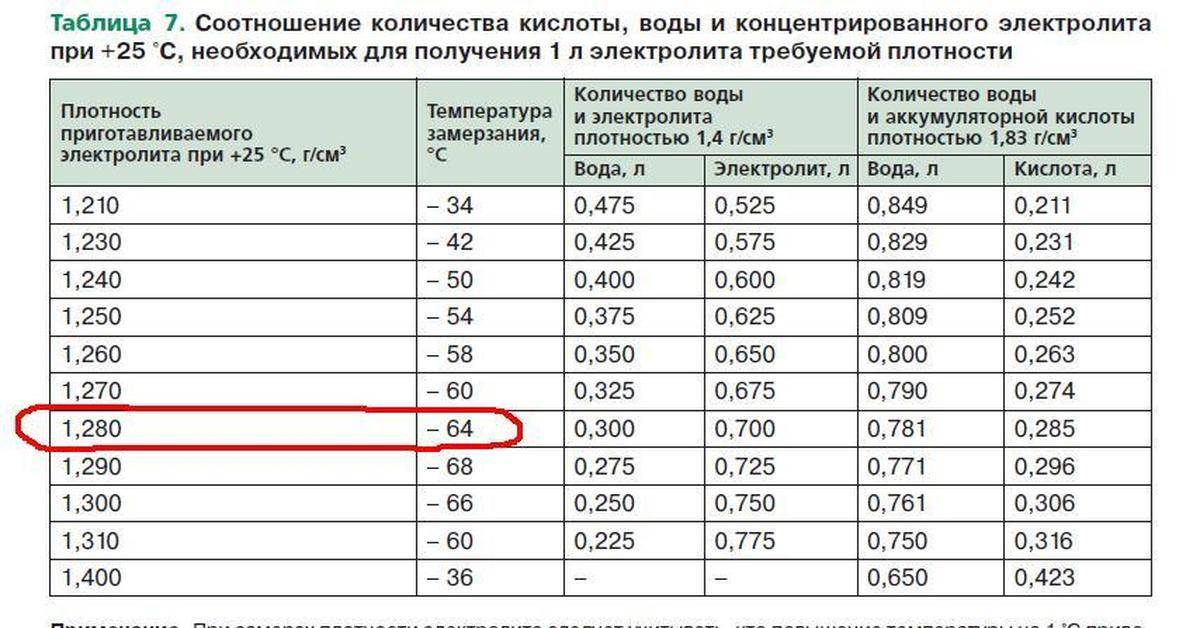
Не забудьте, что плотность электролита в большой степени зависит от его температуры, поэтому результаты измерений нужно всегда приводить к температуре плюс 25 градусов. Делается это так. Если температура электролита выше плюс 25 градусов, то к показаниям ареометра или плотномера добавляется поправка 0,007 г/см3 на каждый градус. Эта же поправка вычитается из показаний ареометра, если температура электролита ниже плюс 25 градусов.
Делается это так. Если температура электролита выше плюс 25 градусов, то к показаниям ареометра или плотномера добавляется поправка 0,007 г/см3 на каждый градус. Эта же поправка вычитается из показаний ареометра, если температура электролита ниже плюс 25 градусов.
Еще одно важное замечание. Плотность электролита полностью заряженной аккумуляторной батареи зависит от климатических условий работы автомобиля. Для проверки по плотности электролита степени заряженности батареи воспользуйтесь таблицей ниже.
Плотность электролита в автомобильном аккумуляторе при различной степени разряженности.
Аккумуляторную батарею, разряженную летом более, чем на 50%, а зимой более, чем на 25%, нужно снять с автомобиля и зарядить. Если плотность электролита у различных банок аккумулятора отличается более, чем на 0,02 г/см3 или же слишком низкая, то подзарядите автомобильный аккумулятор током 1-2 А в течение суток, Если и после этого напряжение аккумуляторной батареи будет меньше 12 В, то ее нужно менять.
Таким образом, плотность электролита показывает степень заряженности аккумуляторной батареи. О том, есть ли в аккумуляторе неисправности подскажут величины ЭДС и напряжения.
Проверка ЭДС и напряжения автомобильного аккумулятора.
Измерить ЭДС и напряжение автомобильного аккумулятора можно с помощью аккумуляторного пробника Э108 или нагрузочной вилки ЛЭ-2. В корпусе пробника (вилки) размещены два параллельно соединенных резистора. Контактной гайкой резисторы могут подключаться между ножками, которые соединены с кронштейном, где закреплены вольтметр и по одному концу резисторов.
Для измерения ЭДС отверните контактную гайку, при этом резисторы отключаются от ножек, и подключите ножки к выводам аккумулятора. Чтобы измерить напряжение, нужно затянуть контактную гайку, нагрузочные резисторы включаются между ножками, и снова соединить пробник с выводами аккумулятора.
Аккумуляторная батарея исправна, если измеренная ЭДС каждой банки не менее рассчитанной по плотности электролита, а напряжение в конце пятой секунды не упадет ниже 1,7 В. Если это не так — аккумуляторная батарея требует заряда или ремонта. Для определения расчетной ЭДС аккумулятора, сложите плотность электролитов каждой банки и к полученной сумме прибавьте 5,04.
Если это не так — аккумуляторная батарея требует заряда или ремонта. Для определения расчетной ЭДС аккумулятора, сложите плотность электролитов каждой банки и к полученной сумме прибавьте 5,04.
Рекомендации по эксплуатации автомобильного аккумулятора.
Срок службы автомобильного аккумулятора зависит не только от его состояния, но и от правильного использования. Старайтесь не допускать длительного разряда батареи большим током — в таких случаях пластины аккумулятора могут быстро покоробиться, активная масса из них выпадает, и аккумулятор выйдет из строя, Поэтому при пуске двигателя стартер включайте лишь на короткое время.
Если двигатель с первой попытки не запустился, сделайте перерыв на полминуты. Если двигатель не запустится после двух-трех попыток, сделайте более длительный перерыв перед новой попыткой. Этим вы дадите аккумуляторной батарее возможность восстановить плотность электролита в порах пластин, а значит и способность отдавать больше энергии.
Зимой после длительной стоянки автомобиля, аккумуляторная батарея работает хуже из-за увеличения вязкости электролита.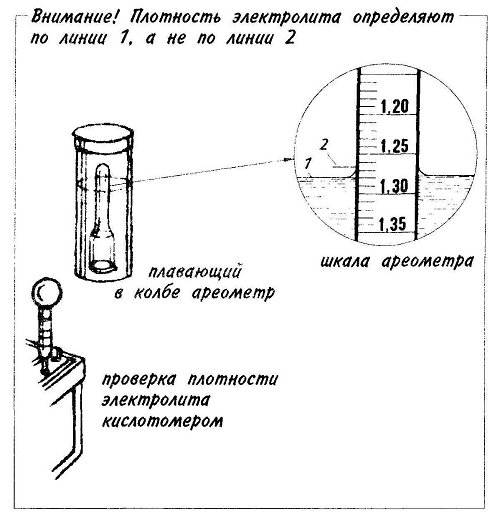 Поэтому в холодное время перед пуском желательно на 5 минут включить габаритные фонари, чтобы немного «прогреть» аккумулятор.
Поэтому в холодное время перед пуском желательно на 5 минут включить габаритные фонари, чтобы немного «прогреть» аккумулятор.
Корректировка — плотность — Большая Энциклопедия Нефти и Газа, статья, страница 1
Cтраница 1
Корректировка плотности производится доливкой дистиллированной воды, если плотность электролита превышает рекомендуемую, или доливкой электролита плотностью 1 40 г / см3 при пониженной плотности. После отключения батареи через 0 5 ч проводятся измерение и корректировка уровня электролита. После первого заряда батареи могут быть сданы в эксплуатацию. [1]
Корректировка плотности продолжается 10 — 12 сек, после чего нормально закрытый ( НЗ) контакт 1ТР1 термореле ТР1 размыкает цепь питания реле Р2, а это приводит к отключению сельсина СПП, лампы 1ЛЖ и магнита фиксатора ТОР. [2]
Корректировку плотности электролита рекомендуется проводить следующим образом. Если плотность электролита, приведенная к 25 С, ниже требуемой, то в аккумуляторы доливают электролит плотностью 1 40 г / см3, а если она выше — доливают дистиллированную воду.
После корректировки плотности и растекаемости раствора определяют сроки его схватывания. Если они недостаточны, то повышают количество ССБ или используют другой замедлитель. Каждый раз проверяют плотность и растекаемость раствора, а затем определяют сроки его схватывания. [4]
После корректировки плотности электролита продолжите зарядку батареи еще в течение 30 мин для перемешивания электролита. [5]
[5]
| Разрядные кривые свинцового аккумулятора. [6] |
По окончании корректировки плотности электролита температура электролита, если она отличается от 30 2 С, должна быть доведена до указанной температуры путем продолжения заряда для нагревания электролита в тех случаях, когда температура его ниже 28 С, и выдерживания батарей в полном покое или путем искусственного охлаждения — в тех случаях, когда температура электролита выше 32 С. [7]
| Световой индикатор уровня электролита с призматической отражательной поверхностью. а — установка в аккумуляторе. б . [8] |
Процессы заливки а корректировки плотности электролита являются трудоемкими и требуют строгого соблюдения правил техники безопасности. При ручном выполнении этих операций трудно предотвратить выливание электролита при переполнении аккумулятора. Чтобы избежать переливов электролита, необходимо при первоначальной заливке строго дозировать его количество, а при корректировке получать сигнал о достижении им определенного уровня. Повышение точности процессов заливки электролита и доливки дистиллированной воды в аккумуляторы может существенно улучшить качество обслуживания и эксплуатации стартерных автомобильных аккумуляторных батарей.
[9]
Чтобы избежать переливов электролита, необходимо при первоначальной заливке строго дозировать его количество, а при корректировке получать сигнал о достижении им определенного уровня. Повышение точности процессов заливки электролита и доливки дистиллированной воды в аккумуляторы может существенно улучшить качество обслуживания и эксплуатации стартерных автомобильных аккумуляторных батарей.
[9]
Заряд батареи продолжают после корректировки плотности не менее 30 мин для хорошего перемешивания электролита. [10]
| Рецептура свинцовых паст. [11] |
Допускается добавка воды для корректировки плотности пасты. Пасты I, II и IV — порошковые, а паста III — глето-сурич-ная; пасты I и III применяются для положительных электродов стартерных аккумуляторов, паста II — для отрицательных электродов стартерных аккумуляторов, а паста IV — для отрицательных электродов стационарных аккумуляторов. [12]
[12]
| Рецепты свинцовых паст. [13] |
Допускается добавка воды для корректировки плотности пасты. Па сты I, II, IV и V -порошковые, а паста III — глето-су-ричная. Пасты I, II и III применяются для положительных электродов, а пасты IV и V — для отрицательных электродов стар-терных аккумуляторов. [14]
Зарядный ток включают после окончания
Страницы: 1 2 3
Новый подход к литий-воздушной батарее с высокой плотностью энергии: трехмерный рост кристаллов Li2O2 с учетом концентрации ионов Li+ в электролите
Новый подход к созданию литий-воздушной батареи с высокой плотностью энергии: трехмерный рост кристаллов Li
2 O 2 , адаптированных к концентрации ионов Li + †Ян Лю, и Люмин Суо, б Хуан Лин, и Вэньчао Ян, и Янцюнь Клык, и Сяньцзюнь Лю, и Дэю Ван, * и Юн-Шэн Ху* б Вэйцян Хан и а также Лицюань Чен б
Принадлежности автора
* Соответствующие авторы
и Нинбоский институт материаловедения и инженерии Китайской академии наук, 509 Zhuangshi Road, Zhenhai, Ningbo 315201, China
Электронная почта: wangdy@nimte.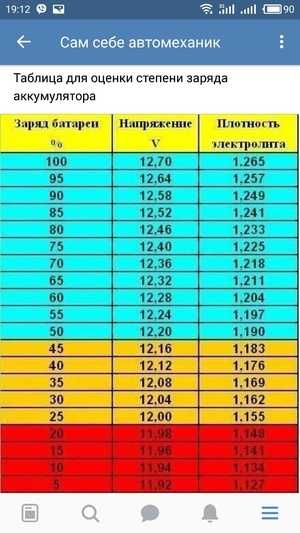 ac.cn
ac.cn
б Национальная лаборатория физики конденсированных сред Института физики Китайской академии наук, Пекин 100190, Китай
Аннотация
Предлагается новая стратегия улучшения коэффициента использования объема электрода посредством регулирования концентрации ионов электролита Li + . Дисперсия объема накопления, а именно разрядной емкости, до ∼600% больше в исследованном диапазоне от 10 −3 М до 5 М. Этот подход предлагает новую идею для дальнейшего повышения плотности энергии практических устройств.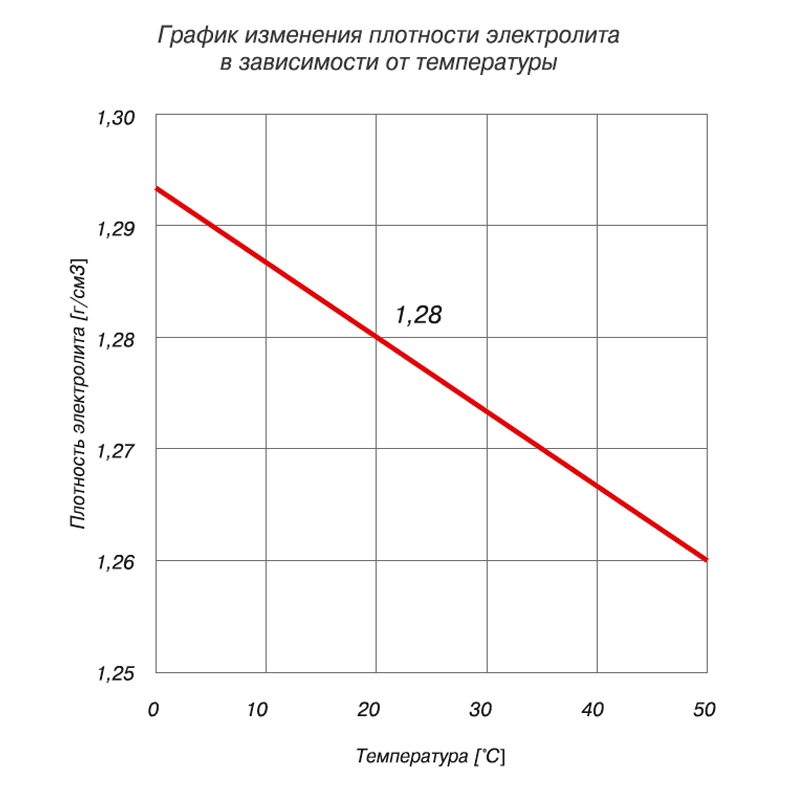
Замена обычных добавок к электролиту для аккумуляторов производными диоксолона для литий-ионных аккумуляторов с высокой плотностью энергии
1. Goodenough JB, Kim Y. Проблемы литиевых перезаряжаемых аккумуляторов. хим. Матер. 2010; 22: 587–603. doi: 10.1021/cm
2z. [CrossRef] [Google Scholar]2. Tarascon JM, Armand M. Вопросы и проблемы, связанные с перезаряжаемыми литиевыми батареями. Природа. 2001;414:359–367. doi: 10.1038/35104644. [PubMed] [CrossRef] [Google Scholar]
3. Арико А.С., Брюс П., Скросати Б., Тараскон Дж.М., ван Шалквейк В. Наноструктурные материалы для передовых устройств преобразования и хранения энергии. Нац. Матер. 2005; 4: 366–377. doi: 10.1038/nmat1368. [PubMed] [CrossRef] [Google Scholar]
4. Liu C, Li F, Ma LP, Cheng HM. Передовые материалы для хранения энергии. Доп. Матер. 2010;22:E28–E62. doi: 10.1002/adma.200903328. [PubMed] [CrossRef] [Google Scholar]
5. Chae S, Choi SH, Kim N, Sung J, Cho J. Интеграция графитовых и кремниевых анодов для коммерциализации высокоэнергетических литий-ионных аккумуляторов. Ангью. хим. Междунар. Эд. 2019;58:2–28. doi: 10.1002/anie.201813331. [PubMed] [CrossRef] [Google Scholar]
Chae S, Choi SH, Kim N, Sung J, Cho J. Интеграция графитовых и кремниевых анодов для коммерциализации высокоэнергетических литий-ионных аккумуляторов. Ангью. хим. Междунар. Эд. 2019;58:2–28. doi: 10.1002/anie.201813331. [PubMed] [CrossRef] [Google Scholar]
6. Liu W, et al. Слоистый оксид переходного металла лития с высоким содержанием никеля для высокоэнергетических литий-ионных аккумуляторов. Ангью. хим. Междунар. Эд. 2015;54:4440–4457. doi: 10.1002/anie.201409262. [PubMed] [CrossRef] [Google Scholar]
7. Manthiram A, Knight JC, Myung ST, Oh SM, Sun YK. Слоистые оксидные катоды с высоким содержанием никеля и лития: прогресс и перспективы. Доп. Энергия Матер. 2016;6:1501010. doi: 10.1002/aenm.201501010. [Перекрестная ссылка] [Академия Google]
8. Kasavajjula U, Wang C, Appleby AJ. Вставные аноды на основе нано- и объемного кремния для литий-ионных вторичных элементов. J. Источники энергии. 2007; 163:1003–1039. doi: 10.1016/j.jpowsour.2006.09.084. [CrossRef] [Google Scholar]
9.
10. Чен З., Шеврье В., Кристенсен Л., Дан Дж. Р. Разработка электродов из аморфного сплава для литий-ионных аккумуляторов. Электрохим. Твердотельное письмо. 2004; 7: А310–А314. doi: 10.1149/1.1792262. [CrossRef] [Google Scholar]
11. Choi N-S, et al. Влияние добавки фторэтиленкарбоната на межфазные свойства кремниевого тонкопленочного электрода. J. Источники энергии. 2006; 161:1254–1259. doi: 10.1016/j.jpowsour.2006.05.049. [CrossRef] [Google Scholar]
12. Shobukawa H, Alvarado J, Yang Y, Meng YS. Электрохимические характеристики и межфазное исследование кремниевого композитного анода для литий-ионных аккумуляторов в полном элементе. J. Источники питания. 2017;359: 173–181. doi: 10.1016/j.jpowsour.2017.05.044.
13. Zhao H, et al. Пленкообразующие электролитные добавки для аккумуляторных литий-ионных аккумуляторов: достижения и перспективы. Дж. Матер. хим. А. 2019;7:8700–8722. doi: 10.1039/C9TA00126C. [CrossRef] [Google Scholar]
14. Xu G, et al. Назначение функциональных добавок для устранения плохих характеристик высоковольтных (класс 5 В) литий-ионных аккумуляторов LiNi0,5 Mn1,5 O4 /MCMB. Доп. Энергия Матер. 2018;8:1701398. doi: 10.1002/aenm.201701398. [CrossRef] [Google Scholar]
15. Han JG, et al. Несимметричный фторированный малонатоборат как амфотерная добавка для литий-ионных аккумуляторов высокой плотности энергии. Энергетическая среда. науч. 2018;11:1552–1562. doi: 10.1039/C8EE00372F. [CrossRef] [Google Scholar]
16. Haregewoin AM, Wotango AS, Hwang BJ. Электролитные добавки для электродов литий-ионных аккумуляторов: достижения и перспективы. Энергетическая среда. науч. 2016; 9:1955–1988. doi: 10.1039/C6EE00123H. [Перекрестная ссылка] [Академия Google]
17. Choi N-S, et al. Проблемы, стоящие перед литиевыми батареями и электрическими двухслойными конденсаторами. Ангью. хим. Междунар. Эд. 2012;51:9994–10024. doi: 10.1002/anie.201201429. [PubMed] [CrossRef] [Google Scholar]
Choi N-S, et al. Проблемы, стоящие перед литиевыми батареями и электрическими двухслойными конденсаторами. Ангью. хим. Междунар. Эд. 2012;51:9994–10024. doi: 10.1002/anie.201201429. [PubMed] [CrossRef] [Google Scholar]
18. Jo H, et al. Стабилизация межфазного слоя твердого электролита и циклирование анода кремний-графитового аккумулятора с помощью бинарной добавки фторированных карбонатов. Дж. Физ. хим. С. 2016; 120:22466–22475. doi: 10.1021/acs.jpcc.6b07570. [Перекрестная ссылка] [Академия Google]
19. Nguyen CC, Lucht BL. Улучшенные циклические характеристики анодов с наночастицами кремния за счет включения метиленэтиленкарбоната. Электрохим. коммун. 2016;66:71–74. doi: 10.1016/j.elecom.2016.03.005. [CrossRef] [Google Scholar]
20. Chen L, Wang K, Xie X, Xie J. Влияние виниленкарбоната (VC) в качестве добавки к электролиту на электрохимические характеристики Si-пленочного анода для литий-ионных аккумуляторов. J. Источники питания. 2007; 174: 538–543. doi: 10.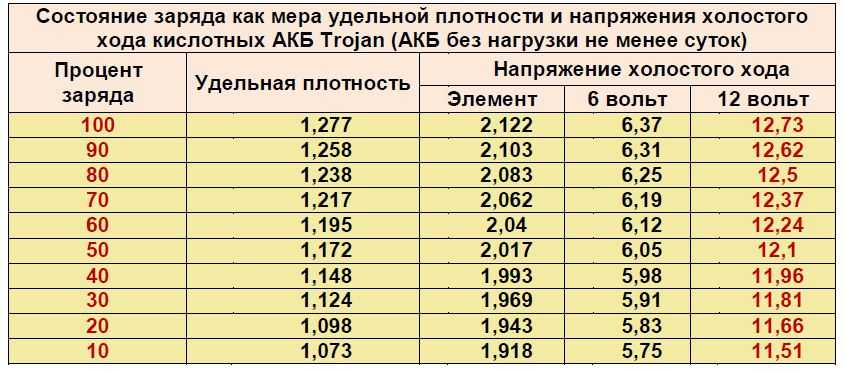 1016/j.jpowsour.2007.06.149. [Перекрестная ссылка] [Академия Google]
1016/j.jpowsour.2007.06.149. [Перекрестная ссылка] [Академия Google]
21. Далави С., Гудуру П., Лучт Б.Л. Добавки к электролиту, повышающие производительность литий-ионных аккумуляторов с кремниевыми анодами. Дж. Электрохим. соц. 2012; 159: A642–A646. doi: 10.1149/2.076205jes. [CrossRef] [Google Scholar]
22. Etacheri V, et al. Влияние фторэтиленкарбоната (FEC) на рабочие характеристики и химический состав поверхности Si-nanowire анодов литий-ионных аккумуляторов. Ленгмюр. 2012; 28: 965–976. doi: 10.1021/la203712s. [PubMed] [CrossRef] [Google Scholar]
23. Xu C, et al. Улучшенные характеристики кремниевого анода для литий-ионных аккумуляторов: понимание механизма модификации поверхности фторэтиленкарбоната как эффективной добавки к электролиту. хим. Матер. 2015;27:2591–2599. doi: 10.1021/acs.chemmater.5b00339. [CrossRef] [Google Scholar]
24. Jaumann T, et al. Срок службы по сравнению с производительностью: понимание роли FEC и VC в высокоэнергетических литий-ионных батареях с анодами из нанокремния.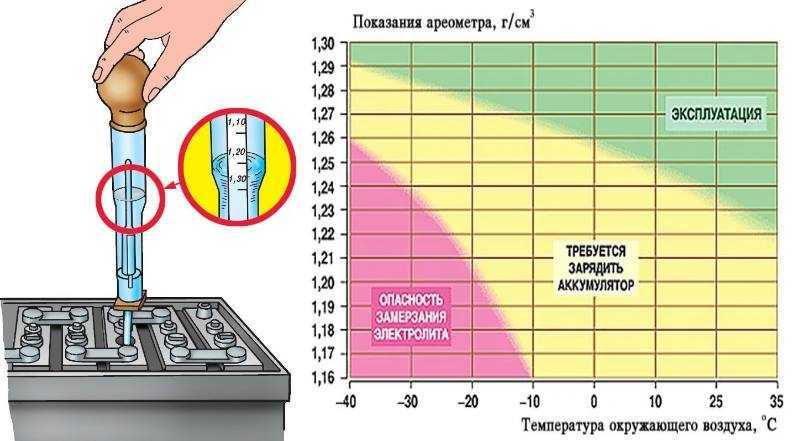 Материя накопления энергии. 2017;6:26–35. doi: 10.1016/j.ensm.2016.08.002. [CrossRef] [Google Scholar]
Материя накопления энергии. 2017;6:26–35. doi: 10.1016/j.ensm.2016.08.002. [CrossRef] [Google Scholar]
25. Kim K, et al. Понимание термической нестабильности фторэтиленкарбоната в электролитах на основе LiPF6 для литий-ионных аккумуляторов. Электрохим. Акта. 2017; 225:358–368. doi: 10.1016/j.electacta.2016.12.126. [Перекрестная ссылка] [Академия Google]
26. Schiele A, et al. Критическая роль фторэтиленкарбоната в газовыделении кремниевых анодов литий-ионных аккумуляторов. ACS Energy Lett. 2017;2:2228–2233. doi: 10.1021/acsenergylett.7b00619. [CrossRef] [Google Scholar]
27. Schwenke KU, Solchenbach S, Demeaux J, Lucht BL, Gasteiger HA. Воздействие CO 2 , выделенного из VC и FEC при формировании графитовых анодов в литий-ионных батареях. Дж. Электрохим. соц. 2019;166:A2035–A2047. doi: 10.1149/2.0821910jes. [Перекрестная ссылка] [Академия Google]
28. Аурбах Д. и соавт. Об использовании виниленкарбоната (ВК) в качестве добавки к растворам электролитов для литий-ионных аккумуляторов.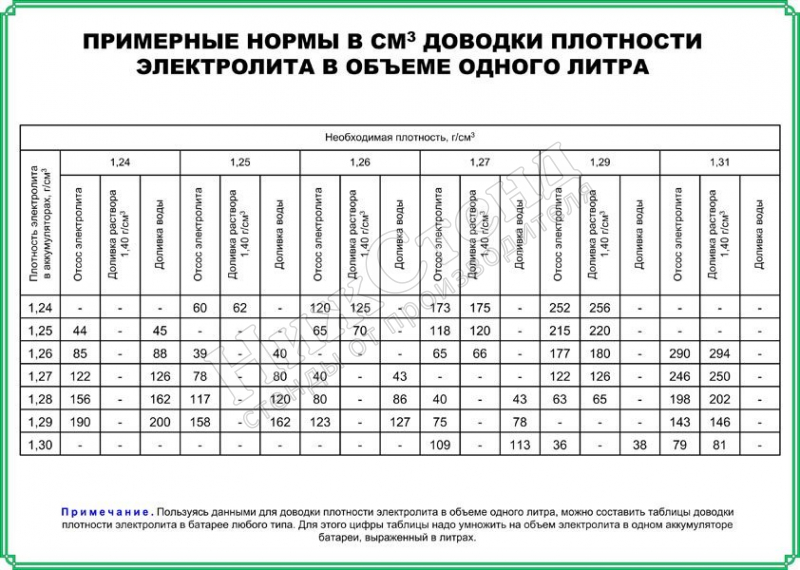 Электрохим. Акта. 2002; 47: 1423–1439. doi: 10.1016/S0013-4686(01)00858-1. [CrossRef] [Google Scholar]
Электрохим. Акта. 2002; 47: 1423–1439. doi: 10.1016/S0013-4686(01)00858-1. [CrossRef] [Google Scholar]
29. Buqa H, et al. Формирование пленки SEI на высококристаллических графитовых материалах в литий-ионных батареях. J. Источники энергии. 2006; 153:385–390. doi: 10.1016/j.jpowsour.2005.05.036. [CrossRef] [Google Scholar]
30. Michan AL, et al. Восстановление фторэтиленкарбоната и виниленкарбоната: понимание добавок к электролиту литий-ионных аккумуляторов и межфазного образования твердого электролита. хим. Матер. 2016;28:8149–8159. doi: 10.1021/acs.chemmater.6b02282. [CrossRef] [Google Scholar]
31. Уширогата К., Содеяма К., Окуно Ю., Татеяма Ю. Аддитивный эффект на восстановительное разложение и связывание растворителя на основе карбоната по отношению к межфазному образованию твердого электролита в литий-ионном аккумуляторе. Варенье. хим. соц. 2013; 135:11967–11974. doi: 10.1021/ja405079s. [PubMed] [CrossRef] [Google Scholar]
32. Ota H, Sakata Y, Inoue A, Yamaguchi S. Анализ слоев SEI, полученных из виниленкарбоната, на графитовом аноде. Дж. Электрохим. соц. 2004;151:А1659–А1669. дои: 10.1149/1.1785795. [CrossRef] [Google Scholar]
Анализ слоев SEI, полученных из виниленкарбоната, на графитовом аноде. Дж. Электрохим. соц. 2004;151:А1659–А1669. дои: 10.1149/1.1785795. [CrossRef] [Google Scholar]
33. Ван Ю., Накамура С., Тасаки К., Бальбуэна П.Б. Теоретические исследования для понимания химии поверхности угольных анодов для литий-ионных аккумуляторов: как виниленкарбонат играет роль добавки к электролиту? Варенье. хим. соц. 2002; 124:4408–4421. дои: 10.1021/ja017073i. [PubMed] [CrossRef] [Google Scholar]
34. Herstedt M, Andersson AM, Rensmo H, Siegbahn H, Edström K. Характеристика SEI, образованного на природном графите в электролитах на основе ПК. Электрохим. Акта. 2004;49: 4939–4947. doi: 10.1016/j.electacta.2004.06.006. [CrossRef] [Google Scholar]
35. Zhang SS, Xu K, Jow TR. EIS-исследование формирования границы твердого электролита в литий-ионном аккумуляторе. Электрохим. Акта. 2006; 51:1636–1640. doi: 10.1016/j.electacta.2005.02.137. [CrossRef] [Google Scholar]
36. Son HB, et al. Влияние восстановительных циклических карбонатных добавок и линейных карбонатных сорастворителей на способность к быстрой зарядке элементов LiNi0,6Co0,2Mn0,2O2/графит. J. Источники питания. 2018; 400:147–156. doi: 10.1016/j.jpowsour.2018.08.022. [Перекрестная ссылка] [Академия Google]
Влияние восстановительных циклических карбонатных добавок и линейных карбонатных сорастворителей на способность к быстрой зарядке элементов LiNi0,6Co0,2Mn0,2O2/графит. J. Источники питания. 2018; 400:147–156. doi: 10.1016/j.jpowsour.2018.08.022. [Перекрестная ссылка] [Академия Google]
37. Дэн Б. и др. Влияние потенциала отсечки заряда на добавку к электролиту для полных ячеек LiNi0.6Co 0.2Mn0.2O2 — мезоуглеродных микробусин. Энергетика. 2019;7:1800981. doi: 10.1002/ente.201800981. [CrossRef] [Google Scholar]
38. Zuo X, et al. Влияние трис(триметилсилил)бората на сохранение высоковольтной емкости ячеек LiNi0,5Co0,2Mn0,3O2/графит. J. Источники питания. 2013; 229:308–312. doi: 10.1016/j.jpowsour.2012.12.056. [CrossRef] [Академия Google]
39. Дэн Б. и др. Исследование влияния высоких температур на циклическую стабильность катода LiNi0,6Co0,2Mn0,2O2 с использованием инновационной добавки к электролиту. Электрохим. Акта. 2017; 236:61–71. doi: 10.1016/j.electacta.2017. 03.155. [CrossRef] [Google Scholar]
03.155. [CrossRef] [Google Scholar]
40. Хан Дж.Г., Ким К., Ли И., Чой Н.С. Продувочные материалы для стабилизации электролитов на карбонатной основе, содержащих LiPF6, для литий-ионных аккумуляторов. Доп. Матер. 2019;31:1804822. doi: 10.1002/adma.201804822. [PubMed] [CrossRef] [Академия Google]
41. Фэн П., Ли К.Н., Ли Дж.В., Чжан С., Нгай М.Ю. Доступ к новому классу синтетических строительных блоков посредством трифторметоксилирования пиридинов и пиримидинов. хим. науч. 2016;7:424–429. doi: 10.1039/C5SC02983J. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
42. Альпегиани М., Зарини Ф., Перроне Э. О получении 4-гидроксиметил-5-метил-1,3-диоксол-2-она. Синтез. коммун. 1992; 22:1277–1282. doi: 10.1080/00397919208019309. [CrossRef] [Google Scholar]
43. Liu JB, et al. Окислительное трифторметилирование фенолов с помощью серебра: прямой синтез арилтрифторметиловых эфиров. Ангью. хим. Междунар. Эд. 2015;54:11839–11842. doi: 10.1002/anie.201506329. [PubMed] [CrossRef] [Google Scholar]
[PubMed] [CrossRef] [Google Scholar]
44. Farlow, M.W., Man, E.H. & Tullock, D.W. Карбонилфторид. Inorganic Syntheses (Rochow, EG ed.), Vol. 6, 155–158 (McGraw-Hill Book Company, Inc., 1960). 10.1002/9780470132371.ч58.
45. Avataneo M, De Patto U, Galimberti M, Marchionni G. Синтез α,ω-диметоксифторполиэфиров: механизм реакции и кинетика. Дж. Флуор. хим. 2005; 126: 631–637. doi: 10.1016/j.jfluchem.2005.01.014. [Перекрестная ссылка] [Академия Google]
46. Petzold D, et al. Опосредованное видимым светом высвобождение и преобразование фторофосгена in situ. хим. Евро. Дж. 2019; 25:361–366. doi: 10.1002/chem.201804603. [PubMed] [CrossRef] [Google Scholar]
47. Xu W, Vegunta SSS, Flake JC. Поверхностно-модифицированные кремниевые нанопроволочные аноды для литий-ионных аккумуляторов. J. Источники энергии. 2011;196:8583–8589. doi: 10.1016/j.jpowsour.2011.05.059. [CrossRef] [Google Scholar]
48. Zhang J, et al. Прямое наблюдение неоднородной межфазной фазы твердого электролита на аноде MnO с помощью атомно-силовой микроскопии и спектроскопии. Нано Летт. 2012;12:2153–2157. doi: 10.1021/nl300570d. [PubMed] [CrossRef] [Академия Google]
Нано Летт. 2012;12:2153–2157. doi: 10.1021/nl300570d. [PubMed] [CrossRef] [Академия Google]
49. Wan G, et al. Подавление дендритного роста лития за счет образования на месте химически стабильной и механически прочной твердой электролитной межфазной фазы. Приложение ACS Матер. Интерфейсы. 2018;10:593–601. doi: 10.1021/acsami.7b14662. [PubMed] [CrossRef] [Google Scholar]
50. Снеддон И.Н. Связь между нагрузкой и проникновением в осесимметричной задаче Буссинеска для штампа произвольного профиля. Междунар. Дж. Инж. науч. 1965; 3: 47–57. doi: 10.1016/0020-7225(65)-4. [Перекрестная ссылка] [Академия Google]
51. Цанга Дж. П., Шуман Х., Леджер Р. Е., Ли С., Вайзел Дж. В. Эластичность отдельного волокна фибрина в сгустке. проц. Натл акад. науч. США. 2005; 102:9133–9137. doi: 10.1073/pnas.0504120102. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
52. Zhan C, Wu T, Lu J, Amine K. Растворение, миграция и отложение ионов переходных металлов в литий-ионных батареях на примере Mn- катоды на основе – критический обзор.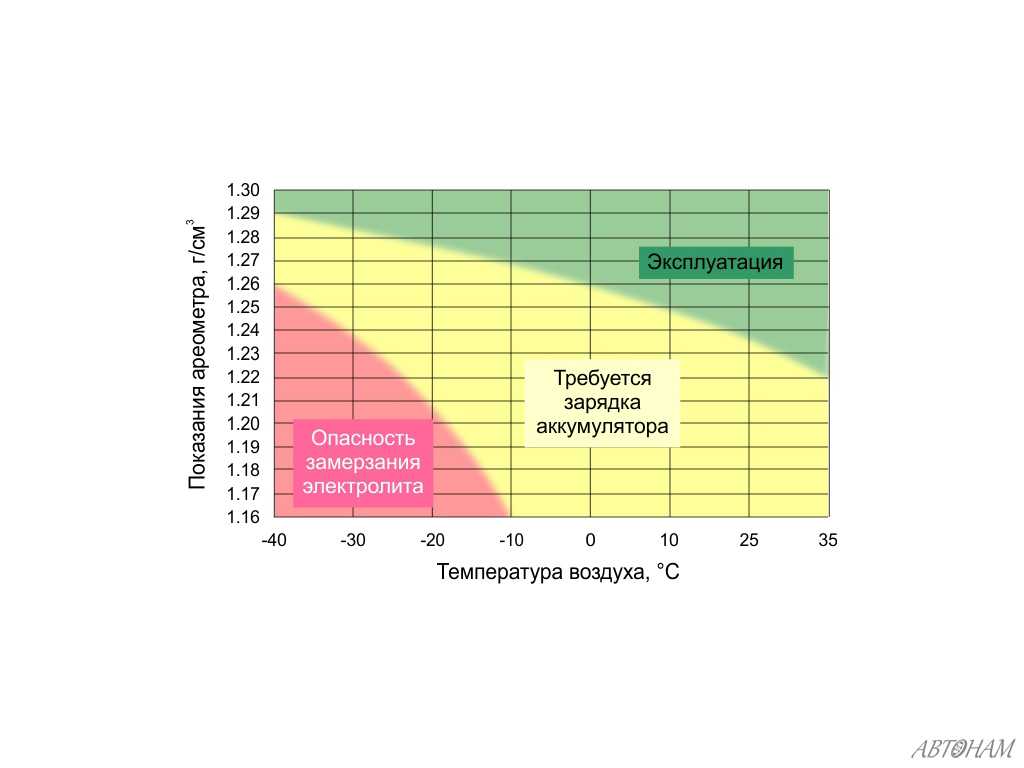 Энергетическая среда. науч. 2018; 11: 243–257. doi: 10.1039/C7EE03122J. [Перекрестная ссылка] [Академия Google]
Энергетическая среда. науч. 2018; 11: 243–257. doi: 10.1039/C7EE03122J. [Перекрестная ссылка] [Академия Google]
53. Гилберт Дж.А., Шкроб И.А., Абрахам Д.П. Растворение переходных металлов, миграция ионов, электрокаталитическое восстановление и потеря емкости в полных литий-ионных элементах. Дж. Электрохим. соц. 2017;164:A389–A399. doi: 10.1149/2.1111702jes. [CrossRef] [Google Scholar]
54. Ravdel B, et al. Термическая стабильность электролитов литий-ионных аккумуляторов. J. Источники питания. 2003; 119–121:805–810. doi: 10.1016/S0378-7753(03)00257-X. [CrossRef] [Google Scholar]
55. Ko M, et al. Масштабируемый синтез графита с кремниевым нанослоем для высокоэнергетических литий-ионных аккумуляторов. Нац. Энергия. 2016;1:16113. doi: 10.1038/nenergy.2016.113. [Перекрестная ссылка] [Академия Google]
56. Делли Б. Всеэлектронный численный метод решения функционала локальной плотности для многоатомных молекул. Дж. Хим. физ. 1990; 92: 508–517. doi: 10.1063/1.
