Что такое сульфатация пластин аккумулятора: причины и последствия
Рано или поздно любой автовладелец сталкивается с такой проблемой, как сульфатация пластин аккумулятора. Давайте разберемся, что же это такое, почему это происходит с аккумулятором и к чему это может привести.
Любые аккумуляторные батареи работают по принципу двойной сульфатации. Дело в том, что при разряде батареи пластины взаимодействуют с электролитом, в результате это ведет к падению плотности электролита. А при зарядке батареи в пластинах аккумулятора происходят обратные процессы, что ведет к повышению удельной плотности электролита. На сульфатацию пластин аккумулятора автомобиля вам укажет повышенное напряжение аккумулятора в начале разряда, а также обильное газовыделение.
Причины сульсификации
К сульфатации пластин вашего аккумулятора чаще всего могут привести следующие причины: разряженное состояние аккумулятора, слишком высокая температура или ее частые колебания, слишком низкое разрядное напряжение, а также чересчур большие разрядные токи. Очень важно соблюдать температурный режим и не допускать перегрева пластин аккумулятора. Потому что при ней процессы сульфатации и обратный процесс происходят быстрее. Но особенно опасны частые колебания температуры хранения пластин аккумулятора, потому как химические реакции со временем будут происходить неравномерно, что приведет к быстрому износу и порче аккумулятора. Для предотвращения сульфатации пластин аккумулятора, лучше не эксплуатировать их в режиме заряд-разряд выше, чем на 75-80% от номинала емкости аккумулятора. Это позволит аккумуляторной батарее быстрее восстановить емкость и перейти в режим заряда. Очень опасно оставлять свинцовый аккумулятор в постоянном разряженном состоянии, так как это способствует началу процессов сульфатации в его пластинах.
Последствия сульфатации
Объем пластин вашего аккумулятора сильно увеличивается.
Емкость аккумулятора постепенно уменьшается. Химические процессы, происходящие в аккумуляторе при его сульфатации, постепенно сокращают площадь самой поверхности его пластин, обязательно покрытую активными веществами. И поэтому емкость такого аккумулятора постепенно сокращается.
Внутреннее сопротивление самого аккумулятора растет. В результате падает напряжение на вашем аккумуляторе при попытке его разрядить и зарядить, а также сам аккумулятор гораздо быстрее перегревается и сульфатируется.
Поэтому, чтобы не допустить и максимально отсрочить наступление сульфатации пластин аккумулятора, соблюдайте правила его эксплуатации и аккумулятор прослужит вам очень долго!
как определить, почему возникает, как избежать
Автомобильный аккумулятор можно считать неким «расходным» устройством, которое водителю за время использования автомобиля приходится менять не один раз. Причин необходимости смены аккумулятора может быть несколько, вплоть до настоящего взрыва устройства. Но одна из самых распространенных из них, которая приводит к потере аккумулятором емкости и, как следствие, невозможности полноценной работы, это сульфатация пластин.
Если такая проблема произошла, аккумулятор не то что не сможет прокрутить стартер при пуске двигателя, но и не проработает большого количества времени даже с включенными фарами. В рамках данной статьи рассмотрим понятие сульфатации пластин аккумулятора, из-за чего возникает такая проблема, как ее определить и избежать.
Оглавление: 1. Что такое сульфатация аккумулятора 2. Причины сульфатации пластин аккумулятора автомобиля 3. Признаки сульфатации аккумуляторной батареи 4. Как избежать сульфатацию аккумулятора
Что такое сульфатация аккумулятора
Рассмотрим подробнее понятие сульфатации аккумулятора.
Если говорить техническим языком, под определением «сульфатация» в автомобильных аккумуляторах понимается образование на поверхности пластин налета из сернокислого свинца. Чем выше разряд аккумулятора, тем больше сернокислого свинца налипает, вплоть до того момента, когда практически вся площадь пластин им не будет заполнена.
Стоит вспомнить о составе аккумуляторов и их принципах работы. Как известно, внутри аккумулятора залит электролит, который собой представляет смесь серной кислоты и дистиллированной воды. Когда аккумулятор заряжается, на пластинах в нем накапливаются активные вещества, на отрицательной свинец, а на положительной окись свинца. В ходе течения данного процесса происходит поглощение дистиллированной воды, а вместе с тем возрастает плотность кислоты АКБ.
Важно: Идеальной считается плотность кислоты аккумулятора на уровне в 1,27 г/см3.
В процессе разряда автомобильного аккумулятора накопленные активные вещества используются, вследствие чего возникает сульфат свинца, который и оседает небольшими частицами на пластинах АКБ, «запечатывая» их.
В обычной ситуации, когда аккумулятор исправен и происходит его заряд, осевшие частички сульфата свинца расходуются, тем самым счищаясь с пластин аккумулятора и позволяя батарее сохранять свою емкость.
Но если в аккумуляторе имеются проблемы, могут возникать частички сульфата свинца большего размера, чем обычно, которые не удастся растворить в процессе заряда. Они покрывают поверхность пластин аккумулятора, из-за чего снижается его емкость.
Исходя из сказанного выше, можно сделать вывод, что под сульфатацией понимается налипание на пластины аккумуляторной батареи «кристаллов», препятствующих ее грамотной работе. Чем сильнее разряжается аккумулятор, тем крупнее становятся эти самые «кристаллы». Если довести аккумуляторную батарею до глубокого разряда, то налет не будет растворяться даже в процессе заряда, вследствие чего аккумулятор практически полностью потеряет свою емкость. Но не только глубокий разряд может стать причиной сульфатации пластин.
Чем сильнее разряжается аккумулятор, тем крупнее становятся эти самые «кристаллы». Если довести аккумуляторную батарею до глубокого разряда, то налет не будет растворяться даже в процессе заряда, вследствие чего аккумулятор практически полностью потеряет свою емкость. Но не только глубокий разряд может стать причиной сульфатации пластин.
Причины сульфатации пластин аккумулятора автомобиля
Как было сказано выше, основной причиной сульфатации является глубокий разряд аккумулятора, но вовсе не единственной. Рассмотрим подробно все имеющиеся причины:
- Глубокий разряд аккумулятора. Если проанализировать описанный выше процесс налипания на пластины аккумулятора «кристаллов», можно сделать вывод, что при глубоком разряде АКБ сульфатация возникает непременно. Исправить ситуацию позволит полный заряд аккумулятора, но даже при нем батарея немного потеряет в емкости. Важно знать, что допустив 1-3 раза полный разряд аккумулятора, можно сразу искать ему замену, поскольку больше необходимую емкость он набрать не сможет;
- Низкие температуры и короткие поездки. Автолюбителям хорошо известно, что в морозную погоду нужно в первую очередь заботиться о сохранности аккумулятора. Как таковая низкая температура не сказывается на процессе сульфатации пластин, но она влияет косвенно. В холодное время года для пуска двигателя путем раскрутки стартера требуется больше энергии, чем при положительной температуре окружающей среды. Кроме того, в холод аккумулятор во время поездки хуже заряжается. Особенно данная проблема актуальна, когда речь идет о коротких поездках. По сути, при пуске двигателя водитель тратит большое количество энергии, после чего через 15-20 минут глушит двигатель, и автомобиль не успевает достаточно прогреться и зарядить аккумулятор;
- Высокая температура. Не только низкая температура окружающей среды негативно сказывается на аккумуляторе, но и высокая. В жаркое время года аккумулятору приходится работать при температуре выше 60 градусов по Цельсию.
 Из-за столь высоких температур все химические процессы в нем протекают быстрее, в том числе и сульфатация. Поэтому в жаркое время года рекомендуется поддерживать аккумулятор максимально заряженным, чтобы на пластинах не образовывался налет;
Из-за столь высоких температур все химические процессы в нем протекают быстрее, в том числе и сульфатация. Поэтому в жаркое время года рекомендуется поддерживать аккумулятор максимально заряженным, чтобы на пластинах не образовывался налет; - Использование концентрированного электролита или серной кислоты. Некоторые водители пытаются устранить скопившийся на пластинах налет при помощи концентрированной серной кислоты или электролита. Так делать ни в коем случае нельзя. Таким образом не удастся «растопить» образовавшиеся «кристаллы», а только усугубится процесс их формирования;
- Хранение разряженного аккумулятора. Еще одна оплошность, которой грешат неопытные водители. Как известно, химические процессы в аккумуляторе не останавливаются, даже когда он отключен от потребителя. Соответственно, если поставить батарею на хранение разряженной на несколько месяцев, она за это время потеряет некоторую емкость. Как мы выяснили выше, при потере емкости и происходит налипание на пластины сульфата свинца, то есть процесс сульфатации. А поскольку отсутствует заряд аккумулятора, «растапливаться кристаллы» не будут, и велик риск возникновения критической сульфатации, при которой восстановить емкость батареи более не удастся.
Как можно видеть из описанного выше, большая часть причин – это просто катализаторы сульфатации. По сути, она происходит в аккумуляторной батарее все время, но только при критической сульфатации ситуация становится практически необратимой для аккумулятора.
Признаки сульфатации аккумуляторной батареи
Водитель не часто задумывается, какие химические процессы происходят внутри его аккумуляторной батареи. К тому же, «банки» с электролитом скрыты, и заметить образование на пластинах налета сульфата невозможно. Но есть несколько признаков, которые указывают, что началась сульфатация пластик аккумулятора:
- Если аккумулятор является обслуживаемым, то есть у него можно открутить пробки, имеется возможность посмотреть на пластины.
 Если видно, что на них осел белый или бело-коричневый налет, это говорит о протекании процесса сульфатации;
Если видно, что на них осел белый или бело-коричневый налет, это говорит о протекании процесса сульфатации; - Во время зарядки автомобильный аккумулятор начинает быстро «закипать» и батарея набирает полный заряд быстрее, чем положено. Например, при серьезных проблемах с аккумулятором, он может закипеть уже через 30 минут заряда;
- Образование белого налета на поверхности аккумулятора. Данную ситуацию можно считать нормальной, если она происходит не часто. Время от времени батарея все равно вскипает, даже в процессе работы, но если такая проблема происходит на регулярной основе, это явно говорит о неисправности аккумулятора;
- Двигатель не стартует с батареей после ее полного заряда. В такой ситуации емкости аккумулятора из-за налипшего сульфата банально не хватает для пуска двигателя. Можете поставить эксперимент, зажечь на таком аккумуляторе фары, минут через 10 они отключатся, а батарея «сядет в ноль»;
- Существенно снижается емкость батареи.
Как можно видеть, признаков протекающего процесса сульфатации предостаточно, но чаще всего водители задумываются о нем только в критическом случае, когда при попытке запустить двигатель, стартер не проворачивается.
Как избежать сульфатацию аккумулятора
Ответ на вопрос «Как избежать сульфатацию» аккумуляторной батареи автомобиля довольно простой – никак! Дело в том, что сульфатация является обычным процессом старения и деградации батареи, который неизбежен. Можно только приблизить или отдалить момент критической сульфатации.
В среднем, аккумуляторная батарея, если особо за ней не следит, работает на автомобиле 5 лет. Чтобы продлить ее срок службы, нужно выполнять каждые 2-3 года процесс десульфатации пластин, что далеко не всегда экономически целесообразно.
Загрузка…Как избавиться от сульфатации пластин аккумулятора!
Прочитав эту статью Вы узнаете, как можно избавиться от сульфатации пластин автомобильного аккумулятора. Но прежде чем мы раскроем перед вами все секреты, давайте узнаем, что же такое сульфатация?
Но прежде чем мы раскроем перед вами все секреты, давайте узнаем, что же такое сульфатация?
Сульфатация — это процесс, в результате которого поверхность аккумуляторных пластин покрывается сернокислым крупнокристаллическим свинцом в виде белого налета. Говоря более простым языком – это окисление и кристаллизация. В конечном итоге, сульфатация становится причиной проблем с зажиганием, и батарея выходит из строя.
Чтобы выявить сульфатацию, необходимо открыть капот автомобиля и внимательно осмотреть контактные пластины и источник аккумулятора. Коричневатые образования на «минусе» и «плюсе» — это и есть первичные признаки сульфатации. Разбухание, появление белых пятен, а также любое изменение внешнего вида пластин аккумулятора говорит о сульфатации.
Сульфатация повышает сопротивление внутри аккумуляторной батареи. Этот процесс способствует быстрому закипанию батареи, и приводит ее в негодность.
Методы десульфатации пластин аккумулятора
Первый метод, это ручной способ, при котором можно избавиться от сульфатации пластин. Необходимо произвести полную зарядку аккумулятора, довести плотность электролита до 1,285 г/см3, при этом доливая электролит немного более высокой плотности — 1,4 г/см3.
Чтобы уменьшить плотность электролита, добавьте дистиллированную воду. После полной зарядки, батарею нужно начать разряжать, подключив к ней лампу накаливания мощностью в 5 ампер: довести напряжение батареи до 10.2 В (что соответствует напряжению в 1.7 В в каждой отдельной банке батареи).
Именно такая процедура может спасти батарею от замены. Ее минус является то, что, во-первых, Вам потребуется какое-то зарядное-устройство, а во-вторых необходимо будет постоянно контролировать параметры аккумулятора. Если необходимо, повторите процесс зарядки-разрядки еще пару раз.
Для зарядки-разрядки аккумуляторных батарей лучше использовать импульсные устройства серии Зевс. Данные устройства обеспечивают заряд аккумулятора полностью в автоматическом режиме.
Второй метод автоматический. В этом случае, все что Вам понадобится, это приобрести зарядно-десульфатирующее устройство серии Зевс-Д и запустить на нем соответствующий метод. В этом случае устройство сделает все самостоятельно в автоматическом режиме.
В этом устройстве, для проведения десульфатации применяется заряд-разряд аккумулятора методом реверсивных токов.
Наша компания производит целый ряд устройств для обслуживания аккумуляторных батарей. Вся продукция производства нашего предприятия выполнена по высоким технологиям, что способствует бесперебойной его эксплуатации долгое время.
В каталоге нашего сайта представлены зарядные, зарядно-разрядные и десульфатирующие устройства различных характеристик.
Рекомендуем ознакомиться со следующими материалами:
Сульфатация аккумулятора — что это такое?
Сульфатация – это одна из самых основных и распространённых причин поломки автомобильных аккумуляторных батарей. Под воздействием сульфатации свинцовая батарея утрачивает свою ёмкость, в результате чего она начинает быстро разряжаться и становится непригодной. К сожалению, не многие автомобильные владельцы знают, что это за процесс. А то, как остановить её пагубное воздействие на аккумулятор и подавно знают единицы. Но всё же сульфатацию можно не только устранить, но и предотвратить! В данном обзоре мы осветим методы борьбы с сульфатацией свинцовых аккумуляторных пластин и то как можно предотвратить её появление.
Что такое сульфатация аккумулятора?
Сульфатация – это процесс, во время которого на поверхности аккумуляторных электродов появляется сернокислый свинец, постепенно покрывающий всю поверхность платин. Кристаллы сульфата предотвращают полный заряд и отдачу необходимого количества энергии, в следствии чего падает ёмкость и понижаются электрохимические показатели аккумуляторной батареи. Если Вы слишком поздно заметили процесс сульфатации, тогда аккумулятор подлежит неизбежному и немедленному «походу на свалку».
Если Вы слишком поздно заметили процесс сульфатации, тогда аккумулятор подлежит неизбежному и немедленному «походу на свалку».
Процесс сульфатации происходит постепенно:
— сначала возрастает внутреннее сопротивление;
— уменьшается площадь активной поверхности заряженных электродов;
— снижается емкость батареи аккумулятора.
Как определить сульфатацию аккумулятора?
Открыв капот автомобиля, внимательно осмотрите источник питания и контактные пластины вашей аккумуляторной батареи. Если Вы заметили на клеммах неестественные образования коричневатого оттенка, то это и есть явный признак сульфатации. Очередным признаком сульфатации является разбухание пластин и появление на них грязновато-белых пятен. Собственно, любое видоизменение внешнего вида вашей батареи уже говорит о признаках сульфатации. Сам процесс окисления и кристаллизации внутренних пластин батареи привод к высокой степени сопротивления внутри неё.
В данном случае происходит резкое повышение нормального сопротивления, что неизбежно приводит к тому, что батарея начинает моментально закипать. Если проигнорировать этот факт, то спустя некоторое время аккумуляторная батарея совсем перестанет функционировать. Сульфат по определению не может проводить реакцию, ведь он – естественный блокиратор. О высокой степени сульфатации электролита могут говорить следующие показатели:
— резкое понижение ёмкости батареи;
— температурные скачки электролита при старте двигателя;
— повышенная степень газовыделения и изменение цвета электролита. Как ликвидировать сульфатацию внутри батареи? Устранить сульфатацию можно только на самых начальных этапах её образования. В данном случае способна выручить лишь разовая разрядка-зарядка аккумулятора.
Причины сульфатации аккумулятора
Сульфатация пластин возникает в случае оставления аккумуляторной батареи в разряженном или недоразряженном состоянии.
Основные причины сульфатации
1. Недостаточный заряд аккумулятора и непридерживание систематического расписания проверок уравнительным зарядом. При частой частичной подзарядке аккумулятора не происходит глубокого перемешивания кислотного состава, а это в свою очередь ведёт к неизбежной сульфатации. В эксплуатационных условиях сложно определить момент начала сульфатации.
Только периодические проверки аккумулятора уравнительным зарядом, сравнение плотности электролита и напряжения в каждом элементе батареи позволяют диагностировать наличие сульфатации на ранних сроках и принять все возможные меры для её немедленного искоренения.
2. Хранение частично или не полностью разряженной аккумуляторной батареи. В данном случае свинцовый налёт затвердевает на пластинах и закупоривает поры активной массы. Здесь необходимо заряжать аккумулятор сразу же после его полного разряда и не оставлять полностью разряженным более чем на сутки и только при плюсовых температурах.
3. Недостаточный уровень кислотного электролита в ёмкости. В случае обнажения верха свинцовых пластин, они начинают поражаться сульфатацией.
4. Добавление кислоты. Если аккумуляторные пластины уже подверглись сульфатации, то добавление в банки кислоты только ускорит и усилит её процесс.
5. Электролит высокой плотности. Если плотность электролита после зарядки аккумулятора увеличивается, то вероятность сульфатации возрастает и над её устранением придётся потрудиться гораздо больше. Если в батарее имеется хотя бы один элемент с плотностью электролита, превышающей норму более чем на 0,015 г/см, процент вероятности сульфатации в нём увеличивается.
6. Высокая температура. На ускорение процесса сульфатации влияют и высокие температуры, в особенности, если аккумулятор частично разряжен и стоит без действий. У всех элементов, с подверженными сульфатации пластинами, показатели плотности электролита и напряжения заметно занижены. Они лишь частично могут конвертировать электрическую энергию в химическую реакцию при заряде. Они лишь частично преобразуют электрическую в химическую при заряде.
Отрицательные пластины под сульфатацией на ощупь схожи со слоистыми структурами. Если потереть частичку такой пластины между пальцами, то можно почувствовать её твердозернистый состав, схожий на песок. Осматривать пластины нужно только после нормальной зарядки батареи, ведь незаряженные пластины всегда отчасти сульфатированы.
Хорошая, полностью заряженная свинцовая пластина отрицательного заряда на ощупь пориста и упруга, она издаёт металлический звук при резком взаимодействии с твёрдыми предметами, например ножом. Положительная пластина, подверженная сульфатации, отличается от «здоровой» цветом, у неё светло-коричневый оттенок.
Как устранить сульфатацию аккумулятора?
Устранить сульфатацию пластин, как правило, можно выполнив следующие операции:
1. Протереть батарею.
2. Довести уровень электролита до нормы, путём добавления в него воды.
3. Далее следует присоединить батарею к зарядному устройству. Установите силу тока заряда с расчётом восьмичасового режима. Если во время зарядки температура электролита перейдёт отметку в 43 градуса по Цельсию, следует уменьшить силу зарядного тока, чтобы удерживать температуру хотя бы на этом уровне или, желательно, снизить её.
Если напряжение на одном из элементом будет меньше среднего напряжения аккумуляторной батареи на 0,2 Вольта, то необходимо немедленно извлекать элемент из батареи и отремонтировать. Только после этих манипуляций работы по ликвидации сульфатации можно продолжать.
4. После поступления в батарею определённого количества электричества, что приравнивается к её номинальной ёмкости, заряд будет продолжаться до тех пор, пока плотность электролита в продолжении четырёх замеров с интервалом в один час, останется константой. Запишите показания вольтметра и ареометра. Пересчитайте значение плотности электролита с учетом температуры. Эти показания характеризуют состояние заряженности батареи.
5. Разрядите батарею током шестичасового режима. Во время разрядки батареи, снимите показания с каждого отдельного её элемента и в целом. Проделывать это стоит через определённые временные интервалы: 15 минут после запуска разряда, после каждый час, пока один из элементов не покажет напряжение около 1,8 Вольт, затем снова каждые 15 минут. После этого строго начинайте контролировать напряжение на каждом элементе и фиксируйте время падения напряжения ниже 1,75 Вольт. Операция закончится тогда, когда большая часть элементов разрядится до 1,75 Вольт. Если в одном из элементов будет происходить обратный процесс, прекратите испытание.
6. Никаких дальнейших испытаний и манипуляций проводить не стоит в том случае, если разрядная ёмкость аккумуляторной батареи сравняется с номинальной. Просто дайте нормальный заряд и выровняйте плотность электролита.
7. Если же она оказалась ниже номинальной, тогда разряд батареи придётся продолжать, не изменяя силу тока, пока напряжение на одном из элементов не станет 1,0 Вольт.
8. Вновь произведите заряд батареи до полной ёмкости и заряжайте до тех пор, пока на протяжении четырёх последующих замеров с интервалом в один час, плотность электролита станет постоянной.
9. Вновь разрядите батарею шестичасовым разрядом. Если после этого её ёмкость сравняется с номинальной, зарядите батарею снова и установите на погрузчик.
10. В случае, если ёмкость будет ниже, но не меньше 90% от номинальной, повторите цикл вновь.
11. Если ёмкость батареи не поддаётся восстановлению, то значит, что сульфатация проникла настолько глубоко, что все дальнейшие манипуляции будут попросту нецелесообразными и остаётся только заменить батарею.
Подписывайтесь на наши ленты в таких социальных сетях как, Facebook, Вконтакте, Instagram, Pinterest, Yandex Zen, Twitter и Telegram: все самые интересные автомобильные события собранные в одном месте.
Что такое сульфатация?
Аккумулятор в вашем автомобиле быстро разряжается и теряет емкость? Возможно, пластины в батарее подверглись воздействию сульфатации.
Сульфатация — процесс постепенного покрытия заряженных электродов сернокислым свинцом, который имеет форму крупных кристаллов. Визуально наличие сульфата определяется довольно просто – есть белый «налет», значит это сульфат на пластинах. Кристаллы закупоривают поры и препятствуют проникновению электролита к активной массе, в результате затрудняется заряд и снижается эффективность работы батареи.
Под воздействием сульфатации увеличивается внутреннее сопротивление аккумуляторной батареи, а из-за сокращения площади активной поверхности электродов заметно падает емкость. С учетом этого можно выделить основные симптомы сульфатации:
· быстрый заряд аккумулятора.
· резкое повышение напряжения и температуры электролита.
· стремительное газовыделение.
· малое повышение плотности электролита во время зарядки.
· преждевременный разряд аккумулятора при попытке запуска двигателя.
Среди основных признаков сульфатации аккумуляторных пластин надо отметить следующие:
1. Положительные
электроды окрасились в светло-коричневый цвет, а на поверхности проявились белые
пятна. Отрицательные электроды, обычно окрашиваются с беловато-серый цвет и могут
раздуваться.
Отрицательные электроды, обычно окрашиваются с беловато-серый цвет и могут
раздуваться.
2. Так как объем сульфата превышает объем активной массы, у неразряженных электродов, то при увеличении объема кристаллов ячейки отрицательных пластин разбухают, а положительные электроды начинают ржаветь из-за неравномерного распределения напряжения.
3. При глубокой сульфатации, когда на поверхности электрода образуется сплошная корка, аккумулятор может полностью потерять проводимость из-за того, что сульфат электричество совсем не проводит.
Итак, самыми показательными признаками сульфатации считается ускоренный заряд, быстрый разряд и резкое активное газовыделение. При первых же симптомах рекомендуется провести профилактику, чтобы избежать усугубления ситуации, когда батарея полностью выйдет из строя.
Для этого автомобильные аккумуляторы подвергаются нескольким выравнивающим зарядам. Сейчас на рынке предлагаются особые зарядные устройства с режимом десульфатации, которые помогают восстановить работоспособность авто аккумулятора путем повторяющихся импульсных зарядов малым током.
Что такое сульфатация АКБ и чем она опасна?
В основу принципа работы аккумулятора автомобиля лежат обратимые химические процессы. Реакции протекают в равной степени при зарядке, так и при разрядке прибора. В свинцово-кислотных автомобильных аккумуляторах важно, чтобы эти реакции протекали правильно и в контрольном режиме.
В заряженном состоянии, электродные пластины собирают вещества, которые отличаются электрической активностью. На отрицательно заряженной пластине свинец и на положительно заряженной пластине – это двуокись свинца.
Если аккумуляторная батарея разряжена, химические реакции протекают в обратную сторону. Образовавшиеся активизированные реагенты «растрачиваются» и генерируется сульфат свинца или сернистокислый свинец. Сульфат оседает и кристаллизуется на пластинах аккумулятора.
Эта «кристаллическая порода» имеет пористую структуру, благодаря, чему электролит легко взаимодействует с кристаллами во время зарядки. Это свойство способствует тому, что возврат в исходное состояние раствора после зарядки не вызывает никаких специфических затруднений.
Однако при некоторых ситуациях имеет место процесс перекристаллизации. В таком случае сульфат от свинца создает слишком крупные кристаллы, которые слабее подвержены растворению, из-за чего восстановление активного вещества аккумулятора из расплава получается более сложным. Это явление получило название процесс сульфатации в аккумуляторе. Следствие этого процесса – ускоренное строение батареи и снижение КПД агрегата в разы.
Кроме всего прочего, сульфатация уменьшает емкость аккумуляторной батареи, т.к. сокращается площадь поверхности тех пластин, с которыми происходит взаимодействие электролита в ходе химических реакций. Это равнозначно тому, если бы часть электролита слили или бы он испарился.
Разряженный аккумулятор с признаками сульфатации на электродах дает намного меньше емкости, чем чистый. С течением времени крупные кристаллы могут полностью закрыть поры в кристаллизированном веществе.
Процесс сульфатации становится причиной серьезных деформаций и разрушения пластин аккумуляторной батареи. В некоторых случаях бывает, заметна деформация и корпуса аккумулятора.
При необходимости замены аккумуляторной батареи на вашей машине портал carkysha.ru предлагает поиск автозапчастей по Москве и регионам России.
Сульфатация пластин аккумулятора. Что это?
Сульфатация – это процесс, во время которого на поверхности аккумуляторных электродов появляется сернокислый свинец, постепенно покрывающий всю поверхность пластин.
Кристаллы сульфата предотвращают полный заряд и отдачу необходимого количества энергии, в следствии чего падает ёмкость и понижаются электрохимические показатели аккумуляторной батареи.
Если Вы слишком поздно заметили процесс сульфатации, тогда аккумулятор подлежит неизбежному и немедленному «походу на свалку».
Признаки сульфатации пластин аккумулятора:
- Большое внутреннее сопротивление АКБ. Этот симптом является наиболее объективным. Естественно, что сопротивление батареи в домашних условиях померить сложно. Но оценить его можно во время зарядки. В этом случае практически невозможно выставить номинальный зарядный ток, или для этого приходится поставить регулятор на максимальные положения. Напряжение заряда при этом, может достигать 20 В.;
- Низкая плотность электролита;
- Раннее закипание аккумулятора при заряде;
- Изменение цвета положительных пластин. Этот признак можно определить только у обслуживаемых аккумуляторов. Для этого нужно выкрутить на банках пробки и через отверстия будут видны «сетки». Пластины подверженные сульфатации будут иметь светло-коричневый цвет.
Условия, способствующие сульфатации свинцового аккумулятора
В любом свинцовом аккумуляторе, оставленном в разряженном состоянии начинается сульфатация. Она может быть более или менее интенсивной, в зависимости от нескольких факторов. Сульфатации способствуют:
- повышенная температура;
- длительное хранение в разряженном состоянии;
- большие разрядные токи;
- пониженное разрядное напряжение;
Сульфатация увеличивает внутреннее сопротивление аккумулятора
Сульфат свинца имеет большое электрическое сопротивление. Поэтому замещение активных веществ (свинца и окиси свинца) сульфатом свинца на поверхности пластин в результате сульфатации аккумулятора приводит к значительному росту внутреннего сопротивления аккумулятора. Увеличение внутреннего сопротивления аккумулятора при сульфатации приводит к увеличенному падению напряжения на аккумуляторе при разряде и зарядке, а также к перегреву аккумулятора, который приводит к ускорению сульфатации.
Восстановление АКБ
Сразу отметим, что реанимировать можно далеко не всякую батарею. Если аккумулятор долгое время находился в разряженном состоянии и сульфатация застарелая, то снять ее практически невозможно. И даже когда автолюбитель своевременно заметил описанные выше признаки и сразу приступил к восстановлению батареи, нельзя гарантировать положительный результат. Прежней емкости уже не будет.
И даже когда автолюбитель своевременно заметил описанные выше признаки и сразу приступил к восстановлению батареи, нельзя гарантировать положительный результат. Прежней емкости уже не будет.
Однако, как показывает практика, процент восстановленных АКБ достаточно велик. Попробовать можно. И для тех, кто решиться это сделать, есть несколько способов устранения сульфатации.
Зарядка импульсным током
Является, пожалуй, самым передовым и простым способом. Суть его заключается в периодическом изменении зарядного тока, от нуля до максимального значения. В результате происходит постепенное разрушение крупных кристаллов налета сульфата свинца. Таким образом, восстанавливается электрическая проводимость между пластинами. Это делает возможным впоследствии зарядить аккумулятор постоянным током.
Этот способ подходит для батарей с сильной сульфатацией. Однако есть и недостатки. Здесь требуется специальное зарядное устройство, способное выдавать импульсный ток большой величины, или достаточно серьезные навыки и познания в области электротехники.
Длительный заряд малым током
Устранение сульфатации этим способом, возможно только при незначительном налете на пластинах. Последовательность действий следующая:
- Неисправный аккумулятор доливают дистиллированной водой на 3-4 мм выше нормального уровня;
- На зарядном устройстве устанавливают номинальный ток;
- Заряд аккумулятора продолжают до начала газообразования;
- Как только батарея «закипит», зарядное устройство выключают на полчаса;
- Уменьшают ток в 10 раз и снова заряжают до усиленного газообразования;
- После этого – снова перерыв 20 минут и опять заряд током 1/10 от номинала;
- Пункт 6 повторяют до тех пор, пока плотность электролита не достигнет нормального значения.
Этот способ достаточно прост и эффективен. Правда требует большого терпения, так как для получения положительного результата иногда необходимо несколько суток.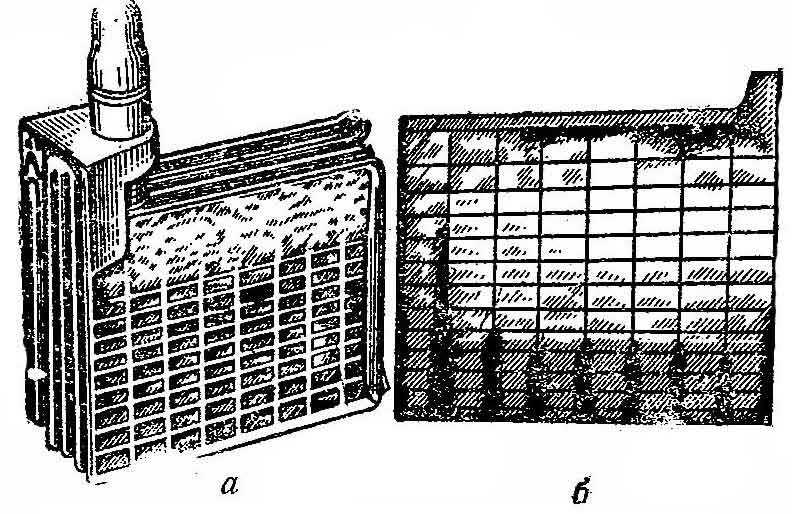
Глубокие разряды малыми токами
Этому способу уже более полувека и в народе он более известен как «заряд – разряд». Позволяет устранить даже довольно старую сульфатацию. Суть его состоит в проведении нескольких циклов зарядов номинальным током, с последующим разрядом – малым. В результате создаются условия для включения в работу более глубоких слоев активной массы пластин. А это, в свою очередь, вызывает отпадание сульфата свинца.
Сначала неисправный аккумулятор заряжается током равным 0,2Q (Q-номинальная емкость аккумулятора). То есть, к примеру, для 55-го аккумулятора это значение будет 11 А. Заряд длиться до того момента, пока напряжение на батарее не достигнет 14,4 В., после чего ток снижают до 0,05Q. Необходимо постоянно следить за плотностью электролита и напряжением на клеммах. Как только они будут оставаться постоянными в течение получаса, заряд прекращают на 1 час.
По истечению этого промежутка времени, батарею вновь заряжают током 0,05Q, до момента ее «закипания». При этом напряжение на клеммах должно перестать меняться. Снова делаем часовой перерыв. И так несколько раз, до тех пор, пока батарея не начнет «кипеть» через 2-3 мин., после начала заряда. Как только это произойдет, аккумулятор нужно будет разрядить током 0,02Q, до напряжения не ниже 10,5 В. В качестве нагрузки лучше всего использовать подходящую лампу накаливания.
Итак, как только разряд будет закончен, полный цикл можно считать завершенным. Для восстановления их потребуется 7-8. Процесс это длительный, с каждым разом заряжаться и разряжаться АКБ будет все дольше. Правда, совсем необязательно делать это непрерывно. На ночь работы можно прекращать.
Что это такое и как этого избежать?
Сульфатирование представляет собой скопление кристаллов сульфата свинца и является основной причиной преждевременного выхода из строя свинцово-кислотных аккумуляторов.
Как происходит сульфатация аккумулятора Сульфатирование происходит, когда аккумулятор лишается полного заряда, он накапливается и остается на пластинах аккумулятора. Когда происходит слишком сильное сульфатирование, это может препятствовать химическому преобразованию в электрическую и сильно повлиять на производительность батареи.
Когда происходит слишком сильное сульфатирование, это может препятствовать химическому преобразованию в электрическую и сильно повлиять на производительность батареи.
Эффекты сульфатирования
Если в аккумуляторе скопились сульфаты, может произойти следующее:
- более длительное время зарядки
- чрезмерное тепловыделение
- сокращение времени работы без подзарядки
- значительно сокращает время автономной работы
- полный отказ батареи
Все свинцово-кислотные батареи накапливают сульфатирование в течение своего срока службы, поскольку это часть естественного химического процесса в батарее.Но сульфатирование накапливается и вызывает проблемы, когда;
- Аккумулятор перезаряжен
- Аккумулятор хранится выше 75 градусов
- Аккумулятор хранится без полного заряда
Чтобы предотвратить сульфатирование при хранении аккумулятора, даже если он хранится с полным зарядом, аккумулятор должен быть достаточно заряжен, чтобы не допустить падения напряжения ниже 12,4 В. Применение этой поддерживающей зарядки предотвратит накопление сульфатов.Также важно отметить, что, хотя мы упоминали, что аккумулятор не следует хранить при температуре выше 75 градусов, на каждые 10 градусов выше комнатной, скорость саморазряда удваивается.
В свинцовой батарее может происходить два типа сульфатирования; обратимый и постоянный. Их названия точно отражают воздействие на вашу батарею. Если проблема обнаружена достаточно рано, можно обратить вспять сульфатацию батареи. Однако делать это должен только человек, имеющий большой опыт работы со свинцовыми батареями, например, в магазине, где ваша батарея была изначально куплена.
Постоянное сульфатирование происходит, когда аккумулятор находился в низком уровне заряда в течение недель или месяцев. Хотя иногда их можно спасти, восстановление маловероятно.
Лучший способ предотвратить сульфатирование — это правильно обслуживать аккумулятор и следовать передовым методам зарядки. Несмотря на то, что существуют устройства защиты от сульфатирования, которые будут подавать импульсы на клеммы аккумулятора, чтобы предотвратить и обратить вспять сульфатирование на исправном аккумуляторе, они не устранят полностью повреждение и не всегда рекомендуются.
Сульфатион — это причина номер один, по которой вы не должны хранить аккумулятор разряженным. После того, как произошло сульфатирование свинцовых пластин, обратить эффекты вспять крайне маловероятно, поэтому очень важно позаботиться о ваших батареях с самого начала.
Вот почему сульфатирование — плохая новость для вашей батареи
При диагностике преждевременного выхода из строя свинцово-кислотной аккумуляторной батареи вашего автомобиля технические специалисты выявляют проблему, называемую сульфатацией. Хотя это обычная проблема, есть большая вероятность, что вы никогда о ней не слышали.Знание азов сульфатирования поможет вам понять объяснение событий вашим техническим специалистом. Это также поможет вам понять, как предотвратить повторение проблемы в будущем. Имея все это в виду, вот краткое изложение того вреда, который сульфатирование может нанести вашей батарее.
Как работают свинцово-кислотные батареи
Прежде чем изучать детали сульфатирования, полезно знать основы работы свинцово-кислотных аккумуляторов. Внутренняя часть батареи этого типа состоит из свинцовых пластин, окруженных раствором серной кислоты.Половина пластин, сделанных из материала, называемого перекисью свинца, несут положительный электрический заряд. Они соединены с отрицательно заряженными пластинами из губчатого свинца.
Когда течет ток и батарея разряжается во время использования, происходит несколько вещей. Во-первых, его положительная и отрицательная пластины покрываются кристаллами вещества, называемого сульфатом свинца. Это вещество образуется, когда сульфат серной кислоты соединяется со свинцом в пластинах. Батарея полностью заряжается, когда образование сульфата свинца достигает максимального уровня.На этом этапе должна произойти подзарядка. В процессе зарядки кристаллы сульфата свинца снова растворяются в растворе серной кислоты. Как только это происходит, свинцовые пластины восстанавливают свой положительный и отрицательный заряды.
Это вещество образуется, когда сульфат серной кислоты соединяется со свинцом в пластинах. Батарея полностью заряжается, когда образование сульфата свинца достигает максимального уровня.На этом этапе должна произойти подзарядка. В процессе зарядки кристаллы сульфата свинца снова растворяются в растворе серной кислоты. Как только это происходит, свинцовые пластины восстанавливают свой положительный и отрицательный заряды.
Что такое сульфатион?
Термин сульфатирование используется для описания накопления сульфата свинца на свинцовых пластинах вашей батареи. Это накопление происходит каждый раз, когда батарея разряжается. Вы можете спросить, почему сульфатирование является проблемой, если оно происходит постоянно? Оказывается, процесс сульфатирования работает на двух уровнях.
При нормальном использовании аккумулятора накопление кристаллов сульфата свинца носит временный характер. Вместо того, чтобы оставаться на месте, кристаллы исчезают во время цикла перезарядки. Проблемы с сульфатированием начинаются, когда покрытие из сульфата свинца становится стойким и не исчезает.
Последствия перманентной сульфатирования
Постоянное сульфатирование может вызвать ряд проблем в свинцово-кислотных аккумуляторах. Список этих проблем включает гораздо более короткий срок службы батареи и полный отказ батареи.Также включает:
- Значительное увеличение времени нормальной зарядки
- Потеря пусковой мощности
- Аномально высокая температура внутри аккумулятора
- Необходимость более частой подзарядки аккумулятора
Постоянное сульфатирование признано экспертами основной причиной преждевременных отказов свинцово-кислотных аккумуляторов.
Как возникает проблема?
Существует множество возможных объяснений проблем с сульфатацией аккумулятора.К известным причинам относятся такие вещи, как:
- Слишком много времени между циклами зарядки аккумулятора
- Аккумулятор, у которого осталось менее 100% заряда после зарядки.

- Неправильная настройка зарядного устройства
- Отсутствие достаточного количества раствора серной кислоты внутри батареи
- Воздействие воздуха на пластины свинцовых аккумуляторов
- Хранение батареи без доступа к источнику энергии
Вы увеличиваете вероятность перезарядки до менее 100%, если часто оставляете автомобиль работать на холостом ходу.Интенсивное использование энергоемких автомобильных плагинов также может привести к той же проблеме.
Предотвращение перманентной сульфации и борьба с ней
Без сомнения, регулярное обслуживание свинцово-кислотной батареи — лучший способ избежать постоянной сульфатирования. Чтобы избежать проблем с сульфатированием во время хранения, аккумулятор должен иметь заряд не менее 12,4 В. Вам также следует избегать хранения свинцово-кислотных аккумуляторов в среде с температурой выше 75 F. Это связано с тем, что каждые 10 градусов выше этой температуры удваивают скорость разряда хранимых аккумуляторов.
Аккумулятор всегда портится из-за перманентной сульфатации? Не обязательно. Иногда проблему можно обратить вспять, если пластины вашей батареи не покрыты толстым слоем кристаллов сульфата свинца. Однако сильно поврежденный аккумулятор может никогда не восстановиться. Из соображений безопасности только профессионал, имеющий опыт работы с свинцово-кислотными аккумуляторами, должен когда-либо пытаться обратить вспять симптомы перманентного сульфирования.
Есть ли у аккумулятора симптомы затяжного сульфатации? Посещение местного специалиста по аккумуляторным батареям в Powertron должно помочь вам проверить наличие проблемы.Если повезет, проблему поможет профессиональная подзарядка. Если это не так, вам придется купить новую батарею. Это помогает знать, что у вас есть выбор, когда дело доходит до поиска подходящего источника питания. Многие люди ищут товары только в автомобильных магазинах с большими ящиками. Однако у Powetron Battery Co. есть все необходимые опции по самой доступной цене.
Что такое сульфатирование аккумуляторов? — Новости о хранении энергии, батареях, изменении климата и окружающей среде
Сульфатирование происходит внутри свинцово-кислотных аккумуляторов, когда начинает разрушаться электролит.Когда серная кислота (электролит) распадается, ионы серы становятся свободными, образуя кристаллы. Эти кристаллы иона серы затем прилипают к свинцовым пластинам батареи, образуя кристаллы сульфата свинца. Со временем кристаллы увеличиваются в размерах и становятся твердыми, полностью покрывая свинцовые пластины. Это покрытие ухудшает общую эффективность и способность аккумулировать энергию. Если не лечить, процесс сульфатирования только ухудшит состояние, и пользователь потеряет батарею.
Общие причины сульфатации аккумулятора:
a) Батареи слишком долго сидят между зарядками. Всего 24 часа в жарком климате и несколько дней в более прохладном климате. Чем дольше батарея сидит и не перезаряжается, тем больше на пластинах образуется сульфатирование.
б) Аккумулятор убирается без какого-либо энергозатрат.
c) Неправильные уровни зарядки и настройки. Например, недозаряд батареи до 90% от предела позволит сульфатировать батарею, используя 10% батареи, которая не была повторно активирована из-за невыполнения цикла зарядки.
d) Низкий уровень электролита — пластины батареи, открытые для воздуха, быстро сульфатируются.
Миф о спасении аккумулятора от сульфатирования — отключение аккумулятора. Отсоединение батареи может предотвратить капельный разряд, но не предохраняет электролит внутри батареи от разрушения. Это может помочь замедлить сульфатирование аккумулятора, но не предотвратит его окончательного возникновения.
Некоторые организации предлагают устройства для «десульфатации», которые подают импульсы на клеммы аккумулятора для предотвращения и обратного сульфатирования.Эти устройства основаны на технологиях, которые снижают сульфатирование здоровой батареи, однако они не могут изменить это состояние. Еще один важный аспект устройств для десульфатации заключается в том, что компании, предлагающие такие устройства, придерживаются подхода «один размер для всех», что является ненаучным.
Еще один важный аспект устройств для десульфатации заключается в том, что компании, предлагающие такие устройства, придерживаются подхода «один размер для всех», что является ненаучным.
Статьи по теме:
Десульфатация
Электролит
Свинцово-кислотные батареи
3 вещи, которые нужно знать о сульфатации аккумуляторов
Автомобиль использует два отдельных, но одинаково важных источника энергии.Во-первых, бензин обеспечивает мощность, необходимую для запуска двигателя и движения колес. Во-вторых, автомобильный аккумулятор обеспечивает электроэнергией, необходимой для питания всего: от фар до радио и зарядного устройства для мобильного телефона. Без исправного аккумулятора ваша машина даже не заведется.
Производители тщательно разработали автомобильные аккумуляторы для подзарядки, когда вы управляете автомобилем. Тем не менее, со временем батарея все еще имеет тенденцию к возникновению проблем, которые могут повлиять на ее способность обеспечивать необходимый заряд.Одна малоизвестная, но слишком распространенная проблема носит название сульфатирования. В этой статье более подробно рассматриваются три ключевых момента, которые необходимо знать о сульфатации аккумуляторных батарей.
- Сульфатирование учитывает многие ранние отказы батарей
Если у вас когда-либо была батарея, которая разряжалась до истечения ожидаемого срока службы, сульфатирование могло сыграть свою роль. Сульфатирование считается частой причиной преждевременного выхода из строя свинцово-кислотных автомобильных аккумуляторов. Еще до того, как ваша батарея полностью разрядится, сульфатирование влияет на вашу машину несколькими потенциально изнурительными способами.
Сульфатирование — это образование кристаллов сульфата свинца на поверхности пластин аккумулятора. На малых уровнях эти кристаллы не представляют серьезной угрозы. Но по мере того, как отложения становятся все больше, они эффективно сокращают количество активного материала внутри вашей батареи. В результате производительность вашего аккумулятора быстро падает.
В результате производительность вашего аккумулятора быстро падает.
Аккумулятор, пострадавший от сульфатирования, демонстрирует значительное снижение пусковой мощности. Вы можете заметить, что батарея разряжается при попытке завести машину.Сульфатирование также увеличивает вероятность выкипания, которое включает кипение кислоты и выливание из батареи. Сульфатирование также снижает эффективное время работы аккумулятора между зарядками. Любой из этих эффектов может привести к тому, что автомобильный аккумулятор разрядится раньше, чем ожидалось.
- Сульфатирование влияет на городских водителей Более
Автовладельцы должны понимать, что сульфатирование происходит естественным путем и в той или иной степени влияет на все аккумуляторы. Небольшие количества кристаллов сульфата образуются практически каждый раз, когда аккумулятор используется.Тем не менее, батареи, подвергнутые определенным условиям, имеют гораздо больший шанс развить изнурительную сульфатацию.
Одна из наиболее частых причин сульфатирования связана с постоянно недозаряженными батареями. Если аккумулятор никогда не заряжается полностью, он не достигнет состояния полного насыщения. На химическом уровне такая недозарядка значительно облегчает образование кристаллов сульфата. Напротив, полностью заряженная батарея обладает достаточным зарядом, чтобы свести к минимуму сульфатирование.
Если вы регулярно используете свой автомобиль для поездок по шоссе, вам не нужно беспокоиться о сульфатировании так сильно, как водителю в городе.Эти более длительные поездки на более высоких скоростях дают генератору достаточно времени, чтобы полностью зарядить аккумулятор. С другой стороны, городские водители подвергаются гораздо большему риску сульфатации, поскольку более короткая поездка с остановками часто не позволяет полностью зарядить аккумулятор.
- Сульфатирование часто можно обратить вспять
Химические изменения, приводящие к сульфатированию, также могут происходить в обратном направлении. Когда ваша батарея работает, образуются сульфаты. В процессе зарядки аккумулятора сульфаты подвергаются процессу, известному как выделение газа.При выделении газа кристаллы сульфата свинца снова превращаются в серную кислоту и свинец.
Когда ваша батарея работает, образуются сульфаты. В процессе зарядки аккумулятора сульфаты подвергаются процессу, известному как выделение газа.При выделении газа кристаллы сульфата свинца снова превращаются в серную кислоту и свинец.
По мере того, как сульфатирование становится все более прогрессивным, часто из-за хронически недозаряженной батареи, обратный процесс становится все труднее и труднее для вашего генератора переменного тока. Тем не менее, вы часто можете восстановить надлежащую производительность с помощью десульфатора батареи. Десульфатор батареи удаляет даже самые сильные сульфатные отложения, подвергая батарею скачкам высокого напряжения.
Сульфаторы для аккумуляторов настолько хорошо справляются со своей задачей, что могут даже вернуть к жизни разряженные аккумуляторы.Для получения дополнительной информации о том, как предотвратить сульфатирование и поддерживать автомобильный аккумулятор в отличном состоянии, обратитесь к автомобильным экспертам в сервисных центрах Evans Tire.
Химическое сульфатирование малых молекул — достижения и проблемы
1. Введение
В отчете 1876 года Ойген Бауманн описал выделение кристаллического «фенолобразующего» вещества из мочи лошади и показал, что это вещество имеет отношение к m — и p, -фенолсульфоновые кислоты. Позже это вещество было идентифицировано как фенилсульфат калия и оказалось практически нетоксичным, поскольку 2.6 г можно вводить кроликам без каких-либо неблагоприятных последствий. Бауманн также заметил, что фенол, катехол и индол широко выводятся из организма в виде ковалентно связанных сложных эфиров серной кислоты при введении собакам и / или пациентам. Это, по-видимому, первое сообщение о детоксикации фенола и родственных ароматических молекул и подчеркивает новаторскую работу Ойгена Баумана в области химии и биохимии сложных эфиров сульфатов. 1 Сложные эфиры сульфатов в настоящее время признаны модуляторами ряда важных физиологических и патологических процессов.
Природа, по-видимому, использует сульфатирование эндогенных и экзогенных молекул в основном для двух целей, включая усиленное выведение во избежание потенциальной токсичности и индукцию специфических клеточных или бесклеточных реакций. Сульфатированные молекулы также могут служить резервуарами биоактивных веществ, которые высвобождаются при гидролизе, опосредованном сульфатазой.
Сульфатирование ксенобиотиков — важный механизм удаления потенциально токсичных веществ из нашего организма. 2 Метаболическое сульфатирование, или более подходящее сульфирование, происходит в цитозоле под действием одной из сульфотрансфераз и 3′-фосфоаденозин-5′-фосфосульфата (PAPS), который отдает активированную сульфонатную группу (SO 3 — ) к акцепторной спиртовой, фенольной или аминогруппе. 3 Это придает молекуле анионный характер, тем самым улучшая ее экскреционные свойства, чтобы избежать возможных побочных эффектов.
Еще более интересным является использование по существу аналогичного механизма для индукции определенного биологического ответа. Этот механизм включает сульфатирование биологических молекул, особенно углеводов, с образованием уникальных сульфатированных лигандов. Ферменты, которые катализируют эти биотрансформации, представляют собой сульфотрансферазы, то есть углеводные сульфотрансферазы, которые играют важную роль в передаче клеточных сигналов, адгезии и некоторых других функциях. 4 — 6 . Ключевым примером является сиалил Льюис X, для которого сульфирование в положении 6 его компонентов N -ацетилглюкозамина и галактозы усиливает распознавание лектинов типа C ( L -селектин) (), таким образом опосредуя рекрутирование лейкоциты в ткани. 7 Сульфатированный тирозин участвует в высокоаффинном связывании гликопротеинового лиганда-1 Р-селектина (PSGL-1) с Р-селектином, 8 — 11 , который играет важную роль в провоспалительном ответе. Точно так же сульфатирование тирозина на N-конце хемокинового рецептора CCR5 облегчает проникновение вируса иммунодефицита человека-1 (ВИЧ-1) в клетки-хозяева. 12 Наконец, в классе уникальных молекул, генерируемых биосинтетическим сульфатированием, специфические последовательности, присутствующие в полимерном гепарине / гепарансульфате (H / HS), являются изобретением природы. 13 , 14 Сконструированные последовательности, например, последовательности HS, связывающие антитромбин и гликопротеин D (), обладают исключительной специфичностью в отношении своих белков-мишеней, прежде всего из-за трехмерного созвездия их ключевых сульфатных групп (- ОСО 3 —). 15 — 18
Точно так же сульфатирование тирозина на N-конце хемокинового рецептора CCR5 облегчает проникновение вируса иммунодефицита человека-1 (ВИЧ-1) в клетки-хозяева. 12 Наконец, в классе уникальных молекул, генерируемых биосинтетическим сульфатированием, специфические последовательности, присутствующие в полимерном гепарине / гепарансульфате (H / HS), являются изобретением природы. 13 , 14 Сконструированные последовательности, например, последовательности HS, связывающие антитромбин и гликопротеин D (), обладают исключительной специфичностью в отношении своих белков-мишеней, прежде всего из-за трехмерного созвездия их ключевых сульфатных групп (- ОСО 3 —). 15 — 18
Сульфатные группы, выделенные синим цветом (Sialyl Lewis X и DEFGH), как известно, необходимы для взаимодействия с мишенью белки. Такие сульфатные группы не были точно идентифицированы для октасахарида гликопротеина D.
Помимо вышеуказанных метаболических и биосинтетических применений, сульфатирование является важным механизмом регулирования биоактивности определенных молекул.Например, стероидные сульфаты могут не функционировать как гормоны, но, по-видимому, служат предшественниками активных стероидов, которые образуются в результате гидролиза сульфатной группы на основе сульфатазы. Появляется все больше свидетельств того, что внутриклеточное сульфатирование и десульфатация играют важную роль в регулировании доступности активных стероидных гормонов вблизи участков-мишеней. 19
Хотя многие взаимодействия сульфатная группа — белок в основном неспецифичны, то есть не требуют уникального «фармакофора» для вызова биологического ответа, известно, что несколько взаимодействий управляются специфическим распознаванием одной или нескольких сульфатных групп. .Основная причина специфичности или ее отсутствия — природа сил, доминирующих во взаимодействии. Электростатическое взаимодействие, присутствующее в чисто анионно-катионной точечной паре, является ненаправленным и, следовательно, неспецифическим (). Напротив, взаимодействие водородных связей, которое может присутствовать между двумя сильно электроотрицательными или ионными точками, окружающими атом водорода, является направленным взаимодействием, ответственным за создание специфичности. Система тромбин-гепарин включает несколько сульфатных групп, взаимодействующих с несколькими остатками аргинина и лизина.Тем не менее, система считается неспецифической, потому что основной вклад в сродство возникает из-за электростатических сил. 20 , 21 С другой стороны, система гепарин пентасахарид DEFGH — антитромбин () очень специфична, поскольку неионные силы, такие как множественные водородные связи, вносят основной вклад в свободную энергию связывания. 22 — 24 Интересно отметить, что сульфатная группа может вводить как специфические, так и неспецифические взаимодействия, и в этом заключается проблема модуляции сульфатно-белкового взаимодействия.
.Основная причина специфичности или ее отсутствия — природа сил, доминирующих во взаимодействии. Электростатическое взаимодействие, присутствующее в чисто анионно-катионной точечной паре, является ненаправленным и, следовательно, неспецифическим (). Напротив, взаимодействие водородных связей, которое может присутствовать между двумя сильно электроотрицательными или ионными точками, окружающими атом водорода, является направленным взаимодействием, ответственным за создание специфичности. Система тромбин-гепарин включает несколько сульфатных групп, взаимодействующих с несколькими остатками аргинина и лизина.Тем не менее, система считается неспецифической, потому что основной вклад в сродство возникает из-за электростатических сил. 20 , 21 С другой стороны, система гепарин пентасахарид DEFGH — антитромбин () очень специфична, поскольку неионные силы, такие как множественные водородные связи, вносят основной вклад в свободную энергию связывания. 22 — 24 Интересно отметить, что сульфатная группа может вводить как специфические, так и неспецифические взаимодействия, и в этом заключается проблема модуляции сульфатно-белкового взаимодействия.
A) Взаимодействие основывается исключительно на ионных зарядах двух групп. Это взаимодействие определяется как взаимодействие кулоновского типа и происходит в более широком диапазоне по сравнению с другими атомными взаимодействиями. Он изотропен и не имеет геометрических ограничений. B) Взаимодействие между Lys или Arg с одной или несколькими сульфатными группами может сэндвич с атомом H, что приводит к образованию водородной связи.Эта водородная связь не может быть линейной, но обеспечивает достаточную энергию для инженерной специфичности распознавания. Стехиометрия взаимодействия здесь может составлять 1: 1 или 1: 2 на атом азота. C) Для аргинина возможна линейная геометрия Н-связи, генерирующая значительную энергию связи и большую специфичность распознавания. Стехиометрия взаимодействия здесь 1: 1. Геометрия C) ожидается наиболее стабильной.
Стехиометрия взаимодействия здесь 1: 1. Геометрия C) ожидается наиболее стабильной.
Структура ко-комплекса была получена из PDB (имя файла «1e03»).Зеленая лента показывает антитромбин, а пурпурный — сайт связывания гепарина. Пентасахарид DEFGH показан в виде шариков и клюшек. Обширные взаимодействия между антитромбином аргинином и лизинами с множественными сульфатными группами DEFGH создают взаимодействие с высокой аффинностью и высокой специфичностью. Считается, что большая часть неионной энергии связи, участвующей во взаимодействии гепарин-антитромбин, возникает из-за взаимодействия типа водородной связи с сульфатными группами. Рисунок изменен из Desai UR. Med. Res. Rev. 2004; 24: 151–181).
Растущее значение природных сульфатированных лигандов, моносульфатированных или полисульфатированных, придает такое же значение надлежащим образом разработанным, неприродным, сульфатированным каркасам. Например, Тамура и Нишихара сообщают о стереоселективном синтезе сульфатированных производных гликозилсерина как о механистических пробах, позволяющих лучше понять механизм сортировки, который происходит на начальных этапах биосинтеза гликозаминогликанов (ГАГ). 25 Точно так же изостеры тирозинсульфата CCR5 были разработаны как инструменты для понимания проникновения ВИЧ-1. 26
Еще одно важное применение разработанных сульфатированных каркасов — это агонисты / антагонисты биологических процессов. Например, несколько больших и малых ароматических миметиков H / HS, включая сульфатированные флавоноиды 27 , 28 , бензофураны 29 , изохинолины 30 и сульфатированные дегидрополимеры лигнинового типа 31 , были разработаны для модуляции функции белков свертывания, таких как антитромбин, тромбин и фактор Ха.Дизайн таких высокосульфатированных неприродных молекул предполагает большую возможность открытия новых сульфатированных неуглеводных фармацевтических агентов.
Хотя сульфатирование, по-видимому, является одностадийной реакцией, химический синтез малых сульфатированных молекул является сложной задачей.Введение сульфатной группы резко изменяет физико-химические свойства небольшой молекулы. Почти все сульфатированные молекулы растворимы в воде, что затрудняет их выделение в очень чистой форме. Распространенной проблемой является присутствие неорганических солей, доля которых обычно выше в небольших синтетических масштабах 34 и которые приводят к значительным несоответствиям. Другой проблемой является лабильность сульфатных групп к кислым условиям и высоким температурам. 35 , 36 Дополнительной проблемой является отсутствие маневренности после введения сульфатной группы.Некоторые превращения функциональных групп могут быть успешно выполнены в присутствии сульфатной группы, что по существу вынуждает дизайн схемы синтеза включать сульфатирование в качестве конечной стадии. Эти сложности геометрически возрастают для полисульфатированного каркаса. Хотя теоретически синтетический подход для моносульфатированного каркаса должен быть легко распространен на полисульфатированный каркас, на практике это синтетический кошмар из-за генерации значительно более высокой плотности отрицательного заряда. 37 Основная проблема — довести реакцию до завершения, чтобы сульфатировать все доступные реакционноспособные функциональные группы (например, ROH или PhOH). По мере увеличения количества спиртовых / фенольных групп на небольшом каркасе сульфатирование становится все более трудным из-за анионного скопления, что приводит к многочисленным частично сульфатированным побочным продуктам. 34 Наконец, можно ожидать, что отсутствие региоселективности станет доминирующей проблемой для полифункциональных субстратов.
34 Наконец, можно ожидать, что отсутствие региоселективности станет доминирующей проблемой для полифункциональных субстратов.
Учитывая растущее значение сульфатированных природных, а также ненатуральных каркасов, мы рассматриваем наиболее широко применяемые протоколы химического сульфатирования.Реакция химического сульфатирования — древняя реакция, и недавние разработки пытаются сделать ее более «удобной для пользователя». Тем не менее, для получения плодов значительных улучшений в понимании биологии сложных эфиров сульфатов необходимо существенное усовершенствование технологии.
2. Подходы к химическому сульфатированию
2.1 Сульфатирование с использованием серной кислоты
Литература показывает, что сульфатирование проводилось с серной кислотой (H 2 SO 4 ) в начале 20 -х годов века. 38 H 2 SO 4 может непосредственно сульфатировать алкены и циклоалкены при умеренных температурах и умеренных давлениях. Механически получается продукт Марковникова. H 2 SO 4 также сульфатирует насыщенные одноатомные спирты, хотя образование воды в реакции приводит только к 65% выходу сульфатного эфира от эквимолярных концентраций кислоты и спирта. 39 Добавление избытка кислоты, удаление воды с помощью дистилляционной установки Динса-Старка и CCl 4 , добавление сульфата бора (дегидратирующий химикат) и сульфатирование в вакууме были предприняты для увеличения выхода. 38
Многоатомные спирты, например полиэтиленгликоль, глицерин и поливиниловый спирт, и полисахариды, азотистые и неазотистые, сульфатированы с использованием H 2 SO 4 . Хотя H 2 SO 4 может сульфатировать целлюлозу в мягких условиях, например 5 ° C в CH 2 Cl 2 или при -10 ° C в жидком SO 2 , рекомендуется преобразовать его в аддукт бис- (2-хлорэтил) эфира, менее реакционноспособную форму, с 1, 2-дихлорэтан в качестве растворителя. 40 Другие подходы в этой области работы, такие как использование SO 2 в качестве замедляющего растворителя, также были исследованы. 41
40 Другие подходы в этой области работы, такие как использование SO 2 в качестве замедляющего растворителя, также были исследованы. 41
Модифицированной формой серной кислоты, используемой для сульфатирования, является сульфаминовая кислота (H 2 NSO 3 H), которая использовалась для синтеза насыщенных сульфатов одноатомных спиртов и сульфатов углеводов. Поскольку он менее реакционноспособен и более дорогой, чем другие сульфатирующие агенты, это реагент, который нужно исследовать, когда другие не справляются. Сульфатирование длинноцепочечных первичных спиртов сульфаминовой кислотой дает низкие выходы и продукты темного цвета.Тем не менее конденсаты фенольного этиленоксида предпочтительно сульфатируются сульфаминовой кислотой. 42 Катализаторы, такие как пиридин, мочевина, тиомочевина и ацетамид, были использованы для улучшения результатов сульфатирования длинноцепочечных вторичных спиртов и моно- и диэфиров глицерина. Сообщается, что целлюлоза разрушается при нагревании только с сульфаминовой кислотой, но в присутствии мочевины удовлетворительное сульфатирование происходит при 140 ° C за 30 минут. 40 Несмотря на то, что сульфатирование на основе H 2 SO 4 на основе H 2 является полезным для сульфатирования простых спиртов, которые доступны в большом количестве, это многочисленные побочные реакции, включая дегидратацию, неселективное сульфатирование и разрушение каркаса.
2.2 Сульфатирование, опосредованное дициклогексилкарбодиимидом
Первое сульфатирование алифатических / алициклических спиртов с использованием дициклогексилкарбодиимида (DCC) и H 2 SO 4 было описано Mumma в 1966 году (). Спирту, DCC и H 2 SO 4 позволяли реагировать в фиксированном соотношении 1: 5: 1, соответственно, в ДМФА при низкой температуре (~ 4 ° C) в течение примерно 15 минут. Было обнаружено, что порядок добавления реагентов важен, когда к DCC добавляют спирт, за которым следует H 2 SO 4 . Предлагаемый механизм включает образование сольватированного протонированного промежуточного соединения DCC-H 2 SO 4 () с последующей нуклеофильной атакой спиртовой группы на атом серы с образованием сложного моносульфатного эфира и дициклогексилмочевины.
Реакция показала зависящую от концентрации региоселективность в отношении спиртов. В разбавленных условиях сульфатируются только беспрепятственные гидроксильные группы, в то время как более высокие концентрации приводят к персульфатированным продуктам. 43 , 44 Например, в разбавленных условиях фенольная группа эстрона или эстрадиол-17β-ацетата не могла быть сульфатирована, тогда как в случае эстрадиола и кортикостерона был получен только один продукт, меченный 35 S. предполагая, что алифатические беспрепятственные 1 ° или 2 ° спирты предпочтительно сульфатированы. 44 Аналогичным образом сульфатирование метил α- и β-d-галактопиранозидов и 4- O -β-d-галактопиранозил-3,6-ангидро-1-галактозодиметилацеталь привело в основном к 6- O -сульфатный продукт. 45 Стерическая масса комплекса DCC-H 2 SO 4 , вероятно, уменьшит доступность реагента для стерически затрудненных гидроксильных групп.
Универсальность этого протокола была проверена путем сульфатирования других функциональных групп, включая фенолы, меркаптаны, амины и оксимы.Эти группы можно сульфатировать с достаточно хорошими выходами, используя по существу идентичный протокол с небольшими модификациями. Тем не менее, эти функциональные группы обычно требуют более высокой концентрации реагентов. 44
Этот протокол также использовали для O -сульфатирования октапептида холецистокинина без защиты боковых цепей аминокислот. Максимальный выход 40% может быть достигнут только при 4-кратном избытке H 2 SO 4 и 40-кратном избытке DCC, что подчеркивает существующие проблемы. Очищенный сульфатированный октапептид 1 был активен в стимуляции секреции амилазы фрагментами поджелудочной железы крысы, и аминокислотный анализ подтвердил сульфатирование остатка тирозина в пептиде. 46 Аналогичным образом остаток тирозина синтетического додекапептида, созданный как имитатор гирудина, сульфатировали методом DCC-H 2 SO 4 . Сульфатированный имитатор гирудина показал на порядок более высокую ингибирующую активность в традиционных анализах свертывания, активированном частичном тромбопластиновом времени (APTT) и тромбиновом времени. 47
Очищенный сульфатированный октапептид 1 был активен в стимуляции секреции амилазы фрагментами поджелудочной железы крысы, и аминокислотный анализ подтвердил сульфатирование остатка тирозина в пептиде. 46 Аналогичным образом остаток тирозина синтетического додекапептида, созданный как имитатор гирудина, сульфатировали методом DCC-H 2 SO 4 . Сульфатированный имитатор гирудина показал на порядок более высокую ингибирующую активность в традиционных анализах свертывания, активированном частичном тромбопластиновом времени (APTT) и тромбиновом времени. 47
Хотя протокол DCC-опосредованного сульфатирования дает хорошие выходы моноалкилсульфатов, образование относительно нерастворимой дициклогексилмочевины затрудняет прямое выделение сульфатированного продукта. Для растворения дициклогексилмочевины требуются довольно большие объемы метанола, особенно во время колоночной хроматографии на ДЭАЭ-целлюлозе. 48 Чтобы облегчить выделение, были исследованы несколько производных карбодиимида. Ароматические производные карбодиимидов обычно давали низкие выходы конечного сульфатированного продукта в отличие от производных с алифатическими группами.Наилучшие выходы были отмечены при использовании метил-циклогексил-3- (2-морфолиноэтил) карбодиимида- p -толуолсульфоната 2 , который высвобождает более растворимое в воде производное карбодиимида. Параллельно исследовали условия реакции с использованием ТГФ, диоксана и спиртов в качестве растворителей. Хотя моноалкилсульфаты были основными продуктами с ТГФ и диоксаном, было получено много нежелательных побочных продуктов, и реакции были неконтролируемыми. Когда спирты использовались как в качестве растворителя, так и в качестве реагента, образовывались моно- и диалкилсульфаты. 49
2.3 Сульфатирование с использованием комплексов триоксида серы и амина
Основание DCC / H 2 SO 4 не поддается сульфатированию для многих чувствительных каркасов, учитывая сильную кислотность серной кислоты, в то время как прямое сульфатирование спиртовой или фенольные группы, использующие триоксид серы (жидкость или газ), чреваты другими многочисленными проблемами, включая полимеризацию и сложность обращения с SO 3 . 43 Таким образом, SO 3 предпочтительно используется в качестве аддукта с молекулами, содержащими амин, амид, простой эфир или фосфат.Эти органические комплексы относительно легко приготовить, барботируя газ SO 3 в раствор предпочтительного органического основания или добавляя основание к суспензии SO 3 -органика; 50 твердые при комнатной температуре; и относительно стабильны при высоких температурах. Эти комплексы использовались для сульфатирования различных каркасов, содержащих спиртовые, фенольные, аминные, тиоловые и другие функциональные группы. Комплексы SO 3 с органическими основаниями, включая пиридин (Py), триметиламин (NMe 3 ) и триэтиламин (NEt 3 ), или амиды, такие как ДМФ, обычно находят широкое применение. 51 — 55
43 Таким образом, SO 3 предпочтительно используется в качестве аддукта с молекулами, содержащими амин, амид, простой эфир или фосфат.Эти органические комплексы относительно легко приготовить, барботируя газ SO 3 в раствор предпочтительного органического основания или добавляя основание к суспензии SO 3 -органика; 50 твердые при комнатной температуре; и относительно стабильны при высоких температурах. Эти комплексы использовались для сульфатирования различных каркасов, содержащих спиртовые, фенольные, аминные, тиоловые и другие функциональные группы. Комплексы SO 3 с органическими основаниями, включая пиридин (Py), триметиламин (NMe 3 ) и триэтиламин (NEt 3 ), или амиды, такие как ДМФ, обычно находят широкое применение. 51 — 55
Комплексы NMe 3 и NEt 3 с SO 3 , по-видимому, хорошо подходят для сульфатирования спиртовых групп, присутствующих в углеводах, стероидах и алифатических или алициклических каркасах. Например, Kakiyama et al. сообщает о химическом синтезе 3β-сульфоокси-7β-гидрокси-24-нор-5-холеновой кислоты 3 в качестве внутреннего стандарта для масс-спектрометрического анализа аномальных Δ 5 -мобильных кислот, возникающих при болезни Ниманна-Пика. 56 Моносульфатированный стероид был синтезирован с выходом 76% с использованием 5 эквивалентов комплекса SO 3 -NMe 3 на группу –ОН в сухом пиридине при комнатной температуре в течение 1 часа. Другим примером является синтез 2-сульфатированной формы α-1-идуронат гликозидов с использованием 1,5 эквивалента SO 3 -NMe 3 на группу -ОН в сухом ДМФ при 55 ° C в течение 24 часов. 57 Был приготовлен длинный ряд стероидных сульфатов с использованием комплекса SO 3 -NEt 3 , в котором наблюдалось селективное сульфатирование беспрепятственных гидроксильных групп при комнатной температуре, а нагревание до 70-95 ° C приводило к сульфатированию затрудненных гидроксильных групп. алкогольные группы. 58 Полигидроксистероиды также были сульфатированы с использованием 1,5 эквивалента SO 3 -NEt 3 на гидроксильную группу при 95 ° C. 59 Высокосульфатированные производные β-d-глюкопиранозида были синтезированы с различными выходами 22–86% с комплексом SO 3 -NMe 3 при 70 ° C в сухом ДМФ. 60
алкогольные группы. 58 Полигидроксистероиды также были сульфатированы с использованием 1,5 эквивалента SO 3 -NEt 3 на гидроксильную группу при 95 ° C. 59 Высокосульфатированные производные β-d-глюкопиранозида были синтезированы с различными выходами 22–86% с комплексом SO 3 -NMe 3 при 70 ° C в сухом ДМФ. 60
Каркасы на основе фенольных структур и содержащие более кислые -ОН-группы, по-видимому, лучше сульфатируются комплексами SO 3 с более слабыми основаниями, такими как пиридин и ДМФ.Дополнительные соображения также играют роль, включая стабильность полученной четвертичной соли, легкость очистки продукта и простоту получения сульфатирующего комплекса. Например, было бы предпочтительно сульфатировать тирозин в нейтральных или слабощелочных условиях. Fujii и др. . сообщить SO 3 -Py комплекс как более подходящий сульфатирующий агент, чем ацетилсульфат пиридиния для сульфатирования тирозина. 61 Тем не менее, сульфатирование с помощью SO 3 -Py, как известно, приводит к значительному окрашиванию, а комплекс SO 3 -Py плохо растворяется в воде или эфире, что затрудняет обработку.Futaki и др. . сообщают, что сульфатирование Boc-тирозин-OH комплексом SO 3 -DMF (соотношение 1: 5) при 25 ° C дает на 20% более высокие выходы, чем комплекс SO 3 -Py в аналогичных условиях. ДМФ является более слабым основанием, чем пиридин, что означает, что частичный положительный заряд на атоме серы комплекса SO 3 -ДМФ будет больше, чем в комплексе SO 3 -Py. Таким образом, вероятно, что нуклеофильная атака на комплекс SO 3 -ДМФ будет более благоприятной, что приведет к более высоким выходам. 62
SO 3 -Py-комплекс наиболее часто используется для сульфатирования углеводных каркасов. Popek et al. получили 2,3: 4,5-ди- O -изопропилиден-β-d-фруктопираноза-1-сульфат 4 с использованием комплекса SO 3 -Py при 55 ° C с выходом ~ 80%. 63 Другой характерный пример — синтез 2-сульфатов глюкозы и галактозы, в котором также используется комплекс SO 3 -Py при комнатной температуре в течение 20 — 36 часов. 64 Аналогичным образом, наиболее часто использовался синтез пентасахарида гепарина и его производных комплексов SO 3 -NMe 3 и SO 3 -Py. 16 , 65 , 66 В одном протоколе O -сульфатирование выполнялось одновременно в пяти положениях (блок D: 6-OSO 3 — , блок F: 3 и 6 -OSO 3 —, блок G: 2-OSO 3 —, блок H: 6-OSO 3 —) с выходом 85% с использованием 2.5 эквивалентов на –ОН комплекса SO 3 -NMe 3 (). После O -сульфатирования было достигнуто тройное N -сульфатирование с 3 эквивалентами комплекса SO 3 -Py на группу –NH 2 с выходом 63% (D-единица: 2-NSO 3 — , Блок F: 2-NSO 3 —, блок H: 2-NSO 3 —). Интересно отметить, что тройное сульфатирование N было достигнуто в H 2 O при pH 9,5 в присутствии экспонированных групп –OH, что указывает на большую региоселективность распознавания аминогрупп ().В недавнем отчете достигается одновременное сульфатирование в семи положениях (блок D: 6-OSO 3 — , блок F: 2, 3 и 6-OSO 3 — , блок H: 2, 3 и 6-OSO 3 —) для синтеза идрапаринукса в одну стадию с использованием избытка SO 3 -NEt 3 с выходом 93% (не показано), что следует рассматривать как достижение с точки зрения синтеза. 67 Наконец, Tully et al. синтезировал тетрасахарид, несущий две сульфатные группы в положениях 4- и -6 единицы D-галактозамина (), минимальный структурный мотив в хондроитинсульфате, необходимый для стимуляции роста нейронов, с использованием 10 эквивалентов SO 3 -NMe 3 на группу –ОН в ДМФА при 50 ° C в течение 2 часов.
63 Другой характерный пример — синтез 2-сульфатов глюкозы и галактозы, в котором также используется комплекс SO 3 -Py при комнатной температуре в течение 20 — 36 часов. 64 Аналогичным образом, наиболее часто использовался синтез пентасахарида гепарина и его производных комплексов SO 3 -NMe 3 и SO 3 -Py. 16 , 65 , 66 В одном протоколе O -сульфатирование выполнялось одновременно в пяти положениях (блок D: 6-OSO 3 — , блок F: 3 и 6 -OSO 3 —, блок G: 2-OSO 3 —, блок H: 6-OSO 3 —) с выходом 85% с использованием 2.5 эквивалентов на –ОН комплекса SO 3 -NMe 3 (). После O -сульфатирования было достигнуто тройное N -сульфатирование с 3 эквивалентами комплекса SO 3 -Py на группу –NH 2 с выходом 63% (D-единица: 2-NSO 3 — , Блок F: 2-NSO 3 —, блок H: 2-NSO 3 —). Интересно отметить, что тройное сульфатирование N было достигнуто в H 2 O при pH 9,5 в присутствии экспонированных групп –OH, что указывает на большую региоселективность распознавания аминогрупп ().В недавнем отчете достигается одновременное сульфатирование в семи положениях (блок D: 6-OSO 3 — , блок F: 2, 3 и 6-OSO 3 — , блок H: 2, 3 и 6-OSO 3 —) для синтеза идрапаринукса в одну стадию с использованием избытка SO 3 -NEt 3 с выходом 93% (не показано), что следует рассматривать как достижение с точки зрения синтеза. 67 Наконец, Tully et al. синтезировал тетрасахарид, несущий две сульфатные группы в положениях 4- и -6 единицы D-галактозамина (), минимальный структурный мотив в хондроитинсульфате, необходимый для стимуляции роста нейронов, с использованием 10 эквивалентов SO 3 -NMe 3 на группу –ОН в ДМФА при 50 ° C в течение 2 часов. 54
Недавно был разработан протокол на основе микроволнового излучения для увеличения скорости сульфатирования фенольных структур, особенно с несколькими фенольными группами. 34 Пер-сульфатирование небольших полифенольных каркасов обычно затруднено из-за анионной перенаселенности, а также из-за пониженной устойчивости высокосульфатированных продуктов к высоким температурам. Было высказано предположение, что микроволны могут вызвать значительное увеличение скорости, потому что сульфатированные промежуточные соединения могут связываться с микроволнами посредством ионной проводимости.В качестве растворителя использовался ацетонитрил вместо обычно используемого ДМФА из-за его благоприятного воздействия на микроволны и легкости испарения. Кроме того, было предложено присутствие свободного основания в реакционной смеси для ускорения сложной реакции пер-сульфатирования. Оптимальные результаты были достигнуты при использовании комплекса SO 3 -амин (-NR 3 или -Py, где R = Me или Et) приблизительно в 6-10-кратном молярном соотношении на фенольную группу в присутствии микроволн при 100 ° C. (). В этих условиях персульфатированные продукты могут быть выделены с выходом ~ 70–95%. 34 Особо следует отметить синтез переполненной 3,4,5-трисульфатной структуры, которую практически невозможно выделить с помощью традиционных протоколов сульфатирования.
Сульфатирование с помощью микроволн открыло новые возможности для доступа к полисульфатированным органическим соединениям, имитирующим гликозаминогликаны. Этот протокол, по-видимому, допускает использование ряда функциональных групп, таких как амиды, сложные эфиры, альдегиды, а также алкены. Кроме того, высокий выход продуктов делает метод удобным для построения библиотеки сульфатированных соединений.Метод может быть применен единообразно к синтезу моногексасульфатированных соединений, что важно, учитывая, что отталкивающие внутримолекулярные силы, как полагают, ограничивают полисульфатирование, приводящее к смеси частично сульфатированных продуктов. Как спиртовые, так и фенольные гидроксильные группы могут быть одинаково хорошо сульфатированы с использованием комплекса SO 3 -Py в качестве сульфатирующего агента. Этот метод, по-видимому, обеспечивает получение пер-сульфатированного продукта высокой чистоты с использованием одноступенчатой водной фильтрационной колонки G-10.Этот метод особенно удобен для количественного выделения небольших количеств (<10 мг) пер-сульфатированных продуктов и может быть расширен. Недавно этот протокол был успешно применен в синтезе несахаридных аллостерических активаторов антитромбина. 30 Применение микроволнового сульфатирования к аминам, тиолам и другим функциональным группам остается неизученным.
Как спиртовые, так и фенольные гидроксильные группы могут быть одинаково хорошо сульфатированы с использованием комплекса SO 3 -Py в качестве сульфатирующего агента. Этот метод, по-видимому, обеспечивает получение пер-сульфатированного продукта высокой чистоты с использованием одноступенчатой водной фильтрационной колонки G-10.Этот метод особенно удобен для количественного выделения небольших количеств (<10 мг) пер-сульфатированных продуктов и может быть расширен. Недавно этот протокол был успешно применен в синтезе несахаридных аллостерических активаторов антитромбина. 30 Применение микроволнового сульфатирования к аминам, тиолам и другим функциональным группам остается неизученным.
В отличие от описанного выше сульфатирования с помощью микроволнового излучения, которое можно отнести к категории высокотемпературных реакций, катализируемых основными катализаторами, Krylov et al. недавно сообщили о низкотемпературной реакции сульфатирования, катализируемой кислотой. 68 Общий протокол включает добавление комплекса SO 3 -NEt 3 к раствору полиспирта в ДМФ с последующим добавлением трифликовой кислоты (1,6–3,0 экв. / Группа OH) при -20 ° C. . Предлагаемый механизм заключается в том, что трифликовая кислота высвобождает SO 3 из аминного комплекса in situ и устраняет необходимость в высоких температурах. Этот подход был использован для пер- неасульфатированная форма олигосахарида ().Выходы пер-сульфатированных продуктов были похвальными от 53 до 77% в зависимости от структуры реагента. 68
2.4 Стратегии защиты / снятия защиты
Несмотря на успех стратегии прямого сульфатирования, синтез сложных молекул, содержащих несколько сульфатных групп, может оказаться сложной задачей. Нерастворимость сульфатированных молекул в органических растворителях и ограниченное развитие химических превращений на водной основе могут создавать значительные препятствия для синтеза сложных сульфатированных молекул. Кроме того, подозревается кислотная стабильность сульфатированных молекул. 36 Следовательно, растет интерес к разработке стратегий защиты / снятия защиты, в которых сульфатные группы вводятся в целевой каркас в замаскированной форме на промежуточном этапе. После соответствующих преобразований демаскирование сульфатной группы достигается за счет простой стадии снятия защиты. Это привлекательный подход, поскольку промежуточное соединение, содержащее замаскированный сульфат, обычно может быть очищено с использованием традиционных методов синтеза, подробно охарактеризовано с использованием стандартных спектроскопических инструментов и обычно устойчиво к более широкому диапазону превращений функциональных групп.
Кроме того, подозревается кислотная стабильность сульфатированных молекул. 36 Следовательно, растет интерес к разработке стратегий защиты / снятия защиты, в которых сульфатные группы вводятся в целевой каркас в замаскированной форме на промежуточном этапе. После соответствующих преобразований демаскирование сульфатной группы достигается за счет простой стадии снятия защиты. Это привлекательный подход, поскольку промежуточное соединение, содержащее замаскированный сульфат, обычно может быть очищено с использованием традиционных методов синтеза, подробно охарактеризовано с использованием стандартных спектроскопических инструментов и обычно устойчиво к более широкому диапазону превращений функциональных групп.
Пенни и Перлин описывают стратегию использования фенилхлорсульфата для введения замаскированного сульфата в моносахариды. 69 Взаимодействие фенилхлорсульфата с 1,2: 5,6-ди- O -изопропилиден-α-D-глюкофураноза () дает соответствующую сульфатированную форму с выходом 75%. Удаление фенильной группы осуществляли каталитическим гидрированием оксида платины в щелочных условиях. Важно отметить, что фенильная группа сначала пергидрируется до циклогексильной группы, которая подвергается циклоалкильному расщеплению с высвобождением циклогексанола и желаемой сульфатированной D-глюкофуранозы. 69 Можно ожидать, что замаскированный промежуточный сульфат, фенилмоносахарилсульфатный диэфир, претерпит ряд превращений, включая селективный кислотный гидролиз, ацетолиз, деацетилирование и опосредованное фтором удаление триалкилсилильных заместителей, что может облегчить важные структурные модификации. Однако сообщения об использовании такой возможности в синтезе сульфатированных сахаридов в литературе ограничены. 70 Вероятная причина этого состояния — низкий или непостоянный выход стадии снятия защиты.
Для устранения этого недостатка был разработан новый протокол, включающий 2,2,2-трифторэтильную защитную группу. 71 В этой стратегии трифторэтильная группа была введена путем обработки сульфатных моноэфиров углеводов 2,2,2-трифтордиазоэтаном, высокотоксичным и потенциально взрывоопасным агентом. После желаемых манипуляций со структурой углеводов трифторэтильную защитную группу удаляли с использованием трет-бутоксида калия при высокой температуре. Важно отметить, что условия демаскировки в обоих вышеупомянутых методах являются сильными, что может быть несовместимо с некоторыми чувствительными структурами.
71 В этой стратегии трифторэтильная группа была введена путем обработки сульфатных моноэфиров углеводов 2,2,2-трифтордиазоэтаном, высокотоксичным и потенциально взрывоопасным агентом. После желаемых манипуляций со структурой углеводов трифторэтильную защитную группу удаляли с использованием трет-бутоксида калия при высокой температуре. Важно отметить, что условия демаскировки в обоих вышеупомянутых методах являются сильными, что может быть несовместимо с некоторыми чувствительными структурами.
Taylor и соавторы описали использование родственной группы, 2,2,2-трихлорэтильной (TCE) группы, в качестве предпочтительной защитной группы для синтеза арилсульфатов. ТХЭ-защищенные сульфатные эфиры могут быть получены с высокими выходами из исходных фенолов с 2,2,2-трихлорэтилхлорсульфатом (TCECS) в присутствии NEt 3 . 72 С образовавшихся сложных эфиров арилдисульфата TCE можно легко снять защиту с превосходными выходами в нейтральных условиях с помощью Pd / C и формиата аммония или формиата цинка и аммония.Этот подход был успешно применен к синтезу производных сульфата эстрона, которые было трудно получить с помощью других методологий (). Условия деблокирования были несовместимы с функциональными группами, чувствительными к восстановителям. Промежуточный сложный диэфир сульфата был устойчив к сильной кислоте и слабому основанию, но реагировал с нуклеофилами или сильными органическими основаниями. Эта стратегия была использована Gunnarsson et al. для синтеза пер-сульфатированных флавоноидов, которые проявляли интересные свойства ингибирования фактора Ха () 73
Вышеупомянутый протокол защиты TCE, по-видимому, не работает для некоторых углеводов.Реакция TCECS с диизопропилиден-D-глюкозой давала соответствующий хлоросахар в различных условиях. 74 Чтобы избежать образования хлорсахара, в качестве сульфатирующего агента был выбран трифлат сульфурилимидазолия. Было высказано предположение, что замена хлоридной группы другой хорошей уходящей группой, которая не обладает нуклеофильными свойствами, будет способствовать защите сахаридов на основе TCE. Реакция TCECS с имидазолом давала соответствующий сульфурилимидазол с выходом 86%, который при дальнейшей обработке метилтрифлатом приводил к количественному осаждению трифлата имидазолиния. 74 , 75 При использовании этого агента в 2-5-кратном избытке по сравнению с сахаридом в присутствии N -метилимидазола первичные и вторичные гидроксильные группы сульфатировались с хорошими или превосходными выходами при комнатной температуре в пределах 16– 48 часов (). Основания, такие как NEt 3 , пиридин, 2,6-лутидин, пиперидин, оказались значительно менее эффективными. 74
Реакция TCECS с имидазолом давала соответствующий сульфурилимидазол с выходом 86%, который при дальнейшей обработке метилтрифлатом приводил к количественному осаждению трифлата имидазолиния. 74 , 75 При использовании этого агента в 2-5-кратном избытке по сравнению с сахаридом в присутствии N -метилимидазола первичные и вторичные гидроксильные группы сульфатировались с хорошими или превосходными выходами при комнатной температуре в пределах 16– 48 часов (). Основания, такие как NEt 3 , пиридин, 2,6-лутидин, пиперидин, оказались значительно менее эффективными. 74
Как упоминалось ранее, с сахаридов, защищенных ТХЭ, можно снять защиту для образования сульфатированных углеводов с хорошими выходами, используя восстанавливающий агент на основе формиата цинка и аммония в метаноле. 74 Разоблачение сульфатных групп можно также проводить с помощью Pd / C и восстановителя формиата аммония, однако выходы были ниже. Особым преимуществом этого метода было то, что неочищенный сульфатированный продукт был почти чистым с небольшими неорганическими примесями, которые можно было удалить, пропустив продукт через короткую колонку с диоксидом кремния. Сульфаты, защищенные TCE, были стабильны во многих реакционных условиях, обычно встречающихся в химии углеводов, таких как ZnCl 2 / уксусная кислота / уксусный ангидрид — опосредованное дебензилирование / ацетилирование, деацетилирование метоксидом натрия, раскрытие бензилиденового цикла трифторметансульфонилом или PhBCl 2 в присутствии Et 3 SiH и образование производного трихлорацетимидата с использованием каталитического DBU. 74
Была сделана попытка объединить реакцию сульфатирования на основе ТХЭ с твердофазным пептидным синтезом (SPPS). Введение тирозина, защищенного TCE, в процесс SPPS оказалось хорошим началом. 76 Защитная группа TCE выдерживает жесткую кислотную обработку, связанную с высвобождением синтезированного пептида из смолы, а также может быть легко удалена в мягких восстановительных условиях. Тем не менее, он не так устойчив к органическим основаниям, которые обычно используются для удаления защитной группы 9-флуоренилметоксикарбонила (Fmoc) во время SPPS, таким как пиперидин, морфолин или DBU.Ловушка вдохновила Али и др. для разработки родственной защитной группы, дихлорвинильной (DCV) группы (см. Соединение 5 ), для SPPS. DCV-защищенный тирозин может быть легко синтезирован, он может выдерживать широкий спектр реакций, в частности, опосредованное трифторуксусной кислотой высвобождение пептида и опосредованное 2-метилпиперидином снятие защиты с Fmoc. Кроме того, его можно удалить с помощью 10% Pd / C и H 2 (газ) или формиата аммония в MeOH при комнатной температуре. Доказано, что этот метод эффективен при синтезе моносульфатированного гексапептида (выход 71%), трисульфатированного октапептида (выход 46%), моносульфатированного октапептида (выход 63%), дисульфатированного 22-мера (выход 58%) и тетрасульфатированного 20-мера. (Выход 39%). 76
Тем не менее, он не так устойчив к органическим основаниям, которые обычно используются для удаления защитной группы 9-флуоренилметоксикарбонила (Fmoc) во время SPPS, таким как пиперидин, морфолин или DBU.Ловушка вдохновила Али и др. для разработки родственной защитной группы, дихлорвинильной (DCV) группы (см. Соединение 5 ), для SPPS. DCV-защищенный тирозин может быть легко синтезирован, он может выдерживать широкий спектр реакций, в частности, опосредованное трифторуксусной кислотой высвобождение пептида и опосредованное 2-метилпиперидином снятие защиты с Fmoc. Кроме того, его можно удалить с помощью 10% Pd / C и H 2 (газ) или формиата аммония в MeOH при комнатной температуре. Доказано, что этот метод эффективен при синтезе моносульфатированного гексапептида (выход 71%), трисульфатированного октапептида (выход 46%), моносульфатированного октапептида (выход 63%), дисульфатированного 22-мера (выход 58%) и тетрасульфатированного 20-мера. (Выход 39%). 76
Симпсон и Видлански изучали алкилхлорсульфаты, особенно изобутил и неопентилхлорсульфаты, как защищенные формы сульфатов. 77 В этом подходе были исследованы неопентильные и изобутильные группы в качестве сульфатзащитных групп. Сульфатные диэфиры, содержащие эти защитные группы, могут быть без особого труда синтезированы из исходных фенолов или спиртов и неопентил- или изобутилхлорсульфатов с высокими выходами (> 70%) путем нуклеофильного замещения хлорид-иона.Было обнаружено, что неопентилированный сложный диэфир сульфата проявляет высокую стабильность к сильным кислотам и основаниям, что исключает эффективную стратегию защиты / снятия защиты. С другой стороны, изобутилированный сложный диэфир сульфата был предложен как устойчивый к сильным кислотам, но чувствительный к пиперидину. Селективные преимущества двух защитных групп включают способность противостоять условиям реакции защиты аминогруппы Fmoc и -трет, -бутоксикарбонил (Boc). Эти две группы также выдерживают условия гидрогенолиза (Pd / C и H 2 ) для снятия защиты с бензильных и бензилоксикарбонильных (Cbz) групп карбоновой кислоты и аминогруппы соответственно. Аналогичным образом, сложные диэфиры неопентила и изобутилсульфата выдерживают кислые водные условия, что предполагает их применимость в комплексном синтезе олигосахаридов, включающем стадии защиты / снятия защиты изопропилидена. Таким образом, в целом неопентил- и изобутилсульфатные защитные группы, по-видимому, обладают хорошими химическими свойствами для использования в синтезе углеводов и пептидов.
Аналогичным образом, сложные диэфиры неопентила и изобутилсульфата выдерживают кислые водные условия, что предполагает их применимость в комплексном синтезе олигосахаридов, включающем стадии защиты / снятия защиты изопропилидена. Таким образом, в целом неопентил- и изобутилсульфатные защитные группы, по-видимому, обладают хорошими химическими свойствами для использования в синтезе углеводов и пептидов.
Снятие защиты с неопентильной и изобутильной групп может осуществляться нуклеофильной реакцией в апротонных полярных растворителях.В частности, небольшие нуклеофилы, такие как азид и цианид в горячем ДМФ (60–70 ° C), эффективны для количественного удаления неопентильной группы из защищенных диэфиров арилсульфата, в то время как деблокирование с помощью NaI в горячем ацетоне (55 ° C) эффективно для сложные диэфиры изобутилаллсульфата. Это условие, по-видимому, является проблематичным для диэфиров изобутиларилсульфата, поскольку йодид может замещать феноксид посредством нуклеофильной атаки на атом серы. Чтобы избежать этой проблемы, был разработан тиоцианат натрия в кипящем с обратным холодильником ацетоне в присутствии основания (NEt 3 ). 77
2.5 Окисление сульфитилированием и высвобождение
Трехэтапная стратегия сульфатирования была разработана Хьюберсом и его сотрудниками на основе стратегии Гао и Шарплесса, которые сообщили о превращении вицинальных диолов в циклические сульфаты с помощью циклических сложных диэфиров сульфита. 78 Протокол выполняется в мягких условиях и требует количества реагентов, близких к стехиометрическому. Первая стадия включает образование алкилэтилсульфитного производного исходного спирта, которое окисляется с использованием периодата натрия и хлорида рутения III до их сульфатных диэфирных форм.Затем намеченные моноэфиры сульфата высвобождали с высокими выходами с использованием йодида натрия при температуре окружающей среды (). 79
Этот подход, описанный как протокол сульфитилирования-окисления, дает несколько преимуществ. Все три стадии являются стадиями с высоким выходом, и их продукты в большинстве случаев требуют минимальной очистки. Было обнаружено, что сульфитные и сульфатные эфиры испытанных спиртов неполярны, стабильны и легко растворяются в органических растворителях, что позволяет проводить традиционную хроматографическую очистку.Эта стратегия, по-видимому, в целом применима, поскольку было обнаружено, что она хорошо работает с рядом различных алифатических и вторичных спиртов, диолов, сахаров и ароматических спиртов. Применимость этого протокола была продемонстрирована в синтезе тетранатриевой соли метил-2,3,4,6-тетра- O -сульфонато-β- D -глюкопиранозида. Это тетрасульфатированное соединение было синтезировано ранее с выходом 41% с использованием комплекса SO 3 -NMe 3 , в то время как применение протокола сульфитилирования-окисления и высвобождения дало общий выход 77%. 60 , 79
Все три стадии являются стадиями с высоким выходом, и их продукты в большинстве случаев требуют минимальной очистки. Было обнаружено, что сульфитные и сульфатные эфиры испытанных спиртов неполярны, стабильны и легко растворяются в органических растворителях, что позволяет проводить традиционную хроматографическую очистку.Эта стратегия, по-видимому, в целом применима, поскольку было обнаружено, что она хорошо работает с рядом различных алифатических и вторичных спиртов, диолов, сахаров и ароматических спиртов. Применимость этого протокола была продемонстрирована в синтезе тетранатриевой соли метил-2,3,4,6-тетра- O -сульфонато-β- D -глюкопиранозида. Это тетрасульфатированное соединение было синтезировано ранее с выходом 41% с использованием комплекса SO 3 -NMe 3 , в то время как применение протокола сульфитилирования-окисления и высвобождения дало общий выход 77%. 60 , 79
Хотя этот протокол кажется многообещающим для синтеза высокосульфатных олигосахаридов, потенциал этилсульфитных эфиров в качестве предшественников сульфата требует подробного исследования, поскольку ацетилирование или силилирование, по-видимому, протекают хорошо, в то время как другие превращения, например, , бензилирование и деацетонирование привели к полному разложению. 79
2.6 Региоселективное сульфатирование
Большинство реакций сульфатирования, о которых сообщалось на сегодняшний день, вращаются вокруг моносульфатирования или пер-сульфатирования соответствующих реагентов.Однако с точки зрения метаболизма сульфатирование только выбранных спиртов или аминов из нескольких доступных было бы более актуальным и привлекательным. Хотя структурные свойства субстратов, такие как стерические ограничения, действительно вызывают некоторую селективность, были разработаны специальные инструменты для создания региоселективности в реакциях сульфатирования.
Хангерфорд и др. . сообщают о региоселективном сульфатировании стероидного каркаса, особенно в 3- и 16-положениях в присутствии нескольких гидроксильных групп, с использованием подхода на основе боронатного эфира. 80 Сульфатированные стероиды C-3 и C-16 желательны в качестве стандартов для метаболитов анаболических стероидов, которыми обычно злоупотребляют в высококонкурентном мире спорта. Подход региоселективного сульфатирования использует образование 16β, 17β-боронатного эфира для введения сульфата по доступной гидроксильной группе. Для получения 16β-моносульфатированного стероида в 3-положение вводили ортогональную защитную группу, то есть TBDMS, с последующим окислительным удалением боронатного эфира и предпочтительным сульфатированием стерически более доступного 16β-положения в присутствии 17β-ОН с использованием SO 3 -Py ().Используя эти две схемы, 3-моносульфатные и 16β-моносульфатные производные 3β, 16β, 17β-тригидрокси-17α-метил-5α-андростана были синтезированы с общим выходом 79 и 69% соответственно. 80
сообщают о региоселективном сульфатировании стероидного каркаса, особенно в 3- и 16-положениях в присутствии нескольких гидроксильных групп, с использованием подхода на основе боронатного эфира. 80 Сульфатированные стероиды C-3 и C-16 желательны в качестве стандартов для метаболитов анаболических стероидов, которыми обычно злоупотребляют в высококонкурентном мире спорта. Подход региоселективного сульфатирования использует образование 16β, 17β-боронатного эфира для введения сульфата по доступной гидроксильной группе. Для получения 16β-моносульфатированного стероида в 3-положение вводили ортогональную защитную группу, то есть TBDMS, с последующим окислительным удалением боронатного эфира и предпочтительным сульфатированием стерически более доступного 16β-положения в присутствии 17β-ОН с использованием SO 3 -Py ().Используя эти две схемы, 3-моносульфатные и 16β-моносульфатные производные 3β, 16β, 17β-тригидрокси-17α-метил-5α-андростана были синтезированы с общим выходом 79 и 69% соответственно. 80
Еще одним реагентом, который был исследован для региоселективного сульфирования полисахаридов, является триметилхлорсилан. Было показано, что этот реагент полезен в селективном синтезе либо С-6, либо С-2 сульфатированного ангидроглюкозного звена целлюлозы путем внедрения SO 3 в связь –O-Si– триметилсилилцеллюлозы. 81 Механизм этой реакции инициируется нуклеофильной атакой, обеспечиваемой одним из атомов кислорода SO 3 на электроположительный Si в целлюлозе, что приводит к образованию соответствующего сложного диэфира целлюлозы триметилсилилсульфата. Чтобы демаскировать сульфатную группу, основная обработка в метаноле расщепляет сложный эфир триметилсульфата, снова используя электрофильность атома Si. Сообщалось о нескольких факторах, объясняющих наблюдаемую селективность.Однако тип партнера SO 3 в сульфатирующем комплексе и полярность –O-Si– в первую очередь определили место сульфатирования.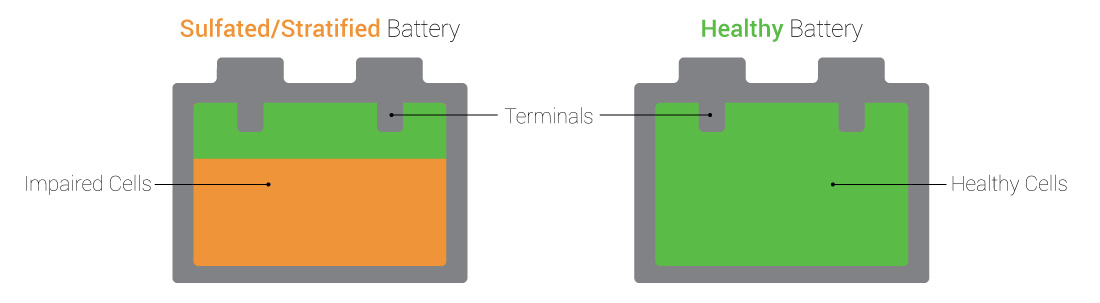 Например, SO 3 в комплексе с ДМФ предпочитает наименее стерически затрудненное положение, которым является C-6, тогда как SO 3 в комплексе с NEt 3 предпочитает наиболее полярное положение –O-Si–, то есть C -2 в полисахариде (). 81
Например, SO 3 в комплексе с ДМФ предпочитает наименее стерически затрудненное положение, которым является C-6, тогда как SO 3 в комплексе с NEt 3 предпочитает наиболее полярное положение –O-Si–, то есть C -2 в полисахариде (). 81
Аналогичным образом было обнаружено, что региоселективный синтез 3’-сульфатированного сиалила Льюиса x из соответствующего 3 ’, 4’-диолтрисахарида 6 зависит от температуры ().Когда диол 6 сульфатировали комплексом SO 3 -Py в ДМФ в течение одного часа при 0 ° C с последующей обработкой метоксидом натрия в метаноле, был получен соответствующий 4′-сульфатированный продукт 7 с общим выходом около 73%. С другой стороны, когда 6 сульфатировали при комнатной температуре, было обнаружено, что продукт представляет собой 3 ’, 4’-дисульфат 8 с общим выходом 66%. Для региоселективного синтеза 3’-сульфатированного производного 9 была введена дополнительная стадия защиты для блокирования 4’-положения с последующим сульфатированием при 0 ° C и снятием блокировки с 4-защитной группы (). 82
Guilbert et al. сообщают об интересном примере региоселективного сульфатирования в синтезе сульфатированных олигосахаридов через с образованием станнильных комплексов. 83 Предпочтительное образование станнильных комплексов цис- диолами было использовано для введения сульфатных групп в стерически менее доступные положения. Тиофениллактозид 10 был преобразован в станниленацеталь оксидом дибутилолова, за которым следовало сульфатирование комплексом SO 3 -NMe 3 в диоксане с получением 3′-сульфатированного лактозида 11 и 3 ‘, 6’- дисульфатированный лактозид 12 с выходами 76 и 10% соответственно ().В отсутствие станнильного комплекса образовывались 6- и 6’-моно- и дисульфатированные сложные эфиры, что указывает на склонность к нормальной реакции с образованием преимущественно сульфатных стерически беспрепятственных групп. Этот селективный метод был также полезен в хемосинтетическом синтезе 3’-сульфо N -ацетиллактозаминида. Интересно, что региоселективность изменилась с мальтозидом, который предпочтительно давал 2’-сульфатированное производное. Региоселективность, по-видимому, возникает из-за повышенной реакционной способности 2’-гидроксильной группы.Кроме того, диокси-конфигурация C1’-C2 ’ cis рядом с α-гликозидной связью, по-видимому, также вносит свой вклад, потому что β-гликозидная связь в лактозиде, по-видимому, способствует 3’-сульфатированию. 57 , 83
Этот селективный метод был также полезен в хемосинтетическом синтезе 3’-сульфо N -ацетиллактозаминида. Интересно, что региоселективность изменилась с мальтозидом, который предпочтительно давал 2’-сульфатированное производное. Региоселективность, по-видимому, возникает из-за повышенной реакционной способности 2’-гидроксильной группы.Кроме того, диокси-конфигурация C1’-C2 ’ cis рядом с α-гликозидной связью, по-видимому, также вносит свой вклад, потому что β-гликозидная связь в лактозиде, по-видимому, способствует 3’-сульфатированию. 57 , 83
Оксид дибутилолова нашел дополнительное применение в селективном 2- O -сульфатировании α-l-идуронат гликозидов, которые используются в качестве субстратов в анализе идуронат-2-сульфатазы Известно, что фермент играет важную роль в синдроме Хантера. 57 Селективное 2- O -сульфатирование α-1-идуроната согласуется с предыдущими сообщениями о селективном 2- O -бензоилировании и ацетилировании моносахаридов и дисахаридов, соответственно, после обработки Bu 2 SnO . Такая обработка приводила к образованию 2 ’, 4’-станниленовых ацеталей, которые способствовали региоселективному бензоилированию и ацетилированию в 2’-положении соответствующими хлоридами. 84 , 85 Как упоминалось ранее, это подчеркивает повышенную реакционную способность положения 2 в α-гликозидах.Наконец, сообщалось о селективном 4- O -сульфатировании ксилопиранозида, ксилобиозида и ксилотриозида с использованием SO 3 -NMe 3 . 86 В нескольких сообщениях предложен механизм региоселективной реакционной способности ксилопиранозидов, опосредованной дибутилоловым оксидом, по отношению к электрофильным реагентам. Однако необходима дальнейшая работа, чтобы более точно прийти к удовлетворительному механизму предпочтительного распознавания в этих субстратах, чтобы реакция была более применимой.
2.7 Разные подходы
Хотя S — и P -сульфаты не распространены в синтетической практике, они могут быть достигнуты по существу теми же протоколами, которые обсуждались выше для O — и N -сульфатов. Например, сложные эфиры тиосульфата обычно можно получить реакцией тиола с комплексом SO 3 в безводных условиях 87 или, в меньшей степени, с H 2 SO 4 / DCC. 88 Что касается синтеза сульфатофосфатов, то арилсульфатофосфаты относительно просты в приготовлении и были получены сульфатированием соответствующей арилфосфорной кислоты в безводном растворе с SO 3 -Py 89 или SO 3 -DMF. 90 С другой стороны, получение сульфатофосфатов нуклеозидов является более трудным из-за вероятности сульфатирования гидроксильных групп сахарного фрагмента. Аденозин-5′-сульфатофосфат был получен сульфатированием его исходного вещества с SO 3 -Py в водной среде (выход 5%), 91 с SO 3 -NEt 3 в безводных условиях (60–75 % выхода) 92 , а также с H 2 SO 4 / DCC (выход 20-25%), что привело к интенсивному сульфатированию гидроксильных групп сахара. 93
В некоторых случаях чувствительность исследуемого каркаса и доступность реагентов требуют изобретения нового протокола или реагента. Например, некоторые каркасы сульфатировали с использованием сульфата пиридиния / уксусного ангидрида. 94 Опосредованное аскорбат-2-сульфатом окислительное сульфатирование 95 и катализируемое Cu 2+ сульфатирование сообщалось для синтеза некоторых сульфатированных стероидов и углеводов. 96 Наконец, большинство вышеперечисленных методов вводят сульфатную группу в существующую группу -ОН.Напротив, персульфатное окисление Elb вводит сульфатную группу непосредственно в ароматическое кольцо путем обработки пероксидисульфатом в щелочных условиях. Окисление фенолов широко изучалось и, наиболее вероятно, включает нуклеофильную атаку резонансной формы p -карбанион феноксида на пероксидную связь в пероксидисульфат-ионе. 38
Окисление фенолов широко изучалось и, наиболее вероятно, включает нуклеофильную атаку резонансной формы p -карбанион феноксида на пероксидную связь в пероксидисульфат-ионе. 38
Интернализация тау-белка регулируется 6-O-сульфатом на гепарансульфат-протеогликанах (HSPG)
Chemicals
Гепарин, хондроитинсульфат, гепарансульфат и десульфатированные гепарины (Neoparin & Galen Labs Supplies).Dynasore Hydrate (Sigma). Hoechst (Thermo Scientific).
Очистка, мечение и фибрилляция белков
Тау-белок полной длины (2N4R, 1-441aa) очищали с небольшими модификациями ранее опубликованных протоколов 39 . Вкратце, тау 2N4R в плазмиде pRK172 экспрессировался в E . coli BL21 (DE3). Осадки клеток собирали и ресуспендировали в буфере для лизиса клеток (50 мМ MES pH 6,5, 5 мМ DTT, 1 мМ PMSF, 1 мМ EGTA) + таблетки полного ингибитора протеазы (Roche).Лизат обрабатывали ультразвуком, кипятили в течение 10 минут, а затем центрифугировали при 50 000 × g в течение 30 минут при 4 ° C. Затем супернатант осаждали сульфатом аммония (20% мас. / Об.) И центрифугировали при 20000 × g в течение 30 мин при 4 ° C. Осадок ресуспендировали в 4 мл буфера A MonoS (50 мМ MES pH 6,5, 50 мМ NaCl, 2 мМ DTT, 1 мМ PMSF, 1 мМ EGTA) и диализовали в течение ночи против того же буфера. Белок загружали в колонку MonoS (GE Healthcare) и элюировали линейным градиентом NaCl с использованием буфера B MonoS (буфер A + 1 M NaCl).Фракции, содержащие 2N4R тау, объединяли, концентрировали и диализовали в течение ночи в PBS, pH 7,4. Концентрацию белка определяли с помощью анализа BCA (Thermo Scientific).
Протеин был помечен Alexa Fluor® 488 или 647 сложным эфиром 5-SDP (Life Technologies) в соответствии с инструкциями поставщиков. После мечения добавляли 100 мМ глицина для гашения реакции и белки подвергали обессоливанию в колонках Zeba (Thermo Scientific) для удаления любой непрореагировавшей метки. Среднее количество добавленных этикеток было от 1 до 1. 5 моль / моль белка, как определено путем измерения флуоресценции и концентрации белка (A max x MW белка / [белок] x ε краситель ). Для получения тау-фибрилл и олигомеров 10 мкМ белка в PBS, 1 мМ DTT, pH 7,4, смешивали с гепарином (0,05 мг / мл) и инкубировали при встряхивании при 37 ° C. Образование олигомеров наблюдали через 4 часа встряхивания, тогда как образование фибрилл формировалось через 5 дней 13 . Для изготовления образцов фибрилл, обработанных ультразвуком, фибриллированный белок обрабатывали ультразвуком с использованием MiSonix Sonicator 4000 (QSonica, LLC) при 50% амплитуде в течение 60 импульсов длительностью 1 с.Мутация 2N4R (C291S, C322S) для удаления обоих остатков цистеина, важных для образования димера, позволила нам дополнительно подтвердить, что тау-мономер действительно может быть интернализован (данные не показаны).
5 моль / моль белка, как определено путем измерения флуоресценции и концентрации белка (A max x MW белка / [белок] x ε краситель ). Для получения тау-фибрилл и олигомеров 10 мкМ белка в PBS, 1 мМ DTT, pH 7,4, смешивали с гепарином (0,05 мг / мл) и инкубировали при встряхивании при 37 ° C. Образование олигомеров наблюдали через 4 часа встряхивания, тогда как образование фибрилл формировалось через 5 дней 13 . Для изготовления образцов фибрилл, обработанных ультразвуком, фибриллированный белок обрабатывали ультразвуком с использованием MiSonix Sonicator 4000 (QSonica, LLC) при 50% амплитуде в течение 60 импульсов длительностью 1 с.Мутация 2N4R (C291S, C322S) для удаления обоих остатков цистеина, важных для образования димера, позволила нам дополнительно подтвердить, что тау-мономер действительно может быть интернализован (данные не показаны).
Просвечивающая электронная микроскопия
Тау-фибриллы и обработанные ультразвуком фибриллы (1 мкМ) абсорбировали на медных сетках размером 200 меш, покрытых формваром, промывали и окрашивали 2% -ным раствором уранилацетата. Затем сетки получали изображение с помощью JEOL JEM-1230 (JEOL USA, Inc) при указанном увеличении.
Динамическое рассеяние света
Растворы белков (1 мкМ) отфильтровывали (0.45 мкм) и анализировали с помощью Zetasizer Nano ZS (Malvern). Зависящая от времени автокорреляционная функция фототока при фиксированном угле 175 ° регистрировалась каждые 10 с, с 15–20 сборами для каждого цикла и как минимум с тремя повторениями. Столбики ошибок, отображаемые на графиках DLS, были получены по стандартному отклонению (SD) между повторами.
Культура клеток, трансфекции и обработки
клеток h5 культивировали в среде DMEM с добавлением 10% FBS, 100 мкг / мл пенициллина / стрептомицина.Клетки SHSY-5Y культивировали в среде DMEM / F12 с добавлением 10% FBS, 100 мкг / мл пенициллина / стрептомицина. Клетки ReN-VM культивировали на планшетах с покрытием Matrigel (Corning) в среде DMEM / F12 с добавлением 2 мкг / мл гепарина (STEMCELL Technologies), 2% B27 (Life Technologies, 100 мкг / мл пенициллина / стрептомицина, 20 мкг / мл bFGF ( Stemgent), 20 мкг / мл EGF (Sigma). Культуры поддерживали в увлажненной атмосфере с 5% CO 2 при 37 ° C.Трансфекцию клеток h5 Sulf1 (Addgene # 13003) или Sulf2 (Addgene # 13004) проводили. выполняли с Lipofectamine 3000 (Invitrogen) в соответствии с инструкциями производителя, и клетки анализировали через 48 часов.Сверхэкспрессия была подтверждена иммуноцитохимическим методом с использованием эпитопа his tag и количественной ПЦР. Для конкурентных экспериментов гепарин (и различные производные) добавляли в среду непосредственно перед добавлением тау в указанных концентрациях.
Культуры поддерживали в увлажненной атмосфере с 5% CO 2 при 37 ° C.Трансфекцию клеток h5 Sulf1 (Addgene # 13003) или Sulf2 (Addgene # 13004) проводили. выполняли с Lipofectamine 3000 (Invitrogen) в соответствии с инструкциями производителя, и клетки анализировали через 48 часов.Сверхэкспрессия была подтверждена иммуноцитохимическим методом с использованием эпитопа his tag и количественной ПЦР. Для конкурентных экспериментов гепарин (и различные производные) добавляли в среду непосредственно перед добавлением тау в указанных концентрациях.
iPS культивирование и дифференциация
CRISPRi iPSc с индуцибельным TRE3G-dCas9KRAB-T2A-mCherry поддерживали в 6-луночных планшетах с покрытием Matrigel (Corning) со средой mTeSR1 (STEMCELL Technologies) и разделяли с помощью ReLeSR (STEMCELL Technologies) : 20 каждые 4–5 дней.Для дифференциации клетки CRISPRi были разделены с помощью Accutase и дважды инфицированы вирусом NeuroD1-IRES-eGFP-Puro (Addgene # 45567) согласно ранее опубликованным методам 40 . Для индукции экспрессии NeuroD1 добавляли доксициклин, и на следующий день клетки отбирали пуромицином (5 мкг / мл). После отбора клетки поднимали обработкой аккутазой и повторно помещали в 24-луночные планшеты, покрытые PEI, в соотношении 1:12. Через три дня среду заменили на нейрональную среду Brain Phys (STEMCELL Technologies) с доксициклином и AraC для удаления любых оставшихся делящихся клеток.На 8 день клетки инфицировали специфическими конструкциями sgRNA. iPS-нейроны анализировали между 14-18 днями зрелости, как описано ниже. Иммуноцитохимия использовалась для подтверждения свойств нейронов (дополнительный рис. 1e).
Проточная цитометрия
клеток h5 высевали по 50 000 клеток на лунку в 24-луночный планшет. На следующий день среду заменяли, и клетки обрабатывали различными концентрациями AF488-меченного тау-белка в течение 1 ч (если не указано иное) при 37 ° C. Для экспериментов по поглощению ReN-VM среду заменяли на DMEM / F12 без B27 или гепарина. Затем клетки дважды промывали PBS и обрабатывали трипсином для подъема клеток с планшета. Идентичные контрольные эксперименты были выполнены при 4 ° C, чтобы подтвердить, что белок тау был интернализован, а не просто прилипал к клеточной мембране. Поднятые клетки анализировали с использованием проточного цитометра Accuri-C6, и йодид пропидия использовали для исключения мертвых клеток из анализа.
Затем клетки дважды промывали PBS и обрабатывали трипсином для подъема клеток с планшета. Идентичные контрольные эксперименты были выполнены при 4 ° C, чтобы подтвердить, что белок тау был интернализован, а не просто прилипал к клеточной мембране. Поднятые клетки анализировали с использованием проточного цитометра Accuri-C6, и йодид пропидия использовали для исключения мертвых клеток из анализа.
CRISPRi screen
Мы создали стабильную линию клеток нейроглиомы h5 с поддержкой CRISPRi путем трансдукции клеток h5 лентивирусной плазмидой pHR-SFFV-dCas9-BFP-KRAB 41 и отбора поликлональной популяции BFP-экспрессирующих клеток с помощью FACS.Эти клетки трансдуцировали с помощью библиотеки sgRNA CRISPRi следующего поколения (подбиблиотека «Рак и апоптоз») 22 , и трансдуцированные клетки отбирали с использованием пуромицина (1 мкг / мл). Среду заменяли свежей DMEM, содержащей мономеры тау-белка, меченные AF488, в конечной концентрации 25 нМ в течение 1 ч при 37 ° C. Клетки дважды промывали, трипсинизировали и ресуспендировали в буфере FACS (PBS с 0,5% FBS). BD-FACAria II использовали для сортировки живых клеток на две популяции на основе верхней и нижней третей флуоресценции AF488; приблизительно 15 миллионов и 17 миллионов клеток были извлечены из популяций с высокой и низкой флуоресценцией соответственно.Полученную ДНК выделяли, кассету, кодирующую sgRNA, амплифицировали с помощью ПЦР, и относительное количество sgRNA определяли секвенированием следующего поколения, как описано ранее 21,24 . Мы проанализировали полученные данные, используя нашу ранее разработанную количественную структуру для объединенных генетических скринингов 23,24 . Статистическая значимость для каждого целевого сайта начала транскрипции была рассчитана с использованием U-критерия Манна-Уитни для сравнения фенотипов 5 sgRNAs, нацеленных на сайт запуска транскрипции, с распределением фенотипов 280 нецелевых sgRNAs в библиотеке.
ELISA
Гепарин был приобретен у AMSBio (AMS. HEP001-100), и все производные гепарина были приобретены у Neoparin (GT6011, GT6012, GT6013, GT6014, GT6020, GT6030). Производные гепарина / гепарина были биотинилированы путем взаимодействия их свободных аминов (оценочное содержание 1–5% для гепарина) с EZ-связью Sulfo-NHS-LC-Biotin (Thermo) в соответствии с протоколом производителя. Вкратце, гепарин / производные гепарина и биотиновый реагент объединяли в PBS (pH 7,4) и инкубировали при комнатной температуре в течение 1 часа.Избыток реагента удаляли, буфер заменяли на воду Milli-Q и образцы концентрировали центрифугированием на центробежных фильтрах Amicon Ultra-0,5 мл (Millipore, отсечение 3k). Для анализов ELISA биотинилированные гепарин / производные гепарина иммобилизовали на планшетах со стрептавидином с последующей 2-часовой инкубацией с тау-белком 2N4R, содержащим C-концевую метку myc (серия 10-кратных разведений). Связанный тау-белок детектировали с использованием антитела, конъюгированного с myc HRP (Bethyl, A190-105P), визуализировали с использованием субстрата TMB (R&D Systems) и количественно оценивали с помощью УФ-видимого излучения.Поглощение для каждой пластины измеряли при 450 и 550 нм. Измерение 550 нм представляет собой поправку на дефекты пластины и было вычтено из значений 450 нм. Данные были нормализованы для контроля гепарина и соответствовали математической модели связывания Хилла, где это необходимо, с использованием уравнения Y = B max * X H / ( K d H + X H ) , где H — наклон холма (переменная), X — концентрация тау, а B max — связывающий максимум.
HEP001-100), и все производные гепарина были приобретены у Neoparin (GT6011, GT6012, GT6013, GT6014, GT6020, GT6030). Производные гепарина / гепарина были биотинилированы путем взаимодействия их свободных аминов (оценочное содержание 1–5% для гепарина) с EZ-связью Sulfo-NHS-LC-Biotin (Thermo) в соответствии с протоколом производителя. Вкратце, гепарин / производные гепарина и биотиновый реагент объединяли в PBS (pH 7,4) и инкубировали при комнатной температуре в течение 1 часа.Избыток реагента удаляли, буфер заменяли на воду Milli-Q и образцы концентрировали центрифугированием на центробежных фильтрах Amicon Ultra-0,5 мл (Millipore, отсечение 3k). Для анализов ELISA биотинилированные гепарин / производные гепарина иммобилизовали на планшетах со стрептавидином с последующей 2-часовой инкубацией с тау-белком 2N4R, содержащим C-концевую метку myc (серия 10-кратных разведений). Связанный тау-белок детектировали с использованием антитела, конъюгированного с myc HRP (Bethyl, A190-105P), визуализировали с использованием субстрата TMB (R&D Systems) и количественно оценивали с помощью УФ-видимого излучения.Поглощение для каждой пластины измеряли при 450 и 550 нм. Измерение 550 нм представляет собой поправку на дефекты пластины и было вычтено из значений 450 нм. Данные были нормализованы для контроля гепарина и соответствовали математической модели связывания Хилла, где это необходимо, с использованием уравнения Y = B max * X H / ( K d H + X H ) , где H — наклон холма (переменная), X — концентрация тау, а B max — связывающий максимум.
Культивирование срезов мышей и измерения EPSP
Протоколы и процедуры были одобрены Комитетом по уходу и использованию институциональных животных Калифорнийского университета в Санта-Барбаре и выполнялись в соответствии с Руководством по уходу и использованию лабораторных животных национальных институтов здоровья. Культуры срезов получали, как описано ранее 27 . Возбуждающие постсинаптические потенциалы гиппокампа (ВПСП) измеряли с помощью многоэлектродной матрицы (МЭА).Стимулирующий ток вводился в область среза гиппокампа с помощью МЭА-электрода с величиной стимулирующего тока в диапазоне от 20 до 80 мкА. Затем измеряли ВПСП, записывая электрод в другой области среза гиппокампа. Меньшие токи стимула возбуждают меньшее количество клеток, и поэтому измеренные ВПСП имеют меньшую величину.
Культуры срезов получали, как описано ранее 27 . Возбуждающие постсинаптические потенциалы гиппокампа (ВПСП) измеряли с помощью многоэлектродной матрицы (МЭА).Стимулирующий ток вводился в область среза гиппокампа с помощью МЭА-электрода с величиной стимулирующего тока в диапазоне от 20 до 80 мкА. Затем измеряли ВПСП, записывая электрод в другой области среза гиппокампа. Меньшие токи стимула возбуждают меньшее количество клеток, и поэтому измеренные ВПСП имеют меньшую величину.
qPCR
Набор для экстракции РНК Purelink (Invitrogen) использовали для выделения РНК из образцов. Затем РНК (1 мкг) была преобразована в кДНК с использованием обратной транскриптазы III SuperScript (Invitrogen) в соответствии с инструкциями поставщика.Количественную ПЦР в реальном времени выполняли с использованием Power SYBR Green PCR Master Mix (Applied Biosystems) в соответствии с протоколом системы ПЦР в реальном времени QuantStudio TM 12 K Flex. Уровень мРНК GAPDH использовали для нормализации образцов.
Иммуноцитохимия
Клетки фиксировали 4% параформальдегидом в течение 15 мин при комнатной температуре с последующими тремя промываниями PBS. Клетки пермеабилизировали 0,25% тритоном X-100 в PBS и блокировали в течение 1 часа в блокирующем буфере при комнатной температуре (1% BSA, 300 мМ глицин, 0,1% желатин, 4% ослиная сыворотка в TBST).После блокирования клетки инкубировали с первичными антителами, разведенными в блокирующем буфере, в течение ночи при 4 ° C. На следующий день после того, как клетки были промыты трижды (по 5 минут каждый) 0,05% Tween-20 в PBS. Были использованы следующие первичные антитела: тау-46 (Invitrogen, 36400, 1: 1000), MAP2 (Millipore, AB5622, 1: 1000) и анти-his (Thermo Scientific, MA1-21315, 1: 1000). Вторичные антитела (Life Technologies, A21422, A21206, 1: 1000) инкубировали в течение 1 часа при комнатной температуре, трижды промывали 0,05% твин-20 в PBS и отображали с помощью микроскопа Olympus IX71 или Olympus Fluoview 1000 Spectral Confocal.
Анализ дисахаридов
Осадки клеток, сверхэкспрессирующих WT, Sulf1 и Sulf2, ресуспендировали в PBS и расщепляли проназой (конечная концентрация 2 мг / мл) в течение ночи при 37 ° C. Образцы пропускали через шприц-фильтр 0,22 мкм для удаления клеточных частиц и наносили на колонки с ДЭАЭ-целлюлозой, уравновешенные 0,2 М NaCl в PBS. Колонки тщательно промывали 0,2 M NaCl в PBS, GAG элюировали 1,0 M NaCl в PBS, и элюированные фракции объединяли, быстро замораживали и лиофилизировали.Очищенные ГАГ переваривали с использованием комбинации гепариназ I, II и III, и полученные дисахариды выделяли фильтрованием по размеру и затем метили AMAC, как описано ранее 42 . Меченый AMAC HS лиофилизировали и восстанавливали в 50% ДМСО и хранили при -20 ° C перед анализом.
Анализ образцов выполняли на колонке Zorbax Eclipse XDB-C18 RP-HPLC (4,6 мм × 75 мм, 3,6 мм; Agilent Technologies), работающей на системе ВЭЖХ Agilent серии 1100.Образцы разбавляли 60 мМ ацетатом аммония (pH 5,6) и наносили на колонку, которую уравновешивали 98% -ным раствором A / 2% -ным раствором B (A: 60 мМ ацетат аммония, pH 5,6; B: ацетонитрил). Колонку выдерживали в 2% растворе в течение 0,5 мин, а затем меченные AMAC дисахариды элюировали мелким градиентом 2–12% раствора B в течение 25 мин при скорости потока 1 мл / мин. Дисахариды были обнаружены на линии УФ-видимым светом (260 нм). Колонку регенерировали 95% -ным раствором B перед уравновешиванием.Для подтверждения идентичности пиков у Iduron было приобретено восемь стандартов (∆UA2S — GlcNS6S, HD001; ∆UA2S — GlcNS, HD002; ∆UA2S — GlcNAc6S, HD003; ∆UA — GlcNS6S, HD004; ∆UA — GlcNS ∆, HD005 , HD006; ∆UA2S — GlcNAc, HD007; ∆UA — GlcNAc6S, HD008) метили AMAC и добавляли в образцы, полученные из клеток.
Регуляторы сульфатирования — Creative Diagnostics
Введение сульфатирования
Сульфатирование относится к биохимическому процессу, при котором неорганический сульфат образует биологически активный органический сульфат при катализе ферментом.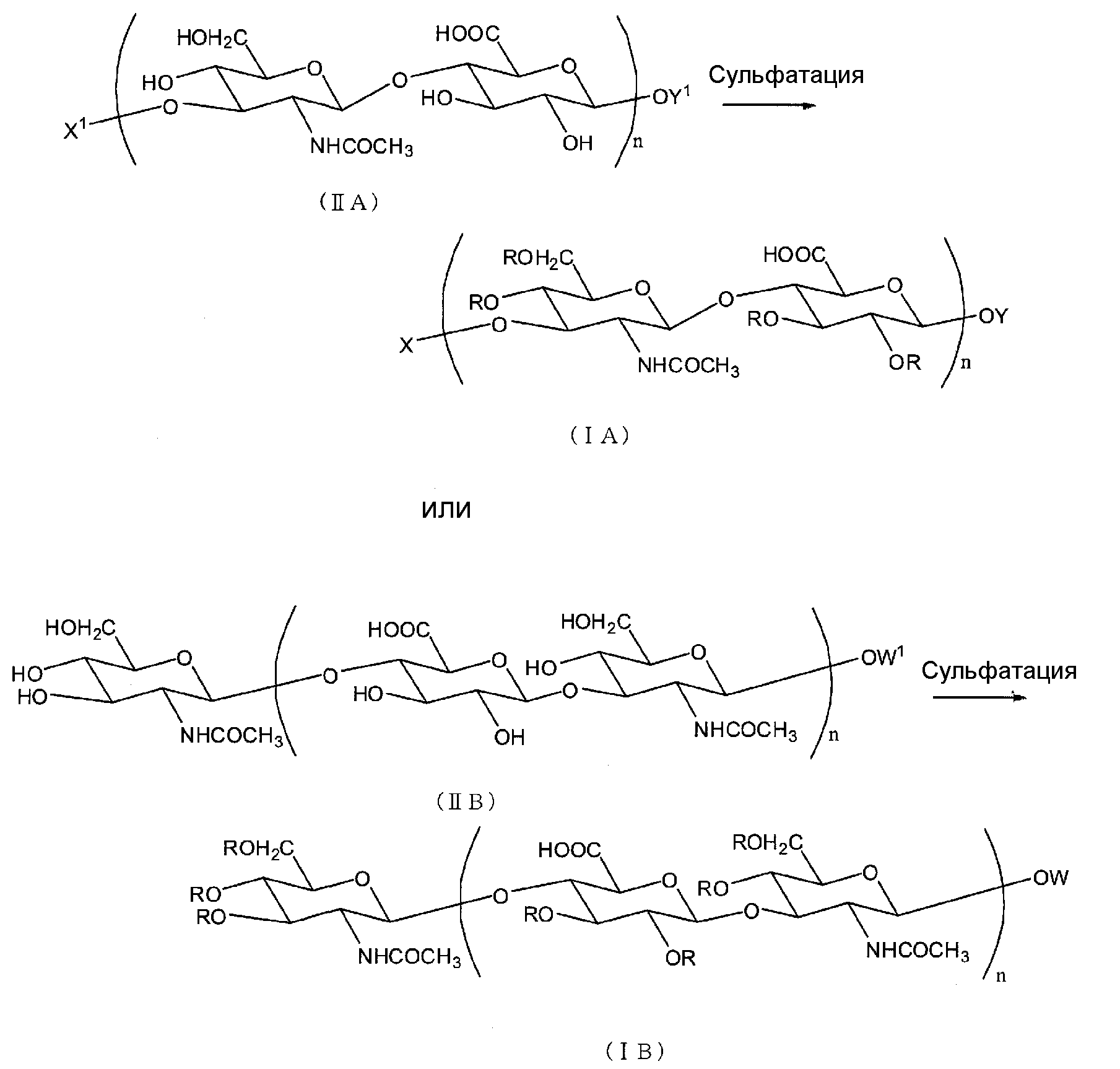 Элементарная сера в форме неорганических сульфатов может быть биодоступной только после метаболической активации, такой как 5′-аденозин-5 ‘фосфосульфат (APS) и 3′-фосфатные железы, 3′-фосфоаденозин-5’-фосфосульфат (PAPS). Синтез PAPS — это двухступенчатый катализ сульфатазы АТФ (аденозинтрифосфат) и киназы APS. Неорганический сульфат реагирует с АТФ с образованием APS и пирофосфата; затем APS реагирует с ATP с образованием PAPS и ADP (аденозиндифосфата). Семейство трансфераз серной кислоты отвечает за перенос активированных сульфатных групп из PAPS в различные биомолекулы, такие как гормоны, нейротрансмиттеры, углеводы и тирозин.Кроме того, APS и PAPS также используются для синтеза восстанавливающих метаболитов серы, таких как компоненты многих белков — метионина и цистеина.
Элементарная сера в форме неорганических сульфатов может быть биодоступной только после метаболической активации, такой как 5′-аденозин-5 ‘фосфосульфат (APS) и 3′-фосфатные железы, 3′-фосфоаденозин-5’-фосфосульфат (PAPS). Синтез PAPS — это двухступенчатый катализ сульфатазы АТФ (аденозинтрифосфат) и киназы APS. Неорганический сульфат реагирует с АТФ с образованием APS и пирофосфата; затем APS реагирует с ATP с образованием PAPS и ADP (аденозиндифосфата). Семейство трансфераз серной кислоты отвечает за перенос активированных сульфатных групп из PAPS в различные биомолекулы, такие как гормоны, нейротрансмиттеры, углеводы и тирозин.Кроме того, APS и PAPS также используются для синтеза восстанавливающих метаболитов серы, таких как компоненты многих белков — метионина и цистеина.
Роль сульфатирования
Сульфатирование важно в организме для сульфатирования белков и сульфатирования полисахаридов; для действия некоторых нейропептидов необходимо сульфатирование тирозина. Например, гормональная активность CCK зависит от сульфатирования остатков тирозина, поскольку активность сульфатированных CCK в 260 раз больше, чем несульфатированных CCK.Сульфат тирозина может быть формой одного продукта трансляции, который образует множество фенотипов. Например, подкисление серы не влияет на способность гастрина стимулировать секрецию желудочного сока. Однако после подкисления тирозиновой кислоты серой гастрин обладает второй биологической активностью. Андерсен и Стодил наблюдали, что предшественник гастрина обрабатывается по-разному в разных тканях. Степень превращения макромолекул в маленькие молекулы связана с присутствием сульфатирования тирозина.Сульфатирование тирозина происходит в сети цис-Гольджи. Следовательно, почти наверняка сульфатирование происходит до ферментативного гидролиза предшественника пептида, поэтому сульфатирование способствует процессингу предшественника гастрина. Недавно Frioderieh et al. провели серию исследований феромона l желтка дрозофилы, которые показали, что сульфатирование тирозина может влиять на транспорт секретируемых белков. Различные полисахариды могут усиливать биологическую активность, и эта активность становится более выраженной после сульфатирования полисахаридов.Декстрансульфат является поликлональным активатором В-лимфоцитов и вызывает пролиферацию Т-лимфоцитов периферической крови. Zhen huanguo изучал влияние сульфатирующего полисахарида астрагала (sAPS), сульфатного полисахарида эпимедиума (sEPS) и сульфатированных полисахаридов дягиля (sCAPS) на пролиферацию лимфоцитов периферической крови цыплят; Результаты показали, что соответствующие дозы пяти видов сульфатированного полисахарида могут отдельно или вместе с глобулином зерен фасоли (ConA) стимулировать пролиферацию лимфоцитов и оказывать определенный эффект.Противовирусная активность сульфатированных полисахаридов в основном обусловлена характеристиками его полианионов, в то время как полианионные свойства в основном обусловлены сульфатными группами в его молекулах. Сильно отрицательно заряженные сульфатные полианионы связываются с вирусами или клеточной поверхностью и положительно заряженными молекулами, что может стереоскопически ингибировать адсорбцию вируса; сульфатированные полисахариды также могут напрямую ингибировать определенные стадии проникновения вирусов в клетки или ингибирования их проникновения в клетки; Кроме того, сульфатированные полисахариды также могут подавлять экспрессию вирусных антигенов, подавлять образование синцитий и подавлять активность обратной транскриптазы и антиоксидантные эффекты.Полисахариды обычно обладают антикоагулянтной активностью после сульфатирования и могут быть эффективным заменителем гепарина. Сюй Чжунпин обнаружил, что сульфат ламинарии может ингибировать адгезию основного фактора роста фибробластов (bFGF) и bFGF-зависимых клеток, тем самым эффективно подавляя образование трубчатых структур эндотелиальных клеток и подавляя образование хориоаллантоисной мембраны курицы, а также обладает антимышиным RIF- 1 активность роста опухоли.
Различные полисахариды могут усиливать биологическую активность, и эта активность становится более выраженной после сульфатирования полисахаридов.Декстрансульфат является поликлональным активатором В-лимфоцитов и вызывает пролиферацию Т-лимфоцитов периферической крови. Zhen huanguo изучал влияние сульфатирующего полисахарида астрагала (sAPS), сульфатного полисахарида эпимедиума (sEPS) и сульфатированных полисахаридов дягиля (sCAPS) на пролиферацию лимфоцитов периферической крови цыплят; Результаты показали, что соответствующие дозы пяти видов сульфатированного полисахарида могут отдельно или вместе с глобулином зерен фасоли (ConA) стимулировать пролиферацию лимфоцитов и оказывать определенный эффект.Противовирусная активность сульфатированных полисахаридов в основном обусловлена характеристиками его полианионов, в то время как полианионные свойства в основном обусловлены сульфатными группами в его молекулах. Сильно отрицательно заряженные сульфатные полианионы связываются с вирусами или клеточной поверхностью и положительно заряженными молекулами, что может стереоскопически ингибировать адсорбцию вируса; сульфатированные полисахариды также могут напрямую ингибировать определенные стадии проникновения вирусов в клетки или ингибирования их проникновения в клетки; Кроме того, сульфатированные полисахариды также могут подавлять экспрессию вирусных антигенов, подавлять образование синцитий и подавлять активность обратной транскриптазы и антиоксидантные эффекты.Полисахариды обычно обладают антикоагулянтной активностью после сульфатирования и могут быть эффективным заменителем гепарина. Сюй Чжунпин обнаружил, что сульфат ламинарии может ингибировать адгезию основного фактора роста фибробластов (bFGF) и bFGF-зависимых клеток, тем самым эффективно подавляя образование трубчатых структур эндотелиальных клеток и подавляя образование хориоаллантоисной мембраны курицы, а также обладает антимышиным RIF- 1 активность роста опухоли.
Регламент сульфатирования
Биомакромолекулы являются основными носителями различных видов жизнедеятельности, таких как полисахариды, белки и нуклеиновые кислоты, которые обладают функциями повышения иммунитета, замедления старения, окисления, рака и ревматоида. Сульфатированные полисахариды и белки привлекли к себе пристальное внимание в последние годы из-за их биологической активности, такой как антиоксидантная, противовирусная и противоопухолевая. Введение сульфата изменяет физические и химические свойства биомакромолекул, тем самым влияя на их биологическую активность. Когда сульфатная группа не вводится, некоторые полисахариды не обладают биологической активностью, такой как устойчивость к окислению и антикоагулянт. После введения сульфата полисахариды и белки получают биологическую активность, такую как антиокислительная и антисвертывающая.Каррагинан и гепарин обладают активностью ингибирования репликации вируса герпеса и антикоагуляции, но если удалить сульфат этих полисахаридов, указанная выше активность исчезает, указывая на то, что введение сульфатных групп улучшает биологическую активность полисахаридов и белков. Сульфатирующие свойства биомакромолекул связаны не только с содержанием сульфата, но также с молекулярной массой и структурой. Yamada et al. приготовил сульфатированный каррагинан и обнаружил, что низкомолекулярный сульфатированный каррагинан (молекулярная масса 50000 Да) имеет более высокую активность против ВИЧ, чем сульфатированный каррагинан с другой молекулярной массой.Низкомолекулярный сульфатированный хитозан, синтезированный Xing и др. , обладает более сильной способностью улавливать супероксидный анион-радикал и гидроксильный радикал, чем хитозан, сульфированный полимером. Указывается, что биоактивность сульфатированного продукта тесно связана с молекулярной массой после модификации сульфатом.
Сульфатированные полисахариды и белки привлекли к себе пристальное внимание в последние годы из-за их биологической активности, такой как антиоксидантная, противовирусная и противоопухолевая. Введение сульфата изменяет физические и химические свойства биомакромолекул, тем самым влияя на их биологическую активность. Когда сульфатная группа не вводится, некоторые полисахариды не обладают биологической активностью, такой как устойчивость к окислению и антикоагулянт. После введения сульфата полисахариды и белки получают биологическую активность, такую как антиокислительная и антисвертывающая.Каррагинан и гепарин обладают активностью ингибирования репликации вируса герпеса и антикоагуляции, но если удалить сульфат этих полисахаридов, указанная выше активность исчезает, указывая на то, что введение сульфатных групп улучшает биологическую активность полисахаридов и белков. Сульфатирующие свойства биомакромолекул связаны не только с содержанием сульфата, но также с молекулярной массой и структурой. Yamada et al. приготовил сульфатированный каррагинан и обнаружил, что низкомолекулярный сульфатированный каррагинан (молекулярная масса 50000 Да) имеет более высокую активность против ВИЧ, чем сульфатированный каррагинан с другой молекулярной массой.Низкомолекулярный сульфатированный хитозан, синтезированный Xing и др. , обладает более сильной способностью улавливать супероксидный анион-радикал и гидроксильный радикал, чем хитозан, сульфированный полимером. Указывается, что биоактивность сульфатированного продукта тесно связана с молекулярной массой после модификации сульфатом.
Артикулы:
- Бай Кью, Сюй Л., Какияма Г., и др. . Сульфатирование 25-гидроксихолестерина с помощью SULT2B1b снижает клеточные липиды через сигнальный путь LXR / SREBP-1c в эндотелиальных клетках аорты человека. Атеросклероз. 2011, 214 (2): 350-356.
- Раух Дж. Н., Чен Дж. Дж., Сорум А. В., и др. Интернализация тау-белка регулируется 6-O сульфатом на гепарансульфатных протеогликанах (HSPG).

