Лекции по термодинамике
Лекции по термодинамике
ОглавлениеПредисловие редактора к первому изданию§ 1.  § 2. Первое начало термодинамики § 3. Другой пример вычисления работы § 4. Приложение к идеальным газам § 5. Стационарный ток жидкости через трубу с переменным сечением § 6. Однородное тело § 7. Применение первого начала к химии: теплота реакции и температура § 8. Второе начало термодинамики § 9. Цикл Карно § 10. Коэффициент полезного действия. Универсальная функция температуры § 11. Другой способ определения универсальной функции температуры § 12. Второе начало для обратимых процессов § 13. Второе начало для обратимых процессов [общий случай] § 14. Различные обратимые пути между двумя состояниями. Энтропия § 15. Несколько простейших приложений § 16. Отношение теплоемкостей § 17. Система с произвольным числом параметров § 18. Значение полученных общих формул § 19. Значение второго начала § 20. Приложения второго начала к адиабатическим процессам § 21. Сжатие жидкостей § 22.  Опыты по адиабатическому растяжению проволок Опыты по адиабатическому растяжению проволок§ 23. Непосредственный вывод уравнения адиабатических процессов § 24. Применение к жидким пленкам § 25. Применение к гальваническому элементу § 26. Уравнение Клапейрона § 27. Опытная проверка уравнения Клапейрона (Клаузиус) § 28. Опыты де-Виссера с уксусной кислотой § 29. Режеляция льда § 30. Закон Стефана-Больцмана § 31. Другие выражения второго начала § 32. Свойства энтропии § 33. Свободная энергия § 34. Термодинамический потенциал § 35. Свободная энергия идеального газа § 36. Неравновесные состояния § 37. Необратимые процессы § 38. Изотермический процесс § 39. Свободная энергия и работа § 40. Обобщенные силы § 41. Условия равновесия § 42. Система в поле консервативных сил § 43. Газ или жидкость в поле силы тяжести § 45. Система жидкость-пар § 46. Равновесие трехфазной системы § 47. Упругость пара над разбавленным раствором § 48.  Различие в давлении пара над чистой водой и над раствором Различие в давлении пара над чистой водой и над раствором§ 49. Смеси § 50. Двухкомпонентная система § 51. Устойчивые и неустойчивые жидкие фазы; равновесие между двумя жидкими фазами § 52. Равновесие между твердой и жидкой фазами; переохлаждение § 53. Равновесие трехфазной системы, состоящей из двух компонент § 54. Равновесие раствора соли с ее твердым гидратом § 55. Равновесие между двумя растворами различной концентрации § 56. Система из двух гидратов § 57. Другой способ построения кривой § 58. Трехкомпонентные системы § 59. Трехфазная система из трех компонент § 60. Форма поверхности § 61. Условия равновесия между твердой и жидкой фазами § 62. Равновесие двух твердых фаз с жидкими фазами § 63. Равновесие между двумя жидкими фазами § 64. Другие способы построения поверхности § 65. Смешанные кристаллы § 66. Равновесие между смесями и растворами § 67. Неопределенность в выражении термодинамического потенциала § 68.  Смесь газов в поле силы тяжести Смесь газов в поле силы тяжести§ 69. Смешение и разделение двух газов § 70. Парадокс Гиббса § 71. Обобщение теоремы Гиббса на случай трех и более газов § 72. Уменьшение свободной энергии при смешении двух газов § 73. Свободная энергия жидкой смеси § 74. Общее выражение для свободной энергии смеси § 75. Случай, когда одна из компонент присутствует в весьма малом количестве § 76. Равновесие двух фаз, каждая из которых состоит из двух компонент § 77. Смесь под действием внешних сил § 79. Второй пример системы под действием внешних сил § 80. Осмотическое давление. Закон вант-Гоффа § 81. Другой вывод закона вант-Гоффа § 82. Общие условия равновесия многофазных систем § 83. Равновесие трех фаз § 84. Вывод условий равновесия с помощью термодинамического потенциала § 85. Число независимых условий равновесия § 86. Сравнение между собой двух состояний равновесия § 87. Общее соотношение между двумя состояниями равновесия § 88.  Смысл полученного соотношения Смысл полученного соотношения§ 89. Добавление некоторого весьма малого количества новой компоненты § 90. Несколько заключительных замечаний § 91. Диссоциация газа § 92. поверхности ван-дер-Ваальса § 93. Изменение формы поверхности с температурой § 94. Сечения Ф-поверхности § 95. Условия равновесия § 96. Сосуществующие фазы § 97. Математическая теория конечных точек складки § 98. Исследование Ф-поверхности в окрестности конечной точки складки § 99. Конечная точка складки первого рода § 100. Индикатриса, бинодаль и спинодаль § 101. Определение координат конечной точки складки непосредственно из самого уравнения Ф-поверхности § 102. Кривая конечных точек складки § 103. Изменение давления при бесконечно малом изменении состояния § 104. Зависимость давления от состава смеси § 105. Изобары § 106. Изотермическое сжатие смесей § 107. Обратная конденсация |
Изменение объема жидкости под давлением (сжимаемость)
УчебаФизика
Этот онлайн калькулятор рассчитывает изменение объема жидкости в зависимости от давления, используя коэффициент сжимаемости
Все знают, что сжимать можно газы, но сжимать можно также и жидкости. Однако, по сравнению с газами, жидкости обладают ничтожной сжимаемостью, и для сколько-нибудь заметного сжатия требуются очень большие давления. Однако, для тех, кому интересно, калькулятор ниже позволяет оценить изменения объема жидкости при изменении давления, с использованием так называемого коэффициента сжимаемости.
Однако, по сравнению с газами, жидкости обладают ничтожной сжимаемостью, и для сколько-нибудь заметного сжатия требуются очень большие давления. Однако, для тех, кому интересно, калькулятор ниже позволяет оценить изменения объема жидкости при изменении давления, с использованием так называемого коэффициента сжимаемости.
В калькуляторе ниже вы вводите коэффициент сжимаемости (в форме ниже вводите коэффициент вручную или выбираете из справочника), начальный объем (в форме ниже это один кубометр) и изменение давления в паскалях (в форме ниже это 100 Мегапаскаль, давление, сравнимое с давлением на дне Марианской впадины). Калькулятор рассчитывает абсолютное изменение объема в кубометрах и относительное в процентах к начальному объему.
Немного теории, как водится, можно посмотреть под калькулятором
Изменение объема жидкости под давлением (сжимаемость)
Коэффициент сжимаемости
выбрать из справочника
ввести вручную
Коэффициент сжимаемости дляОбновление. ..
..
Коэффициент сжимаемости жидкости
Начальный объем жидкости, куб.метров
Изменение давления, Паскаль
Точность вычисления
Знаков после запятой: 3
Изменение объема, куб.метров
Изменение объема, %
Сжимаемость жидкостей
Коэффициент сжимаемости — это отношение относительного изменения объема к изменению давления, вызвавшему это изменение
,
где V — это объём вещества, p — давление; знак минус указывает на уменьшение объёма с повышением давления.
Типовые значения коэффициента сжимаемости для жидкостей лежат в диапазоне от до , например, для дистиллированной воды это , и именно поэтому в большинстве случаев изменение объема жидкости под давлением настолько ничтожно, что им можно пренебречь.
Ссылка скопирована в буфер обмена
Похожие калькуляторы
- • Уровень жидкости в наклоненном цилиндрическом баке
- • Уровень жидкости в цилиндрическом баке
- • Объем жидкости в наклоненном баке со сферическими торцами
- • Гидростатическое давление
- • Объем жидкости в наклоненном цилиндрическом баке
- • Раздел: Физика ( 52 калькуляторов )
#жидкости #физика давление жидкость коэффициент сжимаемости ньютон объем паскаль сжимаемость Физика
PLANETCALC, Изменение объема жидкости под давлением (сжимаемость)
Timur2020-11-03 14:19:40
Что такое сжимаемость жидкостей?
Когда большинство людей думают или говорят о жидкостях, они обычно имеют в виду жидкости. Это не полная картина. По сути, жидкость — это среда , имеющая частицы, легко перемещающиеся и изменяющие свое взаимное положение без разделения массы, и легко поддающаяся действию приложенных сил. Это означает, что жидкости включают газы, потому что они тоже текут. Фактически, корень слова «флюид» происходит от латинского «fluere», что означает «течь».
Это не полная картина. По сути, жидкость — это среда , имеющая частицы, легко перемещающиеся и изменяющие свое взаимное положение без разделения массы, и легко поддающаяся действию приложенных сил. Это означает, что жидкости включают газы, потому что они тоже текут. Фактически, корень слова «флюид» происходит от латинского «fluere», что означает «течь».
Наш сегодняшний опыт может привести нас к заключению, что газы сжимаемы, а жидкости несжимаемы. Обратите внимание на ощущение отскока, когда после сжатия рукоятку шинного насоса быстро отпускают; это демонстрирует силу, создаваемую воздухом, сжимаемым в меньший объем. Объем повторно расширяется до своего первоначального размера, когда сила сжатия удаляется. Точно так же, если мы держим палец над маленьким отверстием в аэрозольном баллончике, мы немедленно чувствуем силу сопротивления при нажатии на спусковой крючок насоса. На основании этого наблюдения жидкость кажется несжимаемой.
Ниже приводится исследование сжимаемости жидкостей и твердых тел в калибровочной лаборатории.
Во-первых, необходимо определить некоторые общие термины:
- Жидкость — материал, который легко течет и требует сосуда для его удержания.
- Газ — состояние вещества, которое принимает форму своего сосуда и не имеет определенного объема.
- Жидкость — состояние вещества, которое принимает форму своего сосуда и имеет определенный объем.
- Твердое тело — состояние вещества, сохраняющее свою форму и имеющее определенный объем.
- Сжимаемые — имеющие способность изменять плотность при приложении давления.
- Плотность — масса в единице объема.
- Химическая связь — передача или совместное использование самых удаленных электронов между двумя или более атомами.
- Сила Ван-дер-Ваальса — силы притяжения между всеми молекулами, вызванные флуктуирующей поляризацией близлежащих частиц, которые становятся значительными только в том случае, если молекулы находятся очень близко друг к другу.

Чем отличаются газы от жидкостей?
Газы ведут себя иначе, чем жидкости. Почему? Чтобы понять, что происходит на макроуровне, нам нужно понять внутреннюю работу материала на атомном и молекулярном уровнях. В любом веществе химические связи, полярность, силы, а также физическая конфигурация атомов в молекуле определяют основные свойства материала, такие как вязкость и сжимаемость. Эти силы, действующие в атомном масштабе, вносят основной вклад в свойства, которые мы наблюдаем в этих объемных материалах.
Рисунок 1. Состояния вещества со связями в каждом состоянии
На рисунке 1 сравнение трех распространенных состояний вещества, твердого, жидкого и газообразного, показывает типы связи в каждом состоянии. На каждой иллюстрации мы видим увеличенный очень маленький объем материала и упрощенное представление соответствующих связей внутри материала. Ниже приведено более подробное объяснение различных состояний со ссылками на иллюстрации.
Твердые тела сохраняют свою форму, потому что химическая связь, показанная в виде пружины между каждым атомом, относительно сильна. Однако одинаковые заряды электронов отталкивают атомы по мере их сближения. И наоборот, если атомы расходятся, они притягиваются связью друг к другу. Расстояние между каждым атомом очень мало из-за силы связи, но эта связь может только удерживать их вместе так сильно из-за сил отталкивания. Таким образом, когда сила прикладывается к этому кубу со всех сторон, сопротивление сжатию между каждым атомом очень велико, что приводит к минимальному сжатию в объемном твердом теле.
Жидкости Жидкости, с другой стороны, имеют больше пространства между молекулами, что позволяет им иметь большее относительное движение. Однако межмолекулярные связи не так прочны, как в твердых телах. Вода, например, представляет собой полярную молекулу и проявляет диполь-дипольное притяжение, как показано пунктирными линиями на рисунке 1. Атом кислорода слегка отрицателен, а два атома водорода слегка положительны. Поскольку эти дипольные заряды намного меньше по силе, чем типичные связи, силы Ван-дер-Ваальса между молекулами слабы и непостоянны. Каждая из них может ломаться и переделываться много миллиардов раз в секунду. Это то, что позволяет воде течь и при этом оставаться жидкостью. Более слабые межмолекулярные силы и более высокое межмолекулярное расстояние являются причиной того, что жидкости могут быть сжаты больше, чем твердые тела.
Атом кислорода слегка отрицателен, а два атома водорода слегка положительны. Поскольку эти дипольные заряды намного меньше по силе, чем типичные связи, силы Ван-дер-Ваальса между молекулами слабы и непостоянны. Каждая из них может ломаться и переделываться много миллиардов раз в секунду. Это то, что позволяет воде течь и при этом оставаться жидкостью. Более слабые межмолекулярные силы и более высокое межмолекулярное расстояние являются причиной того, что жидкости могут быть сжаты больше, чем твердые тела.
В таких газах, как азот или воздух, при нормальных температуре и давлении связи между молекулами отсутствуют. Каждая молекула движется с высокой скоростью в различных направлениях. Когда две молекулы газа сталкиваются, они отскакивают друг от друга с идеальной упругостью. Потерь в столкновениях нет. Межмолекулярное расстояние слишком велико, чтобы межмолекулярные силы могли быть значительными. При комнатной температуре и стандартном давлении среднее расстояние между молекулами газа примерно в десять раз превышает диаметр самих молекул. Таким образом, когда к молекулам газа прикладывается внешняя сила, они сближаются, что делает газы очень сжимаемыми.
Таким образом, когда к молекулам газа прикладывается внешняя сила, они сближаются, что делает газы очень сжимаемыми.
Степень сжимаемости
Теперь, когда мы знаем на молекулярном уровне, что газы и жидкости более сжимаемы, чем твердые тела. Как насчет сжимаемости обычных сред под давлением, используемых в калибровочной лаборатории? Относительная степень сжимаемости материала с приложенной силой определяет наше восприятие жесткости. Когда материал сжимается со всех сторон, он сжимается пропорционально приложенному давлению. Константа пропорциональности называется объемным модулем.
Β = — V * (∂P ⁄ ∂V)
Где B = модуль объемного сжатия
V = начальный объем
∂P/∂V = изменение давления по отношению к изменению объема
Обратите внимание, что увеличение давления вызывает уменьшение объема, это означает, что плотность материала увеличивается. Если одну и ту же силу приложить к равному объему твердого тела, жидкости и газа, становится очевидным относительное уменьшение объема.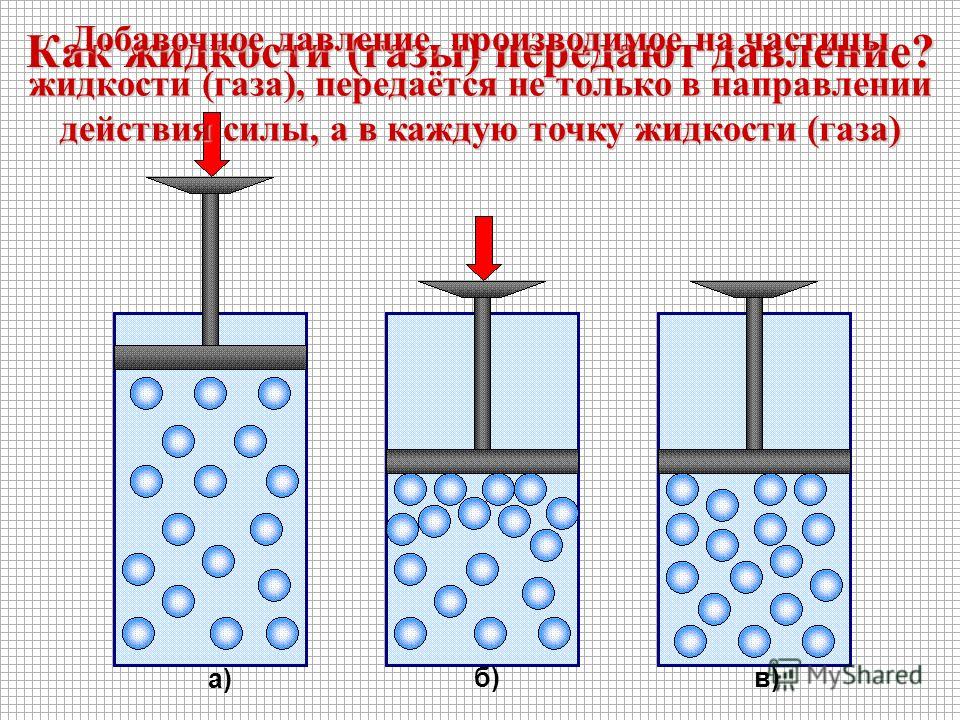 Изотермический объемный модуль каждого состояния вещества можно сравнить, чтобы получить отношение порядка величины. Ниже приведен объемный модуль для некоторых распространенных материалов в каждом состоянии:
Изотермический объемный модуль каждого состояния вещества можно сравнить, чтобы получить отношение порядка величины. Ниже приведен объемный модуль для некоторых распространенных материалов в каждом состоянии:
Нержавеющая сталь: -23 600 000 фунтов силы/кв. дюймов
Вода: -310 000 фунтов/кв. дюйм
Воздух, при нормальных условиях: -14,7 фунт-сила/кв. В.
Сравнительное соотношение материалов выражается здесь:
Нержавеющая сталь : Вода : Воздух = 1 600 000 : 21 000 : 1
Числа представляют собой относительную жесткость материалов. Чем выше число, тем менее сжимаемый материал. Например, соотношение воды к воздуху составляет 21 000:1, поэтому мы не ощущаем сжатия воды в распылительном насосе с забитым отверстием. Он сжимается настолько мало, что мы не можем обнаружить его нашими органами чувств.
Следует отметить, что объемные модули зависят от давления и температуры. Для воды с увеличением давления объемный модуль упругости увеличивается. Когда температура жидкости повышается от 0°C при постоянном давлении, объемный модуль упругости увеличивается, достигая максимума около 330 000 фунтов силы/кв. в. примерно при 45°С, а затем снижается.
Когда температура жидкости повышается от 0°C при постоянном давлении, объемный модуль упругости увеличивается, достигая максимума около 330 000 фунтов силы/кв. в. примерно при 45°С, а затем снижается.
Это создает сложную цепочку событий в среде калибровки. В гидравлических калибровочных системах высокого давления, таких как Mensor CPC8000-H, мы полагаемся на жидкую среду в качестве среды под давлением из соображений безопасности. По мере увеличения давления в системе жидкость сжимается, и все содержащиеся в ней компоненты расширяются (регулятор давления, трубки, фитинги, камера давления и т. д.). Части, окруженные жидкостью, сжимаются, и объемный модуль упругости среды изменяется в зависимости от давления и температуры. В системах высокого давления учет и компенсация относительных объемных модулей, обусловленных сцеплением материалов, а также хорошая инженерия делают системы калибровки точными и надежными.
Заключение
Сжимаемость жидкостей играет решающую роль в разработке технологической системы в промышленном секторе, а также в поддержании эффективности инфраструктуры калибровочной лаборатории. Выбор правильного калибратора при оптимизации системы для компенсации сжимаемости компонентов системы и используемого носителя обеспечит более точные результаты калибровки. Сжимаемость может сильно различаться у разных жидких жидкостей с различиями в модуле объемного сжатия, вязкости, температурном коэффициенте среды и растворимости. Мы углубимся в сравнение сжимаемости различных жидких сред, обычно используемых для гидравлической калибровки, в части II книги «Сжимаемость жидкостей».
Выбор правильного калибратора при оптимизации системы для компенсации сжимаемости компонентов системы и используемого носителя обеспечит более точные результаты калибровки. Сжимаемость может сильно различаться у разных жидких жидкостей с различиями в модуле объемного сжатия, вязкости, температурном коэффициенте среды и растворимости. Мы углубимся в сравнение сжимаемости различных жидких сред, обычно используемых для гидравлической калибровки, в части II книги «Сжимаемость жидкостей».
Связанные материалы:
- Гидравлическое и пневматическое давление при калибровке
- Подходит ли любая газовая среда для пневматической калибровки давления?
- Чистый, сухой воздух: среда под давлением для производства калибровочного оборудования
Сжатие жидкости
Внутри узла Fluidtank_fluid находится сеть, которая объединяет первоначальную настройку вашего резервуара с симуляцией. Как только симуляция завершена, этот узел собирает частицы жидкости, устанавливает материал и создает несколько узлов для всплытия, чтобы завершить эффект. В Houdini 15 также есть новые узлы, которые автоматически добавляют сжатие, и новый плавный слой.
В Houdini 15 также есть новые узлы, которые автоматически добавляют сжатие, и новый плавный слой.
Геометрический узел Fluid Compress сжимает симуляции жидкости перед сохранением данных на диск. Сжатие, как правило, с потерями: частицы FLIP будут отбрасываться ниже указанной глубины, а пропускная способность объема ограничивается обнулением значений. Тем не менее, SOP, такие как Whitewater Source и Particle Fluid Surface, предназначены для обнаружения поступления сжатой жидкости и восстановления любых необходимых недостающих данных.
Параметр Pack Particles разделит частицы FLIP на плитки, которые хранятся как упакованные примитивы. Затем они записываются на диск и впоследствии загружаются с задержкой Параметр Delay Load Geometry на узле comressed_cache . Если вы отобразите узел сжатого_кэша , вы увидите ограничивающую рамку мозаичных точек, которую можно быстро просмотреть. Это очень полезно для получения грубого предварительного просмотра больших симуляций.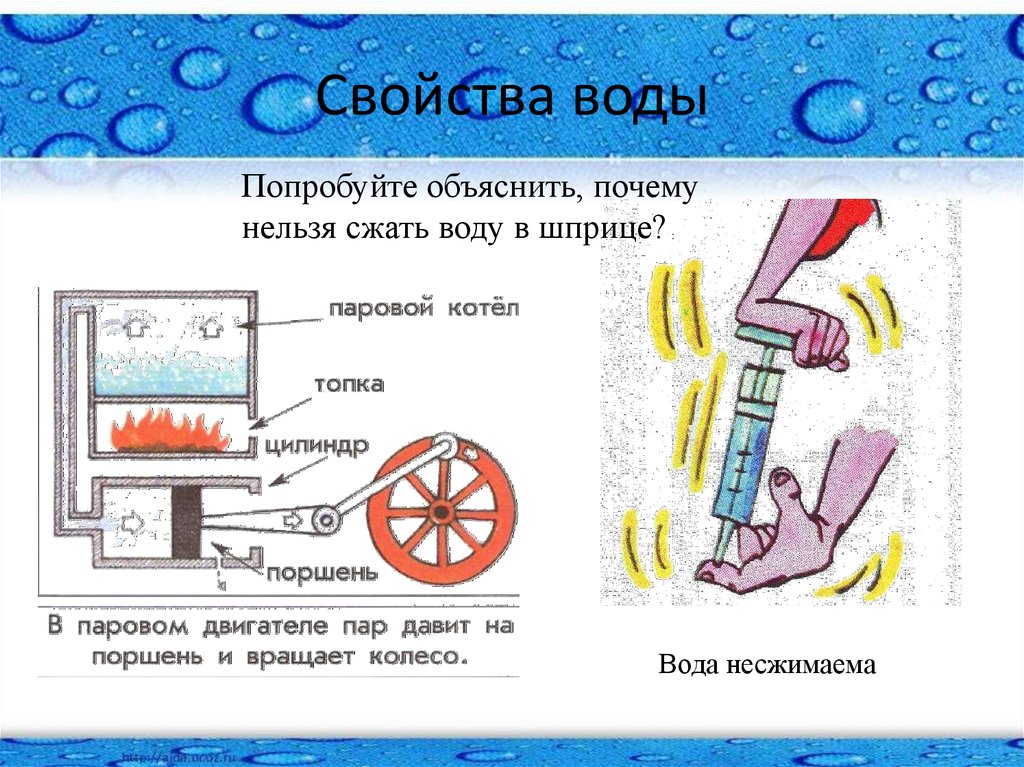
Существует также узел surface_preview , который обеспечивает предварительный просмотр вашего сжатого моделирования. В параметре Convert to на узле Particle Fluid Surface есть 3 варианта предварительного просмотра.
Частицы
Отображает очень тонкий слой частиц в верхней части поверхности жидкости. Эта опция отображает только частицы, сохраненные узлом Fluid Compress. Однако этот вариант может быть не самым полезным для флипбукинга, так как вы можете видеть сквозь тонкий слой частиц.
Поверхность сжатой жидкости
Отображает поле поверхности из моделирования FLIP. Вы не сможете увидеть все детали поверхности, но эта опция полезна для предварительного просмотра симов бурной воды или вторичных симов, чтобы примерно определить, где будут брызги. Этот вариант также часто отображается быстрее всего; как настроено инструментами полки, это позволит избежать загрузки любых частиц FLIP с диска.
