Кинематическая / динамическая вязкость — определение, примеры
- Wiki
- Технология разделения
- Динамическая вязкость
Динамическая вязкость η (η= „Eta“) — это единица измерения вязкости или вязкотекучести жидкости (жидкость: жидкая, текучая субстанция).
Чем выше значение параметра вязкость, тем более тягучая (вязкая) жидкость; чем меньше вязкость, тем он более жидкий (текучий).
Единица измерения динамической вязкости в СИ: [η] = Паскаль * секунду (Па*с) = Н*с/м² = кг/м*с
Факторы, влияющие на динамическую вязкость
Динамическая вязкость η зависит от вещества и температуры и указывается в Паскаль * секунду.
- У жидкостей при повышении температуры динамическая вязкость η сильно уменьшается
- У газов при повышении температуры динамическая вязкость η увеличивается
Взаимосвязь между динамической и кинематической вязкостью ν
Кинематическая вязкость ν (ν= „Ny“) — это динамическая вязкость среды η, разделенная на ее плотность ρ
Формула: ν = η / ρ
Единица измерения кинематической вязкости в СИ: [ν] = м²/c
Другие единицы измерения кинематической вязкости
Устаревшими, но часто используемыми единицами измерениями на парктике являются стоксы (Ст) и сантистоксы (cСт). Они не соответствуют утвержденной системе единиц измерения СИ (СИ — сокращение от французского Système international d’unités):
Пересчет:
1 стокс (Ct) = 10-4 м²/c = 1 см²/s
1 сСт = 10-6 м²/c = 1 мм²/*-s
Примеры для кинематической и динамической вязкости
Таблица примеров со значениями вязкости для кинематической и динамической вязкости
| Жидкости | η / мПа*с при 20°C | η / мПа*с при 0°C | ν / мм²/с при 20°C |
| Вода | 1,002 | 1,792 | 1,004 |
| Оливковое масло | 80,8 | 89 | |
| Этанол | 1,20 | 1,78 | 1,52 |
| Метанол | 0,587 | 0,820 | 0,742 |
| Бензол | 0,648 | 0,91 | 0,737 |
| Газы при 0°C; 1013 гПа | η / μПа*с | ν / мм²/с |
| Воздух | 17,2 | 13,3 |
| Двуокись углерода | 13,7 | 6,93 |
| Азот | 16,5 | 13,2 |
| Кислород | 19,2 | 13,4 |
Источник: Хорст Кухлинг: Справочник по физике; Фахбухферлаг Лейпциг, 16-е издание 1996; 2.
Category Технологии разделения
Наверх
У вас есть вопросы, или вы хотите обратиться к нам с предложением?Обращение Госпожа Господин
* ОбязательныеДинамическая вязкость и кинематическая вязкость
Динамическая вязкость и кинематическая вязкостьДинамическая и кинематическая вязкость для различных жидкостей
Вязкость жидкости — это ее способность оказывать сопротивление перемещению одних частиц относительно других,
то есть оказывать сопротивление перемещению одного «слоя» жидкости относительного другого, работа, затрачиваемая на перемещение, рассеивается в виде тепла.
Движущиеся молекулы жидкости переносят импульс из одного слоя в другой, что приводит к выравниванию скорости по всему потоку.
Выделяют две разновидности вязкости: динамическая (или абсолютная) и кинематическая. Оба показателя уменьшаются при повышении температуры вещества.
Динамическая вязкость (ƞ)
Динамическая вязкость определяет величину сопротивления текучести жидкости при перемещении ее слоя площадью 1 см2 на расстояние в 1 см со скоростью 1 см/сек. В СИ (Международной системе единиц) данный показатель измеряется в Па•с (паскаль•секунда). В системе же СГС единицей измерения вязкости является пуаз (в честь Ж. Пуазейля, французского физика).
Чем выше вязкость жидкости, тем, соответственно, больше время ее истечения, то есть чем дольше по времени жидкость будет вытекать через воронку, тем больше её вязкость.
С точки зрения физики динамическая вязкость обозначает потерю давления за единицу времени (поэтому в системе СИ этот параметр и измеряется в Па•с). У жидкостей данный параметр снижается при росте температуры (то есть когда среда нагревается, она течет легче) и повышается при увеличении давления.
У жидкостей данный параметр снижается при росте температуры (то есть когда среда нагревается, она течет легче) и повышается при увеличении давления.
Кинематическая вязкость (ν)
Кинематическая вязкость — это соотношение коэффициента динамической вязкости жидкости к ее плотности.
ν = ƞ/ρ (где ρ — плотность жидкости)
В системе СИ эта величина выражается в м2/с, а в системе СГС — в стоксах (Ст), или сантистоксах (сСт): 1 Ст=100 сСт.
1 сСт = 1 мм2/c = 10−6 м2
/c.Кинематическая вязкость у жидкостей демонстрирует, насколько легко способно течь данное вещество. В практическом применении это связано с тем, насколько продукт густой. На данный показатель температура влияет несколько меньше, нежели на абсолютную вязкость, ведь тепло также уменьшает и плотность (при нагревании молекулы смещаются дальше друг от друга).
На практике кинематическая и динамическая вязкость используется при гидравлических расчетах трубопроводов в частности для определении числа Рейнольдса.
Кинематическая вязкость ряда жидкостей для различных значений температуры представлена в таблице:
| Название жидкости | Температура Сo | Кинематическая вязкость ν, м2/с |
|---|---|---|
| Бензин | 20 | 0,5…0,7 х 10-6 |
| Вода | 20 | 1,004 х 10-6 |
| Дизельное топливо арктическое (ДТ А) (ГОСТ Р 55475-2013) | 40 | 1,5…4,5 х 10-6 |
| Дизельное топливо зимнее (ДТ З) (ГОСТ Р 55475-2013) | 40 | 1,5…4,5 х 10-6 |
| Дизельное топливо летнее (ДТ Л) (ГОСТ 305-2013) | 40 | 2,0…6,0 х 10-6 |
| Мазут топочный 40 (по ГОСТ 10585-2013) | 80 | 59 х 10-6 |
| Мазут топочный 100 (по ГОСТ 10585-2013) | 100 | 50 х 10-6 |
| Мазут флотский Ф5 (по ГОСТ 10585-2013) | 50 | 36,2 х 10-6 |
| Нефть* | 20 | 40. ..60 х 10-6 ..60 х 10-6 |
| Топливо авиационное ТС-1 (по ГОСТ 10227-2013) | 20 | 1,25 х 10-6 |
| Топливо авиационное РТ (по ГОСТ 10227-2013) | 20 | 1,25 х 10-6 |
| Трансформаторное масло ГОСТ 982-80) | 20 | 30 х 10-6 |
* — Кинематическая вязкость нефти изменяется в широких пределах: от 2 до 300 мм2/с (20 °С). Однако в среднем вязкость большинства нефтей не превышает 40 – 60 мм2/с.
В таблице ниже представлены значения динамической, кинематической вязкости и плотности для различных органических жидкостей, при температурах от 10 до 140 градусов С. Выберете вещество из предложенного списка, показатели для данной жидкости отразятся в таблице автоматически.
| Выбор вещества : | |||
|---|---|---|---|
| Температура, Co | Динамическая вязкость ƞ, мПа·с | Плотность ρ, кг/м3 | Кинематическая вязкость ν, м2/c |
| 10 | |||
| 20 | |||
| 30 | |||
| 40 | |||
| 50 | |||
| 60 | |||
| 70 | |||
| 80 | |||
| 90 | |||
| 100 | |||
| 110 | |||
| 120 | |||
| 130 | |||
| 140 | |||
: как это работает?
НАУКА О ЖИДКОСТИ
как
это
работает
Отличие от Fluidity
Fluidity помогла тысячам пользователей развить более длинные, стройные тела с непреодолимыми изгибами всего за две 30-минутные тренировки в неделю.
Результат реальный потому что наука реальный .
Fluidity объединяет науки физиологии и кинезиологии с изящным искусством балета, чтобы создать метод упражнений, который глубоко меняет жизнь.
Мышцы
Интеграция
Проблема с традиционными тренировками
Физическое движение стало возможным благодаря кинетическим цепным движениям: связи между вашими нервами, мышцами и костями, которые должны работать вместе. Их часто называют движениями с открытой или закрытой кинетической цепью.
Традиционные тренировки, такие как поднятие тяжестей и пилатес, в основном представляют собой движения с открытой кинетической цепью. Упражнения с открытой кинетической цепью обычно выполняются в положении без нагрузки, когда ваша рука или нога могут свободно двигаться. Упражнения, подобные этим, изолируют отдельные группы мышц/суставы, и требуется от 5 до 6 часов, чтобы активировать более 630 мышц, составляющих тело.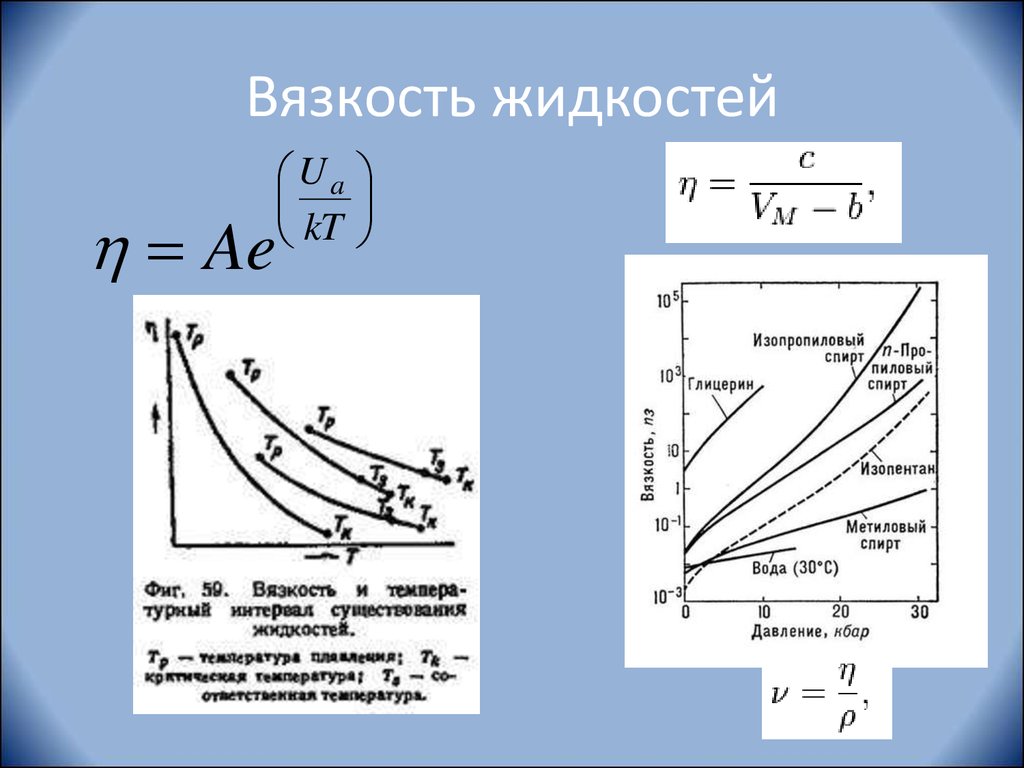
Интеграция текучести мышц
В отличие от этого, Fluidity Barre преимущественно использует движения с закрытой кинетической цепью, выполняемые в положении с нагрузкой на руки и/или ноги, зафиксированные на объекте или земле.
Всего за 30 минут Fluidity эффективно активирует более 630 мышц, что приводит к сбалансированному телосложению, улучшению осанки, усилению стабилизации суставов и усилению неврологической координации.
За счет пропорционального развития мышц с помощью движений всего тела с нагрузкой на тренажер Fluidity Barre стимулирует быстрые изменения и делает тело более длинным и стройным.
сжигать больше калорий, чем кардио
сжигать больше калорий: плавность и кардио
Исследования показали, что силовые тренировки являются более эффективным способом похудеть, чем кардио. Упражнения, основанные исключительно на кардио, сжигают жир и калории, но также уменьшают мышечную массу.
Для сравнения, программы силовых тренировок, такие как Fluidity, увеличивают сухую мышечную массу, что помогает ускорить метаболизм. Силовые тренировки вызывают крошечные разрывы в мышечной ткани, которые тело залечивает в процессе, называемом «после ожога». Этот процесс продолжает сжигать калории до 48 часов после тренировки Fluidity, а не всего 2 часа при кардиотренировках. Пользователи Fluidity сжигают калории даже во сне.
Силовые тренировки вызывают крошечные разрывы в мышечной ткани, которые тело залечивает в процессе, называемом «после ожога». Этот процесс продолжает сжигать калории до 48 часов после тренировки Fluidity, а не всего 2 часа при кардиотренировках. Пользователи Fluidity сжигают калории даже во сне.
задняя часть тела
ЖИДКОСТЬ ЗАДНЕЙ ЧАСТИ
Ключом к красивому, безболезненному телу является пропорциональное укрепление, развитое в правильном выравнивании. Традиционные тренировки, такие как силовые упражнения, пилатес и йога, в основном сосредоточены на передней части тела. Если спину не развить в достаточной степени, эти упражнения могут в конечном итоге привести к боли, нарушению равновесия и проблемам с тазом.
Fluidity Barre тренирует все тело, развивая мышцы спереди назад и из стороны в сторону. Этот метод тренировки создает пропорциональное, сильное и красивое тело — 360 градусов.
Укрепляя как заднюю, так и переднюю мышцы, упражнения Fluidity помогают:
- Улучшить осанку
- Улучшить функцию тазового дна
- Тонус подколенных сухожилий
- Поднять и укрепить ягодицы
0 7 - 5 900
Стабильность таза Сила кора
ДИСФУНКЦИЯ ТАЗА И ПОЗВОНОЧНИКА
Стабильность таза и сила кора жизненно важны для здорового функционирования и подвижности тела.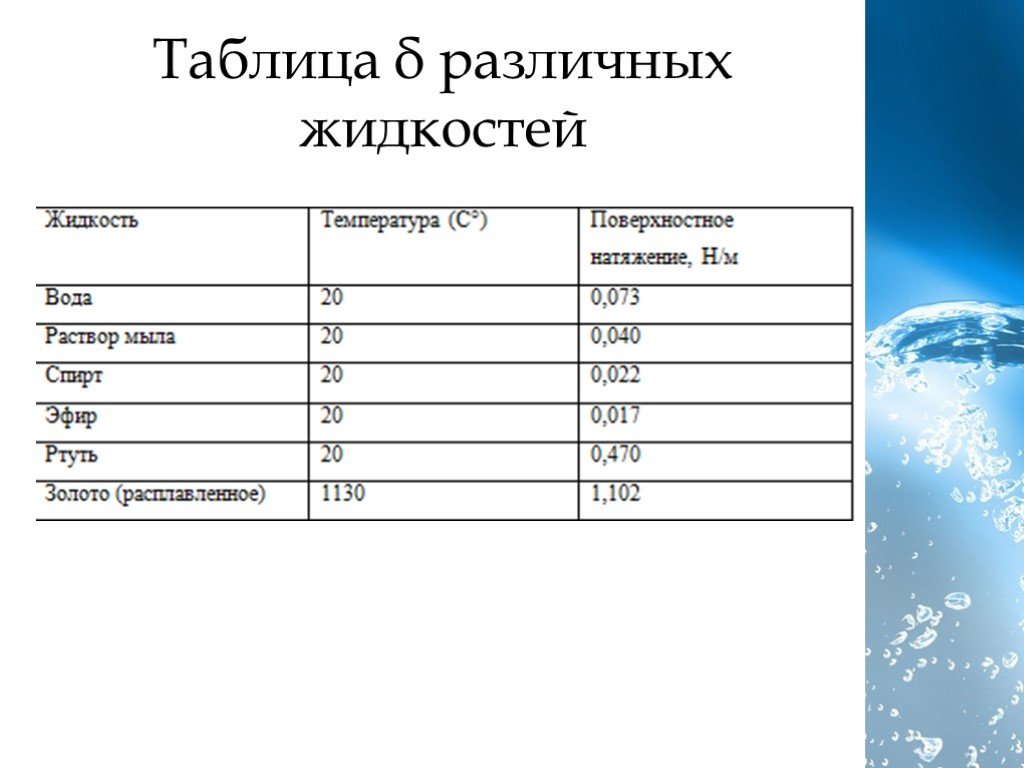 Длительное сидение, неудобные позы для сна, стресс, беременность и старые травмы могут вызвать нестабильность таза.
Длительное сидение, неудобные позы для сна, стресс, беременность и старые травмы могут вызвать нестабильность таза.
Смещенный или несбалансированный таз не может должным образом поддерживать позвоночник. Эта потеря целостности позвоночника может привести к плохой осанке, болям в пояснице или коллапсу тазового дна (основная причина недержания мочи).
ЖИДКОСТЬ ТАЗА И ПРОЧНОСТИ ЦЕНТРА
Текучесть может помочь восстановить стабильность таза и силу кора. Реабилитация начинается с концентрации Fluidity на нейтральном положении таза. Этот метод правильно выравнивает позвоночник с тазом, обеспечивая оптимальное движение между тазом и ногами.
Восстановите и защитите функцию и подвижность всего за две 30-минутные тренировки Fluidity в неделю.
Настоящая функциональная тренировка
ПО-НАСТОЯЩЕМУ ФУНКЦИОНАЛЬНЫЕ ТРЕНИРОВКИ
Современные привычки, такие как сутулость за столом, ношение больших сумок и длительное сидение, приводят к тому, что человек легко теряет правильное положение тела.
Станок Fluidity Barre Функциональная тренировка восстанавливает тело от этих моделей движения, используя многомерные движения с нагрузкой, которые улучшают наше выравнивание, баланс, стабильность и подвижность.
Популярные «функциональные тренажеры», такие как стабилизирующие мячи и качающиеся доски, требуют от пользователя поиска «стабильности». Другими словами, пользователь вынужден укреплять свою плохую осанку, ухудшая равновесие. Только очень небольшой процент населения имеет непроизвольное нейтральное положение таза и фактически может использовать эти устройства, не травмируя себя. К сожалению, старейшины используют эти устройства только для того, чтобы ухудшить их баланс.
Упражнения Fluidity Barre предназначены для того, чтобы помочь вам создать и поддерживать правильное выравнивание во время каждой тренировки. Эти движения всего тела с весовой нагрузкой начинаются и заканчиваются правильным выравниванием, которое способствует непроизвольному нейтральному положению таза. Это ключ к обращению вспять плохих привычек осанки, развитию силы, баланса и оптимизации наших физических функций в повседневной жизни.
Это ключ к обращению вспять плохих привычек осанки, развитию силы, баланса и оптимизации наших физических функций в повседневной жизни.
Shop Barres Fluidity Barres
Контроль текучести мембранных липидов с помощью молекулярных термосенсоров
1. Aguilar, P.S., J.E. Cronan, Jr., and D. de Mendoza. 1998. Ген Bacillus subtilis , индуцированный холодовым шоком, кодирует мембранную фосфолипидную десатуразу. Дж. Бактериол. 180 : 2194-2200. . [Бесплатная статья PMC] [PubMed] [Google Scholar]
2. Агилар, П. С., П. Лопес и Д. де Мендоса. 1999. Транскрипционный контроль низкотемпературного индуцируемого 9Ген 0016 des , кодирующий дельта-5-десатуразу Bacillus subtilis . Дж. Бактериол. 181 : 7028-7033. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Агилар, П. С., А. М. Эрнандес-Арриага, Л. Э. Цибульский, А. К. Эразо и Д. де Мендоса. 2001. Молекулярная основа термочувствия: двухкомпонентный термометр передачи сигнала в Bacillus subtilis . EMBO J. 20 : 1681-1691. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Молекулярная основа термочувствия: двухкомпонентный термометр передачи сигнала в Bacillus subtilis . EMBO J. 20 : 1681-1691. [Бесплатная статья PMC] [PubMed] [Google Scholar]
4. Альбанези Д., М. К. Мансилья и Д. де Мендоса. 2004. Датчик текучести мембраны DeK из Bacillus subtilis контролирует затухание сигнала родственного ему регулятора отклика. Дж. Бактериол. 186 : 2655-2663. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Аллен Э. Э. и Д. Х. Бартлетт. 2000. FabF необходим для пьезорегуляции уровней цис -вакценовой кислоты и пьезофильного роста глубоководных бактерий Photobacterium profundum штамм SS9. Дж. Бактериол. 182 : 1264-1271. [Бесплатная статья PMC] [PubMed] [Google Scholar]
6. Альтабе, С. Г., П. Агилар, Г. М. Кабальеро и Д. де Мендоса. 2003. Ациллипиддесатураза Bacillus subtilis представляет собой δ5-десатуразу. Дж. Бактериол. 185 : 3228-3231. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дж. Бактериол. 185 : 3228-3231. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Бальдассаре, Дж. Дж., К. Б. Райнхарт и Д. Ф. Силберт. 1976. Модификация мембранных липидов: физические свойства по отношению к структуре жирных кислот. Биохимия 15 : 2986-2994. [PubMed] [Google Scholar]
8. Beckering C.L., L. Steil, MH Weber, U. Volker, and M.A. Marahiel. 2002. Полногеномный транскрипционный анализ реакции холодового шока у Bacillus subtilis . Дж. Бактериол. 184 : 6395-6402. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Блох, К. 1963. Биологический синтез ненасыщенных жирных кислот. Биохим. соц. Симп. 24 : 1-16. [PubMed] [Академия Google]
10. Campbell, J.W., and J.E. Cronan, Jr. 2001. Бактериальный биосинтез жирных кислот: цели для открытия антибактериальных препаратов. Анну. Преподобный Микробиолог. 55 : 305-332. [PubMed] [Google Scholar]
55 : 305-332. [PubMed] [Google Scholar]
11. Карти, С. М., К. Р. Шрикумар и К. Р. Раетц. 1999. Влияние холодового шока на биосинтез липида А у Escherichia coli. Индукция при 12°C ацилтрансферазы, специфичной к белку-носителю пальмитолеоил-ацила. Дж. Биол. хим. 274 : 9677-9685. [PubMed] [Google Scholar]
12. Чой, К. Х., Р. Дж. Хит и К. О. Рок. 2001. Бета-кетоацил-ацил-носитель белка-синтазы III (FabH) является определяющим фактором биосинтеза жирных кислот с разветвленной цепью. Дж. Бактериол. 182 : 365-370. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Клеменц, Т., Дж. Дж. Беднарски и С. Р. Раец. 1996. Функция гена высокой температуры htrB Escherichia coli при ацилировании липида A: HtrB катализировал включение лаурата. Дж. Биол. хим. 271 : 12095-12102. [PubMed] [Google Scholar]
14. Клементц Т., З. Чжоу и С. Р. Раец. 1997. Функция гена Escherichia coli msbB , мультикопийного супрессора нокаутов htrB , в ацилировании липида A. Ацилирование с помощью MsbB следует за включением лаурата с помощью HtrB. Дж. Биол. хим. 272 : 10353-10360. [PubMed] [Академия Google]
Клементц Т., З. Чжоу и С. Р. Раец. 1997. Функция гена Escherichia coli msbB , мультикопийного супрессора нокаутов htrB , в ацилировании липида A. Ацилирование с помощью MsbB следует за включением лаурата с помощью HtrB. Дж. Биол. хим. 272 : 10353-10360. [PubMed] [Академия Google]
15. Cronan, J.E., Jr., C.H. Birge, and P.R. Vagelos. 1969. Доказательства наличия двух генов, специфически участвующих в биосинтезе ненасыщенных жирных кислот у Escherichia coli . Дж. Бактериол. 100 : 601-604. [Бесплатная статья PMC] [PubMed] [Google Scholar]
16. Cronan, JE, Jr., and EP Gelmann. 1973. Оценка минимального количества ненасыщенных жирных кислот, необходимого для роста Escherichia coli . Дж. Биол. хим. 248 : 1188-1195. [PubMed] [Google Scholar]
17. Cronan, JE, Jr., RB Gennis, and S.R. Maloy. 1987. Цитоплазматическая мембрана, с. 31-55. В Ф. К. Нейдхардт, Дж. Л. Ингрэм, К. Б. Лоу, Б. Магасаник, М. Шехтер и Х. Э. Умбаргер (ред.), Escherichia coli и Salmonella : клеточная и молекулярная биология. Американское общество микробиологии, Вашингтон, округ Колумбия
31-55. В Ф. К. Нейдхардт, Дж. Л. Ингрэм, К. Б. Лоу, Б. Магасаник, М. Шехтер и Х. Э. Умбаргер (ред.), Escherichia coli и Salmonella : клеточная и молекулярная биология. Американское общество микробиологии, Вашингтон, округ Колумбия
18. Кронан, Дж. Э., младший, и К. О. Рок. 1987. Биосинтез мембранных липидов, с. 474-497. В Ф. К. Нейдхардт, Дж. Л. Ингрэм, К. Б. Лоу, Б. Магасаник, М. Шехтер и Х. Э. Умбаргер (ред.), Escherichia coli и Salmonella : клеточная и молекулярная биология. Американское общество микробиологии, Вашингтон, округ Колумбия
19. Кронан, Дж. Э., младший, и К. О. Рок. 1996. Биосинтез мембранных липидов, с. 612-636. In Ф. К. Нейдхардт, Р. Кертисс III, Дж. Л. Ингрэм, Э. К. С. Лин, К. Б. Лоу, Б. Магасаник, В. С. Резникофф, М. Райли, М. Шехтер и Х. Э. Умбаргер (ред.), Escherichia coli и Salmonella : клеточная и молекулярная биология, 2-е изд. ASM Press, Washington, DC
ASM Press, Washington, DC
20. Cybulski, L.E., D. Albanesi, M.C. Mansilla, S. Altabe, P.S. Aguilar и D. de Mendoza. 2002. Механизм оптимизации текучести мембран: изотермический контроль Bacillus subtilis ацил-липиддесатуразы. Мол. микробиол. 45 : 1379-1388. [PubMed] [Google Scholar]
20a. Cybulski, L.E., G. del Solar, P.O. Craig, M. Espinosa, and D. de Mendoza. Bacillus subtilis DesR действует как переключатель, активируемый фосфорилированием, для контроля текучести липидов мембраны. Дж. Био. хим., в печати. [PubMed]
21. de Mendoza, D., and J. E. Cronan, Jr. 1983. Термическая регуляция текучести липидов мембран у бактерий. Тенденции биохим. науч. 8 : 49-52. [Google Scholar]
22. de Mendoza, D., A. Klages Ulrich, and J. E. Cronan, Jr. 1983. Терморегуляция текучести мембран в Escherichia coli . Эффекты перепроизводства бета-кетоацил-ацил-переносящей протеинсинтазы I. J. Biol. хим. 258 : 2098-2101. [PubMed] [Google Scholar]
J. Biol. хим. 258 : 2098-2101. [PubMed] [Google Scholar]
23. де Мендоса Д., Г. С. Шуйман и П. С. Агилар. 2001. Биосинтез и функция мембранных липидов, с. 43-55. В А. Л. Соненшейн, Дж. А. Хох и Р. Лосик (ред.), Bacillus subtilis и его родственники: от генов к клеткам. ASM Press, Вашингтон, округ Колумбия,
24. Диас, А. Р., М. К. Мансилла, А. Дж. Вила и Д. де Мендоса. 2002. Топология мембраны ацил-липидной десатуразы из Bacillus subtilis . Дж. Биол. хим. 277 : 48099-48106. [PubMed] [Google Scholar]
25. Эдвардс П., Дж. С. Нельсен, Дж. Г. Мец и К. Дехеш. 1997. Клонирование гена fabF в векторе экспрессии и характеристика in vitro рекомбинантных fabF и fabB , кодирующих ферменты из Escherichia coli . ФЭБС лат. 402 : 62-66. [PubMed] [Академия Google]
26. Fujii, D.K.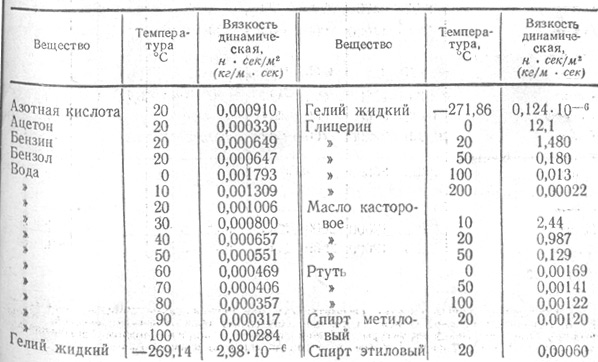 , and A.J. Fulco. 1977. Биосинтез ненасыщенных жирных кислот бациллами. Гипериндукция и модуляция синтеза десатуразы. Дж. Биол. хим. 252 : 3660-3670. [PubMed] [Google Scholar]
, and A.J. Fulco. 1977. Биосинтез ненасыщенных жирных кислот бациллами. Гипериндукция и модуляция синтеза десатуразы. Дж. Биол. хим. 252 : 3660-3670. [PubMed] [Google Scholar]
27. Fulco, AJ 1969. Биосинтез ненасыщенных жирных кислот Bacilli. I. Температурная индукция реакции десатурации. Дж. Биол. хим. 244 : 889-895. [PubMed] [Google Scholar]
28. Гарвин Дж. Л. и Дж. Э. Кронан-младший 1980. Термическая модуляция синтеза жирных кислот у Escherichia coli не включает синтез ферментов de novo. Дж. Бактериол. 141 : 1457-1459. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Garwin, JL, AL Klages, and JE Cronan, Jr. 1980. Синтаза белка-носителя бета-кетоацил-ацила II из Escherichia coli. Доказательства функции терморегуляции синтеза жирных кислот. Дж. Биол. хим. 255 : 3263-3265. [PubMed] [Академия Google]
30. Garwin, J.L., A.L. Klages, and J.E. Cronan, Jr. 1980. Структурные, ферментативные и генетические исследования синтаз белка-носителя β-кетоацил-ацила I и II Escherichia coli . Дж. Биол. хим. 255 : 11949-11956. [PubMed] [Google Scholar]
Garwin, J.L., A.L. Klages, and J.E. Cronan, Jr. 1980. Структурные, ферментативные и генетические исследования синтаз белка-носителя β-кетоацил-ацила I и II Escherichia coli . Дж. Биол. хим. 255 : 11949-11956. [PubMed] [Google Scholar]
31. Gelmann, EP, and JE Cronan, Jr. 1972. Мутант Escherichia coli , дефицитный по синтезу цис--вакценовой кислоты. Дж. Бактериол. 112 : 381-387. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32. Грау Р. и Д. де Мендоса. 1993. Регуляция синтеза ненасыщенных жирных кислот температурой роста у Bacillus subtilis . Мол. микробиол. 8 : 535-542. [PubMed] [Google Scholar]
33. Грау Р., Д. Гардиол, Г. К. Гликин и Д. де Мендоса. 1994. Суперспирализация ДНК и терморегуляция синтеза ненасыщенных жирных кислот у Bacillus subtilis . Мол. микробиол. 11 : 933-941. [PubMed] [Академия Google]
[PubMed] [Академия Google]
34. Gualerzi, C.O., A.M. Giuliodori, and C.L. Pon. 2003. Транскрипционный и посттранскрипционный контроль генов холодового шока. Дж. Мол. биол. 331 : 527-539. [PubMed] [Google Scholar]
35. Хит, Р. Дж., С. В. Уайт и К. О. Рок. 2001. Биосинтез липидов как мишень для антибактериальных средств. прогр. Липид Рез. 40 : 467-497. [PubMed] [Google Scholar]
36. Хит Р. Дж. и К. О. Рок. 2002. Конденсация Клайзена в биологии. Нац. Произв. Представитель 19 : 581-596. [PubMed] [Google Scholar]
37. Hoch, JA 2000. Двухкомпонентная и фосфорелирующая передача сигнала. Курс. мнение микробиол. 3 : 165-170. [PubMed] [Google Scholar]
38. Инаба М., И. Судзуки, Б. Салонтай, Ю. Канесаки, Д. А. Лос, Х. Хаяши и Н. Мурата. 2003. Генно-инженерная ригидность мембранных липидов повышает холодовую индуцируемость экспрессии генов у Synechocystis . Дж. Биол. хим. 278 : 12191-12198. [PubMed] [Google Scholar]
Дж. Биол. хим. 278 : 12191-12198. [PubMed] [Google Scholar]
39. Kaneda, T. 1977. Жирные кислоты рода Bacillus : пример предпочтения разветвленной цепи. бактериол. Ред. 41 : 391-418. [Бесплатная статья PMC] [PubMed] [Google Scholar]
40. Kaneda, T. 1991. Изо- и антеизо-жирные кислоты в бактериях: биосинтез, функция и таксономическое значение. микробиол. Ред. 55 : 288-302. [Бесплатная статья PMC] [PubMed] [Google Scholar]
41. Кляйн В., М. Х. Вебер и М. А. Марахил. 1999. Реакция Bacillus subtilis на холодовой шок: зависимое от изолейцина переключение в модели ветвления жирных кислот для адаптации мембран к низким температурам. Дж. Бактериол. 181 : 5341-5349. [Бесплатная статья PMC] [PubMed] [Google Scholar]
42. Кунст, Ф., Н. Огасавара, И. Мосзер, А. М. Альбертини, Г. Аллони, В. Азеведо, М. Г. Бертеро, П.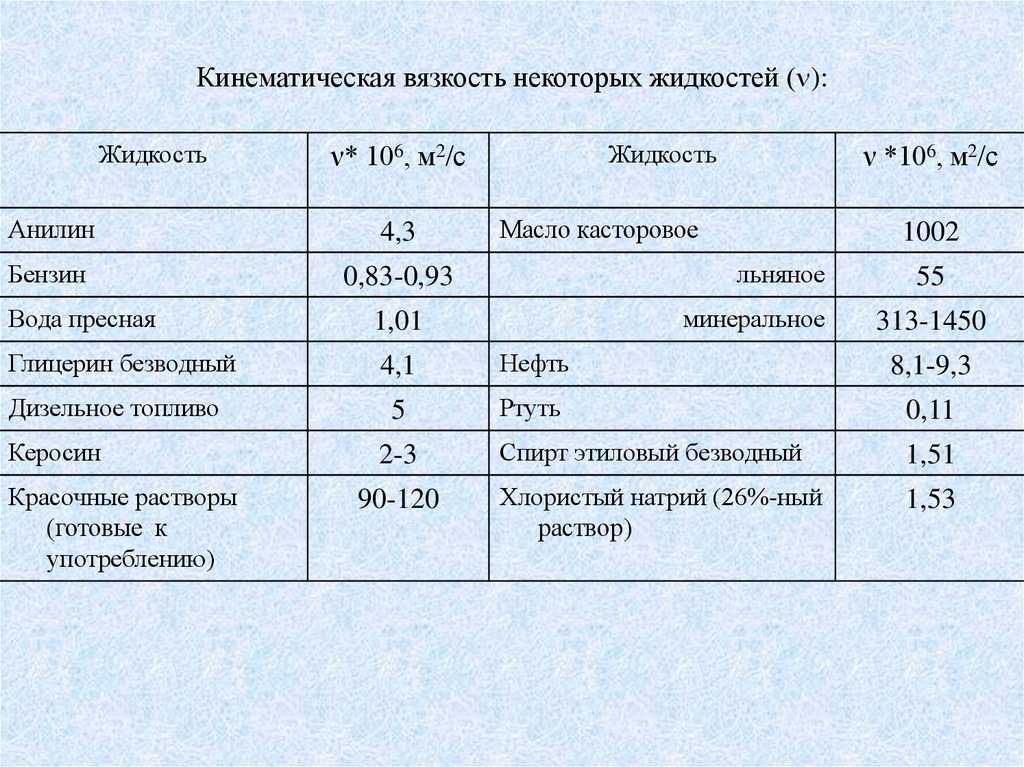 Бессьер, А. Болотин, С. Борхерт, Р. Боррис, Л. Бурсье, А. Бранс, М. Браун, С. К. Бриньелл, С. Брон, С. Бруйе, К. В. Бруски, Б. Колдуэлл, В. Капуано, Н. М. Картер, С. К. Чой, Дж. Дж. Кодани, И. Ф. Коннертон, А. Данчин и др. 1997. Полная последовательность генома грамположительной бактерии Bacillus subtilis . Природа 390 : 249-256. [PubMed] [Google Scholar]
Бессьер, А. Болотин, С. Борхерт, Р. Боррис, Л. Бурсье, А. Бранс, М. Браун, С. К. Бриньелл, С. Брон, С. Бруйе, К. В. Бруски, Б. Колдуэлл, В. Капуано, Н. М. Картер, С. К. Чой, Дж. Дж. Кодани, И. Ф. Коннертон, А. Данчин и др. 1997. Полная последовательность генома грамположительной бактерии Bacillus subtilis . Природа 390 : 249-256. [PubMed] [Google Scholar]
43. Льюис Р. Н. и Р. Н. МакЭлхейни. 1985. Термотропное фазовое поведение модельных мембран, состоящих из фосфатидилхолинов, содержащих изоразветвленные жирные кислоты. 1. Дифференциальные сканирующие калориметрические исследования. Биохимия 24 : 2431-2439. [PubMed] [Google Scholar]
44. Макдональд А. Г. и А. Р. Коссинс. 1985. Теория гомеовязкой адаптации мембран применительно к глубоководным животным. Симп. соц. Эксп. биол. 39 : 301-322. [PubMed] [Google Scholar]
45. Mantsch, H.H., C. Madec, RN Lewis, and RN McElhaney. 1985. Термотропное фазовое поведение модельных мембран, состоящих из фосфатидилхолинов, содержащих изоразветвленные жирные кислоты. 2. Инфракрасные и спектроскопические исследования ЯМР 31Р. Биохимия 24 : 2440-2446. [PubMed] [Академия Google]
1985. Термотропное фазовое поведение модельных мембран, состоящих из фосфатидилхолинов, содержащих изоразветвленные жирные кислоты. 2. Инфракрасные и спектроскопические исследования ЯМР 31Р. Биохимия 24 : 2440-2446. [PubMed] [Академия Google]
46. Mantsch, H.H., C. Madec, R.N. Lewis, and R.N McElhaney. 1987. Термотропное фазовое поведение модельных мембран, состоящих из фосфатидилхолинов, содержащих dl-метил антеизоразветвленные жирные кислоты. 2. Исследование инфракрасной спектроскопии. Биохимия 26 : 4045-4049. [PubMed] [Google Scholar]
47. Марр А. Г. и Дж. И. Ингрэм. 1962. Влияние температуры на состав жирных кислот в Escherichia coli . Дж. Бактериол. 84 : 1260-1267. [Бесплатная статья PMC] [PubMed] [Google Scholar]
48. Marrakchi, H., KH Choi, and CO Rock. 2002. Новый механизм анаэробного образования ненасыщенных жирных кислот у Streptococcus pneumoniae . Дж. Биол. хим. 277 : 44809-44816. [PubMed] [Google Scholar]
Дж. Биол. хим. 277 : 44809-44816. [PubMed] [Google Scholar]
49. Phetsuksiri, B., M. Jackson, H. Scherman, M. McNeil, G.S. Besra, A.R. Baulard, R.A. Slayden, AE DeBarber, C.E. Barry III, M.S. Baird, DC Crick и П. Дж. Бреннан. 2003. Уникальный механизм действия изоксила препарата тиомочевины на Mycobacterium tuberculosis . Дж. Биол. хим. 278 : 53123-53130. [Бесплатная статья PMC] [PubMed] [Google Scholar]
50. Сакамото Т. и Н. Мурата. 2002. Регуляция десатурации жирных кислот и ее роль в толерантности к холоду и солевому стрессу. Курс. мнение микробиол. 5 : 208-210. [PubMed] [Google Scholar]
51. Судзуки И., Д. А. Лос, Ю. Канесаки, К. Миками и Н. Мурата. 2000. Путь восприятия и передачи низкотемпературных сигналов у Synechocystis . EMBO J. 19 : 1327-1334. [Бесплатная статья PMC] [PubMed] [Google Scholar]
52. Судзуки И., Ю. Канесаки, К. Миками, М. Канехиса и Н. Мурата. 2001. Гены холодовой регуляции под контролем холодового сенсора Hik33 у Synechocystis . Мол. микробиол. 40 : 235-244. [PubMed] [Google Scholar]
Судзуки И., Ю. Канесаки, К. Миками, М. Канехиса и Н. Мурата. 2001. Гены холодовой регуляции под контролем холодового сенсора Hik33 у Synechocystis . Мол. микробиол. 40 : 235-244. [PubMed] [Google Scholar]
53. Тотчер Д. Р., М. Дж. Ливер и П. А. Ходжсон. 1988. Последние достижения в области биохимии и молекулярной биологии жирных ацилдесатураз. прогр. Липид Рез. 37 : 73-117. [PubMed] [Google Scholar]
54. Van Alphen, L., B. Lugtenberg, ET Rietschel, and C. Mombers. 1979. Архитектура наружной мембраны Escherichia coli K12. Фазовые переходы рецепторного комплекса бактериофага К3. Евро. Дж. Биохим. 101 : 571-579. [PubMed] [Google Scholar]
55. Виг Л., Д. А. Лос, И. Хорват и Н. Мурата. 1993. Первичный сигнал в биологическом восприятии температуры: Pd-катализируемое гидрирование мембранных липидов стимулировало экспрессию гена desA в Synechocystis PCC6803.
