Тепловые свойства газов
Тепловые свойства газов определяются их теплоемкостью, теплопроводностью, теплосодержанием и теплотой сгорания.
Теплоемкостью газа называется его способность при нагревании поглощать теплоту. Теплоемкость газа С можно выразить отношением подведенного к газу количества теплоты ∆Q к изменению температуры ∆Т:
С=lim ∆Q/∆Т,
∆Т→0
Теплоемкость газа представляет собой количество теплоты, необходимое для нагрева газа на 1 К. Единица измерения теплоемкости — Дж/К. Если теплоемкость отнести к количеству газа, то получим удельную теплоемкость.
Удельной теплоемкостью называется отношение подведенного к газу количества теплоты к произведению единицы количества газа и изменения его температуры.
В зависимости от того, что принимается за единицу количества газа, удельная теплоемкость называется
 Указанные теплоемкости связаны друг
с другом следующими соотношениями:
Указанные теплоемкости связаны друг
с другом следующими соотношениями:Cm = CM /M, СV=CM/VM, CM = CmM = CVVM
где М — молярная масса, кг/моль; VM — молярный объем, м3/моль (для идеального газа при стандартных условиях VM ~ 22,4•10-3 м3/моль).
Удельная теплоемкость зависит от температуры. Различают удельные теплоемкости при постоянном объеме сv и при постоянном давлении ср. Из
термодинамики известно, что в случае
нагревания газа при постоянном объеме
теплота расходуется на увеличение
только внутренней энергии. При
нагревании газа при постоянном давлении
теплота расходуется также и на работу
расширения. Следовательно, ср > сv. Для идеального газа работа расширения
равна универсальной газовой постоянной R и справедливо уравнение:
При
нагревании газа при постоянном давлении
теплота расходуется также и на работу
расширения. Следовательно, ср > сv. Для идеального газа работа расширения
равна универсальной газовой постоянной R и справедливо уравнение:
ср — сv = R
Отношение удельной теплоемкости при постоянном давлении к удельной теплоемкости при постоянном объеме называется
ср / сv = К.
Массовая и объемная теплоемкости с повышением температуры возрастают, а с увеличением молекулярной массы уменьшаются. Показатель адиабаты с повышением температуры и увеличением молекулярной массы уменьшается. Для идеального газа он примерно равен 1,667, для двухатомных газов — 1,41, для трехатомных — 1,34.
Различают
истинную с и среднюю с’ теплоемкости.
Истинной теплоемкостью называется количество теплоты, необходимое для изменения температуры единицы количества газа на 1 К при данных р и Т или V и Т.
Средняя теплоемкость — это количество теплоты, необходимое для изменения температуры единицы количества газа на 1 К в заданном интервале температур, т.е. от Т1 до Т. Среднюю объемную теплоемкость при постоянном давлении газа можно определить по средним теплоемкостям компонентов и их объемным долям:
с’р = 0,01 (с’Н2 *Н2+ с’СО *СО+ с’СН4 *СН4 +….+ с’n *N2)
где с’Н2 с’СО с’СН4 с’n — средние
объемные теплоемкости указанных в
индексах компонентов; Н2,
СО, СН4. ..
N2 — объемные доли компонентов, %. Значения
средней объемной теплоемкости горючих
газов и продуктов сгорания приведены
в табл. 5.6.
..
N2 — объемные доли компонентов, %. Значения
средней объемной теплоемкости горючих
газов и продуктов сгорания приведены
в табл. 5.6.
Теплопроводность газа — это его способность проводить теплоту, т.е. осуществлять молекулярный перенос энергии. Молекулы участков газа, где температура выше, обладают большей энергией и передают ее соседним молекулам, обладающим меньшей энергией. Это приводит к выравниванию разности температур ∆Т, но передача теплоты не связана с переносом частиц.
Таблица 5.6
Средняя объемная теплоемкость при постоянном давлении кДж /(м3К) горючих газов в интервале температур от о до t
Температура, °С | СО | Н2 | H2S | СН4 | С2Н4 | C2H6 | С3Н8 | С4Н10 | С5Н12 |
0 | 1,299 | 1,277 | 1,513 | 1,544 | 1,792 | 2,227 | 3,039 | 4,128 | 5,129 |
100 | 1,302 | 1,292 | 1,543 | 1,653 | 2,031 | 2,525 | 3,450 | 4,517 | 5,837 |
200 | 1,307 | 1,297 | 1,574 | 1,765 | 2,257 | 2,800 | 3,860 | 5,255 | 6,515 |
300 | 1,317 | 1,300 | 1,608 | 1,890 | 2,466 | 3,077 | 4,271 | 5,774 | 7,135 |
400 | 1,329 | 1,302 | 1,644 | 2,019 | 2,658 | 3,333 | 4,681 | 6,268 | 7,742 |
500 | 1,343 | 1,305 | 1,682 | 2,144 | 2,839 | 3,571 | 5,095 | 6,691 | 8,257 |
600 | 1,357 | 1,308 | 1,719 | 2,264 | 3,006 | 3,793 | 5,431 | 7,114 | 8,784 |
700 | 1,372 | 1,312 | 1,756 | 2,381 | 3,157 | 4,003 | 5,724 | 7,486 | 9,232 |
Кратковременная контрольная работа №5 по теме «Тепловые свойства газов, жидкостей и твердых тел».

Главная / Старшие классы / Физика
Скачать
24.5 КБ, 1080457.doc Автор: Маркина Марина Владимировна, 3 Мая 2015
Кратковременная контрольная работа №5 по теме «Тепловые свойства газов, жидкостей и твердых тел».
Автор: Маркина Марина Владимировна
Похожие материалы
| Тип | Название материала | Автор | Опубликован |
|---|---|---|---|
| документ | Кратковременная контрольная работа №5 по теме «Тепловые свойства газов, жидкостей и твердых тел». | Маркина Марина Владимировна | 3 Мая 2015 |
| разное | Контрольная работа Давление твердых тел, жидкостей и газов | Саакян Татьяна Николаевна | 21 Мар 2015 |
| документ | Контрольная работа Давление твердых тел, жидкостей и газов | Саакян Татьяна Николаевна | 21 Мар 2015 |
| разное | Урок-игра по теме: «Давление твердых тел, жидкостей и газов» (7 класс) | Клинкова Татьяна Владимировна | 21 Мар 2015 |
| документ | Конспект урока: Решение задач по теме «Давление твердых тел, жидкостей и газов» (7 класс). | Осипова Галина Николаевна | 31 Мар 2015 |
| документ | Контрольная работа по физике 7 класс «Давление твердых тел, жидкостей и газов» | Свиридова Татьяна Александровна | 4 Апр 2015 |
| документ | Лабораторная работа по физике №4 по теме Измерение объемов твердых тел, жидкостей и газов. 7 класс | Каримова Светлана Азгамовна | 21 Мар 2015 |
| презентация | Презентация к открытому уроку по физике по теме: «Давление твердых тел , жидкостей , газов, закон Архимеда». | Корниенко Светлана Валентиновна | 21 Мар 2015 |
| документ | урок обобщения и систематизации знаний, умений и навыков учащихся по теме «Давление твердых тел, жидкостей и газов», 7 класс | Степура Ирина Алексеевна | 21 Мар 2015 |
| документ | Технологическая карта урока обобщения и систематизации знаний по теме «Давление твердых тел, жидкостей и газов» | Шостак Мария Юрьевна | 6 Дек 2015 |
| документ | 7 класс тесты по физике по теме «Давление твердых тел, жидкостей и газов» | Шведова Светлана Николаевна | 21 Мар 2015 |
| разное | Разработка урока физики в 7 классе по теме «Строение твердых тел, жидкостей и газов» | Беседина Антонина Николаевна | 21 Мар 2015 |
| документ | обобщающий урок по теме «Давление твердых тел, жидкостей и газов» | Николаева Вера Владимировна | 21 Мар 2015 |
| презентация | Тест для 7 класса по теме «Давление твердых тел, жидкостей и газов» | Королева Татьяна Юрьевна | 21 Мар 2015 |
| разное | Урок–игра по теме «Давление твердых тел, жидкостей и газов» (7-й класс) | Хасанова Кадрия Абдрахмановна | 31 Мар 2015 |
| разное | Контрольная работа на тему: « Давление твёрдых тел, жидкостей и газов ». 7 класс. 7 класс. | Царёва Светлана Геннадьевна | 6 Дек 2015 |
| документ | Агрегатные состояния вещества. Свойства газов, жидкостей и твердых тел. Физика, 7 класс. | Григорьева Анна Владимировна | 21 Мар 2015 |
| разное | Свойства твёрдых тел, жидкостей и газов. | Авдошина Валентина Юрьевна | 20 Мар 2015 |
| документ | Разработка урока по теме: «Свойства паров, жидкостей и твердых тел» | Полянин Сергей Борисович | 15 Июн 2015 |
| разное | игра «Давление твердых тел, жидкостей и газов» | Ежукевич Юлия Валериевна | 21 Мар 2015 |
| документ | Давление твердых тел, жидкостей и газов. | Убушаева Маргарита Андреевна | 21 Мар 2015 |
| презентация | Давление твердых тел, жидкостей и газов | Лоскунина Надежда Александровна | 31 Мар 2015 |
| разное | проект «Давление твердых тел, жидкостей и газов» | Захарова Елена Григорьевна | 4 Ноя 2015 |
| документ | 7 класс Тест по теме «Давление твердых тел, жидкостей, газов, архимедова сила» | Желнова Наталья Васильевна | 21 Мар 2015 |
| документ | Контрольная-тест по теме «Давление твёрдых тел, жидкостей и газов» | Юрышева Юлия Генриховна | 21 Мар 2015 |
| документ | Игра-соревнование по физике «Давление твердых тел, жидкостей и газов» | титова-Ивакина Елена Васильевна | 21 Мар 2015 |
| документ | Разработка урока по физике 7 кл. «Три состояния вещества. Различие в молекулярном строении твердых тел, жидкостей и газов» «Три состояния вещества. Различие в молекулярном строении твердых тел, жидкостей и газов» | Головин А.Н. | 22 Мая 2015 |
| презентация, документ | «Три состояния вещества. Различие в молекулярном строении газов, жидкостей, твердых тел», 7 класс | Матвеева Вера Владимировна | 21 Мар 2015 |
| документ | Урок природоведения в 5 классе «Свойства твёрдых тел, жидкостей и газов» | Морозова Марина Викторовна | 31 Мар 2015 |
| документ | Свойства твёрдых тел, жидкостей и газов. | Авдошина Валентина Юрьевна | 20 Мар 2015 |
| документ | Свойства твёрдых тел, жидкостей и газов | Шило Светлана Анатольевна | 20 Мар 2015 |
| презентация, документ | Свойства твердых тел и жидкостей | Кравчук Ирина Станиславовна | 21 Мар 2015 |
| документ | Контрольная работа в формате ЕГЭ 2015 7 класс «Давление твердых тел, жидкостей и газа» | Мельникова Евгения Анатольевна | 21 Мар 2015 |
| разное | Тест по теме «Взаимные превращения жидкостей и газов» 10 класс | Смольянинова Светлана Анатольевна | 4 Апр 2015 |
| документ | Урок 7 класс Три состояния вещества. Различие в молекулярном строении твердых тел, жидкостей и газов. Различие в молекулярном строении твердых тел, жидкостей и газов. | Соболева Алла Ивановна | 21 Мар 2015 |
| презентация | Презентация к аттестации на тему «Давление твердых тел, жидкостей и газов» | Лоскунина Надежда Александровна | 21 Мар 2015 |
| документ | «Три состояния вещества. Различие в молекулярном строении твердых тел, жидкостей и газов.» | Филатова Алла Петровна | 21 Мар 2015 |
| документ | Формирование представлений об отдельных этапах цикла познания при изучении темы «Давление твердых тел, жидкостей и газов» | Казанцева Евгения Александровна | 23 Сен 2015 |
| презентация, документ | Обобщающий урок на тему «Давление твердых тел, жидкостей и газов» | Ширяева Ирина Николаевна | 16 Окт 2015 |
| разное | Интегрированный урок «Строение газов, жидкостей, твердых тел с точки зрения МКТ». | Шмаровоз Анна Николаевна | 21 Мар 2015 |
В отличие от традиционного подхода, здесь в одной таблице объединены основные механические и тепловые свойства. Если не указано иначе, все данные соответствуют нормальным условиям — комнатной температуре (18..25°C) при стандартном атмосферном давлении (101325 Па). Для некоторых веществ даны параметры в нескольких агрегатных состояниях — в соответствующих разделах таблицы. Вещества и материалы в одном агрегатном состоянии размещены в алфавитном порядке. Прочерки означают отсутствие данных. Неприменимость понятия (например, дерево не может плавиться) обозначается словом «нет». В случае диапазона значений какого-либо параметра более предпочтительное выделено курсивом (если курсива нет, в качестве наиболее предпочтительного следует брать среднее). Все величины приведены в базовых единицах системы СИ, то есть в общефизические расчётные формулы следует подставлять именно эти значения. Если же для расчёта применяются специальные технические или эмпирические формулы, то там могут использоваться нестандартные единицы измерения. В таком случае следует проверить, в каких именно единицах измерения туда надо подставить данные, и при необходимости перед расчётом выполнить соответствующие преобразования значений к необходимым единицам измерения. Внимание! Все приведённые данные не являются истиной в последней инстанции и время от времени дополняются и уточняются. Просмотр всей ширины таблиц возможен в полноэкранном режиме при разрешении экрана по горизонтали не менее 1280 пикселей, для меньшей ширины окна браузера может потребоваться использование горизонтальной прокрутки. Основные механические и тепловые свойства твёрдых тел Для гигроскопичных материалов (древесина, мел, уголь и пр.
Основные механические и тепловые свойства жидкостей
Основные механические и тепловые свойства газов и паровЕсли не указано иначе, данные приведены для температуры 0°С и атмосферного давления. Здесь же приводится соотношение теплоёмкостей, используемое при расчётах по уравнению адиабаты (в диапазоне 0° .. 25°С эти значения изменяются менее чем на 1%). Температуры указаны как в градусах Цельсия, так и в кельвинах. В термодинамические формулы следует подставлять именно кельвины! Газокинетические параметры вынесены в отдельную таблицу.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| последняя правка 04.03.2011 21:17:58 |
Глава 16. Свойства газов, жидкостей и твердых тел.Фазовые переходы. Влажность
Задачи и вопросы, в которых рассматриваются свойства газов, жидкостей и твердых тел, а также переходы между ними (фазовые переходы), входят в программу школьного курса физики и часто включаются в ЕГЭ.
Начнем со свойств трех агрегатных состояний вещества. Плотности жидкостей и твердых тел близки друг к другу, но сильно отличаются от плотности газа. Отсюда следует, что расстояния между молекулами в жидкости и твердом теле не сильно отличаются друг от друга, но гораздо меньше расстояния между молекулами в газе. Различие же молекулярного строения жидкостей и твердых тел заключается в том, что большинство твердых тел имеют кристаллическую структуру: их молекулы располагаются в определенном порядке, повторяя определенную структурную единицу, которая называется элементарной ячейкой. Различают моно- и поликристаллы. Монокристаллом называется такое кристаллическое тело, порядок в расположении молекул которого имеет место вдоль всего тела. Очень часто монокристаллическое тело обладает правильной геометрической формой. Поликристалл представляет собой совокупность связанных друг с другом, хаотически ориентированных по отношению друг к другу маленьких монокристаллов.
Различают моно- и поликристаллы. Монокристаллом называется такое кристаллическое тело, порядок в расположении молекул которого имеет место вдоль всего тела. Очень часто монокристаллическое тело обладает правильной геометрической формой. Поликристалл представляет собой совокупность связанных друг с другом, хаотически ориентированных по отношению друг к другу маленьких монокристаллов.
Из-за того, что разные направления в элементарной ячейке кристалла неэквивалентны, ряд его физических свойств, таких как прочность, электро- или теплопроводность неодинаковы в различных направлениях. Это свойство кристалла называется анизотропией. Конечно, это касается только монокристалла. Поликристаллы из-за различных ориентаций монокристаллических частей являются изотропными. Также изотропными являются жидкости, молекулы которых расположены беспорядочно.
Существуют, однако, такие тела, которые являются твердыми, но в расположении молекул которых нет кристаллического порядка. Такие тела называются аморфными. Аморфными являются биополимеры, стекло и ряд других веществ. Отсутствие порядка в расположении молекул проявляется в отсутствие у аморфных тел строго определенной температуры плавления (см. ниже).
Такие тела называются аморфными. Аморфными являются биополимеры, стекло и ряд других веществ. Отсутствие порядка в расположении молекул проявляется в отсутствие у аморфных тел строго определенной температуры плавления (см. ниже).
Как показывает опыт, при изменении температуры и внешнего давления возможны переходы вещества из одного агрегатного состояния в другое. Переход кристаллического твердого тела в жидкое называется плавлением, обратный процесс — кристаллизацией. Переход жидкости в пар называется испарением (или кипением, если этот процесс сопровождается образованием пузырьков пара в жидкости), обратный процесс — конденсацией. Плавление и кристаллизация твердых (кристаллических) тел происходит при строго определенной для каждого вещества (при фиксированном давлении) температуре. При плавлении необходимо сообщить твердому телу энергию, которая расходуется не на нагревание тела, а на разрыв кристаллических связей между его молекулами. При кристаллизации эта дополнительная энергия выделяется. Плавление аморфных тел происходит по-другому: при увеличении температуры они плавятся постепенно (т.е. становятся более мягкими и пластичными), и невозможно указать такую температуру, ниже которой тело твердое, выше — жидкое.
Плавление аморфных тел происходит по-другому: при увеличении температуры они плавятся постепенно (т.е. становятся более мягкими и пластичными), и невозможно указать такую температуру, ниже которой тело твердое, выше — жидкое.
При испарении жидкостей молекулы вылетают с их поверхности и переходят в газовую фазу. При этом из жидкости могут вылететь только самые быстрые молекулы, поэтому температура жидкости в процессе испарения понижается. Испарение может происходить при любой температуре (за исключением абсолютного нуля), однако с ростом температуры интенсивность испарения возрастает.
Благодаря хаотическому тепловому движению наряду с процессом испарения идет и обратный процесс — конденсация пара, — в результате которого молекулы пара могут вернуться в жидкость. Поскольку скорость процесса конденсации зависит от плотности пара над поверхностью жидкости, при определенной концентрации пара скорости процессов испарения и конденсации совпадают. В этом состоянии не происходит изменения количества жидкости и пара, и устанавливается динамическое равновесие между жидкостью и паром. Пар, находящийся в динамическом равновесии со своей жидкостью называется насыщенным. Насыщенный пар — это пар максимально возможной плотности (при фиксированной температуре). Действительно, если плотность пара станет больше плотности насыщенного пара, то скорость процесса конденсации станет больше скорости испарения — излишек пара сконденсируется, а оставшийся пар станет насыщенным. Пар, имеющий плотность, меньшую плотности насыщенного пара при данной температуре, называется ненасыщенным.
Пар, находящийся в динамическом равновесии со своей жидкостью называется насыщенным. Насыщенный пар — это пар максимально возможной плотности (при фиксированной температуре). Действительно, если плотность пара станет больше плотности насыщенного пара, то скорость процесса конденсации станет больше скорости испарения — излишек пара сконденсируется, а оставшийся пар станет насыщенным. Пар, имеющий плотность, меньшую плотности насыщенного пара при данной температуре, называется ненасыщенным.
Поскольку скорость процесса испарения зависит от температуры жидкости, динамическое равновесие между жидкостью и ее паром при большей температуре установится при бóльших концентрациях пара. Это значит, что концентрация насыщенного пара возрастает с температурой, и, следовательно, его давление растет с ростом температуры быстрее, чем по линейному закону.
Характеристикой воздуха, в котором находятся водяные пары, является его относительная влажность , которая показывает какую долю парциальное давление данного пара (или его концентрация) составляет от давления (или концентрации) насыщенного пара при данной температуре :
(16. |
Если, например, парциальное давление водяного пара в воздухе при некоторой температуре равно , а давление насыщенного пара при этой температуре равно , то относительная влажность этого воздуха составляет 50 %. Очевидно, изменяя температуру и объем воздуха можно менять его относительную влажность. Поскольку концентрация насыщенного пара зависит от температуры, при нагревании воздуха, в котором находится неизменное количество водяных паров, будет убывать его относительная влажность, при охлаждении — возрастать. Если в последнем процессе относительная влажность достигает 100 %, излишек пара конденсируется и при дальнейшем охлаждении относительная влажность не изменяется. Процесс конденсации излишка пара при охлаждении можно наблюдать прохладными ночами летом, когда выпадает роса и образуется туман (маленькие капельки воды). Температура, при которой пар становится насыщенным и образуется конденсат, называется точкой росы этого пара. Также можно изменять относительную влажность воздуха, уменьшая или увеличивая его объем при неизменной температуре. В первом процессе растет концентрация пара (и, следовательно, его относительная влажность), во втором убывает. Конечно, в этих рассуждениях предполагается, что масса водяного пара не изменяется (т.е. не происходит дополнительного испарения воды или конденсации пара).
В первом процессе растет концентрация пара (и, следовательно, его относительная влажность), во втором убывает. Конечно, в этих рассуждениях предполагается, что масса водяного пара не изменяется (т.е. не происходит дополнительного испарения воды или конденсации пара).
Процесс испарения жидкости с образованием пузырьков внутри нее называется кипением. Причина кипения заключается в следующем. Благодаря хаотическому тепловому движению в жидкости всегда образуются микроскопические пузырьки пара. Поскольку они очень малы, пар в них мгновенно становится насыщенным. Дальнейшая «судьба» этих пузырьков зависит от соотношения давлений: внутреннего, которое равно давлению насыщенного пара при данной температуре, и внешнего, которое равно давлению атмосферного воздуха (в пренебрежении гидростатическим давлением жидкости). Если внутреннее давление меньше внутреннего, пузырек пара пропадет, а пар из него перейдет в жидкость, если наоборот — пузырек будет расширяться, при этом за счет интенсивного испарения жидкости с поверхности пузырька, пар в нем будет оставаться насыщенным. Затем такие пузырьки всплывают, и пар из них уходит из жидкости. Таким образом, кипение жидкости происходит при такой температуре, при которой давление насыщенного пара этой жидкости равно атмосферному давлению.
Затем такие пузырьки всплывают, и пар из них уходит из жидкости. Таким образом, кипение жидкости происходит при такой температуре, при которой давление насыщенного пара этой жидкости равно атмосферному давлению.
В задаче 16.1.1 жидкому состоянию отвечает рисунок 2. На рисунке 1 представлена схема расположения молекул кристаллического тела (есть порядок в расположении молекул), на рисунке 3 — газ (малая по сравнению с двумя другими состояниями концентрация молекул). Поэтому в процессе перехода вещества из жидкого состояния в кристаллическое (кристаллизации) существенно возрастает упорядоченность в расположении молекул (задача 16.1.2 — ответ 4).
Горизонтальный участок графика в задаче 16.1.3 отвечает плавлению. Действительно, в течение процесса, которому отвечает горизонтальный участок графика, энергия телу сообщалась, а его температура не изменялась. Единственная возможность объяснить эту «потерю» энергии, это допустить, что сообщаемая энергия расходовалась на разрыв кристаллических связей между молекулами. Поэтому температура плавления вещества — 50 (ответ 3), при этом в начале горизонтального участка имеется только твердое вещество, в конце — только жидкость, в промежуточных состояниях — смесь твердого тела и жидкости. Таким образом, из этого опыта следует, что для превращения любого твердого тела при температуре плавления (например, льда при температуре ) в жидкость нужно затратить некоторую энергию (правильный ответ в задаче 16.1.4 — 2). Поэтому внутренняя энергия жидкости при температуре плавления больше внутренней энергии твердого тела при той же температуре (задача 16.1.5 – ответ 1).
Поэтому температура плавления вещества — 50 (ответ 3), при этом в начале горизонтального участка имеется только твердое вещество, в конце — только жидкость, в промежуточных состояниях — смесь твердого тела и жидкости. Таким образом, из этого опыта следует, что для превращения любого твердого тела при температуре плавления (например, льда при температуре ) в жидкость нужно затратить некоторую энергию (правильный ответ в задаче 16.1.4 — 2). Поэтому внутренняя энергия жидкости при температуре плавления больше внутренней энергии твердого тела при той же температуре (задача 16.1.5 – ответ 1).
По этой же причине в процессе кристаллизации, который является обратным плавлению, энергия выделяется. Например при превращении воды, имеющей температуру , в лед, имеющий ту же температуру, выделяется определенная энергия (задача 16.1.6 — ответ 1).
Металлы проводят электрический ток, причем проводимость металла осуществляется электронами, оторвавшимися от атомов металла (свободные электроны). А поскольку электроны заряжены отрицательно, в узлах кристаллической решетки металла находятся положительно заряженные ионы (задача 16.1.7 — ответ 3).
А поскольку электроны заряжены отрицательно, в узлах кристаллической решетки металла находятся положительно заряженные ионы (задача 16.1.7 — ответ 3).
Как это описано во введении к настоящей главе, аморфное тело является твердым, но отличается от кристаллического тела отсутствием кристаллической структуры (задача 16.1.8 — ответ 1). Среди веществ, перечисленных в задаче 16.1.9, аморфным является только стекло (ответ 1). Аморфное тело отличается от монокристаллического отсутствием определенной температуры плавления и изотропией (задача 16.1.10 — ответ 2).
В задаче 16.2.1 на первый взгляд кажется, что влажный воздух тяжелее сухого, поскольку во влажном воздухе содержатся дополнительное количество воды. Это, однако, не так, ведь требуется сравнить массы сухого и влажного воздуха при одинаковых давлениях, а если добавить в сухой воздух молекулы воды, не убирая молекулы собственно воздуха, то давление смеси увеличится. По закону Дальтона (см. гл. 13) давление смеси определяется полным числом молекул газа независимо от их природы. Поэтому чтобы давление сухого и влажного воздуха было одинаковым, число молекул в сухом и влажном воздухе должно быть одинаковым. А поскольку молярная масса воздуха 29 г/моль больше молярной массы воды 18 г/моль, то каждая («усредненная») молекула воздуха тяжелее молекулы воды. Поэтому сухой воздух тяжелее влажного при одинаковых давлении и температуре (ответ 1).
По закону Дальтона (см. гл. 13) давление смеси определяется полным числом молекул газа независимо от их природы. Поэтому чтобы давление сухого и влажного воздуха было одинаковым, число молекул в сухом и влажном воздухе должно быть одинаковым. А поскольку молярная масса воздуха 29 г/моль больше молярной массы воды 18 г/моль, то каждая («усредненная») молекула воздуха тяжелее молекулы воды. Поэтому сухой воздух тяжелее влажного при одинаковых давлении и температуре (ответ 1).
Как отмечалось во введении, жидкости могут испаряться при любой температуре (задача 16.2.2 — ответ 4).
Диффузией называется процесс взаимного проникновения молекул двух разных газов или жидкостей благодаря хаотическому тепловому движению. Поэтому при повышении температуры из-за увеличения скорости теплового движения молекул процесс диффузии ускоряется (задача 16.2.3 — ответ 1).
При испарении из жидкости вылетают наиболее быстрые молекулы, т. е. молекулы, кинетическая энергия которых превышает среднюю кинетическую энергию молекул жидкости (задача 16.2.4 — ответ 2).
е. молекулы, кинетическая энергия которых превышает среднюю кинетическую энергию молекул жидкости (задача 16.2.4 — ответ 2).
По определению насыщенный пар — это такой пар, который находится в динамическом равновесии со своей жидкостью (задача 16.2.5 — ответ 3).
При двукратном увеличении объема сосуда в задаче 16.2.6 при условии, что воды в сосуде нет, и дополнительного испарения не происходит, концентрация водяного пара уменьшается в два раза и, следовательно, составляет половину от концентрации насыщенного пара, каковым пар в сосуде был в начале процесса. Поэтому пар в сосуде перестанет быть насыщенным, его относительная влажность станет равна 50 % (ответ 3).
Наоборот, пар можно сделать насыщенным, либо увеличивая его концентрацию, либо уменьшая температуру при неизменной концентрации (поскольку при этом уменьшается давление насыщенного пара). В свою очередь концентрацию пара можно увеличить, испаряя в воздух дополнительное количество воды, либо уменьшая его объем. Поэтому из данных в задаче 16.2.7 ответов подходит только ответ 2.
Поэтому из данных в задаче 16.2.7 ответов подходит только ответ 2.
Относительная влажность воздуха показывает, какую долю от давления насыщенного пара при данной температуре представляют собой давление паров воды в этом воздухе. Поэтому давление насыщенного пара в задаче 16.2.8 равно (ответ 1).
Давление водяного пара в воздухе в задаче 16.2.9 составляет одну двадцатую от давления насыщенного пара при данной температуре. Поэтому относительная влажность этого воздуха равна 5 % (ответ 2).
Кипение возникает, если давление насыщенного водяного пара совпадает с внешним давлением. Поэтому при увеличении внешнего давления кипение будет происходить при такой температуре, при которой возрастет давление насыщенного водяного пара. А поскольку давление насыщенного пара увеличивается при повышении температуры, то при увеличении внешнего воздействия температура кипения жидкости будет возрастать (задача 16. 2.10 — ответ 2).
2.10 — ответ 2).
8. Тепловые свойства. Физико-химические свойства нефти и газа
Физико-химические свойства нефти и газа
реферат
Главнейшим свойством нефти и горючих газов, принесшим им мировую славу исключительных энергоносителей, является их способность выделять при сгорании значительное количество теплоты.
Теплотой сгорания называется отношение количества теплоты, выделяющейся при горении, к массе сгоревшего до конца (т.е. до образования углекислоты СО 2 и воды Н2О) топлива.
Нефть, природный горючий газ и их производные обладают наивысшей среди всех видов топлива теплотой сгорания. Теплота сгорания нефти — 41 МДж/кг — в 1,3 раза больше теплоты сгорания лучших сортов каменных углей — 31 МДж/кг; теплота сгорания бензина — 42 МДж/кг, дизельного топлива — 42,7 МДж/кг, этана, пропана и бутана — соответственно 64,5; 93,4 и 124, а природного газа — 35,6 МДж/м3.
Теплоту сгорания нефти, керосина и других нефтепродуктов определяют в калориметрической бомбе, а газов — в газовом калориметре. Для нефтей теплота сгорания колеблется в узких пределах: от 40 000 до 45 000 кДж/кг, причем получаемая величина тем больше, чем меньше плотность нефтей (и соответственно их фракций). Теплота сгорания нефтепродуктов зависит также от особенностей их углеводородного состава. Приближенно с погрешностью 3-5% теплоту сгорания нефтей и нефтепродуктов можно вычислить при помощи различных эмпирических формул, например по данным их элементного анализа (Д.И. Менделеев), а также по их плотности (формула Крэго).
Для нефтей теплота сгорания колеблется в узких пределах: от 40 000 до 45 000 кДж/кг, причем получаемая величина тем больше, чем меньше плотность нефтей (и соответственно их фракций). Теплота сгорания нефтепродуктов зависит также от особенностей их углеводородного состава. Приближенно с погрешностью 3-5% теплоту сгорания нефтей и нефтепродуктов можно вычислить при помощи различных эмпирических формул, например по данным их элементного анализа (Д.И. Менделеев), а также по их плотности (формула Крэго).
Делись добром 😉
Анализ эффективности системы разработки Вахского нефтяного месторождения (Тюменская область)
2.4 Коллекторские свойства
Фильтрационно-емкостные характеристики и нефтенасыщенность пластов оценивались по керновым, промыслово-геофизическим и гидродинамическим исследованиям…
Асбест
Физические свойства
Асбест — высокотермостойкий материал, обладающий жаро- и огнестойкостью…
Асбест
Химические свойства
По составу асбест — это природный магниевый гидросиликат, содержащий также окислы других элементов. Существует ряд разновидностей асбеста, но промышленное значение имеют два основных вида, имеющие, в частности…
Существует ряд разновидностей асбеста, но промышленное значение имеют два основных вида, имеющие, в частности…
Бентонит как природный наноматериал
4 Свойства бентонитов
…
Выбор и расчет оборудования для депарафинизации нефтяных скважин в условиях НГДУ «ЛН»
2.3.5 Тепловые методы, применяемые в НГДУ «ЛН» для борьбы с отложениями АСПО
Если интенсивность отложения парафина невелика, то при каждом подземном ремонте поднимают трубы на поверхность и удаляют из них парафин пропариванием с помощью ППУ. Очистка скважин…
Геологические условия формирования коллекторов месторождения Восточный Челекен в Туркменистане
3.1 Коллекторские свойства
По месторождению Восточный Челекен по материалам ранних исследователей (Р. Т. Еганянц, Н. Мамиесенов и др.) характер распределения по площади и по разрезу выделяется несколько типов пород-коллекторов…
Геофизические методы исследования горизонтальных скважин Федоровского нефтегазового месторождения Западной Сибири
4.
 1 Плотностные свойства
1 Плотностные свойстваПлотность для залежей нефти определяется в основном плотностью пород-коллекторов, которая в свою очередь зависит от их пористости и в меньшей степени от минерального состава…
Инженерная геология для строительства
3. Назовите основные физико-механические свойства горных пород, знание которых необходимо для проектирования и строительства. Опишите условия образования и строительные свойства грунтовых отложений (табл. 3)
Для проектирования и строительства необходимо знание о следующих свойствах горных пород: Минеральный состав горных пород: породообразующие минералы, количество минералов в породе, их свойства, состав…
Каштановые почвы — зональный тип почв сухих степей
3. Свойства почвы
…
Минералы и их свойства
СВОЙСТВА
Важнейшими характеристиками минералов являются кристаллохимическая структура и состав. Все остальные свойства минералов вытекают из них или с ними взаимосвязаны. Важнейшие свойства минералов. ..
..
Неметаллические полезные ископаемые. Асбест
СВОЙСТВА АСБЕСТА
Термин <асбест> объединяет различные по своему составу и свойствам минералы: хризотил, крокидолит, амозит, антофиллит, иногда тремолит, актинолит, режикит (близок магнезиорибекиту и магнезиоарфведсониту)…
Особенности, ценность и добыча яшмы
4. Свойства
Яшма — это кремнистая горная порода с волокнистой структурой. Она характеризуется весьма плотным сложением, большой вязкостью, довольно высокой твердостью (7), плотностью около 2,58-2,91 г/см3 и показателями преломления 1,54-1…
Петрофизические свойства намывных отложений г. Гомеля
1.3 Тепловые свойства горных пород
Изучение теплофизических характеристик горных пород лежит в основе применения методов термометрии при поисках, разведке, эксплуатации и контроле разработки нефтяных и газовых месторождений…
Проект зарезки второго ствола в нефтяной скважине Кудако-Киевского месторождения
1.4 Физико-химические свойства нефти, газа, воды и коллекторские свойства горных пород
Свойства пластовой нефти обобщены по 7 глубинным пробам, отобранным из 7 скважин и исследованным в лаборатории пластовых флюидов. Анализ поверхностных проб показал, что нефть рассматриваемого месторождения относится к нафтеновому типу…
Анализ поверхностных проб показал, что нефть рассматриваемого месторождения относится к нафтеновому типу…
Этот многоликий алмаз
1. Свойства алмаза
Этот удивительный минерал известен людям уже более 5000 лет. Описывая алмаз, десятки раз употребляют слово «самый» — самый твёрдый, самый блестящий, самый износостойкий, самый дорогой, самый редкий…
Реферат на тему Физические и тепловые свойства горючих газов
Цены в 2-3 раза ниже
Мы работаем
7 дней в неделю
Только проверенные эксперты
Готовые работы / Рефераты / Энергетика / Физические и тепловые свойства горючих газов
Что найти?
Введение
Еще три века назад слова «газ» не существовало. Его впервые ввел в
Его впервые ввел в
XVII веке голландский ученый Ван-Гельмонт. Оно определяло вещество, в
отличии от твердых и жидких тел способное распространятся по всему
доступному ему пространству без скачкообразного изменения своих свойств.
С тех пор слово «газ» во все основные языки мира. Среди известного
комплекса естественных полезных ископаемых, относящихся к топливно-
энергетичесской группе, одно из основных по использованию в народном
хозяйстве странны занимают природные горючие газы.
В топливно-энергетичесских ресурсах мира природный газ оценивается
в 630 млрд. тут, что составляет 4,9% от общей суммы топливных ресурсов, а
возможное извлекаемое количество его определяется в 500 млрд. тут, т. е.
Около 80% от прогнозных ресурсов. Известно, что доля природного газа в
общемировом энергетическом балансе с 1900 г. возрастала медленными
темпами и в мировом потреблении различных видов топлива в начале
текущего столетия оценивалось в 0,9%.
Природный газ имеет широкое применение в народном хозяйстве.
Также природный газ лучший вид топлива. Его отличают полноте сгорания
без дыма и копоти; отсутствие золы после сгорания; легкость розжига и
регулирование процесса горения. Запасы природного газа на нашей планете
очень велик. Он является источником сырья для химической
промышленности. Помимо природного газа существует искусственный газ.
Впервые он был получен в лабораторных условиях в конце XVIII века.
Искусственным газом сначала освещались улицы и помещения, поэтому его
и назвали «светильным газом». Помимо названных газов существуют также
попутные нефтяные газы. По своему происхождению тоже является
природным газом.
Глава 1. Общие сведения
1.1. Происхождение природных горючих газов
Газы — это одно из агрегатных состояний вещества, в котором его
частицы движутся хаотически, равномерно заполняя весь возможный объем.
В XVII в. нидерландский химик Я. Б. Ван Гельмонт ввел термин «газ»
(от гр. хаос) для обозначения воздухоподобных веществ.
Природные горючие газы состоят в основном из углеводородов
метанового ряда. Они содержат метан, этан, пропан, бутан, пентан и гексан, а
также их изомеры. Кроме углеводородов в составе природных газов могут
присутствовать азот, диоксид углерода, сероводород, водород и инертные
газы.
Природные газы добывают из недр земли. Месторождения природных
газов подразделяются на газовые, газоконденсатные, газонефтяные.
Углеводородные газы содержатся, кроме того, в растворенном виде в
нефтяных месторождениях. Такие газы называются попутными или
нефтяными.
Похожие работы
Стандартизация в Российской Федерации и за рубежом в области защиты от поражения электрическим током (ГОСТ Р 58698-2019)
Реферат, Электроэнергетика
Смотреть
Виды конфигурации схем электроснабжения
Реферат, Общая энергетика
Смотреть
Структурная схема, назначение и работа элементов, схемы, принцип работы станции, КПД трехконтурной АЭС
Реферат, Общая энергетика
Смотреть
Тепловая электростанция
Реферат, Общая энергетика
Смотреть
Основные источники искажения синусоидальности напряжения
Реферат, Энергетика
Смотреть
Сделайте индивидуальный заказ на нашем сервисе. Там эксперты помогают с учебой без посредников Разместите задание – сайт бесплатно отправит его исполнителя, и они предложат цены.
Там эксперты помогают с учебой без посредников Разместите задание – сайт бесплатно отправит его исполнителя, и они предложат цены.
1 000 +
Новых работ ежедневно
Работы выполняют эксперты в своём деле. Они ценят свою репутацию, поэтому результат выполненной работы гарантирован
107074
рейтинг
2642
работ сдано
1206
отзывов
99476
рейтинг
5209
работ сдано
2338
отзывов
72211
рейтинг
1839
работ сдано
1159
отзывов
62710
рейтинг
1046
работ сдано
598
отзывов
Тип работыВыберите тип работыКонтрольнаяРешение задачКурсоваяРефератОнлайн-помощьТест дистанционноЛабораторнаяЧертежЭссеОтветы на билетыПеревод с ин. языкаДокладСтатьяБизнес-планПодбор литературыШпаргалкаПоиск информацииРецензияДругое
Тата
СИБГУФК
Спасибо за отличную работу!)))) Преподаватель поздно проверил!)))) я очень довольна)
Владимир
МИИТ
Выполнялся реферат по корпоративному мошенничеству. Исполнитель справился намного быстрее,…
Исполнитель справился намного быстрее,…
Эльвира
ДВГУПС
очень ответственно подошел к работе! Надеюсь на дальнейшее сотрудничество
Спасибо за отличную работу!)))) Преподаватель поздно проверил!)))) я очень довольна)
Тата
СИБГУФК
Выполнялся реферат по корпоративному мошенничеству. Исполнитель справился намного быстрее, чем требовали сроки. Хорошая работа! Спасибо!
Владимир
МИИТ
очень ответственно подошел к работе! Надеюсь на дальнейшее сотрудничество
Эльвира
ДВГУПС
Ежедневно эксперты готовы работать над 1000 заданиями. Контролируйте процесс написания работы в режиме онлайн
только что
только что
только что
1 минуту назад
1 минуту назад
1 минуту назад
1 минуту назад
1 минуту назад
1 минуту назад
1 минуту назад
2 минуты назад
2 минуты назад
3 минуты назад
3 минуты назад
5 минут назад
6 минут назад
6 минут назад
6 минут назад
Закажи индивидуальную работу за 1 минуту!
Размещенные на сайт контрольные, курсовые и иные категории работ (далее — Работы) и их содержимое предназначены исключительно для ознакомления, без целей коммерческого использования.
 Все права в отношении Работ и их содержимого принадлежат их законным правообладателям. Любое их использование возможно лишь с согласия законных правообладателей. Администрация сайта не несет ответственности за возможный вред и/или убытки, возникшие в связи с использованием Работ и их содержимого.
Все права в отношении Работ и их содержимого принадлежат их законным правообладателям. Любое их использование возможно лишь с согласия законных правообладателей. Администрация сайта не несет ответственности за возможный вред и/или убытки, возникшие в связи с использованием Работ и их содержимого.Теплопроводность, теплопередача
Таблица теплопроводности газов
Проектирование и проектирование теплопередачи
На этой диаграмме показана зависимость теплопроводности газов от температуры.
Если не указано иное, значения относятся к давлению 100 кПа (1 бар) или к давлению насыщенного пара, если оно меньше 100 кПа.
Обозначение P = 0 указывает, что задано предельное значение низкого давления. В целом значения P = 0 и P = 100 кПа отличаются менее чем на 1%.
Единицы: мВт/м·К ( милливатт на метр-кельвин).
МФ | Имя | 100 К | 200 К | 300 К | 400 К | 500 К | 600 К |
— | Воздух | 9. | 18,4 | 26,2 | 33,3 | 39,7 | 45,7 |
Ar | Argon | 6.2 | 12,4 | 17,9 | 22,6 | 26,8 | 30,6 |
BF 3 | Бор трехфтористый | — | — | 19,0 | 24,6 | — | — |
H 2 | Водород (P = 0) | 68,6 | 131,7 | 186,9 | 230,4 | — | — |
F 6 S | Гексафторид серы (P = 0) | — | — | 13,0 | 20,6 | 27,5 | 33,8 |
Н 2 О | Вода | — | — | 18,7 | 27,1 | 35,7 | 47. |
H 2 S | Сероводород | — | — | 14,6 | 20,5 | 26,4 | 32,4 |
NH 3 | Аммиак | — | — | 24,4 | 37,4 | 51,6 | 66,8 |
He | Гелий (P = 0) | 75,5 | 119,3 | 156,7 | 190,6 | 222,3 | 252,4 8 |
Кр | Криптон (P = 0) | 3,3 | 6,4 | 9,5 | 12,3 | 14,8 | 17,1 |
НЕТ | Оксид азота | — | 17,8 | 25,9 | 33,1 | 39,6 | 46. |
N 2 | Азот | 9,8 | 18,7 | 26,0 | 32,3 | 38,3 | 44.0 |
N 2 O | Закись азота | — | 9,8 | 17,4 | 26,0 | 34.1 | 41,8 |
Ne | Неон (P = 0) | 22,3 | 37,6 | 49,8 | 60,3 | 69,9 | 78.7 |
O 2 | Кислород | 9,3 | 18,4 | 26,3 | 33,7 | 41,0 | 48. |
O 2 S | Диоксид серы | — | — | 9,6 | 14,3 | 20,0 | 25,6 |
Xe | Ксенон (P = 0) | 2,0 | 3,6 | 5,5 | 7,3 | 8,9 | 10.4 |
CCl 2 F 2 | Дихлордифторметан | — | — | 9,9 | 15,0 | 20,1 | 25,2 |
CF 4 | Тетрафторметан (P = 0) | — | — | 16,0 | 24. | 32,2 | 39,9 |
СО | Окись углерода (P = 0) | — | — | 25,0 | 32,3 | 39,2 | 45,7 |
CO 2 | Двуокись углерода | — | 9,6 | 16,8 | 25,1 | 33,5 | 41,6 |
CHCl 3 | Трихлорметан | — | — | 7,5 | 11.1 | 15,1 | — |
CH 4 | Метан | — | 22,5 | 34. | 49,1 | 66,5 | 84.1 |
CH 4 O | Метанол | — | — | — | 26,2 | 38,6 | 53.0 |
С 2 Н 2 | Ацетилен | — | — | 21,4 | 33,3 | 45,4 | 56.8 |
C 2 H 4 | Этилен | — | 11.1 | 20,5 | 34,6 | 49,9 | 68,6 |
С 2 Н 6 | Этан | — | 11,0 | 21,3 | 35,4 | 52,2 | 70,5 |
C 2 H 6 O | Этанол | — | — | 14,4 | 25,8 | 38,4 | 53. |
C 3 H 6 O | Ацетон | — | — | 11,5 | 20,2 | 30,6 | 42,7 |
С 3 Н 8 | Пропан | — | — | 18,0 | 30,6 | 45,5 | 61.9 |
C 4 H 10 | Бутан | — | — | 16,4 | 28,4 | 43,0 | 59.1 |
C 5 H 12 | Пентан | — | — | 14,4 | 24,9 | 37,8 | 52,7 |
С 6 Н 14 | Гексан | — | — | — | 23,4 | 35,4 | 48. |
Газы. Тепловые свойства газов
Свойства газов при атмосферном давлении
| Газ | Температура | Проводимость | Плотность | Удельная теплоемкость | Динамическая вязкость | Кинематическая вязкость | Температуропроводность |
| Гелий | -129,0 | 0,0928 | 0,3379 | 5,2 x 10 3 | 12,55 x 10 -6 | 37,11 x 10 -6 | 52,75 x 10 -6 |
| Гелий | -73,0 | 0,1177 | 0,2435 | 5,2 x 10 3 | 15,66 х 10 -6 | 64,38 x 10 -6 | 92,88 x 10 -6 |
| Гелий | -18,0 | 0,1357 | 0,1906 | 5,2 x 10 3 | 18,17 x 10 -6 | 95,5 x 10 -6 | 136,75 х 10 -6 |
| Гелий | 93,0 | 0,1691 | 0,1328 | 5,2 x 10 3 | 23,05 x 10 -6 | 173,6 x 10 -6 | 244,9 x 10 -6 |
| Гелий | 204,0 | 0,197 | 0,10204 | 5,2 x 10 3 | 27,5 x 10 -6 | 269,3 x 10 -6 | 371,6 x 10 -6 |
| Гелий | 316,0 | 0,225 | 0,08282 | 5,2 x 10 3 | 31,13 х 10 -6 | 375,8 x 10 -6 | 521,5 x 10 -6 |
| Гелий | 427,0 | 0,251 | 0,07032 | 5,2 x 10 3 | 34,75 x 10 -6 | 494,2 x 10 -6 | 666,1 х 10 -6 |
| Гелий | 527,0 | 0,275 | 0,06023 | 5,2 x 10 3 | 38,17 x 10 -6 | 634,1 x 10 -6 | 877,4 x 10 -6 |
| Водород | -123,0 | 0,0981 | 0,16371 | 12,602 x 10 3 | 5,595 x 10 -6 | 34,18 x 10 -6 | 47,5 x 10 -6 |
| Водород | -73,0 | 0,1282 | 0,1227 | 13,54 x 10 3 | 6,813 x 10 -6 | 55,53 x 10 -6 | 77,2 x 10 -6 |
| Водород | -23,0 | 0,1561 | 0,09819 | 14,059 x 10 3 | 7,919 x 10 -6 | 80,64 x 10 -6 | 113,0 x 10 -6 |
| Водород | 27,0 | 0,182 | 0,08185 | 14,314 x 10 3 | 8,963 x 10 -6 | 109,5 x 10 -6 | 155,4 x 10 -6 |
| Водород | 77,0 | 0,206 | 0,07016 | 14,436 x 10 3 | 9,954 x 10 -6 | 141,9 x 10 -6 | 203,1 x 10 -6 |
| Водород | 127,0 | 0,228 | 0,06135 | 14,491 х 10 3 | 10,864 x 10 -6 | 177,1 x 10 -6 | 256,8 x 10 -6 |
| Водород | 177,0 | 0,251 | 0,05462 | 14,499 x 10 3 | 11,779 x 10 -6 | 215,6 х 10 -6 | 316,4 x 10 -6 |
| Водород | 227,0 | 0,272 | 0,04918 | 14,507 x 10 3 | 12,636 x 10 -6 | 257,0 x 10 -6 | 381,7 x 10 -6 |
| Водород | 277,0 | 0,292 | 0,04469 | 14,532 x 10 3 | 13,475 x 10 -6 | 301,6 x 10 -6 | 451,6 x 10 -6 |
| Водород | 327,0 | 0,315 | 0,04085 | 14,537 x 10 3 | 14,285 x 10 -6 | 349,7 x 10 -6 | 530,6 x 10 -6 |
| Водород | 427,0 | 0,351 | 0,03492 | 14,574 x 10 3 | 15,89 x 10 -6 | 455,1 x 10 -6 | 690,3 x 10 -6 |
| Водород | 527,0 | 0,384 | 0,0306 | 14,675 x 10 3 | 17,4 x 10 -6 | 569,0 x 10 -6 | 856,3 x 10 -6 |
| Водород | 527,0 | 0,412 | 0,02723 | 14,821 x 10 3 | 18,78 x 10 -6 | 690,0 x 10 -6 | 0,0010217 |
| Кислород | -123,0 | 0,01367 | 2,619 | 917,8 | 11,49 x 10 -6 | 4,387 x 10 -6 | 5,688 x 10 -6 |
| Кислород | -73,0 | 0,01824 | 1,9559 | 913. | 14,85 x 10 -6 | 7,593 x 10 -6 | 10,214 x 10 -6 |
| Кислород | -23,0 | 0,02259 | 1,5618 | 915,7 | 17,87 x 10 -6 | 11,45 x 10 -6 | 15,794 x 10 -6 |
| Кислород | 27,0 | 0,02676 | 1.3007 | 920,3 | 20,63 x 10 -6 | 15,86 x 10 -6 | 22,353 x 10 -6 |
| Кислород | 77,0 | 0,0307 | 1.1133 | 929.1 | 23,16 х 10 -6 | 20,8 x 10 -6 | 29,68 x 10 -6 |
| Кислород | 127,0 | 0,03461 | 0,9755 | 942,0 | 25,54 x 10 -6 | 26,18 x 10 -6 | 37,68 х 10 -6 |
| Кислород | 177,0 | 0,03828 | 0,8682 | 956,7 | 27,77 x 10 -6 | 31,99 x 10 -6 | 46,09 x 10 -6 |
| Кислород | 227,0 | 0,04173 | 0,7801 | 972,2 | 29,91 x 10 -6 | 38,34 x 10 -6 | 55,02 x 10 -6 |
| Кислород | 277,0 | 0,04517 | 0,7096 | 988. | 31,97 x 10 -6 | 45,05 х 10 -6 | 64,1 x 10 -6 |
| Азот | -73,0 | 0,01824 | 1.7108 | 1,0429 x 10 3 | 12,947 x 10 -6 | 7,568 x 10 -6 | 10,224 x 10 -6 |
| Азот | 27,0 | 0,0262 | 1.1421 | 1,0408 x 10 3 | 17,84 x 10 -6 | 15,63 x 10 -6 | 22,044 x 10 -6 |
| Азот | 127,0 | 0,03335 | 0,8538 | 1,0459 x 10 3 | 21,98 x 10 -6 | 25,74 x 10 -6 | 37,34 x 10 -6 |
| Азот | 227,0 | 0,03984 | 0,6824 | 1,0555 x 10 3 | 25,7 х 10 -6 | 37,66 x 10 -6 | 55,3 x 10 -6 |
| Азот | 327,0 | 0,0458 | 0,5624 | 1,0756 x 10 3 | 29,11 x 10 -6 | 51,19 x 10 -6 | 74,86 x 10 -6 |
| Азот | 427,0 | 0,05123 | 0,4934 | 1,0969 x 10 3 | 32,13 x 10 -6 | 65,13 x 10 -6 | 94,66 x 10 -6 |
| Азот | 527,0 | 0,05609 | 0,4277 | 1,1225 x 10 3 | 34,84 x 10 -6 | 81,46 x 10 -6 | 116,85 x 10 -6 |
| Азот | 627,0 | 0,0607 | 0,3796 | 1,1464 x 10 3 | 37,49 x 10 -6 | 91,06 x 10 -6 | 139,46 x 10 -6 |
| Азот | 727,0 | 0,06475 | 0,3412 | 1,1677 x 10 3 | 40,0 x 10 -6 | 117,2 x 10 -6 | 162,5 х 10 -6 |
| Азот | 827,0 | 0,0685 | 0,3108 | 1,1857 x 10 3 | 42,28 x 10 -6 | 136,0 x 10 -6 | 185,91 x 10 -6 |
| Азот | 927,0 | 0,07184 | 0,2851 | 1,2037 x 10 3 | 44,5 x 10 -6 | 156,1 x 10 -6 | 209,32 x 10 -6 |
| Углекислый газ | -53,0 | 0,010805 | 2,4733 | 783,0 | 11,105 x 10 -6 | 4,49 x 10 -6 | 5,92 x 10 -6 |
| Углекислый газ | -23,0 | 0,012884 | 2. | 804.0 | 12,59 x 10 -6 | 5,813 x 10 -6 | 7,401 x 10 -6 |
| Углекислый газ | 27,0 | 0,016572 | 1,7973 | 871,0 | 14,958 x 10 -6 | 8,321 x 10 -6 | 10,588 x 10 -6 |
| Углекислый газ | 77,0 | 0,02047 | 1,5362 | 900,0 | 17,205 x 10 -6 | 11,19 x 10 -6 | 14,808 x 10 -6 |
| Углекислый газ | 127,0 | 0,02461 | 1.3424 | 942,0 | 19.32 x 10 -6 | 14,39 x 10 -6 | 19,463 x 10 -6 |
| Углекислый газ | 177,0 | 0,02897 | 1. | 980,0 | 21,34 x 10 -6 | 17,9 x 10 -6 | 24,813 х 10 -6 |
| Углекислый газ | 227,0 | 0,03352 | 1.0732 | 1,013 x 10 3 | 23,26 x 10 -6 | 21,67 x 10 -6 | 30,84 x 10 -6 |
| Углекислый газ | 277,0 | 0,03821 | 0,9739 | 1,047 x 10 3 | 25,08 x 10 -6 | 25,74 x 10 -6 | 37,5 x 10 -6 |
| Углекислый газ | 327,0 | 0,04311 | 0,8938 | 1,076 x 10 3 | 26,83 x 10 -6 | 30,02 x 10 -6 | 44,83 x 10 -6 |
| Аммиак, NH 3 | 0,0 | 0,022 | 0,7929 | 2,177 x 10 3 | 9,353 x 10 -6 | 11,8 x 10 -6 | 13,08 x 10 -6 |
| Аммиак, NH 3 | 50,0 | 0,027 | 0,6487 | 2,177 x 10 3 | 11,035 x 10 -6 | 17,0 x 10 -6 | 19,2 x 10 -6 |
| Аммиак, NH 3 | 100,0 | 0,0327 | 0,559 | 2,236 x 10 3 | 12,886 x 10 -6 | 23,0 x 10 -6 | 26,19 x 10 -6 |
| Аммиак, NH 3 | 150,0 | 0,0391 | 0,4934 | 2,315 x 10 3 | 14,672 x 10 -6 | 29,7 x 10 -6 | 34,32 x 10 -6 |
| Аммиак, NH 3 | 200,0 | 0,0467 | 0,4405 | 2,395 x 10 3 | 16,49 x 10 -6 | 37,4 х 10 -6 | 44,21 x 10 -6 |
| Водяной пар | 107,0 | 0,0246 | 0,5863 | 2,06 x 10 3 | 12,71 x 10 -6 | 21,6 x 10 -6 | 20,36 x 10 -6 |
| Водяной пар | 127,0 | 0,0261 | 0,5542 | 2,014 x 10 3 | 13,44 x 10 -6 | 24,2 x 10 -6 | 23,38 x 10 -6 |
| Водяной пар | 177,0 | 0,0299 | 0,4942 | 1,98 x 10 3 | 15,25 x 10 -6 | 31,1 x 10 -6 | 30,7 x 10 -6 |
| Водяной пар | 227,0 | 0,0339 | 0,4405 | 1,985 x 10 3 | 17,04 x 10 -6 | 38,6 x 10 -6 | 38,7 x 10 -6 |
| Водяной пар | 277,0 | 0,0379 | 0,4005 | 1,997 x 10 3 | 18,84 x 10 -6 | 47,0 x 10 -6 | 47,5 x 10 -6 |
| Водяной пар | 327,0 | 0,0422 | 0,3652 | 2,026 x 10 3 | 20,67 x 10 -6 | 56,6 x 10 -6 | 57,3 x 10 -6 |
| Водяной пар | 377,0 | 0,0464 | 0,338 | 2,056 x 10 3 | 22,47 x 10 -6 | 66,4 x 10 -6 | 66,6 x 10 -6 |
| Водяной пар | 427,0 | 0,0505 | 0,314 | 2,085 x 10 3 | 24,26 х 10 -6 | 77,2 x 10 -6 | 77,2 x 10 -6 |
| Водяной пар | 477,0 | 0,0549 | 0,2931 | 2,119 x 10 3 | 26,04 x 10 -6 | 88,8 x 10 -6 | 88,3 х 10 -6 |
| Водяной пар | 527,0 | 0,0592 | 0,2739 | 2,152 x 10 3 | 27,86 x 10 -6 | 102,0 x 10 -6 | 100,1 x 10 -6 |
| Водяной пар | 577,0 | 0,0637 | 0,2579 | 2,186 x 10 3 | 29,69 x 10 -6 | 115,2 x 10 -6 | 113,0 x 10 -6 |
Ссылки:
- Кадоя К.
 , Мацунага Н. и Нагасима А. Вязкость и теплопроводность сухого воздуха в газовой фазе // J. Phys. хим. Ссылка Данные, 14, 947, 1985.
, Мацунага Н. и Нагасима А. Вязкость и теплопроводность сухого воздуха в газовой фазе // J. Phys. хим. Ссылка Данные, 14, 947, 1985. - . Янглав, Б. А. и Хэнли, Х. Дж. М., Коэффициенты вязкости и теплопроводности газообразного и жидкого аргона, J. Phys. хим. Ссылка Data, 15, 1323, 1986.
- Holland, P.M., Eaton, B.E., and Hanley, H.J.M., Корреляция данных по вязкости и теплопроводности газообразного и жидкого этилена, J. Phys. хим. Ссылка Данные, 12, 917, 1983.
Теплопроводность газов — tech-science
Теплопроводность идеальных газов не зависит от давления для не слишком сильно разбавленных газов. Это уже не относится к газам с низким давлением.
- 1 Введение
- 2 Независимость теплопроводности от давления при высоких давлениях (плотные газы)
- 3 Зависимость теплопроводности от давления при низких давлениях (разбавленные газы)
- 4 Число Кнудсена
Введение
5 В статье Теплопроводность твердых тел и идеальных газов была выведена следующая формула для оценки теплопроводности λ идеальных газов:
\begin{align}
\label{l}
& \boxed{\lambda = \frac{1}{3} \cdot c_v \cdot \rho \cdot v \cdot l} \\[5px]
\end{align}
В этой формуле c v обозначает удельную теплоемкость при постоянном объеме, ϱ плотность газа, v среднюю скорость молекул газа и l длину свободного пробега. Эта формула будет объяснена более подробно в этой статье, и будут обсуждаться полученные выводы для газов.
Эта формула будет объяснена более подробно в этой статье, и будут обсуждаться полученные выводы для газов.
Используя формулу, можно было предположить, что теплопроводность зависит от давления, ведь чем выше давление, тем выше плотность газа. Этот аргумент также можно ясно понять с помощью корпускулярной модели материи, потому что чем больше частиц, тем больше энергии частицы могут переносить в сумме. Обратите внимание, что согласно кинетической теории газов каждая молекула газа несет энергию ½⋅k B ⋅T на степень свободы (с k B в качестве постоянная Больцмана ).
Однако в той же мере, в какой плотность увеличивается с увеличением давления, длина свободного пробега уменьшается! Фактически, теплопроводность идеальных газов поэтому не зависит от давления или плотности частиц (для ограничения этого утверждения позже)!
Теплопроводность газов не зависит от давления при не слишком низком давлении!
Рисунок: Длина свободного пробега и средняя скорость молекул в газеНезависимость теплопроводности от давления при высоких давлениях (плотные газы)
Независимость теплопроводности от давления также можно показать математически. Для этого плотность ϱ в уравнении (\ref{l}) сначала выражается через частное массы газа m газа и объема газа V газа . Тогда масса газа может быть выражена количеством вещества n газа ( химическое количество ) и молярной массой M газа газа.
Для этого плотность ϱ в уравнении (\ref{l}) сначала выражается через частное массы газа m газа и объема газа V газа . Тогда масса газа может быть выражена количеством вещества n газа ( химическое количество ) и молярной массой M газа газа.
\begin{align}
\lambda &= \frac{1}{3} \cdot c_v \cdot \frac{m_{gas}}{V_{gas}} \cdot v \cdot l \\[5px]
&= \frac{1}{3} \cdot c_v \cdot \frac{n_{gas} \cdot M_{gas}}{V} \cdot v \cdot l \\[5px]
\end{align}
Произведение удельной теплоемкости на молярную массу равно так называемой молярной теплоемкости C m,v , при этом молярная теплоемкость зависит только от степеней свободы f и молярной газовой постоянной R m (C м, v = f/2⋅R м ). Кроме того, количество вещества n газа может быть выражено отношением числа частиц N и константы Авогадро N A (n газ = N/N A ):
\begin{align}
\lambda &= \frac{1}{3} \cdot \underbrace{c_v \cdot M_{gas}} _{C_{m,v}} \cdot \frac{n_{gas}}{V} \cdot v \cdot l \\[5px]
& = \frac{1}{3} \cdot \underbrace {C_ {m,v}}_{=\frac{f}{2}R_m} \cdot \frac{N}{N_A \cdot V} \cdot v \cdot l \\[5px]
& = \frac{1 }{3} \cdot \frac{f}{2} R_{m} \cdot \frac{1}{N_A} \cdot \frac{N}{V} \cdot v \cdot l \\[5px]
& = \frac{f}{6} \frac{R_m}{N_A} \cdot \frac{N}{V} \cdot v \cdot l \\[5px]
\end{align}
Отношение числа частиц к объему газа соответствует плотности частиц n, а частное молярной газовой постоянной и постоянной Авогадро соответствует постоянной Больцмана k B (об этом соотношении см. статью Internal Energy & Теплоемкость):
статью Internal Energy & Теплоемкость):
\begin{align}
\lambda & = \frac{f}{6} \underbrace{\frac{R_m}{N_A}}_{k_B} \cdot \underbrace{\frac{N} {V}}_{n} \cdot v \cdot l \\[5px]
\label{ll}
& = \frac{f}{6} k_B \cdot n \cdot v \cdot l \\[5px ]
\end{align}
Теперь нам нужны только зависимости средней скорости и длины свободного пробега. Согласно распределению Максвелла-Больцмана средняя скорость v молекул газа зависит от температуры газа T и массы молекулы m (m обозначает массу отдельной частицы газа, а не всей массы газа!)
\begin{align}
& \boxed{v = \sqrt{\frac{8 k_B T}{\pi m}}} \\[5px]
\end{align}
молекул зависит не только от плотности частиц n, но и от диаметра частиц d и определяется следующей формулой: 93 м }}} \\[5px]
\end{align}
Теперь эта формула ясно показывает, что теплопроводность идеальных газов не зависит от плотности частиц и, следовательно, не зависит от давления. Это также показывает, что газы с относительно большими молекулами имеют более низкую теплопроводность, чем газы с меньшими молекулами (это связано с уменьшением длины свободного пробега в результате большего диаметра столкновения d). Кроме того, теплопроводность газов с легкими частицами выше, чем у газов с более тяжелыми частицами. Кроме того, теплопроводность зависит от температуры. Теплопроводность увеличивается с повышением температуры!
Кроме того, теплопроводность газов с легкими частицами выше, чем у газов с более тяжелыми частицами. Кроме того, теплопроводность зависит от температуры. Теплопроводность увеличивается с повышением температуры!
Теплопроводность газов тем больше, чем меньше и легче молекулы и чем выше температура!
Зависимость теплопроводности от давления для низких давлений (разбавленные газы)
Если давление не влияет на теплопроводность газов, то зачем использовать вакуум для теплоизоляции?
Тот факт, что теплопроводность не зависит от давления, верен только до тех пор, пока длина свободного пробега много меньше размеров объема, в котором содержится газ. Если давление (плотность частиц) в сосуде все больше и больше снижается, частицы сталкиваются уже не друг с другом, а со стенками сосуда. Таким образом, при очень низких давлениях длина свободного пробега определяется размером контейнера, а не свободным пробегом между столкновениями двух частиц.
Это также применимо, если давление не уменьшается, а уменьшается размер емкости. Это актуально, например, для изоляционных материалов, в которых газы заключены в мелкие поры. Такие ситуации также могут возникнуть с тонкими слоями фольги или небольшими зазорами, если между ними находится газ.
Это актуально, например, для изоляционных материалов, в которых газы заключены в мелкие поры. Такие ситуации также могут возникнуть с тонкими слоями фольги или небольшими зазорами, если между ними находится газ.
Средняя длина свободного пробега в этих случаях примерно соответствует размеру δ объема (например, диаметру пор или зазору) и, следовательно, является постоянной величиной. В этом случае длина свободного пробега больше не зависит от плотности частиц: l≈δ=константа. При постоянной длине свободного пробега уравнение (\ref{ll}) указывает на уменьшение теплопроводности при уменьшении плотности частиц (или давления)!
\begin{align}
\label{a}
&\lambda = \frac{f}{6} k_B \cdot n \cdot v \cdot \delta \\[5px]
\end{align}
В разбавленных газах или при малых объемах газа теплопроводность зависит от давления!
В так называемых манометрах Пирани это соотношение используется для получения выводов о давлении в условиях высокого вакуума на основе теплопроводности.
Номер Кнудсена
Как уже было указано, характерная длина δ пор или расстояние между фольгами в изоляционных материалах часто намного меньше, чем длина свободного пробега l содержащихся в них газов. В этом случае газ уже не может быть описан как сплошная среда, так что уравнение (\ref{a}) уже не может применяться в таком виде (однако качественная формулировка этого уравнения не теряет своей силы).
Характеристическая длина относится к размеру/размеру системы!
В этом контексте так называемая Число Кнудсена указывает, можно ли по-прежнему рассматривать газ как континуум или следует применять кинетику газовой теории. Безразмерное число Кнудсена Kn описывает отношение длины свободного пробега l к характерной длине δ объема газа:
\begin{align}
&\boxed{Kn := \frac{l}{\delta}} \ \[5px]
\end{align}
Для значений намного меньших 1 по-прежнему применяется механика сплошной среды, а для значений намного больших 1 используется описание с помощью законов кинетической теории газов. 92 \cdot p \cdot \delta}} \\[5px]
92 \cdot p \cdot \delta}} \\[5px]
\end{align}
В случае изоляционных материалов, где число Кнудсена часто намного меньше 1, теплопроводность заключенного газа может быть определяется по следующей формуле [см. М.Г. Каганер: « Теплоизоляция в криогенной технике », 1969]:
\begin{align}
\label{lam}
&\boxed{\lambda = \frac{\lambda_0}{1+2\beta \cdot Kn}} \\[5px]
\end{align}
В этой формуле λ 0 обозначает теплопроводность при стандартных условиях (1 атм, 0°C), а β является весовым коэффициентом, который далее здесь обсуждаться не будет. Даже если использование уравнения (\ref{lam}) требует, чтобы число Кнудсена было намного меньше 1, оно все равно должно быть как можно больше, особенно для изоляционных материалов! Это приводит к низкой теплопроводности.
При низкой теплопроводности число Кнудсена должно быть максимально высоким!
Воздух — теплофизические свойства
Thermophysical properties of air:
- Boiling temperature (at 1 bara): 78.
 8 K = -194.4 °C = -317.8 °F
8 K = -194.4 °C = -317.8 °F - Bulk modulus elasticity: 1.01325 x 10 5 Pa or N/m 2
- Температура конденсации (при 1 баре): 81,8 К = -191,4 ° C = -312,5 ° F
- Критическая температура: 132,63 К = -140,52 ° C = -220,94 ° F
- Критическое давление: 37,363 Атм = 37,858 бар = 3,7858 МПа (мн/м 2 ) = 549,08 фунтов на квадратный дюйм (= LB F /в 2 )
- Краткость: 101272 2 )
- : 101272 2 ). кг/м 3 = 0,5871 СЛУГ/ФТ 3 = 18,89 фунта м /фут 3
- (при 0 ° C и 1 бара): 1.276 кг/м 9127 3 3 91 3 9 91 3 9 91 2 3 9 912 3 9 912 3 9 912 3 9 912 3 9 912 3 9 912 3 9 912 3 9 912 3 9 912 3 9 912 3 9 912 3 9 913 3 9 913 3 9 913 3 9 913 3 9 913 3 9 913 3 9 913 3 9 913 3 9 913 3 9 913 3 9 913 3 = 0.00248 slug/ft 3 = 0.0797 lb/ft 3
- Density (at 60°F and 1 atm): 1.
 208 kg/m 3 = 0.00234 slug/ft 3 = 0.0754 lb/ft 3
208 kg/m 3 = 0.00234 slug/ft 3 = 0.0754 lb/ft 3 - Энтальпия (тепло) воздуха при 0 ° C и 1 Bara: 11,57 кДж/моль = 399,4 кДж/кг = 171,7 BTU (IT)/LB
- Энрепи кДж/моль K = 3,796 кДж/кг K = 0,9067 БТЕ(ИТ)/фунт °F
- Плотность жидкости при температуре кипения и 1 бар: 875,50 кг/м 3 = 54,656 фунт/фут 3
- Молярная масса: 28,9647 г/моль
- Специфическая теплоемкость (C P ) воздух при 0 ° C и 1 BARA: 1,006 KJ/KGK = 0,24028). /(фунт м °F) или ккал/(кг·К)
- Удельная теплоемкость (C v ) воздуха при 0°C и 1 бар абс.: 0,7171 кДж/кгK = 0,17128 БТЕ(ИТ)/(фунт м °F) или ккал/(кг·К)
- Теплопроводность при 0°C и 1 бар абс.: 24,35 мВт/(м·К) = 0,02094 ккал(ИТ)/(ч м К) = 0,01407 БТЕ(ИТ)/(ч фут °F)
- Коэффициент теплового расширения при 0°C и 1 бар абс.: 0,00369 1/K = 0,00205 1/°F
- Тройная точка давление: 0,05196 атм = 0,05265 бар = 5265 PA = 0,7636 PSI (= LB F /в 2 )
- ТЕМПЕРАТИЦА: 59,75 K = -213,40 ° C = -35913.
 , динамический, при 0°C и 1 бар абс.: 17,22 мкПа·с = 0,01722 сП = 0,3596×10 -6 (LB F S) /FT 2 = 11,57×10 -6 LB M /(FT S)
, динамический, при 0°C и 1 бар абс.: 17,22 мкПа·с = 0,01722 сП = 0,3596×10 -6 (LB F S) /FT 2 = 11,57×10 -6 LB M /(FT S) - ВИЗКОСТЬ, KINEMATIC, AT AT 0 ° C и
- ВИЗКИНА, KINEMATIC, AT AT 0 ° C и
- . 2 /с = 13,49 сСт = 0,0001452 фута 2 /с
Следуйте приведенным ниже ссылкам, чтобы получить значения для перечисленных свойств воздуха при изменении давления и температуры плотности при изменении давления 339106 : См. Воздух представляет собой смесь газов при стандартных условиях. Однако при низкой температуре и высоком давлении газовая смесь становится жидкостью. Фазовая диаграмма воздуха показывает фазовое поведение при изменении температуры и давления. Кривая между тройной точкой и критической точкой показывает температуру кипения воздуха при изменении давления. В критической точке состояние не изменяется при увеличении давления или при добавлении тепла. Тройная точка вещества — это температура и давление, при которых три фазы (газ, жидкость и твердое тело) этого вещества сосуществуют в термодинамическом равновесии. Скачать и распечатать диаграмму зависимости плотности воздуха от температуры Скачать и распечатать диаграмму зависимости плотности воздуха от температуры Пример — масса воздуха при температуре 100 o C Из приведенной выше таблицы плотность воздуха равна 2,39912 0,39962 кг/м. 3 в 100 или C . Массу 10 м 3 воздуха можно рассчитать как м = V ρ = (10 м 3 ) (0,946 кг/м 3 )53 = 9,46 кг , где M = масса (кг) V = объем (M 3 ) 9397 также дополнительную информацию об атмосферном давлении, а также STP — Стандартная температура и давление и NTP — Нормальная температура и давление,
также дополнительную информацию об атмосферном давлении, а также STP — Стандартная температура и давление и NTP — Нормальная температура и давление,
, а также Теплофизические свойства : Ацетон, Ацетилен, Аммиак, Аргон, Бензол, Бутан, Углекислый газ, Угарный газ, Этан, Этанол, Этилен, Гелий, Водород, Сероводород, Метан, Метанол, Азот, Кислород, Пентан , Пропан, Толуол, Вода и тяжелая вода, D 2 O.
Пример — масса воздуха при температуре 20 O C
Из таблицы выше — плотность воздуха 1,205 кг/м 3 в 20 O . Масса 10 м 3 Воздух можно рассчитать как
Масса 10 м 3 Воздух можно рассчитать как
M = (10 м 3 ) (1,205 кг/м 3 )
= 12,05 кг
Пример — Поживание
Воздушный шар объемом 10 м 3 нагревается до 100 o C . Температура окружающего воздуха 20 o С. Изменение силы тяжести (веса) объема воздуха есть потенциальная подъемная сила воздушного шара. Подъемную силу можно рассчитать как
F L = DM A G
= V D ρ A G
g . ) — (0,946 кг/м 3 )] (9,81 м/с 2 )= 25,4 N
, где = 25,4 N
, где = 25,4
, где =
. в силе тяжести (вес) (Н)
A G = ускорение гравитации (9,81 м/с 2 )
DM = V D ρ = изменение Mass in The Mass in the Mass in the Mass in the Mass in the Mass in the Mass in the Mass in the Mass in the Mass in the Mass in the Mass in the Mass in the Mass in the Mass in the Mass in the Mass in the Mass in the Mass in the Mass. = изменение плотности из-за разницы температур (кг/м 3 )
= изменение плотности из-за разницы температур (кг/м 3 )
Твердые вещества, жидкости и газы. Теплопроводность
Теплопроводность — это свойство материала, которое описывает способность проводить тепло. Теплопроводность можно определить как
«количество тепла, переданное через единицу толщины материала — в направлении, нормальном к поверхности единицы площади — из-за единичного градиента температуры в стационарных условиях»
Единицами теплопроводности являются [Вт/( м·К)] в системе СИ и [БТЕ/(час·фут·°F)] в имперской системе.
См. также изменения теплопроводности в зависимости от температуры и давления , для: воздуха, аммиака, углекислого газа и воды
Теплопроводность обычных материалов и продуктов:
| Thermal Conductivity — k — W/(m K) | |||||
|---|---|---|---|---|---|
| Material/Substance | Temperature | ||||
| 25 o C ( 77 o F) | 125 o C (257 o F) | 225 o C (437 o F) | |||
| Acetals | 0. 23 23 | ||||
| Acetone | 0.16 | ||||
| Acetylene (gas) | 0.018 | ||||
| Acrylic | 0.2 | ||||
| Air, атмосфера (газ) | 0,0262 | 0,0333 | 0,0398 | ||
| Воздух, высота над уровнем моря 10000 м | 0,020 | 7 | |||
| Agate | 10.9 | ||||
| Alcohol | 0.17 | ||||
| Alumina | 36 | 26 | |||
| Aluminum | |||||
| Aluminum Brass | 121 | ||||
| Оксид алюминия | 30 | ||||
| Аммиак (газ) | 0,0249 | 0,0369 | 0.0528 | ||
| Antimony | 18.5 | ||||
Apple (85. 6% moisture) 6% moisture) | 0.39 | ||||
| Argon (gas) | 0.016 | ||||
| Asbestos-cement board 1) | 0,744 | ||||
| Листы асбоцементные 1) | 0,166 | 5 | 2.07 | ||
| Asbestos, loosely packed 1) | 0.15 | ||||
| Asbestos mill board 1) | 0.14 | ||||
| Asphalt | 0,75 | ||||
| BASA Wood | 0,048 | ||||
| Битумен | 0,17 | 0,17 | 055 | Bitumen/felt layers | 0.5 |
| Beef, lean (78.9 % moisture) | 0.43 — 0.48 | ||||
| Benzene | 0. 16 16 | ||||
| Beryllium | |||||
| Bismuth | 8.1 | ||||
| Битум | 0,17 | ||||
| Бластовый газ (газ) | 0,02 | ||||
| .0025 | |||||
| Boiler scale | 1.2 — 3.5 | ||||
| Boron | 25 | ||||
| Brass | |||||
| Breeze block | 0.10 — 0.20 | ||||
| Кирпич плотный | 1,31 | ||||
| Кирпич огнеупорный | 0,47 | ||||
| Кирпич теплоизоляционный | 0.15 | ||||
| Brickwork, common (Building Brick) | 0.6 -1.0 | ||||
| Brickwork, dense | 1.6 | ||||
| Bromine (gas) | 0. 004 004 | ||||
| Бронза | |||||
| Руда бурая железная | 0,58 | ||||
| Масло сливочное (влажность 15% 5 9000)0025 | |||||
| Cadmium | |||||
| Calcium silicate | 0.05 | ||||
| Carbon | 1.7 | ||||
| Carbon dioxide (gas) | 0.0146 | ||||
| Окись углерода | 0,0232 | ||||
| Чугун | |||||
| Целлюлоза, хлопок, древесная масса и регенерированная | 0.23 | ||||
Cellulose acetate, molded, sheet | 0.17 — 0.33 | ||||
| Cellulose nitrate, celluloid | 0.12 — 0.21 | ||||
| Cement, Portland | 0. 29 29 | ||||
| Цемент, раствор | 1,73 | ||||
| Керамические материалы | |||||
| Chalk | 0.09 | ||||
| Charcoal | 0.084 | ||||
| Chlorinated poly-ether | 0.13 | ||||
| Chlorine (gas) | 0.0081 | ||||
| Chrome Никель Сталь | 16.3 | ||||
| Хром | |||||
| Оксид хрома | 0.42 | ||||
| Clay, dry to moist | 0.15 — 1.8 | ||||
| Clay, saturated | 0.6 — 2.5 | ||||
| Coal | 0.2 | ||||
| Кобальт | |||||
| Треска (влажность 83 %) | 0,54 | ||||
| Concrete, lightweight | 0. 1 — 0.3 1 — 0.3 | ||||
| Concrete, medium | 0.4 — 0.7 | ||||
| Concrete, dense | 1.0 — 1.8 | ||||
| Concrete, камень | 1.7 | ||||
| константан | 23.3 | ||||
| Corian (ceramic filled) | 1.06 | ||||
| Cork board | 0.043 | ||||
| Cork, re-granulated | 0.044 | ||||
| Cork | 0.07 | ||||
| Хлопок | 0,04 | ||||
| Вата | 0,029 | ||||
| 025 | |||||
| Cotton Wool insulation | 0.029 | ||||
| Cupronickel 30% | 30 | ||||
| Diamond | 1000 | ||||
| Diatomaceous earth (Sil-o-cel) | 0,06 | ||||
| Диатомит | 0,12 | ||||
| Дюралий | 5 4 77Earth, dry | 1. 5 5 | |||
| Ebonite | 0.17 | ||||
| Emery | 11.6 | ||||
| Engine Oil | 0.15 | ||||
| Ethane (gas ) | 0,018 | ||||
| Эфир | 0,14 | ||||
| Этилен (газ) 2 0 59 | 5 | 47||||
| Epoxy | 0.35 | ||||
| Ethylene glycol | 0.25 | ||||
| Feathers | 0.034 | ||||
| Felt insulation | 0.04 | ||||
| Fiberglass | 0,04 | ||||
| Изоляционная плита из волокна | 0,048 | ||||
| ДВП из волокна | 0.2 | ||||
| Fire-clay brick 500 o C | 1. 4 4 | ||||
| Fluorine (gas) | 0.0254 | ||||
| Foam glass | 0.045 | ||||
| Дихлордифторметан R-12 (газ) | 0,007 | ||||
| Дихлордифторметан R-12 (жидкий) | 0,009|||||
| Gasoline | 0.15 | ||||
| Glass | 1.05 | ||||
| Glass, Pearls, dry | 0.18 | ||||
| Glass, Pearls, saturated | 0.76 | ||||
| Стекло, окно | 0,96 | ||||
| Стекло, вата Изоляция | 0,04 405027 | ||||
| Glycerol | 0.28 | ||||
| Gold | |||||
| Granite | 1.7 — 4.0 | ||||
| Graphite | 168 | ||||
| Gravel | 0. 7 7 | ||||
| Земля или почва, очень влажная зона | 1,4 | ||||
| Земля или почва, влажная зона | 1.0 | ||||
| Ground or soil, dry area | 0.5 | ||||
| Ground or soil, very dry area | 0.33 | ||||
| Gypsum board | 0.17 | ||||
| Войлок | 0,05 | ||||
| Оргалит высокой плотности | 0,15 | 550025 | 0.16 | ||
| Hastelloy C | 12 | ||||
| Helium (gas) | 0.142 | ||||
| Honey (12.6% moisture content) | 0.5 | ||||
| Hydrochloric кислота (газ) | 0,013 | ||||
| Водород (газ) | 0,168 | ||||
| Сероводород | (газ) 0. 013 013 | ||||
| Ice (0 o C, 32 o F) | 2.18 | ||||
| Inconel | 15 | ||||
| Ingot iron | 47 — 58 | ||||
| Insulation materials | 0.035 — 0.16 | ||||
| Iodine | 0.44 | ||||
| Iridium | 147 | ||||
| Iron | |||||
| Iron-oxide | 0.58 | ||||
| Kapok insulation | 0.034 | ||||
| Kerosene | 0.15 | ||||
| Krypton (gas) | 0,0088 | ||||
| Свинец | |||||
| Кожа, сухая | 0,14 | 7 9 44547 | |||
| Limestone | 1.26 — 1.33 | ||||
| Lithium | |||||
| Magnesia insulation (85%) | 0. 07 07 | ||||
| Magnesite | 4.15 | ||||
| Магний | |||||
| Магниевый сплав | 70 — 145 | ||||
| Мрамор | 2.08 — 2.94 | ||||
| Mercury, liquid | |||||
| Methane (gas) | 0.030 | ||||
| Methanol | 0.21 | ||||
| Mica | 0.71 | ||||
| Молоко | 0,53 | ||||
| Изоляционные материалы из минеральной ваты, шерстяные одеяла .. | 0,04 | ||||
| Molybdenum | |||||
| Monel | |||||
| Neon (gas) | 0.046 | ||||
| Neoprene | 0.05 | ||||
| Nickel | |||||
| Оксид азота (газ) | 0,0238 | ||||
| Азот (газ) | 0,024 | ||||
| Nitrous oxide (gas) | 0. 0151 0151 | ||||
| Nylon 6, Nylon 6/6 | 0.25 | ||||
| Oil, machine lubricating SAE 50 | 0.15 | ||||
| Olive Масло | 0,17 | ||||
| Кислород (газ) | 0,024 | ||||
| Палладий | 70,9 | 444444744444444444444444444444444444447 | 70,9 | 70,9 | 7 | 444744444447 | 70,9 | 9007030 Paper | 0.05 |
| Paraffin Wax | 0.25 | ||||
| Peat | 0.08 | ||||
| Perlite, atmospheric pressure | 0.031 | ||||
| Perlite, vacuum | 0,00137 | ||||
| Фенольные литые смолы | 0,15 | ||||
| Phenol-formaldehyde moulding compounds | 0. 13 — 0.25 13 — 0.25 | ||||
| Phosphorbronze | 110 | ||||
| Pinchbeck | 159 | ||||
| Pitch | 0.13 | ||||
| Pit coal | 0,24 | ||||
| Штукатурка светлая | 0,2 | ||||
| Штукатурка, металлическая рейка | 0.47 | ||||
| Plaster, sand | 0.71 | ||||
| Plaster, wood lath | 0.28 | ||||
| Plasticine | 0.65 — 0.8 | ||||
| Plastics, foamed ( изоляционные материалы) | 0,03 | ||||
| Платина | |||||
| Plywood | 0.13 | ||||
| Polycarbonate | 0. 19 19 | ||||
| Polyester | 0.05 | ||||
| Polyethylene low density, PEL | 0.33 | ||||
| Polyethylene высокая плотность, PEH | 0,42 — 0,51 | ||||
| Натуральный полиизопреновый каучук | 0,13 | ||||
| Polyisoprene hard rubber | 0.16 | ||||
| Polymethylmethacrylate | 0.17 — 0.25 | ||||
| Polypropylene, PP | 0.1 — 0.22 | ||||
| Polystyrene, expanded | 0,03 | ||||
| Полистирол | 0,043 | ||||
| Пенополиуретан | 0.03 | ||||
| Porcelain | 1.5 | ||||
| Potassium | 1 | ||||
| Potato, raw flesh | 0. 55 55 | ||||
| Propane (gas) | 0.015 | ||||
| Политетрафторэтилен (ПТФЭ) | 0,25 | ||||
| Поливинилхлорид, ПВХ | 0,19 | ||||
| Pyrex glass | 1.005 | ||||
| Quartz mineral | 3 | ||||
| Radon (gas) | 0.0033 | ||||
| Red metal | |||||
| Rhenium | |||||
| Родий | |||||
| Камень твердый | 2 — 7 | 0025 | |||
| Rock, porous volcanic (Tuff) | 0.5 — 2.5 | ||||
| Rock Wool insulation | 0.045 | ||||
| Rosin | 0.32 | ||||
| Rubber, cellular | 0,045 | ||||
| Натуральный каучук | 0,13 | ||||
| Рубидий | |||||
| Salmon (73% moisture content) | 0. 50 50 | ||||
| Sand, dry | 0.15 — 0.25 | ||||
| Sand, moist | 0.25 — 2 | ||||
| Sand, saturated | 2 — 4 | ||||
| Sandstone | 1.7 | ||||
| Sawdust | 0.08 | ||||
| Selenium | |||||
| Sheep wool | 0.039 | ||||
| Silica aerogel | 0.02 | ||||
| Silicon cast resin | 0.15 — 0.32 | ||||
| Silicon carbide | 120 | ||||
| Силиконовое масло | 0,1 | ||||
| Серебро | |||||
| Slag wool | 0.042 | ||||
| Slate | 2. 01 01 | ||||
| Snow (temp < 0 o C) | 0.05 — 0.25 | ||||
| Sodium | |||||
| Сфальные деревы (FIR, Pine ..) | 0,12 | ||||
| почва, глина | 1,1 | ||||
| 0.15 — 2 | |||||
| Soil, saturated | 0.6 — 4 | ||||
Solder 50-50 | 50 | ||||
Soot | 0.07 | ||||
Пар, насыщенный | 0,0184 | ||||
| Пар, низкое давление | 0,00304547 | ||||
| Steatite | 2 | ||||
| Steel, Carbon | |||||
| Steel, Stainless | |||||
| Straw slab insulation, compressed | 0. 09 09 | ||||
| Styrofoam | 0,033 | ||||
| Сера диоксид (газ) | 0,0086 | ||||
| Сера кристаллическая | 0.2 | ||||
| Sugars | 0.087 — 0.22 | ||||
| Tantalum | |||||
| Tar | 0.19 | ||||
| Tellurium | 4.9 | ||||
| Thorium | |||||
| Древесина ольха | 0,17 | ||||
| Древесина ясень | 0,16 | ||||
| Timber, birch | 0.14 | ||||
| Timber, larch | 0.12 | ||||
| Timber, maple | 0.16 | ||||
| Timber, oak | 0.17 | ||||
| Лес, сосна | 0,14 | ||||
| Лес, рябина | 0,19 | 0. 14 14 | |||
| Timber, red pine | 0.15 | ||||
| Timber, white pine | 0.15 | ||||
| Timber, walnut | 0.15 | ||||
| TIN | |||||
| Титан | |||||
| TUNGSTEN | |||||
| 303030025 | |||||
| Urethane foam | 0.021 | ||||
| Vacuum | 0 | ||||
| Vermiculite granules | 0.065 | ||||
| Vinyl ester | 0,25 | ||||
| Вода | 0,606 | ||||
| Вода, пар (пар) | 0.0267 | 0.0359 | |||
| Wheat flour | 0.45 | ||||
| White metal | 35 — 70 | ||||
| Wood across the grain, white pine | 0. 12 12 | ||||
| Древесина поперек волокон, бальза | 0,055 | ||||
| Древесина поперек волокон, сосна желтая, брус | 0,147 | ||||
| Wood, oak | 0.17 | ||||
| Wool, felt | 0.07 | ||||
| Wood wool, slab | 0.1 — 0.15 | ||||
| Xenon (gas) | 0,0051 | ||||
| Цинк | |||||
1) Это, по-видимому, усугубляется курением сигарет, и в результате возникают такие заболевания, как мезотелиома и рак легких.
- 1 Вт/(м K) = 1 Вт/(м o C) = 0,85984 ккал/(ч·м o C) = 0,5779 БТЕ/(фут·ч o F) = 0,048 БТЕ/( in h o F) = 6,935 (Btu in)/(ft²·h °F)
- Теплопроводность – конвертер единиц измерения
- Что такое кондуктивная теплопередача?
Пример.
 Кондуктивная теплопередача через алюминиевый котел по сравнению с котлом из нержавеющей стали
Кондуктивная теплопередача через алюминиевый котел по сравнению с котлом из нержавеющей сталиКондуктивный перенос тепла через стенку котелка можно рассчитать как
q = (k / s) A dT (1)
or alternatively
q / A = (k / s) dT
where
q = heat теплопередача (Вт, БТЕ/ч)
A = площадь поверхности (м 2 , фут 2 )
q / A = теплопередача на единицу площади (Вт/м 2 , БТЕ/A (высота фут 2 ))
k = теплопроводность (Вт/мК, БТЕ/(час·фут·°F) )
dT = t 1 — t 2 = разность температур )
s = wall thickness (m, ft)
Conductive Heat Transfer Calculator
k = thermal conductivity (W/mK, Btu/(hr ft °F) )
s = толщина стены (м, фут)
A = surface area (m 2 , ft 2 )
dT = t 1 — t 2 = temperature difference ( o C, o F)
Note ! — что общая теплопередача через поверхность определяется » общим коэффициентом теплопередачи » — который помимо кондуктивной теплопередачи — зависит от
- коэффициентов конвективной теплопередачи на внутренней и внешней поверхностях
- коэффициенты лучистой теплопередачи на внутренней и внешней поверхностях
- Калькулятор общей теплопередачи
Кондуктивная теплопередача через стенку алюминиевой емкости толщиной 2 мм — разница температур 80
o C Теплопроводность для алюминия 215 Вт/(м·К) (из таблицы выше). Кондуктивную теплопередачу на единицу площади можно рассчитать как
Кондуктивную теплопередачу на единицу площади можно рассчитать как
q / A = [(215 Вт/(м·К)) / (2 10 -3 M)] (80 O C)
= 8600000 (W/M 2 )
= 8673)
= 8673)
= 8673).
Кондуктивная теплопередача через стенку емкости из нержавеющей стали толщиной 2 мм — разница температур 80
o CТеплопроводность для нержавеющей стали составляет 17 Вт/(м·К) (из таблицы выше). Кондуктивную теплопередачу на единицу площади можно рассчитать как
Q / a = [(17 Вт / (M K)) / (2 10 -3 M) ] (80 O C)
= 68000000 (W / M
= 68000000. )
= 680 (кВт/м 2 )
Теплопроводность жидкостей — газов и жидкостей
Флюиды являются подмножеством фаз материи и включают жидкости , газы , плазма и, в некоторой степени, твердые пластмассы. Поскольку межмолекулярное расстояние намного больше, а движение молекул более хаотично для жидкого состояния, чем для твердого, перенос тепловой энергии менее эффективен. Теплопроводность газов и жидкостей обычно меньше, чем у твердых тел. В жидкостях теплопроводность обусловлена атомной или молекулярной диффузией. В газах теплопроводность обусловлена диффузией молекул с более высокого энергетического уровня на более низкий уровень.
Поскольку межмолекулярное расстояние намного больше, а движение молекул более хаотично для жидкого состояния, чем для твердого, перенос тепловой энергии менее эффективен. Теплопроводность газов и жидкостей обычно меньше, чем у твердых тел. В жидкостях теплопроводность обусловлена атомной или молекулярной диффузией. В газах теплопроводность обусловлена диффузией молекул с более высокого энергетического уровня на более низкий уровень.
Теплопроводность газов
Влияние температуры, давления и химических соединений на теплопроводность газа можно объяснить с точки зрения кинетической теории газов . Воздух и другие газы обычно являются хорошими изоляторами при отсутствии конвекции. Таким образом, многие изоляционные материалы (например, полистирол) функционируют просто благодаря большому количеству заполненных газом карманов, из которых предотвращают крупномасштабную конвекцию . Чередование газового кармана и твердого материала вызывает передачу тепла через множество поверхностей раздела, что приводит к быстрому снижению коэффициента теплопередачи.
Чередование газового кармана и твердого материала вызывает передачу тепла через множество поверхностей раздела, что приводит к быстрому снижению коэффициента теплопередачи.
Теплопроводность газов прямо пропорциональна плотности газа, средней молекулярной скорости и особенно длине свободного пробега молекулы. Длина свободного пробега также зависит от диаметра молекулы, причем более крупные молекулы с большей вероятностью столкнутся, чем мелкие молекулы, что представляет собой среднее расстояние, пройденное энергоносителем (молекулой) до столкновения. Легкие газы, такие как водород и гелий, обычно имеют высокую теплопроводность , а плотные газы, такие как ксенон и дихлордифторметан, имеют низкую теплопроводность.
Как правило, теплопроводность газов увеличивается с повышением температуры.
Теплопроводность жидкостей
Как уже писалось, в жидкостях теплопроводность обусловлена атомной или молекулярной диффузией, но физические механизмы объяснения теплопроводности жидкостей изучены недостаточно. Жидкости, как правило, обладают лучшей теплопроводностью, чем газы, а способность течь делает жидкость подходящей для отвода избыточного тепла от механических компонентов. Тепло можно отводить, пропуская жидкость через теплообменник. Теплоносители, используемые в ядерных реакторах, включают воду или жидкие металлы, такие как натрий или свинец.
Жидкости, как правило, обладают лучшей теплопроводностью, чем газы, а способность течь делает жидкость подходящей для отвода избыточного тепла от механических компонентов. Тепло можно отводить, пропуская жидкость через теплообменник. Теплоносители, используемые в ядерных реакторах, включают воду или жидкие металлы, такие как натрий или свинец.
Теплопроводность неметаллических жидкостей обычно уменьшается с повышением температуры.
Теплопроводность натрия
Жидкий натрий используется в качестве теплоносителя в некоторых типах ядерных реакторов , поскольку он имеет высокую теплопроводность и низкое сечение поглощения нейтронов, необходимое для достижения высокого нейтронного потока в реакторе. Высокие свойства теплопроводности эффективно создают резервуар теплоемкости, который обеспечивает тепловую инерцию против перегрева.
Специальный справочник: Теплофизические свойства материалов для ядерной энергетики: Учебное пособие и сбор данных. IAEA-THPH, МАГАТЭ, Вена, 2008 г. ISBN 978–92–0–106508–7.
IAEA-THPH, МАГАТЭ, Вена, 2008 г. ISBN 978–92–0–106508–7.
Теплопроводность воды и пара
Вода и пар являются общими жидкостями, используемыми для теплообмена в первом контуре (от поверхности твэлов к потоку теплоносителя) и во втором контуре. Он используется из-за его доступности и высокая теплоемкость, как для охлаждения, так и для обогрева. Особенно эффективен перенос тепла посредством испарения и конденсации воды из-за ее очень большой скрытой теплоты испарения .
Недостатком является то, что реакторы с водяным замедлителем должны использовать первичный контур высокого давления для поддержания воды в жидком состоянии и достижения достаточного термодинамического КПД. Вода и пар также реагируют с металлами, обычно используемыми в таких отраслях, как сталь и медь, которые быстрее окисляются необработанной водой и паром. Почти на всех тепловых электростанциях (угольных, газовых, атомных) вода используется в качестве рабочего тела (используется в замкнутом контуре между котлом, паровой турбиной и конденсатором) и теплоносителя (используется для обмена отработанного тепла на тепло). водоем или уносят путем испарения в градирне).
Почти на всех тепловых электростанциях (угольных, газовых, атомных) вода используется в качестве рабочего тела (используется в замкнутом контуре между котлом, паровой турбиной и конденсатором) и теплоносителя (используется для обмена отработанного тепла на тепло). водоем или уносят путем испарения в градирне).
Теплопроводность воды
Теплопроводность пара
IAEA-THPH, МАГАТЭ, Вена, 2008 г. ISBN 978–92–0–106508–7.
Теплопроводность гелия
Гелий — это химический элемент с атомным номером 2, , что означает наличие 2 протонов и 2 электронов в атомной структуре. химический символ для гелия He .
Это бесцветный, без запаха, без вкуса, нетоксичный, инертный, одноатомный газ, первый в группе благородных газов в периодической таблице. Его температура кипения самая низкая среди всех элементов.
Из-за относительно низкой молярной (атомной) массы гелия его теплопроводность, удельная теплоемкость и скорость звука в газовой фазе выше, чем у любого другого газа, кроме водорода. Из-за своей инертности и высокой теплопроводности, нейтронной прозрачности, а также из-за того, что он не образует радиоактивных изотопов в реакторных условиях, гелий используется в качестве теплоносителя в некоторых газоохлаждаемых ядерных реакторах (например, высокотемпературных газоохлаждаемых реакторах — ВТГР).
Специальный справочник: Теплофизические свойства материалов для ядерной энергетики: Учебное пособие и сбор данных. IAEA-THPH, МАГАТЭ, Вена, 2008 г. ISBN 978–92–0–106508–7.
Ссылки:
Теплопередача:
- Основы тепломассообмена, 7-е издание. Теодор Л. Бергман, Эдриенн С. Лавин, Фрэнк П. Инкропера. John Wiley & Sons, Incorporated, 2011. ISBN: 9781118137253.

- Тепло- и массообмен. Юнус А. Ценгель. McGraw-Hill Education, 2011. ISBN: 9780071077866.
- Основы тепломассообмена. CP Котандараман. New Age International, 2006 г., ISBN: 9788122417722.
- Министерство энергетики США, термодинамики, теплопередачи и течения жидкости. Справочник по основам Министерства энергетики США, том 2 из 3, май 2016 г.
Ядерная и реакторная физика:
- Дж. Р. Ламарш, Введение в теорию ядерных реакторов, 2-е изд., Addison-Wesley, Reading, MA (1983).
- Дж. Р. Ламарш, А. Дж. Баратта, Введение в ядерную технику, 3-е изд., Prentice-Hall, 2001, ISBN: 0-201-82498-1.
- В. М. Стейси, Физика ядерных реакторов, John Wiley & Sons, 2001, ISBN: 0-471-39127-1.
- Гласстоун, Сесонске. Разработка ядерных реакторов: разработка реакторных систем, Springer; 4-е издание, 1994 г., ISBN: 978-0412985317
- WSC. Уильямс. Ядерная физика и физика элементарных частиц. Кларендон Пресс; 1 издание, 1991 г.
 , ISBN: 978-0198520467
, ISBN: 978-0198520467 - Г.Р.Кипин. Физика ядерной кинетики. Паб Эддисон-Уэсли. Ко; 1-е издание, 1965 г.
- Роберт Рид Берн, Введение в работу ядерного реактора, стр. 1988.
- Министерство энергетики, ядерной физики и теории реакторов США. Справочник по основам Министерства энергетики, том 1 и 2. Январь 1993 г.
- Пол Ройсс, Нейтронная физика. EDP Sciences, 2008. ISBN: 978-2759800414.
Advanced Reactor Physics:
- К. О. Отт, В. А. Безелла, Введение в статистику ядерных реакторов, Американское ядерное общество, исправленное издание (1989 г.), 1989 г., ISBN: 0-894-48033-2.
- К. О. Отт, Р. Дж. Нойхольд, Введение в динамику ядерных реакторов, Американское ядерное общество, 1985, ISBN: 0-894-48029-4.
- Д. Л. Хетрик, Динамика ядерных реакторов, Американское ядерное общество, 1993, ISBN: 0-894-48453-2.
- Э. Э. Льюис, В. Ф. Миллер, Вычислительные методы переноса нейтронов, Американское ядерное общество, 1993, ISBN: 0-894-48452-4.

Теплопроводность
сообщите об этом объявлении
Транспортные свойства в газах | Понятия теплофизики
Иконка Цитировать Цитировать
Разрешения
- Делиться
- Твиттер
- Подробнее
Ссылка
Блунделл, Стивен Дж. И Кэтрин М. Блунделл,
‘Транспортные свойства в газах
,
Концепции в термической физике
, 2nd Edn
(
Oxford,
2009;
(
,
9 edn,
Oxford Academic
, 1 января 2010 г.
), https://doi.org/10.1093/acprof:oso/978019
, по состоянию на 3 октября 2027 г.
. Выберите формат Выберите format.ris (Mendeley, Papers, Zotero).enw (EndNote).bibtex (BibTex).txt (Medlars, RefWorks)
Закрыть
Фильтр поиска панели навигации Oxford AcademicConcepts in Thermal Physics (2-е изд.) Астрономия и астрофизикаКнигиЖурналы Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации Oxford AcademicConcepts in Thermal Physics (2-е изд.) Астрономия и астрофизикаКнигиЖурналы Термин поиска на микросайте
Advanced Search
Abstract
В этой главе описывается, как газ может переносить импульс, энергию или частицы из одного места в другое. Он рассматривает неравновесные ситуации, но еще в стационарном состоянии, т. е. так, что параметры системы не зависят от времени, но окружение будет зависеть от времени. Изучаемые явления называются транспортными свойствами, и рассматриваются следующие: (i) вязкость, которая представляет собой перенос импульса; (ii) теплопроводность, то есть перенос тепла; и (iii) диффузия, которая представляет собой перенос частиц.
Он рассматривает неравновесные ситуации, но еще в стационарном состоянии, т. е. так, что параметры системы не зависят от времени, но окружение будет зависеть от времени. Изучаемые явления называются транспортными свойствами, и рассматриваются следующие: (i) вязкость, которая представляет собой перенос импульса; (ii) теплопроводность, то есть перенос тепла; и (iii) диффузия, которая представляет собой перенос частиц.
Ключевые слова: импульс, энергия, частицы, вязкость, теплопроводность, диффузия
Предмет
Астрономия и астрофизика
В настоящее время у вас нет доступа к этой главе.
Войти
Получить помощь с доступом
Получить помощь с доступом
Доступ для учреждений
Доступ к контенту в Oxford Academic часто предоставляется посредством институциональных подписок и покупок. Если вы являетесь членом учреждения с активной учетной записью, вы можете получить доступ к контенту одним из следующих способов:
Если вы являетесь членом учреждения с активной учетной записью, вы можете получить доступ к контенту одним из следующих способов:
Доступ на основе IP
Как правило, доступ предоставляется через институциональную сеть к диапазону IP-адресов. Эта аутентификация происходит автоматически, и невозможно выйти из учетной записи с IP-аутентификацией.
Войдите через свое учреждение
Выберите этот вариант, чтобы получить удаленный доступ за пределами вашего учреждения. Технология Shibboleth/Open Athens используется для обеспечения единого входа между веб-сайтом вашего учебного заведения и Oxford Academic.
- Щелкните Войти через свое учреждение.
- Выберите свое учреждение из предоставленного списка, после чего вы перейдете на веб-сайт вашего учреждения для входа в систему.
- : Находясь на сайте учреждения, используйте учетные данные, предоставленные вашим учреждением.
 Не используйте личную учетную запись Oxford Academic.
Не используйте личную учетную запись Oxford Academic. - После успешного входа вы вернетесь в Oxford Academic.
Если вашего учреждения нет в списке или вы не можете войти на веб-сайт своего учреждения, обратитесь к своему библиотекарю или администратору.
Войти с помощью читательского билета
Введите номер своего читательского билета, чтобы войти в систему. Если вы не можете войти в систему, обратитесь к своему библиотекарю.
Члены общества
Доступ члена общества к журналу достигается одним из следующих способов:
Войти через сайт сообщества
Многие общества предлагают единый вход между веб-сайтом общества и Oxford Academic. Если вы видите «Войти через сайт сообщества» на панели входа в журнале:
- Щелкните Войти через сайт сообщества.
- При посещении сайта общества используйте учетные данные, предоставленные этим обществом.
 Не используйте личную учетную запись Oxford Academic.
Не используйте личную учетную запись Oxford Academic. - После успешного входа вы вернетесь в Oxford Academic.
Если у вас нет учетной записи сообщества или вы забыли свое имя пользователя или пароль, обратитесь в свое общество.
Вход через личный кабинет
Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам. Смотри ниже.
Личный кабинет
Личную учетную запись можно использовать для получения оповещений по электронной почте, сохранения результатов поиска, покупки контента и активации подписок.
Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам.
Просмотр учетных записей, вошедших в систему
Щелкните значок учетной записи в правом верхнем углу, чтобы:


 ) данные приведены для воздушно-сухого состояния (5-10% относительной влажности). Некоторые свойства пластмасс и сплавов различных марок одного и того же типа могут отличаться очень сильно (на десятки процентов и даже в несколько раз), поэтому приведённые по ним данные следует считать оценочными и для точных расчётов использовать с осторожностью!
) данные приведены для воздушно-сухого состояния (5-10% относительной влажности). Некоторые свойства пластмасс и сплавов различных марок одного и того же типа могут отличаться очень сильно (на десятки процентов и даже в несколько раз), поэтому приведённые по ним данные следует считать оценочными и для точных расчётов использовать с осторожностью! 51·103
51·103 35·103 .. 2.6·103
35·103 .. 2.6·103 12·103
12·103 10..0.15
10..0.15 8·103
8·103 7·10–6
7·10–6 5·103 .. 3.0·103
5·103 .. 3.0·103 7·103
7·103 4·103
4·103 8·107
8·107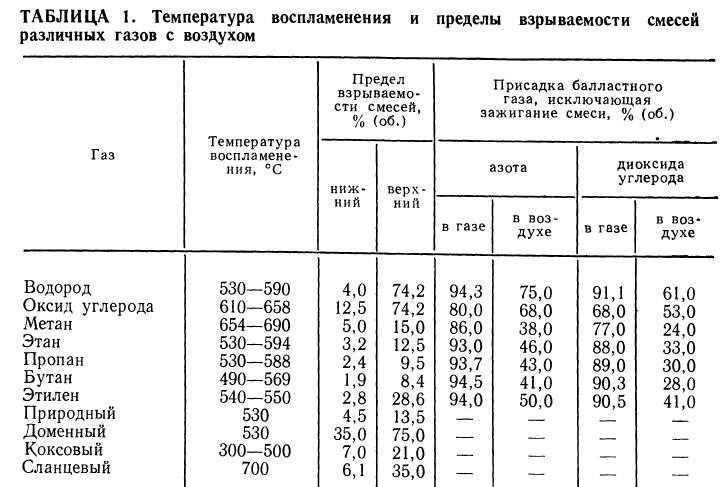 6·103 .. 0.8·103
6·103 .. 0.8·103 45·103
45·103 2·103 .. 1.5·103
2·103 .. 1.5·103 . 3900
. 3900 8·103
8·103 8·103 .. 2.0·103
8·103 .. 2.0·103 4·1010..3.6·1010
4·1010..3.6·1010 1·10–6
1·10–6 49·103
49·103 5·1010..5.0·1010 / 1.4·1010..4.4·1010
5·1010..5.0·1010 / 1.4·1010..4.4·1010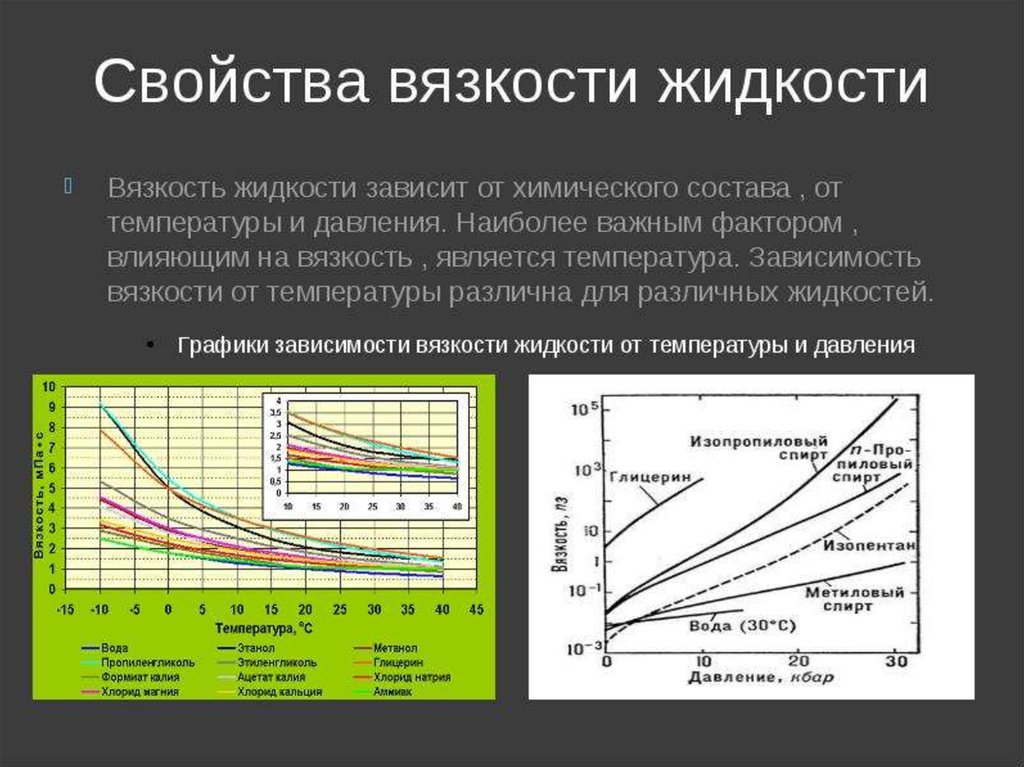 3
3 29·103
29·103 209·103
209·103 25·103
25·103 6·109..4.0·109 / —
6·109..4.0·109 / — .4.0·107 / —
.4.0·107 / — .5·107 / —
.5·107 / — 91·103 .. 0.97·103(0.95·103)
91·103 .. 0.97·103(0.95·103) 042 .. 0.054
042 .. 0.054 6%
6% 720·103
720·103 50·103 .. 2.59·103
50·103 .. 2.59·103 3·103 .. 1.4·103
3·103 .. 1.4·103 1·103
1·103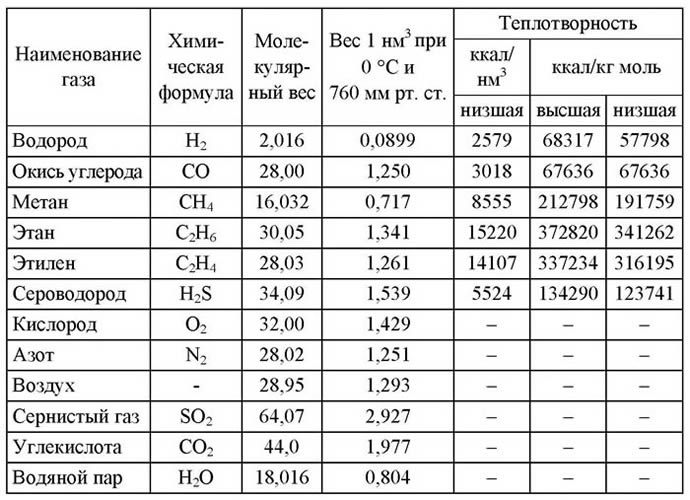 92·103 .. 1.05·103
92·103 .. 1.05·103 9%
9% 4%..3.6%
4%..3.6% 38·103
38·103 18·103
18·103 5
5 260·106
260·106 684·103
684·103 30·106
30·106 7·10-10
7·10-10 19·103
19·103 7·10-10
7·10-10 928·103
928·103 6·103
6·103 8·10-4
8·10-4 350·106
350·106 0226
0226 0·10-4
0·10-4 71·103
71·103 251
251 8 (-122.4°C)
8 (-122.4°C) 673
673 3 (-239.9°C)
3 (-239.9°C) 1558 (при 43°С)
1558 (при 43°С)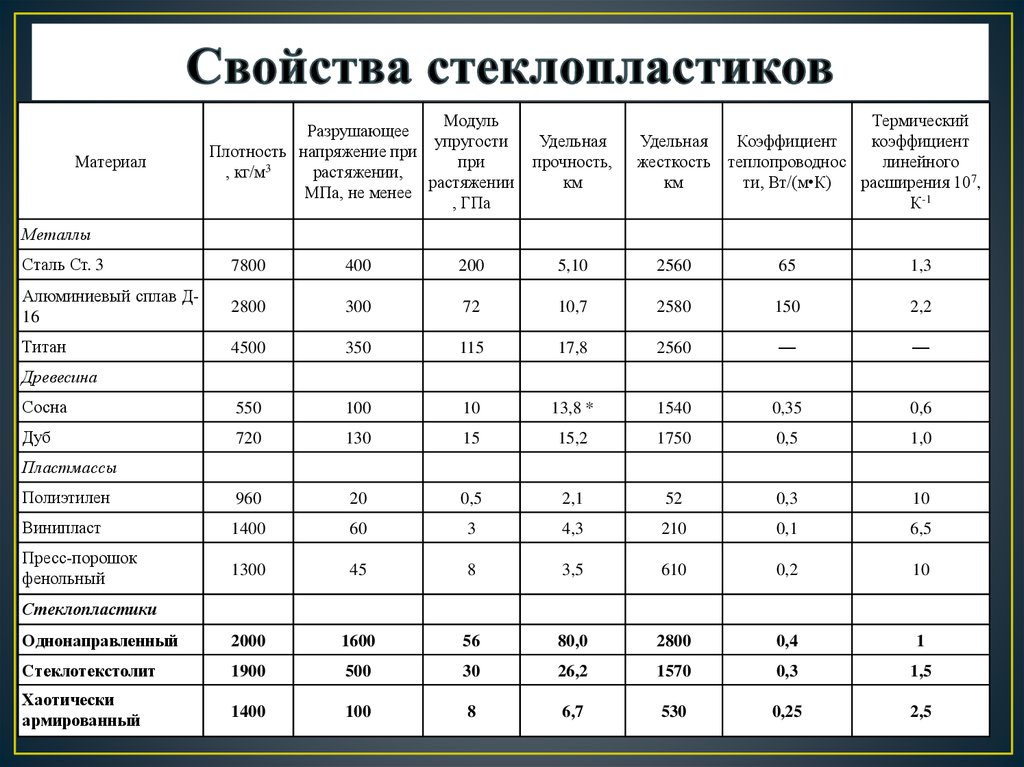 977
977 72
72 139
139 91
91 696
696 47·106
47·106 8 (+34.6°С)
8 (+34.6°С) 1)
1) 4
4 1
1 2
2 1
1 1
1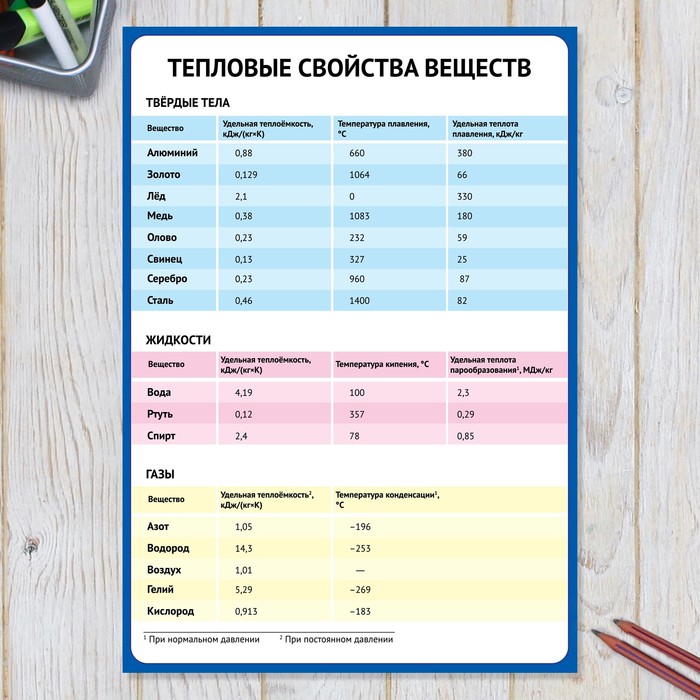 1
1 2
2 7
7 1
1 1
1 1657
1657 1918
1918