Формула Майера для теплоемкостей идеального газа, пример задачи
Многие газы в физике принято описывать в рамках идеальной модели, с помощью которой можно легко определить основные термодинамические характеристики системы. В данной статье приведем вывод формулы Майера для газа идеального и покажем, как ее можно использовать для решения задачи.
Идеальный газ и его уравнение
Чтобы понять вывод формулы Майера, следует ближе познакомиться с моделью идеального газа. Согласно ей, термодинамическая система представляет собой совокупность частиц, которые не обладают размерами (являются материальными точками). Их кинетическая энергия является единственной компонентой внутренней энергии системы (потенциальная энергия взаимодействий равна нулю), и скорости частиц подчиняются классическому распределению Максвелла-Больцмана.
Описанная модель хорошо подходит для многих реальных газообразных систем, состоящих из химически инертных атомов и молекул, и имеющих невысокие давления и температуры в несколько сотен кельвин.
Идеальный газ описывается универсальным выражением, которое называется законом Клапейрона-Менделеева. Оно приведено ниже:
P*V = n*R*T.
Здесь P, V, T — три термодинамических величины: давление, объем и температура. Параметры n и R — это количество вещества в системе и постоянная для всех газов, соответственно.
Внутренняя энергия и изохорный процесс
Согласно определению, внутренняя энергия U произвольной системы равна сумме потенциальной и кинетической энергий ее элементов. Выше отмечалось, что в идеальной модели газовые молекулы и атомы друг с другом не взаимодействуют, это означает, что внутренняя энергия определяется исключительно кинетической составляющей.
Из кинетической теории газов следует равенство, связывающее среднюю кинетическую энергию частицы с абсолютной температурой в системе:
m*v2/2 = z/2*kB*T.
Где m — масса одной частицы, kB — Больцмана константа, v — скорость средняя квадратичная, z — число степеней свободы. Если обе части равенства умножить на количество N частиц в системе, то мы получим выражение для внутренней энергии U:
Если обе части равенства умножить на количество N частиц в системе, то мы получим выражение для внутренней энергии U:
U = z/2*N*kB*T = z/2*n*R *T.
При записи этого выражения мы воспользовались следующими равенствами:
n = N/NA; R = kB*NA.
Теперь рассмотрим вопрос определения внутренней энергии газа с точки зрения термодинамики. Обратимся к изохорному процессу. В результате него все подводимое тепло идет на нагрев системы, поскольку объем остается постоянный, и работа газа равна нулю, то есть:
dU = Q.
В свою очередь, изменение величины U можно записать так:
dU = CV*dT.
Где CV — теплоемкость системы при постоянном объеме. Эта величина показывает, сколько энергии в джоулях необходимо затратить, чтобы нагреть систему на 1 Кельвин. Сравнивая это выражение с формулой для U, которая получена из кинетической теории, приходим к равенству:
CV = z/2*n*R.
Вместо теплоемкости CV часто пользуются молярной изохорной теплоемкостью, то есть той же величиной, только для 1 моля газа:
CV = z/2*R.
Формула Майера для теплоемкостей
Чтобы получить названную формулу, следует рассмотреть с точки зрения термодинамики изобарный процесс. Под ним понимают переход системы между двумя равновесными состояниями, при котором давление не изменяется. Предположим, что в рассматриваемой системе содержится 1 моль газа, тогда первое начало термодинамики для изобарного процесса примет вид:
Q = dU + P*dV.
Теперь введем понятие об изобарной теплоемкости CP. Под ней понимают количество теплоты, которое следует системе сообщить, чтобы она нагрелась на 1 Кельвин, а ее давление при этом не изменилось. Это определение позволяет переписать равенство выше в виде:
CP*dT = dU + P*dV.
Если вспомнить уравнение для 1 моля идеального газа и выражение для изменения внутренней энергии, то это равенство запишется так:
CP*dT = CV*dT + R*dT =>
CP = CV + R.
Это выражение называется формулой Майера для идеального газа. Оно показывает, что изобарная теплоемкость всегда больше изохорной на величину газовой постоянной для 1 моля газа. Значение же газовой постоянной R также приобретает конкретный физический смысл — это работа, которую совершает один моль газа во время его изобарного расширения при нагреве на один Кельвин.
Задача на определение теплоемкостей воздуха
Необходимо вычислить молярные теплоемкости CP и CV для воздуха, полагая его идеальным газом.
Решить эту задачу несложно, если вспомнить, что изохорная молярная теплоемкость равна:
CV = z/2*R.
Тогда в соответствии с формулой Майера молярная величина CP будет равна:
CP = CV + R = (2+z)/2*R.
Поскольку воздух на 99% образован двухатомными молекулами O2 и N2, то z для него равно 5. Подставляя это значение, а также значение R=8,314 Дж/(К*моль) в формулы, получаем ответы на задачу: CV = 20,8 Дж/(К*моль), CP = 29,1 Дж/(К*моль).
Подставляя это значение, а также значение R=8,314 Дж/(К*моль) в формулы, получаем ответы на задачу: CV = 20,8 Дж/(К*моль), CP = 29,1 Дж/(К*моль).
5.2. Теплоемкости изохорная и изобарная
Процесс нагревания или охлаждения может происходить при различных условиях. Рассмотрим процесс нагревания газа одного и того же количества (1 кг) в одинаковых цилиндрах с одинаковыми начальными параметрами (рис. 5.1).
В обоих цилиндрах газ будем нагревать до одинаковой температуры Т2. В первом цилиндре (рис.5.1, а) теплота будет подводиться при постоянном объеме, т.е. процесс будет изохорным. Во втором цилиндре (рис.5.1, б) газ будет расширяться от v1до v2 при постоянном давлении (р), т.е. процесс будет изобарным.
Рис. 5.1. Изохорный (а) и изобарный (б) процессы
Так как в первом случае газ не расширяется, он не совершает работу и поэтому вся подводимая теплота тратится на повышение внутренней энергии и на повышения давления.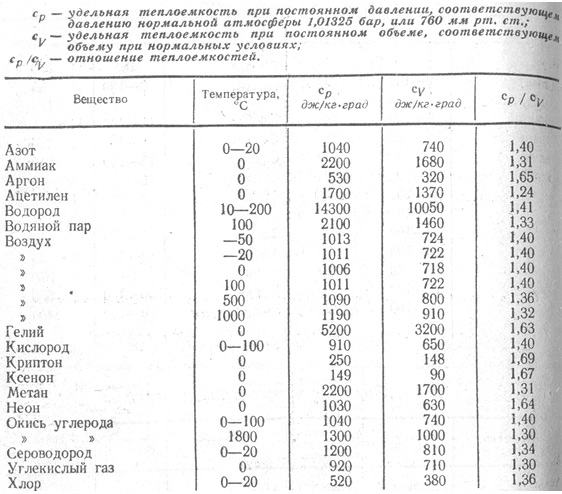 Удельное количество теплоты можно определить по формуле:
Удельное количество теплоты можно определить по формуле:
.
Во втором цилиндре подведенная к газу теплота расходуется как на повышение температуры, так и на перемещение поршня (т.е. на совершение работы). Удельное количество теплоты в этом случае можно определить по формуле:
. (5.2)
Подогрев газа в обоих цилиндрах идет до одинаковой температуры Т2, но во втором случае теплоты необходимо затратить больше на величину работы l, совершенной для перемещения поршня. Тогда:
или .
Известно, что работа (l) при р = const составляет:
или .
Так как , то .
Следовательно, имеем:
.
откуда
. (5.3)
Полученная связь между изобарной и изохорной теплоемкостями (5.
.
Таким образом, в зависимости от того к какой количественной единице вещества относится теплоемкость, различают следующие виды изобарной и изохорной теплоемкостей:
– массовые изобарная и изохорная теплоемкости;
– объемные изобарная и изохорная теплоемкости;
– мольные изобарная и изохорная теплоемкости.
В термодинамических расчетах часто встречается величина (), называемая показателем адиабаты и равная отношению изобарной теплоемкости к изохорной:
.
Значение показателя адиабаты зависит от температуры, но для газов и паров эта зависимость незначительна, и ею пренебрегают, принимая величиной постоянной. Для идеальных газов значение показателя адиабаты принимают равным:
· одноатомных газов – 1,67;
· двухатомных газов – 1,4;
· трех- и многоатомных газов – 1,29.
Точные значения для некоторых газов и водяных паров приводятся в справочниках в зависимости от их температур.
ТЕПЛОЕМКОСТЬ — Студопедия
Теплоемкость – это количество теплоты, которое необходимо сообщить системе для увеличения ее температуры на 1 (К) при отсутствии полезной работы и постоянстве соответствующих параметров.
Если в качестве системы мы берем индивидуальное вещество, то общая теплоемкость системы равняется теплоемкости 1 моль вещества () умноженное на число моль ().
. (16 )
Теплоемкость может быть удельная и молярная.
Удельная теплоемкость – это количество теплоты, необходимое для нагревания единицы массы вещества на 1 град (интенсивная величина).
Молярная теплоемкость – это количество теплоты, необходимое для нагревания одного моль вещества на 1 град.
Различают истинную и среднюю теплоемкость.
В технике обычно используют понятие средней теплоемкости.
Средняя– это теплоемкость для определенного интервала температур.
Если системе, содержащей количество вещества или массой , сообщили количество теплоты , а температура системы повысилась от до , то можно рассчитать среднюю удельную или молярную теплоемкость:
, . (17)
, . (18)
Истинная молярная теплоемкость – это отношение бесконечно малого количества теплоты, сообщенной 1 моль вещества при определенной температуре, к приращению температуры, которое при этом наблюдается.
. (19)
Согласно уравнению (19), теплоемкость, как и теплота, не является функцией состояния. При постоянном давлении или объеме, согласно уравнениям (11) и (12), теплота, а, следовательно, и теплоемкость приобретают свойства функции состояния, то есть становятся характеристическими функциями системы. Таким образом, получаем изохорную и изобарную теплоемкости.
Изохорная теплоемкость – количество теплоты, которое необходимо сообщить системе, чтобы повысить температуру на 1 , если процесс происходит при .
. (20)
Изобарная теплоемкость – количество теплоты, которое необходимо сообщить системе, чтобы повысить температуру на 1 при .
. (21)
Теплоемкость зависит не только от температуры, но и от объема системы, поскольку между частицами существуют силы взаимодействия, которые изменяются при изменении расстояния между ними, поэтому в уравнениях (20) и (21) используют частные производные.
Энтальпия идеального газа, как и его внутренняя энергия, является функцией только температуры:
,
а в соответствии с уравнением Менделеева–Клапейрона , тогда
. (22)
Поэтому для идеального газа в уравнениях (20), (21) частные производные можно заменить на полные дифференциалы:
. (23)
. (24)
Из совместного решения уравнений (23) и (24) с учетом (22), получим уравнение взаимосвязи между и для идеального газа.
. (25)
Разделив переменные в уравнениях (23) и (24), можно рассчитать изменение внутренней энергии и энтальпии при нагревании 1 моль идеального газа от температуры до
. (26)
(26)
. (27)
Если в указанном интервале температур теплоемкость можно считать постоянной, то в результате интегрирования получаем:
. (28)
. (29)
Установим взаимосвязь между средней и истинной теплоемкостью. Изменение энтропии с одной стороны выражается уравнением (27), с другой –
.
Приравняв правые части уравнений и выразив среднюю теплоемкость, имеем:
. (30)
Аналогичное выражение можно получить для средней изохорной теплоемкости.
Теплоемкость большинства твердых, жидких и газообразных веществ повышается с ростом температуры. Зависимость теплоемкости твердых, жидких и газообразных веществ от температуры выражается эмпирическим уравнением вида:
. (31)
где а, b, c и – эмпирические коэффициенты, вычисленные на основе экспериментальных данных о , причем коэффициент относится к органическим веществам, а – к неорганическим. Значения коэффициентов для различных веществ приведены в справочнике и применимы только для указанного интервала температур.
Теплоемкость идеального газа не зависит от температуры. Согласно молекулярно-кинетической теории теплоемкость, приходящаяся на одну степень свободы, равна (степень свободы – число независимых видов движения на которые можно разложить сложное движение молекулы). Для одноатомной молекулы характерно поступательное движение, которое можно разложить на три составляющие в соответствии с тремя взаимно перпендикулярными направлениями по трем осям. Поэтому изохорная теплоемкость одноатомного идеального газа равна
. (32)
Тогда изобарная теплоемкость одноатомного идеального газа согласно (25) определится по уравнению
. (33)
Двухатомные молекулы идеального газа помимо трех степеней свободы поступательного движения имеют и 2 степени свободы вращательного движения. Следовательно:
, .
Изохорная теплоемкость идеального газа — OneKu
Содержание статьи:В термодинамике при изучении переходов из начального в конечное состояние некоторой системы важно знать тепловой эффект процесса. С этим эффектом тесно связано понятие теплоемкости. В данной статье рассмотрим вопрос, что понимают под изохорной теплоемкостью газа.
Идеальный газ
Идеальным называется такой газ, частицы которого считаются материальными точками, то есть не имеют размеров, но обладают массой, и у которого вся внутренняя энергия состоит исключительно из кинетической энергии движения молекул и атомов.
Вам будет интересно:Баба-яга – это кто?
Любой реальный газ в идеале никогда не будет удовлетворять описанной модели, поскольку его частицы все же имеют некоторые линейные размеры и взаимодействуют между собой с помощью слабых ван-дер-ваальсовых связей или химических связей другого типа. Однако при низких давлениях и высоких температурах расстояния между молекулами велики, а их кинетическая энергия превышает потенциальную в десятки раз. Все это позволяет применять с высокой степенью точности идеальную модель для реальных газов.
Внутренняя энергия газа
Внутренняя энергия любой системы — это физическая характеристика, которая равна сумме потенциальной и кинетической энергии. Поскольку в идеальных газах можно пренебречь потенциальной энергией, то для них можно записать равенство:
U = Ek.
Где Ek — энергия кинетическая системы. Используя молекулярно-кинетическую теорию и применяя универсальное уравнение состояния Клапейрона-Менделеева, несложно получить выражение для U. Оно записано ниже:
U = z/2*n*R*T.
Здесь T, R и n — абсолютная температура, газовая постоянная и количество вещества соответственно. Величина z — это целое число, показывающее количество степеней свободы, которыми обладает молекула газа.
Изобарная и изохорная теплоемкость
В физике теплоемкостью называется количество теплоты, которое необходимо предоставить изучаемой системе, чтобы нагреть ее на один кельвин. Справедливо также и обратное определение, то есть теплоемкость — это количество теплоты, которое система выделяет при охлаждении на один кельвин.
Проще всего для системы определить изохорную теплоемкость. Под ней понимают теплоемкость при постоянном объеме. Поскольку система в таких условиях работу не совершает, то вся энергия расходуется на повышение внутренних энергетических запасов. Обозначим изохорную теплоемкость символом CV, тогда можно записать:
dU = CV*dT.
То есть изменение внутренней энергии системы прямо пропорционально изменению ее температуры. Если сравнить это выражение, с записанным в предыдущем пункте равенством, то приходим к формуле для CV в идеальном газе:
СV = z/2*n*R.
Данной величиной на практике неудобно пользоваться, поскольку она зависит от количества вещества в системе. Поэтому было введено понятие удельной изохорной теплоемкости, то есть величины, которую рассчитывают либо на 1 моль газа, либо на 1 кг. Обозначим первую величину символом CVn, вторую — символом CVm. Для них можно записать такие формулы:
CVn = z/2*R;
CVm = z/2*R/M.
Здесь M — молярная масса.
Изобарной называется теплоемкость при поддержании постоянного давления в системе. Примером такого процесса является расширение газа в цилиндре под поршнем при его нагревании. В отличие от изохорного, во время изобарного процесса подводимое к системе тепло расходуется на повышение внутренней энергии и на выполнение механической работы, то есть:
H = dU + P*dV.
Энтальпия изобарного процесса представляет собой произведение изобарной теплоемкости на изменение температуры в системе, то есть:
H = CP*dT.
Если рассмотреть расширение при постоянном давлении 1 моль газа, то первое начало термодинамики запишется в виде:
CPn*dT = CVn*dT + R*dT.
Последнее слагаемое получено из уравнения Клапейрона-Менделеева. Из этого равенства следует связь между изобарной и изохорной теплоемкостями:
CPn = CVn + R.
Для идеального газа удельная молярная теплоемкость при постоянном давлении всегда больше соответствующей изохорной характеристики на величину R=8,314 Дж/(моль*К).
Степени свободы молекул и теплоемкость
Выпишем еще раз формулу для удельной молярной изохорной теплоемкости:
CVn = z/2*R.
В случае газа одноатомного величина z = 3, поскольку атомы в пространстве могут перемещаться лишь в трех независимых направлениях.
Если же речь идет о газе, состоящем из двухатомных молекул, например, кислород O2 или водород h3, то, помимо поступательного движения, эти молекулы могут еще вращаться вокруг двух взаимно перпендикулярных осей, то есть z будет равно 5.
В случае более сложных молекул для определения CVn следует использовать z=6.
Источник
Изохорная теплоемкость — Большая Энциклопедия Нефти и Газа, статья, страница 1
Изохорная теплоемкость
Cтраница 1
Изохорная теплоемкость cv в околокритической области также имеет максимумы на изотермах ( рис. 1 — 28) и изобарах с тем лишь отличием, что в критической точке съ имеет большую, но конечную величину, в то время как Ср здесь бесконечно велика. [1]
Изохорная теплоемкость cv в околокритической области также имеет максимумы на изотермах ( рис. 1 — 28) и изобарах, с тем лишь отличием, что в критической точке cv имеет большую, но конечную величину, в то время как изобардая теплоемкость ср здесь бесконечно велика. [2]
Изохорная теплоемкость н-нонана и н-декана / X. [3]
Изохорная теплоемкость ( Cv) или теплоемкость при постоянном объеме соответствует случаю, когда изменение температуры путем нагрева ( или охлаждения) производят при постоянном объеме. [4]
Средняя мольная изохорная теплоемкость cv ккал / моль — град некоторых горючих газов М. В. Вукаловича, В. А. Кириллина, В. Н. Тимофеева, С. А. Ремизова и В. [5]
Но изохорная теплоемкость в критической точке обращаться в нуль не может; она всегда в соответствии с условиями устойчивости отлична от нуля и положительна. [6]
Значение изохорной теплоемкости и адиабатной сжимаемости чистых веществ в критической точке / / Журн. [7]
Исследование изохорной теплоемкости проведено методом непосредственного нагрева вещества в адиабатном калориметре. Количество тепла, идущего на нагрев калориметра и имеющегося в нем вещества, определялось по мощности калориметрического нагревателя и времени его работы. [8]
Исследование изохорной теплоемкости прямым методом дает возможность выяснить некоторые вопросы, связанные с двухфазным состоянием вещества. [9]
Для изохорной теплоемкости Су постоянство соблюдается несколько лучше. [11]
Для изохорной теплоемкости Cv постоянство соблюдается несколько лучше. [13]
Для изохорной теплоемкости Су постоянство соблюдается несколько лучше. [14]
Для изохорной теплоемкости Cv постоянство соблюдается несколько лучше. [15]
Страницы: 1 2 3 4
| | Навигация по справочнику TehTab.ru: главная страница / / Техническая информация / / Свойства рабочих сред / / Водород H2 (хладагент R702) / / Водород (h3). Удельная теплоемкость cp . Температурный диапазон 175 / 6000 °K (-98 /+5727 °С ).
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Нашли ошибку? Есть дополнения? Напишите нам об этом, указав ссылку на страницу. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| TehTab.ru Реклама, сотрудничество: [email protected] | Обращаем ваше внимание на то, что данный интернет-сайт носит исключительно информационный характер. Информация, представленная на сайте, не является официальной и предоставлена только в целях ознакомления. Все риски за использование информаци с сайта посетители берут на себя. Проект TehTab.ru является некоммерческим, не поддерживается никакими политическими партиями и иностранными организациями. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Удельная теплоемкость при постоянном давлении и переменной температуре
Удельная теплоемкость (C) — это количество тепла, необходимое для изменения температуры единицы массы вещества на один градус.
- Изобарическая теплоемкость (C p ) используется для воздуха в системе постоянного давления (ΔP = 0).
- I Сохорическая удельная теплоемкость (C v ) используется для воздуха в замкнутой системе постоянного объема , (= изометрической или изометрической ).
Примечание! При нормальном атмосферном давлении 1,013 бар удельная теплоемкость сухого воздуха — C P и C V — будет изменяться в зависимости от температуры. Это может повлиять на точность расчетов процессов кондиционирования и кондиционирования воздуха. При расчете массового и объемного расхода воздуха в обогреваемых или охлаждаемых системах с высокой точностью — удельную теплоемкость (= теплоемкость) следует скорректировать в соответствии со значениями на рисунках и в таблице ниже или вычислить с помощью калькулятора.
- Для обычных расчетов значение теплоемкости c p = 1,0 кДж / кг K (равно кДж / кг o C) или 0,24 Btu (IT) / фунт ° F — обычно достаточно точный
- Для более высокой точности — значение C p = 1,006 кДж / кг K (равно кДж / кг o C) или 0,2403 Btu (IT) / фунт ° F — это better
Онлайн-калькулятор удельной теплоемкости воздуха
Калькулятор, представленный ниже, можно использовать для оценки удельной теплоемкости воздуха при постоянном объеме или постоянном давлении, а также при заданных температуре и давлении.
Выходная тепловая мощность выражается в кДж / (кмоль * K), кДж / (кг * K), кВтч / (кг * K), ккал / (кг * K), Btu (IT) / (моль * ° R). ) и британских тепловых единиц (IT) / (фунт м * ° R)
См. также другие свойства Air при изменяющейся температуре и давлении: Плотность и удельный вес при различной температуре, плотность при переменном давлении, коэффициенты диффузии Газы в воздухе, число Прандтля, удельная теплоемкость при переменном давлении, теплопроводность, температуропроводность, свойства в условиях равновесия газ-жидкость и теплофизические свойства воздуха при стандартных условиях, а также состав и молекулярная масса,
, а также Удельная теплоемкость аммиака Бутан, диоксид углерода, монооксид углерода, этан, этанол, этилен, водород, метан, метанол, азот, кислород, пропан и вода.
Вернуться к началу
Вернуться к началу
Вернуться к началу
Удельная теплоемкость воздуха при 1 бар (= 0,1 МПа = 14,5 фунтов на кв. Дюйм):
Для полного стола с Isobaric теплоемкость — поворот экрана!
| Температура | Изохорная удельная теплоемкость (Cv) | Изобарическая теплоемкость (Cp) | Cp / Cv | [° F] | [кДж / моль K] | [кДж / кг K] | [кВтч / (кг K)] | [ккал (IT) / (кг K)] | [ккал (IT) / (фунт ° F)] | [кДж / моль K] | [кДж / кг K] | [(кВт-ч) / (кг K)] | [ккал (IT) / (кг K)] [BTU (IT) / фунт ° F] | [ккал (IT) / (фунт ° F)] | [-] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 60 | -213 | -352 | 0.03398 | 1,173 | 0,0003258 | 0,2802 | 0,2287 | 0,05506 | 1,901 | 0,000528 | 0,45405 | 0,37071 9011 9011 9011 | 1,621 | 0,37071 | 1,621 | 1,621 | 1,621 | 0,0002919 | 0,2510 | 0,2050 | 0,05599 | 1,933 | 0,000537 | 0,46169 | 0.37695 | 1,839 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 81,61 | -192 | -313 | 0,02172 | 0,7500 | 0,0002083 | 0,1791 | 0,1463 | 0,1791 | 0,1463 | | 0,1463 | 0,1463 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 100 | -173 | -280 | 0,02109 | 0,7280 | 0,0002022 | 0,1739 | 0.1420 | 0,03012 | 1,040 | 0,000289 | 0,24833 | 0,20276 | 1,428 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 120 | -153 | -244 | -153 | -244 | 0,02011 | -244 | 1,022 | 0,000283 | 0,24350 | 0,19930 | 1,415 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 140 | -133 | -208 | 0.02081 | 0,7184 | 0,0001996 | 0,1716 | 0,1401 | 0,02937 | 1,014 | 0,000282 | 0,24219 | 0,19774 | | 0,0001992 | 0,1713 | 0,1399 | 0,02928 | 1,011 | 0,000281 | 0,24147 | 0.19716 | 1,410 | | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 180 | -93,2 | -136 | 0,02076 | 0,7166 | 0,0001991 | 0,1712 | 0,1397 | 0,1712 | 0,1397 | 0,029203 | 0,1397 | 0,029203 | | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 200 | -73,2 | -99,7 | 0,02075 | 0,7163 | 0,0001990 | 0,1711 | 0.1397 | 0,02917 | 1,007 | 0,000280 | 0,24052 | 0,19638 | 1,406 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 220 | -53,2 | -63,7 | -53,2-63,7 | 0,02011-63,7 | 0,02011 | -63,7 | 1,006 | 0,000279 | 0,24028 | 0,19618 | 1,404 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 240 | -33,2 | -27.7 | 0,02075 | 0,7164 | 0,0001990 | 0,1711 | 0,1397 | 0,02914 | 1,006 | 0,000279 | 0,24028 | 0,19618 | 0,24028 | 0,19618 | 0,24028 | 0,19618 | 0,19618 | 0,7168 | 0,0001991 | 0,1712 | 0,1398 | 0,02914 | 1,006 | 0,000279 | 0,24028 | 0.19618 | 1,403 | 273,2 | 0,0 | 32,0 | 0,02077 | 0,7171 | 0,0001992 | 0,1713 | 0,1398 | 0,02914 | 1,006 | 0,000279 | 0,24028 | 0,19618 | 1,403 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 280 | 6,9 | 44,3 | 0,02078 | 0,7173 | 0,0001993 | 0,1713 | 0.1399 | 0,02914 | 1,006 | 0,000279 | 0,24028 | 0,19618 | 1,402 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 288,7 | 15,6 | 60,0 | 0,02078 | 0,7175 | 0,0001993 | 0,1714 | 0,1399 | 0,02914 | 1,006 | 0,000279 | 0,24030 | 0,19620 | 1,402 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 300 | 26,9 | 80.3 | 0,02080 | 0,7180 | 0,0001994 | 0,1715 | 0,1400 | 0,02915 | 1,006 | 0,000280 | 0,24036 | 0,19625 | 0,19625 | 0,19625 0,7192 | 0,0001998 | 0,1718 | 0,1403 | 0,02917 | 1,007 | 0,000280 | 0,24052 | 0.19638 | 1,400 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 340 | 66,9 | 152 | 0,02087 | 0,7206 | 0,0002002 | 0,1721 | 0,1405 | 0,02923 0,1405 | 0,02923 | 0,1405 | 0,02923 | 360 | 86,9 | 188 | 0,02092 | 0,7223 | 0,0002006 | 0,1725 | 0.1409 | 0,02926 | 1,010 | 0,000281 | 0,24123 | 0,19696 | 1,398 | 380 | 107 | 224 | 0,02011 | | 0,02011 | 224 | 0,020112 | 0,020112 1,012 | 0,000281 | 0,24171 | 0,19735 | 1,397 | 400 | 127 | 260 | 0.02105 | 0,7266 | 0,0002018 | 0,1735 | 0,1417 | 0,02937 | 1,014 | 0,000282 | 0,24219 | 0,19774 | 0,24219 | 0,19774 | 0,0002062 | 0,1773 | 0,1448 | 0,02983 | 1,030 | 0,000286 | 0,24597 | 0.20083 | 1,387 | 600 | 327 | 620 | 0,02213 | 0,7641 | 0,0002123 | 0,1825 | 0,1490 | 0,1825 | 0,1490 | 0,03044 0,14 | 700 | 427 | 800 | 0,02282 | 0,7877 | 0,0002188 | 0,1881 | 0.Снимка 1536 | 0,03114 | 1,075 | 0,000299 | 0,25675 | 0,20963 | 1,365 | 800 | 527 | 980 | 0,02351 | 0,8117 | 0,0002255 | 0,1939 | 0,1583 | 0,03183 | 1,099 | 0,000305 | 0,26249 | 0,21432 | 1,354 | 900 | 627 | 1160 | 0.02415 | 0,8338 | 0,0002316 | 0,1991 | 0,1626 | 0,03247 | 1,121 | 0,000311 | 0,26772 | 0,21858 | 0,26772 | 0,21858 | 11252 | 0,0002421 | 0,2082 | 0,1700 | 0,03356 | 1,159 | 0,000322 | 0,27675 | 0.22596 | 1,329 | 1500 | 1227 | 2240 | 0,02673 | 0,9230 | 0,0002564 | 0,2204 | 0,1800 | 0,2204 | 0,1800 | 0,035029011 | 0,035029011 | 0,035029011 | 1900 | 1627 | 2960 | 0,02762 | 0,9535 | 0,0002649 | 0,2277 | 0.1859 | 0,03593 | 1,241 | 0,000345 | 0,29631 | 0,24193 | 1,301 | |
Вернуться к началу
Преобразование единиц:
0009Удельная единица измерения тепла [BTU (IT)], градус Цельсия = [° C], градус Фаренгейта = [° F], градус Кельвина = [K], градус ранкин = [° R], джоуль = [Дж], килокалория (международная таблица) = [ккал (IT)], килограмм = [кг], килоджоуль = [кДж], киловатт-час = [кВтч], моль = [моль], фунт = [фунт]
K в единицах измерения можно заменить на ° C, и наоборот.° R в единицах измерения можно заменить на ° F, и наоборот.
- 1 БТЕ / (фунт ° F) = 1 БТЕ / (фунт ° R) = 1 ккал (IT) / (кг ° C) = 1 ккал (IT) / (кг K) = 4186,8 Дж / (кг K) ) = 0,81647 ккал (IT) / (фунт ° F) = 1,163×10 -3 кВтч / (кг K)
- 1 Дж / (кг K) = 1 Дж / (кг ° C) = 2,3885×10 -4 ккал (IT) / (кг o C) = 2.3885×10 -4 Btu / (фунт ° F) = 1.9501×10 -4 ккал (IT) / (фунт ° F)
- 1 ккал (IT ) / (кг ° C) = 1 британских тепловых единиц / (фунт ° F) = 4186,8 Дж / (кг · K) = 0,81647 ккал (IT) / (фунт ° F) = 1.163×10 -3 кВтч / (кг K)
- 1 ккал (IT) / (фунт ° F) = 1,2248 Btu / (фунт ° F) = 1,2248 ккал (IT) / (кг ° C) = 5127,9 Дж / ( кг K)
- 1 кДж / (кг K) = 1 кДж / (кг ° C) = 1000 Дж / (кг K) = 1000 Дж / (кг ° C) = 0,23885 ккал (IT) / (кг ° C) = 0,23885 БТЕ / (фунт ° F) = 0,19501 ккал (IT) / (фунт ° F) = 2,7778×10 -4 кВтч / (кг K)
- 1 кВтч / (кг K) = 0,85985 ккал (IT) / (кг ° C) = 0,85985 БТЕ / (фунт ° F) = 3,6 кДж / (кг K)
- 1 моль воздуха = 28,96546 г
Вернуться к началу
Теплоемкость или тепловая мощность | Примечания, видео, контроль качества и тесты | 11 класс> Физика> Калориметрия
Теплоемкость или тепловая мощность
КалориметрВведение
Калориметрия — это экспериментальный метод количественного измерения теплообмена.Взгляните на калориметр, показанный на рисунке. Он состоит из цилиндрического сосуда, обычно сделанного из меди, и мешалки из того же материала. Калориметр хорошо изолирован, чтобы предотвратить передачу тепла в калориметр или из него. Итак, сосуд помещают в деревянный ящик, оборачивая его шерстяной одеждой. Термометр, вставленный внутри калориметра, измеряет температуру содержимого калориметра. Калория — это единица тепла в системе СГС, а джоуль в единицах СИ. Одна калория — это количество тепла, необходимое для повышения температуры одного грамма воды на один градус Цельсия.Одна калория равна 4,2 джоуля.
Удельная теплоемкость
Рассмотрим два разных тела, и они нагреваются с одинаковой скоростью горелкой в течение равного времени. Мы заметим, что температура двух тел не будет одинаковой. Итак, количество тепла, необходимое для повышения температуры, зависит от следующих факторов:
Количество тепла Q, необходимое для повышения температуры вещества, прямо пропорционально его массе, m
$$ \ text {i.oC \), то
$$ Q = s $$
Таким образом, удельная теплоемкость вещества определяется как количество тепла, необходимое для изменения температуры единицы массы вещества на 1 градус. Его единица измерения — Джкг -1 k -1 в системе СИ и 1 калгм -1 C -1 в системе СКГ.
Вещество | Джмоль -1 k -1 | кал-моль -1 C -1 | |
| Алюминий | 0.215 | ||
Медь | 390 | 0,092 | |
Этанол | 2428 | 0,1 — 0,27 | |
Лед (0) | 2100 | 0,5 | |
Железо | 470 | 470 | 470 112 |
Свинец | 130 | 0,013 | |
Серебро | 4200 | 1 0,46 | |
Вода | 4200 | 1 |
Тепловая мощность или тепловая мощность
Теплоемкость, необходимая для изменения тепла вещества, определяется как количество тепла, необходимое для его изменения. температура через один градус.Ее еще называют теплоемкостью. Если Q — количество тепла, необходимое для изменения температуры тела массой m, то
$$ Q = ms \ Delta \ theta $$
Если разница температур = 1, то
$$ Q = ms $ $
Его единица измерения — J k -1 в системе SI и cal C -1 в системе CGS.
Водный эквивалент вещества
Это масса тела, которая поглощает или излучает повышение или понижение температуры на один и тот же градус.
Предположим, что m — это масса тела, которой требуется Q количества тепла для повышения температуры на \ (\ theta \).Если S — удельная теплоемкость тела, тогда
$$ Q = ms \ Delta \ theta \ dots (i) $$
Если w — водный эквивалент тела. s w — удельная теплоемкость воды. Затем из определения водного эквивалента.
$$ Q = ws_w \ Delta \ theta \ dots (ii) $$
Сравнение уравнений (i) и (ii)
$$ ws_w \ Delta \ theta \ = ms \ Delta \ theta \ $$
$$ ws_w = ms $$
$$ w = \ frac {ms} {s_w} $$
В системе CGS удельная теплоемкость воды, с w = 1 кал. -1 C — 1 , то
$$ w = ms $$
Итак, водный эквивалент вещества численно равен его теплоемкости в системе ХГС.Но единицей эквивалента воды являются граммы, а единицей измерения теплоемкости — калории.
УДЕЛЬНАЯ ТЕПЛОЕМКОСТЬ
Удельная теплоемкость чистого вещества или смеси условно определяется как тепло, необходимое для повышения температуры 1 моля вещества в определенных условиях. Однако формально он определяется как предел отношения d / dT, когда dT, изменение температуры, и d, подвод тепла, стремятся к нулю. В зависимости от условий можно определить несколько теплоемкостей, и сначала мы рассмотрим теплоемкость при постоянном объеме.В этом случае тепло передается веществу, предположительно жидкости, в жестком контейнере фиксированного объема. Термодинамическая система является замкнутой, и подходящей формой первого закона термодинамики является
(1)где dũ — изменение внутренней энергии и проделанной работы. Но поскольку = pext и равно нулю, проделанная работа равна нулю и
(2)где энтропия.
Реализация второй удельной молярной теплоемкости, которая при постоянном давлении для жидкости или твердого тела, может быть осуществлена просто путем подачи тепла к образцу под постоянным давлением, p.Соответствующий первый закон остается прежним, но
(3)не ноль, поэтому
(4)но поскольку мы можем легко показать, что
(5)Также возможно определить удельную молярную теплоемкость при насыщении, которая связана с количеством тепла, которое должно быть подано на 1 моль системы для изменения температуры на единицу при сохранении фазового равновесия вдоль линии насыщения. Теплоемкость и насыщенность можно записать
(6)Эти три теплоемкости могут быть взаимосвязаны посредством термодинамических соотношений, включающих уравнение состояния материала [Bett et al.(1975)]. Три теплоемкости являются функциями термодинамического состояния и обычно выражаются как функция от p и T и как функция от и T.
Измерения теплоемкости твердых тел и жидкостей довольно легко выполнять рутинно с очень скромной точностью (несколько процентов) с помощью современных дифференциальных сканирующих калориметров [Grolier (1994)]. Однако, поскольку для многих инженерных целей интересует разница энтальпий между потоками с энтальпиями одинаковой величины, такой точности часто бывает недостаточно.Значительные усилия были затрачены на разработку приборов для измерения теплоемкости. Такие приборы почти всегда представляют собой калориметры с электрическим приводом. Почти во всех калориметрах известное количество вещества нагревается электрическим током и измеряется повышение температуры. Система, в которой это делается, может быть закрытой (для твердого, жидкого или газообразного) или стационарным потоком (жидкость или газ). Исчерпывающий обзор классических методов был дан McCullough и Scott (1968).Методы измерения теплоемкости жидкостей недавно были рассмотрены Grolier (1994) в контексте более широкого обзора калориметрии .
Изобарная теплоемкость и изохорная теплоемкость связаны уравнением
(7)что для идеального газа приводит к простому результату
(8)Для состояния идеального газа теплоемкость может быть выражена с помощью статистической механики через вклады в поступательную и внутреннюю энергии молекул [Рашбрук (1949)].В свою очередь, часть внутреннего вклада, обусловленного вращательными, колебательными и электронными модами движения, часто может быть затем определена путем спектроскопических измерений частот нормального режима движения молекулы. Для многих молекул этот процесс обеспечивает более точный способ определения теплоемкости материала идеального газа, чем прямое измерение [de Reuck and Craven (1993)].
Когда плотность увеличивается от состояния идеального газа, энергия ансамбля молекул приобретает компонент, возникающий из взаимодействий между молекулами (конфигурационная часть), и это невозможно оценить теоретически ни для каких молекул, кроме простейших, так что единственный источник информация о теплоемкости получается в результате прямого или косвенного измерения.Когда нет доступных измерений, необходимо прибегнуть к методам оценки [Reid et al. (1975)].
ССЫЛКИ
Бетт К. Э., Роулинсон Дж. С. и Сэвилл Г. (1975) Термодинамика для инженеров-химиков , Атлон, Лондон. DOI: 10.1016 / 0300-9467 (76) 80049-4
де Реук, К. М. и Крейвен, Р. Дж. Б. (1993) Международные термодинамические таблицы флюидного состояния — 12: метанол , Blackwell Scientific, Оксфорд.
Гролье, Дж.-П. (1994) Теплоемкость органических жидкостей в экспериментальной термодинамике IV, Калориметрия раствора , К. Н. Марш и П. А. Дж. О’Хара, ред., Blackwell Scientific, Oxford.
Маккалоу, Дж. П. и Скотт, Д. У. (1968) Экспериментальная термодинамика 1, Калориметрия нереагирующих систем , Баттервортс, Лондон.
Рид Р.К., Праусниц Дж. М. и Шервуд Т. К. (1977) Свойства газов и жидкостей , МакГроу-Хилл, Нью-Йорк.
Рашбрук, Г.С. (1949) Введение в статистическую механику , Кларендон, Оксфорд.


