Свойства жидкостей.
Мы уже знаем, что жидкости имеют фиксированный объем и принимают форму того сосуда, в котором они находятся. Мы знаем также, что плотности жидкостей намного больше, чем у газов. В общем случае плотности жидкостей имеют значения, подобные плотностям твердых веществ. Сжимаемость жидкостей очень невелика, поскольку между частицами жидкости остается совсем немного свободного пространства.
Свободно падающая капля воды. Ее сферическая форма обусловлена поверхностным натяжением.
Нам предстоит рассмотреть еще три других важных свойства жидкостей. Все эти свойства можно объяснить на основе представлений кинетической теории жидкостей.
Текучесть и вязкость. Подобно газам жидкости могут течь, и это их свойство называется текучестью. Сопротивляемость течению называется вязкостью. На текучесть и вязкость влияет целый ряд факторов. Наиболее важными из них являются силы притяжения между молекулами жидкости, а также форма, структура и относительная молекулярная масса этих молекул.
Поверхностное натяжение. На молекулу, находящуюся в глубине жидкости, со всех сторон равномерно действуют силы межмолекулярного притяжения. Однако на поверхности жидкости эти силы оказываются несбалансированными, и вследствие этого поверхностные молекулы испытывают действие результирующей силы, направленной внутрь жидкости. Поэтому поверхность жидкости оказывается в состоянии натяжения-она все время стремится сократиться. Поверхностное натяжение жидкости-это минимальная сила, необходимая, чтобы преодолеть устремление частиц жидкости внутрь и тем самым удержать поверхность жидкости от сокращения. Существованием поверхностного натяжения объясняется сферическая форма свободно падающих капель жидкости.
Диффузия. Так называется процесс, посредством которого вещество перераспределяется из области с высокой концентрацией или высоким давлением в область с меньшей концентрацией или меньшим давлением. Диффузия в жидкостях осуществляется гораздо медленнее, чем в газах, потому что частицы жидкости упакованы гораздо плотнее, чем частицы газа. Частица, диффундирующая в жидкости, подвергается частым столкновениям и поэтому подвигается с трудом. В газах между частицами много свободного пространства, и они могут перераспределяться значительно быстрее. Диффузия осуществляется между взаимно растворимыми, или смешивающимися, жидкостями. Она не происходит между несмешивающимися жидкостями. В отличие от жидкостей все газы смешиваются друг с другом и поэтому могут диффундировать один в другой.
Диффузия в жидкостях осуществляется гораздо медленнее, чем в газах, потому что частицы жидкости упакованы гораздо плотнее, чем частицы газа. Частица, диффундирующая в жидкости, подвергается частым столкновениям и поэтому подвигается с трудом. В газах между частицами много свободного пространства, и они могут перераспределяться значительно быстрее. Диффузия осуществляется между взаимно растворимыми, или смешивающимися, жидкостями. Она не происходит между несмешивающимися жидкостями. В отличие от жидкостей все газы смешиваются друг с другом и поэтому могут диффундировать один в другой.
Оглавление:
- часть 1 (Cтроение атома, Химическая связь)
- часть 2 (Газы, жидкости и твердые вещества, Стехиометрия, Энергетика)
- часть 3 (Фазовые равновесия, Химическое равновесие, Ионы, Химическая кинетика)
- часть 4 (Электрохимия)
Свойства жидкостей и твёрдых тел
Все тела состоят из атомов или молекул (частицы вещества), которые беспорядочно двигаются, а также взаимодействуют с силами притяжения и отталкивания.
Именно различиями в тепловом движении этих частиц, а также их взаимодействием при разных условиях обуславливается факт существования у вещества нескольких агрегатных состояний:
1) газообразного;
2) жидкого;
3) твёрдого.
Твёрдые тела
Отличие твёрдых тел от газов заключается в том, что при незначительных изменениях объёма в твёрдых телах возникают значительные силы упругости, тогда как в газах даже при значительном изменения объёма (до определённого предела) увеличения сил упругости почти не происходит.
От жидкостей твёрдые тела отличаются тем, что силы упругости в них возникают при изменении формы (сдвиг), чего не происходит в жидкости, способной принимать любую форму.
В твёрдых телах не происходит свободного передвижения частиц. Молекулы находятся в узлах кристаллической решётки. То есть существует строгий периодический порядок в расположении частиц, составляющих твёрдое тело.
В твёрдых телах потенциальная энергия взаимодействия очень существенна; кинетическая энергия, по сравнению с потенциальной, не велика.
Атомы, молекулы или ионы совершают лишь колебательные движения возле положения равновесия.
Расстояния между соседними частицами примерно равно самим размерам частиц.
Твёрдые тела могут существовать в двух различных состояниях:
1) кристаллическом;
2) аморфном.
Аморфными называются тела, физические свойства которых одинаковы по всем направлениям (изотропность).
Примерами аморфных тел могут служить куски затвердевшей смолы, янтарь, изделия из стекла.
Изотропность физических свойств аморфных тел объясняется беспорядочностью расположения составляющих их атомов и молекул.
Кристаллическое состояние характеризуется упорядоченным расположением атомов или молекул, которые образуют периодически повторяющуюся внутреннюю структуру.
Физические свойства кристаллических тел неодинаковы в различных направлениях, но совпадают в параллельных направлениях. Это свойство кристаллов называется анизотропностью.
Причиной анизотропности является то, что при упорядоченном расположении атомов, молекул или ионов силы взаимодействия между ними и межатомные расстояния оказываются неодинаковыми по различным направлениям.
Кристаллические тела делятся на монокристаллы, у которых внутренняя структура периодически повторяется во всём их объёме, и поликристаллы, представляющие собой множество сросшихся между собой хаотически расположенных маленьких кристаллов – кристаллитов.
Жидкость – это вещество, находящееся в жидком агрегатном состоянии, занимающем промежуточное положение между твёрдым и газообразным состоянием.
Жидкости, в отличие от твёрдых тел, обладают ближним порядком в расположении частиц вещества.
Частицы в жидких телах «упакованы» плотно и, как в твёрдых телах, совершают колебания около положения равновесия.
Попытка сжать жидкость быстро приводит к деформации молекул и встречает мощное сопротивление со стороны жидкости. То есть жидкости прктически несжимаемы.
Хотя молекулы жидкости расположены почти так же, как в твёрдом теле, жидкость обладает текучестью. Это объясняется тем, что, в отличие от твёрдого тела, колебания молекул около положения равновесия в жидкости не вечны, а в какой-то момент времени молекула совершает «скачок», переходя в другое положение.
Следовательно, жидкость хорошо сохраняет объём, но не сохраняет форму.
С энергетической точки зрения жидкость занимает промежуточное положение между твёрдым телом и газом – частицы жидкости обладают существенной (на микроскопическом уровне) как кинетической энергией движения, так и потенциальной энергией взаимодействия.
| Расположение молекул | «Хаос» | «Порядок» |
| Характер движения молекул | Колеблются на месте, перескакивают с места на место | Колеблются на месте |
| Взаимодействие молекул | Сильное | Огромное |
| Основные свойства | 1. 2. Сохраняет объём. 3. Не сжимаема. 4. Текуча. | 1. Сохраняет форму. 2. Сохраняет объём. 3. Не сжимаемо. |
Свойства жидкостей | Химия для специальностей
Результаты обучения
- Различие между силами сцепления и силами сцепления
- Определение вязкости, поверхностного натяжения и капиллярного подъема
- Опишите роль сил межмолекулярного притяжения в каждом из этих свойств/явлений
Когда вы наливаете воду в стакан или заправляете машину бензином, вы видите, что вода и бензин текут свободно. Но когда поливаешь сиропом блины или заливаешь масло в двигатель автомобиля, то замечаешь, что сироп и моторное масло текут не так легко.  Мы можем измерить вязкость, измеряя скорость, с которой металлический шарик падает через жидкость (мячик падает медленнее через более вязкую жидкость), или измеряя скорость, с которой жидкость течет через узкую трубку (более вязкие жидкости текут медленнее). ).
Мы можем измерить вязкость, измеряя скорость, с которой металлический шарик падает через жидкость (мячик падает медленнее через более вязкую жидкость), или измеряя скорость, с которой жидкость течет через узкую трубку (более вязкие жидкости текут медленнее). ).
Рис. 1. Мед (а) и моторное масло (б) являются примерами жидкостей с высокой вязкостью; они текут медленно. (кредит a: модификация работы Скотта Бауэра; кредит b: модификация работы Дэвида Наги)
Вы можете просмотреть стенограмму «Поверхностное натяжение | Состояния вещества и межмолекулярные силы | Химия | Академия Хана» здесь (открывается в новом окне).
IMF между молекулами жидкости, размер и форма молекул, а также температура определяют, насколько легко течет жидкость. Как видно из табл. 1, чем сложнее по строению молекулы жидкости и чем сильнее ММП между ними, тем труднее им двигаться друг мимо друга и тем больше вязкость жидкости. По мере повышения температуры молекулы движутся быстрее, и их кинетическая энергия лучше способна преодолевать силы, удерживающие их вместе; таким образом, вязкость жидкости уменьшается.
1, чем сложнее по строению молекулы жидкости и чем сильнее ММП между ними, тем труднее им двигаться друг мимо друга и тем больше вязкость жидкости. По мере повышения температуры молекулы движутся быстрее, и их кинетическая энергия лучше способна преодолевать силы, удерживающие их вместе; таким образом, вязкость жидкости уменьшается.
| Таблица 1. Вязкости обычных веществ при 25 °C | ||
|---|---|---|
| Вещество | Формула | Вязкость (мПа•с) |
| вода | Н 2 О | 0,890 |
| ртуть | рт.ст. | 1,526 |
| этанол | С 2 Н 5 ОХ | 1,074 |
| Октан | С 8 Н 18 | 0,508 |
| этиленгликоль | СН 2 (ОН)СН 2 (ОН) | 16,1 |
| мед | переменная | ~2 000–10 000 |
| моторное масло | переменная | ~50–500 |
Различные ММП между идентичными молекулами вещества являются примерами сил сцепления . Молекулы внутри жидкости окружены другими молекулами и одинаково притягиваются во всех направлениях силами сцепления внутри жидкости. Однако молекулы на поверхности жидкости притягиваются вдвое меньшим количеством молекул. Из-за неуравновешенного молекулярного притяжения на поверхности молекул жидкости сжимаются, образуя форму, при которой количество молекул на поверхности минимально, т. е. форму с минимальной площадью поверхности. Небольшая капля жидкости стремится принять сферическую форму, как показано на рисунке 2, потому что в сфере отношение площади поверхности к объему минимально. Более крупные капли в большей степени подвержены влиянию гравитации, сопротивления воздуха, взаимодействия с поверхностью и т. д. и, как следствие, имеют менее сферическую форму.
Молекулы внутри жидкости окружены другими молекулами и одинаково притягиваются во всех направлениях силами сцепления внутри жидкости. Однако молекулы на поверхности жидкости притягиваются вдвое меньшим количеством молекул. Из-за неуравновешенного молекулярного притяжения на поверхности молекул жидкости сжимаются, образуя форму, при которой количество молекул на поверхности минимально, т. е. форму с минимальной площадью поверхности. Небольшая капля жидкости стремится принять сферическую форму, как показано на рисунке 2, потому что в сфере отношение площади поверхности к объему минимально. Более крупные капли в большей степени подвержены влиянию гравитации, сопротивления воздуха, взаимодействия с поверхностью и т. д. и, как следствие, имеют менее сферическую форму.
Рис. 2. Силы притяжения приводят к образованию сферической капли воды с минимальной площадью поверхности; силы сцепления удерживают сферу вместе; Силы сцепления удерживают каплю прикрепленной к полотну. (кредит: модификация работы OliBac/Flickr)
Поверхностное натяжение определяется как энергия, необходимая для увеличения площади поверхности жидкости, или сила, необходимая для увеличения длины поверхности жидкости на заданную величину. . Это свойство является результатом сил сцепления между молекулами на поверхности жидкости и заставляет поверхность жидкости вести себя как натянутая резиновая мембрана. Поверхностное натяжение некоторых жидкостей представлено в табл. 2. Среди обычных жидкостей вода обладает отчетливо высоким поверхностным натяжением из-за сильных водородных связей между ее молекулами. В результате этого высокого поверхностного натяжения поверхность воды представляет собой относительно «твердую кожу», которая может выдерживать значительные нагрузки, не ломаясь. Стальная игла, осторожно помещенная в воду, будет плавать. Некоторые насекомые, подобные изображенному на рис. 3, хотя и плотнее воды, передвигаются по ее поверхности, потому что их поддерживает поверхностное натяжение.
. Это свойство является результатом сил сцепления между молекулами на поверхности жидкости и заставляет поверхность жидкости вести себя как натянутая резиновая мембрана. Поверхностное натяжение некоторых жидкостей представлено в табл. 2. Среди обычных жидкостей вода обладает отчетливо высоким поверхностным натяжением из-за сильных водородных связей между ее молекулами. В результате этого высокого поверхностного натяжения поверхность воды представляет собой относительно «твердую кожу», которая может выдерживать значительные нагрузки, не ломаясь. Стальная игла, осторожно помещенная в воду, будет плавать. Некоторые насекомые, подобные изображенному на рис. 3, хотя и плотнее воды, передвигаются по ее поверхности, потому что их поддерживает поверхностное натяжение.
| Таблица 2. Поверхностное натяжение обычных веществ при 25 °C | ||
|---|---|---|
| Вещество | Формула | Поверхностное натяжение (мН/м) |
| вода | Н 2 О | 71,99 |
| ртуть | рт. ст. ст. | 458,48 |
| этанол | С 2 Н 5 ОХ | 21,97 |
| октановое число | С 8 Н 18 | 21.14 |
| этиленгликоль | СН 2 (ОН)СН 2 (ОН) | 47,99 |
Рис. 3. Поверхностное натяжение (справа) препятствует погружению этого насекомого, водомерки, в воду (слева).
ММП притяжения между двумя различными молекулами называются силами сцепления . Рассмотрим, что происходит, когда вода соприкасается с какой-либо поверхностью. Если силы сцепления между молекулами воды и молекулами поверхности слабы по сравнению с силами сцепления между молекулами воды, вода не «смачивает» поверхность.
Рисунок 4. Различия в относительных силах когезии и адгезии приводят к различной форме мениска для ртути (слева) и воды (справа) в стеклянных трубках. (кредит: Марк Отт)
(кредит: Марк Отт)
Например, вода не смачивает вощеные поверхности или многие пластмассы, такие как полиэтилен. Вода образует капли на этих поверхностях, потому что силы сцепления внутри капель больше, чем силы сцепления между водой и пластиком. Вода растекается по стеклу, потому что сила сцепления между водой и стеклом больше, чем сила сцепления внутри воды. Когда вода находится в стеклянной трубке, ее мениск (поверхность) имеет вогнутую форму, потому что вода смачивает стекло и стекает вверх по стенке трубки. С другой стороны, силы сцепления между атомами ртути намного больше, чем силы сцепления между ртутью и стеклом. Таким образом, ртуть не смачивает стекло и образует выпуклый мениск, когда заключена в трубку, потому что силы сцепления внутри ртути стремятся превратить ее в каплю (рис. 4).
Если вы поместите один конец бумажного полотенца в пролитое вино, как показано на рис. 5, жидкость впитает бумажное полотенце. Аналогичный процесс происходит с тканевым полотенцем, когда вы используете его, чтобы вытереться после душа. Это примеры капиллярного действия — когда жидкость течет внутри пористого материала из-за притяжения молекул жидкости к поверхности материала и к другим молекулам жидкости. Силы сцепления между жидкостью и пористым материалом в сочетании с силами сцепления внутри жидкости могут быть достаточно сильными, чтобы перемещать жидкость вверх против силы тяжести.
Это примеры капиллярного действия — когда жидкость течет внутри пористого материала из-за притяжения молекул жидкости к поверхности материала и к другим молекулам жидкости. Силы сцепления между жидкостью и пористым материалом в сочетании с силами сцепления внутри жидкости могут быть достаточно сильными, чтобы перемещать жидкость вверх против силы тяжести.
Рисунок 5. Вино впитывает бумажное полотенце (слева) из-за сильного притяжения молекул воды (и этанола) к группам −OH на целлюлозных волокнах полотенца и сильного притяжения молекул воды к другой воде (и этанолу) молекулы (справа). (кредитное фото: модификация работы Марка Блазера)
Полотенца впитывают жидкости, как вода, потому что волокна полотенца состоят из молекул, которые притягиваются к молекулам воды. Большинство тканевых полотенец изготовлены из хлопка, а бумажные полотенца обычно изготавливаются из бумажной массы. Оба состоят из длинных молекул целлюлозы, которые содержат много групп -ОН. Молекулы воды притягиваются к этим группам -OH и образуют с ними водородные связи, что притягивает H 2 Молекулы О вверх по молекулам целлюлозы. Молекулы воды также притягиваются друг к другу, поэтому большое количество воды втягивается в волокна целлюлозы.
Молекулы воды также притягиваются друг к другу, поэтому большое количество воды втягивается в волокна целлюлозы.
Капиллярное действие также может возникать, когда один конец трубки малого диаметра погружается в жидкость, как показано на рис. 6. Если молекулы жидкости сильно притягиваются к молекулам трубки, жидкость ползет вверх по внутренней части трубки до тех пор, пока вес жидкости и силы сцепления находятся в равновесии. Чем меньше диаметр трубки, тем выше поднимается жидкость. Частично благодаря капиллярному действию, происходящему в растительных клетках, называемых ксилемой, вода и растворенные питательные вещества переносятся из почвы вверх через корни в растение. Капиллярное действие лежит в основе тонкослойной хроматографии, лабораторного метода, обычно используемого для разделения небольших количеств смесей. Вы зависите от постоянного притока слез, чтобы ваши глаза были смазаны, и от капиллярного действия, которое откачивает слезную жидкость.
Рис. 6. В зависимости от относительной силы адгезии и сил сцепления жидкость может подниматься (например, вода) или опускаться (например, ртуть) в стеклянной капиллярной трубке.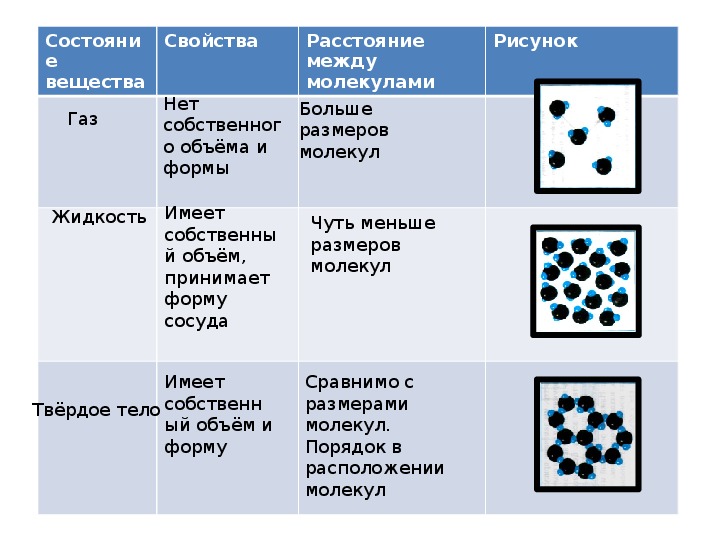 Степень подъема (или падения) прямо пропорциональна поверхностному натяжению жидкости и обратно пропорциональна плотности жидкости и радиусу трубки.
Степень подъема (или падения) прямо пропорциональна поверхностному натяжению жидкости и обратно пропорциональна плотности жидкости и радиусу трубки.
Высота, на которую жидкость поднимется в капиллярной трубке, определяется несколькими факторами, как показано в следующем уравнении:
[латекс]\displaystyle{h=\dfrac{2T\text{cos}\theta }{r\rho g}}[/latex]
В этом уравнении h — высота жидкости внутри капиллярной трубки относительно поверхности жидкости вне трубки, T — поверхностное натяжение жидкости, θ — краевой угол между жидкостью и трубкой, r — радиус трубки, ρ — плотность жидкости, г — ускорение свободного падения, 9.8 м/с 2 . Когда трубка изготовлена из материала, к которому сильно притягиваются молекулы жидкости, они полностью растекаются по поверхности, что соответствует краевому углу 0°. Это ситуация с водой, поднимающейся в стеклянной трубке.
Пример 1:
Капиллярный подъемНасколько высоко будет подниматься вода в стеклянной капиллярной трубке с внутренним диаметром 0,25 мм при 25 °C?
Для воды T = 71,99 мН/м и ρ = 1,0 г/см 3 .
Вода поднимается в стеклянной капиллярной трубке на высоту 8,4 см. Какой диаметр капиллярной трубки?
Показать растворПрименение капиллярного действия в биомедицинских целях
Рис. 7. Кровь для медицинского анализа берется с помощью капиллярного действия, которое набирает кровь в стеклянную пробирку небольшого диаметра. (кредит: модификация работы Центров по контролю и профилактике заболеваний)
Многие медицинские тесты требуют взятия небольшого количества крови, например, для определения количества глюкозы у человека с диабетом или уровня гематокрита у спортсмена. Эту процедуру можно легко выполнить из-за капиллярного действия, способности жидкости течь вверх по небольшой трубке против силы тяжести, как показано на рисунке 7. Когда ваш палец уколот, образуется капля крови, которая удерживается вместе благодаря поверхностному натяжению— неуравновешенное межмолекулярное притяжение на поверхности капли. Затем, когда открытый конец стеклянной трубки узкого диаметра касается капли крови, силы сцепления между молекулами крови и молекулами на поверхности стекла вытягивают кровь вверх по трубке. Насколько далеко кровь поднимается по трубке, зависит от диаметра трубки (и типа жидкости). Маленькая пробирка имеет относительно большую площадь поверхности для данного объема крови, что приводит к большим (относительным) силам притяжения, позволяющим втягивать кровь дальше вверх по пробирке. Сама жидкость удерживается вместе силами собственного сцепления. Когда вес жидкости в трубке создает нисходящую силу, равную восходящей силе, связанной с капиллярным действием, жидкость перестает подниматься.
Затем, когда открытый конец стеклянной трубки узкого диаметра касается капли крови, силы сцепления между молекулами крови и молекулами на поверхности стекла вытягивают кровь вверх по трубке. Насколько далеко кровь поднимается по трубке, зависит от диаметра трубки (и типа жидкости). Маленькая пробирка имеет относительно большую площадь поверхности для данного объема крови, что приводит к большим (относительным) силам притяжения, позволяющим втягивать кровь дальше вверх по пробирке. Сама жидкость удерживается вместе силами собственного сцепления. Когда вес жидкости в трубке создает нисходящую силу, равную восходящей силе, связанной с капиллярным действием, жидкость перестает подниматься.
Вы можете просмотреть стенограмму «Капиллярное действие и почему мы видим мениск | Химия | Академия Хана» здесь (открывается в новом окне).
Ключевые понятия и резюме
Межмолекулярные силы между молекулами в жидком состоянии различаются в зависимости от их химической идентичности и приводят к соответствующим изменениям различных физических свойств. Силы сцепления между одноименными молекулами ответственны за вязкость жидкости (сопротивление течению) и поверхностное натяжение (упругость поверхности жидкости). Силы сцепления между молекулами жидкости и различными молекулами, составляющими поверхность, находящуюся в контакте с жидкостью, ответственны за такие явления, как смачивание поверхности и капиллярный подъем.
Ключевые уравнения
- [латекс]h=\dfrac{2T\text{cos}\theta }{r\rho g}[/latex]
Попробуйте
- Показанные здесь пробирки содержат равные количества указанных моторных масел. В каждую из труб одновременно были брошены одинаковые металлические сферы, и через мгновение сферы упали на высоту, указанную на рисунке.
Расположите моторные масла в порядке возрастания вязкости и объясните свое решение: - Хотя сталь плотнее воды, стальную иглу или канцелярскую скрепку, аккуратно помещенную вдоль на поверхность стоячей воды, можно заставить плавать.
 Объясните на молекулярном уровне, как это возможно:
Объясните на молекулярном уровне, как это возможно: - Здесь показаны значения поверхностного натяжения и вязкости для диэтилового эфира, ацетона, этанола и этиленгликоля.
- Объясните их различия в вязкости с точки зрения размера и формы их молекул и их IMF.
- Объясните их различия в поверхностном натяжении с точки зрения размера и формы их молекул и их IMF.
- Возможно, вы слышали, как кто-то использует фигуру речи «медленнее, чем патока зимой», чтобы описать процесс, который происходит медленно. Объясните, почему это уместная идиома, используя понятия размера и формы молекул, молекулярных взаимодействий и влияния изменения температуры.
- Часто рекомендуется дать двигателю автомобиля поработать на холостом ходу, чтобы он прогрелся перед поездкой, особенно в холодные зимние дни. Хотя польза от продолжительной работы на холостом ходу сомнительна, безусловно верно, что прогретый двигатель более экономичен по топливу, чем холодный.
 Объясните причину этого.
Объясните причину этого. - Поверхностное натяжение и вязкость воды при различных температурах приведены в этой таблице.
Вода Поверхностное натяжение (мН/м) Вязкость (мПа·с) 0 °С 75,6 1,79 20 °С 72,8 1,00 60 °С 66,2 0,47 100 °С 58,9 0,28 - Что происходит с поверхностным натяжением воды при повышении температуры? Объясните, почему это происходит, с точки зрения молекулярных взаимодействий и влияния изменения температуры.
- Что происходит с вязкостью воды при повышении температуры? Объясните, почему это происходит, с точки зрения молекулярных взаимодействий и влияния изменения температуры.

- На какую высоту при 25 °С поднимется вода в стеклянной капиллярной трубке с внутренним диаметром 0,63 мм? Обратитесь к примеру 10.4 за необходимой информацией.
- Вода поднимается по стеклянной капиллярной трубке на высоту 17 см. Какой диаметр капиллярной трубки?
сила сцепления: сила притяжения между молекулами различной химической принадлежности
капиллярное действие: поток жидкости внутри пористого материала из-за притяжения молекул жидкости к поверхности материала и к другим молекулам жидкости
сила сцепления: сила притяжения между идентичными молекулами
поверхностное натяжение: энергия, необходимая для увеличения площади или длины поверхности жидкости на заданную величину
вязкость: мера сопротивления жидкости течению
Жидкости обладают свойствами — Американское химическое общество
Обзор урока для учителей
Посмотрите видео ниже, чтобы узнать, что вы и ваши ученики будете делать на этом уроке.
Идентификатор Youtube: ooH9YiOMlig
Материалы для загрузки:
План урока (PDF) | Лист активности учащихся (PDF) | История учителя (PDF) | Подключения к NGSS (PDF)
Учащиеся смогут планировать и проводить исследования для обнаружения и сравнения свойств жидкостей. Учащиеся разовьют понимание того, что жидкости, как и твердые тела, имеют свои характерные свойства.
Ключевые понятия- Жидкости имеют свои характерные свойства.
- Даже если жидкости выглядят одинаково, они могут иметь разные свойства.
- Свойства жидкостей можно узнать, проводя над ними тесты.
- Чтобы сравнить свойства жидкостей, жидкости необходимо испытать таким же образом.
- NGSS 2-PS1-1: Спланируйте и проведите исследование для описания и классификации различных видов материалов по их наблюдаемым свойствам.
Учащиеся рассмотрели свойства твердых тел и на этом уроке увидят, что жидкости также обладают свойствами.
- Учащиеся исследуют три прозрачные бесцветные жидкости: воду, минеральное масло и кукурузный сироп.
- Учащиеся наносят капли каждой жидкости на поверхность пластикового пакета с застежкой-молнией и видят, что жидкости выглядят и действуют по-разному.
- Учащиеся наклоняют пакет и видят, что жидкости стекают по пластику с разной скоростью.
- Наконец, учащиеся видят демонстрацию, в которой капля пищевого красителя помещается в каждую жидкость, и учащиеся делают наблюдения о том, как пищевой краситель выглядит в каждой жидкости по-разному.
Загрузите лист с заданиями для учащихся (PDF) и раздайте каждому учащемуся, если это указано в задании. Рабочий лист будет служить компонентом оценки плана урока 5-E.
БезопасностьУбедитесь, что учащиеся носят правильно подобранные защитные очки.
Материалы- Вода
- Минеральное масло
- Кукурузный сироп (хорошо подойдет прозрачный бесцветный сироп Каро)
- 3 маленьких пластиковых стаканчика на каждую группу
- 3 одноразовые капельницы на каждую группу
- 1 пластиковый пакет размером в четверть
- Карточки
- Бумажные полотенца s
- Несмываемым маркером пометьте 3 маленьких пластиковых стаканчика для каждой группы: Вода , Минеральное масло и Кукурузный сироп.
 Поместите примерно 1 чайную ложку жидкости в каждую промаркированную чашку
Поместите примерно 1 чайную ложку жидкости в каждую промаркированную чашку - Пометьте один дополнительный набор чашек, чтобы использовать их в части урока «Задействовать» и «Расширить». В чашках наполните каждую примерно наполовину указанной жидкостью.
- Разрежьте картон так, чтобы он поместился в пластиковый пакет с застежкой-молнией. Пометьте части картона Вода , Масло и Сироп , как показано на рисунке. Поместите кусок картона в пластиковый пакет и запечатайте пакет. Сделайте по одному для каждой группы учащихся.
- Раздайте стаканчики с жидкостью, три пипетки и полиэтиленовый пакет с промаркированным картоном каждой группе.
- Чашка с водой
- Чашка с минеральным маслом
- Чашка с кукурузным сиропом
- 3 одноразовые пипетки
- Пластиковый пакет с картоном
- Бумажные полотенца
 Покажите учащимся образцы воды, минерального масла и кукурузного сиропа и скажите учащимся, что они будут исследовать сходства и различия между ними.
Покажите учащимся образцы воды, минерального масла и кукурузного сиропа и скажите учащимся, что они будут исследовать сходства и различия между ними. Объясните учащимся, что до сих пор они изучали свойства множества различных объектов и материалов, но все они были твердыми телами.
Спросите учащихся:- Как вы думаете, жидкости тоже обладают свойствами?
Предложите учащимся провести мозговой штурм возможных свойств жидкостей. Они могут быть бесцветными или окрашенными, иметь густоту (вязкость), запах (запах) и т. д.
Покажите учащимся образец воды, минерального масла и кукурузного сиропа в трех отдельных прозрачных пластиковых стаканчиках.
Примечание: Сохраните эти жидкости, потому что вы будете использовать их в демонстрации в разделе РАСШИРЕНИЕ урока.
Скажите учащимся, что хотя жидкости выглядят одинаково, они могут иметь разные свойства или характеристики. Объясните учащимся, что ученые делают открытия, наблюдая и тестируя различные вещества. Скажите учащимся, что они могут стать учеными, наблюдая за жидкостями и проверяя их, пытаясь обнаружить их свойства.
Скажите учащимся, что они могут стать учеными, наблюдая за жидкостями и проверяя их, пытаясь обнаружить их свойства.
Примечание:
- Минеральное масло и кукурузный сироп могут быть очень грязными, если их пролить. Вы можете поставить чашки на подносы или попросить учеников поставить чашки в середине парты или стола.
- Обязательно используйте одноразовые капельницы, так как минеральное масло и кукурузный сироп, оставшиеся в капельницах, будет трудно удалить. Кроме того, в зависимости от пипетки может быть немного сложно набрать кукурузный сироп в пипетку и выдавить ровно 3 капли. Если это произойдет, учащиеся могут использовать маленькую пластиковую ложку или палочку от эскимо, чтобы нанести на пластиковый пакет небольшое количество кукурузного сиропа, которое выглядит примерно как 3 капли.
- Вполне вероятно, что использование капельниц заинтригует ваших учеников. Если у вас есть время в начале дня или в начале урока, вы можете предложить своим ученикам попробовать использовать пипетки с небольшим количеством воды перед самим экспериментом.
 Таким образом, новизна использования капельниц будет уменьшена, и учащиеся смогут больше сосредоточиться на науке, а не на игре с капельницами.
Таким образом, новизна использования капельниц будет уменьшена, и учащиеся смогут больше сосредоточиться на науке, а не на игре с капельницами.
Раздайте каждому учащемуся Рабочий лист (PDF) .
Учащиеся записывают свои наблюдения и отвечают на вопросы о задании в листе заданий.
Вопрос для исследования: Имеют ли внешне похожие жидкости разные свойства?
Материалы для каждой группы
- Чашка с водой
- Чашка с минеральным маслом
- Чашка с кукурузным сиропом
- 3 одноразовые пипетки
- Пластиковый пакет с картоном
- Бумажные полотенца
- Положите сумку горизонтально на рабочий стол или поверхность стола.
- Используйте пипетки, чтобы поместить три капли каждой жидкости вместе на пластиковый пакет под этикеткой для этой жидкости.

- Что вы заметили в том, как каждая жидкость выглядит на пластике?
Вода выглядит очень круглой.
Масло стало более плоским и растекается больше.
Сироп похож на воду, но может быть немного более плоским.
Покажите, как учащиеся должны наклонять свою сумку.
Сначала покажите, как учащиеся должны медленно поднимать и наклонять сумку, удерживая ее двумя руками за верхние углы. При демонстрации используйте пакет с картой внутри, но без жидкостей на пакете.
- Держитесь за верхние углы пакета и медленно поднимайте и наклоняйте пакет, чтобы увидеть, как жидкости стекают по пластику.
- Что вы заметили в том, как каждая жидкость двигалась по пластику?
Вода текла очень быстро и превзошла другие жидкости. Он оставался вместе на всем пути вниз.
Нефть шла медленнее, но все же доходила до дна. Это создало длинную серию.
Это создало длинную серию.
Сироп едва двигался, а затем двигался очень медленно, когда пластик наклонялся сильнее. Он двигался немного быстрее, когда пластик держали прямо вверх и вниз.
Показать анимацию Жидкости обладают свойствами.
Примечание: В этой анимации используются модели молекул, чтобы объяснить, почему жидкости ведут себя по-разному. Он предназначен для того, чтобы познакомить учащихся с термином «молекула» и с идеей о том, что окружающие их вещества состоят из крошечных частиц, которые они не могут видеть. Студенты также знакомятся с идеей о том, что разные молекулы придают веществам разные характеристики.
Объясните учащимся, что на скорость движения жидкости влияют две вещи: 1. Степень прилипания жидкости к пластику и 2. Способ взаимодействия молекул жидкости друг с другом. (липкость на анимации не показана)
Способ взаимодействия молекул жидкости друг с другом. (липкость на анимации не показана)
Молекулы воды практически не прилипают к пластику. Кроме того, они очень маленькие и могут легко проходить мимо друг друга. Молекулы масла немного прилипают к пластику. Они также длинные и могут запутываться друг с другом и не могут двигаться друг мимо друга так же легко, как молекулы воды. Молекулы глюкозы лучше всего прилипают к пластику. Они также очень большие и имеют такую форму, что им трудно двигаться друг мимо друга.
EXTEND 4. Проведите демонстрацию, добавив пищевой краситель в каждую жидкость и попросив учащихся сделать наблюдения. Материалы для демонстрации- 3 маленьких прозрачных пластиковых стаканчика
- Вода
- Минеральное масло
- Кукурузный сироп
- Пищевой краситель
- Добавьте столько жидкости, чтобы каждая чашка была заполнена примерно на ½.

- Несмываемым маркером пометьте три куска малярной ленты или бумаги Вода , Масло , и Сироп .
- Поместите их на передний стол или письменный стол, где вы будете проводить демонстрацию.
- Поставьте чашки с водой, маслом и сиропом в отмеченные места.
Попросите учащихся встать перед классом, чтобы они могли рассмотреть три жидкости вблизи.
Объясните учащимся, что для исследования различных свойств жидкостей можно использовать еще один тест.
Скажите учащимся, что вы будете добавлять по 1 капле пищевого красителя в каждую жидкость, чтобы увидеть, есть ли разница между тем, как пищевой краситель действует в разных жидкостях. Скажите учащимся, чтобы они внимательно следили за тем, что делает пищевой краситель.
Процедура- Держите контейнер с пищевым красителем над поверхностью воды и осторожно добавьте одну каплю.
- Повторите шаг 1 для масла и кукурузного сиропа.


 Не имеет формы.
Не имеет формы.